文档内容
专题二 化学计量与化学计算
考 点 高考年 考频解密 考点分布
2022年海南卷〔7〕;2022年辽宁卷
〔3〕;2022年河北卷〔4,8〕;2022年
2022 年 广东卷〔9〕;2022年全国甲卷〔5〕;
2022年浙江卷1月〔12〕;2022年浙江卷
6月〔12〕;
化学计量 阿伏伽德罗常数及应用〔8
次〕,与阿伏伽德罗常数有
与化学计
关的计算〔16次〕,化学计
2021年福建卷〔3〕;2021年海南卷
算 算〔10次〕,
〔7〕;2021年河北卷〔7〕;2021年天津
卷〔7〕;2021年湖北卷〔6〕;2021年广
东卷〔11〕;
2021 年
2021年全国甲卷〔2〕;2021年辽宁卷
〔4〕;2021年湖南卷〔5〕;2021年山东
卷〔4〕;2021年浙江卷1月〔18〕;
2021年浙江卷6月〔18〕;
一、物质的量、摩尔质量
<一>物质的量
(1)物质的量(n):表示含有一定数目粒子的集合体的物理量,单位为摩尔(mol)。
(2)物质的量的规范表示方法:
(3)阿伏加德罗常数(N ):0.012 kg 12C中所含的碳原子数为阿伏加德罗常数,其数值约为6.02×1023,单位
A
为mol-1。公式:N =。
A
(4)物质的量只能衡量微观粒子,必须指明具体粒子的种类或化学式,故摩尔后面应为确切的微粒名称;如
1 mol氢(不确切)和1 mol大米(宏观物质)皆为错误说法。
(5)6.02×1023是个纯数值,没有任何物理意义,而阿伏加德罗常数(N )是指1 mol任何微粒所含的粒子数,
A
它与0.012 kg12C所含的碳原子数相同,数值约为6.02×1023。
2.摩尔质量(1)单位物质的量的物质所具有的质量。常用的单位是 g·mol-1。公式:M=。
(2)数值:以 g·mol-1为单位时,任何粒子的摩尔质量在数值上都等于该粒子的相对分子(原子)质量。
(3)物质的量是计量微观粒子“集体”的物理量,只适用于微观粒子(即分子、原子、离子、质子、中子、
电子等),不适用于宏观物质。
(4)摩尔质量、相对原子(或分子)质量的含义不同,不是同一个物理量。二者单位也不同,摩尔质量的单位
是g·mol-1或kg·mol-1,相对原子(或分子)质量的单位为1,当摩尔质量以g·mol-1为单位时,二者在数值
上相等。
(5)对具体的物质,其摩尔质量是确定的,不随物质的量的多少而变化,也不随物质的聚集状态而变化。
<二>气体摩尔体积 阿伏加德罗定律
1.影响物质体积大小的因素
①粒子的大小(物质的本性);②粒子间距的大小(由温度与压强共同决定);③粒子的数目(物质的量的大
小)。
2.气体摩尔体积:单位物质的量的气体所占的体积,符号为V ,标准状况下,V 约为 22.4_L·mol-1。
m m
(1)数值:在标准状况下(指温度为0℃,压强为101 kPa)约为22.4 L·mol-1。
(2)基本关系式:n===
(3)影响因素:气体摩尔体积的数值不是固定不变的,它决定于气体所处的温度和压强。
(4)气体摩尔体积(22.4 L·mol-1)应用的“五大误区”
①使用“条件”是标准状况,即0 ℃、101 kPa,而不是常温、常压。
②使用对象必须是气体物质,可以是单一气体,也可以是混合气体。标准状况下不是气体而又常在题中出
现的物质有:水、苯、SO 、HF、CCl 、己烷、CS、CHCl 、Br 、乙醇等。
3 4 2 3 2
③标准状况下的气体摩尔体积约为22.4 L·mol-1,其他条件下V 一般不是22.4 L·mol-1。
m
④22.4 L气体,在标准状况下的物质的量是1 mol,在非标准状况下,可能是1 mol,也可能不是1 mol。
⑤物质的质量、物质的量一定时,所含微粒数与物质处于何种条件无关。如常温常压下32 g O 所含的原子
2
数目是2N 。注意不要形成定势思维,看到“常温常压”就排除选项。
A
3.阿伏加德罗定律及其推论
(1)阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体,含有相同数目的粒子(或气体的物质
的量相同)。
(2)阿伏加德罗定律的推论(以下用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质
量,V为体积,T为热力学温度)
条件 推论公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比
T、p相同 = 同温、同压下,气体的密度与其摩尔质量(或相对分子质量)成正比T、p、m相
= 同温同压下,相同质量的任何气体的体积与它们的摩尔质量成反比
同
T、V、m相
= 同温同体积时,相同质量的任何气体的压强与它们的摩尔质量成反比
同
T、p、V相 同温同压下,同体积的任何气体的质量比等于它们的摩尔质量之比,
==
同 也等于它们的密度之比
二、化学计算的常用方法
<一>守恒法
1.所谓“守恒”就是物质在发生“变化”或两物质在发生“相互作用”的过程中某些物理量的总量保持
“不变”。在化学变化中的各种各样的守恒,如质量守恒、元素守恒、原子守恒、得失电子守恒、电荷守
恒、能量守恒等。
2.一般解题步骤如下:
第一步:明确题目要求解的量;
第二步:根据题目要求解的量,分析反应过程中物质的变化,找出守恒类型及相关的量;
第三步:根据守恒原理,梳理出反应前后守恒的量,列式求解。
3.守恒类型
(1)质量守恒(原子守恒):依据化学反应的实质是原子的重新组合,因而反应前后原子的总数和质量保持不
变。质量守恒法解题时可利用①整体守恒:即反应中反应物的总质量与生成物的总质量守恒;②局部守
恒:即反应中反应物与产物中某元素的原子或离子守恒或元素守恒。
(2)电荷守恒:依据电解质溶液呈电中性,即阳离子所带正电荷总数等于阴离子所带负电荷总数或离子方程
式前后离子所带电荷总数不变。利用电荷守恒法可以①配平离子方程式;②巧解某些化学计算题。
(3)得失电子守恒关系式:依据氧化还原反应中电子得失数目相等,即氧化剂得到的电子总数目等于还原剂
失去的电子总数目。利用得失电子守恒法可以①计算元素的化合价;②计算氧化(或还原)产物的量;③
计算氧化剂、还原剂的消耗量;④计算混合物的组成。
<二>差量法
1.差量法是指根据化学反应前后有关物理量发生的变化,找出“理论差量”。这种物理量可以是质量、物
质的量、气态物质的体积和压强、反应过程中的热量等。用差量法解题时先把化学方程式中的对应差量(理
论差量)跟实际差量列成比例,然后求解。
2.一般解题步骤如下:
第一步:准确写出有关反应的化学方程式;
第二步:深入细致地分析题意,关键在于有针对性地找出产生差量的“对象”及“理论差量”。该“理论
差量”可以是质量、物质的量、气体体积、压强等,且该差量的大小与参加反应的物质的有关量成正比;
第三步:根据反应方程式,从“实际差量”寻找比例关系,列比例式求解。
<三>关系式法
1.关系式法是一种巧妙利用已知量与未知量之间关系进行解题的一种方法,一般适用于多步进行的连续反
应,因前一个反应的产物是后一个反应的反应物,可以根据中间物质的传递关系,找出原料和最终产物的
相应关系式。它是化学计算中的基本解题方法之一,利用关系式法可以将多步计算转化为一步计算,免去
逐步计算中的麻烦,简化解题步骤,减少运算量,且计算结果不易出错,准确率高。2.一般解题步骤如下:
第一步:准确写出各步反应的化学方程式;
第二步:找出“中介”的物质,并确定最初反应物、中介物质、最终生成物之间量的关系;
第三步:确定最初反应物和最终生成物之间量的关系;
第四步:根据已知条件及关系式列出比例式计算求解。
3.关系式建立的类型
(1)某元素质量守恒关系式:在化学反应中,任何一种元素的总质量是守恒的,即最初反应物中该元素
的质量等于最终产物中该元素的质量。
(2)物质的量关系式:各步反应的化学方程式,找出最初反应物与最终生成物的物质的量的关系式,再
进行一步计算。
<四>十字交叉法
1.十字交叉法是解二元一次方程式的图解形式,应用于解二元混合体系且与平均值有关的计算问题。它是
一种具有简化解题思路、运算简便、计算速度快、计算不易出差错等优点的解题方法。其原理如下:若
a、b(a > b)分别表示某二元组分中两种组分的量,c 表示 a、b 两组分的相对平均值,x、y 分别表示
a、b 在混合体系中所占的比例,则有二元一次方程组:
,整理得: ,由此可得到如下图式:
。
2.一般解题步骤如下:
第一步:确定交叉点上的物质物理量的平均数;
第二步:写出合成物质物理量的平均数的两个分量;
第三步:按斜线作差取绝对值,得出相应物质物理量的配比关系。
探究一 阿伏伽德罗常数问题
1.(2022·全国·高考真题) 为阿伏加德罗常数的值,下列说法正确的是( )
A.25℃, 下, 氢气中质子的数目为
B. 溶液中, 的数目为C. 苯甲酸完全燃烧,生成 的数目为
D.电解熔融 ,阴极增重 ,外电路中通过电子的数目为
2.(2022·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.在25℃时,1LpH为12的Ba(OH) 溶液中含有OH-数目为0.01N
2 A
B.1.8g重水(D O)中所含质子数为N
2 A
C.足量的浓盐酸与8.7gMnO 反应,转移电子的数目为0.4N
2 A
D.32g甲醇的分子中含有C—H键的数目为4N
A
规律总结:解答阿伏加德罗常数问题的一般思路:
1.注意分析题目中概念的层次,抓住题目中的关键词。研究对象是什么,是分子、原子、离子、转移电子还
是化学键数目?条件是什么?条件对解题是否有影响?
2.结合“万能恒等式” 计算出所给微粒的物质的量,分析物质的组成和
结构,计算指定微粒的物质的量,最后结合关系式“ ”计算指定微粒的个数。
【变式练习】
1.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol乙醇中含有C-H键的数目为6N
A
B.0.78gNa O 与足量的水反应,转移的电子数为0.01N
2 2 A
C.1L0.01mol•L-1NaCO 溶液中含有CO 的数目为0.01N
2 3 A
D.标准状况下,22.4LHF中含有的分子数为N
A
2.设N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol D18O+(其中D代表 )中含有的中子数为10 N
3 A
B.2N 个HCl分子与44.8 L H 和Cl 的混合气体所含的原子数目均为4N
A 2 2 A
C.物质的量浓度均为1mol/L的NaCl和MgCl 混合溶液中,含有Cl-的数目为3N
2 A
D.32gCu将足量浓、稀硝酸分别还原为NO 和NO,浓、稀硝酸得到的电子数均为N
2 A
3.设 为阿伏加德罗常数的值。下列说法正确的是( )A. 中含有的碳氢键数目为5
B. 晶体中含有 键数目为2
C. 水溶液中含有的氧原子数为0.2
D. 的 的 溶液中 数为0.1
探究二 物质的量在化学方程式中的计算问题
3.(2022·海南·高考真题)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的
A
值,下列说法正确的是( )
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
4.(2022·辽宁·高考真题)设 为阿伏加德罗常数的值。下列说法正确的是( )
A. 中含有的中子数为
B. 分子中含有的 键数目为
C.标准状况下, 气体中 数目为
D. 的 溶液中 数目为
规律总结:解答此类问题的基本步骤:
1.根据题意写出相关反应的化学(或离子)方程式。
2.根据化学(或离子)方程式中化学计量数写出相关物质的物质的量关
系(根据需要有时要将某些物质的物质的量转化成质量或标准状况下气体的体积)。
3.对应化学计量数,找出已知量和要求的量分别写在化学方程式中相关物质下面,其中要求的量用n(B)、
V(B)或设未知数x、y等表示。
4.挖掘题目中的隐含条件,确立正确的解题方法和思路,根据化学计量数的关系,列出比例式,求出未知数。
【变式练习】
1.向27.2gCu和Cu O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO ),
2 3 2在所得溶液中加入1.0mol•L-1的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为
39.2g,下列有关说法不正确的是( )
A.Cu与Cu O的物质的量之比为2:1
2
B.硝酸的物质的量浓度为2.4mol•L-1
C.产生的NO在标准状况下的体积为6.72L
D.Cu、Cu O与硝酸反应后剩余HNO 为0.2mol
2 3
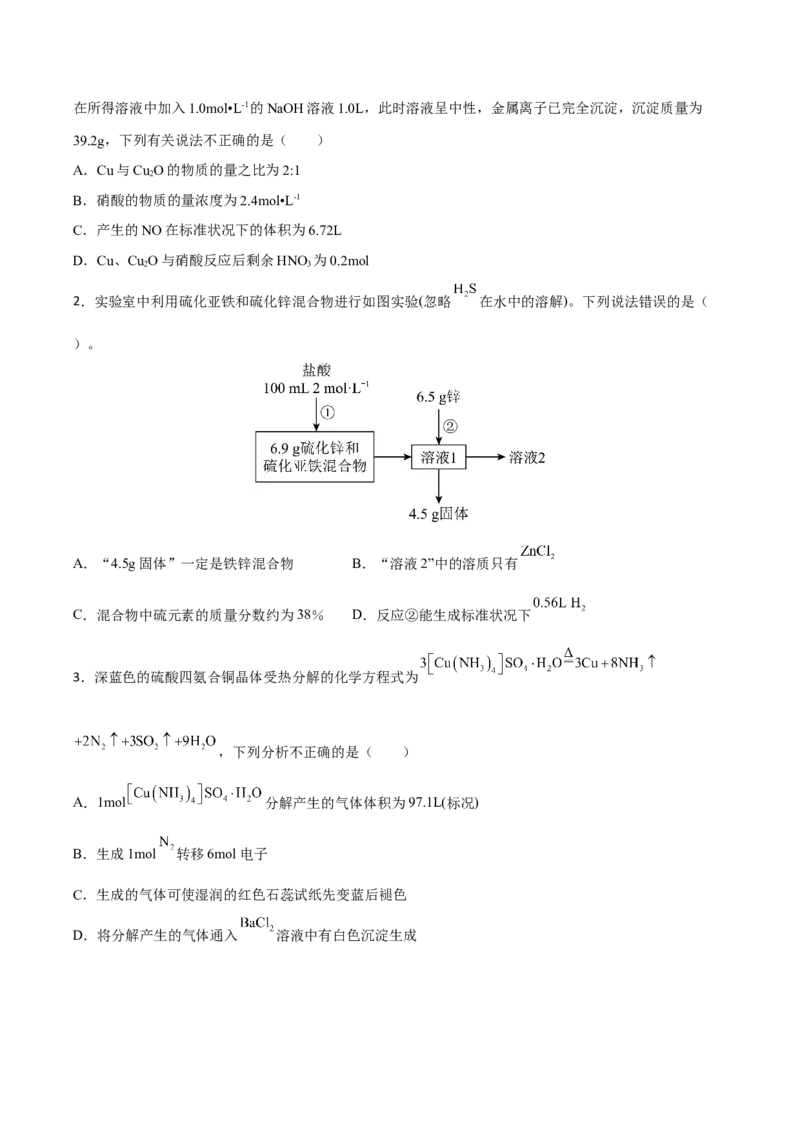
2.实验室中利用硫化亚铁和硫化锌混合物进行如图实验(忽略 在水中的溶解)。下列说法错误的是(
)。
A.“4.5g固体”一定是铁锌混合物 B.“溶液2”中的溶质只有
C.混合物中硫元素的质量分数约为38% D.反应②能生成标准状况下
3.深蓝色的硫酸四氨合铜晶体受热分解的化学方程式为
,下列分析不正确的是( )
A.1mol 分解产生的气体体积为97.1L(标况)
B.生成1mol 转移6mol电子
C.生成的气体可使湿润的红色石蕊试纸先变蓝后褪色
D.将分解产生的气体通入 溶液中有白色沉淀生成1.设 表示阿伏伽德罗常数的值,下列说法正确的是( )
A.12.4g白磷(P )中所包含的 共价键有
4
B. 的 溶液中通入适量氨气后呈中性,此溶液中 数目为
C.向含有 的溶液中通入适量氯气,当有 被氧化时,该反应转移电子数目为
D.10g环己烷与2-丙醇的混合液中,碳元素的质量分数为72%,其中所含的氧原子数目为
2.氨法脱硫工艺是利用氨水吸收烟气中的 生成亚硫酸铵溶液,并在富氧条件下将亚硫酸氨氧化成硫
酸铵,再经加热蒸发结晶析出硫酸铵,过滤干燥后得化肥产品。关于该工艺说法正确的是( )
A.1 L0.1mol/L氨水中含有的 数目为0.1N
A
B.0.01mol/L 溶液中, 、 与 的数目之和为0.01N
A
C.每氧化1mol ,转移的电子数为2 N
A
D.若将2mol 与1mol 置于密闭容器中充分反应,产物的分子数为2N
A
3.N 表示阿伏加德罗常数,下列说法正确的是( )
A
A.常温常压下,2.24LCO和 混合气体中含有的碳原子数目为0.1
B.12gC(金刚石)中含有的C-C健数目为
C.标准状况下,将 ,完全溶于水,与水反应转移的电子数目为0.1
D.常温下, 的NaOH溶液中含有的 的数目为
4.标准状况下,将3.36 L CO 气体通入200 mL 1.00 mol·L-1 NaOH溶液中,充分反应后溶液中c(HCO )与
2c(CO )的比值为(不考虑CO 、HCO 的水解)( )
A.l:1 B.1:2 C.2:1 D.1:3
5.阿伏加德罗常数的值为 ,下列说法正确的是( )
A.用电解粗铜的方法精炼铜,当电路中通过的电子数为 时,阳极应有 转化为
B. 中所含 键数目为
C. 含电子数为
D. 晶体中含有 个阳离子
6.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.11g 和 的混合物中含有的离子数目为0.3N
A
B.标准状况下,4.48L 所含的分子数为0.2N
A
C.56gFe与足量水蒸气充分反应,转移电子数为3N
A
D. 溶液中含有的氧原子数为0.4N
A
7. 表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 与足量氧气反应生成 的分子数为
B. 铁与足量稀硝酸反应转移的电子数为
C. 氧气与 硫所含的质子数相等
D. 核素 发生裂变反应: ,净产生的中子 数为10
8.用N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.7.8gNa O 中的离子总数为0.4N
2 2 A
B.pH=2的盐酸中的H+总数为0.01N
A
C.2.3gNa和足量氧气反应转移电子数为0.1N
AD.5.6LH S所含S-H键的数目为0.5N
2 A
9.下列说法正确的是( )
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5molH 所占体积为11.2L
2
③标准状况下,1molH O的体积约为22.4L
2
④标准状况下,28gCO与N 的混合气体的体积约为22.4L
2
⑤各种气体的摩尔体积都约为22.4L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤ B.④⑥ C.③④⑥ D.②④⑥
10.若20g密度为 的硝酸钙溶液里含有1g ,则 的物质的量浓度为( )
A. B. C.2.5d D.1.25d
11.设N 为阿伏加德罗常数的值。下列说法正确的是( )。
A
A.1.4 g 14C中含有的中子数为0. 8N
A
B.2.8g乙烯分子中含有0. 5N 对共用电子
A
C.标准状况下,2. 24 L二氯甲烷(CHCl)中氢原子数目为0. 2N
2 2 A
D.室温下,pH=12的NaS溶液中OH- 数目为0.01N
2 A
12.下列说法正确的是( )
A.摩尔既是物质的数量单位又是物质的质量单位
B.阿伏加德罗常数是12 kg 12C中含有的碳原子数
C.1 mol水分子中含有2 mol氢原子和1 mol氧原子
D.一个NO分子的质量是a g,一个NO 分子的质量是b g,则氧原子的摩尔质量是(b-a) g
2
13.设N 为阿伏伽德罗常数的值。下列说法正确的是( )
A
A.常温常压下,4.4gCO 与NO混合气体中含有的原子总数为0.3N
2 2 A
B.常温常压下11.2L的甲烷气体含有的分子数为0.5N
A
C.1mol·L-1的CuCl 溶液中含有Cl-的数目为2N
2 A
D.在过氧化钠与水的反应中,每反应0.1mol过氧化钠,转移电子的数目为0.2N
A
14.N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.3.6g由CaS和CaO 组成的混合物中含有阴、阳离子总数为0.1N
2 A
B.S 和S 的混合物共6.4g,其中所含硫原子数一定为0.2N .
2 8 A
C.将0.1molCl 溶于水中,溶液中Cl-、ClO-、HClO的数目之和为0.2N
2 AD.标准状况下,11.2L1H37Cl气体中含有的中子数为10N
A
15.N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.0.1L0.5mol/LCH COOH溶液中含有的氢离子数为0.05N
3 A
B.密闭容器中2molNO与1molO 充分反应,产物的分子数为2N
2 A
C.由N(g)+3H(g)⇌2NH (g)△H=-92.2kJ/mol,可知在相同条件下2molN 与6molH 反应方出的热量
2 2 3 2 2
184.4kJ/mol
D.某电池的总反应为Fe+2Fe3+=3Fe2+,当有5.6gFe溶解时电路中有0.2mole-通过
16.N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.某种元素的原子质量是mg,一个12C的原子质量是ng,则wg该原子的物质的量一定是 mol
B.已知R2-离子的核内有n个中子,R的质量数为M,则mgR2-离子里含有电子的物质的量为
C.由N 和CH 组成的混合气体的密度是同温同压下氢气密度的9.2倍,则混合气体中N 和CH 的体积比
2 4 2 4
为4∶1
D.将标准状况下的VLA气体(摩尔质量为Mg·mol-1)溶于0.1L水中,所得溶液的密度为ρg·cm-3,则此溶液
的物质的量浓度为 mol·L-1
17.打火机里装有液态的丙烷和丁烷。下列说法错误的是( )
A.打开打火机开关,分子间距变大
B.摩擦打火石,达到气体着火点
C. 丙烷完全燃烧需要空气约为
D.若n(丙烷):n(丁烷) ,该混合物的摩尔质量为
18.下列溶液Cl-物质的量浓度与200mL1mol·L-1AlCl 溶液中Cl-物质的量浓度相等的是( )
3
A.150mL3mol·L-1NaClO溶液 B.75mL3mol·L-1CaCl 溶液
2
C.150mL3mol·L-1KCl溶液 D.150mL2mol·L-1MgCl 溶液
2
19.2021年4月29日11时23分,搭载空间站天和核心舱的长征五号B遥二运载火箭,在我国文昌航天发
射场升空,任务圆满成功。偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭
2 8 2
的推动力。下列叙述正确的是( )
A.偏二甲肼的摩尔质量为60g
B.6.02×1023个偏二甲肼分子的质量约为60gC.1mol偏二甲肼的质量为60g·mol-1
D.6g偏二甲肼含有N 个偏二甲肼分子
A
20.设N 为阿伏伽德罗常数的值,下列有关叙述正确的是( )
A
A.2HS+SO=3S↓+2H O反应中,每生成1mol氧化产物时转移电子数为N
2 2 2 A
B.物质的量相等的重水与水相差2N 个中子
A
C.乙烯和丙烯组成的28g 混合气体中含氢原子数为4N
A
D.pH=13的1LBa(OH) 溶液中所含有OH-数目为0.2N
2 A
1.设 为阿伏加德罗常数的值。下列说法正确的是( )
A. 含有 键的数目为
B. 的盐酸含有阴离子总数为
C. 与 混合后的分子数目为
D. 与足量 反应生成的 分子数目为
2.设 为阿伏加德罗常数的值.下列说法正确的是( )
A. 所含极性共价键的数目为
B. 晶体中阴、阳离子总数为
C. 与足量 反应生成 的分子数为
D.电解熔融 制 ,电路中通过的电子数为
3.向三个密闭容器中分别充入Ne、H、O 三种气体,下列有关这三种气体的叙述中正确的是( )
2 2
A.温度、压强相同时,三中气体的密度关系:B.质量、温度、压强均相同时,三种气体的体积关系:
C.温度、密度相同时,三种气体的压强关系:
D.温度、压强、体积均相同,三种气体的质量关系:
4.下列叙述错误的是( )
①摩尔是国际单位制中七个基本物理量之一;
②1 mol任何物质都含有约6.02×1023个原子;③6.02×1023就是阿伏加德罗常数;④氢原子的摩尔质量是1
g;⑤HCl的摩尔质量等于1 mol HCl分子的质量;⑥1 mol CO 中含有1 mol碳和2 mol氧。
2
A.①②③ B.②③④
C.②③④⑥ D.全部
5.有BaCl 和NaCl的混合溶液aL, 将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀, 消耗
2
xmolH SO ;另一份滴加AgNO 溶液,使Cl-离子完全沉淀,消耗ymol AgNO 。则原混合溶液中的c(Na+)
2 4 3 3
( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
6.在4L密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生反应:3A(g)+B(g)⇌2C(g)+
xD(g),达到平衡时,生成了2mol C,经测定,D的浓度为0.5mol·L-1,下列判断正确的是( )
A.x=1
B.B的转化率为20%
C.平衡时A的浓度为1.50mol·L-1
D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
7.我国“金牌火箭”长征二号用 NH 做燃料,发生反应:2NH+ 2NO 3N+4H O。设 N 为阿伏
2 4 2 4 2 2 2 A
伽德罗常数的值,下列有关说法正确的是( )
A.标准状况下,22.4L H O 中质子数目为 10 N
2 A
B.16g N H 中含有极性共价键数目为 2.5 N
2 4 A
C.反应生成 1.5molN 时转移的电子数目为 4 N
2 A
D.密闭容器中 2molNO 和 1molO 充分反应生成 NO ,其分子数目为 2 N
2 2 A8.工业上常用“碳氯法”制备MgCl ,原理为MgO+C+Cl MgCl +CO。N 代表阿伏加德罗常数的值,
2 2 2 A
下列叙述错误的是( )
A.反应中断裂1molCl—Cl键,转移的电子数为2N
A
B.反应中消耗6gC,生成CO的体积为11.2L(标准状况)
C.密度、体积均相同的Cl 和CO,CO的分子数更多
2
D.将MgCl 溶于水配成0.1mol·L-1MgC1 溶液,阴离子总数大于0.2N
2 2 A
9.设N 是阿伏加德罗常数的值,下列叙述正确的是( )
A
A.7g环丁烷含有的极性键数为2N
A
B.标准状况下,1.12L HF中含有氢原子数为0.05N
A
C.1L 0.1mol/L HCOONa溶液中,Na+数为0.1N
A
D.氨气与钙发生置换反应生成Ca(NH ) 和2.24LH 时转移的电子数为0.2N
2 2 2 A
10.2021年,我国科学家利用 为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程
中发生反应: ,设 为阿伏伽德罗常数,下列有关说法正确的是( )。
A. 中含有过氧键数目为
B.标况下, 中含有的羟基数为
C.反应过程中HCHO为还原产物
D. 参与反应转移电子数为
11.N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.22.4L(标准状况)氟气所含的质子数为18N
A
B.1mol碘蒸气和1mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2N
A
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
D.1L1mol•L-1溴化铵水溶液中NH 与H+离子数之和大于N
A
12. 为阿伏加德罗常数的值。下列说法正确的是( )A. , 完全反应转移的电子数
为
B.用电解粗铜的方法精炼铜,当电路中通过的电子数为 时,阳极应有 转化为
C.常温下, 的 溶液中,水电离出的 数为
D. 浓度为 的 溶液中,阴离子数为
13.X、Y均为短周期金属元素,同温同压下,0.1molX的单质与足量稀盐酸反应,生成H 体积为VL;
2 1
0.1molY的单质与足量稀硫酸反应,生成H 体积为VL。下列说法错误的是( )
2 2
A.X、Y生成H 的物质的量之比一定为
2
B.X、Y消耗酸的物质的量之比一定为
C.产物中X、Y化合价之比一定为
D.由 一定能确定产物中X、Y的化合价
14.设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1mol/LHCl溶液中,HCl分子的数目为N
A
B.22.4L氢气中,H 分子的数目为N
2 A
C.180g葡萄糖中,C原子的数目为6N
A
D.1molN 中,σ键的数目为3N
2 A
15.下列叙述中正确的是( )
A.常温常压下,32gO 所含的原子数目为2×6.02×1023
2
B.标准状况下,22.4LH O所含的分子数目为6.02×1023
2
C.0.1molFe与足量Cl 充分反应,失去的电子数目为0.2×6.02×1023
2
D.0.5mol•L﹣1的AlCl 溶液中含有的Cl﹣的数目为1.5 ×6.02×1023
316.设阿伏加德罗常数的值为 ,下列说法正确的是( )
A. 与水反应,生成 转移的电子数为
B. (分子结构: )中的共价键数目为
C. 溶液中含有的 离子数为
D.标准状况下,22.4L甲烷和乙烯混合物中含有的氢原子数为
17.用N 表示阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1 mol NaHSO 晶体中含有的阳离子数目为2N
4 A
B.用电解粗铜的方法精炼铜,当阳极质量减轻32 g时,电路中通过的电子数为N
A
C.常温下,1 L pH=9的CHCOONa溶液中,水电离出的H+数目为10–9N
3 A
D.向1 L 0.1 mol·L−1盐酸中滴加氨水至中性,溶液中含有的 数目为0.1N
A
18.13.6gFe和Fe O 的混合物,加入150mL足量的稀硫酸,在标准状况下收集到1.12LH ,向反应后的溶
2 3 2
液中滴加KSCN溶液不变红。为中和过量的稀硫酸,并使Fe元素全部转化为Fe(OH) 沉淀,恰好消耗了
2
200mL3mol/L的NaOH溶液,则该稀HSO 的物质的量浓度为( )
2 4
A.2.25mol/L B.2mol/L C.3mol/L D.0.6mol/L
19.用N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.所含共价键数目均为N 的白磷和甲烷的物质的量相等
A
B.向含1molCl-的NH Cl溶液中加入适量氨水使溶液呈中性,此时溶液中 数目为N
4 A
C.2molSO 与1molO 在密闭容器中充分反应后,容器中的分子总数为2N
2 2 A
D.用铜作电极电解饱和NaCl溶液,当电路上通过0.2mole-时,阴、阳两极产生的气体分子总数为0.2N
A
20.用N 表示阿伏加德罗常数的值。下列叙述正确的有( )
A
①1molFeCl 溶于水形成的胶体中含有N 个Fe(OH) 胶体粒子
3 A 3
②3.9gNa O 固体所含阴离子数为0.05N
2 2 A
③标准状况下,46g乙醇中含有N 个分子
A④常温下,2g氦气所含的原子数目为N
A
⑤1molCl 通入足量的水中,最多生成1molHClO
2
⑥56g铁与氯气在一定条件下充分反应,最多消耗氯气的体积是33.6L
⑦142gNa SO 和NaHPO 的固体混合物中所含阴、阳离子的总数为3N
2 4 2 4 A
A.1个 B.2个 C.3个 D.4个
1.(2022·河北·高考真题)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.3.9gNa O 与足量水反应,转移电子个数为0.1N
2 2 A
B.1.2gMg在空气中燃烧生成MgO和MgN,转移电子个数为0.1N
3 2 A
C.2.7gAl与足量NaOH溶液反应,生成H 的个数为0.1N
2 A
D.6.0gSiO 与足量NaOH溶液反应,所得溶液中SiO 的个数为0.1N
2 A
2.(2022·河北·高考真题) 溶液可作为替代氟利昂的绿色制冷剂。合成 工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的 用 溶液吸收,吸收液直接返回还原工序
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为
D.参与反应的 为1∶1∶1
3.(2022·浙江·高考真题) 为阿伏加德罗常数的值,下列说法正确的是( )
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为C. 含有中子数为
D. 和 于密闭容器中充分反应后, 分子总数为
4.(2021·海南·高考真题) 代表阿伏加德罗常数的值。下列说法正确的是( )
A. 中含有的电子数为1.3
B. 中含有的共价键的数目为0.1
C. 肼 含有的孤电子对数为0.2
D. ,生成 乙烷时断裂的共价键总数为
5.(2021·湖北·高考真题)N 为阿伏加德罗常数的值。下列说法错误的是( )
A
A.23gCHCHOH中sp3杂化的原子数为N
3 2 A
B.0.5molXeF 中氙的价层电子对数为3N
4 A
C.1mol[Cu(H O) ]2+中配位键的个数为4N
2 4 A
D.标准状况下,11.2LCO和H 的混合气体中分子数为0.5N
2 A
6.(2021·全国·高考真题) 为阿伏加德罗常数的值。下列叙述正确的是( )
A. 重水( )中含有的质子数为
B. 的 与 完全反应时转移的电子数为
C. 环状 ( )分子中含有的 键数为
D. 的 溶液中 离子数为
7.(2021·湖南·高考真题) 为阿伏加德罗常数的值。下列说法正确的是( )
A. 含有的中子数为
B. 溶液中含有的 数为C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
8.(2021·浙江·高考真题)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol NH F晶体中含有的共价键数目为3N
4 A
B.CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C.向100mL 0.10mol·L-1FeCl 溶液中加入足量Cu粉充分反应,转移电子数目为0.01N
3 A
D.0.1 mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 2 3 A
9.(2020·海南·高考真题)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.1molHC≡CH分子中所含σ键数为5 N
A
B.1L0.1 mol·L-1的NaCO 溶液含 的数目为0.1 N
2 3 A
C.78 g Na O 与足量水完全反应,电子转移数为N
2 2 A
D.标准状况下,2.24 L C HOH所含氢原子数为0.6 N
2 5 A
10.(2020·北京·高考真题)下列说法正确的是( )
A.同温同压下,O 和CO 的密度相同
2 2
B.质量相同的HO和DO(重水)所含的原子数相同
2 2
C.物质的量相同的CHCHOH和CHOCH 所含共价键数相同
3 2 3 3
D.室温下,pH相同的盐酸和硫酸中,溶质的物质的量浓度相同