文档内容
2025新教材化学高考第一轮
专题五 金属及其化合物
1.陈述Ⅰ和Ⅱ均正确且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
金 属 钠 在 O 中 点 燃 产 生
A 2 Na O 可在潜水艇中作为O 的来源
Na O 2 2 2
2 2
B 碳酸钠受热分解产生CO 用碳酸钠作膨松剂制作面包
2
C 浓硫酸与Fe不反应 可用钢瓶运输浓硫酸
D Zn的金属性比Fe强 船身焊接锌块可减缓船体腐蚀
2.陈述Ⅰ和Ⅱ均正确并具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 用明矾净水 Al(OH) 胶体具有吸附性
3
B Na着火不能用水扑灭 Na可与水反应产生O
2
C 二氧化硅可用于制备光导纤维 二氧化硅是良好的半导体材料
D 用84消毒液进行消毒 NaClO溶液呈碱性
3.氯化亚铜(CuCl)难溶于水,不溶于乙醇,潮湿时易水解氧化,广泛应用于化工、印染、电
镀等行业。由含[Cu(NH ) ]Cl 的印刷线路板刻蚀废液制取CuCl的流程如下图:
3 4 2
下列有关说法正确的是( )
A.“沉铜”时发生了氧化还原反应
B.“沉铜”得到的滤液中大量存在的离子有Na+、NH+、Cl-和OH-
4
C.“浸取”时的离子方程式为SO2−+2Cu2++H O SO2−+2Cu++2H+
3 2 4
D.“洗涤”时宜用乙醇作为洗涤剂
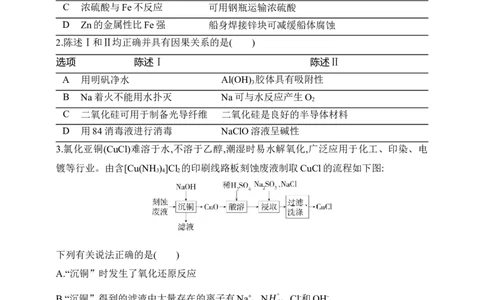
4.如图为常见物质的化合价与类别示意图,其中X、Y、Z、W均含有同一种元素R,下列
有关离子方程式的说法错误的是( )A.若R为Na,则X→Z的离子方程式可以是2Na+2H O 2Na++2OH-+H ↑
2 2
B.若R为Al,则Y→W的离子方程式一定是Al O +6H+ 2Al3++3H O
2 3 2
C.若R为Fe,则W→Z的离子方程式可以是Fe2++2NH ·H O Fe(OH) ↓+2NH+
3 2 2 4
D.若R为Mg,则Y→W的离子方程式可以是MgO+2H+ Mg2++H O
2
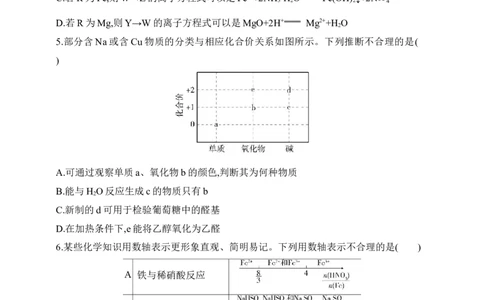
5.部分含Na或含Cu物质的分类与相应化合价关系如图所示。下列推断不合理的是(
)
A.可通过观察单质a、氧化物b的颜色,判断其为何种物质
B.能与H O反应生成c的物质只有b
2
C.新制的d可用于检验葡萄糖中的醛基
D.在加热条件下,e能将乙醇氧化为乙醛
6.某些化学知识用数轴表示更形象直观、简明易记。下列用数轴表示不合理的是( )
A 铁与稀硝酸反应
向烧碱溶液通入SO
B 2
后的产物
Na与O 加热反应的
C 2
产物
D 分散系的分类
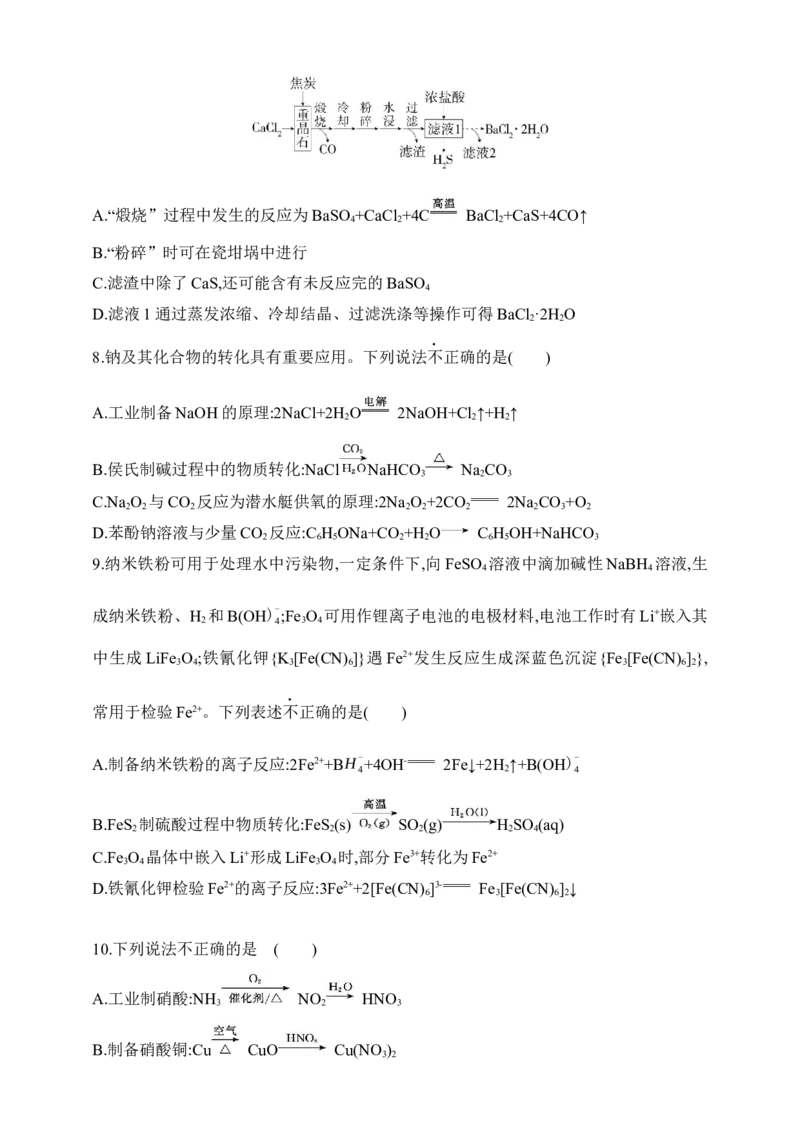
7.实验室模拟工业制备BaCl ·2H O的一种工艺流程如图所示,已知常温下CaS的溶解度
2 2
为0.2 g/L,CaCl 的溶解度较大,且随温度变化不大。下列说法错误的是( )
2A.“煅烧”过程中发生的反应为BaSO +CaCl +4C BaCl +CaS+4CO↑
4 2 2
B.“粉碎”时可在瓷坩埚中进行
C.滤渣中除了CaS,还可能含有未反应完的BaSO
4
D.滤液1通过蒸发浓缩、冷却结晶、过滤洗涤等操作可得BaCl ·2H O
2 2
8.钠及其化合物的转化具有重要应用。下列说法不正确的是( )
A.工业制备NaOH的原理:2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
B.侯氏制碱过程中的物质转化:NaCl NaHCO Na CO
3 2 3
C.Na O 与CO 反应为潜水艇供氧的原理:2Na O +2CO 2Na CO +O
2 2 2 2 2 2 2 3 2
D.苯酚钠溶液与少量CO 反应:C H ONa+CO +H O C H OH+NaHCO
2 6 5 2 2 6 5 3
9.纳米铁粉可用于处理水中污染物,一定条件下,向FeSO 溶液中滴加碱性NaBH 溶液,生
4 4
成纳米铁粉、H 和B(OH)- ;Fe O 可用作锂离子电池的电极材料,电池工作时有Li+嵌入其
2 4 3 4
中生成LiFe O ;铁氰化钾{K [Fe(CN) ]}遇Fe2+发生反应生成深蓝色沉淀{Fe [Fe(CN) ] },
3 4 3 6 3 6 2
常用于检验Fe2+。下列表述不正确的是( )
A.制备纳米铁粉的离子反应:2Fe2++BH- +4OH- 2Fe↓+2H ↑+B(OH)-
4 2 4
B.FeS 制硫酸过程中物质转化:FeS (s) SO (g) H SO (aq)
2 2 2 2 4
C.Fe O 晶体中嵌入Li+形成LiFe O 时,部分Fe3+转化为Fe2+
3 4 3 4
D.铁氰化钾检验Fe2+的离子反应:3Fe2++2[Fe(CN) ]3- Fe [Fe(CN) ] ↓
6 3 6 2
10.下列说法不正确的是 ( )
A.工业制硝酸:NH NO HNO
3 2 3
B.制备硝酸铜:Cu CuO Cu(NO )
3 2C.ClO 除去NO的反应:3ClO +5NO+4H O 3HCl+5HNO
2 2 2 3
D.过量的Fe粉与稀HNO 反应:3Fe+8H++2NO- 3Fe2++2NO↑+4H O
3 3 2
11.纯碱在食品加工、制药等方面有重要应用。实验室以碳酸氢铵(温度高于35 ℃分解)
和食盐水为原料模拟纯碱的制取,流程如下:
下列说法错误的是( )
A.“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下
B.在“搅拌、加热”对应的温度下,NH HCO 、NaCl、NaHCO 、NH Cl 四种物质
4 3 3 4
中,NaHCO 的溶解度最低
3
C.“洗涤、抽滤”操作中用到的主要仪器有:普通漏斗、烧杯、玻璃棒
D.利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为酚酞,第2指示剂
为甲基橙
12.生产软磁铁氧体的主要原料是 α-FeOOH,以硫铁矿(主要成分是 FeS ,含少量Al O 、
2 2 3
SiO 和Fe O )为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的
2 3 4
是( )
物质 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀pH(25 ℃) 1.9 7.6 4.0
沉淀完全pH(25 ℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸
C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成α-FeOOH
13.以钢铁厂灰渣(主要成分为ZnO,并含少量CuO、Fe O 等)为原料制备氧化锌的一种工
2 3
艺流程如下:已知:过量氨水使ZnO、CuO溶解,转化为[Zn(NH ) ]2+和[Cu(NH ) ]2+配离子。
3 4 3 4
下列说法正确的是( )
A.滤液①中大量存在HCO-、CO2−、OH-
3 3
B.滤渣②的成分为Cu
C.“ 蒸 氨 沉 锌 ” 过 程 中 反 应 的 化 学 方 程 式 为 2[Zn(NH ) ]CO +H O
3 4 3 2
8NH ↑+ZnCO ·Zn(OH) ↓+CO ↑
3 3 2 2
D.“煅烧”过程需使用蒸发皿
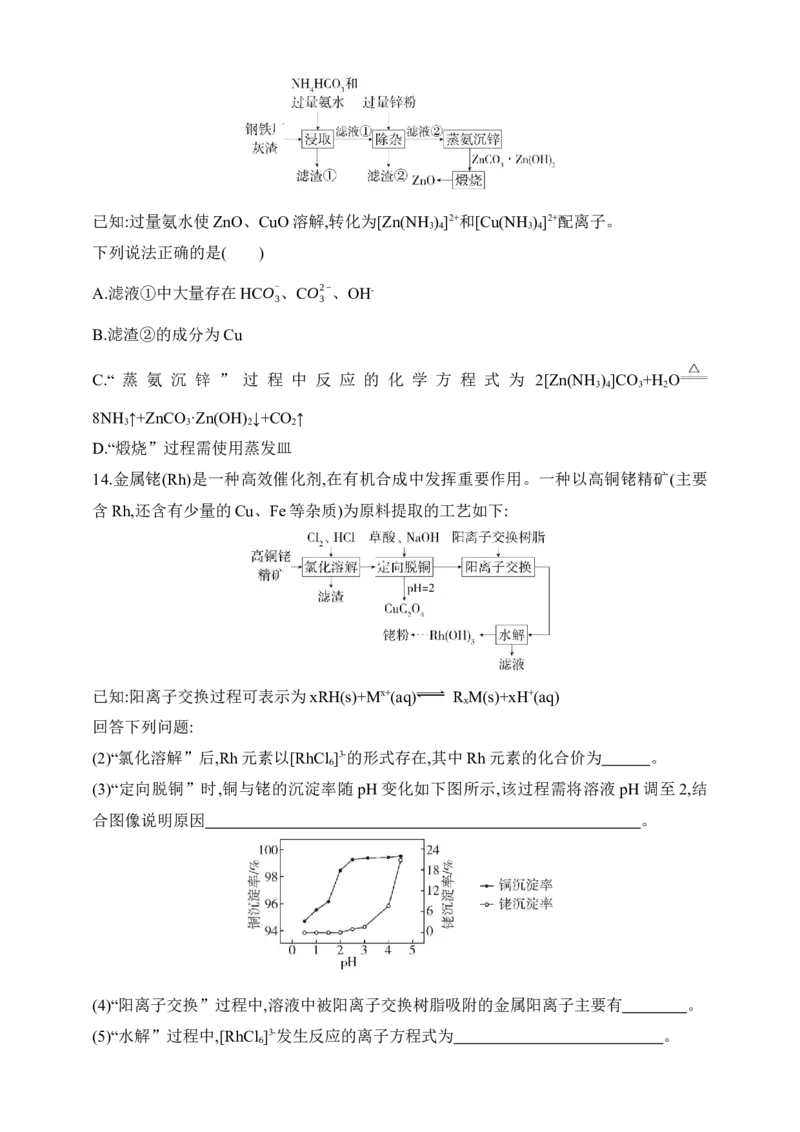
14.金属铑(Rh)是一种高效催化剂,在有机合成中发挥重要作用。一种以高铜铑精矿(主要
含Rh,还含有少量的Cu、Fe等杂质)为原料提取的工艺如下:
已知:阳离子交换过程可表示为xRH(s)+Mx+(aq) R M(s)+xH+(aq)
x
回答下列问题:
(2)“氯化溶解”后,Rh元素以[RhCl ]3-的形式存在,其中Rh元素的化合价为 。
6
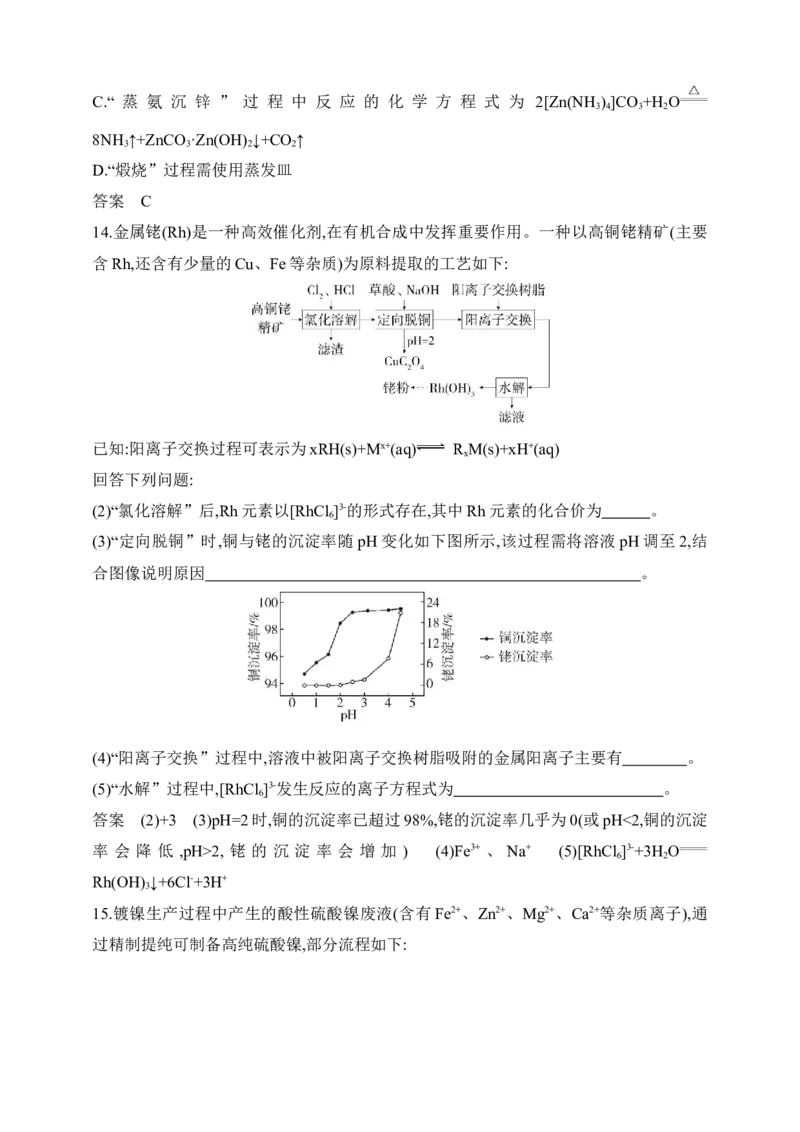
(3)“定向脱铜”时,铜与铑的沉淀率随pH变化如下图所示,该过程需将溶液pH调至2,结
合图像说明原因 。
(4)“阳离子交换”过程中,溶液中被阳离子交换树脂吸附的金属阳离子主要有 。
(5)“水解”过程中,[RhCl ]3-发生反应的离子方程式为 。
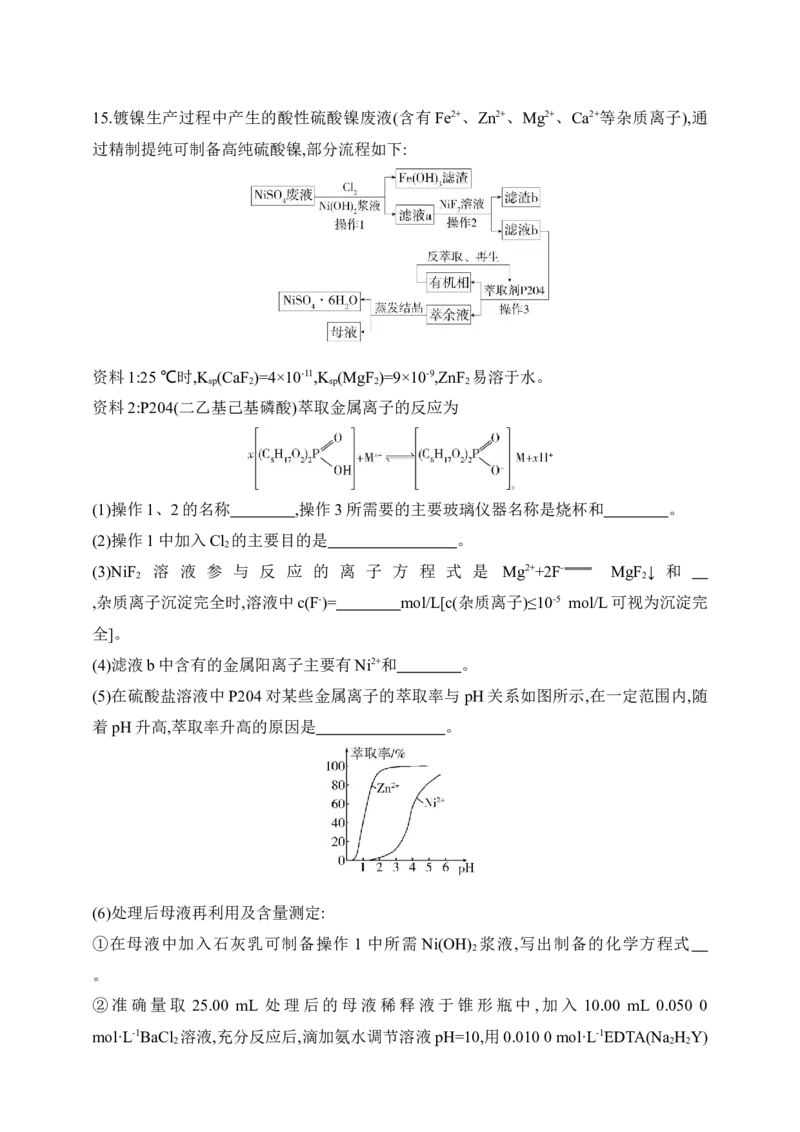
615.镀镍生产过程中产生的酸性硫酸镍废液(含有Fe2+、Zn2+、Mg2+、Ca2+等杂质离子),通
过精制提纯可制备高纯硫酸镍,部分流程如下:
资料1:25 ℃时,K (CaF )=4×10-11,K (MgF )=9×10-9,ZnF 易溶于水。
sp 2 sp 2 2
资料2:P204(二乙基己基磷酸)萃取金属离子的反应为
(1)操作1、2的名称 ,操作3所需要的主要玻璃仪器名称是烧杯和 。
(2)操作1中加入Cl 的主要目的是 。
2
(3)NiF 溶 液 参 与 反 应 的 离 子 方 程 式 是 Mg2++2F- MgF ↓ 和
2 2
,杂质离子沉淀完全时,溶液中c(F-)= mol/L[c(杂质离子)≤10-5 mol/L可视为沉淀完
全]。
(4)滤液b中含有的金属阳离子主要有Ni2+和 。
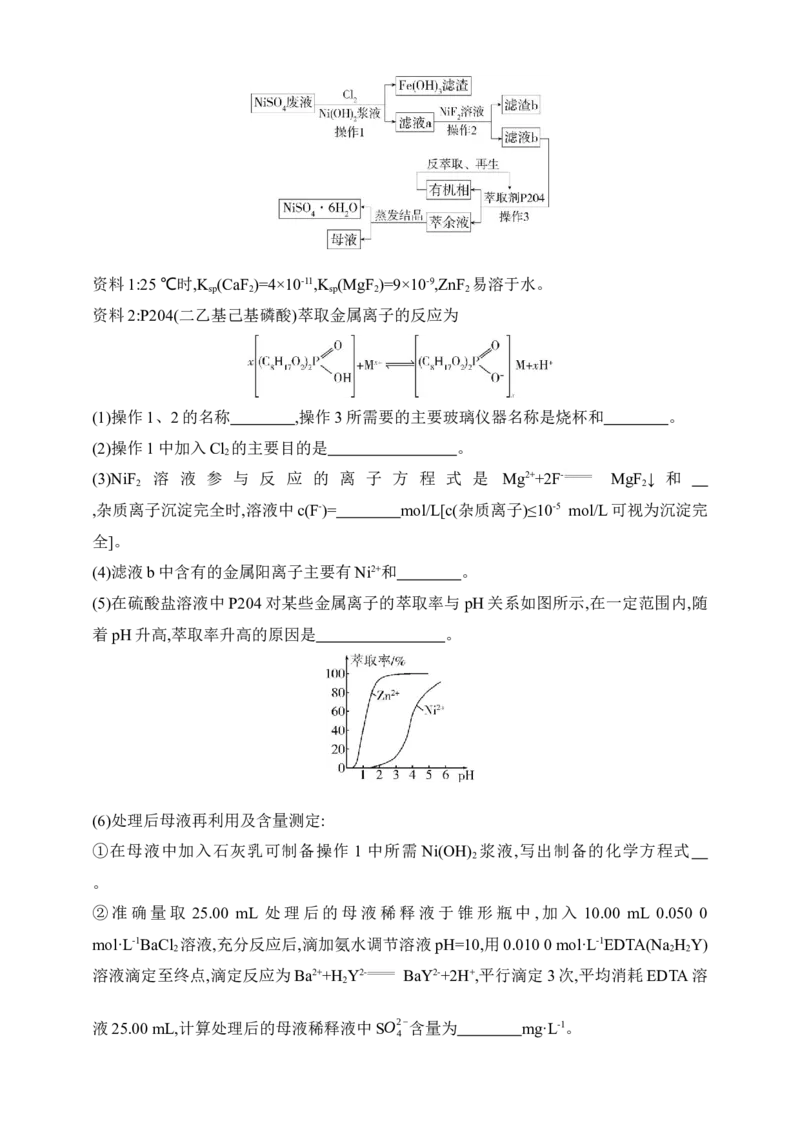
(5)在硫酸盐溶液中P204对某些金属离子的萃取率与 pH关系如图所示,在一定范围内,随
着pH升高,萃取率升高的原因是 。
(6)处理后母液再利用及含量测定:
①在母液中加入石灰乳可制备操作 1 中所需 Ni(OH) 浆液,写出制备的化学方程式
2
。
②准确量取 25.00 mL 处理后的母液稀释液于锥形瓶中,加入 10.00 mL 0.050 0
mol·L-1BaCl 溶液,充分反应后,滴加氨水调节溶液pH=10,用0.010 0 mol·L-1EDTA(Na H Y)
2 2 2溶液滴定至终点,滴定反应为Ba2++H Y2- BaY2-+2H+,平行滴定3次,平均消耗EDTA溶
2
液25.00 mL,计算处理后的母液稀释液中SO2−含量为 mg·L-1。
4
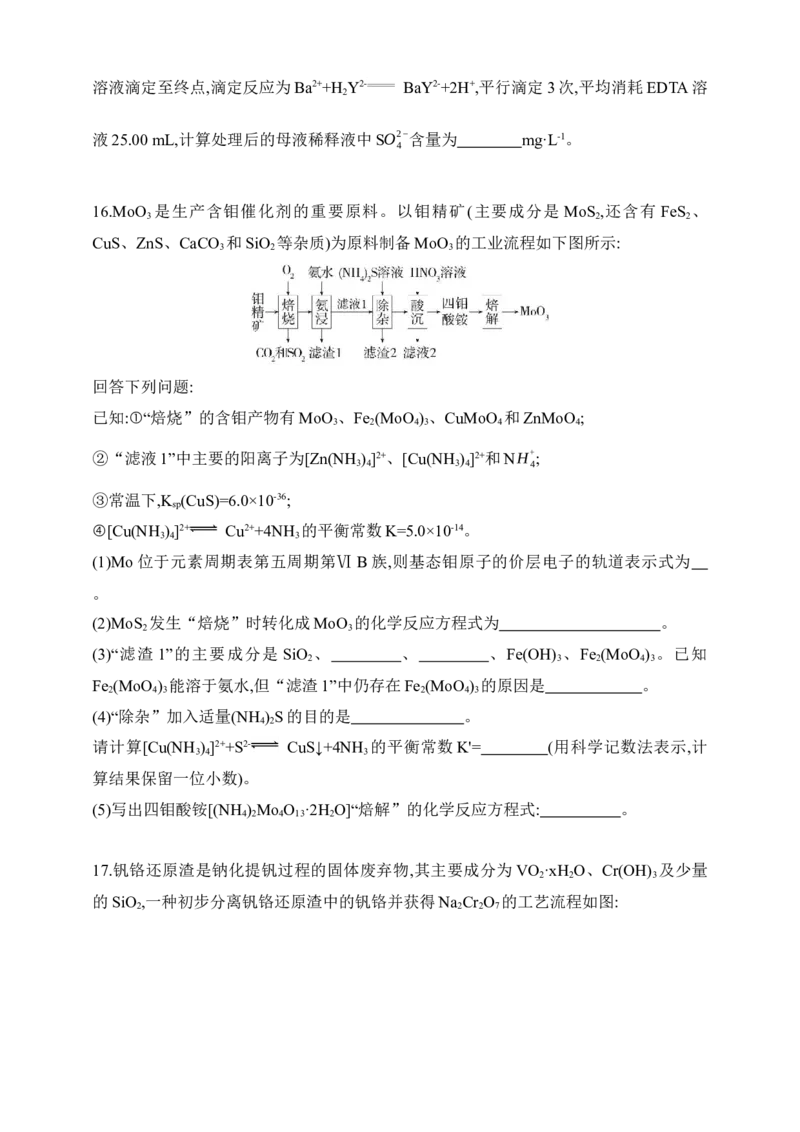
16.MoO 是生产含钼催化剂的重要原料。以钼精矿(主要成分是 MoS ,还含有 FeS 、
3 2 2
CuS、ZnS、CaCO 和SiO 等杂质)为原料制备MoO 的工业流程如下图所示:
3 2 3
回答下列问题:
已知:①“焙烧”的含钼产物有MoO 、Fe (MoO ) 、CuMoO 和ZnMoO ;
3 2 4 3 4 4
②“滤液1”中主要的阳离子为[Zn(NH ) ]2+、[Cu(NH ) ]2+和NH+ ;
3 4 3 4 4
③常温下,K (CuS)=6.0×10-36;
sp
④[Cu(NH ) ]2+ Cu2++4NH 的平衡常数K=5.0×10-14。
3 4 3
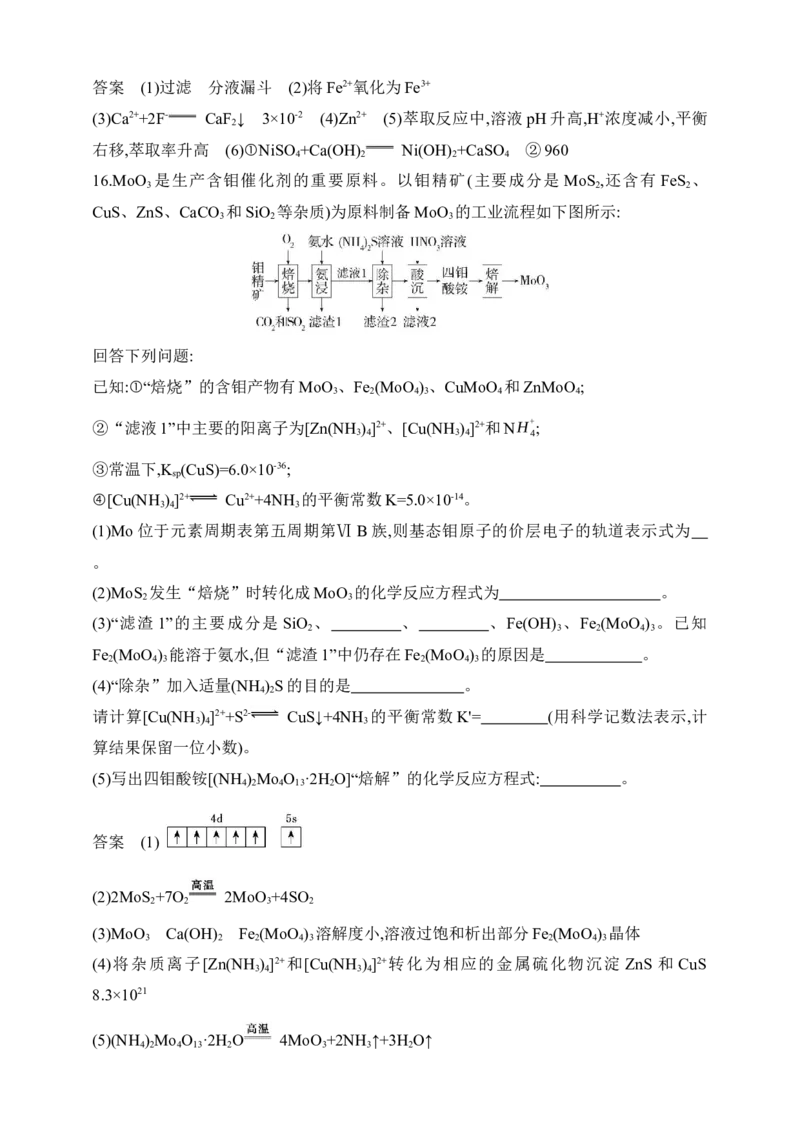
(1)Mo位于元素周期表第五周期第Ⅵ B族,则基态钼原子的价层电子的轨道表示式为
。
(2)MoS 发生“焙烧”时转化成MoO 的化学反应方程式为 。
2 3
(3)“滤渣 1”的主要成分是 SiO 、 、 、Fe(OH) 、Fe (MoO ) 。已知
2 3 2 4 3
Fe (MoO ) 能溶于氨水,但“滤渣1”中仍存在Fe (MoO ) 的原因是 。
2 4 3 2 4 3
(4)“除杂”加入适量(NH ) S的目的是 。
4 2
请计算[Cu(NH ) ]2++S2- CuS↓+4NH 的平衡常数K'= (用科学记数法表示,计
3 4 3
算结果保留一位小数)。
(5)写出四钼酸铵[(NH ) Mo O ·2H O]“焙解”的化学反应方程式: 。
4 2 4 13 2
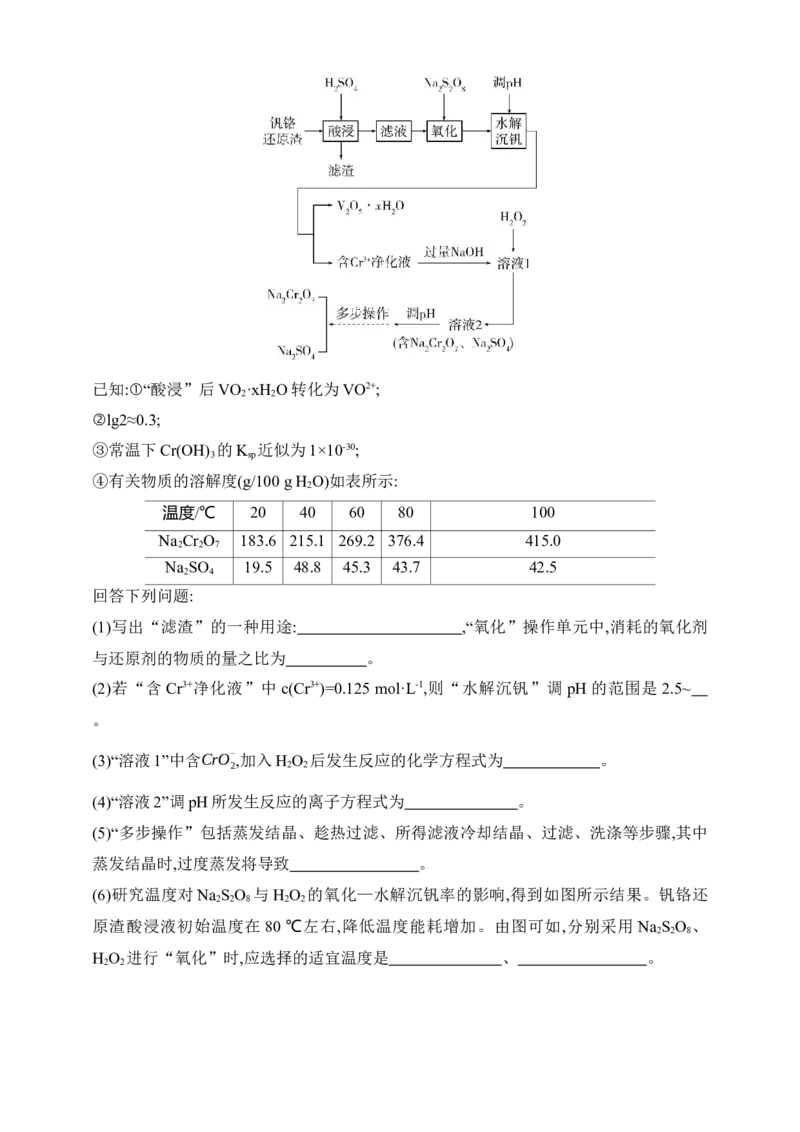
17.钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO ·xH O、Cr(OH) 及少量
2 2 3
的SiO ,一种初步分离钒铬还原渣中的钒铬并获得Na Cr O 的工艺流程如图:
2 2 2 7已知:①“酸浸”后VO ·xH O转化为VO2+;
2 2
②lg2≈0.3;
③常温下Cr(OH) 的K 近似为1×10-30;
3 sp
④有关物质的溶解度(g/100 g H O)如表所示:
2
温度/℃ 20 40 60 80 100
Na Cr O 183.6 215.1 269.2 376.4 415.0
2 2 7
Na SO 19.5 48.8 45.3 43.7 42.5
2 4
回答下列问题:
(1)写出“滤渣”的一种用途: ,“氧化”操作单元中,消耗的氧化剂
与还原剂的物质的量之比为 。
(2)若“含 Cr3+净化液”中 c(Cr3+)=0.125 mol·L-1,则“水解沉钒”调 pH的范围是 2.5~
。
(3)“溶液1”中含CrO- ,加入H O 后发生反应的化学方程式为 。
2 2 2
(4)“溶液2”调pH所发生反应的离子方程式为 。
(5)“多步操作”包括蒸发结晶、趁热过滤、所得滤液冷却结晶、过滤、洗涤等步骤,其中
蒸发结晶时,过度蒸发将导致 。
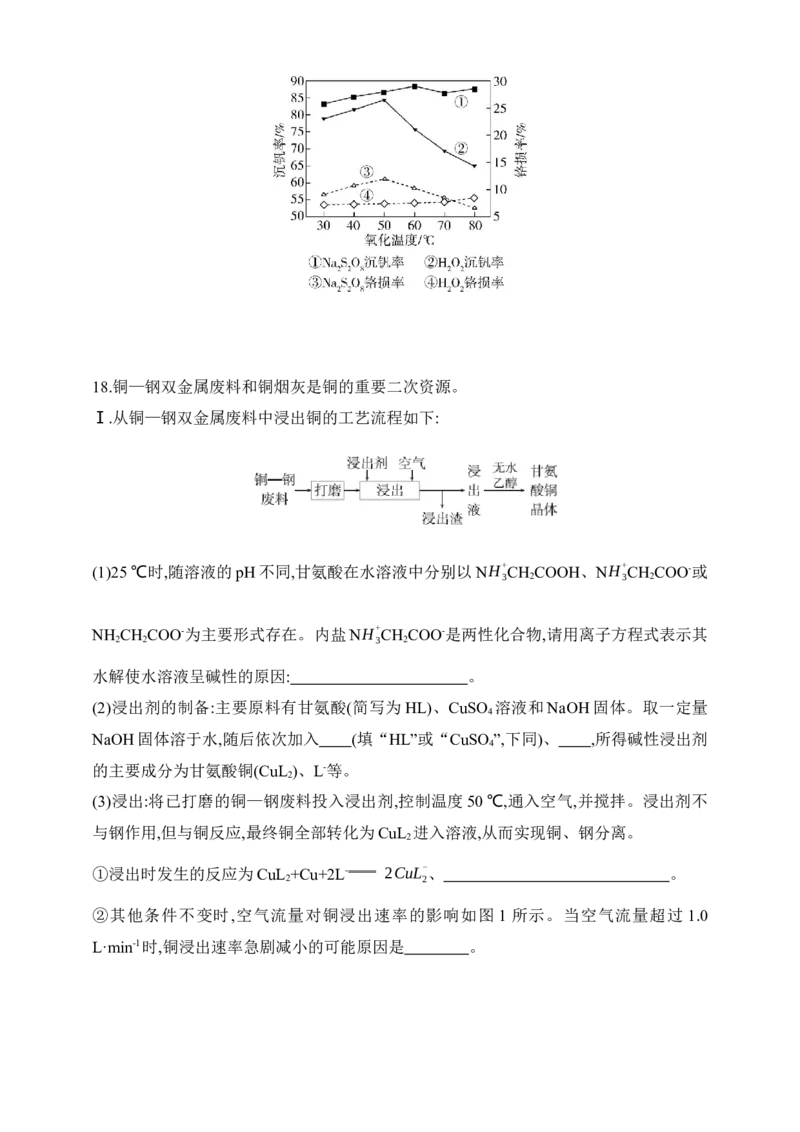
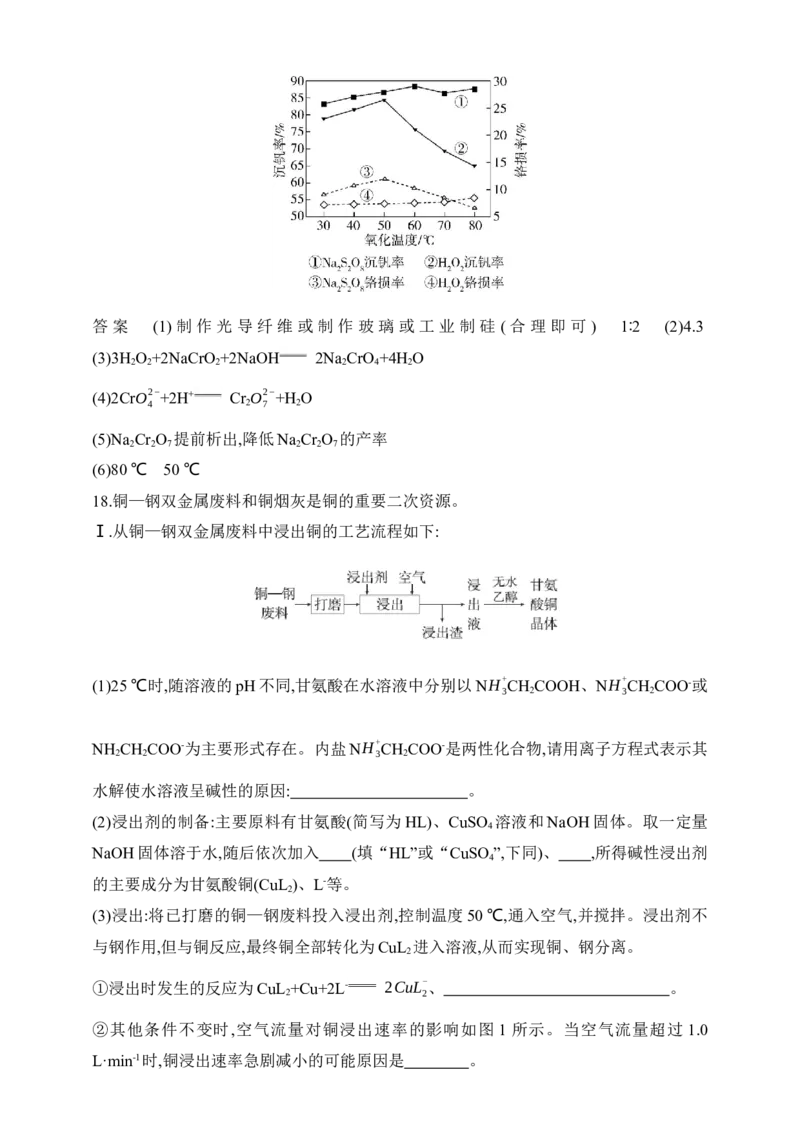
(6)研究温度对Na S O 与H O 的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还
2 2 8 2 2
原渣酸浸液初始温度在 80 ℃左右,降低温度能耗增加。由图可如,分别采用Na S O 、
2 2 8
H O 进行“氧化”时,应选择的适宜温度是 、 。
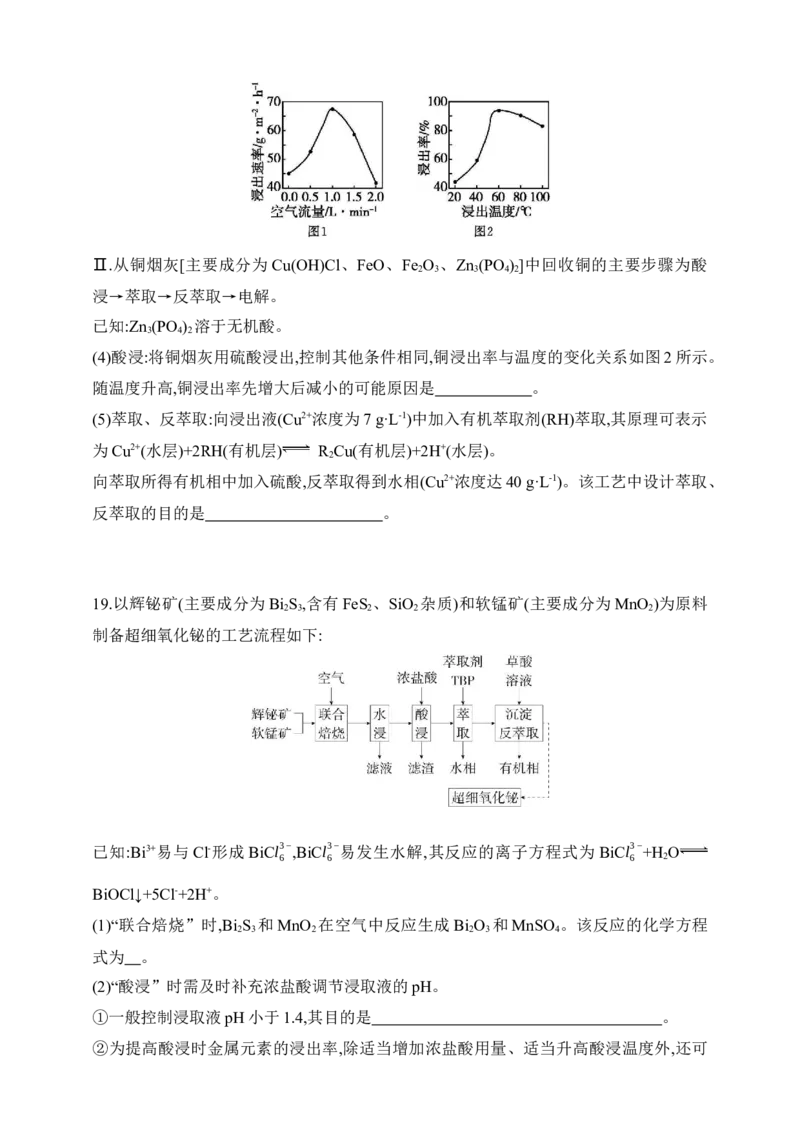
2 218.铜—钢双金属废料和铜烟灰是铜的重要二次资源。
Ⅰ.从铜—钢双金属废料中浸出铜的工艺流程如下:
(1)25 ℃时,随溶液的pH不同,甘氨酸在水溶液中分别以NH+ CH COOH、NH+ CH COO-或
3 2 3 2
NH CH COO-为主要形式存在。内盐NH+ CH COO-是两性化合物,请用离子方程式表示其
2 2 3 2
水解使水溶液呈碱性的原因: 。
(2)浸出剂的制备:主要原料有甘氨酸(简写为HL)、CuSO 溶液和NaOH固体。取一定量
4
NaOH固体溶于水,随后依次加入 (填“HL”或“CuSO ”,下同)、 ,所得碱性浸出剂
4
的主要成分为甘氨酸铜(CuL )、L-等。
2
(3)浸出:将已打磨的铜—钢废料投入浸出剂,控制温度50 ℃,通入空气,并搅拌。浸出剂不
与钢作用,但与铜反应,最终铜全部转化为CuL 进入溶液,从而实现铜、钢分离。
2
①浸出时发生的反应为CuL +Cu+2L- 2CuL-、 。
2 2
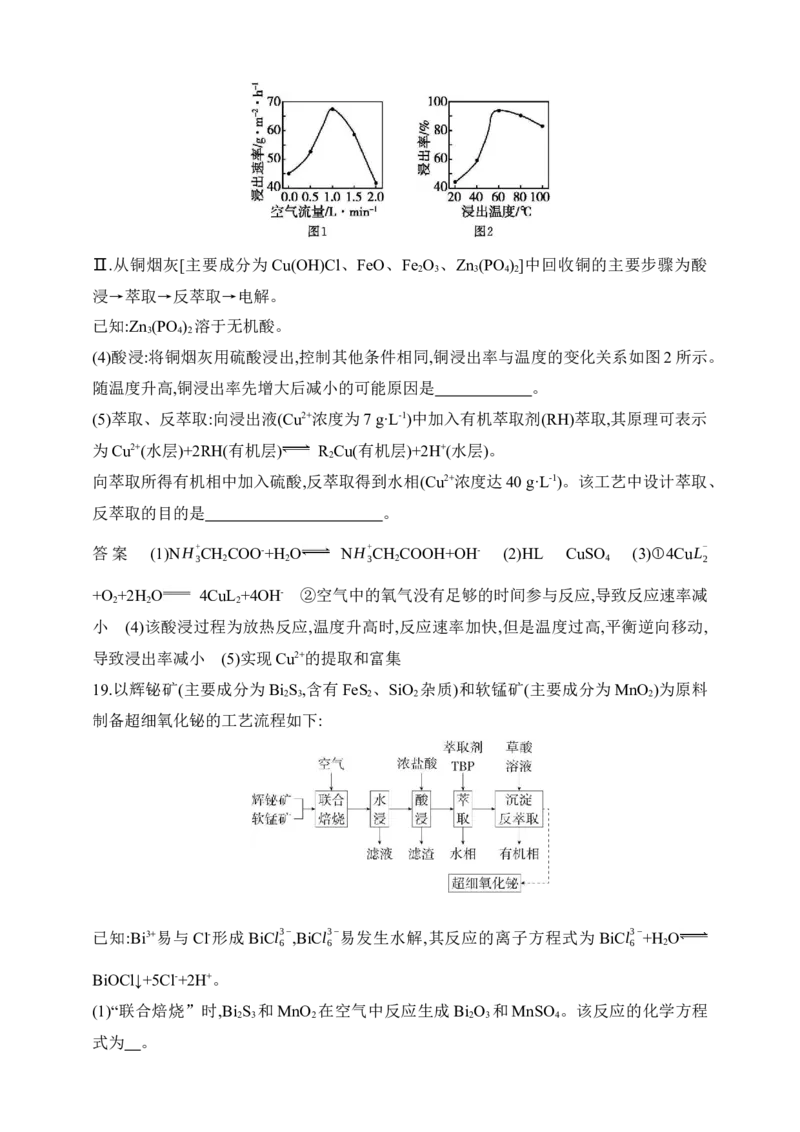
②其他条件不变时,空气流量对铜浸出速率的影响如图 1 所示。当空气流量超过 1.0
L·min-1时,铜浸出速率急剧减小的可能原因是 。Ⅱ.从铜烟灰[主要成分为Cu(OH)Cl、FeO、Fe O 、Zn (PO ) ]中回收铜的主要步骤为酸
2 3 3 4 2
浸→萃取→反萃取→电解。
已知:Zn (PO ) 溶于无机酸。
3 4 2
(4)酸浸:将铜烟灰用硫酸浸出,控制其他条件相同,铜浸出率与温度的变化关系如图2所示。
随温度升高,铜浸出率先增大后减小的可能原因是 。
(5)萃取、反萃取:向浸出液(Cu2+浓度为7 g·L-1)中加入有机萃取剂(RH)萃取,其原理可表示
为Cu2+(水层)+2RH(有机层) R Cu(有机层)+2H+(水层)。
2
向萃取所得有机相中加入硫酸,反萃取得到水相(Cu2+浓度达40 g·L-1)。该工艺中设计萃取、
反萃取的目的是 。
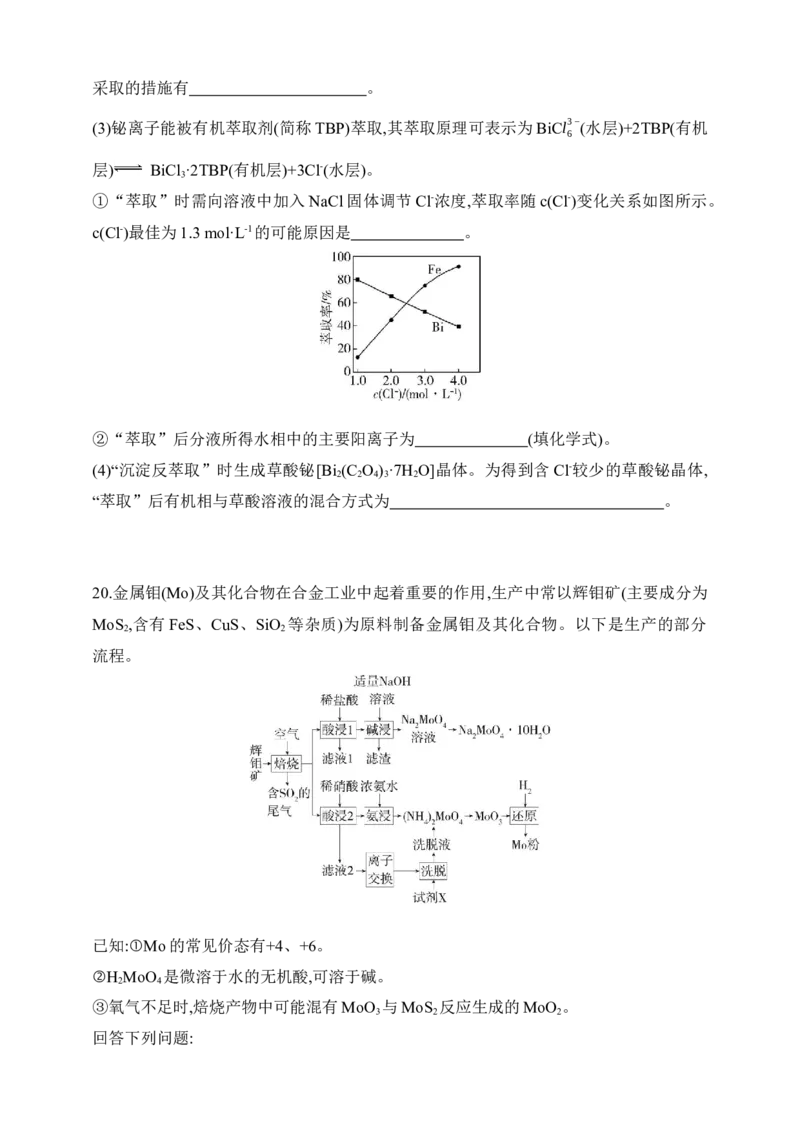
19.以辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)和软锰矿(主要成分为MnO )为原料
2 3 2 2 2
制备超细氧化铋的工艺流程如下:
已知:Bi3+易与Cl-形成BiCl3−,BiCl3−易发生水解,其反应的离子方程式为 BiCl3−+H O
6 6 6 2
BiOCl↓+5Cl-+2H+。
(1)“联合焙烧”时,Bi S 和MnO 在空气中反应生成Bi O 和MnSO 。该反应的化学方程
2 3 2 2 3 4
式为 。
(2)“酸浸”时需及时补充浓盐酸调节浸取液的pH。
①一般控制浸取液pH小于1.4,其目的是 。
②为提高酸浸时金属元素的浸出率,除适当增加浓盐酸用量、适当升高酸浸温度外,还可采取的措施有 。
(3)铋离子能被有机萃取剂(简称TBP)萃取,其萃取原理可表示为BiCl3−(水层)+2TBP(有机
6
层) BiCl ·2TBP(有机层)+3Cl-(水层)。
3
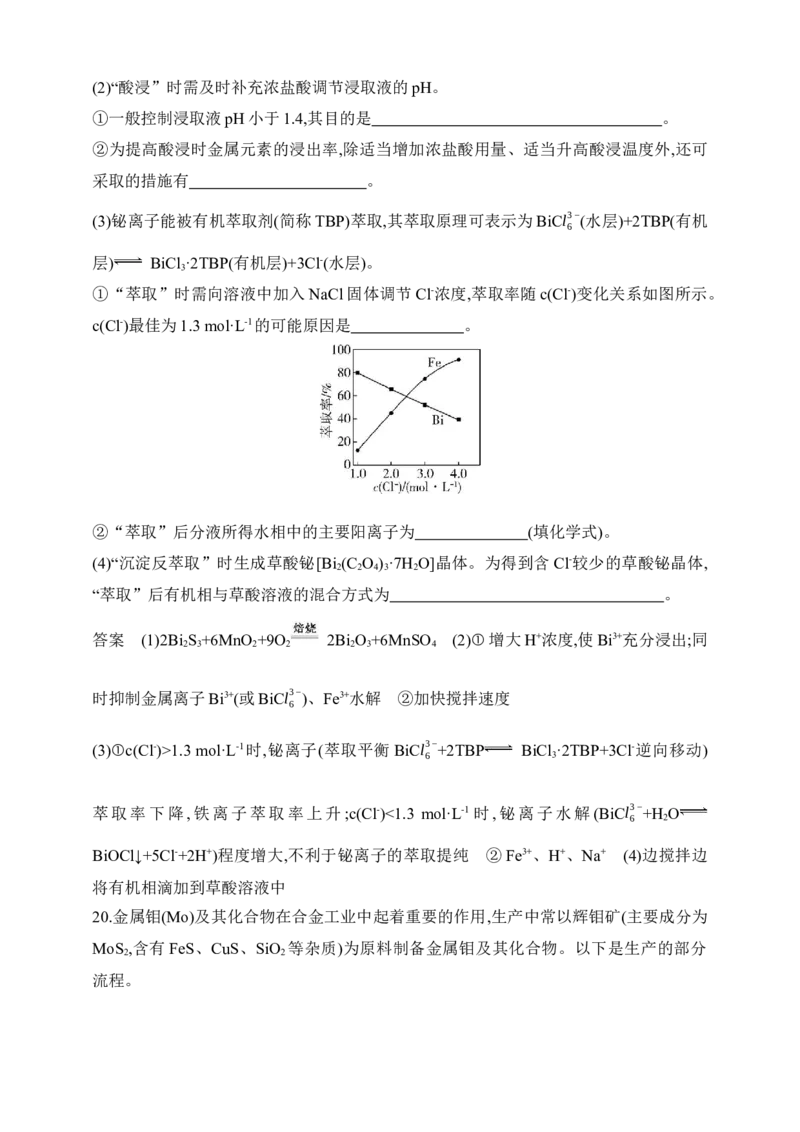
①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。
c(Cl-)最佳为1.3 mol·L-1的可能原因是 。
②“萃取”后分液所得水相中的主要阳离子为 (填化学式)。
(4)“沉淀反萃取”时生成草酸铋[Bi (C O ) ·7H O]晶体。为得到含Cl-较少的草酸铋晶体,
2 2 4 3 2
“萃取”后有机相与草酸溶液的混合方式为 。
20.金属钼(Mo)及其化合物在合金工业中起着重要的作用,生产中常以辉钼矿(主要成分为
MoS ,含有FeS、CuS、SiO 等杂质)为原料制备金属钼及其化合物。以下是生产的部分
2 2
流程。
已知:①Mo的常见价态有+4、+6。
②H MoO 是微溶于水的无机酸,可溶于碱。
2 4
③氧气不足时,焙烧产物中可能混有MoO 与MoS 反应生成的MoO 。
3 2 2
回答下列问题:(1)焙烧的产物中Mo元素主要以MoO 、MoO2−盐的形式存在。生成MoO 的反应的化学
3 4 3
方程式为 。
(2)与酸浸1相比,酸浸2使用稀硝酸的优点是 ,但是缺
点是会产生NO 造成污染。
x
(3)滤渣的成分主要是 。碱浸时pH不宜过大,原因是 。
(4)已知离子交换环节中,阴离子交换树脂 R—OH 的工作原理为 2R—OH+MeMoO
4
R MoO +Me(OH) (Me代表金属阳离子),洗脱时使用的试剂X为 。
2 4 2
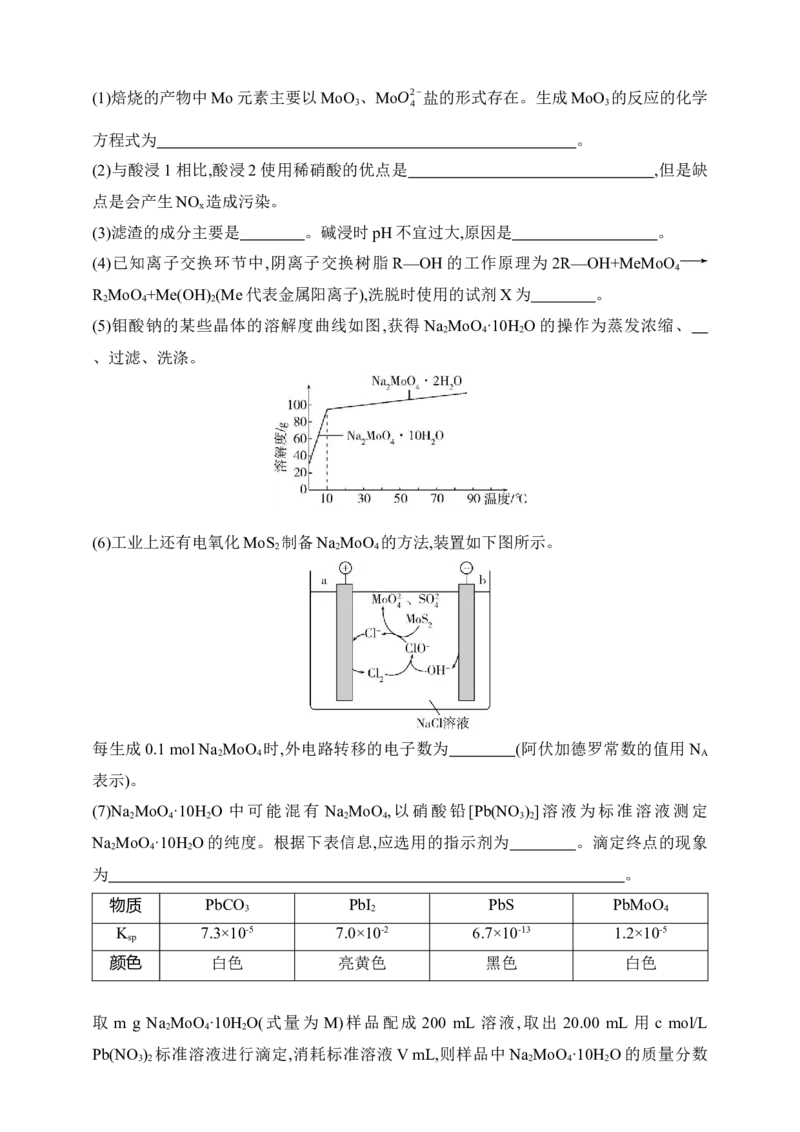
(5)钼酸钠的某些晶体的溶解度曲线如图,获得Na MoO ·10H O的操作为蒸发浓缩、
2 4 2
、过滤、洗涤。
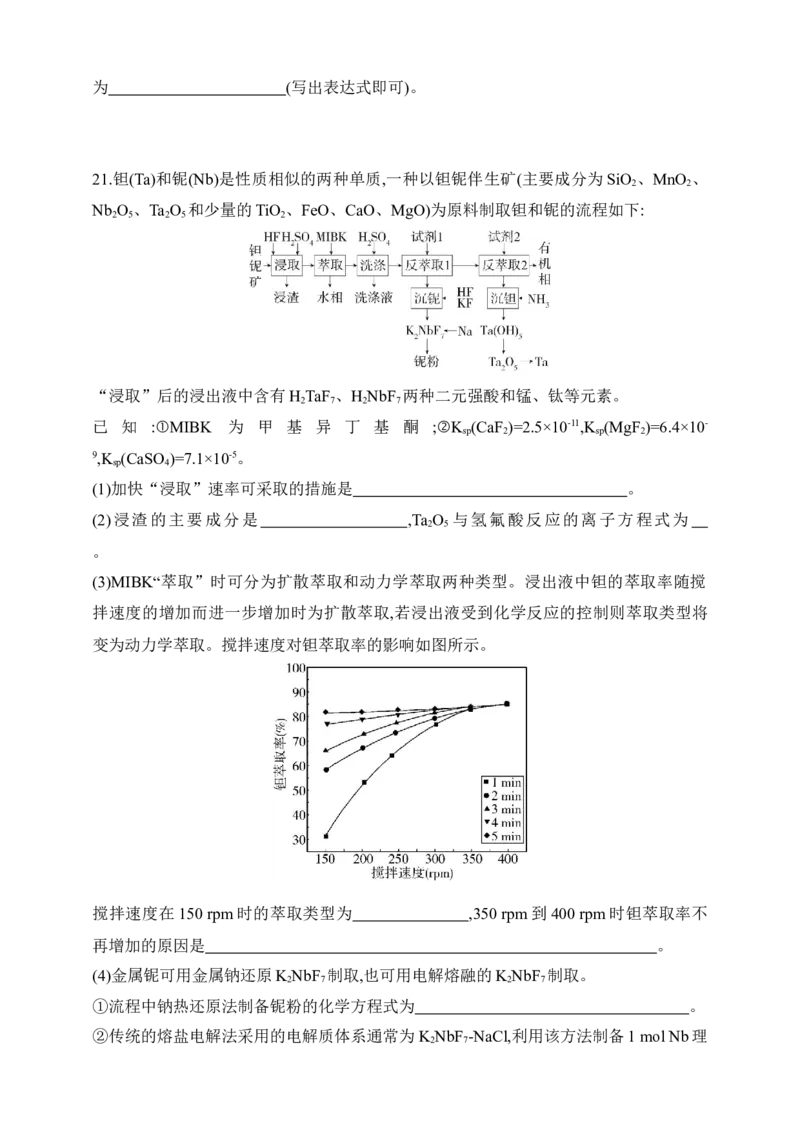
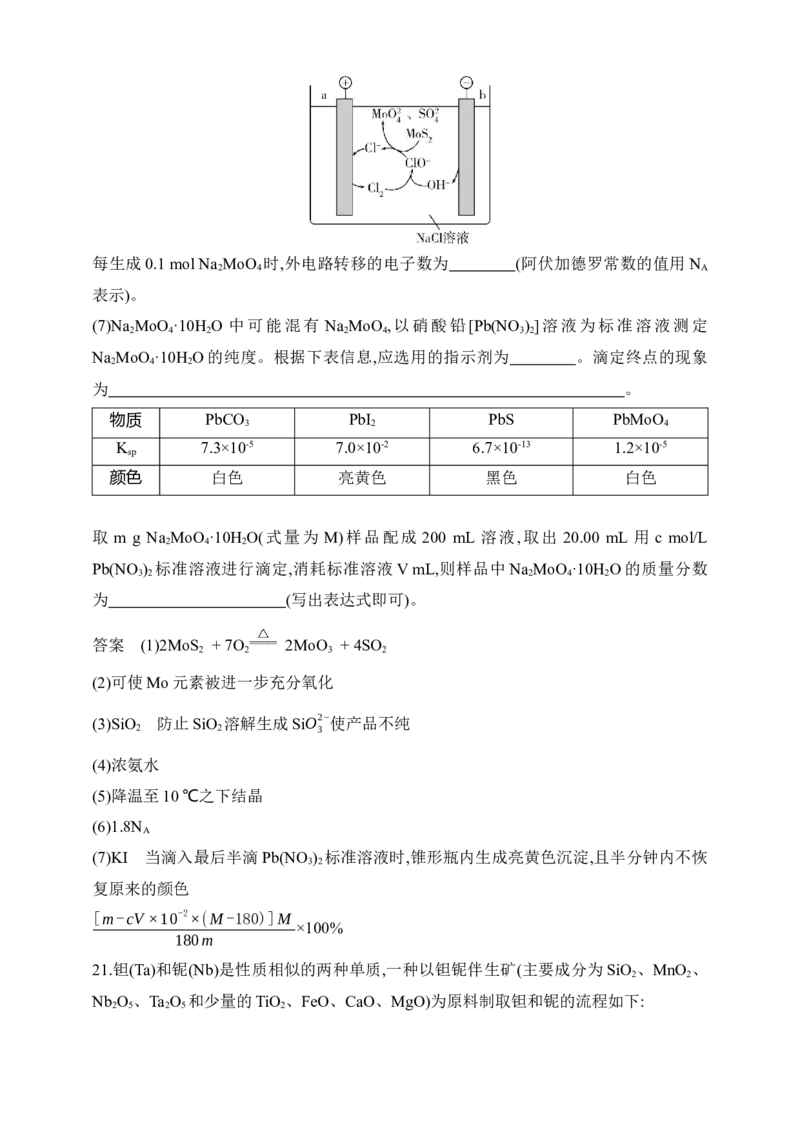
(6)工业上还有电氧化MoS 制备Na MoO 的方法,装置如下图所示。
2 2 4
每生成0.1 mol Na MoO 时,外电路转移的电子数为 (阿伏加德罗常数的值用N
2 4 A
表示)。
(7)Na MoO ·10H O 中可能混有 Na MoO ,以硝酸铅[Pb(NO ) ]溶液为标准溶液测定
2 4 2 2 4 3 2
Na MoO ·10H O的纯度。根据下表信息,应选用的指示剂为 。滴定终点的现象
2 4 2
为 。
物质 PbCO PbI PbS PbMoO
3 2 4
K 7.3×10-5 7.0×10-2 6.7×10-13 1.2×10-5
sp
颜色 白色 亮黄色 黑色 白色
取 m g Na MoO ·10H O(式量为 M)样品配成 200 mL 溶液,取出 20.00 mL 用 c mol/L
2 4 2
Pb(NO ) 标准溶液进行滴定,消耗标准溶液 V mL,则样品中Na MoO ·10H O的质量分数
3 2 2 4 2为 (写出表达式即可)。
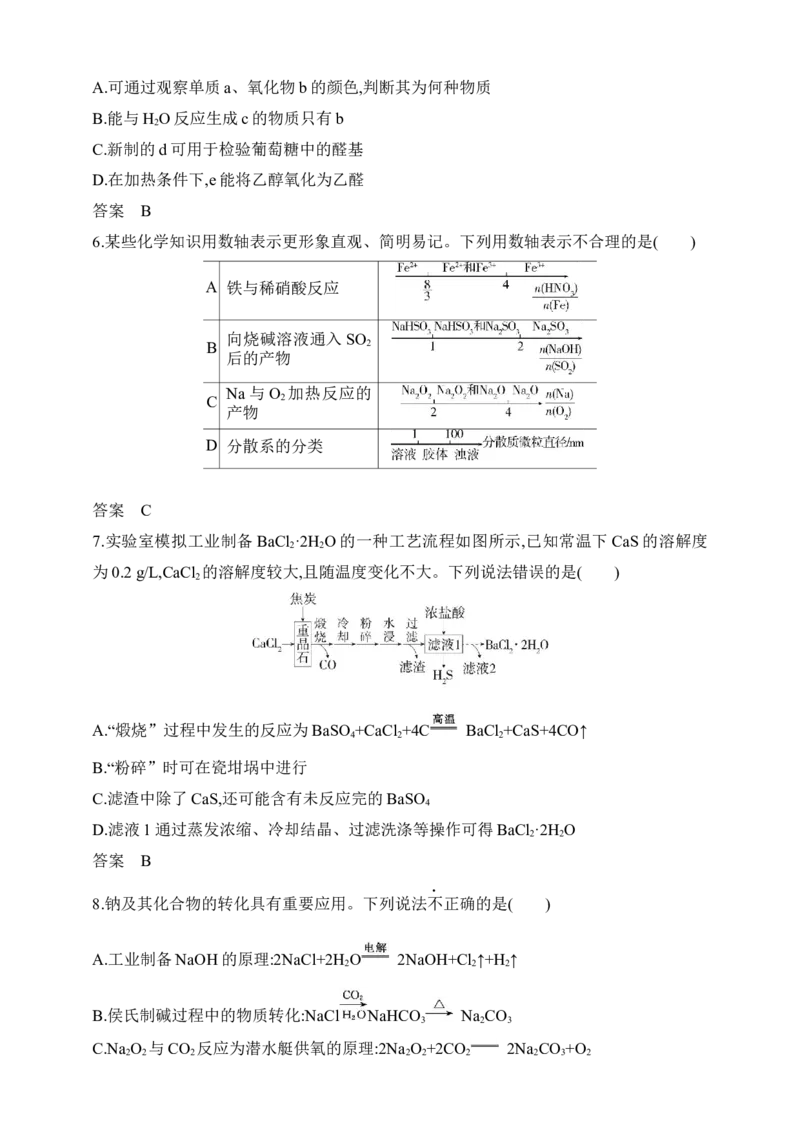
21.钽(Ta)和铌(Nb)是性质相似的两种单质,一种以钽铌伴生矿(主要成分为SiO 、MnO 、
2 2
Nb O 、Ta O 和少量的TiO 、FeO、CaO、MgO)为原料制取钽和铌的流程如下:
2 5 2 5 2
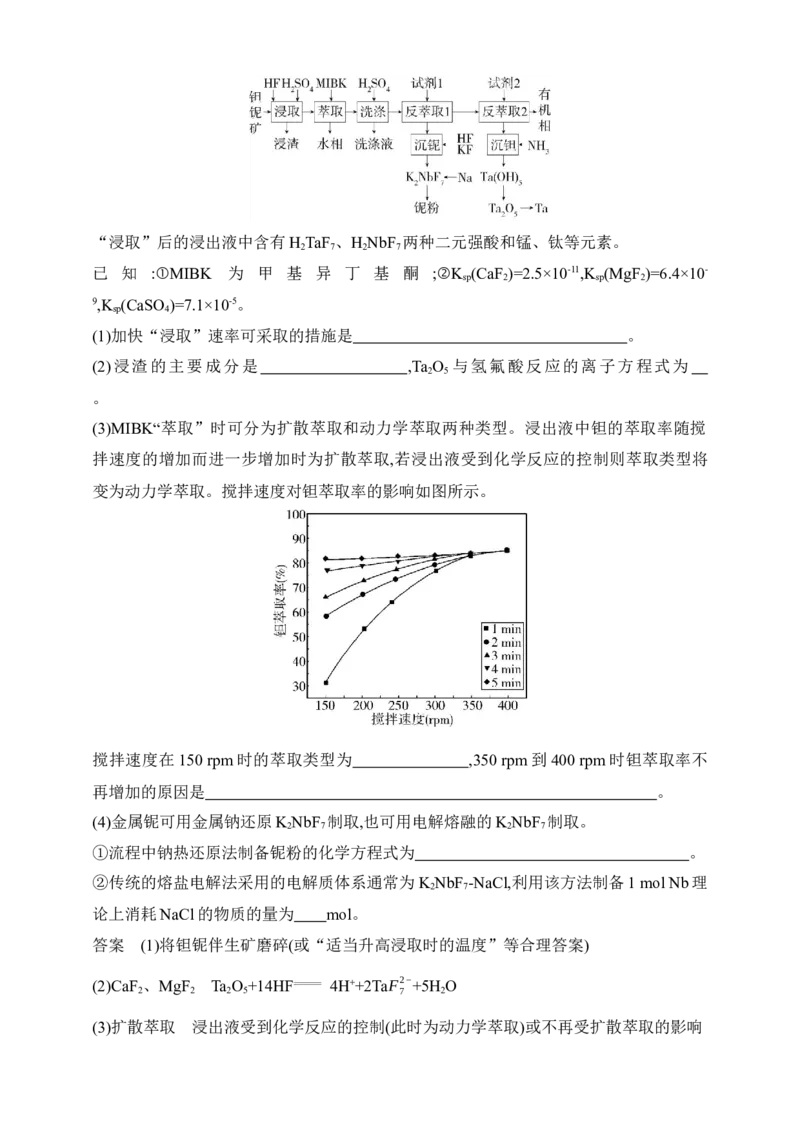
“浸取”后的浸出液中含有H TaF 、H NbF 两种二元强酸和锰、钛等元素。
2 7 2 7
已 知 :①MIBK 为 甲 基 异 丁 基 酮 ;②K (CaF )=2.5×10-11,K (MgF )=6.4×10-
sp 2 sp 2
9,K (CaSO )=7.1×10-5。
sp 4
(1)加快“浸取”速率可采取的措施是 。
(2)浸渣的主要成分是 ,Ta O 与氢氟酸反应的离子方程式为
2 5
。
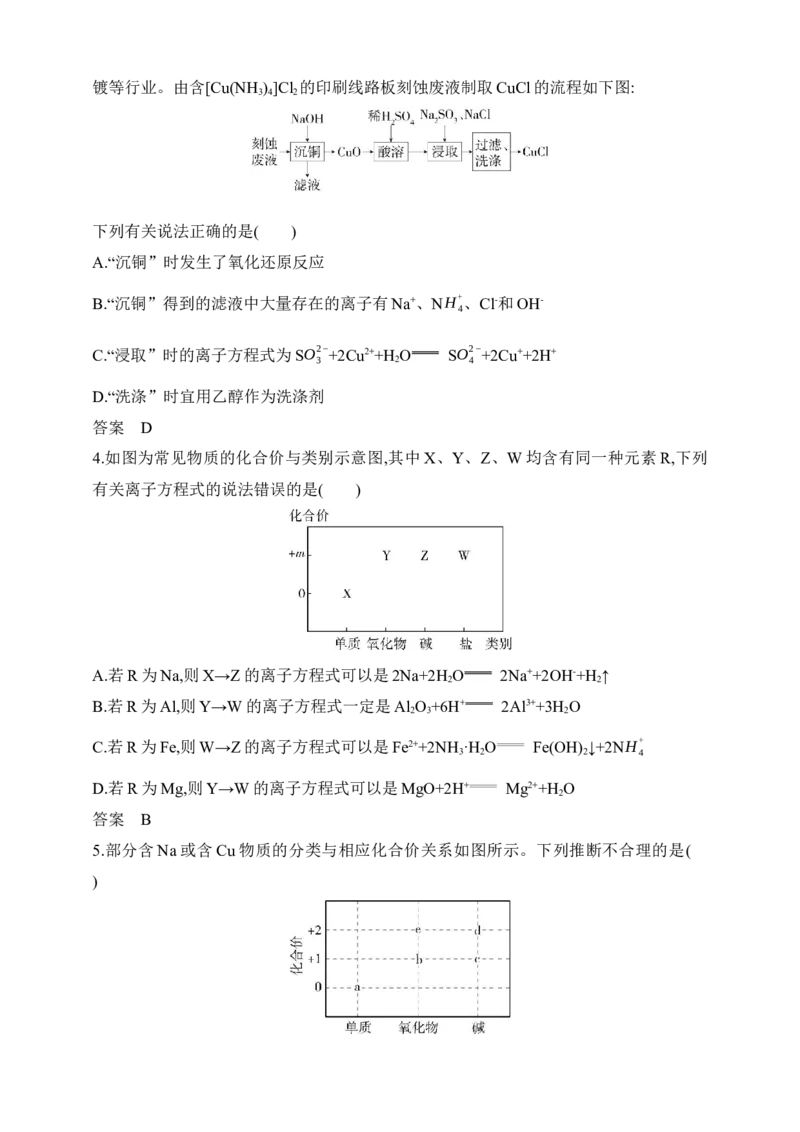
(3)MIBK“萃取”时可分为扩散萃取和动力学萃取两种类型。浸出液中钽的萃取率随搅
拌速度的增加而进一步增加时为扩散萃取,若浸出液受到化学反应的控制则萃取类型将
变为动力学萃取。搅拌速度对钽萃取率的影响如图所示。
搅拌速度在150 rpm时的萃取类型为 ,350 rpm到400 rpm时钽萃取率不
再增加的原因是 。
(4)金属铌可用金属钠还原K NbF 制取,也可用电解熔融的K NbF 制取。
2 7 2 7
①流程中钠热还原法制备铌粉的化学方程式为 。
②传统的熔盐电解法采用的电解质体系通常为K NbF -NaCl,利用该方法制备1 mol Nb理
2 7论上消耗NaCl的物质的量为 mol。
专题五 金属及其化合物
1.陈述Ⅰ和Ⅱ均正确且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
金 属 钠 在 O 中 点 燃 产 生
A 2 Na O 可在潜水艇中作为O 的来源
Na O 2 2 2
2 2
B 碳酸钠受热分解产生CO 用碳酸钠作膨松剂制作面包
2
C 浓硫酸与Fe不反应 可用钢瓶运输浓硫酸
D Zn的金属性比Fe强 船身焊接锌块可减缓船体腐蚀
答案 D
2.陈述Ⅰ和Ⅱ均正确并具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A 用明矾净水 Al(OH) 胶体具有吸附性
3
B Na着火不能用水扑灭 Na可与水反应产生O
2
C 二氧化硅可用于制备光导纤维 二氧化硅是良好的半导体材料
D 用84消毒液进行消毒 NaClO溶液呈碱性
答案 A
3.氯化亚铜(CuCl)难溶于水,不溶于乙醇,潮湿时易水解氧化,广泛应用于化工、印染、电镀等行业。由含[Cu(NH ) ]Cl 的印刷线路板刻蚀废液制取CuCl的流程如下图:
3 4 2
下列有关说法正确的是( )
A.“沉铜”时发生了氧化还原反应
B.“沉铜”得到的滤液中大量存在的离子有Na+、NH+、Cl-和OH-
4
C.“浸取”时的离子方程式为SO2−+2Cu2++H O SO2−+2Cu++2H+
3 2 4
D.“洗涤”时宜用乙醇作为洗涤剂
答案 D
4.如图为常见物质的化合价与类别示意图,其中X、Y、Z、W均含有同一种元素R,下列
有关离子方程式的说法错误的是( )
A.若R为Na,则X→Z的离子方程式可以是2Na+2H O 2Na++2OH-+H ↑
2 2
B.若R为Al,则Y→W的离子方程式一定是Al O +6H+ 2Al3++3H O
2 3 2
C.若R为Fe,则W→Z的离子方程式可以是Fe2++2NH ·H O Fe(OH) ↓+2NH+
3 2 2 4
D.若R为Mg,则Y→W的离子方程式可以是MgO+2H+ Mg2++H O
2
答案 B
5.部分含Na或含Cu物质的分类与相应化合价关系如图所示。下列推断不合理的是(
)A.可通过观察单质a、氧化物b的颜色,判断其为何种物质
B.能与H O反应生成c的物质只有b
2
C.新制的d可用于检验葡萄糖中的醛基
D.在加热条件下,e能将乙醇氧化为乙醛
答案 B
6.某些化学知识用数轴表示更形象直观、简明易记。下列用数轴表示不合理的是( )
A 铁与稀硝酸反应
向烧碱溶液通入SO
B 2
后的产物
Na与O 加热反应的
C 2
产物
D 分散系的分类
答案 C
7.实验室模拟工业制备BaCl ·2H O的一种工艺流程如图所示,已知常温下CaS的溶解度
2 2
为0.2 g/L,CaCl 的溶解度较大,且随温度变化不大。下列说法错误的是( )
2
A.“煅烧”过程中发生的反应为BaSO +CaCl +4C BaCl +CaS+4CO↑
4 2 2
B.“粉碎”时可在瓷坩埚中进行
C.滤渣中除了CaS,还可能含有未反应完的BaSO
4
D.滤液1通过蒸发浓缩、冷却结晶、过滤洗涤等操作可得BaCl ·2H O
2 2
答案 B
8.钠及其化合物的转化具有重要应用。下列说法不正确的是( )
A.工业制备NaOH的原理:2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
B.侯氏制碱过程中的物质转化:NaCl NaHCO Na CO
3 2 3
C.Na O 与CO 反应为潜水艇供氧的原理:2Na O +2CO 2Na CO +O
2 2 2 2 2 2 2 3 2D.苯酚钠溶液与少量CO 反应:C H ONa+CO +H O C H OH+NaHCO
2 6 5 2 2 6 5 3
答案 B
9.纳米铁粉可用于处理水中污染物,一定条件下,向FeSO 溶液中滴加碱性NaBH 溶液,生
4 4
成纳米铁粉、H 和B(OH)- ;Fe O 可用作锂离子电池的电极材料,电池工作时有Li+嵌入其
2 4 3 4
中生成LiFe O ;铁氰化钾{K [Fe(CN) ]}遇Fe2+发生反应生成深蓝色沉淀{Fe [Fe(CN) ] },
3 4 3 6 3 6 2
常用于检验Fe2+。下列表述不正确的是( )
A.制备纳米铁粉的离子反应:2Fe2++BH- +4OH- 2Fe↓+2H ↑+B(OH)-
4 2 4
B.FeS 制硫酸过程中物质转化:FeS (s) SO (g) H SO (aq)
2 2 2 2 4
C.Fe O 晶体中嵌入Li+形成LiFe O 时,部分Fe3+转化为Fe2+
3 4 3 4
D.铁氰化钾检验Fe2+的离子反应:3Fe2++2[Fe(CN) ]3- Fe [Fe(CN) ] ↓
6 3 6 2
答案 B
10.下列说法不正确的是 ( )
A.工业制硝酸:NH NO HNO
3 2 3
B.制备硝酸铜:Cu CuO Cu(NO )
3 2
C.ClO 除去NO的反应:3ClO +5NO+4H O 3HCl+5HNO
2 2 2 3
D.过量的Fe粉与稀HNO 反应:3Fe+8H++2NO- 3Fe2++2NO↑+4H O
3 3 2
答案 A
11.纯碱在食品加工、制药等方面有重要应用。实验室以碳酸氢铵(温度高于35 ℃分解)
和食盐水为原料模拟纯碱的制取,流程如下:
下列说法错误的是( )
A.“搅拌、加热”操作中,应采用水浴加热,且温度控制在35 ℃以下B.在“搅拌、加热”对应的温度下,NH HCO 、NaCl、NaHCO 、NH Cl 四种物质
4 3 3 4
中,NaHCO 的溶解度最低
3
C.“洗涤、抽滤”操作中用到的主要仪器有:普通漏斗、烧杯、玻璃棒
D.利用“双指示剂”法测定碳酸钠中碳酸氢钠的含量时,第1指示剂为酚酞,第2指示剂
为甲基橙
答案 C
12.生产软磁铁氧体的主要原料是 α-FeOOH,以硫铁矿(主要成分是 FeS ,含少量Al O 、
2 2 3
SiO 和Fe O )为原料制备α-FeOOH的工艺流程如下,相关数据见下表。下列说法错误的
2 3 4
是( )
物质 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀pH(25 ℃) 1.9 7.6 4.0
沉淀完全pH(25 ℃) 3.2 9.7 5.2
A.“焙烧”的产物之一可用于工业制硫酸
B.“试剂a”可以为FeS,主要目的是除去过量硫酸
C.“试剂b”可以为氨水,调pH的范围为5.2~7.6
D.“沉淀”时,pH过高或者过低均不利于生成α-FeOOH
答案 B
13.以钢铁厂灰渣(主要成分为ZnO,并含少量CuO、Fe O 等)为原料制备氧化锌的一种工
2 3
艺流程如下:
已知:过量氨水使ZnO、CuO溶解,转化为[Zn(NH ) ]2+和[Cu(NH ) ]2+配离子。
3 4 3 4
下列说法正确的是( )
A.滤液①中大量存在HCO-、CO2−、OH-
3 3
B.滤渣②的成分为CuC.“ 蒸 氨 沉 锌 ” 过 程 中 反 应 的 化 学 方 程 式 为 2[Zn(NH ) ]CO +H O
3 4 3 2
8NH ↑+ZnCO ·Zn(OH) ↓+CO ↑
3 3 2 2
D.“煅烧”过程需使用蒸发皿
答案 C
14.金属铑(Rh)是一种高效催化剂,在有机合成中发挥重要作用。一种以高铜铑精矿(主要
含Rh,还含有少量的Cu、Fe等杂质)为原料提取的工艺如下:
已知:阳离子交换过程可表示为xRH(s)+Mx+(aq) R M(s)+xH+(aq)
x
回答下列问题:
(2)“氯化溶解”后,Rh元素以[RhCl ]3-的形式存在,其中Rh元素的化合价为 。
6
(3)“定向脱铜”时,铜与铑的沉淀率随pH变化如下图所示,该过程需将溶液pH调至2,结
合图像说明原因 。
(4)“阳离子交换”过程中,溶液中被阳离子交换树脂吸附的金属阳离子主要有 。
(5)“水解”过程中,[RhCl ]3-发生反应的离子方程式为 。
6
答案 (2)+3 (3)pH=2时,铜的沉淀率已超过98%,铑的沉淀率几乎为0(或pH<2,铜的沉淀
率 会 降 低 ,pH>2, 铑 的 沉 淀 率 会 增 加 ) (4)Fe3+ 、 Na+ (5)[RhCl ]3-+3H O
6 2
Rh(OH) ↓+6Cl-+3H+
3
15.镀镍生产过程中产生的酸性硫酸镍废液(含有Fe2+、Zn2+、Mg2+、Ca2+等杂质离子),通
过精制提纯可制备高纯硫酸镍,部分流程如下:资料1:25 ℃时,K (CaF )=4×10-11,K (MgF )=9×10-9,ZnF 易溶于水。
sp 2 sp 2 2
资料2:P204(二乙基己基磷酸)萃取金属离子的反应为
(1)操作1、2的名称 ,操作3所需要的主要玻璃仪器名称是烧杯和 。
(2)操作1中加入Cl 的主要目的是 。
2
(3)NiF 溶 液 参 与 反 应 的 离 子 方 程 式 是 Mg2++2F- MgF ↓ 和
2 2
,杂质离子沉淀完全时,溶液中c(F-)= mol/L[c(杂质离子)≤10-5 mol/L可视为沉淀完
全]。
(4)滤液b中含有的金属阳离子主要有Ni2+和 。
(5)在硫酸盐溶液中P204对某些金属离子的萃取率与 pH关系如图所示,在一定范围内,随
着pH升高,萃取率升高的原因是 。
(6)处理后母液再利用及含量测定:
①在母液中加入石灰乳可制备操作 1 中所需 Ni(OH) 浆液,写出制备的化学方程式
2
。
②准确量取 25.00 mL 处理后的母液稀释液于锥形瓶中,加入 10.00 mL 0.050 0
mol·L-1BaCl 溶液,充分反应后,滴加氨水调节溶液pH=10,用0.010 0 mol·L-1EDTA(Na H Y)
2 2 2
溶液滴定至终点,滴定反应为Ba2++H Y2- BaY2-+2H+,平行滴定3次,平均消耗EDTA溶
2
液25.00 mL,计算处理后的母液稀释液中SO2−含量为 mg·L-1。
4答案 (1)过滤 分液漏斗 (2)将Fe2+氧化为Fe3+
(3)Ca2++2F- CaF ↓ 3×10-2 (4)Zn2+ (5)萃取反应中,溶液pH升高,H+浓度减小,平衡
2
右移,萃取率升高 (6)①NiSO +Ca(OH) Ni(OH) +CaSO ②960
4 2 2 4
16.MoO 是生产含钼催化剂的重要原料。以钼精矿(主要成分是 MoS ,还含有 FeS 、
3 2 2
CuS、ZnS、CaCO 和SiO 等杂质)为原料制备MoO 的工业流程如下图所示:
3 2 3
回答下列问题:
已知:①“焙烧”的含钼产物有MoO 、Fe (MoO ) 、CuMoO 和ZnMoO ;
3 2 4 3 4 4
②“滤液1”中主要的阳离子为[Zn(NH ) ]2+、[Cu(NH ) ]2+和NH+ ;
3 4 3 4 4
③常温下,K (CuS)=6.0×10-36;
sp
④[Cu(NH ) ]2+ Cu2++4NH 的平衡常数K=5.0×10-14。
3 4 3
(1)Mo位于元素周期表第五周期第Ⅵ B族,则基态钼原子的价层电子的轨道表示式为
。
(2)MoS 发生“焙烧”时转化成MoO 的化学反应方程式为 。
2 3
(3)“滤渣 1”的主要成分是 SiO 、 、 、Fe(OH) 、Fe (MoO ) 。已知
2 3 2 4 3
Fe (MoO ) 能溶于氨水,但“滤渣1”中仍存在Fe (MoO ) 的原因是 。
2 4 3 2 4 3
(4)“除杂”加入适量(NH ) S的目的是 。
4 2
请计算[Cu(NH ) ]2++S2- CuS↓+4NH 的平衡常数K'= (用科学记数法表示,计
3 4 3
算结果保留一位小数)。
(5)写出四钼酸铵[(NH ) Mo O ·2H O]“焙解”的化学反应方程式: 。
4 2 4 13 2
答案 (1)
(2)2MoS +7O 2MoO +4SO
2 2 3 2
(3)MoO Ca(OH) Fe (MoO ) 溶解度小,溶液过饱和析出部分Fe (MoO ) 晶体
3 2 2 4 3 2 4 3
(4)将杂质离子[Zn(NH ) ]2+和[Cu(NH ) ]2+转化为相应的金属硫化物沉淀 ZnS 和 CuS
3 4 3 4
8.3×1021
(5)(NH ) Mo O ·2H O 4MoO +2NH ↑+3H O↑
4 2 4 13 2 3 3 217.钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO ·xH O、Cr(OH) 及少量
2 2 3
的SiO ,一种初步分离钒铬还原渣中的钒铬并获得Na Cr O 的工艺流程如图:
2 2 2 7
已知:①“酸浸”后VO ·xH O转化为VO2+;
2 2
②lg2≈0.3;
③常温下Cr(OH) 的K 近似为1×10-30;
3 sp
④有关物质的溶解度(g/100 g H O)如表所示:
2
温度/℃ 20 40 60 80 100
Na Cr O 183.6 215.1 269.2 376.4 415.0
2 2 7
Na SO 19.5 48.8 45.3 43.7 42.5
2 4
回答下列问题:
(1)写出“滤渣”的一种用途: ,“氧化”操作单元中,消耗的氧化剂
与还原剂的物质的量之比为 。
(2)若“含 Cr3+净化液”中 c(Cr3+)=0.125 mol·L-1,则“水解沉钒”调 pH的范围是 2.5~
。
(3)“溶液1”中含CrO- ,加入H O 后发生反应的化学方程式为 。
2 2 2
(4)“溶液2”调pH所发生反应的离子方程式为 。
(5)“多步操作”包括蒸发结晶、趁热过滤、所得滤液冷却结晶、过滤、洗涤等步骤,其中
蒸发结晶时,过度蒸发将导致 。
(6)研究温度对Na S O 与H O 的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还
2 2 8 2 2
原渣酸浸液初始温度在 80 ℃左右,降低温度能耗增加。由图可如,分别采用Na S O 、
2 2 8
H O 进行“氧化”时,应选择的适宜温度是 、 。
2 2答 案 (1) 制 作 光 导 纤 维 或 制 作 玻 璃 或 工 业 制 硅 ( 合 理 即 可 ) 1∶2 (2)4.3
(3)3H O +2NaCrO +2NaOH 2Na CrO +4H O
2 2 2 2 4 2
(4)2CrO2−+2H+ Cr O2−+H O
4 2 7 2
(5)Na Cr O 提前析出,降低Na Cr O 的产率
2 2 7 2 2 7
(6)80 ℃ 50 ℃
18.铜—钢双金属废料和铜烟灰是铜的重要二次资源。
Ⅰ.从铜—钢双金属废料中浸出铜的工艺流程如下:
(1)25 ℃时,随溶液的pH不同,甘氨酸在水溶液中分别以NH+ CH COOH、NH+ CH COO-或
3 2 3 2
NH CH COO-为主要形式存在。内盐NH+ CH COO-是两性化合物,请用离子方程式表示其
2 2 3 2
水解使水溶液呈碱性的原因: 。
(2)浸出剂的制备:主要原料有甘氨酸(简写为HL)、CuSO 溶液和NaOH固体。取一定量
4
NaOH固体溶于水,随后依次加入 (填“HL”或“CuSO ”,下同)、 ,所得碱性浸出剂
4
的主要成分为甘氨酸铜(CuL )、L-等。
2
(3)浸出:将已打磨的铜—钢废料投入浸出剂,控制温度50 ℃,通入空气,并搅拌。浸出剂不
与钢作用,但与铜反应,最终铜全部转化为CuL 进入溶液,从而实现铜、钢分离。
2
①浸出时发生的反应为CuL +Cu+2L- 2CuL-、 。
2 2
②其他条件不变时,空气流量对铜浸出速率的影响如图 1 所示。当空气流量超过 1.0
L·min-1时,铜浸出速率急剧减小的可能原因是 。Ⅱ.从铜烟灰[主要成分为Cu(OH)Cl、FeO、Fe O 、Zn (PO ) ]中回收铜的主要步骤为酸
2 3 3 4 2
浸→萃取→反萃取→电解。
已知:Zn (PO ) 溶于无机酸。
3 4 2
(4)酸浸:将铜烟灰用硫酸浸出,控制其他条件相同,铜浸出率与温度的变化关系如图2所示。
随温度升高,铜浸出率先增大后减小的可能原因是 。
(5)萃取、反萃取:向浸出液(Cu2+浓度为7 g·L-1)中加入有机萃取剂(RH)萃取,其原理可表示
为Cu2+(水层)+2RH(有机层) R Cu(有机层)+2H+(水层)。
2
向萃取所得有机相中加入硫酸,反萃取得到水相(Cu2+浓度达40 g·L-1)。该工艺中设计萃取、
反萃取的目的是 。
答案 (1)NH+ CH COO-+H O NH+ CH COOH+OH- (2)HL CuSO (3)①4CuL-
3 2 2 3 2 4 2
+O +2H O 4CuL +4OH- ②空气中的氧气没有足够的时间参与反应,导致反应速率减
2 2 2
小 (4)该酸浸过程为放热反应,温度升高时,反应速率加快,但是温度过高,平衡逆向移动,
导致浸出率减小 (5)实现Cu2+的提取和富集
19.以辉铋矿(主要成分为Bi S ,含有FeS 、SiO 杂质)和软锰矿(主要成分为MnO )为原料
2 3 2 2 2
制备超细氧化铋的工艺流程如下:
已知:Bi3+易与Cl-形成BiCl3−,BiCl3−易发生水解,其反应的离子方程式为 BiCl3−+H O
6 6 6 2
BiOCl↓+5Cl-+2H+。
(1)“联合焙烧”时,Bi S 和MnO 在空气中反应生成Bi O 和MnSO 。该反应的化学方程
2 3 2 2 3 4
式为 。(2)“酸浸”时需及时补充浓盐酸调节浸取液的pH。
①一般控制浸取液pH小于1.4,其目的是 。
②为提高酸浸时金属元素的浸出率,除适当增加浓盐酸用量、适当升高酸浸温度外,还可
采取的措施有 。
(3)铋离子能被有机萃取剂(简称TBP)萃取,其萃取原理可表示为BiCl3−(水层)+2TBP(有机
6
层) BiCl ·2TBP(有机层)+3Cl-(水层)。
3
①“萃取”时需向溶液中加入NaCl固体调节Cl-浓度,萃取率随c(Cl-)变化关系如图所示。
c(Cl-)最佳为1.3 mol·L-1的可能原因是 。
②“萃取”后分液所得水相中的主要阳离子为 (填化学式)。
(4)“沉淀反萃取”时生成草酸铋[Bi (C O ) ·7H O]晶体。为得到含Cl-较少的草酸铋晶体,
2 2 4 3 2
“萃取”后有机相与草酸溶液的混合方式为 。
答案 (1)2Bi S +6MnO +9O 2Bi O +6MnSO (2)①增大H+浓度,使Bi3+充分浸出;同
2 3 2 2 2 3 4
时抑制金属离子Bi3+(或BiCl3−)、Fe3+水解 ②加快搅拌速度
6
(3)①c(Cl-)>1.3 mol·L-1时,铋离子(萃取平衡BiCl3−+2TBP BiCl ·2TBP+3Cl-逆向移动)
6 3
萃取率下降,铁离子萃取率上升;c(Cl-)<1.3 mol·L-1 时,铋离子水解(BiCl3−+H O
6 2
BiOCl↓+5Cl-+2H+)程度增大,不利于铋离子的萃取提纯 ②Fe3+、H+、Na+ (4)边搅拌边
将有机相滴加到草酸溶液中
20.金属钼(Mo)及其化合物在合金工业中起着重要的作用,生产中常以辉钼矿(主要成分为
MoS ,含有FeS、CuS、SiO 等杂质)为原料制备金属钼及其化合物。以下是生产的部分
2 2
流程。已知:①Mo的常见价态有+4、+6。
②H MoO 是微溶于水的无机酸,可溶于碱。
2 4
③氧气不足时,焙烧产物中可能混有MoO 与MoS 反应生成的MoO 。
3 2 2
回答下列问题:
(1)焙烧的产物中Mo元素主要以MoO 、MoO2−盐的形式存在。生成MoO 的反应的化学
3 4 3
方程式为 。
(2)与酸浸1相比,酸浸2使用稀硝酸的优点是 ,但是缺
点是会产生NO 造成污染。
x
(3)滤渣的成分主要是 。碱浸时pH不宜过大,原因是 。
(4)已知离子交换环节中,阴离子交换树脂 R—OH 的工作原理为 2R—OH+MeMoO
4
R MoO +Me(OH) (Me代表金属阳离子),洗脱时使用的试剂X为 。
2 4 2
(5)钼酸钠的某些晶体的溶解度曲线如图,获得Na MoO ·10H O的操作为蒸发浓缩、
2 4 2
、过滤、洗涤。
(6)工业上还有电氧化MoS 制备Na MoO 的方法,装置如下图所示。
2 2 4每生成0.1 mol Na MoO 时,外电路转移的电子数为 (阿伏加德罗常数的值用N
2 4 A
表示)。
(7)Na MoO ·10H O 中可能混有 Na MoO ,以硝酸铅[Pb(NO ) ]溶液为标准溶液测定
2 4 2 2 4 3 2
Na MoO ·10H O的纯度。根据下表信息,应选用的指示剂为 。滴定终点的现象
2 4 2
为 。
物质 PbCO PbI PbS PbMoO
3 2 4
K 7.3×10-5 7.0×10-2 6.7×10-13 1.2×10-5
sp
颜色 白色 亮黄色 黑色 白色
取 m g Na MoO ·10H O(式量为 M)样品配成 200 mL 溶液,取出 20.00 mL 用 c mol/L
2 4 2
Pb(NO ) 标准溶液进行滴定,消耗标准溶液 V mL,则样品中Na MoO ·10H O的质量分数
3 2 2 4 2
为 (写出表达式即可)。
答案 (1)2MoS + 7O 2MoO + 4SO
2 2 3 2
(2)可使Mo元素被进一步充分氧化
(3)SiO 防止SiO 溶解生成SiO2−使产品不纯
2 2 3
(4)浓氨水
(5)降温至10 ℃之下结晶
(6)1.8N
A
(7)KI 当滴入最后半滴Pb(NO ) 标准溶液时,锥形瓶内生成亮黄色沉淀,且半分钟内不恢
3 2
复原来的颜色
[m-cV ×10-2×(M-180)]M
×100%
180m
21.钽(Ta)和铌(Nb)是性质相似的两种单质,一种以钽铌伴生矿(主要成分为SiO 、MnO 、
2 2
Nb O 、Ta O 和少量的TiO 、FeO、CaO、MgO)为原料制取钽和铌的流程如下:
2 5 2 5 2“浸取”后的浸出液中含有H TaF 、H NbF 两种二元强酸和锰、钛等元素。
2 7 2 7
已 知 :①MIBK 为 甲 基 异 丁 基 酮 ;②K (CaF )=2.5×10-11,K (MgF )=6.4×10-
sp 2 sp 2
9,K (CaSO )=7.1×10-5。
sp 4
(1)加快“浸取”速率可采取的措施是 。
(2)浸渣的主要成分是 ,Ta O 与氢氟酸反应的离子方程式为
2 5
。
(3)MIBK“萃取”时可分为扩散萃取和动力学萃取两种类型。浸出液中钽的萃取率随搅
拌速度的增加而进一步增加时为扩散萃取,若浸出液受到化学反应的控制则萃取类型将
变为动力学萃取。搅拌速度对钽萃取率的影响如图所示。
搅拌速度在150 rpm时的萃取类型为 ,350 rpm到400 rpm时钽萃取率不
再增加的原因是 。
(4)金属铌可用金属钠还原K NbF 制取,也可用电解熔融的K NbF 制取。
2 7 2 7
①流程中钠热还原法制备铌粉的化学方程式为 。
②传统的熔盐电解法采用的电解质体系通常为K NbF -NaCl,利用该方法制备1 mol Nb理
2 7
论上消耗NaCl的物质的量为 mol。
答案 (1)将钽铌伴生矿磨碎(或“适当升高浸取时的温度”等合理答案)
(2)CaF 、MgF Ta O +14HF 4H++2TaF2−+5H O
2 2 2 5 7 2
(3)扩散萃取 浸出液受到化学反应的控制(此时为动力学萃取)或不再受扩散萃取的影响(4)①K NbF +5Na Nb+5NaF+2KF ②5
2 7