文档内容
专题五 物质结构 元素周期律
考 点 高考年 考频解密 考点分布
2022年河北卷〔6,8,10〕;2022年山东
卷〔3,5〕;2022年湖北卷〔7,8,9,10,
元素周期律〔16次〕,原子
11〕;2022年湖南卷〔2,5〕;2022年广
物质结构 结构 化学键〔8次〕,原
东卷〔2,7〕;2022年江苏卷〔2,3,5,
2022 年 子结构与性质〔5次〕,分
7〕;2022年辽宁卷〔2,3,5,7,8〕;
元素周期律 子结构与性质〔18次〕,晶
2022年海南卷〔5,11〕;2022年北京卷
体结构与性质〔8次〕
〔1,2,3,7,8,9,11,13〕;2022年
全国甲卷〔6〕;2022年全国乙卷〔5〕等
一、元素、核素、同位素
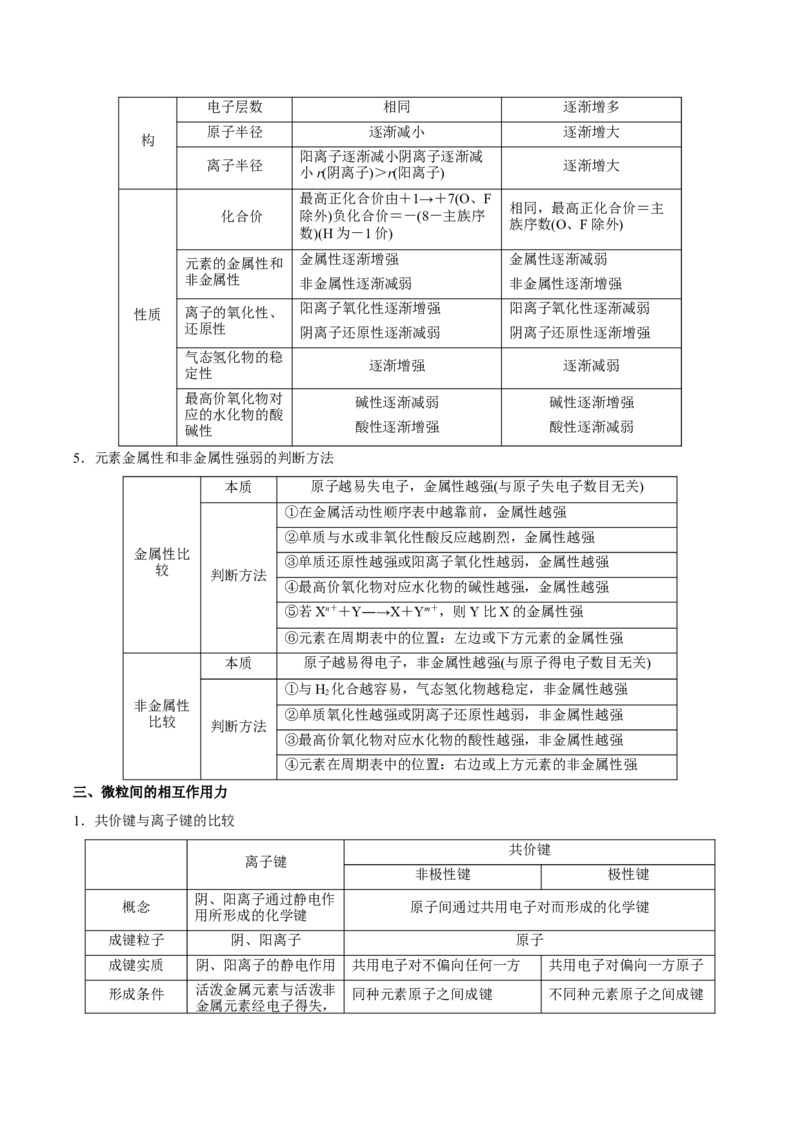
1.“三素”关系
2.同位素的“六同三不同”3.几种重要的核素及其应用
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
4.核外电子排布
(1)核外电子排布规律
(2)原子结构示意图
二、元素周期表与元素周期律
1.元素周期表的结构
①“七横七周期,三短三长一不全;十八纵行十六族,七主七副一Ⅷ一0”。
②从左到右族的分布:
ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ、ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
Ⅷ族:包括8、9、10三个纵列。
③0族:第18纵列,该族元素又称为稀有气体元素。
其原子序数为He 2,Ne 10,Ar 18,Kr 36,Xe 54,Rn 86。
④同周期第ⅡA和第ⅢA原子序数的差值可能为:1、11、25。
2.分区
①分界线:沿着元素周期表中硼、硅、砷、碲、砹与铝、锗、锑、钋的交界处画一条虚线,即为金属元素
区和非金属元素区的分界线。
②各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
3.元素周期表中的特殊位置
①过渡元素:元素周期表中部从ⅢB族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元素。
②镧系:元素周期表第6周期中,57号元素镧到71号元素镥共15种元素。
③锕系:元素周期表第7周期中,89号元素锕到103号元素铹共15种元素。
④超铀元素:在锕系元素中92号元素轴(U)以后的各种元素。
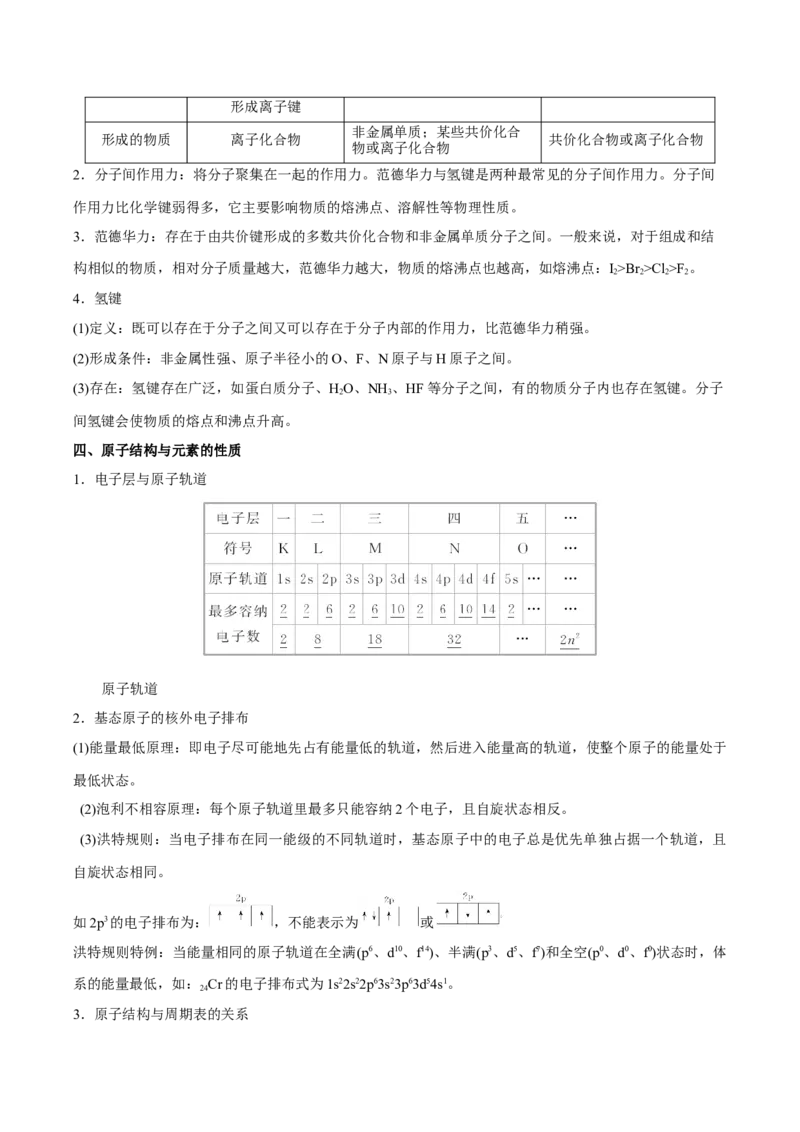
4.主族元素的周期性变化规律
项目 同周期(左→右) 同主族(上→下)
原子结 核电荷数 逐渐增大 逐渐增大电子层数 相同 逐渐增多
原子半径 逐渐减小 逐渐增大
构
阳离子逐渐减小阴离子逐渐减
离子半径 逐渐增大
小r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F
相同,最高正化合价=主
化合价 除外)负化合价=-(8-主族序
族序数(O、F除外)
数)(H为-1价)
元素的金属性和 金属性逐渐增强 金属性逐渐减弱
非金属性 非金属性逐渐减弱 非金属性逐渐增强
性质 离子的氧化性、 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
还原性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物的稳
逐渐增强 逐渐减弱
定性
最高价氧化物对 碱性逐渐减弱 碱性逐渐增强
应的水化物的酸
碱性 酸性逐渐增强 酸性逐渐减弱
5.元素金属性和非金属性强弱的判断方法
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性比
③单质还原性越强或阳离子氧化性越弱,金属性越强
较
判断方法
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y―→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
本质 原子越易得电子,非金属性越强(与原子得电子数目无关)
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属性
②单质氧化性越强或阴离子还原性越弱,非金属性越强
比较
判断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
三、微粒间的相互作用力
1.共价键与离子键的比较
共价键
离子键
非极性键 极性键
阴、阳离子通过静电作
概念 原子间通过共用电子对而形成的化学键
用所形成的化学键
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子的静电作用 共用电子对不偏向任何一方 共用电子对偏向一方原子
形成条件 活泼金属元素与活泼非 同种元素原子之间成键 不同种元素原子之间成键
金属元素经电子得失,形成离子键
非金属单质;某些共价化合
形成的物质 离子化合物 共价化合物或离子化合物
物或离子化合物
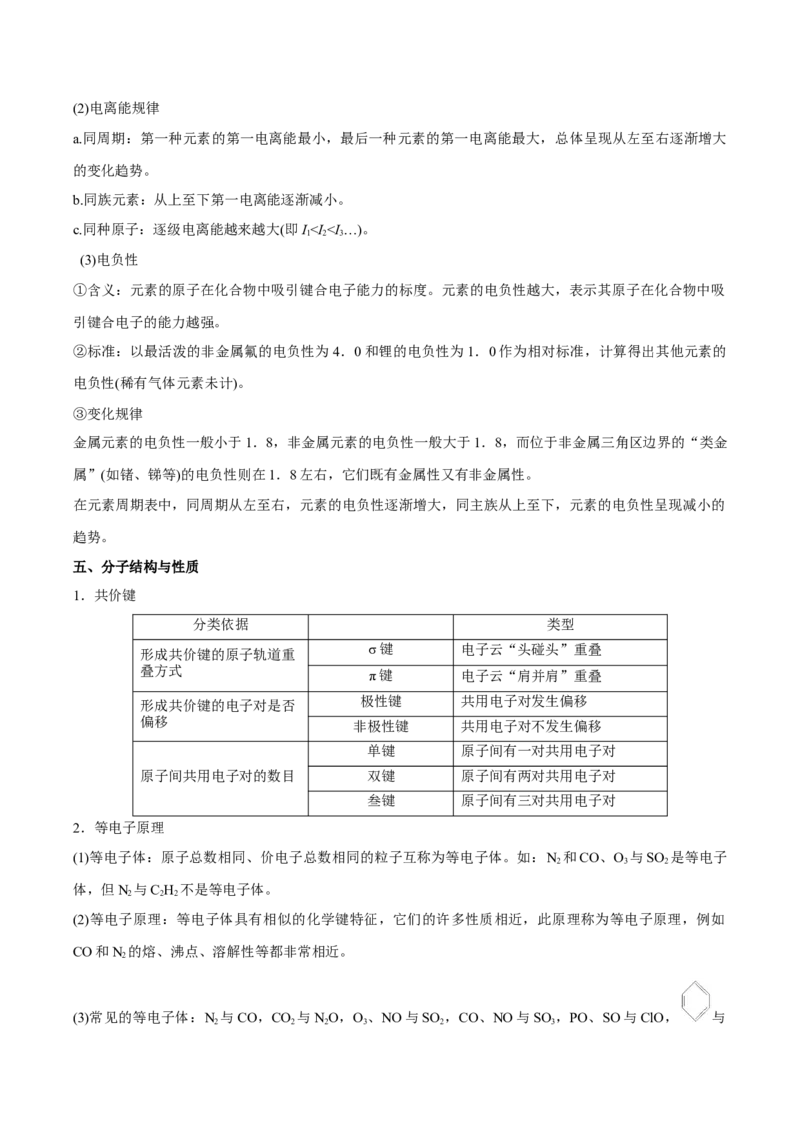
2.分子间作用力:将分子聚集在一起的作用力。范德华力与氢键是两种最常见的分子间作用力。分子间
作用力比化学键弱得多,它主要影响物质的熔沸点、溶解性等物理性质。
3.范德华力:存在于由共价键形成的多数共价化合物和非金属单质分子之间。一般来说,对于组成和结
构相似的物质,相对分子质量越大,范德华力越大,物质的熔沸点也越高,如熔沸点:I>Br >Cl>F 。
2 2 2 2
4.氢键
(1)定义:既可以存在于分子之间又可以存在于分子内部的作用力,比范德华力稍强。
(2)形成条件:非金属性强、原子半径小的O、F、N原子与H原子之间。
(3)存在:氢键存在广泛,如蛋白质分子、HO、NH 、HF等分子之间,有的物质分子内也存在氢键。分子
2 3
间氢键会使物质的熔点和沸点升高。
四、原子结构与元素的性质
1.电子层与原子轨道
原子轨道
2.基态原子的核外电子排布
(1)能量最低原理:即电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于
最低状态。
(2)泡利不相容原理:每个原子轨道里最多只能容纳2个电子,且自旋状态相反。
(3)洪特规则:当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且
自旋状态相同。
如2p3的电子排布为: ,不能表示为 或
洪特规则特例:当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、f0)状态时,体
系的能量最低,如: Cr的电子排布式为1s22s22p63s23p63d54s1。
24
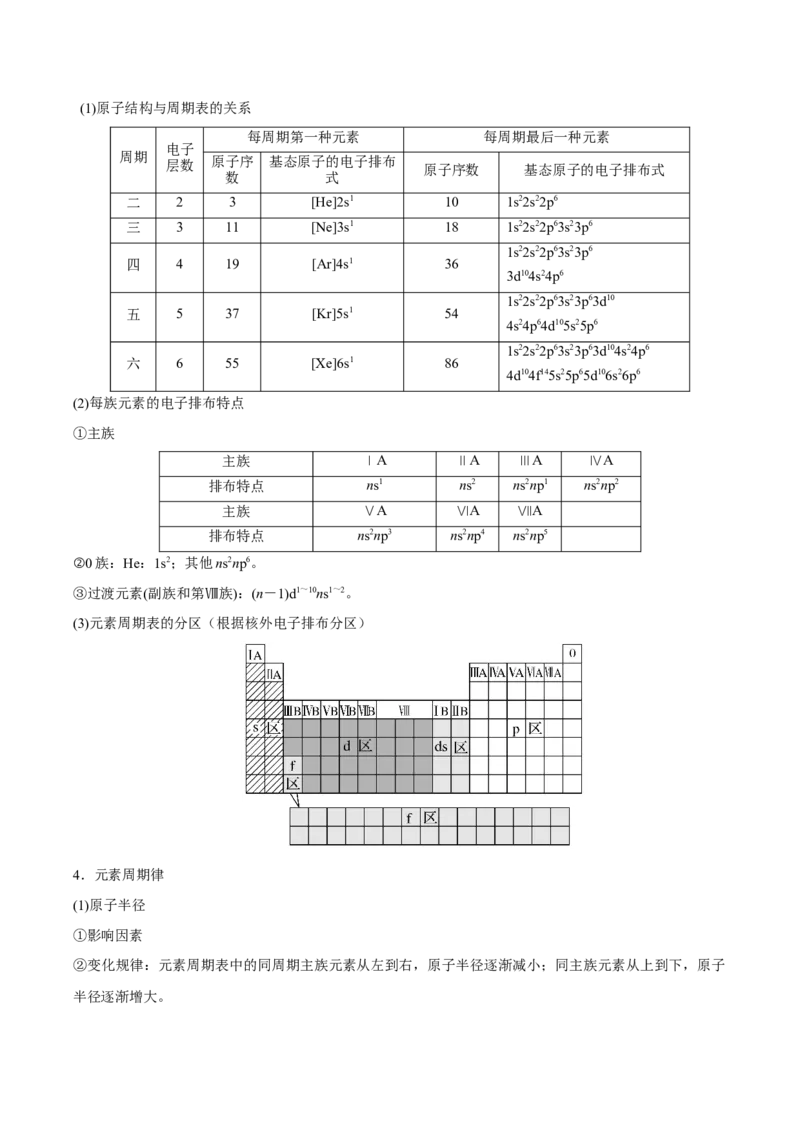
3.原子结构与周期表的关系(1)原子结构与周期表的关系
每周期第一种元素 每周期最后一种元素
电子
周期
层数 原子序 基态原子的电子排布
原子序数 基态原子的电子排布式
数 式
二 2 3 [He]2s1 10 1s22s22p6
三 3 11 [Ne]3s1 18 1s22s22p63s23p6
1s22s22p63s23p6
四 4 19 [Ar]4s1 36
3d104s24p6
1s22s22p63s23p63d10
五 5 37 [Kr]5s1 54
4s24p64d105s25p6
1s22s22p63s23p63d104s24p6
六 6 55 [Xe]6s1 86
4d104f145s25p65d106s26p6
(2)每族元素的电子排布特点
①主族
主族 ⅠA ⅡA ⅢA ⅣA
排布特点 ns1 ns2 ns2np1 ns2np2
主族 ⅤA ⅥA ⅦA
排布特点 ns2np3 ns2np4 ns2np5
②0族:He:1s2;其他ns2np6。
③过渡元素(副族和第Ⅷ族):(n-1)d1~10ns1~2。
(3)元素周期表的分区(根据核外电子排布分区)
4.元素周期律
(1)原子半径
①影响因素
②变化规律:元素周期表中的同周期主族元素从左到右,原子半径逐渐减小;同主族元素从上到下,原子
半径逐渐增大。(2)电离能规律
a.同周期:第一种元素的第一电离能最小,最后一种元素的第一电离能最大,总体呈现从左至右逐渐增大
的变化趋势。
b.同族元素:从上至下第一电离能逐渐减小。
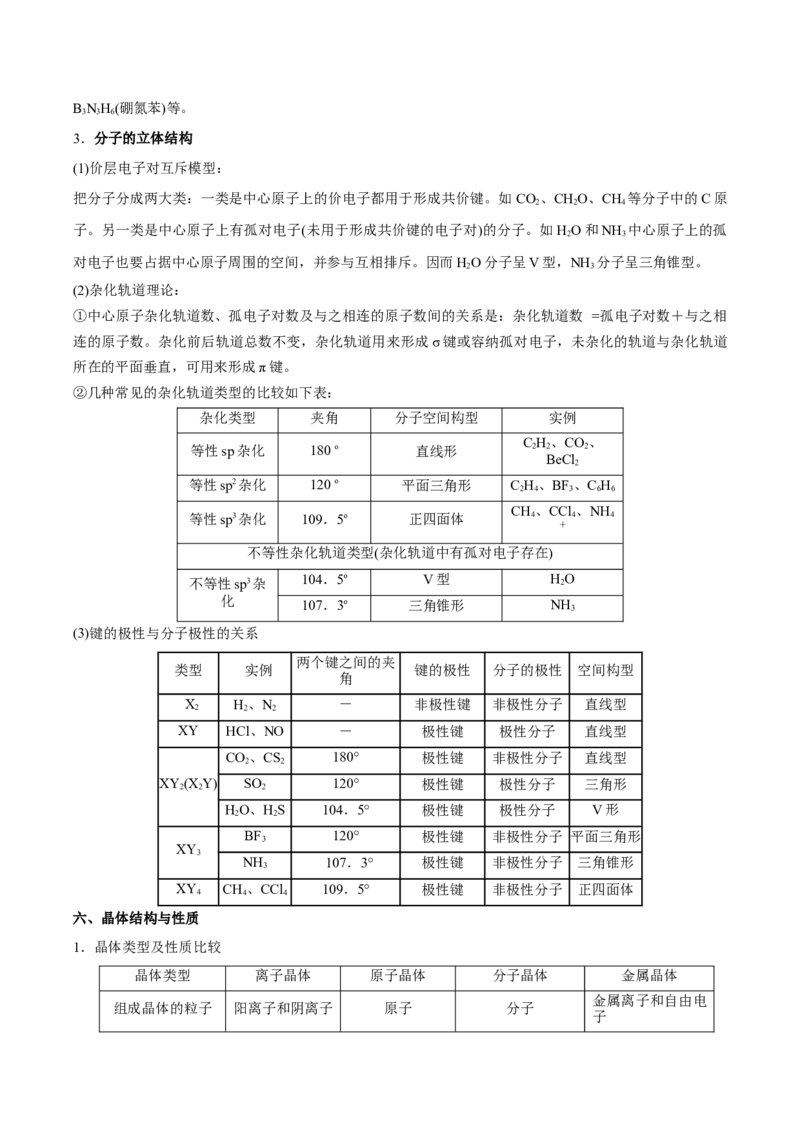
c.同种原子:逐级电离能越来越大(即I离子晶体>分子晶体。
不同类型晶体的熔、沸金属晶体的熔、沸点差别很大,如钨、铂等沸点很高,如汞、镓、铯等沸点很
点高低一般规律
低,金属晶体一般不参与比较。
由共价键形成的原子晶体中,原子半径小的键长短,键能大,晶体的熔、沸点
原子晶体
高。如熔点:金刚石>碳化硅>硅。
一般地说,阴、阳离子所带电荷数越多,离子半径越小,则离子间的作用就越
离子晶体
强,其离子晶体的熔、沸点就越高,如熔点:MgO>MgCl >NaCl>CsCl。
2
分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体,熔、沸点反
常地高。如HO>HTe>H Se>H S。
2 2 2 2
组成和结构相似的分子晶体,相对分子质量越大,晶体的熔、沸点越高,如
SnH >GeH>SiH >CH ,FN,CHOH>CH CH。
2 3 3 3
同 分 异 构 体 分 子 中 , 支 链 越 少 , 其 熔 沸 点 就 越 高 , 如
CH(CH)CH>CH CHCH(CH )>C(CH )。
3 2 3 3 3 2 3 2 3 4
金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,
金属晶体
如熔、沸点:NaNa>K>Rb>Cs。
探究一 金属性和非金属性强弱的判断
下列方案设计、现象和结论有不正确的是( )
目的 方案设计 现象和结论
氯化铬化学式的 氯化铬 在水溶 产生 沉淀,则此氯化铬化学
A
测定 液中用过量硝酸银溶液处理,观察现
式的
象
探究B、C、S
分别向饱和酸 溶液和稀硫酸 前者无气泡冒出,后者有气泡冒出,非金
B 三种元素的非金
属性:
属性 溶液中加入少量 粉末
向碳酸钠溶液中加入稀硫酸,反应产
检验碳酸与苯酚
C 生的气体通入苯酚钠溶液中,观察现 溶液变浑浊,说明酸性:碳酸>苯酚
的酸性强弱
象
向含 的 溶液中通入
检验 与 的
D 溶液变蓝色,不能说明还原性:
还原性强弱 ,再滴加淀粉溶液,观察现
象
A.A B.B C.C D.D
规律总结:解答元素的金属性和非金属性强弱的比较题,要抓住其本质,依据元素及其化合物的性质与元素的金属
性、非金属性的关系进行判断。
1.元素金属性强弱的比较方法
分类 判断依据 规律
单质与水或酸反应置换出金属单质与水或酸(非氧化性酸)反应置换出氢气越容易(反应
氢气的难易 越剧烈),表明元素金属性越强
单质的还
一种金属能把另一种金属从它的盐溶液中置换出来,表明前一种
元素金 原性 金属单质之间的置换反应
金属元素的金属性较强
属性强
与同一种非金属单质反应 反应越剧烈,金属元素的金属性越强,反之越弱
弱的
金属阳离子的氧化性 金属阳离子的氧化性越弱,其对应金属元素的金属性越强
判断
最高价氧化物对应水化物的碱性 最高价氧化物对应水化物的碱性越强,表明元素的金属性越强
同一周期,从左到右,金属性逐渐减弱;同一主族,从上到下,
元素在周期表中的位置
金属性逐渐增强
2.元素非金属性强弱的比较方法
分类 判断依据 规律
单质与氢气化合的难易程度 非金属单质与氢气化合越容易,元素的非金属性越强
一种非金属单质能把另一种非金属单质从它的盐溶液或酸溶
非金属单质之间的置换反应
单质的
液中置换出来,表明前一种元素的非金属性较强
氧化性
与同一种金属单质反应 反应越剧烈,非金属元素的非金属性越强,反之越弱
与同种变价金属反应 被氧化后的金属元素价态越高,非金属元素的非金属性越强
元素非
金属性
气态氢化物的稳定性 气态氢化物越稳定,元素的非金属性越强
强弱的
气态氢化物或非金属阴离子的还原性越弱,表明元素的非金
判断 气态氢化物或非金属阴离子的还原性
属性越强
最高价氧化物对应水化物的酸性越强,表明元素的非金属性
最高价氧化物对应水化物的酸性
越强
同一周期元素,从左到右,非金属性逐渐增强;同一主族元
元素在周期表中的位置
素,从上到下,非金属性逐渐减弱
【变式练习】
1.(2022·湖南郴州·一模)由实验操作和现象可得出相应正确结论的是( )
选
实验操作 现象 结论
项
A 往 溶液中通入 有透明凝胶生成 非金属性:
向两支均盛有 的 溶液的试管中分别加入 前者产生气泡较 催化能力:
B
快
2滴 溶液和 溶液该无色溶液中一定
C 铂丝蘸取某无色溶液后再火焰上灼烧 火焰呈黄色
含有
产生有刺激性气 该无色溶液中一定
D 向某无色溶液中滴入盐酸 味的气体和淡黄
色沉淀 含有
A.A B.B C.C D.D
2.硫元素的几种化合物在一定条件下可发生下列转化。下列说法错误的是( )。
A.反应①高温煅烧时,另外一种产物为
B.反应②可以说明S元素的非金属性强于C元素
C.做反应③实验后附着在试管壁上的硫可以用 清洗
D.反应④中当生成1mol硫时,转移电子为2mol
3.我国“祝融号”火星车成功着陆火星,其矿脉中含有原子序数依次增大的短周期主族元素W、X、Y、
Z。已知W、Z同主族,且Z的原子序数是W的2倍,X的氢化物可用于蚀刻玻璃,Y与Z最外层电子数
之和等于8,下列说法正确的是( )
A.原子半径:Z>Y>W>X B.简单氢化物的稳定性:X>W>Z
C.X与Z可形成离子化合物 D.工业上电解Y的氧化物得到单质Y
探究二 微粒半径大小的比较
元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。
下列判断不正确的是( )
A. 的分子空间结构为直线形B.简单离子半径顺序为:
C.Z与Q的单质分别与铁燃烧后的产物化学式分别为 和
D.R的最高价氧化物对应的水化物的碱性比Y的强
规律总结:解答原子(或离子)半径大小的比较题,要考虑电子层数、核电荷数、核外电子数等因素对原
子(或离子)半径的影响。
【变式练习】
1.“律动世界”国际化学元素周期表主题年活动报告中,提到了一种具有净水作用的物质,它由Q、W、
X、Y、Z五种原子序数依次增大的元素组成。该五种元素的性质或结构信息如下表:
元
信息
素
Q 基态原子只有一种形状的轨道填有电子,并容易形成共价键
W 基态原子有5个原子轨道填充有电子,有2个未成对电子
X 最高价氧化物对应的水化物与Y、Z最高价氧化物对应的水化物都能反应
Y 在元素周期表中位于第3周期、第ⅥA族
Z 焰色反应为紫色
下列说法正确的是( )A.电负性:Q<W<Y B.第一电离能:W<X<Z
C.简单离子半径:X<W<Z<Y D.这种物质只含离子键
2.世界资源储量最大的滑石矿位于江西上饶,经分析发现滑石中含有4种短周期元素W、X、Y、Z,它
们的原子序数依次增大,最外层电子数之和为13,且位于不同的主族,X的某种气体单质被喻为“地球的
保护伞”,WX 分子中含有18个电子,下列说法正确的是( )
2 2
A.原子半径大小顺序为Z>Y>X>W
B.化合物YX是一种很好的耐火材料
C.Y单质只能与空气中的主要成分氧气反应
D.Z的最高价氧化物的水化物的酸性强于碳酸
3.(2022·山西临汾·高三期中)短周期主族元素X、Y、Z、W在元素周期表的相对位置如图所示,它们
的原子序数之和为39。下列说法错误的是( )
A.常温常压下,X单质为固态 B.Z和W的主要化合价相同
C.原子半径: D.Y的氢化物与W的氢化物相遇产生白烟
探究三 元素周期表中“位-构-性”的关系及应用
(2022·四川雅安·模拟预测)短周期主族元素X、Y、Z、W的原子序数依次增大。X是地壳中含量最高的
元素,Z与X同主族,W的最外层电子数等于Y与Z的最外层电子数之和。下列说法错误的是( )
A.简单离子的还原性:X>W>Z
B.简单氢化物的沸点:X>Z
C.X、Y形成的化合物一定含离子键
D.X、Y、W形成的一种化合物可用于消毒杀菌
规律总结:解答元素周期表中“位-构-性”的关系及应用题,要明确原子结构、元素在周期表中的位置和
元素性质的“三角关系”,掌握三者之间互推的方法。
1.结构与位置的互推是解题的核心
(1)掌握四个基本关系(对于原子):
①质子数=核电荷数=核外电子数=原子序数;②电子层数=周期序数;
③最外层电子数=主族序数;
④主族元素的最高正价=主族序数(O、F除外),最低负价=主族序数-8(H除外)。
(2)掌握周期表中“序、层”规律:若一种阳离子和阴离子的电子层结构相同,则“阴前右” “阳后
左”,即阴离子对应元素在前一周期右侧,阳离子对应元素在后一周期左侧。
(3)根据原子序数推断元素在周期表中的位置:按照原子核外电子排布规律画出原子结构示意图,根据电子
层数和最外层电子数确定其周期序数和主族序数。
2.性质与位置的互推是解题的关键
(1)根据元素的金属性和非金属性变化规律,推断元素在周期表中处于同周期、同主族的相对位置关系。
(2)根据元素在周期表中的位置关系,推断元素的性质变化,如金属性和非金属性、简单气态氢化物的稳定
性、最高价氧化物对应水化物的酸性(或碱性)。
3.结构与性质的互推是解题的要素
(1)电子层数和最外层电子数决定元素的金属性和非金属性。
(2)同主族元素原子的最外层电子数相同,其化学性质具有相似性。
(3)正确推断原子半径和离子半径的大小及结构特点。
【变式练习】
1.五种短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大,甲和丙同族。乙和丁同族。乙和丁的
原子序数之和是甲和丙的2倍。下列判断错误的是( )
A.上述元素中原子半径最大的是丙
B.元素的电负性大小为戊>丁>甲
C.甲和乙、丁、戊均只能形成一种共价型化合物
D.乙和戊形成的某种化合物是常用的消毒剂
2.某化合物可用于制造激光器,其结构如图所示。已知元素X、Y、Z、W原子序数依次递增,且均不大
于20,X与W同族,元素W的原子比Z原子多4个电子。下列说法错误的是( )
A.该化合物中,X、Y、Z之间均为共价键
B.W的单质既能与水反应,也能与甲醇反应
C.Y的氟化物 中,Y的化合价为 价D.Z的氧化物对应的水化物均是强酸
3.物质W常用作漂白剂和氧化剂,其组成元素均为短周期主族元素,各元素原子半径与原子序数的关系
如图所示,实验室中常用CS 洗涤残留在试管壁上的N单质。下列说法正确的是( )
2
A.X、Z形成的化合物与M、N形成的化合物不能发生氧化还原反应
B.实验室中用CS 洗涤残留在试管壁上的N单质,利用了N单质的还原性
2
C.Z的氢化物的沸点一定大于Y的氢化物的沸点
D.化合物W常用作氧化剂,不宜在高温下使用
探究四 基态原子核外电子排布
已知A、B、C、D、E是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素。B元素原
子最高能级的不同轨道都有电子,并且自旋方向相同。C元素原子的价层电子排布式nsnnp2n。D元素原子
中只有三个能层,最外层只有一种自旋方向的电子。E元素原子的最外层只有一个电子,其次外层内的所
有轨道的电子均成对。下列说法正确的是( )
A.元素A与B形成化合物,均为气态
B.B、C、D元素第一电离能:C>B>D
C.元素C、D形成的化合物中,阴阳离子个数比为1∶2
D.元素C、E只能形成一种黑色化合物
规律总结:解答基态原子核外电子排布题,要明确核外电子排布“三原则”,考虑电子在能级轨道上的填
充顺序,确定原子核外电子排布情况。
1.基态原子核外电子排布式书写的思维流程
(1)简化电子排布式的书写方法:用“[X]+价电子排布式”来表示,X是上周期稀有气体的元素符号。
(2)基态离子电子排布式的书写方法:先写出基态原子核外电子排布式,再根据电子得失数目,确定基态离
子电子排布式。
注意:第四周期过渡金属元素原子失电子变成离子时,要先失去4s轨道电子,后失去3d轨道电子。
2.基态原子(价层电子)电子排布图(轨道表示式)书写的思维流程注意:电子排布图(轨道表示式)中,用“□”或“◯”表示原子轨道,用“↑” “↓”表示自旋方向不同
的电子。
【变式练习】
1.关于硅原子核外电子的描述错误的是( )
A.有5种运动状态不同的电子 B.有4种空间伸展方向
C.有5种能量不同电子 D.占据了8个轨道
2.《明会典》中记载:“嘉靖中则例,通宝钱六百万文,合用二火黄铜四万七千二百七十二斤……”这
里黄铜是铜锌合金。下列说法错误的是( )
A.锌、铜均位于元素周期表的 区
B.在铜、锌中,第二电离能与第一电离能相差较大的是锌
C.在潮湿空气中,与黄铜中的铜相比,纯铜中的铜更容易被腐蚀
D.用黄铜不用铁铸造“通宝钱”,主要因为黄铜的化学性质比铁稳定
3.下列有关化学用语中错误的是( )
A. 的结构示意图:
B.乙醇的空间填充模型:
C.用电子式表示 的形成过程:
D.镍的基态原子的价电子排布式:
探究五 中心原子杂化轨道问题根据下列实验现象和有关数据,推断错误的是( )
A.原混合物中含0.03molCuO B.白色沉淀M为CuI
C.CCl 和I 都是非极性分子 D.气体R分子是V形分子
4 2
规律总结:中心原子杂化轨道类型的判断题,常根据σ键和孤对电子的数进行确定,思维流程如下:
1.分析分子(或离子)中心原子形成σ键的数目,看是否含有孤对电子。
2.杂化轨道用于形成σ键和容纳孤对电子,则有:杂化轨道数目=σ数+孤对电子对数,故用杂化轨道数目
减去1个参与杂化的s轨道,剩余为参与杂化的p轨道数目。
杂化类型 用于杂化的原子轨道 杂化轨道数 杂化轨道间的夹角
sp杂化 1个ns轨道和1个np轨道 2 180°
sp²杂化 1个ns轨道和2个np轨道 3 120°
sp³杂化 1个ns轨道和3个np轨道 4 109°28′
【变式练习】
1.中国科学院制备出超小铜纳米晶嵌入的氮掺杂碳纳米片催化剂,该催化剂可用来实现高效电催化CO
2
转化为所期望的新能源产物。下列说法正确的是( )
A.基态Cu原子外围电子排布式为3d94s2 B.中子数为8的N原子可表示为
C.第一电离能大小: D. CO 是非极性分子
2
2.氯气及其化合物在生产和生活中具有重要应用。下列有关说法正确的是( )
A. 中氯原子的杂化轨道类型为
B.为了增强 溶液的氧化性,可选用浓盐酸进行酸化
C.氯气有毒,在通风棚中制备氯气可以消除氯气的污染
D.50mL 12 浓盐酸与足量 共热反应,可生成0.15mol
3.类比是学习化学的重要方法,下列类比结果合理的是( )选项 已知 结论
A 沸点: 沸点:HFHI
C 的分子构型为V形 二甲醚的分子骨架(C—O—C)构型为V形
溶解度:
D 溶解度:
A.A B.B C.C D.D
探究六 晶胞结构及计算题
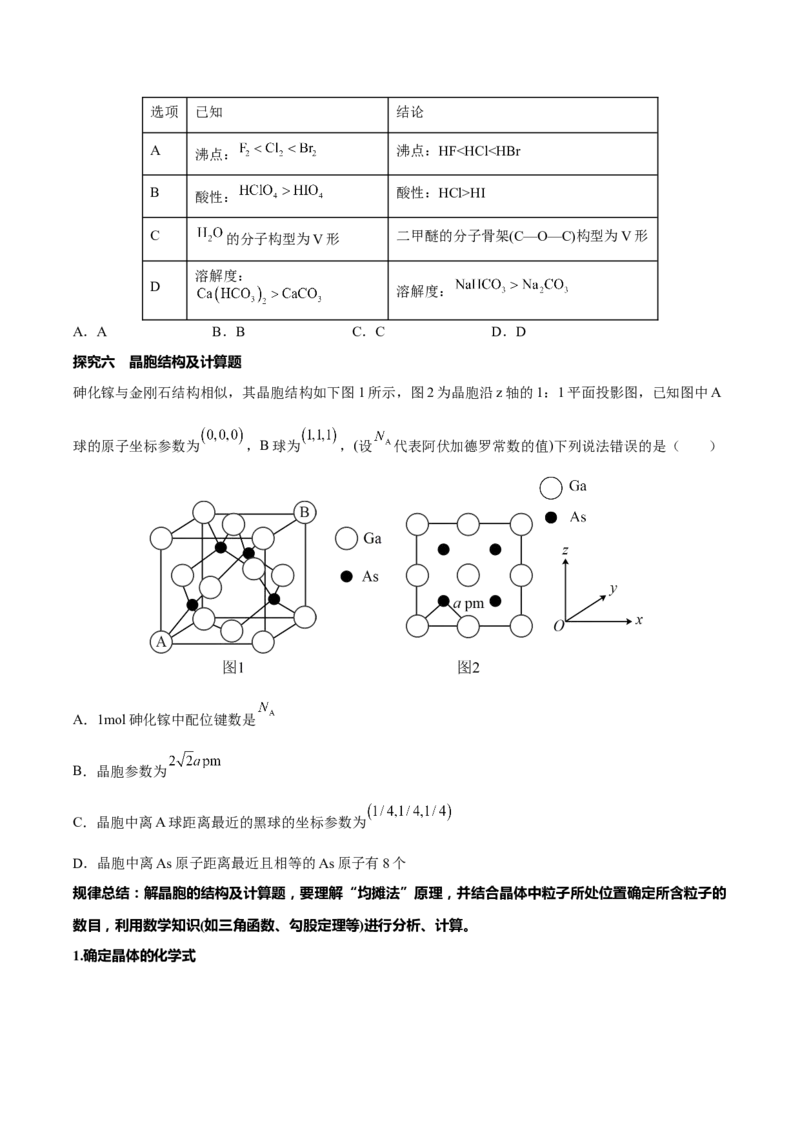
砷化镓与金刚石结构相似,其晶胞结构如下图1所示,图2为晶胞沿z轴的1:1平面投影图,已知图中A
球的原子坐标参数为 ,B球为 ,(设 代表阿伏加德罗常数的值)下列说法错误的是( )
A.1mol砷化镓中配位键数是
B.晶胞参数为
C.晶胞中离A球距离最近的黑球的坐标参数为
D.晶胞中离As原子距离最近且相等的As原子有8个
规律总结:解晶胞的结构及计算题,要理解“均摊法”原理,并结合晶体中粒子所处位置确定所含粒子的
数目,利用数学知识(如三角函数、勾股定理等)进行分析、计算。
1.确定晶体的化学式2.计算晶体的密度
3.计算晶体中粒子间的距离
4.计算空间利用率
【变式练习】
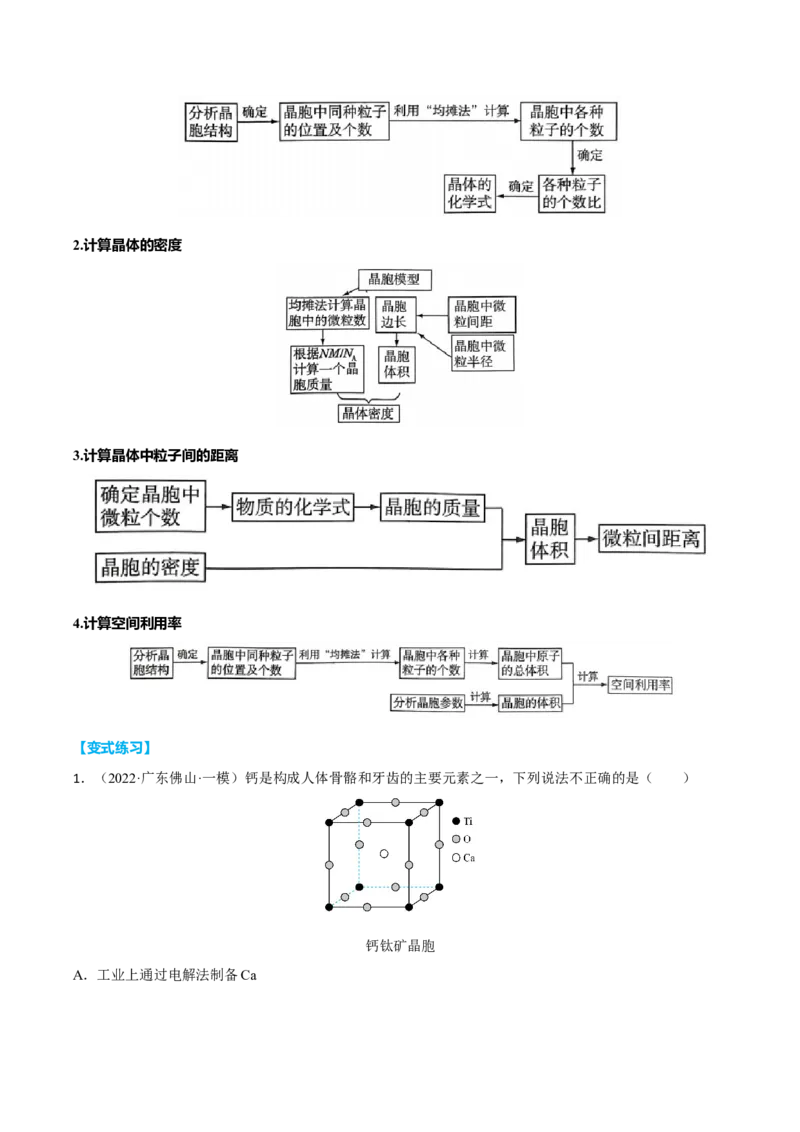
1.(2022·广东佛山·一模)钙是构成人体骨骼和牙齿的主要元素之一,下列说法不正确的是( )
钙钛矿晶胞
A.工业上通过电解法制备CaB. 可用于海水提镁,其阴离子空间构型为平面三角形
C.钙钛矿晶体中钛离子周围与它最近且距离相等的钛离子个数为8
D.钙钛矿晶胞中氧、钙、钛的粒子个数比为3:1:1
2.几种离子晶体的晶胞如图所示,下列说法正确的是( )
A.熔沸点:NaClY>X
B.氢化物的沸点:Z>Y
C.常温下可以用铁制容器盛装Y的最高价氧化物对应水化物的浓溶液
D.两种配体中的键角:
10.(2022·广西南宁·模拟预测)W、X、Y、Z为原子序数依次增大的短周期元素。W的简单氢化物与Z的单质相遇可产生白烟;W与X的最外层电子数之和为Y与Z最外层电子数之和的一半。下列叙述正确的
是( )
A.简单离子半径:Z>X>W
B.含氧酸的酸性:Z>W>Y
C.W、X形成的化合物是离子化合物
D.Y、Z形成的化合物中各原子均满足8电子稳定结构
1.(2022·安徽师范大学附属中学模拟预测)一种由短周期主族元素组成的化合物(如图所示),具有良好
的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是(
)
A.该化合物中,W、X、Y之间均为共价键
B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
2.(2022·浙江·金华市曙光学校模拟预测)现有4种短周期主族元素X、Y、Z和Q,原子序数依次增
大,其中Z、Q在同一周期。相关信息如下表:
元素 相关信息
X 最外层电子数是核外电子总数的一半
Y 最高化合价和最低化合价之和为零
Z 单质为淡黄色固体,常存在于火山喷口附近
Q 同周期元素中原子半径最小
下列说法正确的是( )
A.常温时,X单质能与水发生剧烈反应
B.Y与Q元素组成的YQ 分子,空间构型为正四面体
4C.Y、Z、Q最高价氧化物对应水化物的酸性依次减弱
D.第五周期且与Q同主族元素的单质在常温常压下呈液态
3.(2022·安徽黄山·二模)一种药物原料的分子结构式如图所示。其中W、X、Y、Z均为短周期主族元
素,且仅X、Y位于同一周期;Z原子的核外电子数比X原子的多10。下列说法正确的是( )
A.原子半径:r(Y)>r(X)>r(W)
B.XZ 中X的化合价为+2
2
C.X的最简单氢化物的沸点比Y的高
D.X、Y、Z均可形成至少两种常见的含氧酸
14.(2022·辽宁·阜新实验中学一模)近日,科学家研究利用CaF 晶体释放出的Ca2+和F-脱除硅烷,拓展
2
了金属氟化物材料的生物医学功能。下列说法错误的是( )
A.F、Si和Ca 电负性依次减小,原子半径依次增大
B.OF 与 SiO 中含有化学键类型和氧原子杂化方式均相同
2 2
C.图中A处原子分数坐标为(0,0,0),则B 处原子分数坐标为
D.脱除硅烷反应速率依赖于晶体提供自由氟离子的能力,脱硅能力
5.(2022·湖北·随州市曾都区第一中学二模)下列有关物质性质与应用的对应关系正确的是( )
选项 性质 实际应用
A 小苏打不稳定,受热分解生成CO 用于泡沫灭火器
2
B 聚乙炔是无限延伸的线状结构 用于导电材料C Al(OH) 受热分解,生成高熔点物质和水 用作塑料的阻燃剂
3
D 石墨是混合型晶体,含大π键 用作润滑剂
A.A B.B C.C D.D
6.(2022·辽宁·东北育才学校三模)下表是周期表中5种元素的相关信息,其中Q、W、X位于同一周
期。
元
信息 元素 信息
素
位于周期表的第3周期第ⅢA
Q Y 焰色反应为紫色
族
W 最高正化合价为+7价 原子结构示意图为
Z
X 本周期中原子半径最大
下列说法正确的是( )
A.Q在地壳中含量最高
B.元素的金属性:
C.气态氢化物的稳定性:
D.Q的最高价氧化物对应的水化物既能与NaOH反应,又能与HCl反应
7.(2022·广东深圳·一模)亚铁氰化铁又名普鲁士蓝,化学式为 ,是一种配位化合物,可
以用来上釉、用作油画染料等。下列有关普鲁士蓝构成微粒的符号表征正确的是( )
A.基态 的价电子排布图为
B.氮原子的结构示意图为
C. 的电子式为D.阴离子的结构式为
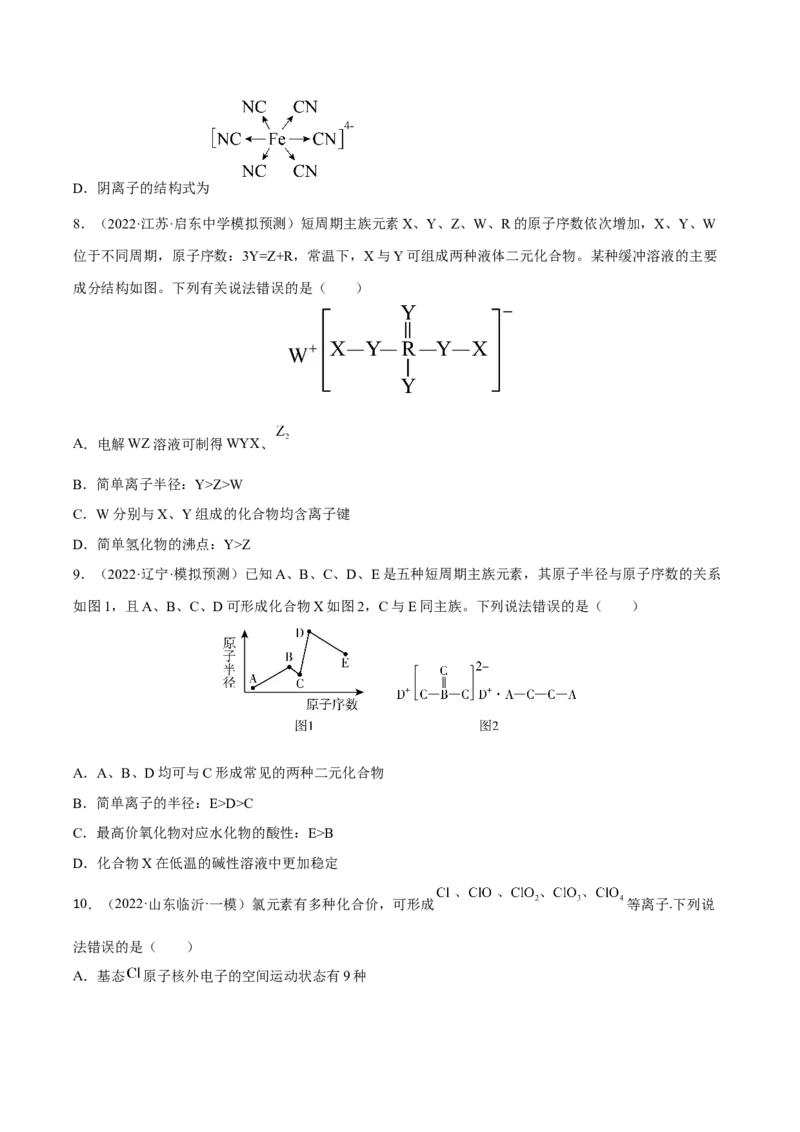
8.(2022·江苏·启东中学模拟预测)短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W
位于不同周期,原子序数:3Y=Z+R,常温下,X与Y可组成两种液体二元化合物。某种缓冲溶液的主要
成分结构如图。下列有关说法错误的是( )
A.电解WZ溶液可制得WYX、
B.简单离子半径:Y>Z>W
C.W分别与X、Y组成的化合物均含离子键
D.简单氢化物的沸点:Y>Z
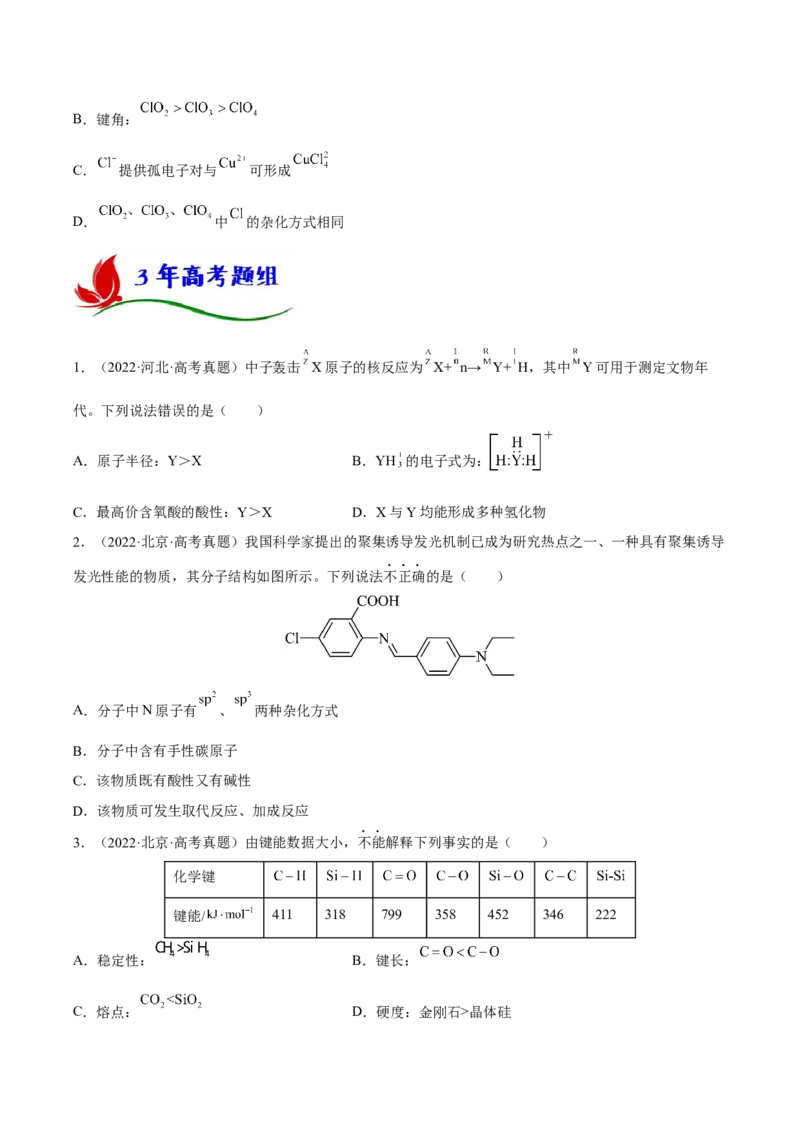
9.(2022·辽宁·模拟预测)已知A、B、C、D、E是五种短周期主族元素,其原子半径与原子序数的关系
如图1,且A、B、C、D可形成化合物X如图2,C与E同主族。下列说法错误的是( )
A.A、B、D均可与C形成常见的两种二元化合物
B.简单离子的半径:E>D>C
C.最高价氧化物对应水化物的酸性:E>B
D.化合物X在低温的碱性溶液中更加稳定
10.(2022·山东临沂·一模)氯元素有多种化合价,可形成 等离子.下列说
法错误的是( )
A.基态 原子核外电子的空间运动状态有9种B.键角:
C. 提供孤电子对与 可形成
D. 中 的杂化方式相同
1.(2022·河北·高考真题)中子轰击 X原子的核反应为 X+ n→ Y+ H,其中 Y可用于测定文物年
代。下列说法错误的是( )
A.原子半径:Y>X B.YH 的电子式为:
C.最高价含氧酸的酸性:Y>X D.X与Y均能形成多种氢化物
2.(2022·北京·高考真题)我国科学家提出的聚集诱导发光机制已成为研究热点之一、一种具有聚集诱导
发光性能的物质,其分子结构如图所示。下列说法不正确的是( )
A.分子中N原子有 、 两种杂化方式
B.分子中含有手性碳原子
C.该物质既有酸性又有碱性
D.该物质可发生取代反应、加成反应
3.(2022·北京·高考真题)由键能数据大小,不能解释下列事实的是( )
化学键
键能/ 411 318 799 358 452 346 222
A.稳定性: B.键长:
C.熔点: D.硬度:金刚石>晶体硅4.(2022·湖北·高考真题)磷酰三叠氮是一种高能分子,结构简式为 。下列关于该分子的说法
正确的是( )
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出 D.分解产物 的电子式为
5.(2022·湖北·高考真题) 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下列关
于该碳玻璃的说法错误的是( )
A.具有自范性 B.与 互为同素异形体
C.含有 杂化的碳原子 D.化学性质与金刚石有差异
6.(2022·江苏·高考真题)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的
是( )
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
7.(2022·江苏·高考真题)下列说法正确的是( )
A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
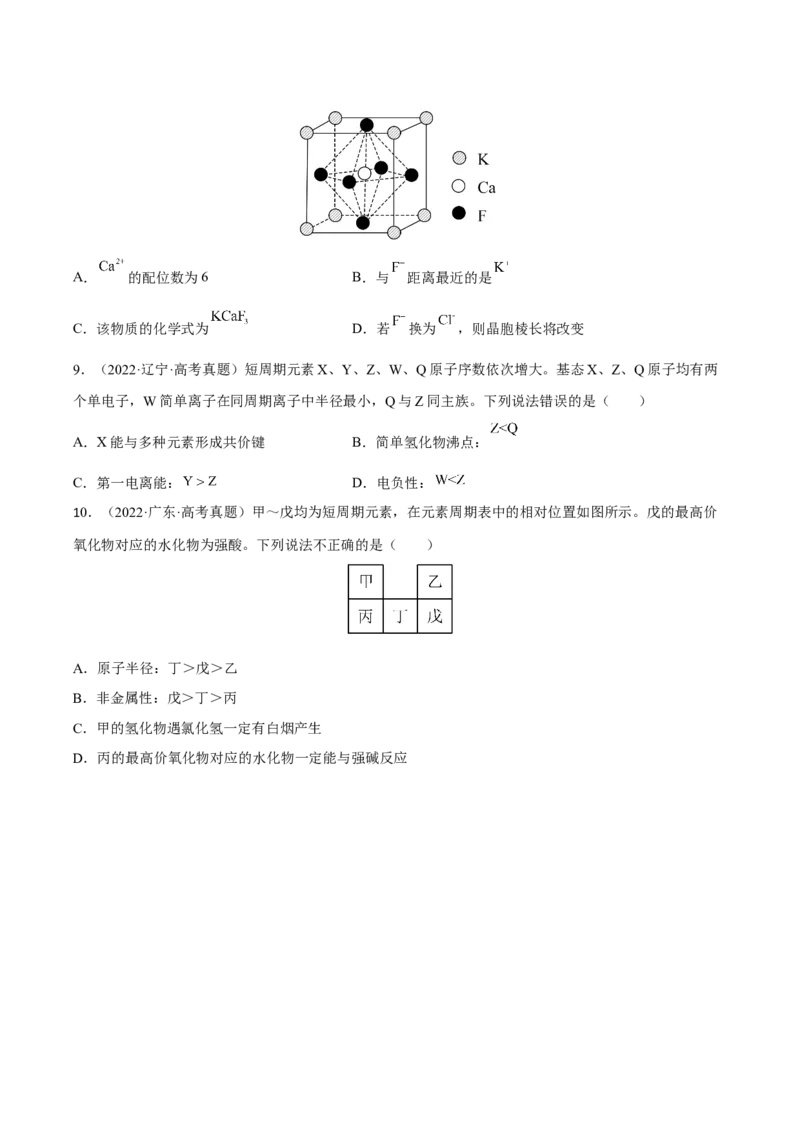
8.(2022·湖北·高考真题)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
( )A. 的配位数为6 B.与 距离最近的是
C.该物质的化学式为 D.若 换为 ,则晶胞棱长将改变
9.(2022·辽宁·高考真题)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两
个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:
C.第一电离能: D.电负性:
10.(2022·广东·高考真题)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价
氧化物对应的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应