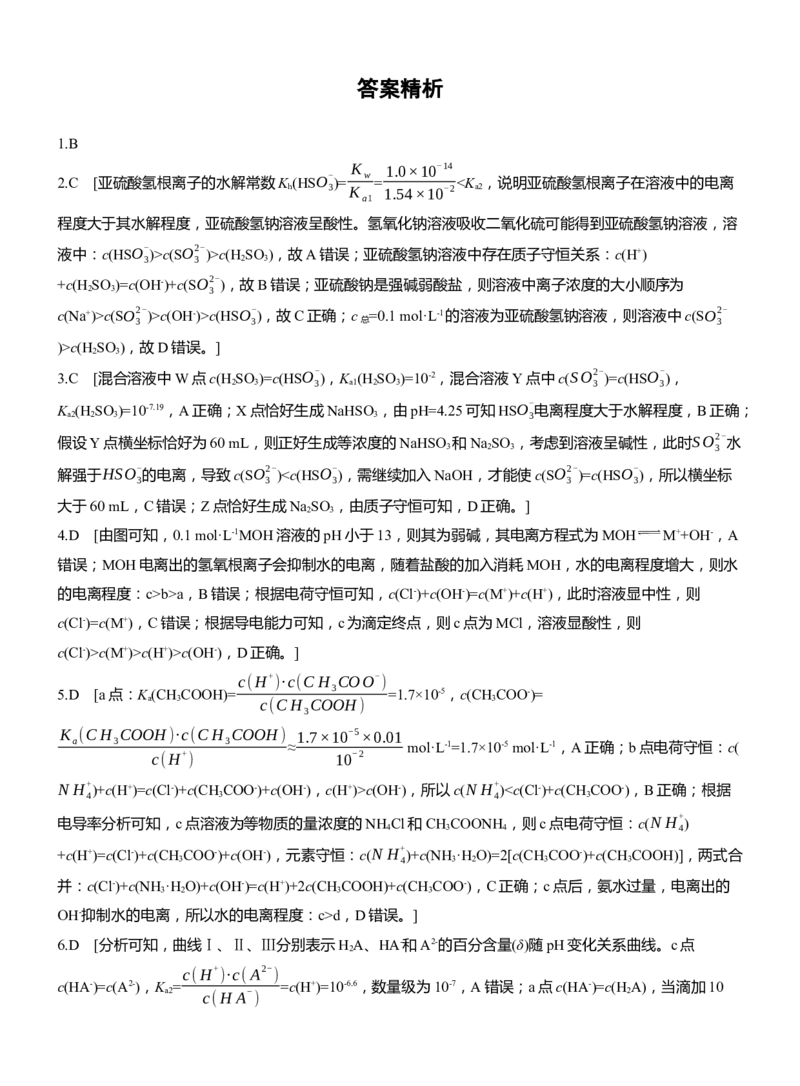文档内容
溶液中的离子浓度关系与滴定曲线分析
(选择题1~5题,每小题3分,6~12题,每小题5分,共50分)
1.下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1
NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO2- )>c(HCO-
3 3 3
)>c(OH-)
B.20 mL 0.1 mol·L-1 CH COONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CH COO-)>c(Cl-)>c(CH COOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH+
)+c(OH-)
4
D.0.1 mol·L-1 CH COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CH COOH)
3
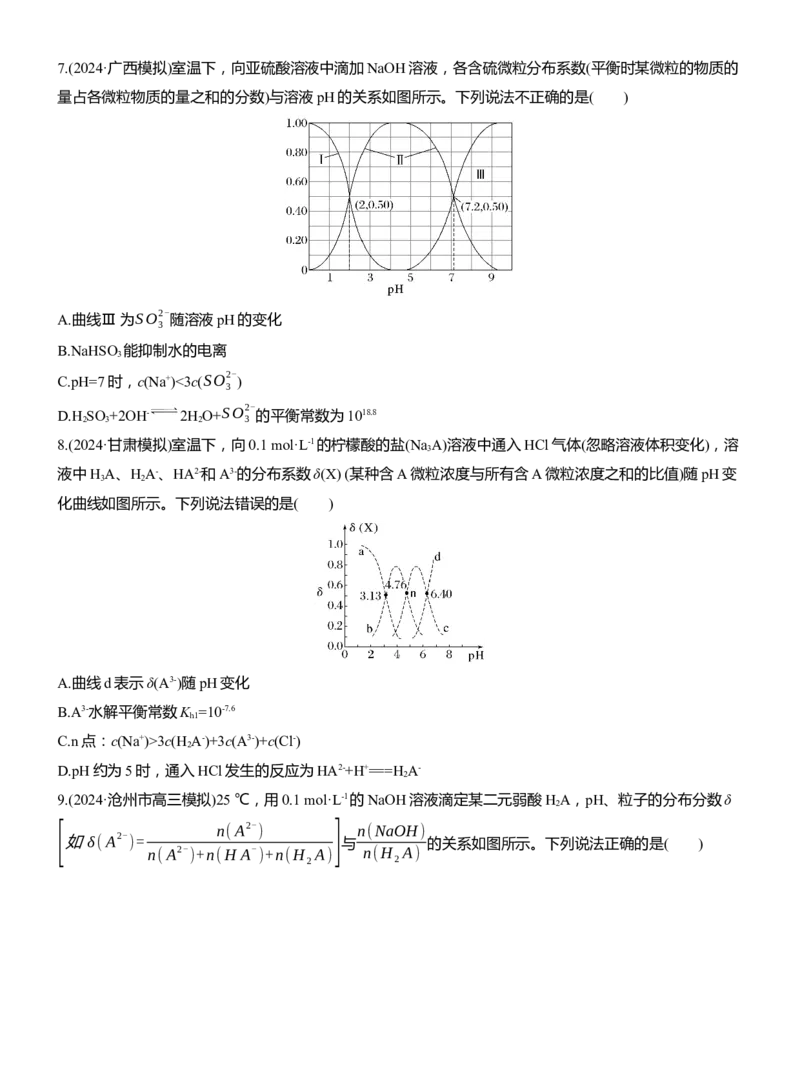
2.(2023·江苏百校联考高三第一次考试)室温下用0.1 mol·L-1 NaOH溶液吸收SO ,若通入SO 所引起的溶液
2 2
体积变化和H O挥发可忽略,溶液中含硫物种的浓度c =c(H SO
)+c(HSO- )+c(SO2-
)。H SO 的电离常数分
2 总 2 3 3 3 2 3
别为K =1.54×10-2、K =1.00×10-7。下列说法正确的是( )
a1 a2
A.NaOH溶液吸收SO
所得到的溶液中:c(SO2- )>c(HSO-
)>c(H SO )
2 3 3 2 3
B.NaOH完全转化为NaHSO
时,溶液中:c(H+)+c(SO2-
)=c(OH-)+c(H SO )
3 3 2 3
C.NaOH完全转化为Na SO
时,溶液中:c(Na+)>c(SO2- )>c(OH-)>c(HSO-
)
2 3 3 3
D.NaOH溶液吸收SO ,c =0.1 mol·L-1溶液中:c(H SO
)>c(SO2-
)
2 总 2 3 3
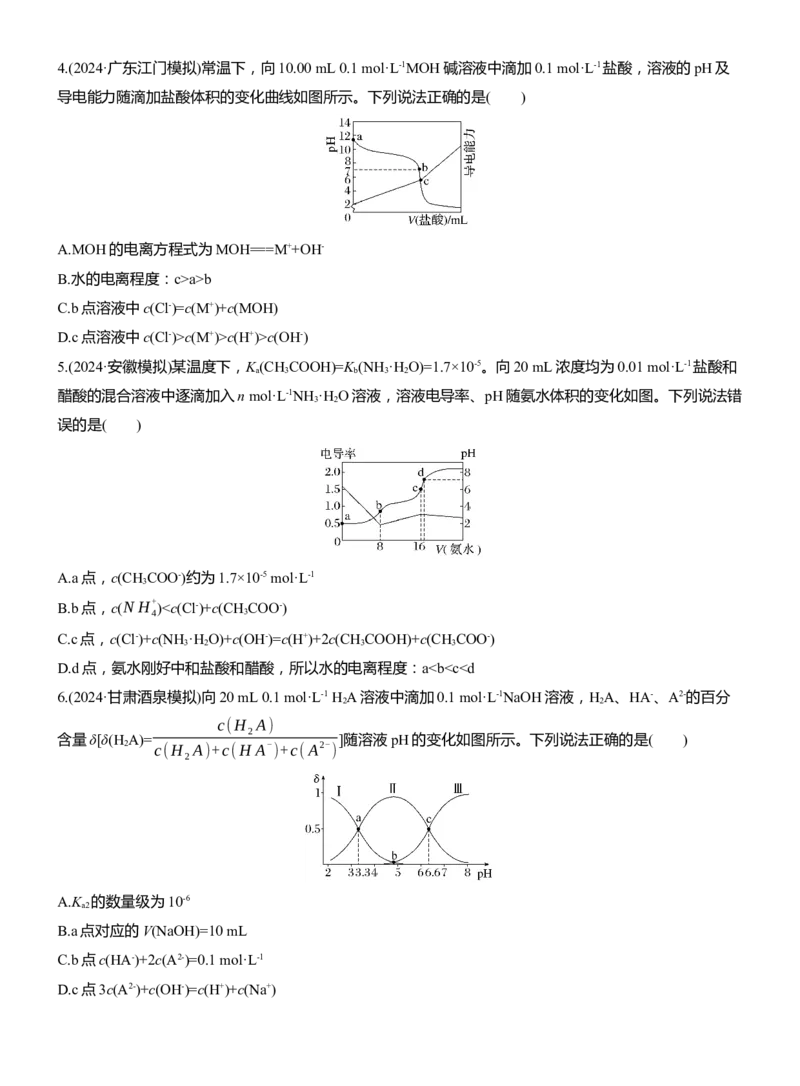
3.(2024·湖南邵阳模拟)常温下,用0.1 mol·L-1NaOH溶液滴定40 mL 0.1 mol·L-1H SO 溶液,所得滴定曲线
2 3
如图所示(忽略混合时溶液体积的变化)。下列叙述错误的是( )
A.由W点可求出K (H SO ) =10-2
a1 2 3
B.图中X点对应的溶液中:c(Na+)>c(HSO- )>c(SO2-
)>c(OH-)
3 3
C.图中Y点对应的横坐标小于60 mL
D.图中Z点对应的溶液中:c(H+)+c(HSO-
)+2c(H SO )=c(OH-)
3 2 34.(2024·广东江门模拟)常温下,向10.00 mL 0.1 mol·L-1MOH碱溶液中滴加0.1 mol·L-1盐酸,溶液的pH及
导电能力随滴加盐酸体积的变化曲线如图所示。下列说法正确的是( )
A.MOH的电离方程式为MOH===M++OH-
B.水的电离程度:c>a>b
C.b点溶液中c(Cl-)=c(M+)+c(MOH)
D.c点溶液中c(Cl-)>c(M+)>c(H+)>c(OH-)
5.(2024·安徽模拟)某温度下,K(CH COOH)=K (NH ·H O)=1.7×10-5。向20 mL浓度均为0.01 mol·L-1盐酸和
a 3 b 3 2
醋酸的混合溶液中逐滴加入n mol·L-1NH ·H O溶液,溶液电导率、pH随氨水体积的变化如图。下列说法错
3 2
误的是( )
A.a点,c(CH COO-)约为1.7×10-5 mol·L-1
3
B.b点,c(N H+ )3c(H A-)+3c(A3-)+c(Cl-)
2
D.pH约为5时,通入HCl发生的反应为HA2-+H+===H A-
2
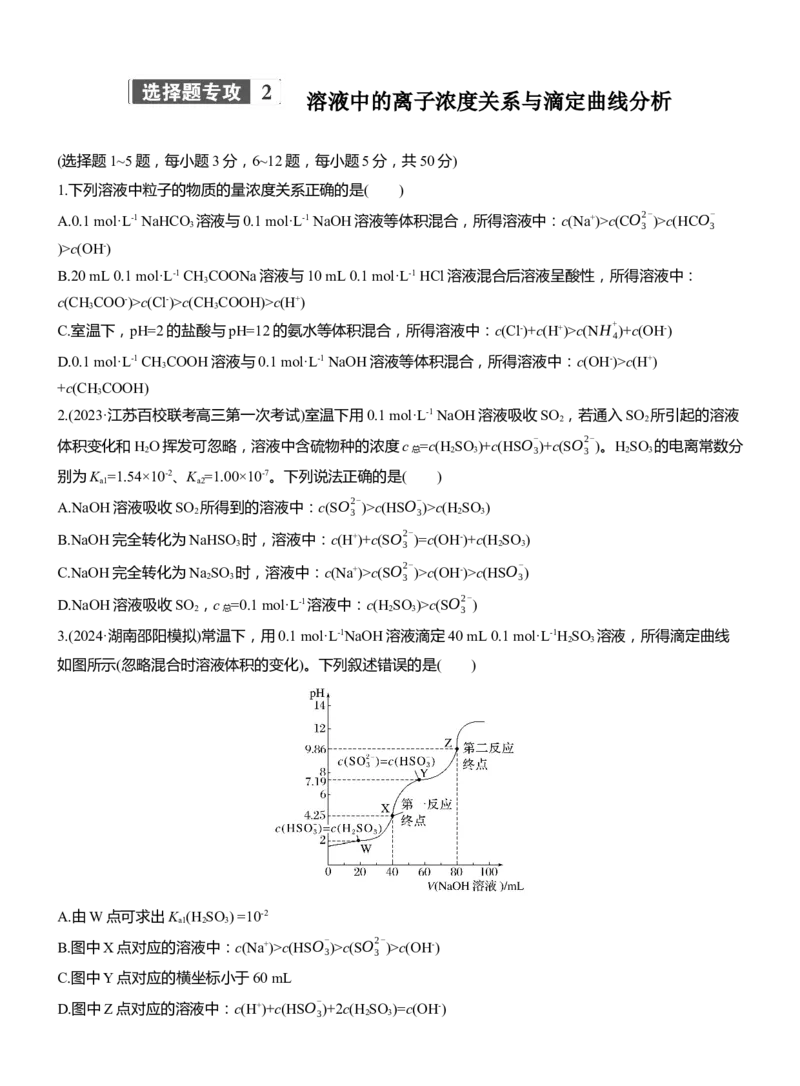
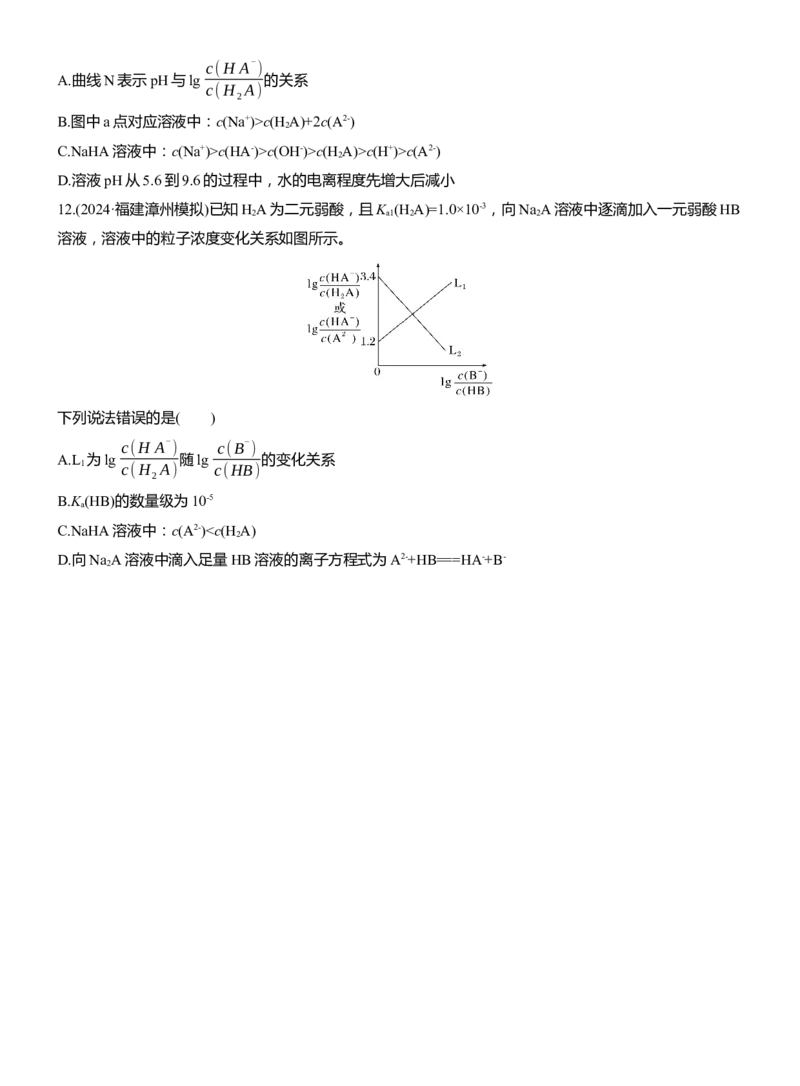
9.(2024·沧州市高三模拟)25 ℃,用0.1 mol·L-1的NaOH溶液滴定某二元弱酸H A,pH、粒子的分布分数δ
2
[ n(A2- ) ] n(NaOH)
如δ(A2- )= 与 的关系如图所示。下列说法正确的是( )
n(A2- )+n(H A- )+n(H A) n(H A)
2 2A.曲线Ⅱ表示δ(A2-)的变化曲线
n(NaOH)
B. =1时,c(Na+)>c(HA-)>c(H A)>c(A2-)
n(H A) 2
2
n(NaOH)
C. =1.5时,3(Na+)=2[c(H A- )+c(H A)+c(A2- )]
n(H A) 2
2
D.a、b、c、d、e、f六点溶液中,f中水的电离程度最大
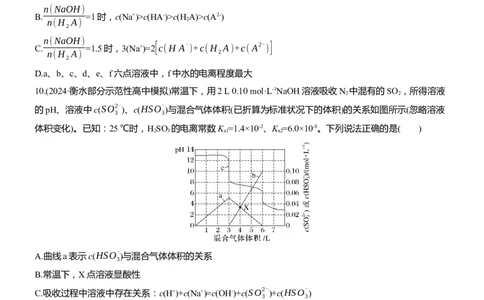
10.(2024·衡水部分示范性高中模拟)常温下,用2 L 0.10 mol·L-1NaOH溶液吸收N 中混有的SO ,所得溶液
2 2
的pH、溶液中c(SO2- )、c(HSO-
)与混合气体体积(已折算为标准状况下的体积)的关系如图所示(忽略溶液
3 3
体积变化)。已知:25 ℃时,H SO 的电离常数K =1.4×10-2、K =6.0×10-8。下列说法正确的是( )
2 3 a1 a2
A.曲线a表示c(HSO-
)与混合气体体积的关系
3
B.常温下,X点溶液显酸性
C.吸收过程中溶液中存在关系:c(H+)+c(Na+)=c(OH-)+c(SO2- )+c(HSO-
)
3 3
D.混合气体中SO 的体积分数约为74.7%
2
11.(2024·广西模拟)常温下将NaOH溶液滴加到H A溶液中,混合溶液的pH与离子浓度变化的关系如图所
2
c(H A- ) c(A2- )
示[纵坐标为lg 或lg ]。下列叙述正确的是( )
c(H A) c(H A- )
2c(H A- )
A.曲线N表示pH与lg 的关系
c(H A)
2
B.图中a点对应溶液中:c(Na+)>c(H A)+2c(A2-)
2
C.NaHA溶液中:c(Na+)>c(HA-)>c(OH-)>c(H A)>c(H+)>c(A2-)
2
D.溶液pH从5.6到9.6的过程中,水的电离程度先增大后减小
12.(2024·福建漳州模拟)已知H A为二元弱酸,且K (H A)=1.0×10-3,向Na A溶液中逐滴加入一元弱酸HB
2 a1 2 2
溶液,溶液中的粒子浓度变化关系如图所示。
下列说法错误的是( )
c(H A- ) c(B- )
A.L 为lg 随lg 的变化关系
1 c(H A) c(HB)
2
B.K(HB)的数量级为10-5
a
C.NaHA溶液中:c(A2-)c(SO2-
)>c(H SO ),故A错误;亚硫酸氢钠溶液中存在质子守恒关系:c(H+)
3 3 2 3
+c(H SO
)=c(OH-)+c(SO2-
),故B错误;亚硫酸钠是强碱弱酸盐,则溶液中离子浓度的大小顺序为
2 3 3
c(Na+)>c(SO2- )>c(OH-)>c(HSO-
),故C正确;c =0.1
mol·L-1的溶液为亚硫酸氢钠溶液,则溶液中c(SO2-
3 3 总 3
)>c(H SO ),故D错误。]
2 3
3.C [混合溶液中W点c(H SO
)=c(HSO-
),K (H SO
)=10-2,混合溶液Y点中c(SO2- )=c(HSO-
),
2 3 3 a1 2 3 3 3
K (H SO )=10-7.19,A正确;X点恰好生成NaHSO
,由pH=4.25可知HSO-
电离程度大于水解程度,B正确;
a2 2 3 3 3
假设Y点横坐标恰好为60 mL,则正好生成等浓度的NaHSO 和Na SO
,考虑到溶液呈碱性,此时SO2-
水
3 2 3 3
解强于HSO- 的电离,导致c(SO2- )b>a,B错误;根据电荷守恒可知,c(Cl-)+c(OH-)=c(M+)+c(H+),此时溶液显中性,则
c(Cl-)=c(M+),C错误;根据导电能力可知,c为滴定终点,则c点为MCl,溶液显酸性,则
c(Cl-)>c(M+)>c(H+)>c(OH-),D正确。]
c(H+ )·c(CH COO- )
5.D [a点:K(CH COOH)= 3 =1.7×10-5,c(CH COO-)=
a 3 c(CH COOH) 3
3
K (CH COOH)·c(CH COOH) 1.7×10-5×0.01
a 3 3 ≈ mol·L-1=1.7×10-5 mol·L-1,A正确;b点电荷守恒:c(
c(H+
)
10-2
N H+ )+c(H+)=c(Cl-)+c(CH COO-)+c(OH-),c(H+)>c(OH-),所以c(N H+ )d,D错误。]
6.D [分析可知,曲线Ⅰ、Ⅱ、Ⅲ分别表示H A、HA-和A2-的百分含量(δ)随pH变化关系曲线。c点
2
c(H+ )·c(A2-
)
c(HA-)=c(A2-),K = =c(H+)=10-6.6,数量级为10-7,A错误;a点c(HA-)=c(H A),当滴加10
a2 c(H A- ) 2mL NaOH溶液时,二者恰好反应生成NaHA,由于HA-的电离和水解程度不同,c(HA-)≠c(H A),B错误;
2
0.02 L×0.1mol·L-1
b点时c(A2-)=c(H A),c(A2-)+c(H A)+c(HA-)= <0.1 mol·L-1,C错误;c点
2 2 0.02 L+V(NaOH)
c(HA-)=c(A2-),存在电荷守恒:c(OH-)+c(HA-)+2c(A2-)=c(H+)+c(Na+),则3c(A2-)+c(OH-)=c(H+)+c(Na+),D正
确。]
7.C [分析可知,曲线Ⅰ为亚硫酸随溶液pH的变化,曲线Ⅱ为亚硫酸氢根离子随溶液pH的变化,曲线Ⅲ
为亚硫酸根离子随溶液pH的变化,A正确;根据图中信息得到NaHSO 溶液的pH大约为4,说明溶液显
3
酸性,即亚硫酸氢根离子的电离程度大于水解程度,所以抑制水的电离,B正确;pH=7时,
c(H+)=c(OH-),再根据电荷守恒得到c(Na+)=2c(SO2- )+c(HSO- ),又根据图像知,pH=7时c(SO2- )3c(SO2-
),C错误;Ⅰ、Ⅱ交点时,c(H SO
)=c(HSO-
),pH=2,c(H+)=10-2 mol·L-1,
3 2 3 3
K (H SO
)=1×10-2,Ⅱ、Ⅲ交点时,c(SO2- )=c(HSO-
),pH=7.2,c(H+)=10-7.2 mol·L-1,K (H SO )=1×10-7.2,
a1 2 3 3 3 a2 2 3
c(SO2- ) K (H SO )·K (H SO )
则H SO +2OH- 2H
O+SO2-
的平衡常数K=
3
=
a1 2 3 a2 2 3
=
2 3 2 3 c(H SO )·c2 (OH- ) K2
2 3 w
10-2×10-7.2
=1018.8,D正确。]
10-28
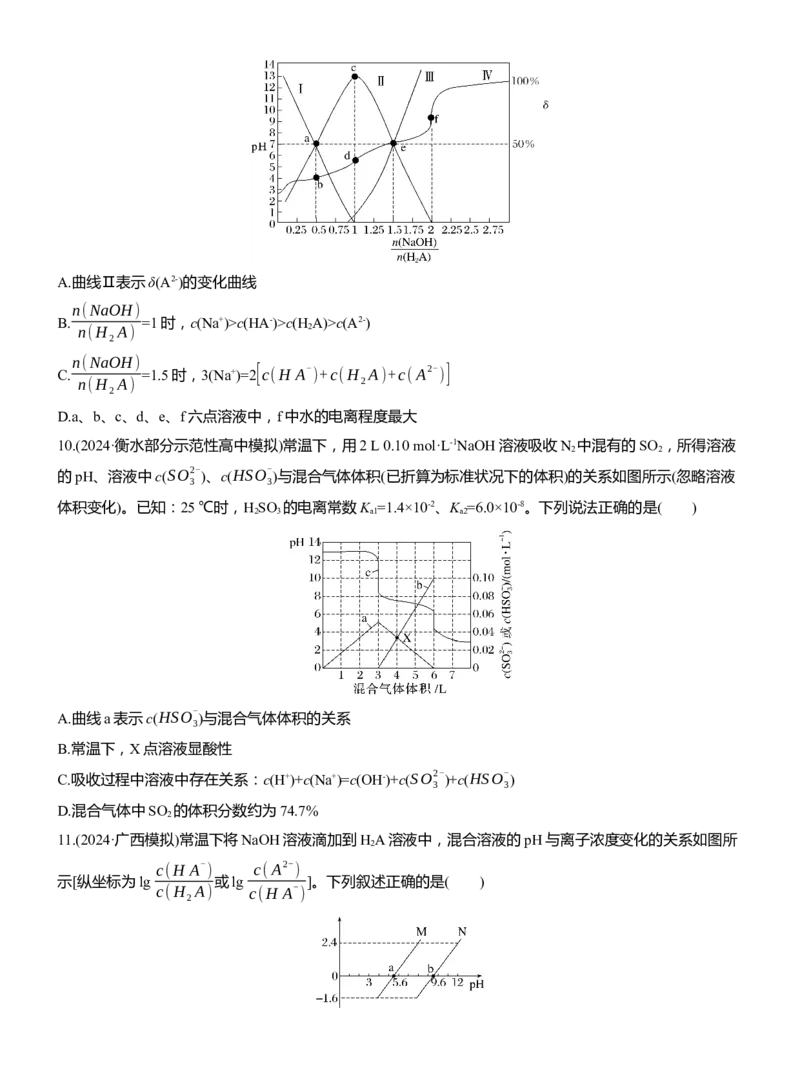
8.C [向0.1 mol·L-1的柠檬酸的盐(Na A)溶液中通入HCl气体,依次发生反应:A3-+H+===HA2-、HA2-
3
+H+===H A-、H A-+H+===H A,所以根据溶液pH及含A微粒浓度关系可知a、b、c、d依次表示H A、
2 2 3 3
H A-、HA2-、A3-的分布系数随pH变化的曲线,A正确;由图可知H A的三级电离平衡常数K =10-3.13、
2 3 a1
c(H A2- )·c(OH- ) K 10-14
w
K =10-4.76、K =10-6.40,A3-水解平衡常数K = = = =10-7.6,B正确;n点:
a2 a3 h1 c(A3- ) K 10-6.40
a3
c(H A-)=c(HA2-),溶液pH<7,故c(H+)>c(OH-),电解质溶液电荷守恒为c(Na+)+c(H+)=c(H A-)+2c(HA2-)
2 2
+3c(A3-)+c(OH-)+c(Cl-),故溶液中离子浓度关系为c(Na+)<3c(H A-)+3c(A3-)+c(Cl-),C错误;根据图中信息当
2
溶液pH约为5时,随着pH减小,c(HA2-)逐渐减小、c(H A-)逐渐增大,发生反应:HA2-+H+===H A-,D正
2 2
确。]
9.D [由图可知,曲线Ⅳ为0.1 mol·L-1 NaOH溶液滴定二元弱酸H A的滴定曲线,曲线Ⅰ、Ⅱ、Ⅲ为0.1
2
mol·L-1 NaOH溶液滴定二元弱酸H A的各粒子的分布分数曲线。曲线Ⅰ代表δ(H A),曲线Ⅱ代表δ(HA-),
2 2
n(NaOH)
曲线Ⅲ代表δ(A2-)。 =1时,反应生成NaHA,NaHA溶液显酸性,HA-的电离程度大于水解程度,
n(H A)
2
n(NaOH)
c(A2-)>c(H A),B项错误; =1.5时,得到等浓度的NaHA和Na A混合溶液,由元素守恒得
2 n(H A) 2
2
n(NaOH)
2c(Na+)=3[c(HA-)+c(H A)+c(A2-)],C项错误;f点 =2,溶液中溶质为Na A,水的电离程度最大,
2 n(H A) 2
2
D项正确。]10.D [NaOH溶液吸收N 中混有的SO 时,随所吸收的气体体积增大,依次发生反应:
2 2
①2NaOH+SO ===Na SO +H O,②Na SO +SO +H O===2NaHSO ,所以溶液的pH出现两次突跃,曲线c
2 2 3 2 2 3 2 2 3
为溶液的pH与混合气体体积的关系,曲线a为c(SO2- )与混合气体体积的关系,曲线b为c(HSO-
)与混合
3 3
气体体积的关系,故A错误;常温下,X点c(SO2- )=c(HSO-
),则c(H+)=K (H SO )=6.0×10-8 mol·L-1,溶
3 3 a2 2 3
液显弱碱性,故B错误;根据电荷守恒,吸收过程中溶液中存在关系:c(H+)+c(Na+)=c(OH-)+2c(SO2-
)+c(
3
1 1
HSO-
),故C错误;图中出现第一次pH突跃时,反应①恰好反应完全,n(SO )= n(NaOH)= ×0.2 mol=0.1
3 2 2 2
0.1mol×22.4 L·mol-1
mol,则混合气体中SO 的体积分数为 ×100%≈74.7%,故D正确。]
2 3 L
c(H A- ) c(A2- )
11.C [因为纵坐标为lg 或lg ,分别取a、b点,则此时对应曲线上有c(H A)=c(HA-)和
c(H A) c(H A- ) 2
2
c(A2-)=c(HA-),可以算出对应曲线的电离平衡常数为10-5.6和10-9.6,因为K >K ,所以K =10-5.6,K =10-
a1 a2 a1 a2
c(H A- ) c(A2- )
9.6,所以曲线M、N分别表示pH与lg 和pH与lg 的关系,A项错误;a点对应溶液中存
c(H A) c(H A- )
2
在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)且此时c(H A)=c(HA-),所以c(Na+)+c(H+)=c(OH-)+c(H A)
2 2
K
w
+2c(A2-),a点pH=5.6,则c(H+)>c(OH-),所以c(Na+)c(HA-)>c(OH-)>c(H A)>c(H+)>c(A2-),C项正确;初始溶质为H A,呈酸性,电离出的氢离子抑制水
2 2
的电离,完全反应时生成Na A,Na A水解呈碱性,促进水的电离,所以由H A到完全生成Na A的过程
2 2 2 2
中,水的电离程度一直增大,则溶液pH从5.6到9.6的过程中,水的电离程度逐渐增大,D项错误。]
c(B-
)
12.C [向Na A溶液中逐滴加入一元弱酸HB溶液,c(H+)增大,根据电离平衡常数不变可知lg 、lg
2 c(HB)
c(H A- ) c(H A- ) c(H A- ) c(B- ) c(H A- )
减小,lg 增大,即L 为lg 随lg 的变化关系,A正确;当lg
c(H A) c(A2- ) 1 c(H A) c(HB) c(H A)
2 2 2
c(B- ) c(H A- )
=1.2时,lg =0,结合K (H A)=1.0×10-3, =101.2,此时c(H+)=10-4.2 mol·L-1,则K(HB)=10-
c(HB) a1 2 c(H A) a
2
c(B- ) c(H A- )
4.2,数量级为10-5,B正确;在直线L 上,lg =0时, =103.4 ,此时c(H+)=10-4.2 mol·L-1,则
2 c(HB) c(A2- )
K
w
K (H A)=1.0×10-7.6,NaHA溶液中,K = =1.0×10-11,即HA-的电离程度大于水解程度,则
a2 2 h K
a1
c(A2-)>c(H A),C错误;因K (H A)>K(HB)>K (H A),则酸性:H A>HB>HA-,所以向Na A溶液中滴入
2 a1 2 a a2 2 2 2
足量HB溶液的离子方程式为A2-+HB===HA-+B-,D正确。]