文档内容
专题六 元素周期律与元素周期表 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含16小题,每题3分,共48分。每题只有一个选项符合题意)
1.(2022·上海闵行·统考模拟预测)如图所示的四种短周期主族元素,已知元素X的
原子核外电子数是M的2倍。相关叙述中,错误的是
A.X元素是镁 B.M元素可形成一种温室气体
C.最高价氧化物对应水化物酸性:N>M D.Y的氧化物是铝热剂的成分之一
2.(2022·四川成都·统考模拟预测)已知短周期元素M、N、P、Q原子序数依次增大,
M是短周期中原子半径最大的元素,M、N、P、Q最高价氧化物对应水化物分别为
X、Y、Z、W,常温下X、Z、W均可与Y反应,0.1 mol/L Z、W溶液的pH分别为
0.7和1,下列说法正确的是
A.M的离子半径小于N的离子半径 B.Y是常见的阻燃剂
C.简单氢化物稳定性P大于Q D.X、W含有的化学键类型完全相同
3.(2022·浙江·统考一模)关于化合物HCS 的性质,下列推测不合理的是
2 3
A.在水中缓慢分解产生HCO 和HSO B.可由KCS 酸化制成
2 3 2 3 2 3
C.水溶液为弱酸 D.易分解成HS和CS
2 2
4.(2022·上海徐汇·统考二模)高纯度的锗是一种半导体材料,下图是锗在元素周期
表中的信息,下列说法正确的是A.位于VIA族,处于金属元素与非金属元素分界处
B.原子序数为32
C.最外层电子数为2
D.原子的相对原子质量为72.61
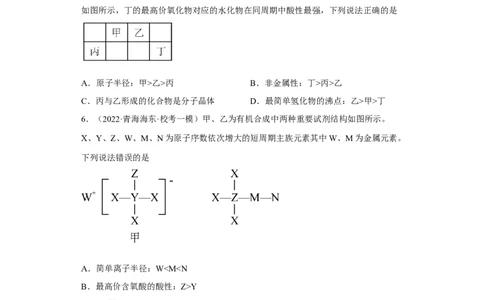
5.(2023·广东广州·一模)甲~丁均为短周期主族元素,在元素周期表中的相对位置
如图所示,丁的最高价氧化物对应的水化物在同周期中酸性最强,下列说法正确的是
A.原子半径:甲>乙>丙 B.非金属性:丁>丙>乙
C.丙与乙形成的化合物是分子晶体 D.最简单氢化物的沸点:乙>甲>丁
6.(2022·青海海东·校考一模)甲、乙为有机合成中两种重要试剂结构如图所示。
X、Y、Z、W、M、N为原子序数依次增大的短周期主族元素其中W、M为金属元素。
下列说法错误的是
A.简单离子半径:WY
C.金属性:W>M
D.工业上可用电解法制备W和M的单质
7.(2022·湖北·模拟预测)1934年,约里奥·居里夫妇用α粒子(即氦核 He)轰击某金
属原子 X得到 Y,具有放射性,可衰变为 ,
。基态Y原子3p能级半充满。下列说法错误的是
A.X原子核内中子数与质子数之比为14∶13
试卷第2页,共9页B.X和Y的氧化物分别为碱性氧化物、酸性氧化物
C.第一电离能:XQ
8.(2022·浙江·模拟预测)已知前四周期主族元素M、W、X、Y、Z的原子序数依次
增大。M为地壳中含量最多的元素,且M、Y、Z位于同一族,Y和Z彼此相邻。W、
X、Y为同周期互不相邻的元素,Y元素原子的最外层电子数是W和X原子的最外层
电子数之和。下列说法正确的是
A. 和 的晶体类型相同
B.简单氢化物的沸点:
C. 和 分子的中心原子Z的杂化方式不同
D.工业上通常利用电解熔融WM的方法来制备W的单质
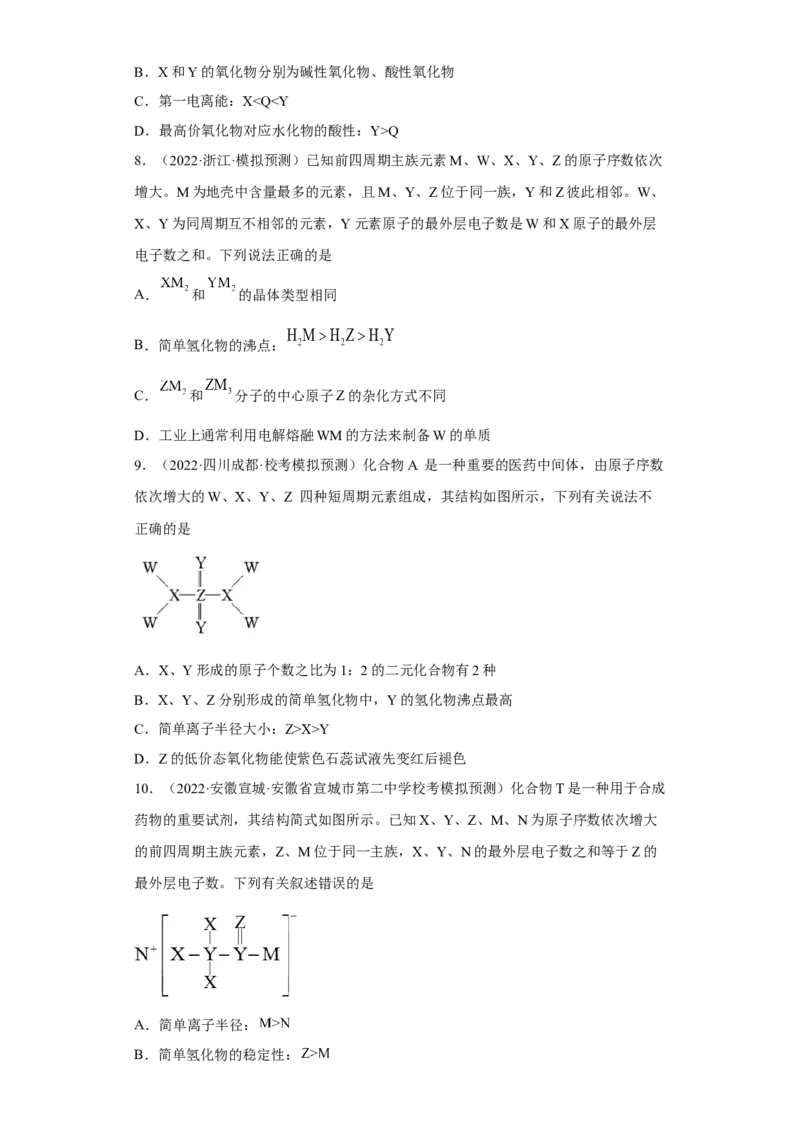
9.(2022·四川成都·校考模拟预测)化合物A 是一种重要的医药中间体,由原子序数
依次增大的W、X、Y、Z 四种短周期元素组成,其结构如图所示,下列有关说法不
正确的是
A.X、Y形成的原子个数之比为1:2的二元化合物有2种
B.X、Y、Z分别形成的简单氢化物中,Y的氢化物沸点最高
C.简单离子半径大小:Z>X>Y
D.Z的低价态氧化物能使紫色石蕊试液先变红后褪色
10.(2022·安徽宣城·安徽省宣城市第二中学校考模拟预测)化合物T是一种用于合成
药物的重要试剂,其结构简式如图所示。已知X、Y、Z、M、N为原子序数依次增大
的前四周期主族元素,Z、M位于同一主族,X、Y、N的最外层电子数之和等于Z的
最外层电子数。下列有关叙述错误的是
A.简单离子半径:
B.简单氢化物的稳定性:C.化合物 与 均为共价化合物
D.化合物T中所有原子均满足8电子相对稳定结构
11.(2022·湖南湘潭·湘乡市第一中学校考三模)W、X、Y和Z为原子序数依次增大
的四种短周期主族元素。常温常压下,Y的单质和氧化物均能与X的氢化物的水溶液
反应生成一种相同的气体,该气体分子与CH 具有相同的空间结构。Z原子最外层的
4
电子数是W原子的最外层电子数的2倍。下列叙述错误的是
A.元素X的氢化物比其他三种元素的氢化物更稳定
B.元素Z的含氧酸只有两种
C.元素Y在自然界中只以化合态形式存在
D.元素W、Y位于周期表中金属与非金属分界线附近
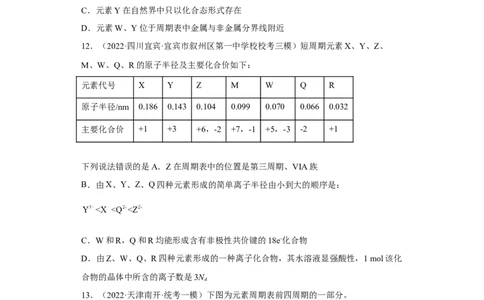
12.(2022·四川宜宾·宜宾市叙州区第一中学校校考三模)短周期元素X、Y、Z、
M、W、Q、R的原子半径及主要化合价如下:
元素代号 X Y Z M W Q R
原子半径/nm 0.186 0.143 0.104 0.099 0.070 0.066 0.032
主要化合价 +1 +3 +6,-2 +7,-1 +5,-3 -2 +1
下列说法错误的是A.Z在周期表中的位置是第三周期、VIA族
B.由X、Y、Z、Q四种元素形成的简单离子半径由小到大的顺序是:
C.W和R,Q和R均能形成含有非极性共价键的18e-化合物
D.由Z、W、Q、R四种元素形成的一种离子化合物,其水溶液显强酸性,1 mol该化
合物的晶体中所含的离子数是3N
A
13.(2022·天津南开·统考一模)下图为元素周期表前四周期的一部分。
X
W Y
Z
下列有关W、X、Y、Z四种元素的说法中,正确的是A.电负性:Z>X B.单质熔点:
Y>Z
试卷第4页,共9页C.原子半径:Y>W D.第一电离能:Y>W
14.(2022·浙江·模拟预测)几种短周期元素的原子半径及主要化合价如表:
元素代号 X Y Z W M
1.86 1.43 0.99 1.60 0.75
原子半径
最高正价
主要化合价
最低负价 - - -
下列说法不正确的是A.M和Z简单氢化物的沸点:M>Z
B.X、Y、Z的最高价氧化物对应的水化物可相互反应
C.离子半径:
D.W的单质与M的单质可反应生成离子化合物
15.(2022·上海·一模)短周期主族元素W、X、Y、Z在周期表中的位置如图所示。
下列说法不正确的是
W X
Y Z
A.W的最简单氢化物的稳定性比X的弱 B.X、Y形成的化合物水溶液显碱性
C.W与Y形成的化合物中一定含有离子键 D.原子半径:Z>Y>X>W
16.(2022·广东茂名·化州市第一中学校考一模)某离子液体含有体积较大的阴、阳离
子(如图所示),其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z在元素
周期表中处于相邻位置。下列说法正确的是
A.原子半径:Z>X>Y B.氢化物的稳定性:Z>X>Y
C.键角: D.此阴离子中Y、Z均满足8电子稳定
结构二、非选择题 (本题共5小题,1-3题每题10分,4-5题每题11分,共52分)
17.(2022·上海松江·统考一模)新工艺采用金属氧化物 催化尿素与甲醇合成
碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
反应①: +2CH OH(g)
3
+2NH(g)
3
反应②:2NH (g)+CO (g) +H O(l)
3 2 2
完成下列填空:
(1)C原子核外能量最高的电子有______个,比较 、N、O简单离子的半径大小
__________。
(2)下列事实能说明氮的非金属性比碳强的是______(选填编号)。
a.酸性: b.最高正价:氮>碳
c.沸点: d.吸引电子能力强弱:氮>碳
(3)达到平衡时,反应①碳酸二甲酯的产率 随温度T的变化关系如图所示,则反应
是__________反应(选填“放热”或“吸热”), ______ (选填“>”或
“<”)。
(4)某一恒温恒容 装置内, 与 发生反应②, 后,气体的密度减少
试卷第6页,共9页,则 内氨气的平均反应速率为__________。
(5)传统合成DMC的方法是以光气( ,有剧毒)和甲醇为原料,请写出相应
的化学方程式__________。
(6)新工艺合成DMC的方法和传统方法相比,优点有__________(任写两点)。
18.(2022·上海宝山·上海市行知中学校考模拟预测)氮元素和氯元素在自然界广泛存
在,请回答下列问题:
(1)氮元素原子核外有_______个未成对电子,有_______种能量不同的电子。
(2)氯元素在周期表中的位置是_______,其原子最外层电子排布式为_______。
(3)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是_______(填编号)。
a. 比 稳定性强
b.氮气性质很稳定,而磷较活泼,可在空气中燃烧。
c.硝酸显强氧化性,磷酸不显强氧化性
d.氮气常温是气体,磷单质是固体
(4)已知,氯胺 熔点-66℃, 熔点340℃,氯胺中所有原子最外层均满足饱
和结构,则其电子式为_______;从物质结构的角度解释两者熔点相差较大的原因
_______。
(5) 比HClO稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用
水的缓释消毒剂, 发生水解的化学方程式为_______。
(6)实验室常用排饱和食盐水的方法收集氯气,请用平衡移动原理解释用饱和食盐水而
不用水的原因:_______。
19.(2022·上海·模拟预测)下表为元素周期表的一部分。
碳 氮 Y
X 硫 Z
回答下列问题:
(1)表中元素原子半径最大的是(写元素符号)___,Y原子的电子排布式是__,Z
原子核外电子能量最高的电子亚层是___。(2)下列事实能说明Y元素的非金属性比S元素强的是___;
a.Y单质与HS溶液反应,溶液变浑浊
2
b.在氧化还原反应中,1mol Y单质比1mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(3)CCl 是一种常见的有机溶剂,写出其电子式___,判断其属于含有___(填“极
4
性”、“非极性”)共价键的____分子(填“极性”或“非极性”)。SiH 的沸点比
4
CH 高,原因是___。
4
(4)碳酸钠溶液中滴入酚酞,溶液显红色,请用离子方程式说明产生该现象的原因:
___,在上述红色的溶液中加入少许氯化钙固体,溶液颜色变浅,请用平衡理论解释产
生该现象的原因____。
20.(2022·上海普陀·统考二模)氨基磺酸( )是一种固体强酸,制备
原理:CO(NH)+HSO +SO 2HOSONH +CO,完成下列填空:
2 2 2 4 3 2 2 2
(1)O、S属同一主族,该族元素的最外层电子轨道表示式为___;CO 的电子式是___。
2
(2)反应原理中涉及的第二周期元素的非金属性由强到弱的顺序是_______。
(3)完成氨基磺酸受热分解的化学方程式_______,其中还原产物是_______。
____HOSONH SO ↑+____SO ↑+____N↑+2H↑+______HO
2 2 2 3 2 2 2
(4)用过量的NaOH(aq)充分吸收氨基磺酸热解产生的混合气体,所得吸收液中含硫微粒
浓度由大到小的顺序是_______。向吸收液中加入_______试剂,有_______现象,说明
氨基磺酸热解产生SO 。
3
(5)氨基磺酸趋向于形成内盐:HNSO H→H NSO ,可作氯水的稳定剂。HNSO 与Cl
2 3 3 3 3 3 2
经取代反应生成的一氯代物缓慢水解成HClO,写出该一氯代物水解的化学方程式
_______。
21.(2020·北京海淀·清华附中校考三模)金属镓(Ga)应用广泛,在半导体和光电材料、
合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是__________________。
(2)GaAs 是一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是___________(填字母)。
a. 碱性:Ga (OH) > Al (OH) b. 非金属性:As>Ga c. 酸性:
3 3
HAsO >H AsO
3 4 3 3
试卷第8页,共9页②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释原因_________________。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 HAsO 和 Ga3+,写出该
3 4
反应的化学方程式_________。
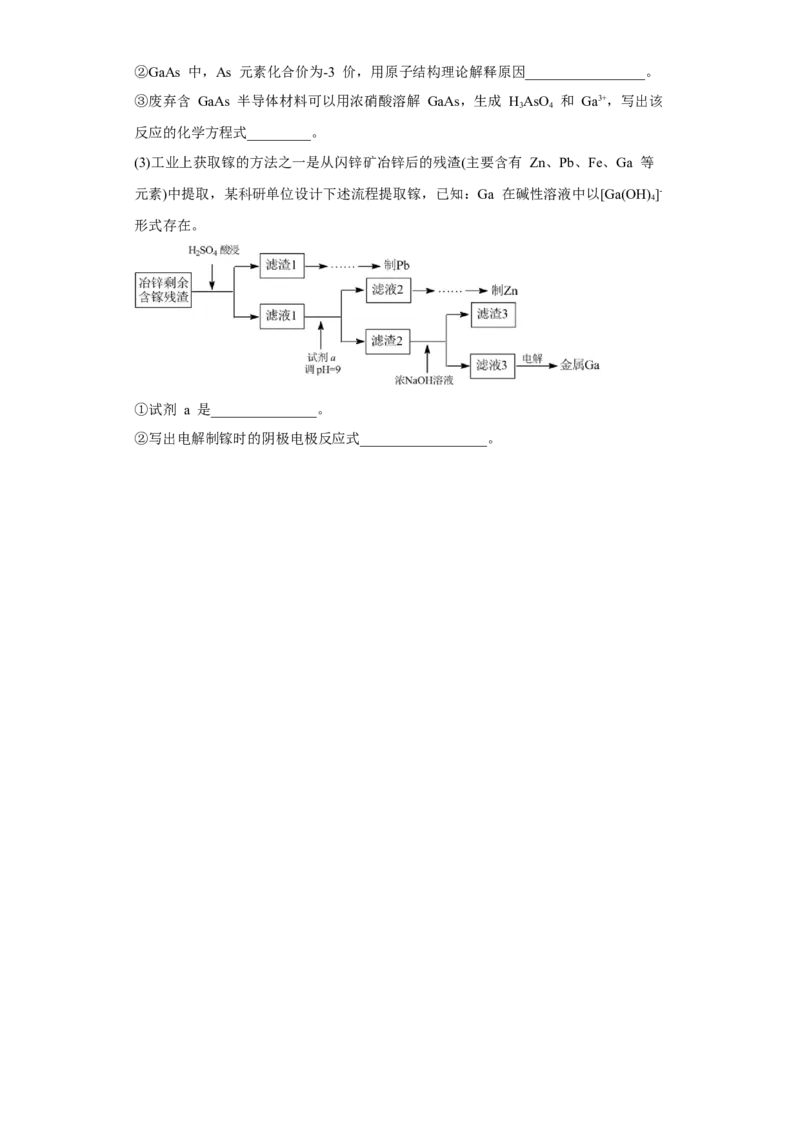
(3)工业上获取镓的方法之一是从闪锌矿冶锌后的残渣(主要含有 Zn、Pb、Fe、Ga 等
元素)中提取,某科研单位设计下述流程提取镓,已知:Ga 在碱性溶液中以[Ga(OH)]-
4
形式存在。
①试剂 a 是_______________。
②写出电解制镓时的阴极电极反应式__________________。试卷第10页,共9页