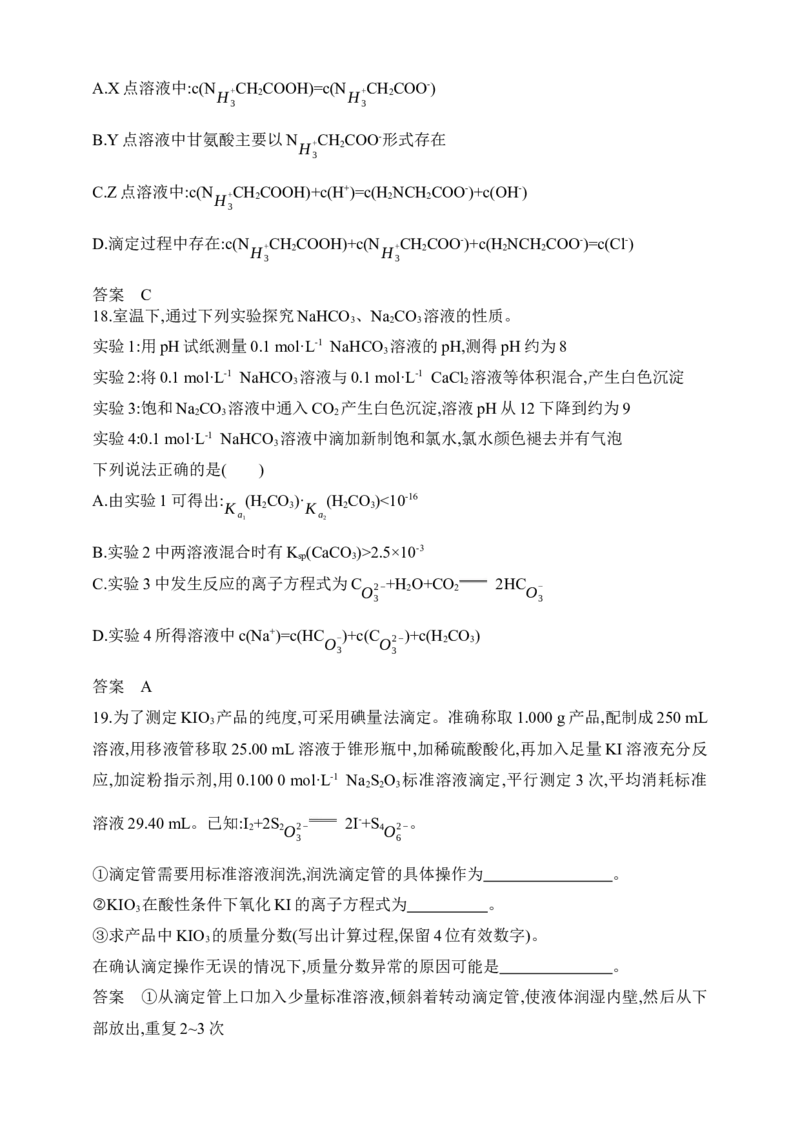文档内容
2025新教材化学高考第一轮
专题十二 弱电解质的电离平衡和溶液的酸碱性
1. NaBiO 是分析化学中的重要试剂,不溶于冷水。实验测定 NaBiO 粗产品纯度的步骤如
3 3
下:
①将一定质量的NaBiO 粗产品加入含有足量Mn2+的强酸性溶液中,充分反应后,溶液变为
3
紫红色,同时生成Bi3+;
②用一定浓度的草酸(H C O )标准溶液滴定①中反应后的溶液,通过消耗草酸标准溶液的
2 2 4
体积计算产品纯度。
下列有关说法正确的是( )
A.步骤①中用硝酸溶液提供强酸性环境
B.步骤①中反应的离子方程式为5BiO- +2Mn2++14H+ 5Bi3++2MnO- +7H O
3 4 2
C.步骤②达到滴定终点时紫红色褪去
D.步骤②中反应的还原剂和氧化产物的物质的量之比为1∶1
2. 25 ℃时,两种不同浓度(c =1.0×10-1 mol·L-1、c =1.0×10-4 mol·L-1)的弱酸 HB 溶液
1 2
中,lgc(HB)、lgc(B-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。K 为HB的电离常
a
已电离的溶质分子数
数,电离度α= ×100%,下列说法错误的是( )
原有溶质分子总数
A.d曲线表示c 溶液中B-的变化情况
2
B.当溶液的pH>-lgK 时,c 溶液中满足c(B-)>c(HB)
a 1
C.P点时c(H+)=c(B-)+c(OH-)
K
a
D.c 溶液中HB的电离度α= ×100%(忽略水的电离)
1 c(H+)+K
a
3.常温下,下列实验方案以及得出的结论均正确的是( )A.用广泛pH试纸测NaClO溶液的pH=9,证明HClO为弱酸
B.分别测NaHA溶液和NaHB溶液的pH,若NaHA溶液的pH大,则H A的酸性比H B弱
2 2
C.取等体积、等浓度的HA溶液和盐酸,均稀释相同倍数,若稀释后HA溶液的pH较大,则
HA为弱酸
D.H A 为二元弱酸,其电离平衡常数为K 、K ,用广泛 pH 试纸测 NaHA 溶液的 pH,若
2 a a
1 2
pH<7,则K >K ·K
W a a
1 2
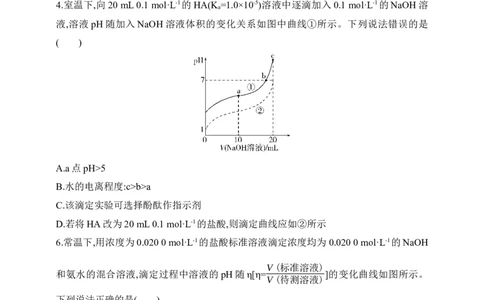
4.室温下,向20 mL 0.1 mol·L-1的HA(K =1.0×10-5)溶液中逐滴加入0.1 mol·L-1的NaOH溶
a
液,溶液pH随加入NaOH溶液体积的变化关系如图中曲线①所示。下列说法错误的是
( )
A.a点pH>5
B.水的电离程度:c>b>a
C.该滴定实验可选择酚酞作指示剂
D.若将HA改为20 mL 0.1 mol·L-1的盐酸,则滴定曲线应如②所示
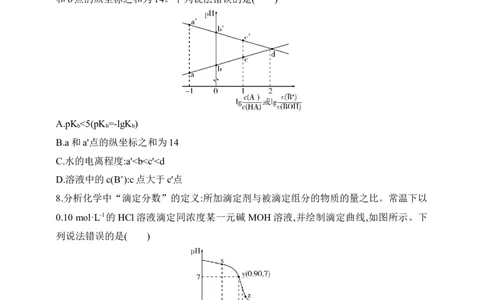
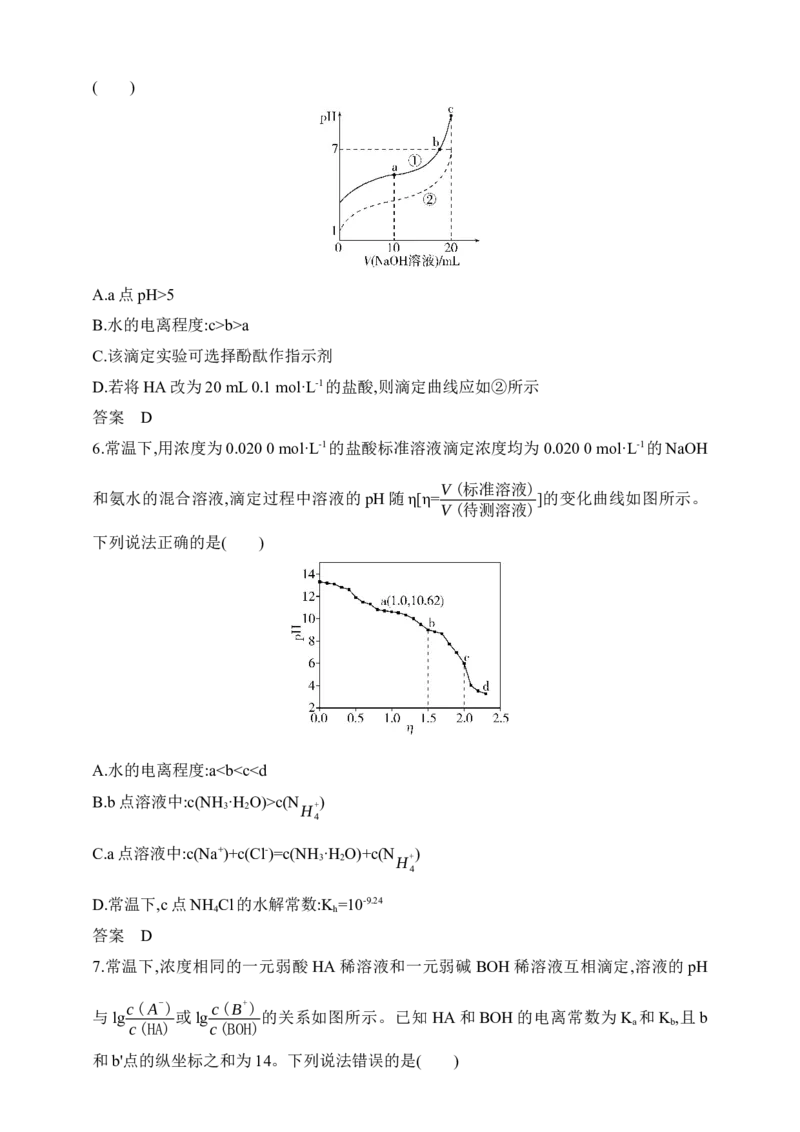
6.常温下,用浓度为0.020 0 mol·L-1的盐酸标准溶液滴定浓度均为0.020 0 mol·L-1的NaOH
V(标准溶液)
和氨水的混合溶液,滴定过程中溶液的pH随η[η= ]的变化曲线如图所示。
V(待测溶液)
下列说法正确的是( )
A.水的电离程度:ac(N )
3 2 H+
4
C.a点溶液中:c(Na+)+c(Cl-)=c(NH ·H O)+c(N )
3 2 H+
4
D.常温下,c点NH Cl的水解常数:K =10-9.24
4 h
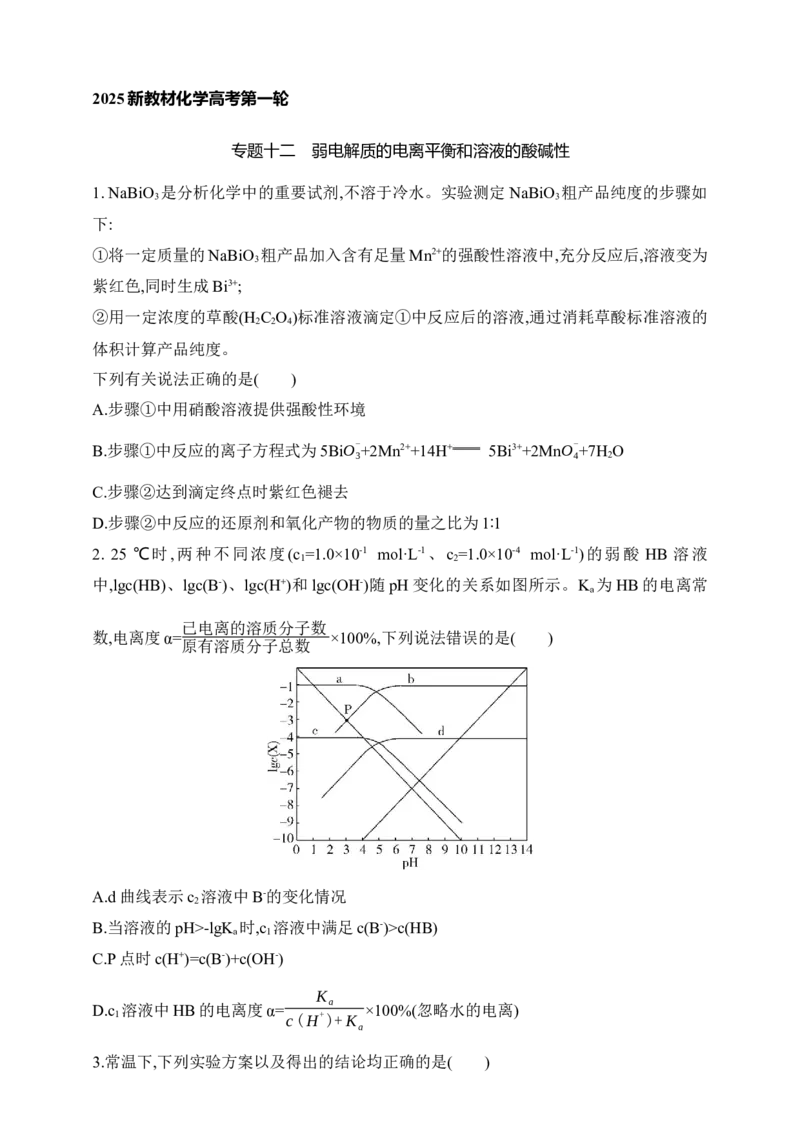
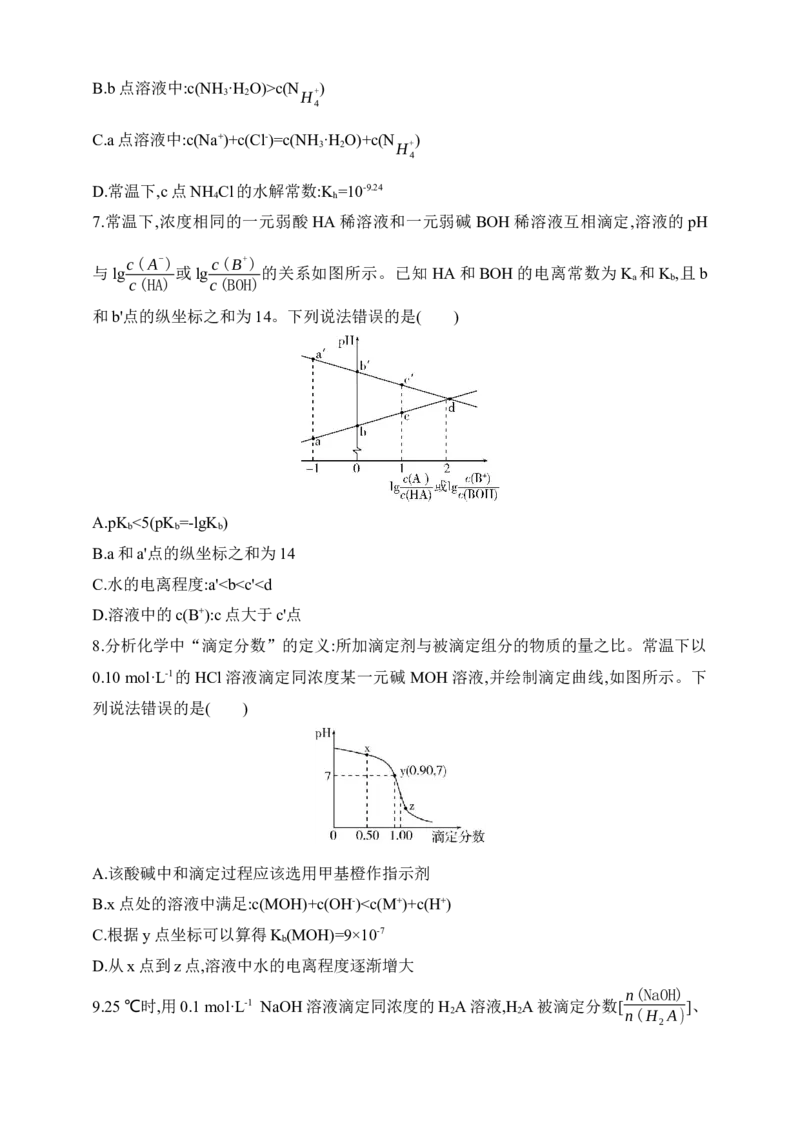
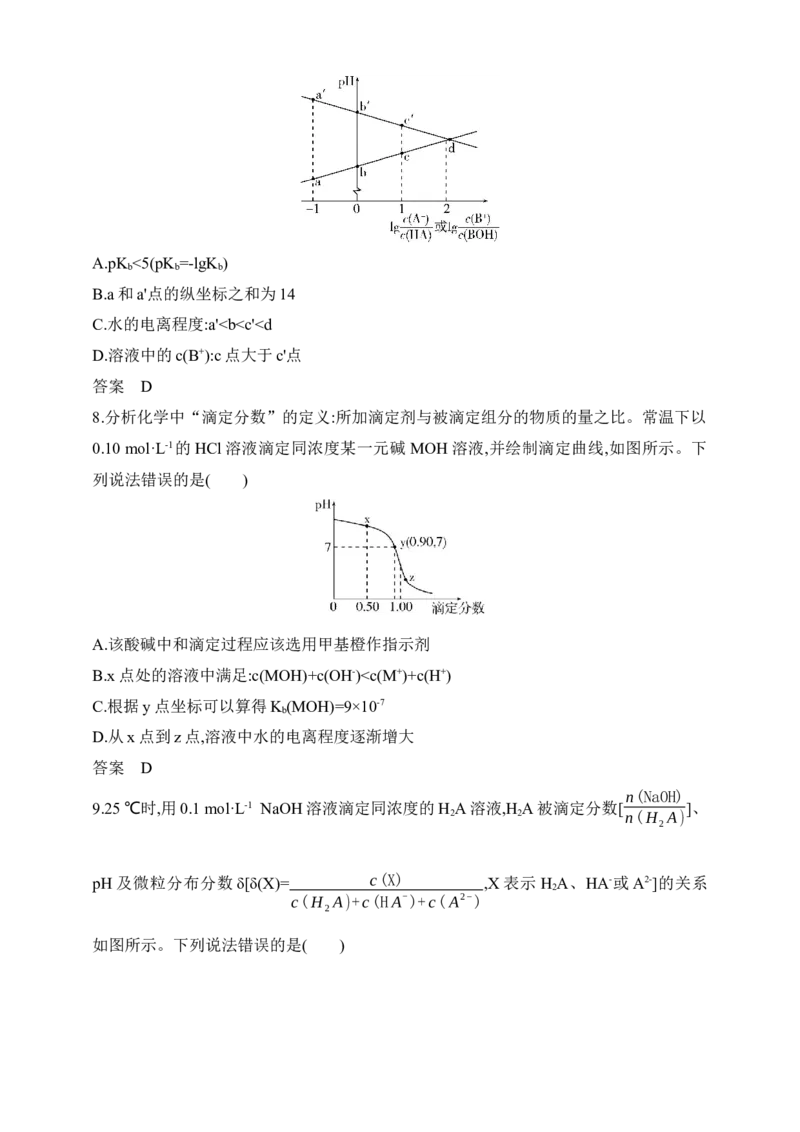
7.常温下,浓度相同的一元弱酸 HA稀溶液和一元弱碱 BOH稀溶液互相滴定,溶液的pH
c(A-) c(B+)
与lg 或lg 的关系如图所示。已知 HA和BOH的电离常数为 K 和K ,且b
c(HA) c(BOH) a b
和b'点的纵坐标之和为14。下列说法错误的是( )
A.pK <5(pK =-lgK )
b b b
B.a和a'点的纵坐标之和为14
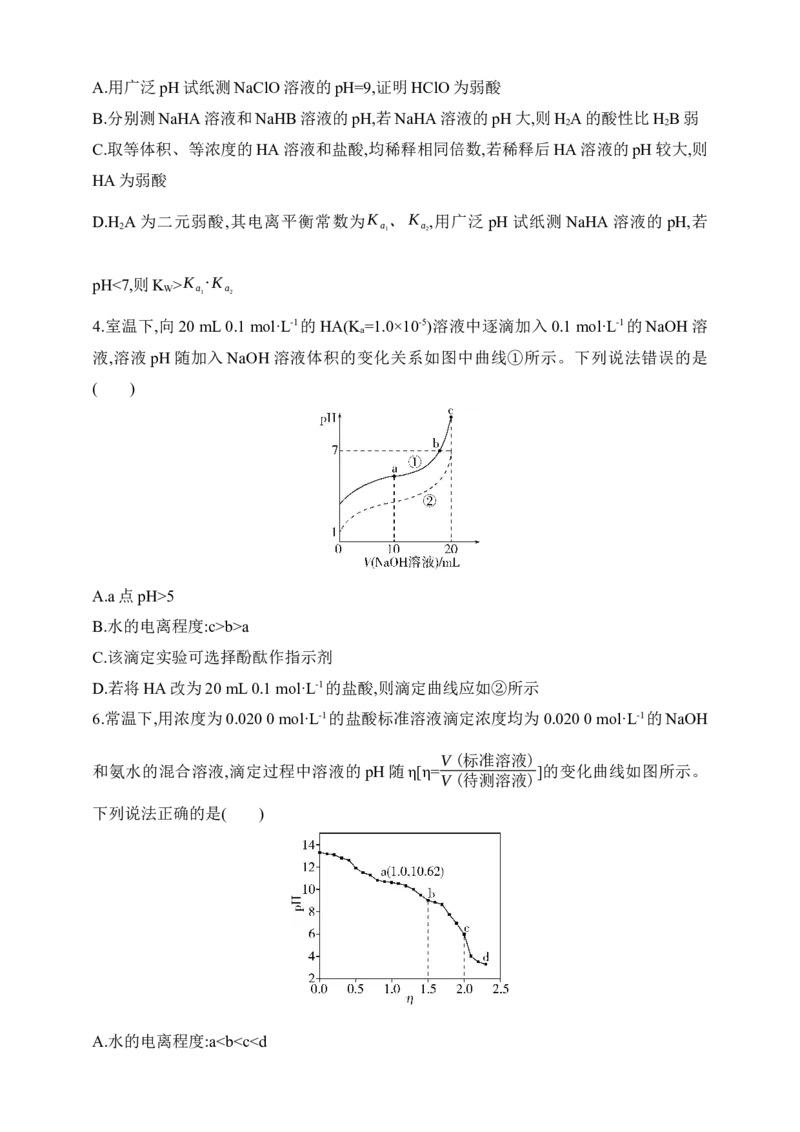
C.水的电离程度:a'c>b>a
D.用NaOH溶液滴定0.1 mol·L-1 NaHA溶液可用甲基橙作指示剂
10.25 ℃时,苯胺(C H NH )的电离平衡常数K =4×10-10。下列说法正确的是( )
6 5 2 b
A.苯胺的电离方程式为C H NH +H O C H N +OH-
6 5 2 2 6 5 H+
3
B.分别加热浓度均为0.01 mol·L-1的C H NH Cl溶液和HCl溶液,两者的pH均增大
6 5 3
C.浓度为0.01 mol·L-1的C H NH 溶液中,c(C H N )>c(OH-)>c(H+)
6 5 2 6 5 H+
3
D.等体积、等浓度的C H NH Cl溶液和C H NH 溶液混合后,溶液呈酸性
6 5 3 6 5 2
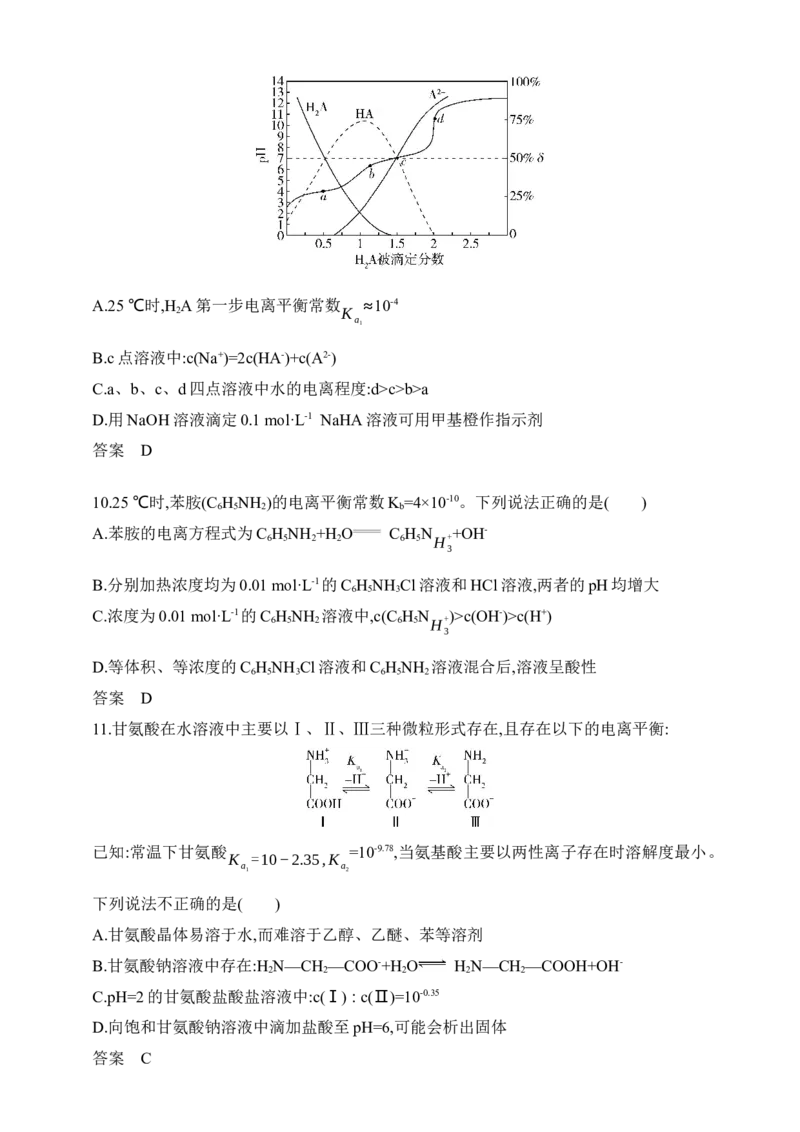
11.甘氨酸在水溶液中主要以Ⅰ、Ⅱ、Ⅲ三种微粒形式存在,且存在以下的电离平衡:
已知:常温下甘氨酸 =10-9.78,当氨基酸主要以两性离子存在时溶解度最小。
K =10−2.35,K
a a
1 2
下列说法不正确的是( )
A.甘氨酸晶体易溶于水,而难溶于乙醇、乙醚、苯等溶剂
B.甘氨酸钠溶液中存在:H N—CH —COO-+H O H N—CH —COOH+OH-
2 2 2 2 2
C.pH=2的甘氨酸盐酸盐溶液中:c(Ⅰ)∶c(Ⅱ)=10-0.35D.向饱和甘氨酸钠溶液中滴加盐酸至pH=6,可能会析出固体
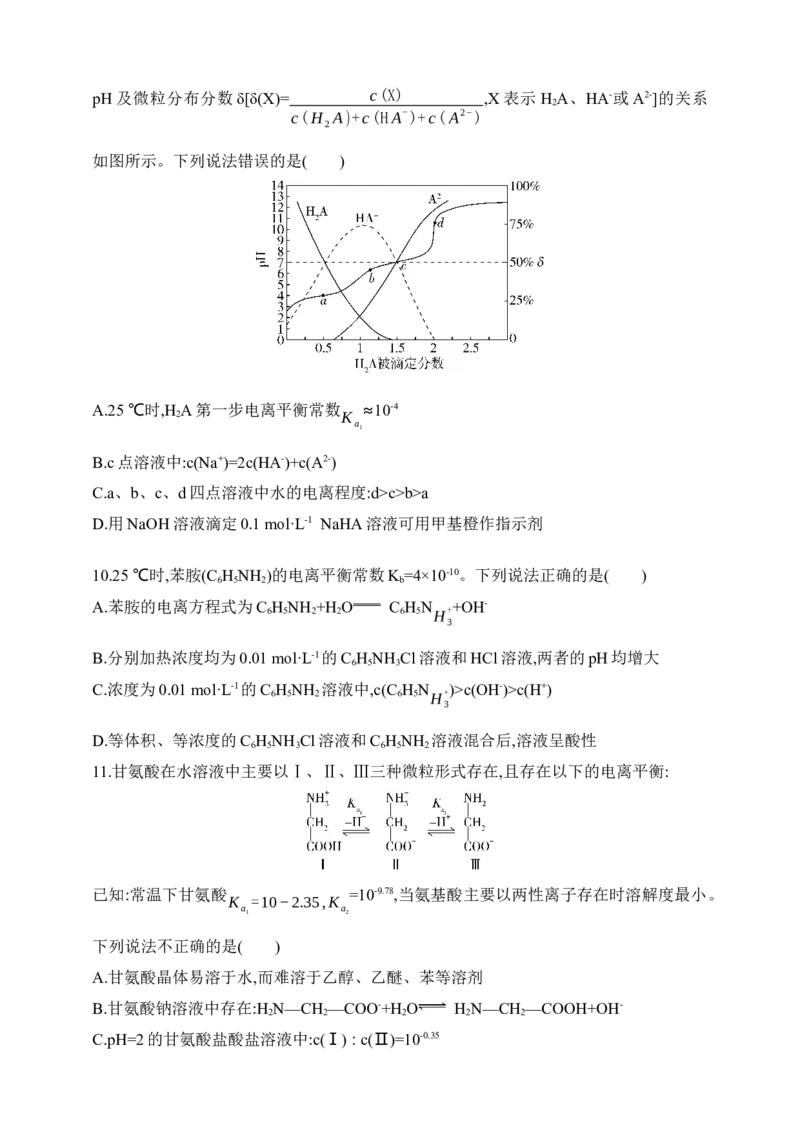
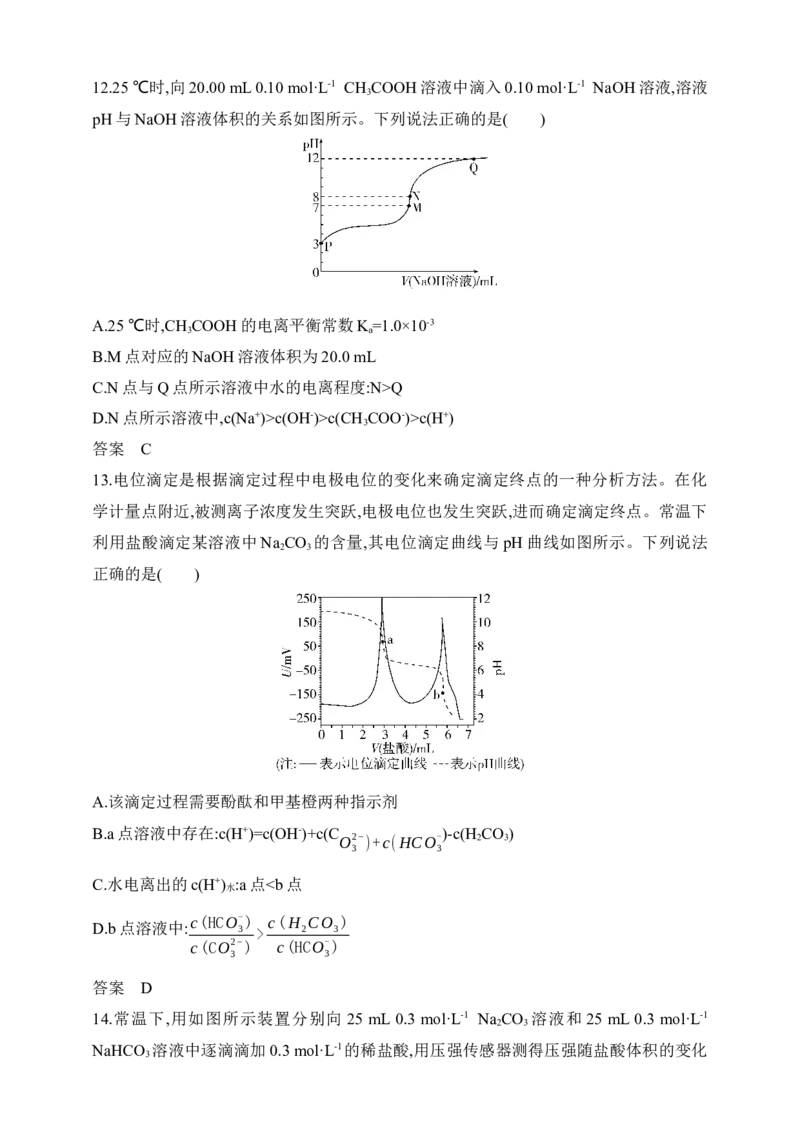
12.25 ℃时,向20.00 mL 0.10 mol·L-1 CH COOH溶液中滴入0.10 mol·L-1 NaOH溶液,溶液
3
pH与NaOH溶液体积的关系如图所示。下列说法正确的是( )
A.25 ℃时,CH COOH的电离平衡常数K =1.0×10-3
3 a
B.M点对应的NaOH溶液体积为20.0 mL
C.N点与Q点所示溶液中水的电离程度:N>Q
D.N点所示溶液中,c(Na+)>c(OH-)>c(CH COO-)>c(H+)
3
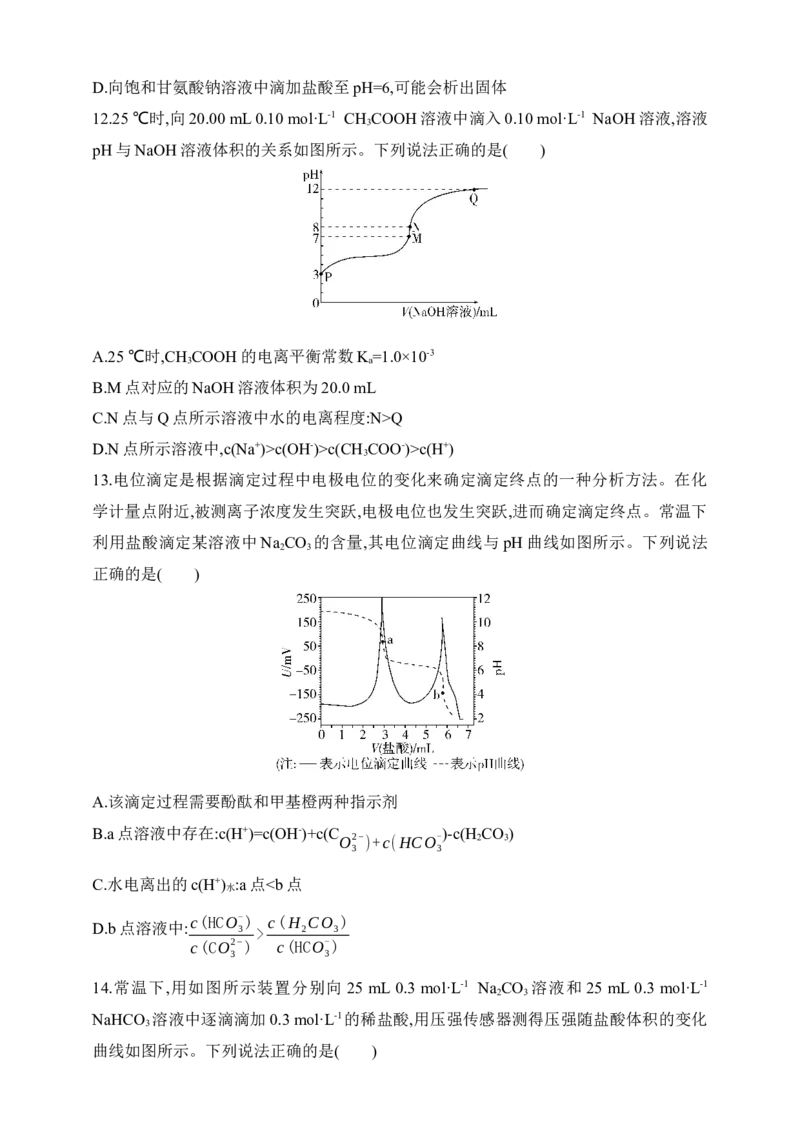
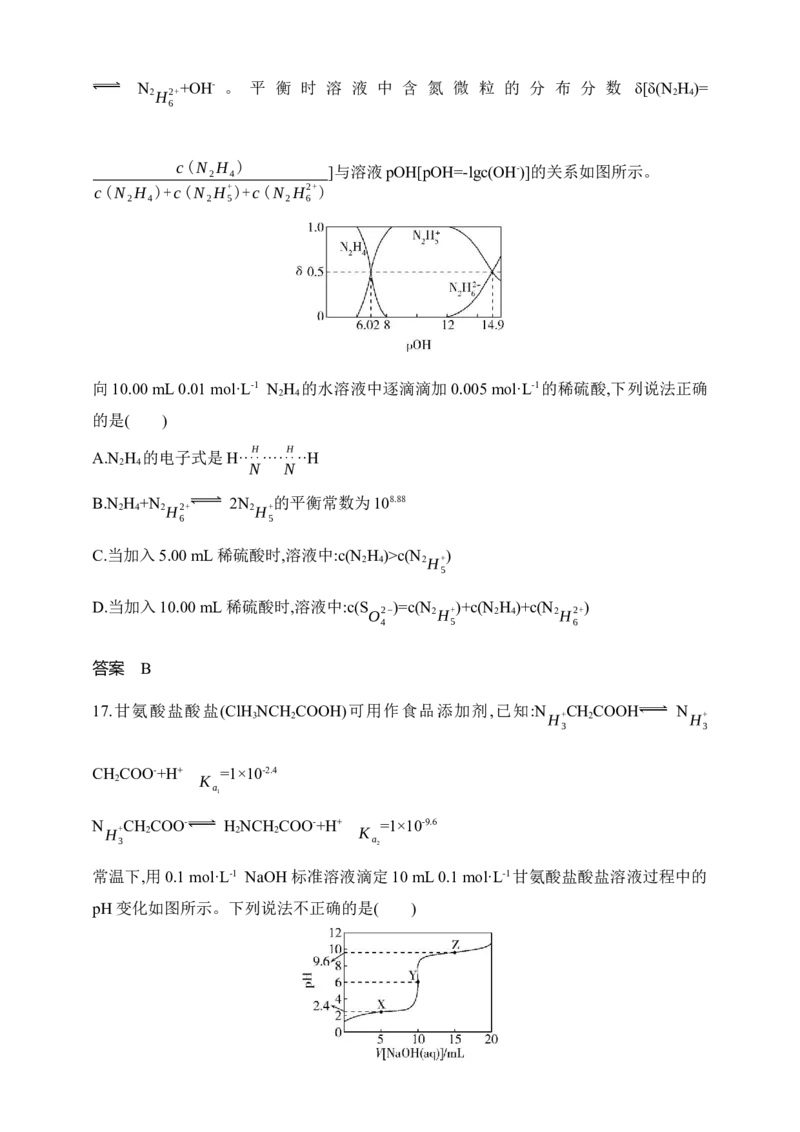
13.电位滴定是根据滴定过程中电极电位的变化来确定滴定终点的一种分析方法。在化
学计量点附近,被测离子浓度发生突跃,电极电位也发生突跃,进而确定滴定终点。常温下
利用盐酸滴定某溶液中Na CO 的含量,其电位滴定曲线与pH曲线如图所示。下列说法
2 3
正确的是( )
A.该滴定过程需要酚酞和甲基橙两种指示剂
B.a点溶液中存在:c(H+)=c(OH-)+c(C )-c(H CO )
O2− )+c(HCO- 2 3
3 3
C.水电离出的c(H+) :a点 2 3
c(CO2−) c(HCO-)
3 3
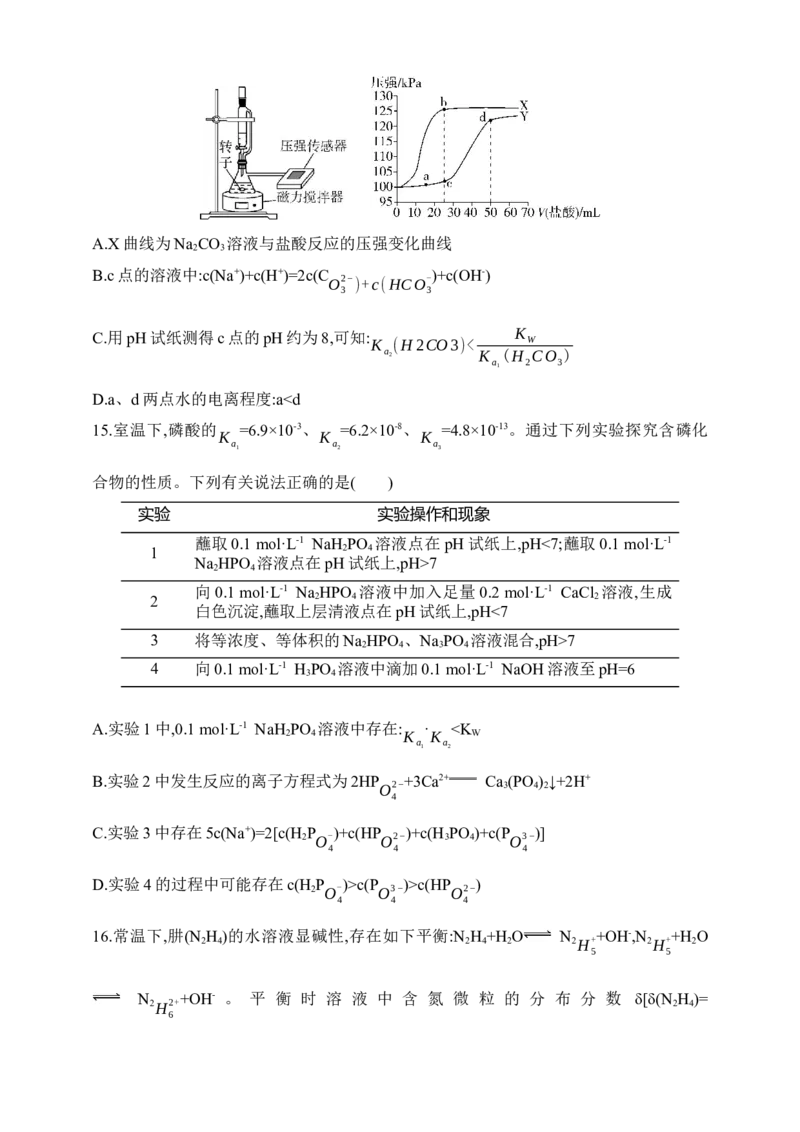
14.常温下,用如图所示装置分别向 25 mL 0.3 mol·L-1 Na CO 溶液和 25 mL 0.3 mol·L-1
2 3
NaHCO 溶液中逐滴滴加0.3 mol·L-1的稀盐酸,用压强传感器测得压强随盐酸体积的变化
3
曲线如图所示。下列说法正确的是( )A.X曲线为Na CO 溶液与盐酸反应的压强变化曲线
2 3
B.c点的溶液中:c(Na+)+c(H+)=2c(C )+c(OH-)
O2− )+c(HCO-
3 3
C.用pH试纸测得c点的pH约为8,可知: K
K (H2CO3)< W
a 2 K (H CO )
a 2 3
1
D.a、d两点水的电离程度:a7
2 4
向0.1 mol·L-1 Na HPO 溶液中加入足量0.2 mol·L-1 CaCl 溶液,生成
2 2 4 2
白色沉淀,蘸取上层清液点在pH试纸上,pH<7
3 将等浓度、等体积的Na HPO 、Na PO 溶液混合,pH>7
2 4 3 4
4 向0.1 mol·L-1 H PO 溶液中滴加0.1 mol·L-1 NaOH溶液至pH=6
3 4
A.实验1中,0.1 mol·L-1 NaH PO 溶液中存在: · c(P )>c(HP )
2 O- O3− O2−
4 4 4
16.常温下,肼(N H )的水溶液显碱性,存在如下平衡:N H +H O N +OH-,N +H O
2 4 2 4 2 2H+ 2H+ 2
5 5
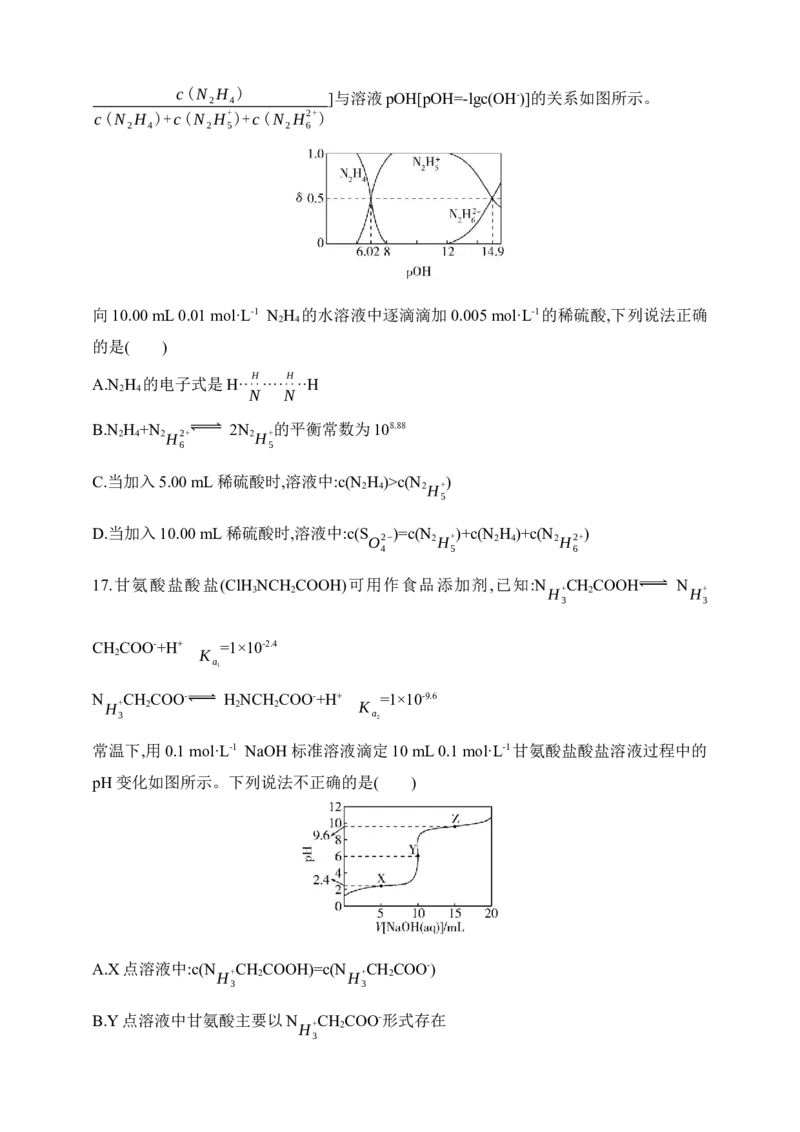
N +OH- 。 平 衡 时 溶 液 中 含 氮 微 粒 的 分 布 分 数 δ[δ(N H )=
2H2+ 2 4
6c(N H ) ]与溶液pOH[pOH=-lgc(OH-)]的关系如图所示。
2 4
c(N H )+c(N H+)+c(N H2+)
2 4 2 5 2 6
向10.00 mL 0.01 mol·L-1 N H 的水溶液中逐滴滴加0.005 mol·L-1的稀硫酸,下列说法正确
2 4
的是( )
H H
A.N
2
H
4
的电子式是H············H
N N
B.N H +N 2N 的平衡常数为108.88
2 4 2H2+ 2H+
6 5
C.当加入5.00 mL稀硫酸时,溶液中:c(N H )>c(N )
2 4 2H+
5
D.当加入10.00 mL稀硫酸时,溶液中:c(S )=c(N )+c(N H )+c(N )
O2− 2H+ 2 4 2H2+
4 5 6
17.甘氨酸盐酸盐(ClH NCH COOH)可用作食品添加剂,已知:N CH COOH N
3 2 H+ 2 H+
3 3
CH COO-+H+ =1×10-2.4
2 K
a
1
N CH COO- H NCH COO-+H+ =1×10-9.6
H+ 2 2 2 K
3 a 2
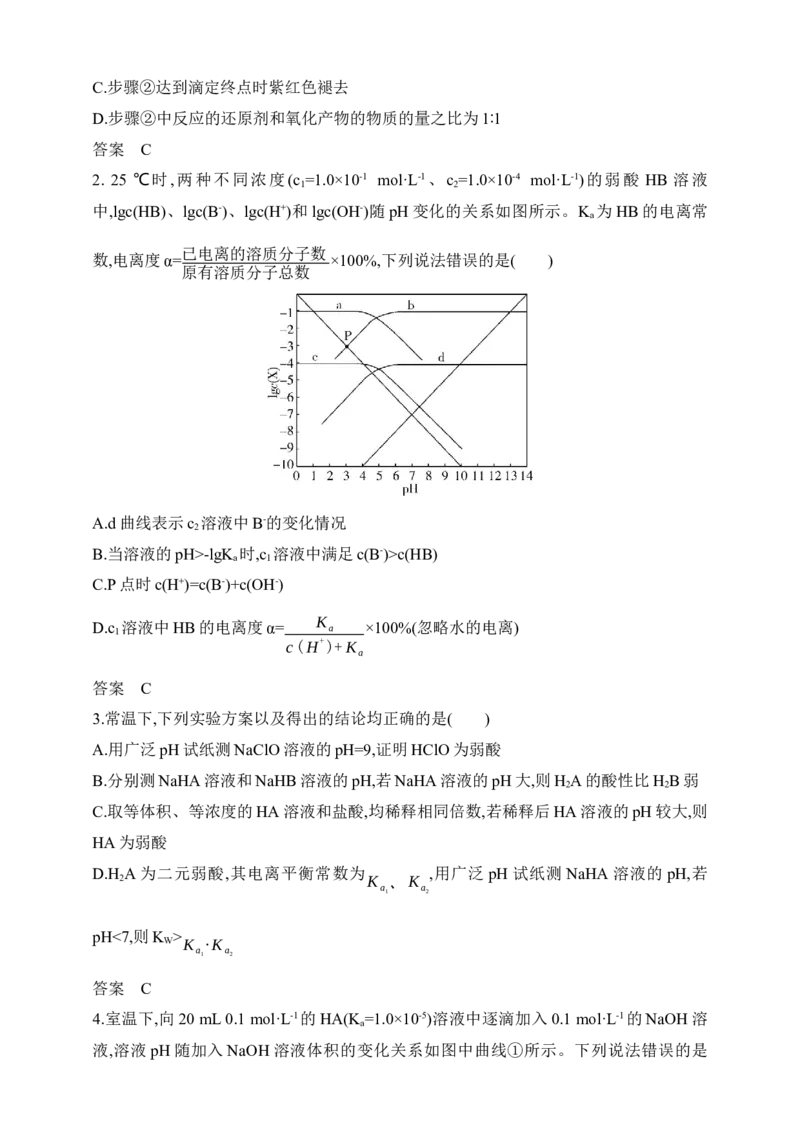
常温下,用0.1 mol·L-1 NaOH标准溶液滴定10 mL 0.1 mol·L-1甘氨酸盐酸盐溶液过程中的
pH变化如图所示。下列说法不正确的是( )
A.X点溶液中:c(N CH COOH)=c(N CH COO-)
H+ 2 H+ 2
3 3
B.Y点溶液中甘氨酸主要以N CH COO-形式存在
H+ 2
3C.Z点溶液中:c(N CH COOH)+c(H+)=c(H NCH COO-)+c(OH-)
H+ 2 2 2
3
D.滴定过程中存在:c(N CH COOH)+c(N CH COO-)+c(H NCH COO-)=c(Cl-)
H+ 2 H+ 2 2 2
3 3
18.室温下,通过下列实验探究NaHCO 、Na CO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1 mol·L-1 NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:饱和Na CO 溶液中通入CO 产生白色沉淀,溶液pH从12下降到约为9
2 3 2
实验4:0.1 mol·L-1 NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡
3
下列说法正确的是( )
A.由实验1可得出: (H CO )· (H CO )<10-16
K 2 3 K 2 3
a a
1 2
B.实验2中两溶液混合时有K (CaCO )>2.5×10-3
sp 3
C.实验3中发生反应的离子方程式为C +H O+CO 2HC
O2− 2 2 O-
3 3
D.实验4所得溶液中c(Na+)=c(HC )+c(C )+c(H CO )
O- O2− 2 3
3 3
19.为了测定KIO 产品的纯度,可采用碘量法滴定。准确称取1.000 g产品,配制成250 mL
3
溶液,用移液管移取25.00 mL溶液于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液充分反
应,加淀粉指示剂,用0.100 0 mol·L-1 Na S O 标准溶液滴定,平行测定3次,平均消耗标准
2 2 3
溶液29.40 mL。已知:I +2S 2I-+S 。
2 2O2− 4O2−
3 6
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为 。
②KIO 在酸性条件下氧化KI的离子方程式为 。
3
③求产品中KIO 的质量分数(写出计算过程,保留4位有效数字)。
3
在确认滴定操作无误的情况下,质量分数异常的原因可能是 。
20.铼(Re)是具有重要军事战略意义的金属。NH ReO 是制备高纯度Re的重要中间体。
4 4
一种测定NH ReO 纯度的方法如下:
4 4
称取w g NH ReO 样品(NH ReO 的相对分子质量为268),加适量水溶解,注入如图所示的
4 4 4 4
三颈烧瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用
V mL c mol·L-1的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用 c mol·L-1
1 1 2
NaOH标准溶液滴定过剩的HCl,达到终点时消耗V mL NaOH溶液。
2(4)根据下表,滴定操作时宜选用 (填一种指示剂名称);滴定终点的现象是
。
部分指示剂变色的 pH范围如下表:
指示剂名称 变色的pH范围 酸色 中间色 碱色
甲基橙 3.1~4.4 红 橙 黄
甲基红 4.4~6.2 红 橙 黄
溴百里酚蓝 6.0~7.6 黄 绿 蓝
酚酞 8.2~10.0 无 浅红 红
(5)样品中NH ReO 的质量分数为 (填表达式)。
4 4
专题十二 弱电解质的电离平衡和溶液的酸碱性
1. NaBiO 是分析化学中的重要试剂,不溶于冷水。实验测定 NaBiO 粗产品纯度的步骤如
3 3
下:
①将一定质量的NaBiO 粗产品加入含有足量Mn2+的强酸性溶液中,充分反应后,溶液变为
3
紫红色,同时生成Bi3+;
②用一定浓度的草酸(H C O )标准溶液滴定①中反应后的溶液,通过消耗草酸标准溶液的
2 2 4
体积计算产品纯度。
下列有关说法正确的是( )
A.步骤①中用硝酸溶液提供强酸性环境
B.步骤①中反应的离子方程式为5Bi +2Mn2++14H+ 5Bi3++2Mn +7H O
O- O- 2
3 4C.步骤②达到滴定终点时紫红色褪去
D.步骤②中反应的还原剂和氧化产物的物质的量之比为1∶1
答案 C
2. 25 ℃时,两种不同浓度(c =1.0×10-1 mol·L-1、c =1.0×10-4 mol·L-1)的弱酸 HB 溶液
1 2
中,lgc(HB)、lgc(B-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。K 为HB的电离常
a
已电离的溶质分子数
数,电离度α= ×100%,下列说法错误的是( )
原有溶质分子总数
A.d曲线表示c 溶液中B-的变化情况
2
B.当溶液的pH>-lgK 时,c 溶液中满足c(B-)>c(HB)
a 1
C.P点时c(H+)=c(B-)+c(OH-)
K
D.c 1 溶液中HB的电离度α= a ×100%(忽略水的电离)
c(H+)+K
a
答案 C
3.常温下,下列实验方案以及得出的结论均正确的是( )
A.用广泛pH试纸测NaClO溶液的pH=9,证明HClO为弱酸
B.分别测NaHA溶液和NaHB溶液的pH,若NaHA溶液的pH大,则H A的酸性比H B弱
2 2
C.取等体积、等浓度的HA溶液和盐酸,均稀释相同倍数,若稀释后HA溶液的pH较大,则
HA为弱酸
D.H A 为二元弱酸,其电离平衡常数为 ,用广泛 pH 试纸测 NaHA 溶液的 pH,若
2 K 、K
a a
1 2
pH<7,则K >
W K ·K
a a
1 2
答案 C
4.室温下,向20 mL 0.1 mol·L-1的HA(K =1.0×10-5)溶液中逐滴加入0.1 mol·L-1的NaOH溶
a
液,溶液pH随加入NaOH溶液体积的变化关系如图中曲线①所示。下列说法错误的是( )
A.a点pH>5
B.水的电离程度:c>b>a
C.该滴定实验可选择酚酞作指示剂
D.若将HA改为20 mL 0.1 mol·L-1的盐酸,则滴定曲线应如②所示
答案 D
6.常温下,用浓度为0.020 0 mol·L-1的盐酸标准溶液滴定浓度均为0.020 0 mol·L-1的NaOH
V(标准溶液)
和氨水的混合溶液,滴定过程中溶液的pH随η[η= ]的变化曲线如图所示。
V(待测溶液)
下列说法正确的是( )
A.水的电离程度:ac(N )
3 2 H+
4
C.a点溶液中:c(Na+)+c(Cl-)=c(NH ·H O)+c(N )
3 2 H+
4
D.常温下,c点NH Cl的水解常数:K =10-9.24
4 h
答案 D
7.常温下,浓度相同的一元弱酸 HA稀溶液和一元弱碱 BOH稀溶液互相滴定,溶液的pH
c(A-) c(B+)
与lg 或lg 的关系如图所示。已知 HA和BOH的电离常数为 K 和K ,且b
c(HA) c(BOH) a b
和b'点的纵坐标之和为14。下列说法错误的是( )A.pK <5(pK =-lgK )
b b b
B.a和a'点的纵坐标之和为14
C.水的电离程度:a'c>b>a
D.用NaOH溶液滴定0.1 mol·L-1 NaHA溶液可用甲基橙作指示剂
答案 D
10.25 ℃时,苯胺(C H NH )的电离平衡常数K =4×10-10。下列说法正确的是( )
6 5 2 b
A.苯胺的电离方程式为C H NH +H O C H N +OH-
6 5 2 2 6 5 H+
3
B.分别加热浓度均为0.01 mol·L-1的C H NH Cl溶液和HCl溶液,两者的pH均增大
6 5 3
C.浓度为0.01 mol·L-1的C H NH 溶液中,c(C H N )>c(OH-)>c(H+)
6 5 2 6 5 H+
3
D.等体积、等浓度的C H NH Cl溶液和C H NH 溶液混合后,溶液呈酸性
6 5 3 6 5 2
答案 D
11.甘氨酸在水溶液中主要以Ⅰ、Ⅱ、Ⅲ三种微粒形式存在,且存在以下的电离平衡:
已知:常温下甘氨酸 =10-9.78,当氨基酸主要以两性离子存在时溶解度最小。
K =10−2.35,K
a a
1 2
下列说法不正确的是( )
A.甘氨酸晶体易溶于水,而难溶于乙醇、乙醚、苯等溶剂
B.甘氨酸钠溶液中存在:H N—CH —COO-+H O H N—CH —COOH+OH-
2 2 2 2 2
C.pH=2的甘氨酸盐酸盐溶液中:c(Ⅰ)∶c(Ⅱ)=10-0.35
D.向饱和甘氨酸钠溶液中滴加盐酸至pH=6,可能会析出固体
答案 C12.25 ℃时,向20.00 mL 0.10 mol·L-1 CH COOH溶液中滴入0.10 mol·L-1 NaOH溶液,溶液
3
pH与NaOH溶液体积的关系如图所示。下列说法正确的是( )
A.25 ℃时,CH COOH的电离平衡常数K =1.0×10-3
3 a
B.M点对应的NaOH溶液体积为20.0 mL
C.N点与Q点所示溶液中水的电离程度:N>Q
D.N点所示溶液中,c(Na+)>c(OH-)>c(CH COO-)>c(H+)
3
答案 C
13.电位滴定是根据滴定过程中电极电位的变化来确定滴定终点的一种分析方法。在化
学计量点附近,被测离子浓度发生突跃,电极电位也发生突跃,进而确定滴定终点。常温下
利用盐酸滴定某溶液中Na CO 的含量,其电位滴定曲线与pH曲线如图所示。下列说法
2 3
正确的是( )
A.该滴定过程需要酚酞和甲基橙两种指示剂
B.a点溶液中存在:c(H+)=c(OH-)+c(C )-c(H CO )
O2− )+c(HCO- 2 3
3 3
C.水电离出的c(H+) :a点 2 3
c(CO2−) c(HCO-)
3 3
答案 D
14.常温下,用如图所示装置分别向 25 mL 0.3 mol·L-1 Na CO 溶液和 25 mL 0.3 mol·L-1
2 3
NaHCO 溶液中逐滴滴加0.3 mol·L-1的稀盐酸,用压强传感器测得压强随盐酸体积的变化
3曲线如图所示。下列说法正确的是( )
A.X曲线为Na CO 溶液与盐酸反应的压强变化曲线
2 3
B.c点的溶液中:c(Na+)+c(H+)=2c(C )+c(OH-)
O2− )+c(HCO-
3 3
C.用pH试纸测得c点的pH约为8,可知: K
K (H2CO3)< W
a 2 K (H CO )
a 2 3
1
D.a、d两点水的电离程度:a7
2 4
向0.1 mol·L-1 Na HPO 溶液中加入足量0.2 mol·L-1 CaCl 溶液,生成
2 2 4 2
白色沉淀,蘸取上层清液点在pH试纸上,pH<7
3 将等浓度、等体积的Na HPO 、Na PO 溶液混合,pH>7
2 4 3 4
4 向0.1 mol·L-1 H PO 溶液中滴加0.1 mol·L-1 NaOH溶液至pH=6
3 4
A.实验1中,0.1 mol·L-1 NaH PO 溶液中存在: · c(P )>c(HP )
2 O- O3− O2−
4 4 4
答案 B
16.常温下,肼(N H )的水溶液显碱性,存在如下平衡:N H +H O N +OH-,N +H O
2 4 2 4 2 2H+ 2H+ 2
5 5N +OH- 。 平 衡 时 溶 液 中 含 氮 微 粒 的 分 布 分 数 δ[δ(N H )=
2H2+ 2 4
6
c(N H ) ]与溶液pOH[pOH=-lgc(OH-)]的关系如图所示。
2 4
c(N H )+c(N H+)+c(N H2+)
2 4 2 5 2 6
向10.00 mL 0.01 mol·L-1 N H 的水溶液中逐滴滴加0.005 mol·L-1的稀硫酸,下列说法正确
2 4
的是( )
H H
A.N
2
H
4
的电子式是H············H
N N
B.N H +N 2N 的平衡常数为108.88
2 4 2H2+ 2H+
6 5
C.当加入5.00 mL稀硫酸时,溶液中:c(N H )>c(N )
2 4 2H+
5
D.当加入10.00 mL稀硫酸时,溶液中:c(S )=c(N )+c(N H )+c(N )
O2− 2H+ 2 4 2H2+
4 5 6
答案 B
17.甘氨酸盐酸盐(ClH NCH COOH)可用作食品添加剂,已知:N CH COOH N
3 2 H+ 2 H+
3 3
CH COO-+H+ =1×10-2.4
2 K
a
1
N CH COO- H NCH COO-+H+ =1×10-9.6
H+ 2 2 2 K
3 a 2
常温下,用0.1 mol·L-1 NaOH标准溶液滴定10 mL 0.1 mol·L-1甘氨酸盐酸盐溶液过程中的
pH变化如图所示。下列说法不正确的是( )A.X点溶液中:c(N CH COOH)=c(N CH COO-)
H+ 2 H+ 2
3 3
B.Y点溶液中甘氨酸主要以N CH COO-形式存在
H+ 2
3
C.Z点溶液中:c(N CH COOH)+c(H+)=c(H NCH COO-)+c(OH-)
H+ 2 2 2
3
D.滴定过程中存在:c(N CH COOH)+c(N CH COO-)+c(H NCH COO-)=c(Cl-)
H+ 2 H+ 2 2 2
3 3
答案 C
18.室温下,通过下列实验探究NaHCO 、Na CO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1 mol·L-1 NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:饱和Na CO 溶液中通入CO 产生白色沉淀,溶液pH从12下降到约为9
2 3 2
实验4:0.1 mol·L-1 NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡
3
下列说法正确的是( )
A.由实验1可得出: (H CO )· (H CO )<10-16
K 2 3 K 2 3
a a
1 2
B.实验2中两溶液混合时有K (CaCO )>2.5×10-3
sp 3
C.实验3中发生反应的离子方程式为C +H O+CO 2HC
O2− 2 2 O-
3 3
D.实验4所得溶液中c(Na+)=c(HC )+c(C )+c(H CO )
O- O2− 2 3
3 3
答案 A
19.为了测定KIO 产品的纯度,可采用碘量法滴定。准确称取1.000 g产品,配制成250 mL
3
溶液,用移液管移取25.00 mL溶液于锥形瓶中,加稀硫酸酸化,再加入足量KI溶液充分反
应,加淀粉指示剂,用0.100 0 mol·L-1 Na S O 标准溶液滴定,平行测定3次,平均消耗标准
2 2 3
溶液29.40 mL。已知:I +2S 2I-+S 。
2 2O2− 4O2−
3 6
①滴定管需要用标准溶液润洗,润洗滴定管的具体操作为 。
②KIO 在酸性条件下氧化KI的离子方程式为 。
3
③求产品中KIO 的质量分数(写出计算过程,保留4位有效数字)。
3
在确认滴定操作无误的情况下,质量分数异常的原因可能是 。
答案 ①从滴定管上口加入少量标准溶液,倾斜着转动滴定管,使液体润湿内壁,然后从下
部放出,重复2~3次②I +5I-+6H+ 3I +3H O
O- 2 2
3
③KIO ~3I ~6S
3 2 2O2−
3
1
n(KIO )= ×0.100 0 mol·L-1×29.40×10-3 L=4.900×10-4 mol
3
6
250mL
m(KIO ) 4.900×10-4mol×214g·mol-1×
产 品 中 KIO 的 质 量 分 数 = 3 ×100%= 25.00mL
3
m(样品)
1.000g
×100%=104.9% 滴定摇动锥形瓶时,过量I-被空气氧化成I (或含有KClO 杂质)
2 3
20.铼(Re)是具有重要军事战略意义的金属。NH ReO 是制备高纯度Re的重要中间体。
4 4
一种测定NH ReO 纯度的方法如下:
4 4
称取w g NH ReO 样品(NH ReO 的相对分子质量为268),加适量水溶解,注入如图所示的
4 4 4 4
三颈烧瓶中,然后逐滴加入足量10% NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用
V mL c mol·L-1的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用 c mol·L-1
1 1 2
NaOH标准溶液滴定过剩的HCl,达到终点时消耗V mL NaOH溶液。
2
(4)根据下表,滴定操作时宜选用 (填一种指示剂名称);滴定终点的现象是
。
部分指示剂变色的 pH范围如下表:
指示剂名称 变色的pH范围 酸色 中间色 碱色
甲基橙 3.1~4.4 红 橙 黄
甲基红 4.4~6.2 红 橙 黄
溴百里酚蓝 6.0~7.6 黄 绿 蓝
酚酞 8.2~10.0 无 浅红 红
(5)样品中NH ReO 的质量分数为 (填表达式)。
4 4
答案 (4)甲基红 滴入最后半滴NaOH溶液,溶液由红色恰好变为橙色,且30 s内不变色
(5)[268×(c V -c V )×10-3/w]×100%
1 1 2 2