文档内容
专题十四 物质结构和性质(选修)
必备知识 解读
1
必备知识 原子结构和性质
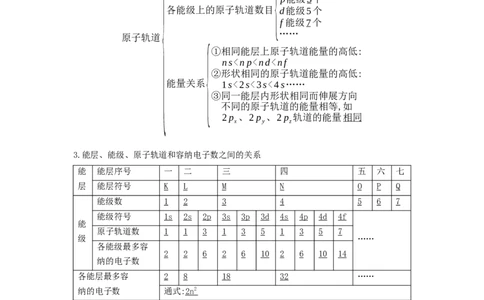
一.能层、能级
1.能层(n):在多电子原子中,核外电子的能量是不同的,按照电子的能量差异将其分成不同
能层,即电子层。通常用 K 、 L 、 M 、 N……表示,能量依次升高。
2.能级:在多电子原子中,同一能层里的电子,能量也可能不同,又将其分成不同的能级,通常
用s、p、d、f 等表示,同一能层里,各能级的能量按 s 、 p 、 d 、 f 的顺序依次升高,
即:E(s)氢键>范德华力
度
影
响
①随着分子极性和相对分子
其 质量的增大而增大 对于 成键原子半径越
强 A—H…B—,A、B的电负性越 小,键长越短,键
度 ②组成和结构相似的物质,相 大,B原子的半径越小,氢键键能 能越大,共价键越
的 对分子质量越大,范德华力越 越大 稳定
大
因
素
对
物 ①影响分子的稳
①影响物质的熔沸点、溶解 ①分子间氢键的存在,使物质的
定性,共价键键能
质 度等物理性质 熔、沸点升高,在水中的溶解度
越大,分子稳定性
性 增大,如熔、沸
②组成和结构相似的物质,随 越强
点:HO>HS,HF>HCl,NH>PH
质 相对分子质量的增大,物质的 2 2 3 3
②对于原子晶体,
的 熔、沸点升高,如 ②分子内氢键使物质的熔、沸
共价键键能越大,
FO>C>B
1 3 3
(4)( , , )
4 4 4
1081021
(5) 正四面体形 8 N a3
A
【解析】(1)铝元素的原子序数为13,基态原子的电子排布式为1s22s22p63s23p1,则原子中
球形的s能级与哑铃形的p能级上电子数之比为6∶7,故答案为:6∶7;
(2)①由方程式可知,制氢反应的化合物中硼、碳、氮、氧四种原子的价层电子对数都为
4,杂化方式均为sp3杂化,故答案为:4;
H NBH
②氨分子中氮原子含有1对孤对电子, 3 3中氨分子的孤对电子与硼原子形成配位键,
H NBH
孤电子对对成键电子对的排斥力大,所以氨分子中键角∠HNH小于 3 3中键角
∠HNH,故答案为:小于;③同周期元素,从左到右原子半径依次减小,得电子能力依次增强,元素的非金属性依次
增强,元素的电负性依次增大,则硼、碳、氮、氧四种元素的电负性依次增大,故答案为:
原子半径依次减小,得电子能力依次增强;
④由电负性的大小可知,氢元素的电负性大于硼元素,则在氨硼烷中,H—B键中共用电子
对偏向氢原子,氢原子带部分负电荷,故答案为:负;
(3)有机物分子中单键为σ键,双键中含有1个σ键和1个π键,由有机硼化合物的结构简
式可知,1mol有机物中含有42molσ键;同周期元素,从左到右第一电离能呈增大趋势,
氮原子的2p轨道为稳定的半充满结构,第一电离能大于相邻元素,则硼、碳、氮、氧四种
元素的第一电离能由大到小的顺序为N>O>C>B,故答案为:42;N>O>C>B;
(4)由位于顶点a点磷原子的坐标为(0,0,0)、顶点b点磷原子的坐标为(1,1,0)可知,晶
1 1 3 3 1
胞的边长为1,则位于体对角线 处的c点硼原子的坐标为( , , ),故答案为:( ,
4 4 4 4 4
3 3
, );
4 4
(5)①四氢合铝酸根离子中铝原子的价层电子对数为4、孤对电子对数为0,则离子的空间构
型为正四面体形;由晶胞结构可知,位于体心的四氢合铝酸根离子与位于棱上和面心的钠
离子距离最近,则四氢合铝酸根离子的配位数为8,故答案为:正四面体形,8;
1
1
②由晶胞结构可知,位于体心、顶点和面上的四氢合铝酸根离子的个数为1+8× +4×
8 2
1
=4,位于棱上、面上的钠离子个数为4× +6× 1 =4,设晶体的密度为dg/cm3,由晶胞的质
4 2
454 1081021 1081021
量公式可得: N =(a×10—7)2×2a×10—7×d,解得d= N a3 ,故答案为: N a3 。
A A A
【高考实例二】
2.(2022·全国乙卷)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答
下列问题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. b. c. d.
(2)①一氯乙烯 分子中,C的一个_______杂化轨道与Cl的 轨道形成_______键,并且Cl的 轨道与C的 轨道形成3中心4电子的大 键 。
②一氯乙烷 、一氯乙烯 、一氯乙炔 分子中, 键长的顺序是
_______,理由:(ⅰ)C的杂化轨道中s成分越多,形成的 键越强:(ⅱ)_______。
(3)卤化物 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。
解释X的熔点比Y高的原因_______。
(4) 晶体中 离子作体心立方堆积(如图所示), 主要分布在由 构成的四面体、八
面体等空隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此,
晶体在电池中可作为_______。
已知阿伏加德罗常数为 ,则 晶体的摩尔体积 _______ (列出算式)。
【答案】(1) ad d
(2) sp2 σ 一氯乙烷>一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的
C-Cl键的键长越短
(3) CsCl CsCl为离子晶体,ICl为分子晶体
(4) 电解质
【解析】(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5,
a.1s22s22p43s1,基态氟原子2p能级上的1个电子跃迁到3s能级上,属于氟原子的激发态,
a正确;
b.1s22s22p43d2,核外共10个电子,不是氟原子,b错误;
c.1s22s12p5,核外共8个电子,不是氟原子,c错误;d.1s22s22p33p2,基态氟原子2p能级上的2个电子跃迁到3p能级上,属于氟原子的激发态,
d正确;
答案选ad;
而同一原子3p能级的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,答案选
d。
(2)①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个sp2
杂化轨道与Cl的3p 轨道形成C-Clσ键。
x
②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取
sp3杂化,一氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化时p成分少,sp3
杂化时p成分多,因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,同
时Cl参与形成的大π键越多,形成的C-Cl键的键长越短,一氯乙烯中Cl的3p 轨道与C的
x
2p 轨道形成3中心4电子的大π键( ),一氯乙炔中Cl的3p 轨道与C的2p 轨道形成2
x x x
套3中心4电子的大π键( ),因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>
一氯乙炔。
(3)CsICl 发生非氧化还原反应,各元素化合价不变,生成无色晶体和红棕色液体,则无色晶
2
体为CsCl,红棕色液体为ICl,而CsCl为离子晶体,熔化时,克服的是离子键,ICl为分子晶
体,熔化时,克服的是分子间作用力,因此CsCl的熔点比ICl高。
(4)由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是
优良的离子导体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8 +1=2个,依
据化学式AgI可知,银离子个数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504 10-12)3m3,则α-AgI晶体的摩尔体积V = = =
m
m3/mol。
【实战演练】
1.(2022·陕西汉中·二模)主族元素N、F、Si、As、Se、Cl等的某些化合物对工农业生产
意义重大,回答下列问题:
(1)Si N 陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
3 4
_______晶体;SiCl 中Si采取的杂化类型为_______。
4
(2)O、F、Cl电负性由大到小的顺序为_______;OF 分子的空间构型为_______;OF 的熔、
2 2
沸点低于Cl O,原因是_______。
2
(3)Se元素基态原子的原子核外电子排布式为_______;As的第一电离能比Se的第一电离能
大的原因为_______。
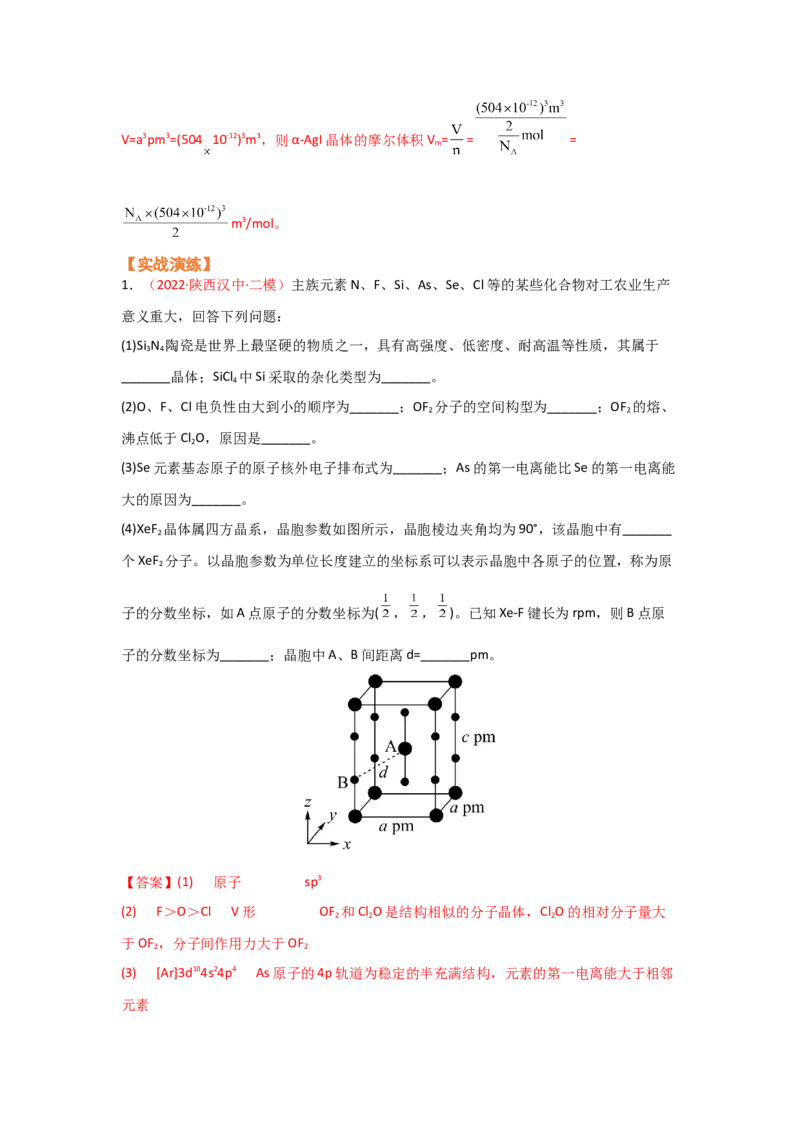
(4)XeF 晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有_______
2
个XeF 分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原
2
子的分数坐标,如A点原子的分数坐标为( , , )。已知Xe-F键长为rpm,则B点原
子的分数坐标为_______;晶胞中A、B间距离d=_______pm。
【答案】(1) 原子 sp3
(2) F>O>Cl V形 OF 和Cl O是结构相似的分子晶体,Cl O的相对分子量大
2 2 2
于OF ,分子间作用力大于OF
2 2
(3) [Ar]3d104s24p4 As原子的4p轨道为稳定的半充满结构,元素的第一电离能大于相邻
元素(4) 2 (0,0, )
【解析】(1)由物理性质可知,四氮化三硅为熔沸点高、硬度大的原子晶体;四氯化硅中硅
原子的价层电子对数为4,硅原子的杂化方式为sp3杂化,故答案为:原子;sp3;
(2)元素的非金属性越强,电负性越大,氟、氧、氯三种元素的非金属性强弱顺序为F>O>
Cl,则电负性的大小顺序为F>O>Cl;OF 分子中氧原子的价层电子对数为4,孤对电子对
2
数为2,则分子的空间构型为V形;结构相似的分子晶体,相对分子量越大,分子间作用
力越大,熔沸点越高,OF 和Cl O是结构相似的分子晶体,Cl O的相对分子量大于OF ,分
2 2 2 2
子间作用力大于OF ,所以OF 的熔、沸点低于Cl O,故答案为:F>O>Cl;V形;OF 和
2 2 2 2
Cl O是结构相似的分子晶体,Cl O的相对分子量大于OF ,分子间作用力大于OF ;
2 2 2 2
(3)硒元素的原子序数为34,位于元素周期表第四周期ⅥA族,基态原子的原子核外电子排
布式为[Ar]3d104s24p4;砷原子的4p轨道为稳定的半充满结构,元素的第一电离能大于相邻
元素,所以砷的第一电离能比硒的第一电离能大,故答案为:[Ar]3d104s24p4;As原子的4p
轨道为稳定的半充满结构,元素的第一电离能大于相邻元素;
(4)由晶胞结构可知,晶胞中原子半径大的氙原子位于顶点和体心,原子个数为8× +1=2,
原子半径小的氟原子位于棱上和体内,原子个数为原子半径小的氟原子位于棱上和体内,
原子个数为8× +2=4,所以晶胞中有2个XeF 分子;由晶胞中体心A点原子的分数坐标为(
2
, , )可知,晶胞的边长为1,则位于棱的 处B点原子的分数坐标为(0,0, );由
晶胞结构可得如下示意图: ,图中y为面对角线的 ,则y为 ,x
为( —r),则A、B间距离d为 ,故答案为:2;(0,0, ); 。2.(2022·湖南卷)铁和硒( )都是人体所必需的微量元素,且在医药、催化、材料等领
域有广泛应用,回答下列问题:
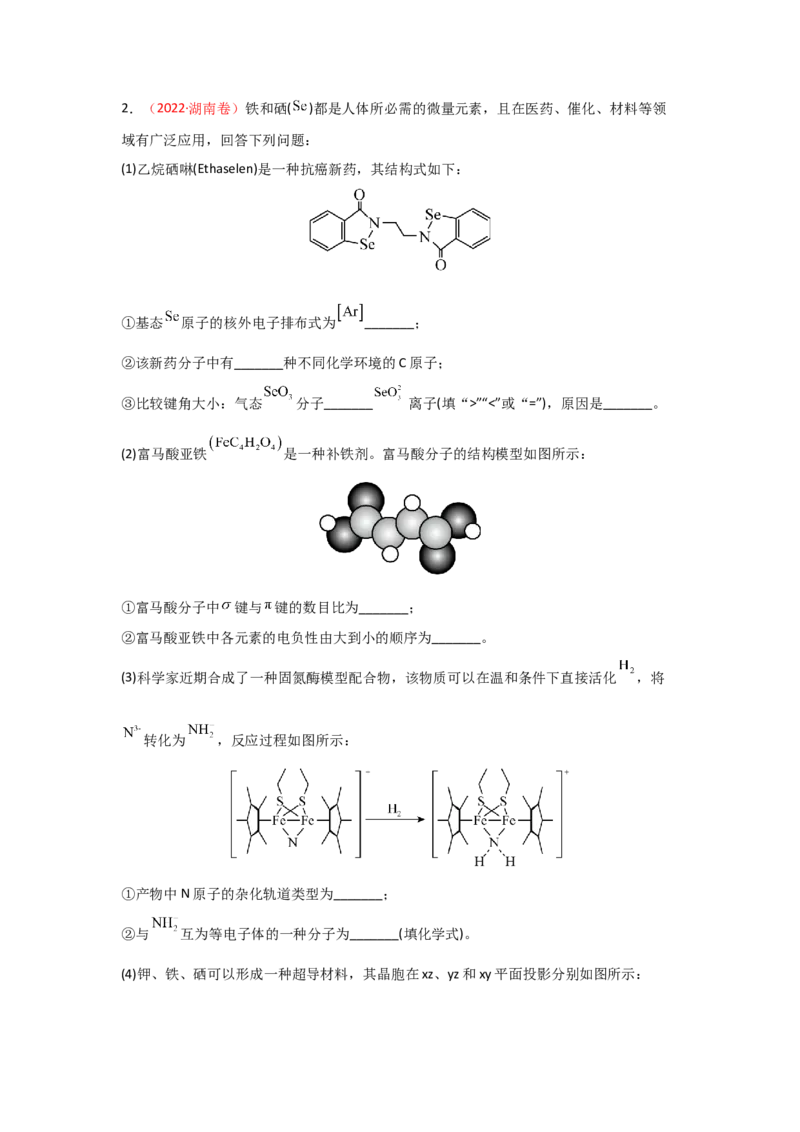
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:
①基态 原子的核外电子排布式为 _______;
②该新药分子中有_______种不同化学环境的C原子;
③比较键角大小:气态 分子_______ 离子(填“>”“<”或“=”),原因是_______。
(2)富马酸亚铁 是一种补铁剂。富马酸分子的结构模型如图所示:
①富马酸分子中 键与 键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将
转化为 ,反应过程如图所示:
①产物中N原子的杂化轨道类型为_______;
②与 互为等电子体的一种分子为_______(填化学式)。
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数 、 。阿伏加德罗常数的值为 ,则该晶体的密度为
_______ (列出计算式)。
【答案】(1) [Ar] 3d104s24p4 6 > SeO 的空间构型为平面三角形,SeO 的空间
3
构型为三角锥形
(2) 11:3 O>C>H>Fe
(3) sp3杂化 H O
2
(4) KFe Se 4
2 2
【解析】(1)①硒元素的原子序数为34,基态原子的电子排布式为[Ar] 3d104s24p4;
②由结构简式可知,乙烷硒啉的分子结构对称,分子中含有6种化学环境不同的碳原子;
③三氧化硒分子中硒原子的价层电子对数为3,孤对电子对数为0,分子的空间构型为平面
三角形,键角为120°,亚硒酸根离子中硒原子的价层电子对数为4,孤对电子对数为1,离
子的空间构型为三角锥形,键角小于120°;
(2)①由球棍模型可知,富马酸的结构式为HOOCCH=CHCOOH,分子中的单键为σ键,双键
中含有1个σ键和1个π键,则分子中σ键和π键的数目比为11:3;
②金属元素的电负性小于非金属元素,则铁元素的电负性最小,非金属元素的非金属性越
强,电负性越大,氢碳氧的非金属性依次增强,则电负性依次增大,所以富马酸亚铁中四
种元素的电负性由大到小的顺序为O>C>H>Fe;
(3)①由结构简式可知,产物中氮原子的价层电子对数为4,原子的杂化方式为sp3杂化,故答案为:sp3杂化;
②水分子和氨基阴离子的原子个数都为3、价电子数都为8,互为等电子体;
(4)①由平面投影图可知,晶胞中位于顶点和体心的钾原子个数为8× +1=2,均位于棱上和
面上的铁原子和硒原子的个数为12× +2× =4,则超导材料最简化学式为KFe Se ;
2 2
②由平面投影图可知,位于棱上的铁原子与位于面上的硒原子的距离最近,所以铁原子的
配位数为4;
③设晶体的密度为dg/cm3,由晶胞的质量公式可得: =abc×10—21×d,
解得d= 。