文档内容
电解原理的多方面应用
(选择题1~5题,每小题3分,6~12题,每小题5分,共50分)
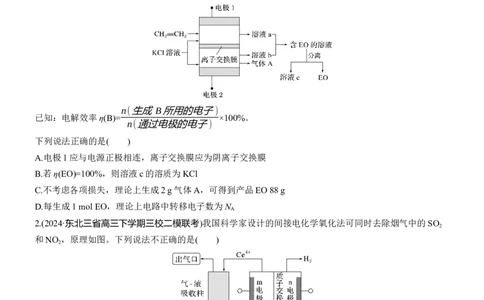
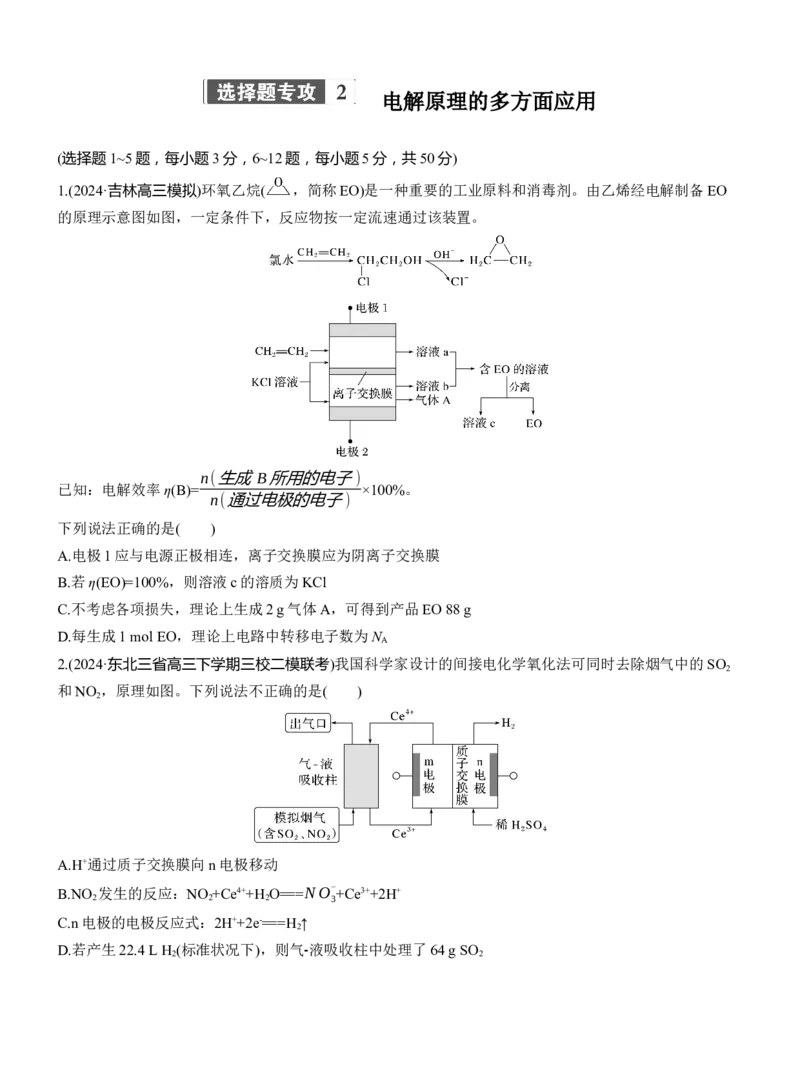
1.(2024·吉林高三模拟)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO
的原理示意图如图,一定条件下,反应物按一定流速通过该装置。
n(生成B所用的电子)
已知:电解效率η(B)= ×100%。
n(通过电极的电子)
下列说法正确的是( )
A.电极1应与电源正极相连,离子交换膜应为阴离子交换膜
B.若η(EO)=100%,则溶液c的溶质为KCl
C.不考虑各项损失,理论上生成2 g气体A,可得到产品EO 88 g
D.每生成1 mol EO,理论上电路中转移电子数为N
A
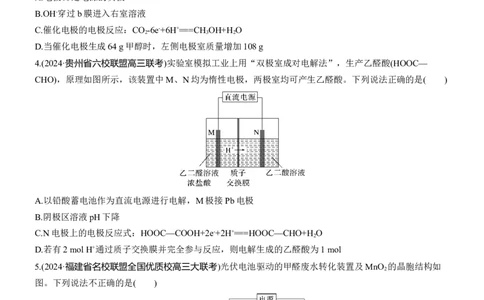
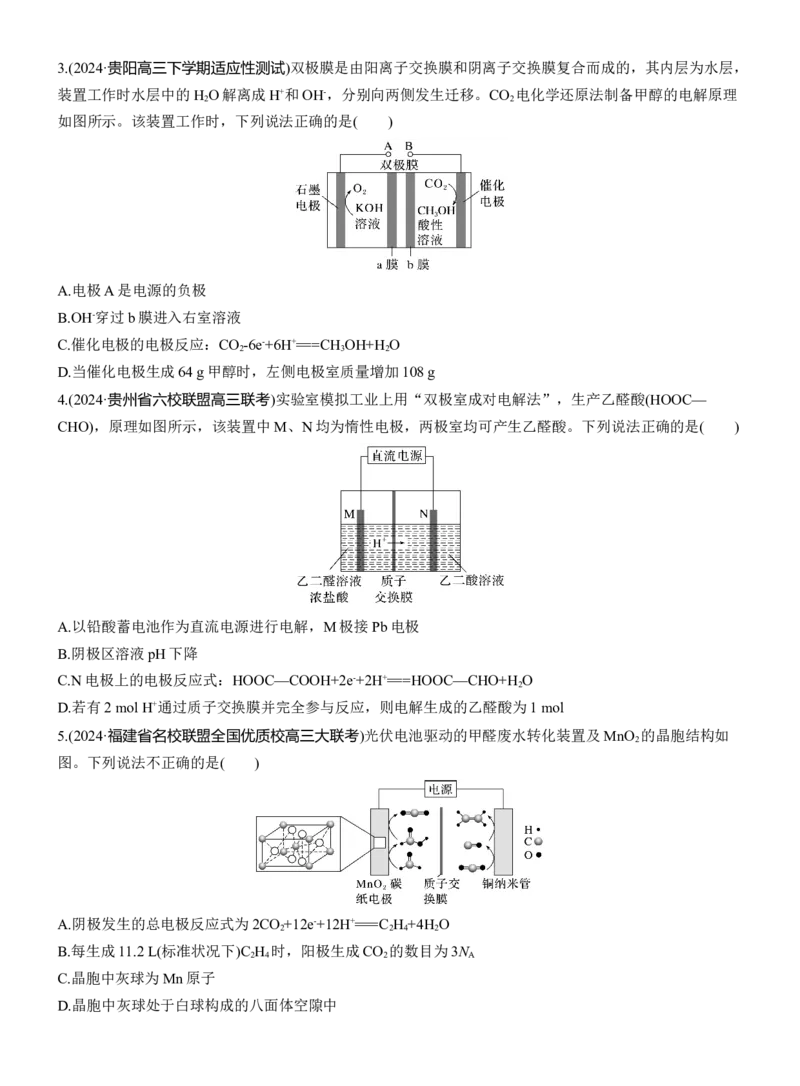
2.(2024·东北三省高三下学期三校二模联考)我国科学家设计的间接电化学氧化法可同时去除烟气中的SO
2
和NO ,原理如图。下列说法不正确的是( )
2
A.H+通过质子交换膜向n电极移动
B.NO 发生的反应:NO +Ce4++H
O===NO-
+Ce3++2H+
2 2 2 3
C.n电极的电极反应式:2H++2e-===H ↑
2
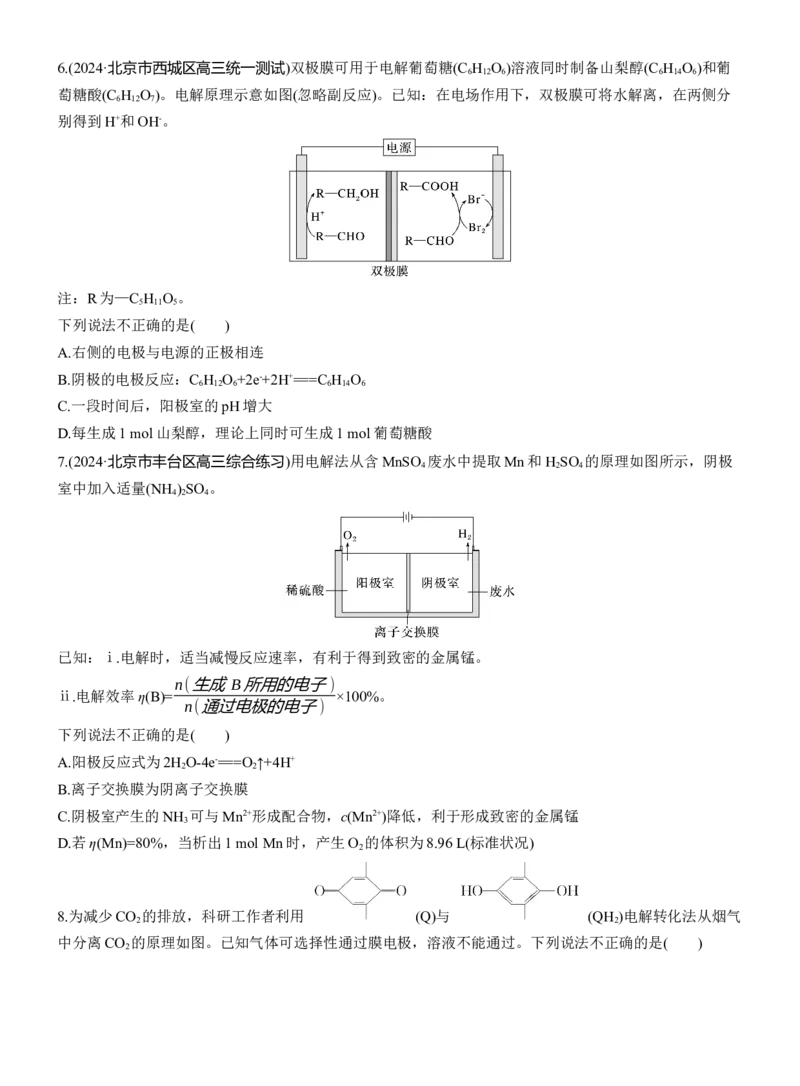
D.若产生22.4 L H 2 (标准状况下),则气 ⁃ 液吸收柱中处理了64 g SO 23.(2024·贵阳高三下学期适应性测试)双极膜是由阳离子交换膜和阴离子交换膜复合而成的,其内层为水层,
装置工作时水层中的H O解离成H+和OH-,分别向两侧发生迁移。CO 电化学还原法制备甲醇的电解原理
2 2
如图所示。该装置工作时,下列说法正确的是( )
A.电极A是电源的负极
B.OH-穿过b膜进入右室溶液
C.催化电极的电极反应:CO -6e-+6H+===CH OH+H O
2 3 2
D.当催化电极生成64 g甲醇时,左侧电极室质量增加108 g
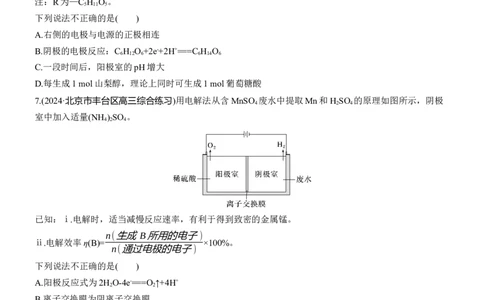
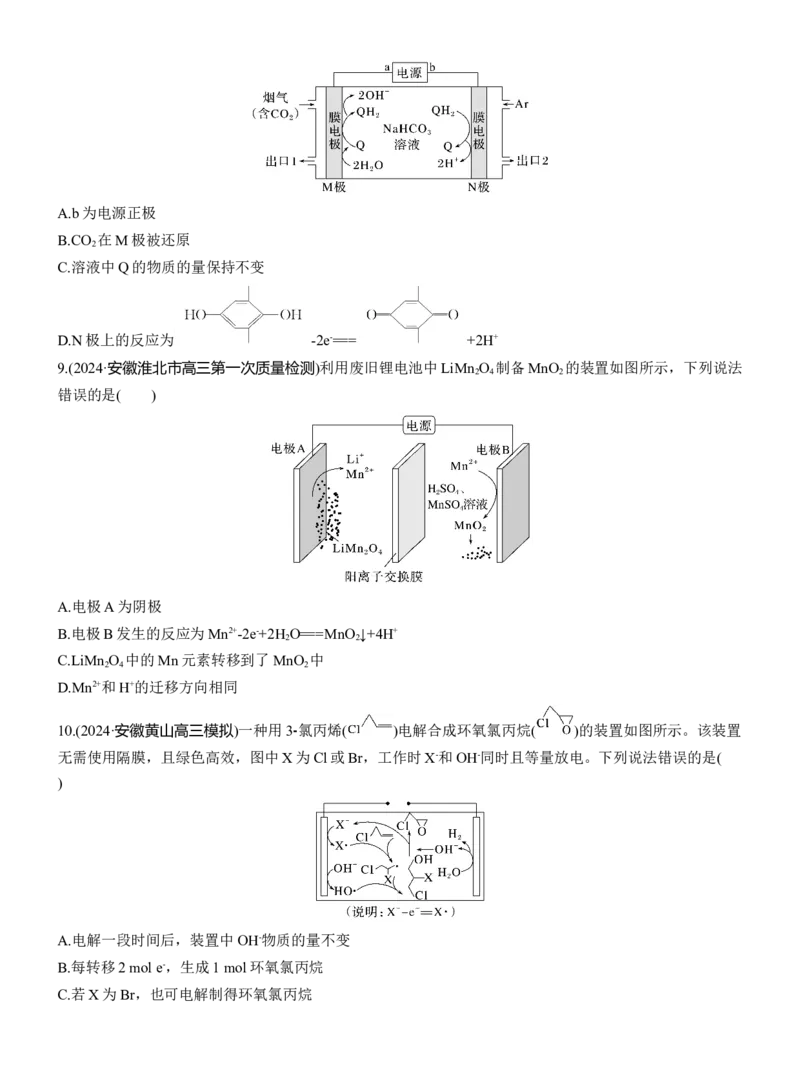
4.(2024·贵州省六校联盟高三联考)实验室模拟工业上用“双极室成对电解法”,生产乙醛酸(HOOC—
CHO),原理如图所示,该装置中M、N均为惰性电极,两极室均可产生乙醛酸。下列说法正确的是( )
A.以铅酸蓄电池作为直流电源进行电解,M极接Pb电极
B.阴极区溶液pH下降
C.N电极上的电极反应式:HOOC—COOH+2e-+2H+===HOOC—CHO+H O
2
D.若有2 mol H+通过质子交换膜并完全参与反应,则电解生成的乙醛酸为1 mol
5.(2024·福建省名校联盟全国优质校高三大联考)光伏电池驱动的甲醛废水转化装置及MnO 的晶胞结构如
2
图。下列说法不正确的是( )
A.阴极发生的总电极反应式为2CO +12e-+12H+===C H +4H O
2 2 4 2
B.每生成11.2 L(标准状况下)C H 时,阳极生成CO 的数目为3N
2 4 2 A
C.晶胞中灰球为Mn原子
D.晶胞中灰球处于白球构成的八面体空隙中6.(2024·北京市西城区高三统一测试)双极膜可用于电解葡萄糖(C H O )溶液同时制备山梨醇(C H O )和葡
6 12 6 6 14 6
萄糖酸(C H O )。电解原理示意如图(忽略副反应)。已知:在电场作用下,双极膜可将水解离,在两侧分
6 12 7
别得到H+和OH-。
注:R为—C H O 。
5 11 5
下列说法不正确的是( )
A.右侧的电极与电源的正极相连
B.阴极的电极反应:C H O +2e-+2H+===C H O
6 12 6 6 14 6
C.一段时间后,阳极室的pH增大
D.每生成1 mol山梨醇,理论上同时可生成1 mol葡萄糖酸
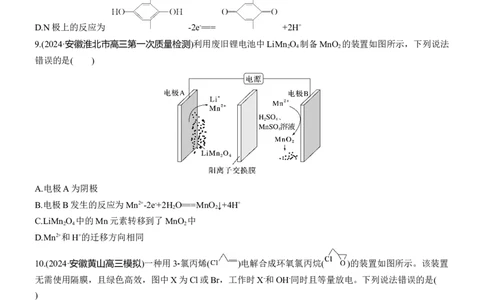
7.(2024·北京市丰台区高三综合练习)用电解法从含MnSO 废水中提取Mn和H SO 的原理如图所示,阴极
4 2 4
室中加入适量(NH ) SO 。
4 2 4
已知:ⅰ.电解时,适当减慢反应速率,有利于得到致密的金属锰。
n(生成B所用的电子)
ⅱ.电解效率η(B)= ×100%。
n(通过电极的电子)
下列说法不正确的是( )
A.阳极反应式为2H O-4e-===O ↑+4H+
2 2
B.离子交换膜为阴离子交换膜
C.阴极室产生的NH 可与Mn2+形成配合物,c(Mn2+)降低,利于形成致密的金属锰
3
D.若η(Mn)=80%,当析出1 mol Mn时,产生O 的体积为8.96 L(标准状况)
2
8.为减少CO 的排放,科研工作者利用 (Q)与 (QH )电解转化法从烟气
2 2
中分离CO 的原理如图。已知气体可选择性通过膜电极,溶液不能通过。下列说法不正确的是( )
2A.b为电源正极
B.CO 在M极被还原
2
C.溶液中Q的物质的量保持不变
D.N极上的反应为 -2e-=== +2H+
9.(2024·安徽淮北市高三第一次质量检测)利用废旧锂电池中LiMn O 制备MnO 的装置如图所示,下列说法
2 4 2
错误的是( )
A.电极A为阴极
B.电极B发生的反应为Mn2+-2e-+2H O===MnO ↓+4H+
2 2
C.LiMn O 中的Mn元素转移到了MnO 中
2 4 2
D.Mn2+和H+的迁移方向相同
10.(2024·安徽黄山高三模拟)一种用3⁃ 氯丙烯( )电解合成环氧氯丙烷( )的装置如图所示。该装置
无需使用隔膜,且绿色高效,图中X为Cl或Br,工作时X-和OH-同时且等量放电。下列说法错误的是(
)
A.电解一段时间后,装置中OH-物质的量不变
B.每转移2 mol e-,生成1 mol环氧氯丙烷
C.若X为Br,也可电解制得环氧氯丙烷D.该装置工作时不需要补充X-
11.(2024·湖南邵阳市高三模拟)ClO 是一种高效、安全的消毒用品。某电解法制备ClO 的装置如图,有关
2 2
说法错误的是( )
A.与a相连的电极上发生氧化反应
B.电解过程中转移2 mol电子时,有2 mol Cl-通过离子交换膜进入阳极区
C.整个生产过程中,理论上得到两种气体产物ClO 和H 的体积比为1∶2
2 2
D.“二氧化氯发生器”中生成的X溶液的主要溶质为NaCl和NaOH
12.(2024·辽宁鞍山市高三第二次质量监测)工业上通过电解NaCl⁃CaCl
2
共熔物制取金属Na的装置如图所示,
已知在电解过程中会产生一定量的金属Ca,下列说法错误的是( )
A.b电极为阳极
B.添加CaCl 的目的之一是降低电解质体系的熔点
2
C.阴极反应:Na++e-===Na;Ca2++2e-===Ca
D.为防止生成的Na与Cl 接触,阴、阳两极之间应用钢板隔开
2答案精析
1.B [电极1电解氯化钾溶液产生氯气,氯气与水反应得次氯酸,乙烯与次氯酸反应,故电极1为阳极,
应与电源正极相连,如果离子交换膜为阴离子交换膜,电极2电解水产生的氢氧根离子进入电极室1会影
响次氯酸生成,故应是电极室1中钾离子进入电极室2,离子交换膜为阳离子交换膜,A错误;若
η(EO)=100%,则HOCH CH Cl与溶液b中的KOH恰好反应:HOCH CH Cl+KOH===KCl+H O+ ,则溶
2 2 2 2 2
液c的溶质为KCl,B正确;气体A是阴极产生的氢气,2 g气体A即1 mol,转移电子2 mol,对应电极1
产生氯气1 mol,生成HOCH CH Cl的物质的量为1 mol,则产品EO也为1 mol,质量为44 g,C错误;每
2 2
生成1 mol EO,需要1 mol氯气,理论上电路中转移电子数为2N ,D错误。]
A
2.D [m为阳极,H+通过质子交换膜向阴极(n电极)移动,故A正确;NO
被Ce4+氧化为NO-
,离子方程式
2 3
为NO +Ce4++H
O===NO-
+Ce3++2H+,故B正确;n极电极反应式为2H++2e-===H ↑,若产生22.4 L H (标
2 2 3 2 2
准状况下),转移电子2 mol,SO
被Ce4+氧化为SO2-
,反应的离子方程式为SO +2Ce4++2H
O===SO2-
2 4 2 2 4
+2Ce3++4H+,当转移2 mol电子时,消耗1 mol SO ,质量为64 g,但实际上SO 、NO 同时与Ce4+反应,因
2 2 2
此处理的SO 小于64 g,故C正确、D错误。]
2
3.D [由图可知,左侧电极-2价氧失去电子发生氧化反应,为电解池的阳极,右侧电极二氧化碳得到电子
发生还原反应,为电解池的阴极,以此解题。右侧电极为阴极,左侧电极为阳极,在电解池中阴离子向阳
极移动,则OH-穿过a膜进入左室溶液,B错误;催化电极为阴极,电极反应为CO +6e-
2
+6H+===CH OH+H O,64 g甲醇的物质的量为2 mol,此时转移12 mol电子,左侧电极有如下对应关系:
3 2
12
O ~4e-~4OH-~Δm(36),则当转移12 mol电子时,左侧电极室质量增加 ×36 g=108 g,C错误,D正确。]
2 4
4.C [该装置M为阳极、N为阴极,铅酸蓄电池中Pb电极为负极,以铅酸蓄电池作为直流电源进行电解,
N极接Pb电极,故A错误;N为阴极,阴极发生反应HOOC—COOH+2e-+2H+===HOOC—CHO+H O,消
2
耗氢离子,阴极区溶液pH升高,故B错误、C正确;M为阳极,阳极反应式为OHC—CHO-2e-
+H O===HOOC—CHO+2H+,N为阴极,电极反应式为HOOC—COOH+2e-+2H+===HOOC—CHO+H O,若
2 2
有2 mol H+通过质子交换膜并完全参与反应,阴极、阳极各生成1 mol乙醛酸,则电解生成的乙醛酸为2
mol,故D错误。]
5.B [由图可知,右侧电极上二氧化碳转化为CO,CO最终转化为乙烯,C元素化合价降低,发生还原反
应,则右侧电极为阴极,左侧电极为阳极,阳极甲醛失电子生成HCOOH,HCOOH继续失电子生成二氧
化碳,据此分析解答。由上述分析可知阴极发生的总电极反应式为2CO +12e-+12H+===C H +4H O,故A
2 2 4 2
1 1
正确;晶胞中灰球位于顶角和体心,个数为8× +1=2,白球位于面上和体内,个数为4× +2=4,结合
8 2
MnO 的化学式可知灰球为Mn,故C正确;以体心灰球为观察对象,可知其周围有4个白球位于面上,2
2
个白球位于体内,灰球处于白球构成的八面体空隙中,故D正确。]6.C [左边电极葡萄糖被还原为山梨醇,为阴极,右边电极溴离子失电子被氧化为溴,为阳极,与电源正
极相连,故A正确;左边电极为阴极,葡萄糖中的醛基被还原,电极反应式:C H O +2e-
6 12 6
+2H+===C H O ,故B正确;阳极室中还发生:H O+Br +RCHO===RCOOH+2H++2Br-,电解一段时间后,
6 14 6 2 2
溶液pH减小,故C错误;制备山梨醇的反应为C H O +2e-+2H+===C H O ,制备葡萄糖酸的总反应为
6 12 6 6 14 6
C H O -2e-+H O===C H O +2H+,根据得失电子守恒可知每生成1 mol山梨醇,理论上同时可生成1 mol葡
6 12 6 2 6 12 7
萄糖酸,故D正确。]
7.D [根据图示,阳极放出氧气,阳极反应式为2H O-4e-===O ↑+4H+,故A正确;电解过程中,阴极室
2 2
硫酸根离子移向阳极室生成硫酸,所以离子交换膜为阴离子交换膜,故B正确;电解时,适当减慢反应速
率,有利于得到致密的金属锰,阴极室产生的NH 可与Mn2+形成配合物,c(Mn2+)降低,有利于形成致密的
3
1mol×2
金属锰,故C正确;若η(Mn)=80%,当析出1 mol Mn时,转移电子 =2.5 mol,阳极发生反应:
80%
2.5mol
2H O-4e-===O ↑+4H+,产生O 的体积为 ×22.4 L·mol-1=14 L,故D错误。]
2 2 2 4
8.B [结合该电解池图示中的信息可知,M极发生的是由 转化为 的反应,
从分子组成上看,该过程中是一个加氢的过程,属于还原反应,故M极为阴极,则阴极的电极反应式为
+2H O+2e-=== +2OH-,故与M相连的a电极为电源负极,b为电源正极,N
2
为阳极,阳极的电极反应式为 -2e-=== +2H+,由此分析回答。由阴极的电极
反应式可知整个过程CO 并未被还原,CO 在M极上发生的反应为CO
+OH-===HCO-
,B错误;结合阴
2 2 2 3
极和阳极的电极反应式可知,该电解池中的总反应的方程式可表示为H O H++OH-,在该电解池中Q相
2
当于是反应的催化剂,结合该电解装置中气体可选择性通过膜电极、溶液不能通过,则溶液中Q的物质的
量保持不变,C、D正确。]
9.C [由图可知,该装置为电解池,电极A与直流电源负极相连为阴极,酸性条件下,LiMn O 在阴极得
2 4
到电子发生还原反应生成锰离子,电极反应式为LiMn O +3e-+8H+===Li++2Mn2++4H O,电极B为阳极,锰
2 4 2
离子在阳极失去电子发生氧化反应生成二氧化锰,电极反应式为2H O+Mn2+-2e-===MnO +4H+,则电解的
2 2
总反应方程式为2LiMn O +4H+ 2Li++Mn2++3MnO +2H O。由上述电解的总反应方程式知LiMn O 中的
2 4 2 2 2 4
Mn元素转移到了MnO 和Mn2+中,故C错误;电解池中阳离子移向阴极,Mn2+和H+的迁移方向相同,都
2
向阴极移动,故D正确。]
10.A [由图可知,右电极上H O被还原生成H ,即右电极作阴极,则左电极作阳极,阳极上X-和OH-同
2 2
时且等量放电:X--e-===X·、OH--e-===·OH;由装置原理图可知,每生成1个环氧氯丙烷,阳极上消耗1个
OH-,阴极上生成2个OH-,反应消耗1个,还剩1个OH-,则电解一段时间后,装置中OH-的物质的量增大,A错误;由装置原理图可知,阳极上X-和OH-各失去1个电子,即转移2个电子,就生成1个环氧氯
丙烷,则每转移2 mol e-,生成1 mol环氧氯丙烷,B正确;由装置原理图可知,X为Cl或Br,电解制备
产物均为环氧氯丙烷,C正确;由装置原理图可知,每生成1个环氧氯丙烷,阳极上先消耗1个X-,最终
生成环氧氯丙烷时又释放1个X-,即X-为可循环离子,则该装置工作时无需补充X-,D正确。]
11.C [图中右室生成H ,发生还原反应,b连接电解池的阴极,b为电源负极,则a连接电解池的阳极,
2
发生氧化反应,故A正确;电解池中阴离子向阳极移动,则电解过程中转移2 mol电子时,有2 mol Cl-通
过离子交换膜进入阳极区,故B正确;阴极反应式为2H++2e-===H ↑,阳极反应式为N H+ +3Cl--6e-
2 4
===NCl +4H+,每转移6个电子,生成1个NCl ,3个H ,二氧化氯发生器中发生反应的化学方程式为
3 3 2
NCl +6NaClO +3H O===6ClO ↑+NH ↑+3NaCl+3NaOH,每转移6个电子,生成6个ClO ,则整个生产过
3 2 2 2 3 2
程中,理论上得到两种气体产物ClO 和H 的物质的量比为2∶1,故C错误、D正确。]
2 2
12.D [依据图示可知,b电极出口有Cl ,故b为阳极,电极反应为2Cl--2e-===Cl ↑,则a为阴极,电极反
2 2
应为Na++e-===Na。添加CaCl 的目的是降低电解质熔点,节省能源,同时减少单质钠的挥发;增大密度,
2
使得被还原出的密度较低的液态钠单质能漂浮在混合盐之上,易于分离得到产物,B正确;电解过程中会
产生一定量的金属Ca,说明部分钙离子会在阴极放电,C正确;为了防止生成的Na与Cl 接触,阴、阳两
2
极应该用离子交换膜,以保持两极区电解质的电中性,不能使用钢板,D错误。]