文档内容
专题四 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Cr 52 Mn 55 Fe 56 Ni 59 Cu 64 La 139
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘我国古代精美的青瓷工艺品。
玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法中正确的是( )
A.玻璃是人类最早使用的硅酸盐制品
B.制水泥的原料为纯碱、石灰石和石英
C.硅酸盐制品的性质稳定、熔点较高
D.沙子和黏土的主要成分均为硅酸盐
【答案】C
【解析】陶瓷是人类最早使用的硅酸盐制品,A项错误;纯碱、石灰石和石英是制玻璃的原料,而制
水泥的原料是黏土和石灰石,B项错误;硅酸盐制品性质稳定、熔点高,C项正确;沙子的主要成分是
SiO,黏土的主要成分是硅酸盐,D项错误。
2
2.由下列实验事实得出的结论正确的是( )
A.由SiO 不能与水反应生成HSiO 可知,SiO 不是HSiO 的酸酐
2 2 3 2 2 3
B.由SiO+2C=====Si+2CO↑可知,碳的非金属性强于硅
2
C.CO 通入NaSiO 溶液产生白色沉淀,可知酸性HCO>HSiO
2 2 3 2 3 2 3
D.SiO 可与NaOH溶液反应,也可与氢氟酸反应,可知SiO 为两性氧化物
2 2
【答案】C
【解析】SiO 是HSiO 的酸酐,A错误;SiO +2C=====Si+2CO↑,说明还原性C>Si,但不能比较非金属
2 2 3 2
性,B错误;CO +NaSiO +HO===HSiO↓+NaCO ,说明酸性HCO> HSiO ,C正确;两性氧化物是指和
2 2 3 2 2 3 2 3 2 3 2 3
酸、碱反应生成盐和水的氧化物,二氧化硅和氢氟酸反应是其特殊性质,不能和其他酸发生反应,二氧化硅和
碱溶液反应生成盐和水,是酸性氧化物,D项错误。
3.为了从海带浸取液中提取碘,某同学设计了如图实验方案,下列说法正确的是( )A.①中反应的离子方程式:2I-+HO===I +2OH-
2 2 2
B.②中分液时含I 的CCl 溶液从分液漏斗上口倒出
2 4
C.③中得到的上层溶液中含有I-
D.操作Z的名称是加热
【答案】C
【解析】反应条件为酸性环境,①中反应的离子方程式:2I-+2H++HO===I +2HO,故A错误;
2 2 2 2
四氯化碳比水的密度大,在下层,②中分液时含I 的CCl 溶液从分液漏斗下口放出,故B错误;操作Z的
2 4
名称是过滤,故D错误。
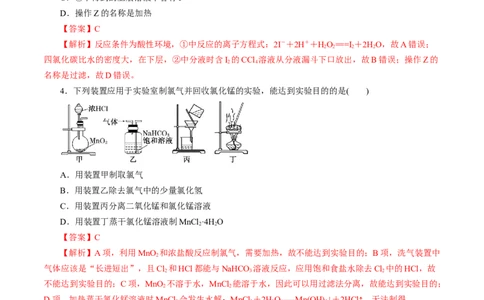
4.下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl ·4H O
2 2
【答案】C
【解析】A项,利用MnO 和浓盐酸反应制氯气,需要加热,故不能达到实验目的;B项,洗气装置中
2
气体应该是“长进短出”,且Cl 和HCl都能与NaHCO 溶液反应,应用饱和食盐水除去Cl 中的HCl,故
2 3 2
不能达到实验目的;C项,MnO 不溶于水,MnCl 能溶于水,因此可以用过滤法分离,故能达到实验目的;
2 2
D项,加热蒸干氯化锰溶液时MnCl 会发生水解:MnCl +2HO Mn(OH) ↓+2HCl↑,无法制得
2 2 2 ===== 2
MnCl ·4H O,故不能达到实验目的。
2 2
5.漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为Ca(ClO) ,相应的生产流程如下。
2
下列说法不正确的是( )A.①中阳极的电极反应式为2Cl--2e-===Cl↑
2
B.②中反应的化学方程式为2Cl+2Ca(OH) ===Ca(ClO) +CaCl +2HO
2 2 2 2 2
C.上述过程涉及氧化还原反应、化合反应、复分解反应
D.制备漂粉精过程中,Cl 转化为Ca(ClO) 时,Cl的原子利用率为100%
2 2
【答案】D
【解析】饱和食盐水进行电解可以制得Cl,将得到的Cl 分别与Ca(OH) 和NaCO 反应经一系列流程
2 2 2 2 3
可以分别制得漂白粉和漂粉精;电解过程中,溶液中的Cl-失电子生成氯气,发生氧化反应,水中的H+得
电子生成氢气,发生还原反应,溶液中剩余氢氧化钠;氯气与氢氧化钙浆料反应生成次氯酸钙,同时还生
成氯化钙和水;氯气与湿润的碳酸钠反应生成ClO,ClO与水发生化合反应生成HClO,HClO与氢氧化
2 2
钙浆料反应生成次氯酸钙,据此分析。电解过程中阳极失电子,溶液中Cl-在阳极发生氧化反应生成Cl,
2
阳极的电极反应式为2Cl--2e-===Cl↑,A正确;反应②为氯气和氢氧化钙的反应,反应方程式为2Cl+
2 2
2Ca(OH) ===Ca(ClO) +CaCl +2HO,B正确;上述过程中反应①②③为氧化还原反应,反应④为化合反
2 2 2 2
应,反应⑤为复分解反应,C正确;制备漂粉精过程中,Cl 转化为Ca(ClO) 时有CaCl 生成,Cl原子没有
2 2 2
完全转化为Ca(ClO) ,因此Cl的原子利用率小于100%,D错误。
2
6.海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图,则下列说法正确
的是( )
A.除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,①中加入试剂的顺序为NaCO 溶液―→NaOH溶
2 3
液―→BaCl 溶液―→过滤后加盐酸
2
B.②中包含制取MgCl 溶液、无水MgCl 及电解熔融状态的MgCl 几个阶段
2 2 2
C.③④⑤中溴元素均被氧化
D.蒸馏法是技术最成熟也是最具发展前景的海水淡化方法
【答案】B
【解析】A项中加入试剂的顺序会导致Ba2+无法除尽,A错误;单质镁是通过电解熔融MgCl 的方法
2
制取的,B正确;流程图中的第④步中溴元素被还原,C错误;蒸馏法会消耗大量的能源,不是最具有发
展前景的方法,D错误。
7.下列由相关实验现象推出的结论正确的是( )
A.NH Cl和NH HCO 受热都能分解,说明可以用加热NH Cl和NH HCO 固体的方法制氨
4 4 3 4 4 3
B.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定含有SO
3 2
C.Fe与稀硝酸、稀硫酸反应均有气泡产生,说明Fe与两种酸均发生置换反应
D.NH 遇到浓盐酸产生白烟,说明二者发生反应生成白色固体
3
【答案】D【解析】NH Cl受热分解生成氨和氯化氢,冷却后二者又重新结合生成NH Cl,不能制备氨,A项错
4 4
误;向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,在酸性条件下NO具有强氧化性,会把SO氧化成
3 2
SO,故不能说明原溶液中一定含有SO,也可能含有SO,B项错误;Fe与稀硝酸、稀硫酸反应均有气泡产
生,前者是由于稀硝酸的强氧化性,后者是由于Fe与稀硫酸发生置换反应,C项错误;NH 遇到浓盐酸产
3
生白烟,说明二者发生反应生成白色固体氯化铵,D项正确。
8.根据下图海水综合利用的工艺流程图,判断下列说法正确的是( )
已知:MgCl ·6H O受热生成Mg(OH)Cl和HCl气体等。
2 2
A.过程①的粗盐提纯是物理过程,过程②通过氧化还原反应可产生两种单质
B.在过程③中将MgCl ·6H O灼烧即可制得无水MgCl
2 2 2
C.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
D.在过程④⑥反应中每氧化0.2 mol Br-需要消耗2.24 L Cl
2
【答案】C
【解析】过程①中除去Mg2+、CO和SO需要用化学方法,A错误;根据已知信息可知,B错误;过程
⑤发生的反应为SO +2HO+Br ===H SO +2HBr,溶液呈强酸性,C正确;每氧化0.2 mol Br-需要消耗
2 2 2 2 4
0.1 mol Cl ,但不一定是2.24 L,D错误。
2
9.某学习小组设计制取SO 并验证其部分性质的实验装置图如图(夹持装置省略),下列叙述正确的是(
2
)
A.取反应后D中溶液少许,滴加品红溶液,红色褪去,能说明SO 具有漂白性
2
B.A装置中比较理想的反应物质是NaSO 固体和质量分数为10%的硫酸
2 3
C.B装置溶液变红色,说明SO 是酸性氧化物;C装置产生白色沉淀的原因为BaCl +SO +
2 2 2
HO=====BaSO↓+2HCl
2 3
D.关闭弹簧夹a,打开弹簧夹b,用酒精灯在三颈烧瓶下微热,若能观察到C中长导管口有明显气泡
现象,冷却后长导管中出现一段水柱,就能判断装置A、B部分气密性良好
【答案】D
【解析】氯水中存在次氯酸,次氯酸具有漂白作用,也可以使品红溶液褪色,不能确定一定为二氧化
硫的漂白性,故A错误;二氧化硫易溶于水,比较理想的反应物质是亚硫酸钠固体和浓硫酸,故B错误;C装置中产生的白色沉淀为BaSO,故C错误;检查装置中A、B两部分的气密性,进行的操作是:关闭
4
弹簧夹a,打开弹簧夹b,用酒精灯在三颈烧瓶下微热,观察到B中长导管口有明显气泡现象,冷却后长导
管中出现一段水柱,说明该装置A、B部分气密性良好,故D正确。
10.如图所示,将相同条件下的m体积NO和n体积O 同时通入倒立于水槽中且盛满水的试管内,充分
2
反应后,试管内残留体积的气体,该气体与空气接触后立即变为红棕色。则m与n的比值为( )
A.3∶2 B.2∶3
C.8∶3 D.3∶8
【答案】C
【解析】该过程中涉及的反应有2NO+O===2NO、3NO +HO===2HNO +NO,可将两个方程式合
2 2 2 2 3
并为4NO+3O+2HO===4HNO ,剩余气体与空气接触立即变为红棕色,说明剩余气体为NO,则可知体
2 2 3
积的NO气体与n体积的O 恰好完全反应,
2
4NO+3O+2HO===4HNO
2 2 3
4 3
n
4∶=3∶n,解得m∶n=8∶3,故选C。
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.金刚砂(SiC)可由SiO 和碳在一定条件下反应制得,反应的化学方程式为SiO+3C=====SiC+2CO↑,
2 2
下列有关制造金刚砂的说法正确的是( )
A.该反应中的氧化剂是SiO,还原剂为C
2
B.该反应中的氧化产物和还原产物的物质的量之比为2∶1
C.该反应中转移12e-
D.该反应中的还原产物是SiC、氧化产物是CO
【答案】BD
【解析】反应产物SiC中Si、C的化合价分别为+4、-4价,所以SiO 既不是氧化剂,又不是还原剂;碳
2
元素从0价转变成-4价(SiC)和+2价(CO),CO是氧化产物,SiC是还原产物,两者的物质的量之比为2∶1;
根据化学方程式可知,该反应转移4e-。
12.将一定质量的镁、铜合金加入到稀硝酸中,合金完全溶解,假设反应过程中还原产物全部是
NO,向所得溶液中加入物质的量浓度为3 mol·L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合
金的质量增加5.1 g,则下列有关叙述正确的是( )A.反应中转移电子的总物质的量为0.2 mol
B.反应过程中,消耗硝酸的物质的量为0.3 mol
C.沉淀完全时消耗NaOH溶液的体积为100 mL
D.开始加入合金的质量可能为6.4 g
【答案】D
【解析】生成沉淀的质量比原合金的质量增加5.1 g,即结合氢氧根离子的物质的量为=0.3 mol,根据
电荷守恒、得失电子守恒,合金失电子数等于金属离子结合氢氧根离子数,反应中转移电子的总物质的量
为0.3 mol,A项错误;根据上述分析,反应中转移的电子总物质的量为0.3 mol,根据电荷守恒,合金与硝
酸反应时,表现酸性的硝酸的物质的量为0.3 mol;合金的还原产物为NO,表现氧化性的硝酸的物质的量
为0.1 mol,反应过程中,消耗硝酸的物质的量为0.4 mol,B项错误;合金完全溶解后硝酸可能剩余,沉淀
完全时消耗NaOH溶液的体积≥100 mL,C项错误;转移电子的总物质的量为0.3 mol,合金的物质的量为
0.15 mol,利用极值法,合金的质量介于3.6~9.6 g之间,D项正确。
13.水玻璃(NaSiO 溶液)广泛应用于耐火材料、洗涤剂生产等领域,是一种重要的工业原料。如图是用稻
2 3
壳灰(SiO:65%~70%、C:30%~35%)制取水玻璃的工艺流程:
2
下列说法正确的是( )
A.原材料稻壳灰价格低廉,且副产品活性炭有较高的经济价值
B.操作A与操作B完全相同
C.该流程中硅元素的化合价没有发生改变
D.反应器中发生的反应为氧化还原反应
【答案】AC
【解析】A项,稻壳灰来源广泛,价格低廉,活性炭具有吸附性,有较高的经济价值,正确;B项,操作A
为过滤,操作B为蒸发浓缩,是两种不同的操作,错误;C项,二氧化硅中硅元素的化合价是+4价,硅酸钠中
硅元素的化合价也是+4价,所以该流程中硅元素的化合价没有发生改变,正确;D项,反应器中发生的反应为
SiO+2NaOH===NaSiO+HO,此反应没有元素化合价的变化,属于非氧化还原反应,错误。
2 2 3 2
14.实验室可用如图装置制取少量氮气。下列说法不正确的是( )A.反应过程中,③中硬质玻璃管中固体由黑变红
B.②中盛放的固体是碱石灰
C.实验开始时先点燃③中的酒精灯,再点燃①中的酒精灯
D.实验结束时,先将导管从水槽中拿出,再熄灭①③中的酒精灯
【答案】C
【解析】加热条件下,氨气与CuO反应生成氮气、Cu和水,反应的方程式为2NH +3CuO N↑+
3 ===== 2
3Cu+3HO,所以反应过程中,③中硬质玻璃管中固体由黑变红,故A正确;干燥氨气应该用碱性干燥剂,
2
所以②中盛放的是碱石灰,不能是五氧化二磷,故B正确;先用①中产生的氨气排尽装置中的空气,所以
实验开始时先点燃①中的酒精灯,再点燃③中的酒精灯,故C错误;结束实验时,先把水槽中的导管取出,
然后熄灭酒精灯,否则水槽中的导管会发生倒吸,故D正确。
15.实验室用H 还原SiHCl(沸点:31.85 ℃)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),
2 3
下列说法正确的是( )
A.装置Ⅱ、Ⅲ中依次盛装的是浓硫酸、冰水
B.实验时,应先打开活塞K,再加热管式炉
C.为鉴定制得的硅中是否含有微量铁单质,需要用到的试剂为盐酸、双氧水、KSCN溶液
D.该实验中制备氢气的装置也可用于饱和食盐水与电石反应制备乙炔
【答案】BC
【解析】制备高纯硅的反应为H +SiHCl=====Si+3HCl,此反应应在装置Ⅳ中进行。装置Ⅰ的目的是制
2 3
取氢气,氢气中含有水蒸气,对后续实验产生干扰,必须除去,因此装置Ⅱ的目的是除去氢气中的水蒸气,即
装置Ⅱ中盛放浓硫酸;装置Ⅲ的目的是使SiHCl 汽化,与氢气充分混合,因此应在热水浴中加热,A项错误;
3
实验时应先打开活塞K,通入氢气,排尽装置中的空气,防止加热时发生爆炸,B项正确;硅不能与盐酸反应,
铁与盐酸反应生成Fe2+,Fe2+被HO 氧化成Fe3+,遇KSCN溶液变红,可以鉴定制得的硅中是否含有铁单质,
2 2
C项正确;饱和食盐水与电石反应制备乙炔,反应迅速放出大量热且生成微溶的氢氧化钙,因此不能用启普发生器进行实验,D项错误。
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)氮化硅可用作高温陶瓷复合材料,在航空航天、汽车发动机、机械等领域有着广泛的应用。
由石英砂合成氮化硅粉末的路线如图所示:
――→――→――→――→――→
其中—NH 中各元素的化合价与NH 相同。请回答下列问题:
2 3
(1)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因:
________________________。
(2)图示①~⑤的变化中,属于氧化还原反应的是________。
(3)在反应⑤中,3 mol Si(NH) 在高温下加热可得1 mol 氮化硅粉末和8 mol A气体,则氮化硅的化学式为
2 4
________。
(4)在高温下将SiCl 在B和C两种气体的气氛中,也能反应生成氮化硅,B和C两种气体在一定条件下化合
4
生成A。写出SiCl 与B和C两种气体反应的化学方程式:_____________________________________________。
4
【解析】(1)石英砂不能与碱性物质共同存放的原因是SiO 与碱性物质可以发生反应。(2)反应①是石英砂与
2
焦炭发生氧化还原反应;反应②是硅单质与Cl 发生氧化还原反应。(3)氮化硅的化学式可通过题目信息运用质量
2
守恒求得:3Si(NH)=====SiN+8NH↑。(4)结合题给信息,SiCl 与N、H 反应可得到SiN 和HCl。
2 4 3 4 3 4 2 2 3 4
【答案】(1)SiO+2NaOH===NaSiO+HO
2 2 3 2
(2)①②
(3)SiN
3 4
(4)3SiCl+2N+6H=====SiN+12HCl
4 2 2 3 4
17.(10分)某化学小组同学发现84消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混
合有Cl 生成,于是尝试在实验室利用该反应原理制取Cl。
2 2
(1)若以次氯酸钙、浓盐酸为原料,利用如图装置制取Cl。装置中仪器a的名称为______。甲同学为证明
2
Cl 溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO 粉末,观察有无色气泡
2 3
产生,乙同学认为不合理,理由是________________________________________________________________。
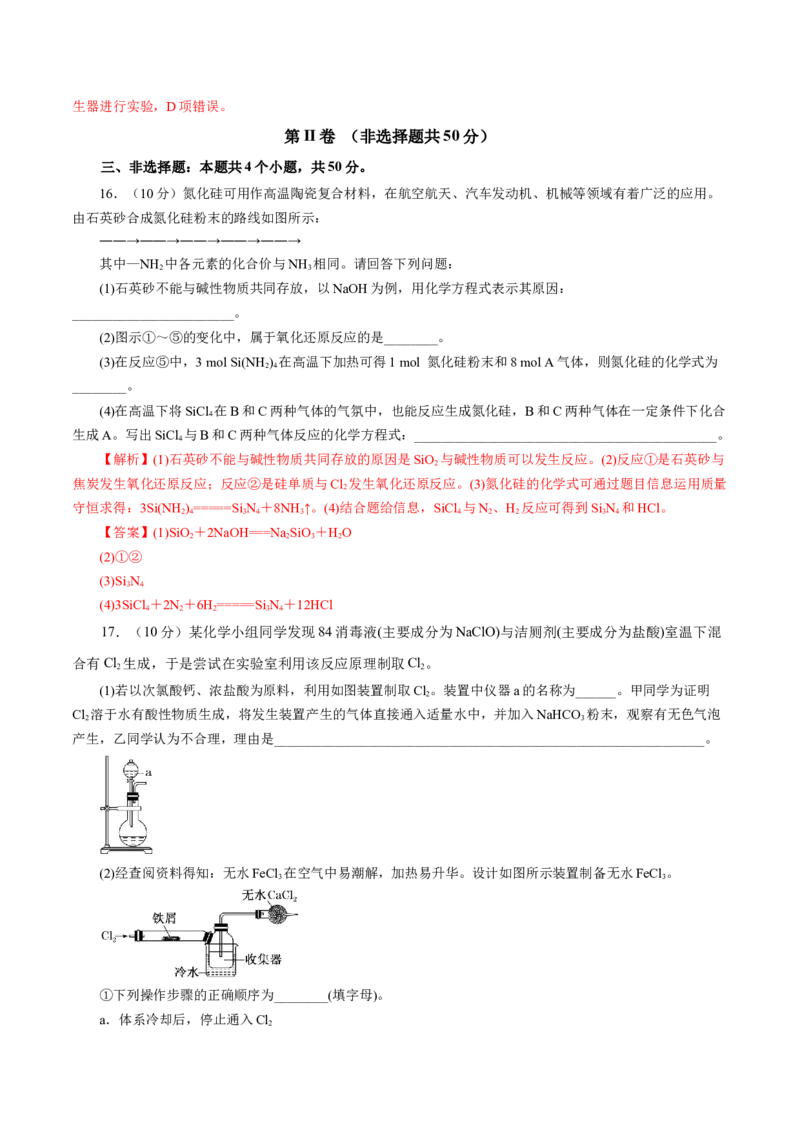
(2)经查阅资料得知:无水FeCl 在空气中易潮解,加热易升华。设计如图所示装置制备无水FeCl。
3 3
①下列操作步骤的正确顺序为________(填字母)。
a.体系冷却后,停止通入Cl
2b.通入干燥的Cl 赶尽装置中的空气
2
c.在铁屑下方加热至反应完成
d.用干燥的H 赶尽Cl
2 2
e.检查装置的气密性
②该实验装置存在的明显缺陷是__________________________________________。
(3)世界环保联盟要求ClO 逐渐取代Cl 作为自来水消毒剂。
2 2
已知:NaCl+3HO=====NaClO+3H↑,2NaClO+4HCl===2ClO↑+Cl↑+2NaCl+2HO。
2 3 2 3 2 2 2
有关物质的熔、沸点如下表:
物质 熔点/℃ 沸点/℃
ClO -59 11
2
Cl -107 -34.6
2
ClO 的生产流程示意图如下:
2
该工艺中,需要补充的物质X为________(填化学式,下同),能参与循环的物质是________。从ClO 发生
2
器中分离出ClO,可采用的方法是____________________________。
2
【解析】(2)①根据题给信息,无水氯化铁制备时应排除装置中的空气,所以先检查装置的气密性,再通入
干燥的氯气以排尽装置内的空气,然后加热使氯气与铁反应生成氯化铁,因为氯化铁加热易升华,所以加热使
反应完全后继续通入氯气至装置冷却,最后通入干燥的氢气以排尽氯气。②氯气是有毒气体,所以不能直接排
放,因此该装置的明显缺陷是缺少尾气处理装置。(3)根据工艺流程可知,电解食盐水得到的是氯酸钠和氢气,
而合成氯化氢需要氯气、氢气,所以需要补充的物质X是氯气;氯酸钠与氯化氢反应生成氯化钠、氯气及二氧
化氯,且氯化钠、氯气又可参与反应,所以参与循环的物质是氯化钠、氯气;二氧化氯的熔、沸点较低,所以
将生成的气体冷凝,使二氧化氯转化为液体分离出来。
【答案】(1)分液漏斗 制取的氯气中含HCl气体,HCl溶于水后能与NaHCO 反应产生气泡
3
(2)①ebcad ②缺少尾气处理装置
(3)Cl Cl、NaCl 将生成的气体冷水浴降温,使ClO 液化分离出来
2 2 2
18.(15分)某化学自主实验小组通过实验探究NH、NO 的性质。
3 2
探究Ⅰ:利用如图所示装置探究NO 能否被NH 还原(K、K 为止水夹,夹持固定装置略去)。
2 3 1 2
(1)A装置中制取NH 的化学方程式是________________________________。
3
(2)甲、乙分别是________(填字母)。
a.浓硫酸、碱石灰b.碱石灰、碱石灰
c.碱石灰、无水氯化钙
d.五氧化二磷、五氧化二磷
(3)若NO 能够被NH 还原,预期C装置中能观察到的现象是____________________。
2 3
(4)此实验装置存在一个明显的缺陷是_____________________。
探究Ⅱ:探究NO、O 混合气体的喷泉实验。
2 2
(5)请在G装置中的虚线上描出导管实线图。
(6)G装置中浓硫酸有三种作用:混合NO、O;干燥NO、O;_________________。
2 2 2 2
(7)将G装置上面的圆底烧瓶收集满气体进行喷泉实验,若混合气体全部被吸收,则所得溶液物质的量浓度
为________ mol·L-1(保留两位有效数字)。
【解析】(1)将浓氨水滴入生石灰中,发生反应:CaO+NH·HO===NH↑+Ca(OH),放出氨气。(2)干燥氨
3 2 3 2
只能用碱石灰,干燥二氧化氮可用五氧化二磷固体或无水氯化钙。(3)如果能反应,消耗NO 使装置中混合气体
2
颜色变浅。(4)由于NH、NO 均能污染空气,所以与它们相关的实验均应有尾气处理装置。(5)O、NO 密度比
3 2 2 2
空气大,故应进气管短,出气管长。(6)观察气泡的生成速率,控制混合气体的比例。(7)烧瓶中充满溶液,反应
4NO+O+2HO===4HNO 恰好发生,HNO 的物质的量是恰好完全反应的NO 和O(体积比为4∶1)总物质的
2 2 2 3 3 2 2
量的,溶液体积等于恰好完全反应的NO 和O 的总体积,设烧瓶中恰好完全反应的NO 和O 的总体积为V,则
2 2 2 2
溶液浓度为=× mol·L-1,即c(HNO)≈0.036 mol·L-1。
3
【答案】(1)CaO+NH·HO===NH↑+Ca(OH)
3 2 3 2
(2)c
(3)混合气体颜色变浅
(4)缺少尾气处理装置
(5) (进气管短,出气管长)
(6)观察气泡的生成速率,控制混合气体的比例
(7)0.036
19.(15分)探究NaSO 固体的热分解产物。查阅资料:
2 3
①4NaSO=====NaS+3NaSO。
2 3 2 2 4
②NaS能与S反应生成NaS,NaS 与酸反应生成S和HS。
2 2 x 2 x 2
③BaS易溶于水。
隔绝空气条件下,加热无水NaSO 固体得到黄色固体A,过程中未检测到气体生成。黄色固体A加水得到
2 3
浊液,放置得无色溶液B。(1)检验分解产物NaS:取少量溶液B,向其中滴加CuSO 溶液,产生黑色沉淀,证实有S2-。反应的离子
2 4
方程式是______________________。
(2)检验分解产物NaSO:取少量溶液B,滴加BaCl 溶液,产生白色沉淀,加入盐酸,沉淀增多(经检验该
2 4 2
沉淀含S),同时产生有臭鸡蛋气味的气体(HS),由于沉淀增多对检验造成干扰,另取少量溶液B,加入足量盐
2
酸,离心沉降(固液分离)后,____________________(填操作和现象),可证实分解产物中含有SO。
(3)探究(2)中S的来源。
来源1:固体A中有未分解的NaSO,在酸性条件下与NaS反应生成S。
2 3 2
来源2:溶液B中有NaS,加酸反应生成S。
2 x
针对来源1进行如图实验:
①实验可证实来源1不成立。实验证据是____________________________。
②不能用盐酸代替硫酸的原因是_____________________________________________________。
③写出来源2产生S的反应的离子方程式:____________________________。
(4)实验证明NaSO 固体热分解有NaS,NaSO 和S产生。运用氧化还原反应规律分析产物中S产生的合理
2 3 2 2 4
性:_______________________________________________________________________。
【解析】(1)NaS和CuSO 溶液反应生成硫化铜和硫酸钠,反应的离子方程式是S2-+Cu2+===CuS↓。
2 4
(2)根据题干资料:NaS能与S反应生成NaS,NaS 与酸反应生成S和HS,取少量溶液B,滴加BaCl 溶
2 2 x 2 x 2 2
液,产生白色沉淀,加入盐酸,沉淀增多(经检验该沉淀含S),同时产生有臭鸡蛋气味的气体(HS),说明B溶液
2
中含有NaS,NaS 与酸反应生成S和HS,由于沉淀增多对检验造成干扰,另取少量溶液B,加入足量盐酸,
2 x 2 x 2
离心沉降(固液分离)后,滴加BaCl 溶液,产生白色沉淀,可证实分解产物中含有SO。
2
(3)①实验可证实来源1不成立。根据来源1分析,溶液2为HSO,向溶液2中加入少量KMnO 溶液,
2 3 4
HSO 具有还原性,酸性条件下KMnO 具有强氧化性,二者混合后发生氧化还原反应,KMnO 溶液应该褪色,
2 3 4 4
但得到的溶液仍为紫色,说明溶液B中不含NaSO,即来源1不成立。
2 3
②不能用盐酸代替硫酸的原因是盐酸中Cl元素为-1价,是Cl元素的最低价,具有还原性,会与KMnO
4
溶液发生氧化还原反应,使KMnO 溶液褪色,干扰实验现象和实验结论;③来源2认为溶液B中有NaS,加
4 2 x
酸反应生成S,反应离子方程式:S+2H+===HS↑+(x-1)S↓。
2
(4)根据已知资料:4NaSO=====NaS+3NaSO,亚硫酸钠中硫元素化合价为+4价,硫酸钠中硫元素化合
2 3 2 2 4
价为+6价,硫化钠中硫元素化合价为-2价,根据反应可知NaSO 发生歧化反应,其中的S元素化合价既可升
2 3
高也可降低,能从+4价降为-2价,也应该可以从+4价降到0价生成硫单质。
【答案】(1)S2-+Cu2+===CuS↓
(2)滴加BaCl 溶液,产生白色沉淀
2
(3)①向溶液2中加入KMnO 溶液,溶液没有褪色
4
②盐酸中Cl元素化合价为-1价,是Cl元素的最低价,具有还原性,会与KMnO 溶液发生氧化还原反应,
4
使KMnO 溶液褪色,干扰实验现象和实验结论 ③S+2H+===HS↑+(x-1)S↓
4 2(4)根据反应4NaSO=====NaS+3NaSO 可知,NaSO 发生歧化反应,其中的S元素化合价既可升高也可
2 3 2 2 4 2 3
降低,能从+4价降为-2价,也应该可以从+4价降到0价生成硫单质