文档内容
专题突破 02 物质的化学计量
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项是符合题目要求的)
1.1.某兴趣小组需要500 mL 2 mol·L-1的HSO 溶液,若用质量分数为98%、密度为1.84 g· mL-1的浓硫
2 4
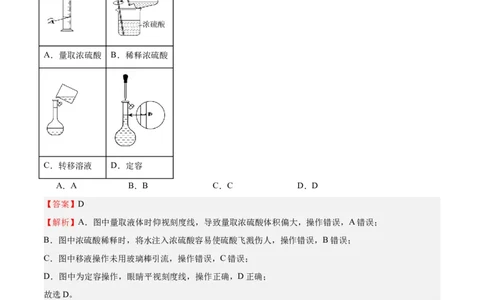
酸配制该溶液。下列操作正确的是
A.量取浓硫酸 B.稀释浓硫酸
C.转移溶液 D.定容
A.A B.B C.C D.D
【答案】D
【解析】A.图中量取液体时仰视刻度线,导致量取浓硫酸体积偏大,操作错误,A错误;
B.图中浓硫酸稀释时,将水注入浓硫酸容易使硫酸飞溅伤人,操作错误,B错误;
C.图中移液操作未用玻璃棒引流,操作错误,C错误;
D.图中为定容操作,眼睛平视刻度线,操作正确,D正确;
故选D。
2.阿伏加德罗常数的值用N 表示。下列说法中正确的是
A
A.常温常压下,11.2 L SO 含有的氧原子数大于N
2 A
B.0.1 mol Na O 和NaO的混合物中含有的离子总数等于0.3N
2 2 2 A
C.10 g质量分数为98%的浓硫酸含有的氢原子数为0.2N
A
D.一定条件下,Ca与O 反应生成7.2 g CaO ,转移电子的个数为0.4N
2 2 A
【答案】B
【解析】A.常温常压下,V >22.4 L∙mol-1,则11.2 L SO 的物质的量小于0.5 mol,含有的氧原子数小于
m 2N ,A不正确;
A
B.1个NaO 由2个Na+和1个 构成,1个NaO由2个Na+和1个O2-构成,则0.1 mol Na O 和NaO的
2 2 2 2 2 2
混合物中含有的离子总数等于0.3N ,B正确;
A
C.10 g质量分数为98%的浓硫酸中含有HSO 的物质的量为 =0.1 mol,则HSO 中含有的氢原
2 4 2 4
子数为0.2N ,另外,浓硫酸中存在水,水中也含有氢原子,所以10 g质量分数为98%的浓硫酸中含有的
A
氢原子数大于0.2N ,C不正确;
A
D.一定条件下,Ca与O 反应生成CaO,可建立关系式:CaO~2 e-,7.2 g CaO 的物质的量为0.1 mol,则
2 2 2 2
转移电子的个数为0.2N ,D不正确;
A
故选B。
3.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.12 g NaHSO 晶体中含有0.2 N 个阳离子
4 A
B.1.12 L C H 所含极性共价键的数目为0.2N
2 4 A
C.1L 0.05mol/L的NH HSO 溶液中NH 的微粒数小于0.05N
4 4 A
D.0.1 mol CH COOH与足量乙醇充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 A
【答案】C
【解析】A.n(NaHSO)= =0.1 mol,由于NaHSO 晶体没有电离,阳离子仅有Na+,故NaHSO
4 4 4
中含有0.1N 个阳离子,A错误;
A
B.没有指明标准状况,不能计算1.12 L C H 物质的量,B错误;
2 4
C.1L 0.05mol/L的NH HSO 物质的量为1L ×0.05mol/L=0.05mol,由于铵根离子要水解, 的微粒数小
4 4
于0.05N ,C正确;
A
D.乙酸和乙醇的酯化反应是可逆反应,则0.1 mol CH COOH与足量CHCHOH充分反应生成的
3 3 2
CHCOOCH CH 分子数目小于0.1N ,D错误;
3 2 3 A
故选C。
4.现有硫酸钠溶液V mL,它的密度是ρ g· mL-1,其中钠离子的质量分数是a%,则下列有关该溶液的说法
错误的是。
A.溶质的质量分数是 %B.溶液的物质的量浓度是 mol·L-1
C.溶质和溶剂的物质的量之比是9a∶(2300-71a)
D.硫酸根离子的质量分数是
【答案】D
【解析】A.现有硫酸钠溶液V mL,它的密度是ρ g· mL-1,溶液质量是ρV g,其中钠离子的质量分数是
a%,则钠离子的质量是ρVa% g,物质的量是 mol,所以硫酸钠的物质的量是 mol,质量是
mol×142 g· mol-1= g,则溶质的质量分数是 ×100%= %,A正确;
B.溶液的物质的量浓度是 = mol·L-1,B正确;
C.溶质和溶剂的物质的量之比是 mol∶ =9a∶(2300-71a),C正确;
D.硫酸根离子的质量分数是 ×100%= %,D错误;
故选D。
5.设 为阿伏加德罗常数的值。下列说法正确的是
A.0.1mol乙烷中含非极性键的数目为0.2N
A
B.1L 溶液中 数目等于
C.标准状况下,11.2L HF含有的电子数等于
D.18g重水(D O)中含有的中子数为9N
2 A
【答案】D
【解析】A.0.1mol乙烷中含非极性键的数目为0.1N ,故A错误;
A
B. 溶液中 会水解,所以数目小于N ,故B错误;
AC.标准状况下,HF是液态,不可以用气体摩尔体积,故C错误;
D.18g重水(DO)物质的量为0.9mol,其中所含中子数为9N ,故D正确;
2 A
答案选D。
6.超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为 ,
为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D.该反应中每转移 电子生成 的数目为
【答案】A
【解析】A. (即 ) 中 键的数目为 ,A正确;
B. 由 和 构成, 晶体中离子的数目为 ,B错误;
C. 在水溶液中会发生水解: ,故 溶液中 的数目小于
,C错误;
D.该反应中部分氧元素化合价由 价升至0价,部分氧元素化合价由 价降至 价,则每
参加反应转移 电子,每转移 电子生成 的数目为 ,D错误;
故选A。
7.硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是A.标准状况下, 中原子总数为
B. 溶液中, 数目为
C.反应①每消耗 ,生成物中硫原子数目为
D.反应②每生成 还原产物,转移电子数目为
【答案】D
【解析】A.标况下SO 为气体,11.2L SO 为0.5mol,其含有1.5mol原子,原子数为1.5N ,A错误;
2 2 A
B.SO 为弱酸阴离子,其在水中易发生水解,因此,100mL 0.1mol L-1 Na SO 溶液中SO 数目小于
2 3
0.01N ,B错误;
A
C.反应①的方程式为SO +2H S=3S +2H O,反应中每生成3mol S消耗2mol HS,3.4g HS为0.1mol,
2 2 2 2 2
故可以生成0.15mol S,生成的原子数目为0.15N ,C错误;
A
D.反应②的离子方程式为3S+6OH-=SO +2S2-+3H O,反应的还原产物为S2-,每生成2mol S2-共转移4mol
2
电子,因此,每生成1mol S2-,转移2mol电子,数目为2N ,D正确;
A
故答案选D。
8.常温常压下,电化学还原制氨气的总反应方程式: 。设 为阿伏加德罗
常数的值,下列说法正确的是
A. 水中含有的孤电子对数为
B.每生成 , 得到的电子数为
C. 氨水中,含有的 分子数少于
D.每消耗 (标准状况下) ,生成 键的数目为
【答案】D
【解析】A.HO分子中O原子上孤电子对数为2,0.5mol H O的含有的孤电子对数为1N ,故A错误;
2 2 A
B.该反应中N 中N元素化合价由0价下降到-3价,34gNH 的物质的量为2mol,每产生2molNH ,得到
2 3 36mol电子,数目为6N ,故B错误;
A
C.氨水的体积未知,无法计算NH ⋅HO的分子数,故C错误;
3 2
D.22.4L(标准状况下)N 的物质的量为1mol,由方程式可知,消耗1molN ,产生的NH 为2mol,N−H键
2 2 3
的数目为6N ,故D正确;
A
故选D。
9.CuCl 和SO 发生氧化还原反应,离子方程式为 。设
2 2
为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol氯化铜固体含有的Cu2+数目小于
B.标准状况下,2.24 L H O中心O原子的价层电子对数为0.4
2
C.1 mol SO 溶于水,电离出的H+数目为2
2
D.生成1 mol CuCl,转移的电子数为
【答案】D
【解析】A.固体中不存在水解,1 mol氯化铜固体含有的Cu2+数目为 ,故A项错误;
B.标准状况下,水不是气体,不能用标准状况下的气体摩尔体积计算,故B项错误;
C.亚硫酸是弱酸,1 mol H SO 电离出的氢离子数目小于2 ,故C项错误;
2 3
D.根据方程式可知,生成1 mol CuCl,转移的电子数为 ,故D项正确;
故本题选D。
10.如图所示为硫元素在自然界中的循环示意图。设 为阿伏加德罗常数的值,下列说法正确的是A.0.1 硫酸溶液含有的 数目约为0.2
B.2.24L 中含有的孤电子对数目为0.2
C.2mol 与1mol 充分反应后转移的电子数目为2
D.1mol 晶体中所含阳离子数目为
【答案】D
【解析】A.溶液只有浓度没有体积,不能求 的数目,A错误;
B.没有给出气体所处的状况,无法计算HS的物质的量,B错误;
2
C. 与 不能完全反应,反应后转移的电子数不等于 ,C错误;
D. 晶体中含有1mol钠离子和1mol硫酸氢根离子,则晶体中含有的阳离子总数为 ,D正
确;
故答案选D。
11.下列描述正确的是
A.14g14C中质子数目为8N
A
B.0.1mol/L1L酸性重铬酸钾溶液中 数目为0.1N
A
C.1mol石墨晶体中形成六元环的数目为0.5N
A
D.142gPO ( )中含9N 个σ键
4 10 A
【答案】C
【解析】A.14g14C物质的量为1mol,14C的质子数为6,即14g14C中质子数目为6N ,故A错误;
A
B.酸性重铬酸钾溶液中存在 ,则0.1mol/L1L酸性重铬酸钾溶液中 数
目小于0.1N ,故B错误;
A
C.一个六元环中平均含有2个碳原子,1mol石墨晶体中形成六元环的数目为0.5N ,故C正确;
AD.142gPO 物质的量为:0.5mol,1个PO ( )中含16个σ键,即142gPO (
4 10 4 10 4 10
)中含8N 个σ键,故D错误;
A
故选C。
12.亚铁氰化钾 俗名黄血盐,在烧制青花瓷时用于绘画。一种制备方法为
。设 为阿伏加德罗常数的值,下列说法正确的是
A. 分子中含有 键的数目为
B.配合物 的中心离子为
C.每生成 时,反应过程中转移电子的数目为
D. 中碳原子的价层电子对数目为4
【答案】B
【解析】A. 物质的量为1mol,其结构式为:H—C≡N,含有 键的数目为2 ,A错误;
B.配合物 的中心离子为 ,中心离子的配体为 ,B正确;
C.该反应中,铁由0价升高到+2价,两个+1价氢变为0价,则转移2个电子,故每生成 时,反
应过程中转移电子数目为 ,C错误;
D. 中碳原子的价层电子对数目为 ,无孤电子对,D错误;答案选B。
13. 代表阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2L苯中含有的原子数目为
B.0.3 的 溶液中含有 的数目为
C.用石灰乳完全吸收2mol 时,转移电子的数目是
D.在常温常压下,44g 与 混合物气体中所含的原子数目一定为
【答案】D
【解析】A.标准状况下,苯为非气态,不能用气体摩尔体积计算物质的量,A错误;
B.溶液体积未知,无法计算物质的量,B错误;
C.用石灰乳完全吸收2mol 时,反应为 ,关系式为:
,可知转移电子的数目是 ,C错误;
D.在常温常压下,44g 与 混合物,两者摩尔质量相同,因此混合气体的物质的量为1mol,所以
气体中所含的原子数目一定为 ,D正确;
故答案选D。
14.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.25℃,101kPa下,22.4L氮气中的共用电子对数目为3N
A
B.2.0L1.0mol·L−1NH Cl溶液中,NH 的数目为2N
4 A
C.0.3mol葡萄糖完全燃烧,生成CO 的数目为1.8N
2 A
D.质量比为2:1的SO 和O 充分反应生成SO 小于2N
2 2 3 A
【答案】C
【解析】A.25℃,101kPa不是标准状况,不能用气体摩尔体积计算,故A项错误;
B.NH Cl溶液中,强酸弱碱盐, 发生水解, 的数目小于2N ,故B项错误;
4 AC.根据葡萄糖完全燃烧方程式可知,1mol葡萄糖彻底氧化为6mol二氧化碳,则0.3mol葡萄糖完全燃烧,
生成CO 的数目为1.8N ,故C项正确;
2 A
D.质量比为2:1的SO 和O 充分反应生成SO 可能大于2N ,可能等于2N ,可能小于2N ,不能确定,
2 2 3 A A A
故D项错误;
故本题选C。
二、非选择题(本题包括4小题,共58分)
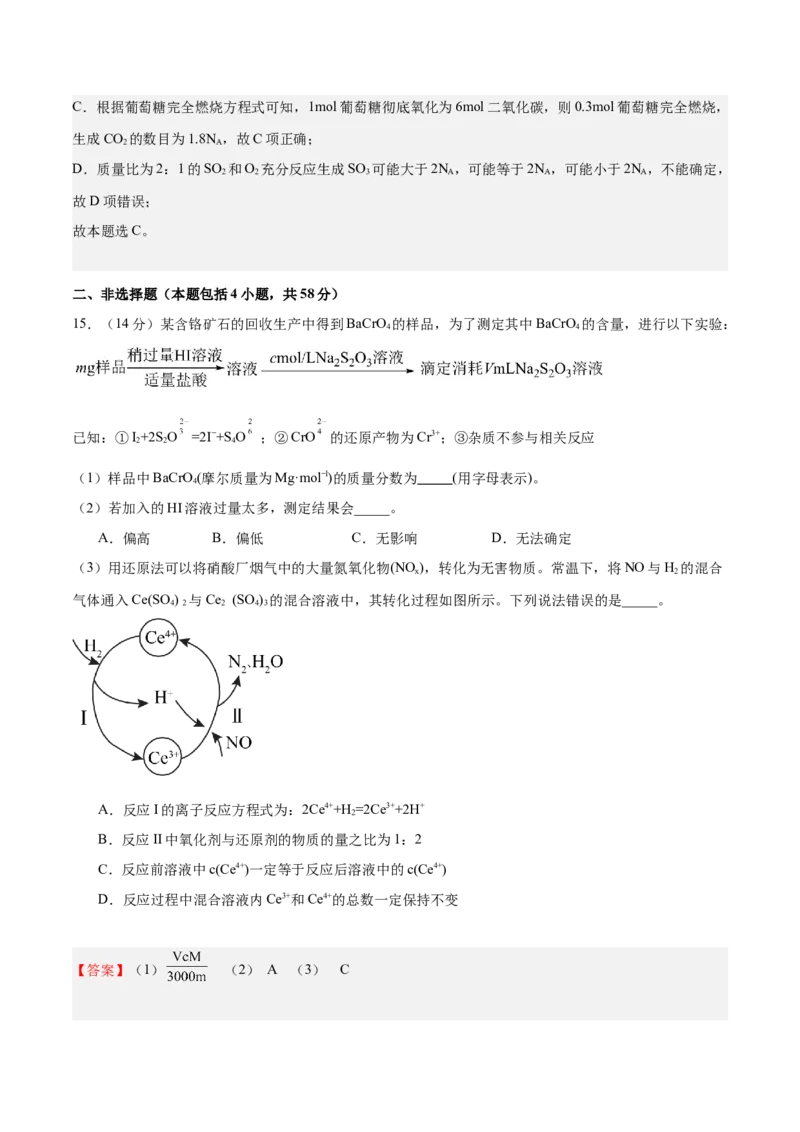
15.(14分)某含铬矿石的回收生产中得到BaCrO 的样品,为了测定其中BaCrO 的含量,进行以下实验:
4 4
已知:①I+2S O =2I−+S O ;②CrO 的还原产物为Cr3+;③杂质不参与相关反应
2 2 4
(1)样品中BaCrO(摩尔质量为Mg·mol−l)的质量分数为 (用字母表示)。
4
(2)若加入的HI溶液过量太多,测定结果会_____。
A.偏高 B.偏低 C.无影响 D.无法确定
(3)用还原法可以将硝酸厂烟气中的大量氮氧化物(NO ),转化为无害物质。常温下,将NO与H 的混合
x 2
气体通入Ce(SO) 与Ce (SO ) 的混合溶液中,其转化过程如图所示。下列说法错误的是_____。
4 2 2 4 3
A.反应I的离子反应方程式为:2Ce4++H =2Ce3++2H+
2
B.反应II中氧化剂与还原剂的物质的量之比为1:2
C.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
D.反应过程中混合溶液内Ce3+和Ce4+的总数一定保持不变
【答案】(1) (2) A (3) C【解析】(1)加入HI发生反应:2BaCrO+6I-+16H+=2Ba2++2Cr3++3I +8H O,结合I+ =2I-+ ,
4 2 2 2
消耗NaSO 的物质的量为:V×10-3L×cmol/L=cV×10-3mol,由关系式:2BaCrO~3I~6 ,可知
2 2 3 4 2
n(BaCrO)= ×cV×10-3mol,BaCrO 质量为 ×cV×10-3mol×Mg·mol−l= ,样品中BaCrO 质量分数
4 4 4
为 ;
(2)若加入的HI溶液过量太多,部分HI被空气氧化为I,或 在酸性条件下反应生成为S与二氧化硫,
2
均导致消耗NaSO 的量偏大,测定结果会偏高,故选A;
2 2 3
(3)A.根据图示可知反应Ⅰ的离子方程式为:2Ce4++H =2Ce3++2H+,A项正确;
2
B.反应Ⅱ的反应物为Ce3+、H+、NO,生成物为Ce4+、N、HO,根据得失电子守恒、电荷守恒及质量
2 2
守恒,可得反应的离子方程式为:4Ce3++4H++2NO=4Ce4++N +2H O,NO是氧化剂,Ce3+是还原剂,故氧
2 2
化剂与还原剂的物质的量之比为2∶4=1∶2,B项正确;
C.反应前后溶液中n(Ce4+)不变,但由于反应后溶液中水的物质的量增大,所以反应后溶液中c(Ce4+)减小,
C项错误;
D.由于反应前后各种元素的原子个数相等,根据Ce元素守恒可知,反应过程中混合溶液内Ce3+和Ce4+
的总数不变,D项正确;
故选C。
16.(14分)铁的化合物在生产生活中有极其重要的作用。请回答下列有关问题:
(1)七水硫酸亚铁可作木材防火剂、磁性材料等。某课外活动小组配制100mL 溶液,需要
用到的主要玻璃仪器有玻璃棒、烧杯、胶头滴管、量筒和 ;需要称取 g 晶体;
一天后,小组同学发现溶液变为黄色,其原因是 ;为了防止溶液变黄,在配制时需要加入少量
; 在高温和隔绝空气条件下可以分解生成 ,其化学方程式为 。
(2)高铁酸钾( )是一种新型高效的水处理剂, 中铁元素的化合价为 ;用 溶液、KClO溶液和KOH溶液反应可生成 ,其离子方程式为 。
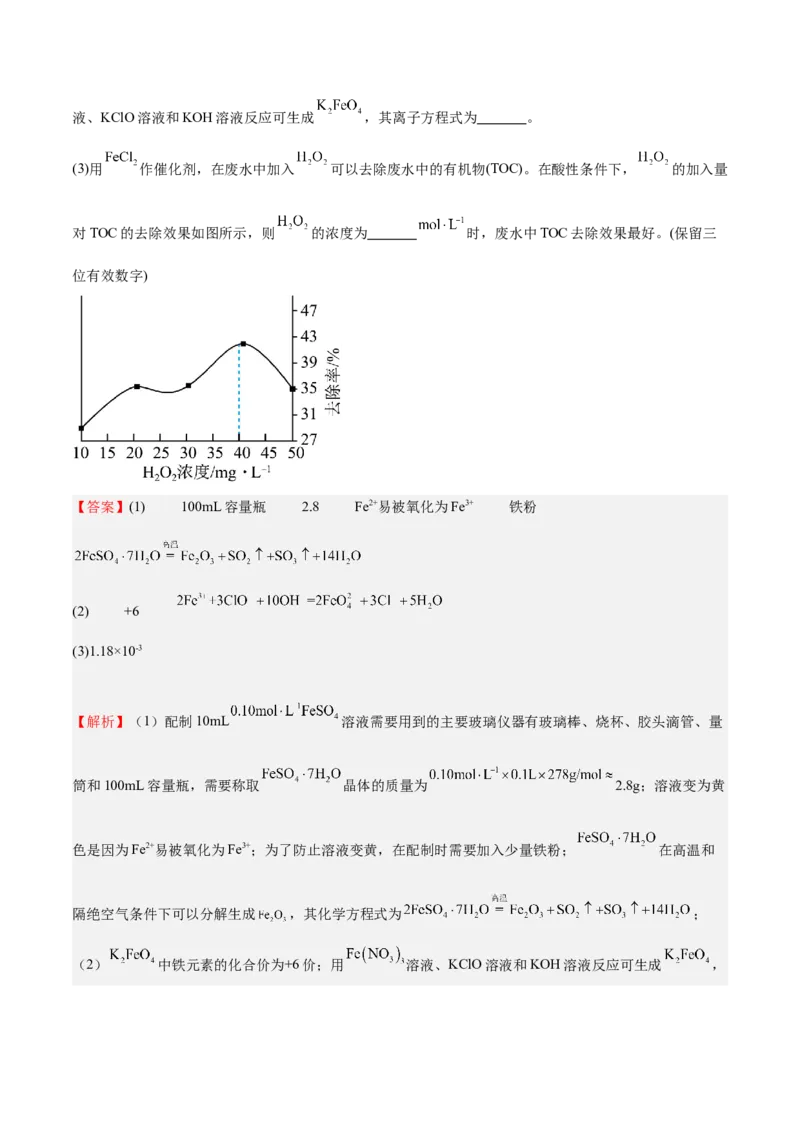
(3)用 作催化剂,在废水中加入 可以去除废水中的有机物(TOC)。在酸性条件下, 的加入量
对TOC的去除效果如图所示,则 的浓度为 时,废水中TOC去除效果最好。(保留三
位有效数字)
【答案】(1) 100mL容量瓶 2.8 Fe2+易被氧化为Fe3+ 铁粉
(2) +6
(3)1.18×10-3
【解析】(1)配制10mL 溶液需要用到的主要玻璃仪器有玻璃棒、烧杯、胶头滴管、量
筒和100mL容量瓶,需要称取 晶体的质量为 2.8g;溶液变为黄
色是因为Fe2+易被氧化为Fe3+;为了防止溶液变黄,在配制时需要加入少量铁粉; 在高温和
隔绝空气条件下可以分解生成 ,其化学方程式为 ;
(2) 中铁元素的化合价为+6价;用 溶液、KClO溶液和KOH溶液反应可生成 ,其离子方程式为 ;
(3)根据图中可知 的浓度为40mg/L时废水中TOC去除效果最好,即浓度为 ≈1.18×10-
3mol/L。
17.(15分)钠及其化合物在生产和生活中有广泛的应用。回答下列问题:
(1)金属钠非常活泼,在实验室中要把钠保存在 中,以隔绝空气。
(2)汽车安全气囊内装有NaN 、Fe O 和NaHCO 等物质。
3 2 3 3
①当汽车发生严重碰撞时,引发NaN 分解并放出大量的热:2NaN 2Na+3N↑。若安全气囊内有
3 3 2
65gNaN ,其完全分解所释放的N 在标准状况下的体积为 L。
3 2
②产生的Na立即与Fe O 发生置换反应生成NaO,反应的化学方程式为 。
2 3 2
③NaHCO 可用作冷却剂,吸收体系释放的热量。NaHCO 作冷却剂的工作原理是 (用化学方程式
3 3
表示)。
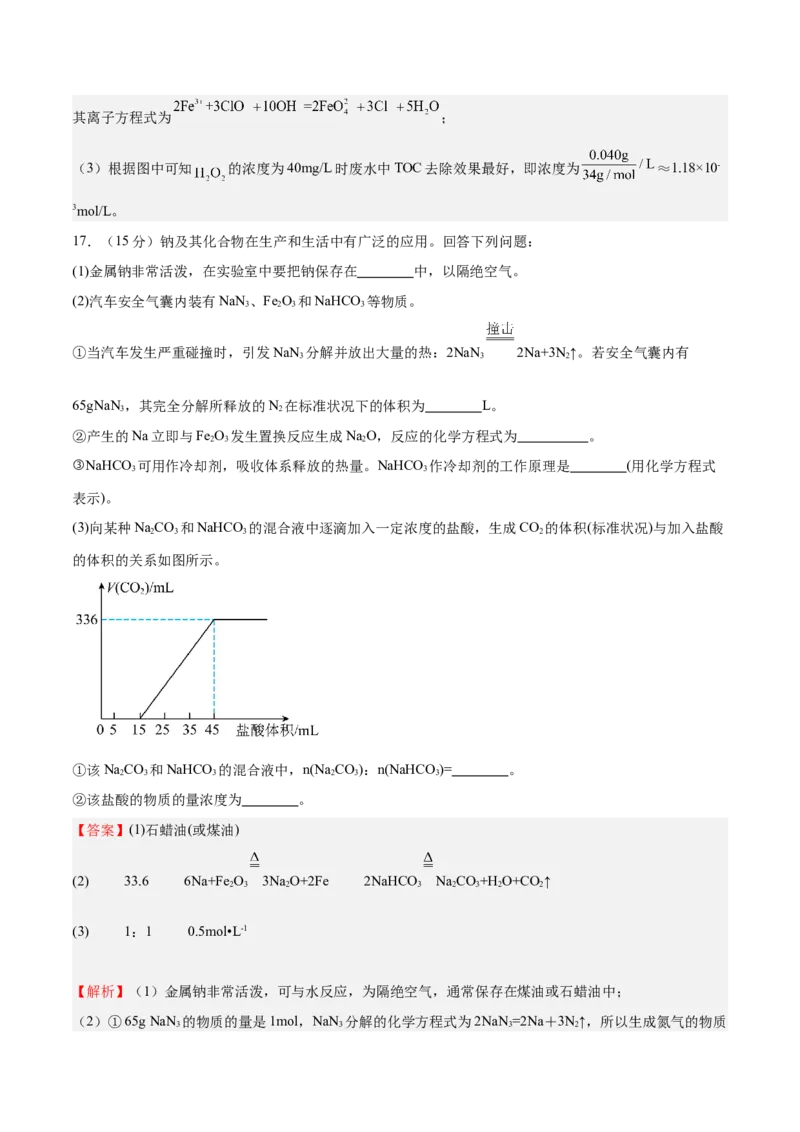
(3)向某种NaCO 和NaHCO 的混合液中逐滴加入一定浓度的盐酸,生成CO 的体积(标准状况)与加入盐酸
2 3 3 2
的体积的关系如图所示。
①该NaCO 和NaHCO 的混合液中,n(Na CO):n(NaHCO )= 。
2 3 3 2 3 3
②该盐酸的物质的量浓度为 。
【答案】(1)石蜡油(或煤油)
(2) 33.6 6Na+Fe O 3NaO+2Fe 2NaHCO NaCO+H O+CO↑
2 3 2 3 2 3 2 2
(3) 1:1 0.5mol•L-1
【解析】(1)金属钠非常活泼,可与水反应,为隔绝空气,通常保存在煤油或石蜡油中;
(2)①65g NaN 的物质的量是1mol,NaN 分解的化学方程式为2NaN =2Na+3N↑,所以生成氮气的物质
3 3 3 2的量是1.5mol,在标况下的体积为1.5mol×22.4L/mol=33.6L;
②置换反应的反应物和产物均为单质和化合物,Na与Fe O 发生置换反应生成NaO和Fe,反应的化学方
2 3 2
程式为:6Na+Fe O 3NaO+2Fe;
2 3 2
③NaHCO 不稳定,受热易分解,生成稳定的NaCO、HO、CO,反应方程式为2NaHCO
3 2 3 2 2 3
NaCO+H O+CO↑;
2 3 2 2
(3)①设盐酸浓度为cmol/L,加入15mL盐酸发生反应NaCO+HCl=NaCl+NaHCO ,则
2 3 3
n(Na CO)=n(HCl)=cmol/L×0.015L=0.015cmol。加入45mL盐酸时,根据碳元素守恒可知:
2 3
n(NaHCO )=(0.045-0.015)c mol-0.015c mol=0.015c mol,故该样品中NaCO 和NaHCO 的质量之比=0.015c
3 2 3 3
mol:0.015c mol=1:1;
②加入15mL~45mL盐酸,消耗盐酸体积=45mL-15mL=30mL,生成336mL二氧化碳,其物质的量为
=0.015mol,则根据方程式NaHCO +HCl=NaCl+CO ↑+H O可知n(HCl)=0.015mol,则c(HCl)=
3 2 2
=0.5mol/L。
18.(15分)回答下列问题:
(1)NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
2
步骤一:利用NaClO 在硫酸作用下与SO 反应生成ClO 和一种酸式盐
3 2 2
步骤二:将ClO 在NaOH溶液中与HO 反应即可生成NaClO
2 2 2 2
①NaClO 中Cl的化合价为 。
2
②写出步骤一中生成ClO 的化学方程式 。
2
③步骤二反应中,氧化剂与还原剂的物质的量之比为 ,该反应中氧化产物是 。
(2)NaClO 溶液可同时吸收含有SO 、NO的烟气。反应温度为323K,NaClO 溶液浓度为5×10-3mol/L。在
2 2 2
碱性环境中,反应一段时间后溶液中离子浓度的分析结果如表。
离子 SO SO NO NO Cl-
c/(mol/L) 8.35×10-4 6.87×10-6 1.5×10-4 1.2×10-6 3.4×10-3
脱硫过程中SO 主要转化为 (填离子符号);脱硝过程NO主要转化为 (填离子符号),脱硝
2过程主要反应的离子方程式为 。
(3)NaClO 可以促使氨转化为氮肥,含氮量是衡量肥效的指标之一,常见氮肥:CO(NH)(尿素)、NH NO
2 2 2 4 3
和(NH )SO 。等物质的量NH NO 和(NH )SO 的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状
4 2 4 4 3 4 2 4
况下),固体混合物质量为 g。
【答案】(1) +3 2NaClO +SO+H SO =2NaHSO +2ClO 2:1 O
3 2 2 4 4 2 2
(2) SO NO 3ClO +4NO+4OH-=4NO +3Cl-+2H O
2
(3)31.8
【解析】(1)①NaClO 中Na元素为+1价,O元素为-2价,根据正负化合价的代数和为0,氯元素的化合
2
价为+3价;
②NaClO 在硫酸作用下与SO 反应生成ClO 和一种酸式盐,根据质量守恒可知,酸式盐为NaHSO,反应
3 2 2 4
中氯元素化合价由+5变为+4、硫元素化合价由+4变为+6,根据电子守恒可知,反应为
2NaClO+SO+H SO =2NaHSO +2ClO ;
3 2 2 4 4 2
③步骤二将ClO 在NaOH溶液中与HO 反应即可生成NaClO,反应中氯元素化合价由+4变为+3,ClO 为
2 2 2 2 2
氧化剂,过氧化氢中氧元素化合价由-1变为0,为还原剂,发生氧化反应生成氧化产物氧气,根据电子守
恒可知 ,氧化剂与还原剂的物质的量之比为2:1,该反应中氧化产物是O;
2
(2)由表可知,脱硫过程中SO 主要转化为SO ;脱硝过程NO主要转化为NO ,脱硝过程主要反应为
2
次氯酸根离子和NO在碱性环境中生成硝酸根离子和氯离子,离子方程式为3ClO +4NO+4OH-=4NO
+3Cl-+2H O;
2
(3)等物质的量NH NO 和(NH )SO 的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,为
4 3 4 2 4
0.45mol),则等物质的量NH NO 和(NH )SO 均为0.45mol÷3=0.15mol,固体混合物质量为
4 3 4 2 4
。