文档内容
专题突破卷 04 非金属及其化合物
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2024·陕西安康联考)我国是历史悠久的文明古国。下列相关叙述有误的是( )
A.毛笔(主要为动物毛发)和墨(含炭墨烟和动物胶)中都含有蛋白质
B.西汉南越王墓出土的铜钱表面有绿色斑点,其主要成分是碱式碳酸铜
C.“凡火药,硫为纯阳,硝为纯阴”,纯阴指化合价降低,利用硝酸钾的氧化性
D.《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”,描述的是升华和凝华过程
2.(2024·江苏无锡调研)含氯物质在生产生活中应用广泛。下列有关物质的性质与用途具有对应关系的是(
)
A.Cl 能溶于水,可用于工业制盐酸
2
B.ClO 有强氧化性,可用于水体消毒
2
C.HClO溶液显酸性,可用作漂白剂
D.NH Cl受热易分解,可用作氮肥
4
3.有关硫及其化合物的说法合理的是( )
A.可用酒精洗刷做过硫黄性质实验的试管
B.SO 具有很强的还原性,在化学反应中只能作还原剂
2
C.浓硫酸具有强氧化性,常温下与铜反应可制取SO
2
D.1 mol硫与其他物质完全反应,转移的电子数不一定是2 mol
4.(2022·江苏卷)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A. 自然固氮、人工固氮都是将N 转化为NH
2 3
B. 侯氏制碱法以H O、NH 、CO 、NaCl为原料制备NaHCO 和NH Cl
2 3 2 3 4
C. 工业上通过NH 催化氧化等反应过程生产HNO
3 3
D. 多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
5.下列溶液中能够区别SO 和CO 的是( )
2 2
①石灰水 ②HS溶液 ③酸性KMnO 溶液
2 4
④氯水 ⑤品红溶液
A.①②③ B.②③④
C.除①以外 D.①②③④⑤
6.(2024·江苏扬州中学高三下考前模拟)含氮化合物在生产生活中具有重要应用,下列说法不正确的是
A.工业上常以向饱和氨的食盐水中通入CO 制备NaHCO 和NH Cl
2 3 4
B.实验室可将苯和浓硝酸混合共热制备硝基苯
C.浓硝酸和浓盐酸以体积比1∶3组成的混合物可用于溶解金、铂等金属D.尿素是一种中性肥料,可水解成碳酸铵或碳酸氢铵,缓慢释放氨气被作物吸收
7.某研究性学习小组利用下列装置制备漂白粉,下列说法不正确的是( )
A.装置④中的X试剂为NaOH溶液
B.装置②中饱和食盐水的作用是除去Cl 中的HCl
2
C.装置③中的石灰乳可以用石灰水代替
D.制备漂白粉的反应是放热反应,温度较高时有副反应发生,可以将装置③放在冷水中
8.某化学小组用如图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )
A.E处棉花球变成黄色,说明Cl 的氧化性比Br 强
2 2
B.F处棉花球变成蓝色,说明Br 的氧化性比I 强
2 2
C.E处发生反应的离子方程式为Cl+2Br-===2Cl-+Br
2 2
D.G装置中NaOH溶液与Cl 反应的离子方程式为2OH-+Cl===ClO-+Cl-+HO
2 2 2
9.部分含硫物质的分类与相应硫元素的化合价关系如图所示。下列说法正确的是( )
A.S与过量的O 充分反应可以生成Z
2
B.Y可使紫红色的酸性高锰酸钾溶液褪色,说明其有漂白性
C.密闭体系中,Y与足量的O 充分反应可使Y完全转化为Z
2
D.P的一种结晶水合物俗称芒硝,是一种常见的中药
10.中学化学常见物质之间,在一定条件下可以发生如图所示的转化关系(部分反应中的HO没有标明),
2
其中A、B、C中均含有同一种元素。下列说法错误的是( )
A.若A、B、C、D都是中学化学常见气体,则D可能是氧气
B.若A是气体,D是常见金属,则反应①、②、③都是化合反应C.若B物质具有两性,A、B、C、D都是化合物,则C溶液可能呈酸性,也可能呈碱性
D.若①、②、③反应都是氧化还原反应,则A、B、C中含有的同一种元素一定呈现三种不同化合价
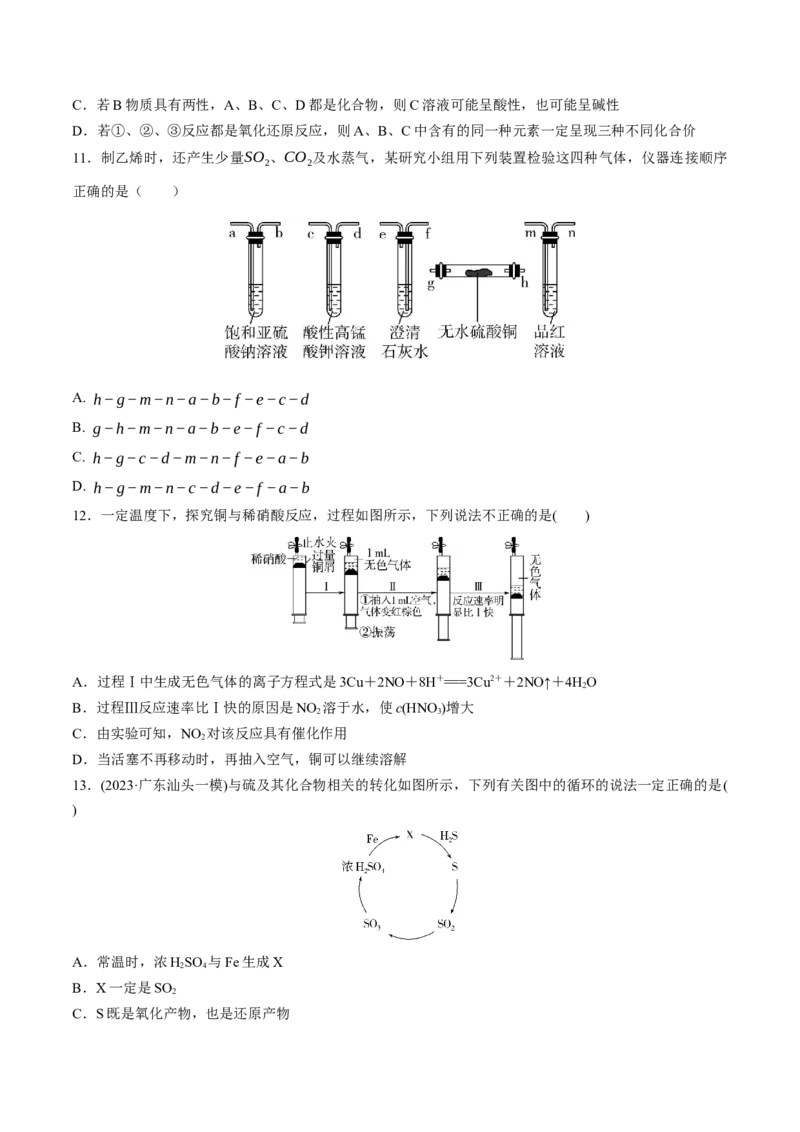
11.制乙烯时,还产生少量SO 、CO 及水蒸气,某研究小组用下列装置检验这四种气体,仪器连接顺序
2 2
正确的是( )
A. h−g−m−n−a−b−f −e−c−d
B. g−h−m−n−a−b−e−f −c−d
C. h−g−c−d−m−n−f −e−a−b
D. h−g−m−n−c−d−e−f −a−b
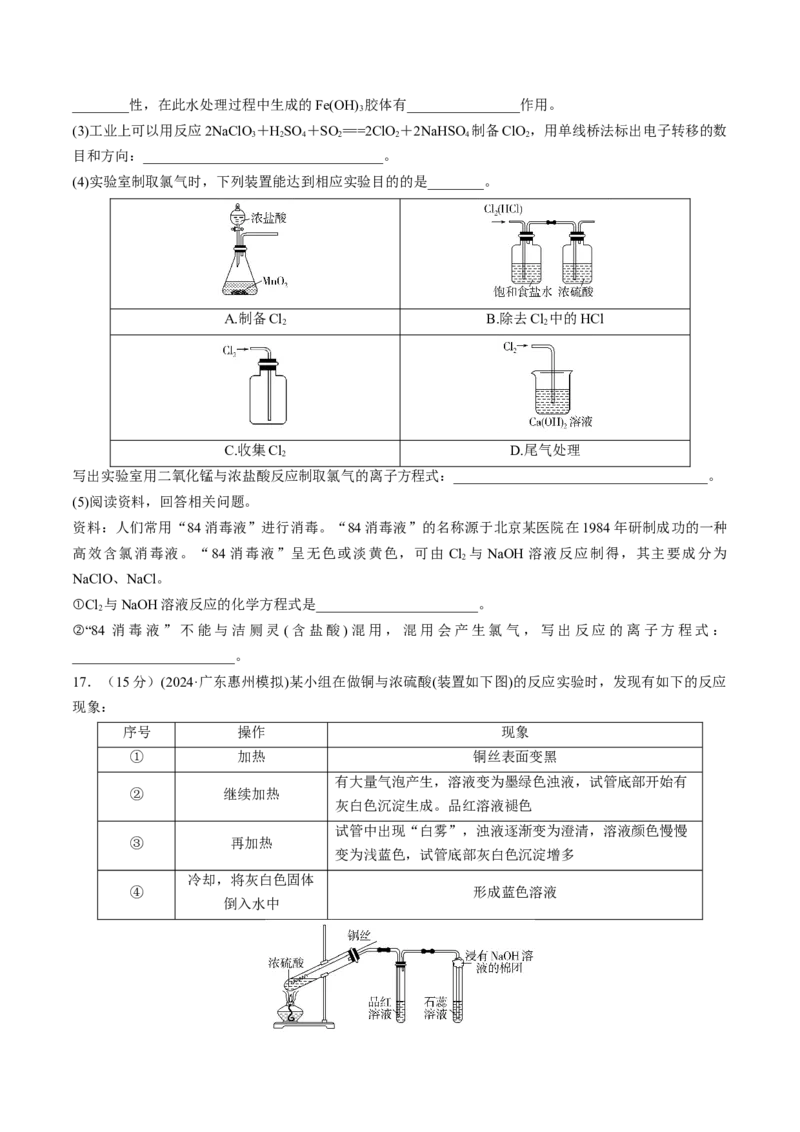
12.一定温度下,探究铜与稀硝酸反应,过程如图所示,下列说法不正确的是( )
A.过程Ⅰ中生成无色气体的离子方程式是3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
B.过程Ⅲ反应速率比Ⅰ快的原因是NO 溶于水,使c(HNO)增大
2 3
C.由实验可知,NO 对该反应具有催化作用
2
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
13.(2023·广东汕头一模)与硫及其化合物相关的转化如图所示,下列有关图中的循环的说法一定正确的是(
)
A.常温时,浓HSO 与Fe生成X
2 4
B.X一定是SO
2
C.S既是氧化产物,也是还原产物D.工业生产中,用98.3%的浓硫酸吸收SO
3
14.(2023·湖南邵阳二模)某化学兴趣小组设计一种从硫矿石(主要成分为硫黄及少量FeS)中提取硫黄的方
2
法如下:
查阅资料:S的熔点为115.2 ℃;CS 的沸点为46.2 ℃。
2
下列说法错误的是( )
A.单质硫是分子晶体
B.过程①中CS 可用乙醇代替
2
C.过程③的目的是使CS 挥发,同时使硫从水中析出
2
D.将趁热过滤所得滤渣煅烧:4FeS +11O=====2Fe O +8SO ,反应中每生成1 mol SO ,转移电子的物
2 2 2 3 2 2
质的量为5.5 mol
15.(2023·北京西城区二模)探究Cu与Fe(NO ) 溶液的反应,进行如下实验。
3 3
实验①:向 10 mL 0.2 mol/L Fe(NO ) 溶液(pH≈1)中加入0.1 g Cu粉,振荡后静置,取上层清液,滴加
3 3
K[Fe(CN) ]溶液,有蓝色沉淀产生。6 h后,溶液由棕黄色变为蓝绿色。实验过程中未见有气泡产生,溶
3 6
液的pH几乎不变。
实验②:在密闭容器中向10 mL 0.6 mol/L HNO 溶液中加入0.1 g Cu粉,10 h后溶液变为淡蓝色。
3
实验③:在密闭容器中向10 mL 0.6 mol/L HNO 溶液中分别加入0.1 g Cu粉和0.1 g FeSO 固体,0.5 h后溶
3 4
液变黄,3 h后溶液变为黄绿色。下列说法不正确的是( )
A.实验①中发生了反应:Cu+2Fe3+===Cu2++2Fe2+
B.推测实验②的离子方程式是3Cu+2NO+8H+===3Cu2++2NO↑+4HO
2
C.对比实验①和②,①中溶解Cu的主要是NO(H+)
D.对比实验②和③,HNO 与Fe2+反应的速率大于HNO 与Cu反应的速率
3 3
二、非选择题(本题包括4小题,共55分)
16.(10分)分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物
质的性质进行解释和预测。以下为含氯物质的“价-类”二维图,请回答下列问题:
(1)a物质的化学式为________,b属于________(填“酸性”或“碱性”)氧化物。
(2)用ClO消毒水时,ClO还可将水中的Fe2+转化为Fe3+,Fe3+再水解生成Fe(OH) 胶体,说明ClO具有
2 2 3 2________性,在此水处理过程中生成的Fe(OH) 胶体有________________作用。
3
(3)工业上可以用反应2NaClO+HSO +SO ===2ClO +2NaHSO 制备ClO ,用单线桥法标出电子转移的数
3 2 4 2 2 4 2
目和方向:__________________________________。
(4)实验室制取氯气时,下列装置能达到相应实验目的的是________。
A.制备Cl B.除去Cl 中的HCl
2 2
C.收集Cl D.尾气处理
2
写出实验室用二氧化锰与浓盐酸反应制取氯气的离子方程式:____________________________________。
(5)阅读资料,回答相关问题。
资料:人们常用“84消毒液”进行消毒。“84消毒液”的名称源于北京某医院在1984年研制成功的一种
高效含氯消毒液。“84 消毒液”呈无色或淡黄色,可由 Cl 与 NaOH 溶液反应制得,其主要成分为
2
NaClO、NaCl。
①Cl 与NaOH溶液反应的化学方程式是_______________________。
2
②“84 消毒液”不能与洁厕灵(含盐酸)混用,混用会产生氯气,写出反应的离子方程式:
_______________________。
17.(15分)(2024·广东惠州模拟)某小组在做铜与浓硫酸(装置如下图)的反应实验时,发现有如下的反应
现象:
序号 操作 现象
① 加热 铜丝表面变黑
有大量气泡产生,溶液变为墨绿色浊液,试管底部开始有
② 继续加热
灰白色沉淀生成。品红溶液褪色
试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色慢慢
③ 再加热
变为浅蓝色,试管底部灰白色沉淀增多
冷却,将灰白色固体
④ 形成蓝色溶液
倒入水中【查阅资料】 聚四氯乙烯受热分解产生氯化氢,[CuCl ]2-呈黄色,[Cu(H O) ]2+呈蓝色,两者混合则成绿
4 2 4
色,铜的化合物中CuO、CuS、Cu S都为黑色,其中CuO溶于盐酸;CuS、Cu S不溶于稀盐酸,但溶于浓
2 2
盐酸。
(1)铜丝与浓硫酸反应的化学方程式为_____________________。
(2) 试 管 中 品 红 溶 液 褪 色 , 体 现 SO 的 ________ 性 , 浸 有 NaOH 溶 液 的 棉 团 作 用 是
2
__________________________________。
(3)甲组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
操作 现象
直接取其铜丝(表面有聚四氯乙烯薄膜)做实
Ⅰ组 溶液变成墨绿色
验
Ⅱ组 实验前,先将铜丝进行灼烧处理 溶液变蓝
请解释形成墨绿色的原因:_________________________。
(4)乙组同学对白雾的成分进行探究,经检验为 HSO ,请设计实验证明该白雾为硫酸:
2 4
_____________________________________。
(5)丙组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有________。滴加
适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,生成呈黄色的[CuCl ]2-n(n=1~4)。写出CuS
n
与浓盐酸反应的离子方程式:________________________________________。
(6)某工厂将热空气通入稀硫酸中来溶解废铜屑制备CuSO ·5H O,消耗含铜元素80%的废铜屑240 kg固体
4 2
时,得到500 kg产品,产率为________(结果保留两位小数)。
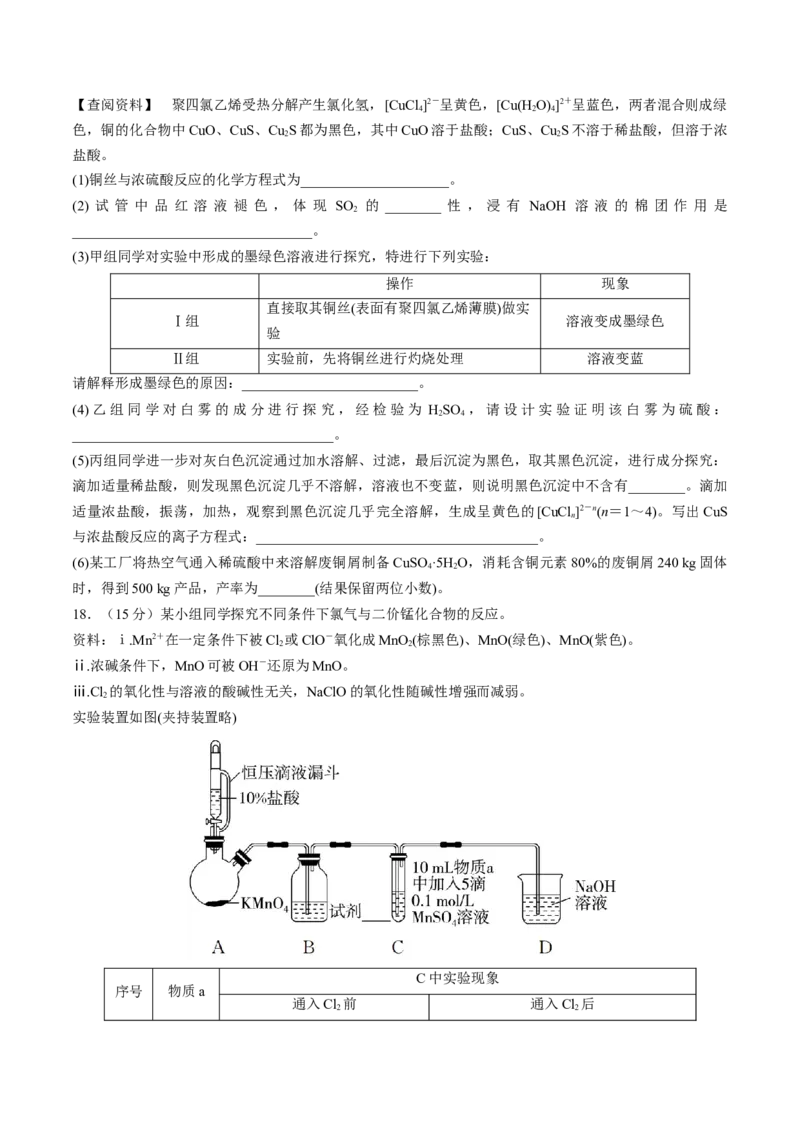
18.(15分)某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:ⅰ.Mn2+在一定条件下被Cl 或ClO-氧化成MnO (棕黑色)、MnO(绿色)、MnO(紫色)。
2 2
ⅱ.浓碱条件下,MnO可被OH-还原为MnO。
ⅲ.Cl 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
2
实验装置如图(夹持装置略)
C中实验现象
序号 物质a
通入Cl 前 通入Cl 后
2 2Ⅰ 水 得到无色溶液 产生棕黑色沉淀,且放置后不发生变化
5%
产生白色沉淀,在空气中缓慢 棕黑色沉淀增多,放置后溶液变为紫
Ⅱ NaOH
变成棕黑色沉淀 色,仍有沉淀
溶液
40%
产生白色沉淀,在空气中缓慢 棕黑色沉淀增多,放置后溶液变为紫
Ⅲ NaOH
变成棕黑色沉淀 色,仍有沉淀
溶液
(1)B中试剂是________。
(2)通入Cl 前,Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为__________。
2
(3)对比实验Ⅰ、Ⅱ通入Cl 后的实验现象,对于二价锰化合物还原性的认识是_____________。
2
(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl 导致溶液的碱性减弱。
2
原因二:可能是氧化剂过量,氧化剂将MnO氧化为MnO。
①化学方程式表示可能导致溶液碱性减弱的原因:_______,
但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的1 mL悬浊液,加入4 mL 40% NaOH溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。
溶液紫色变为绿色的离子方程式为_____,溶液绿色缓慢加深,原因是MnO 被________(填“化学式”)氧
2
化,可证明Ⅲ的悬浊液中氧化剂过量。
③取Ⅱ中放置后的1 mL悬浊液,加入4 mL水,溶液紫色缓慢加深,发生的反应是_____________(写离子
方程式)。
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:______。
19.(15分)(2024·江苏南京第二次模拟)高效氧化剂亚氯酸钠(NaClO)常用于烟气脱硝(NO)和废水脱
2 x
除氨氮。
(1) NaClO 的制备。一种制备NaClO 的过程可表示如下:
2 2
① “反应2”的化学方程式为________。
② “反应1”的产物ClO 经净化后常作为饮用水消毒剂替代传统的Cl ,从消毒后饮用水水质和消毒效率
2 2
(单位质量消毒剂被还原时得电子数)的角度考虑,用ClO 替代Cl 的原因是________。
2 2
(2) NaClO 溶液对烟气脱硝。
2
① 酸性条件下,Fe3+可催化溶液中的NaClO 产生氧化性更强的ClO 气体,总反应可表示为5ClO+4H+
2 2
4ClO +Cl-+2HO。 请补充完整过程Ⅱ的离子方程式:
2 2Ⅰ. Fe3++ClO===FeClO;
Ⅱ. ________________________________________;
Ⅲ. 5Fe2++ClO +4H+===5Fe3++Cl-+2HO。
2 2
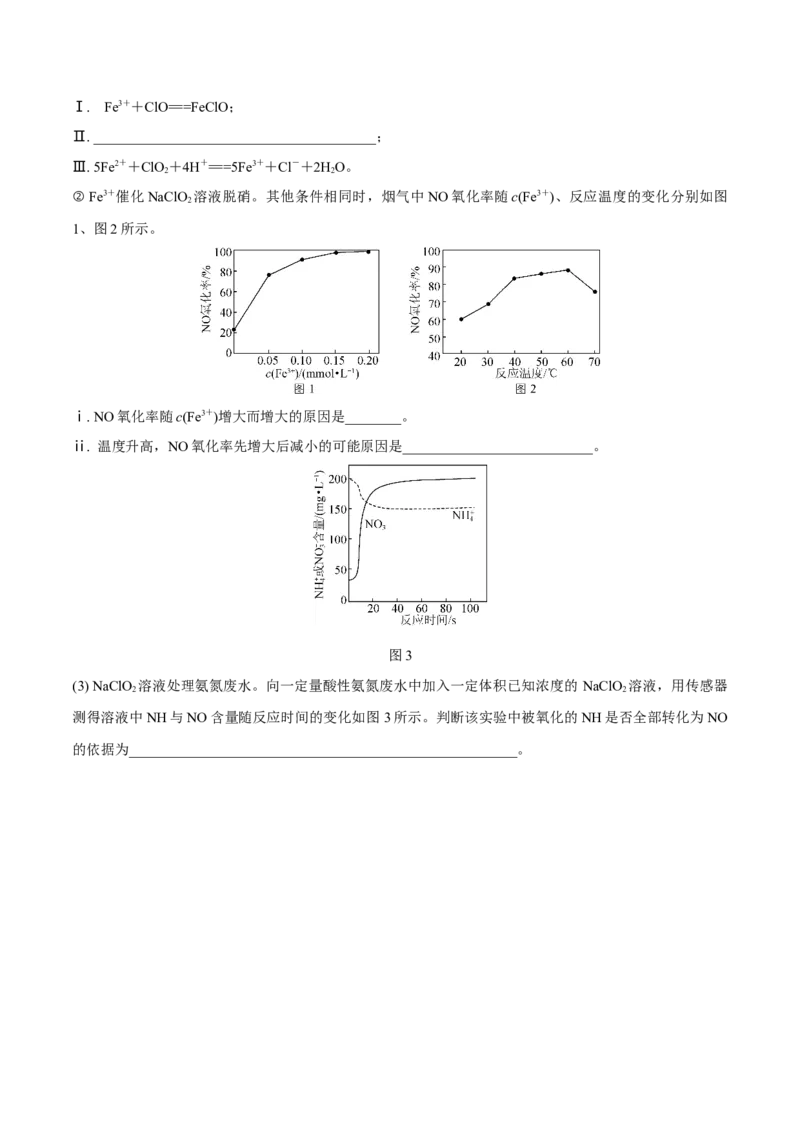
② Fe3+催化NaClO 溶液脱硝。其他条件相同时,烟气中NO氧化率随c(Fe3+)、反应温度的变化分别如图
2
1、图2所示。
ⅰ. NO氧化率随c(Fe3+)增大而增大的原因是________。
ⅱ. 温度升高,NO氧化率先增大后减小的可能原因是___________________________。
图3
(3) NaClO 溶液处理氨氮废水。向一定量酸性氨氮废水中加入一定体积已知浓度的 NaClO 溶液,用传感器
2 2
测得溶液中NH与NO含量随反应时间的变化如图3所示。判断该实验中被氧化的NH是否全部转化为NO
的依据为_______________________________________________________。