文档内容
专题突破卷 05 物质结构与性质 元素周期律(一)
——原子结构与性质 元素周期表、元素周期律
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列有关化学元素周期表的说法正确的是( )
A.元素周期表共有18列,所以共有18个族
B.ⅦA族元素的非金属性自上而下依次减弱
C.主族元素均呈现与其族数相同的最高化合价
D.第二周期主族元素的原子半径自左向右依次增大
【答案】B
【解析】元素周期表共有18纵列,也就是共有18列,但只有16个族,A错误;由于同一主族的元素从上
到下,原子半径逐渐增大,原子获得电子的能力逐渐减弱,所以Ⅶ A族元素的非金属性自上而下依次减弱,
B正确;主族元素一般呈现与其族数相同的最高化合价,O、F非金属性强,O没有与族序数相等的最高正
化合价,F没有正价,C错误;第二周期主族元素的原子半径自左向右依次减小,D错误。
2.一定量的锎(Cf)在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是( )
A.Cf原子中,中子数为154
B.Cf原子中,质子数为98
C.Cf原子中,核外电子数为98
D.锎元素的相对原子质量为252
【答案】D
【解析】Cf是锎元素的一种核素,其质量数为252,核外电子数=核内质子数=98,中子数=252-98=
154。锎元素的相对原子质量等于锎元素的各种同位素的相对原子质量与它们的原子个数百分比之积的和,
而不等于某一核素的质量数,故D错误。
3. (2024·陕西西安模拟)下列化学用语表述错误的是( )
A.中子数为18的氯原子:Cl
B.基态N原子的价层电子排布图:
C.基态 Cu原子的电子排布式:
29
1s22s22p63s23p63d94s2
D.标准状况下,2.24 L C H 和N 的混合气体中含有的π键数为0.2N
2 2 2 A
1
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司【答案】C
【解析】原子序数为17,中子数为18的氯原子的质量数为35,可表示为Cl,A项正确;N原子位于第二
周期第ⅤA族,基态N原子的价层电子排布图为 ,B项正确;铜元素位于第四周
期第ⅠB族,基态 Cu原子的电子排布式为1s22s22p63s23p63d103s1,C项错误;标准状况下,2.24 L C H 和
29 2 2
N 的混合气体的物质的量为0.1 mol,1个C H 分子中含有2个π键,1个N 分子中含有2个π键,所以0.1
2 2 2 2
mol的混合气体中含有的π键数为0.2 N ,D项正确。
A
4. (2024·天津南开区一模)科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复
轰击含95个质子的镅元素,结果4次成功制成4个第115号元素的原子,这4个原子在生成数微秒后衰变
成第113号元素。第115号元素的一种核素为X。下列有关叙述错误的是( )
A.核素X的质量数为288
B.核素X的质量数与中子数之差为173
C.113号元素属于金属元素
D.155号元素的最高正化合价是+5
【答案】B
【解析】核素X的质量数为288,A项正确;核素X的中子数为288-115=173,核素X的质量数与中子
数之差为115,B项错误;113号元素与B元素位于同一主族,该族元素从Al开始为金属元素,所以113
号元素属于金属元素,C项正确;115号元素位于第ⅤA族,最外层有5个电子,最高正化合价为+5,D
项正确。
5.下列说法正确的是( )
①在氮原子中,质子数为7,而中子数不一定为7 ②O与O是不同的核素,因此分别由这两种原子构成
的分子化学性质不同 ③O 和O 互为同素异形体 ④Ti和Ti的质量数不同,属于两种元素 ⑤实际存在
2 3
的H、H、H、H+和H ,是氢的五种核素 ⑥H 、H 、H 互为同位素 ⑦稀土元素Sm与Sm 是同一种核
2 2 2 2
素
A.①⑥ B.②④ C.⑤⑦ D.①③
【答案】D
【解析】②中的原子核外电子数相同,所以其分子化学性质相同,错误;④、⑦分别属于同一种元素的不
同核素,错误;⑤H、H、H是氢元素的三种核素,H+与H 不是氢元素的核素;同位素研究对象是原子与
2
原子之间,⑥均为分子,错误。
6.某元素的一种同位素X原子的质量数为A,它与2H原子组成2H X分子,此分子含N个中子,在a g
m
2H X中所含电子的物质的量是( )
m
A.(A-N+m)mol
B.(A-N)mol
C.(A-N+m)mol
2
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司D.(A-N+2m)mol
【答案】D
【解析】2H X分子含N个中子,则X原子含中子数为(N-m),由X原子的质量数为A可知,质子数为(A
m
-N+m),则每个2H X分子含有质子数为(A-N+2m),a g 2H X的物质的量为 mol,因中性分子中质子
m m
数等于电子数,则a g 2H X中所含电子的物质的量是(A-N+2m)mol,故选D。
m
7.(2024·河北保定模拟)医学界通过用放射性14C来标记C ,发现C 的一种羧酸衍生物在特定条件下可通
60 60
过DNA来杀死细胞,从而抑制艾滋病(AIDS)。下列说法正确的是( )
A.C 与石墨互为同位素
60
B.14C的中子数与质子数相差2
C.常温下,C 易溶于氯化钠溶液
60
D.基态碳原子L层的轨道表示式为
【答案】B
【解析】C 与石墨互为同素异形体,A项错误;14C质子数为6,质量数为14,中子数为8,则中子数与质
60
子数相差2,B项正确;常温下,C 不溶于氯化钠溶液,C项错误;基态碳原子L层的轨道表示式为
60
,D项错误。
8.(2024·江苏苏锡常镇四市调研一)一种超导材料中含 Cu、P、O、S等元素。下列说法正确的是
( )
A. 原子半径:r(P)>r(S)>r(O) B. 第一电离能:I(O)>I(S)>I(P)
1 1 1
C. 酸性强弱:HPO >H SO D. 基态Cu原子3d轨道上有9个电子
3 4 2 4
【答案】A
【解析】同主族从上到下,原子半径逐渐增大,同周期从左到右,原子半径逐渐减小,则原子半径:
r(P)>r(S)>r(O),A正确;同一周期主族元素从左向右第一电离能呈增大的趋势,但第Ⅱ A族、第ⅤA族比
同周期相邻元素的都大,则第一电离能:I(P)>I(S),B错误;元素非金属性越强,其最高价氧化物对应水
1 1
化物的酸性越强,非金属性:P<S,酸性:HPO <HSO ,C 错误;基态 Cu 原子的价电子排布为
3 4 2 4
3d104s1,D错误。
9.(2024·广东佛山一模)现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p2、②1s22s22p63s23p3、
③1s22s22p3、④1s22s22p5。下列有关比较正确的是( )
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
3
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司C.电负性:①>②>③>④
D.最高正化合价:④>③>②>①
【答案】A
【解析】根据四种元素的基态原子的电子排布式可知①是Si、②是P、③是N、④是F。同主族元素从上
到下第一电离能逐渐降低,同周期元素从左到右第一电离能呈增大趋势,因此第一电离能F>N>P>Si,A
项正确;同主族元素从上向下,原子半径逐渐增大,同周期元素从左向右,原子半径逐渐减小,因此原子
半径:Si>P>N>F,B项错误;元素的非金属性越强,则电负性越大,同周期主族元素从左到右电负性逐渐
增强,同主族元素从上到下电负性逐渐减弱,因此电负性:F>N >P >Si,C项错误;元素的最高正化合价
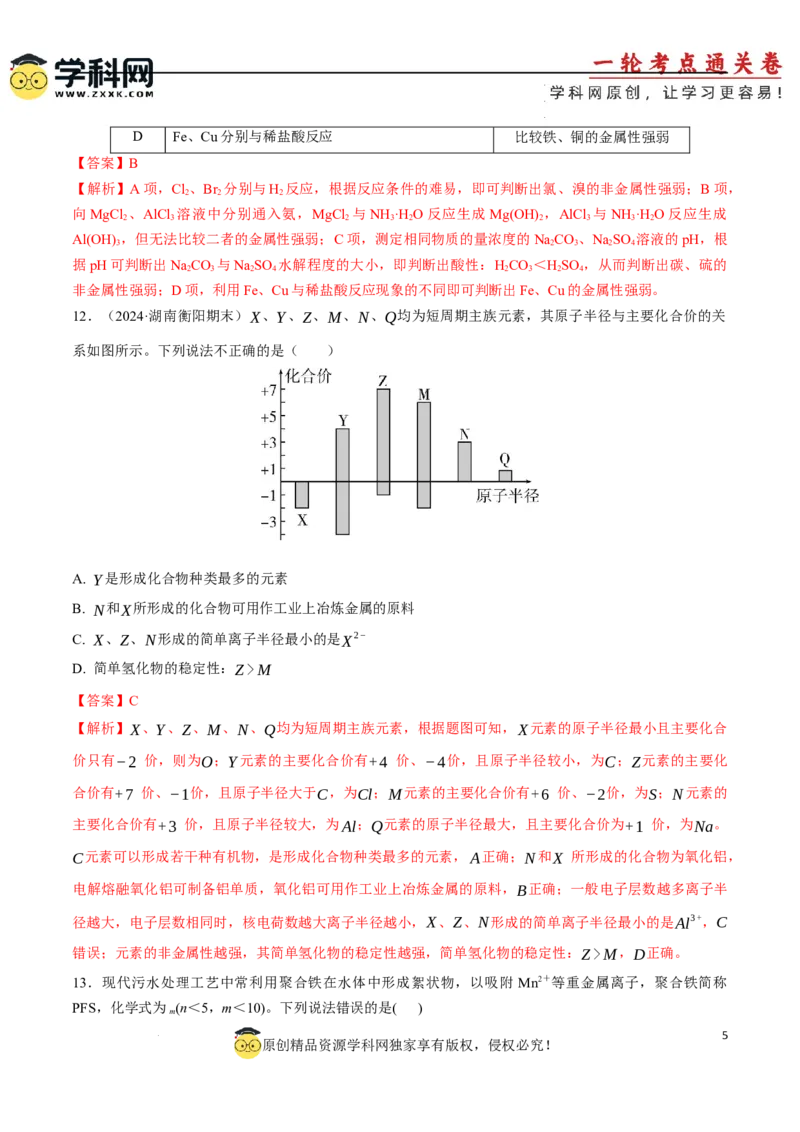
等于其族序数,F无正化合价,因此最高正化合价:SiM
【答案】C
【解析】X、Y、Z、M、N、Q均为短周期主族元素,根据题图可知,X元素的原子半径最小且主要化合
价只有−2 价,则为O;Y元素的主要化合价有+4 价、−4价,且原子半径较小,为C;Z元素的主要化
合价有+7 价、−1价,且原子半径大于C,为Cl;M元素的主要化合价有+6 价、−2价,为S;N元素的
主要化合价有+3 价,且原子半径较大,为Al;Q元素的原子半径最大,且主要化合价为+1 价,为Na。
C元素可以形成若干种有机物,是形成化合物种类最多的元素,A正确;N和X 所形成的化合物为氧化铝,
电解熔融氧化铝可制备铝单质,氧化铝可用作工业上冶炼金属的原料,B正确;一般电子层数越多离子半
径越大,电子层数相同时,核电荷数越大离子半径越小,X、Z、N形成的简单离子半径最小的是Al3+,C
错误;元素的非金属性越强,其简单氢化物的稳定性越强,简单氢化物的稳定性:Z>M,D正确。
13.现代污水处理工艺中常利用聚合铁在水体中形成絮状物,以吸附 Mn2+等重金属离子,聚合铁简称
PFS,化学式为 (n<5,m<10)。下列说法错误的是( )
m
5
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司元素 Mn Fe
I 717 762
1
电离能/
I 1 509 1 561
2
(kJ·mol-1)
I 3 248 2 957
3
A.PFS中铁元素显+3价
B.基态铁原子的价层电子排布式为3d64s2
C.由FeSO 溶液制备PFS需经过氧化、水解和聚合等过程
4
D.由表可知再失去一个电子时,气态Fe2+比气态Mn2+难
【答案】D
【解析】根据化合物中各元素的化合价代数和为0,铁元素的化合价为+3价,故A正确;铁的核外电子
排布式为1s22s22p63s23p63d64s2,所以铁原子的价层电子排布式是 3d64s2,故B正确;硫酸亚铁中铁元素的
化合价是+2价,聚合铁中铁元素的化合价是+3价,铁离子水解生成氢氧化铁,所以由FeSO 溶液制PFS
4
需经过氧化、水解和聚合的过程,故C正确;电离能越大,其失电子越难,所以气态Fe2+再失去一个电子
比气态Mn2+再失去一个电子容易,故D错误。
14.(2023·山东烟台模拟)短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总数
目是其最高能级电子数目的2倍,Y与X能形成一种以如图所示形式存在的阴离子,Z与X的最外层电子数
目相同。下列说法中错误的是( )
A. 原子半径:Y>Z>X B. 简单离子的还原性:Z>W>X
C. 四种元素中,Y的电负性最小 D. 同周期元素中,W的第一电离能最大
【答案】D
【解析】基态X 原子的电子总数目是其最高能级电子数目的 2倍,则X 的基态原子核外电子排布为
1s22s22p4,X为O;根据题给信息结合题给结构,可知Y 可以形成4个共价键,则Y 为Si;Z与X 的
最外层电子数目相同,则Z 为S;根据X、Y、Z、W为短周期主族元素,且原子序数依次增大可知,W
为Cl。同一周期主族元素,从左到右原子半径依次减小,同一主族元素,自上而下原子半径依次增大,原
子半径:Si>S>O,A项正确;元素的非金属性越强,其简单阴离子还原性越弱,非金属性:O>Cl>S,
故简单离子还原性:S2−>Cl−>O2−,B项正确;同一周期从左到右主族元素的电负性递增,同一主族自上
而下元素的电负性递减,故电负性:SiX>Y>Z
B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z
D.氢化物水溶液的酸性:Y>W
【答案】C
【解析】四种短周期主族元素,基态X原子的电子总数是其最高能级电子数的2倍,若X为第二周期元素
原子,则X可能为Be或O,若X为第三周期元素原子,则均不满足题意,Z与X能形成ZX 的淡黄色化
2 2
合物,该淡黄色固体为NaO ,则X为O元素,Z为Na元素;Y与W的最外层电子数相同,则Y为F元
2 2
素,W为Cl元素。同一周期从左向右第一电离能总趋势为逐渐增大,同一主族从上到下第一电离能逐渐
减小,故四种元素中第一电离能从大到小的顺序为F>O>Cl>Na,A错误;单质的氧化性越强,简单离子的
还原性越弱,O、F、Cl三种元素中F 的氧化性最强,O 的氧化性最弱,故简单离子的还原性:O2->Cl-
2 2
>F-,B错误;电子层数越多简单离子半径越大,相同结构的离子,原子序数越大半径越小,故四种元素
中离子半径从大到小的顺序为Cl->O2->F->Na+,C正确;F元素的非金属性强于Cl元素,则形成氢化物
后F原子束缚H原子的能力强于Cl原子,在水溶液中HF不容易发生电离,故HCl的酸性强于HF,D错
误。
二、非选择题(本题包括4小题,共55分)
16.(10分)(1)下列原子或离子的电子排布正确的是________(填标号,下同),违反能量最低原理的是
________,违反洪特规则的是________,违反泡利不相容原理的是________。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:
(2)①氮原子价层电子的轨道表示式为_____。
②Co基态原子核外电子排布式为______。
③Fe3+基态核外电子排布式为______。
【答案】(1)①⑤⑥(1分) ②④(1分) ③(1分) ⑦(1分)
7
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司(2)① (2分)
②1s22s22p63s23p63d74s2(或[Ar]3d74s2) (2分)
③1s22s22p63s23p63d5(或[Ar]3d5) (2分)
【解析】(1)根据核外电子排布规律,②中错误在于电子排完 2s轨道后应排2p轨道而不是3p轨道,正确的
应为1s22s22p6;③中没有遵循洪特规则,价层电子的轨道表示式应为 ;④中忽略了能
量相同的原子轨道在半充满状态时,体系的能量较低,原子较稳定,正确的应为 1s22s22p63s23p63d54s1;⑦
中违反泡利不相容原理,正确的应为 。(2)①氮是7号元素,其价层电子的轨道
表 示 式 为 。 ② Co 的 原 子 序 数 为 27 , 其 基 态 原 子 核 外 电 子 排 布 式 为
1s22s22p63s23p63d74s2或[Ar]3d74s2。③Fe3+基态核外电子排布式为1s22s22p63s23p63d5或[Ar]3d5。
17.(14分)下面给出14种元素的电负性:
元素 Al B Be C Cl F Li
电负性 1.5 2.0 1.5 2.5 3.0 4.0 1.0
元素 Mg N Na O P S Si
电负性 3.0 0.9 3.5 2.1 2.5 1.8
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价
键。
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是________。
(2)通过分析电负性值变化规律,确定镁元素电负性的最小范围是________。
(3)判断下列物质是离子化合物还是共价化合物:
A.LiN B.BeCl
3 2
C.AlCl D.SiC
3
属于离子化合物的是________;
属于共价化合物的是________;
请设计一个实验方案证明上述所得到的结论:________。
(4)在P与Cl组成的化合物中,Cl元素显________(填“正”或“负”)价,理由是________。
【答案】(1)随着原子序数的递增,元素的电负性呈周期性变化(2分)
(2)0.9~1.5(2分)
(3)A(2分) BCD(2分) 测定各物质在熔融状态下能否导电,若导电则为离子化合物,反之则为共价
8
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司化合物(2分)
(4)负(2分) Cl的电负性大于P,Cl对键合电子的吸引能力强(2分)
【解析】(2)根据电负性的递变规律:同周期元素从左到右,元素电负性逐渐变大,同族元素从上到下,元
素电负性逐渐变小,可知在同周期中电负性:Na<Mg<Al,同主族:Be>Mg>Ca,最小范围应为0.9~
1.5。(3)根据已知条件及表中数值:LiN中元素的电负性差值为2.0,大于1.7,形成离子键,为离子化合物;
3
BeCl 、AlCl 、SiC中元素的电负性差值分别为1.5、1.5、0.7,均小于1.7,形成共价键,为共价化合物。
2 3
共价化合物和离子化合物最大的区别在于熔融状态下能否导电。 离子化合物在熔融状态下以离子形式存
在,可以导电,但共价化合物却不能。
18.(12分)现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子
序数依次增大。
A元素原子的核外p电子数比s电子数少3
B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作
切割工具
C元素基态原子p轨道有3个未成对电子
D原子核外所有p轨道全充满或半充满
E在该周期中未成对电子数最多
F能形成红色(或砖红色)的FO和黑色的FO两种氧化物
2
某同学根据上述信息,完成下列各题。
(1)画出A基态原子的核外电子轨道表示式: 。
(2)B 基态原子的核外电子轨道表示式为 该同学所画的轨道表示式违背了
。
(3)D基态原子中能量最高的电子,其电子云在空间有 个伸展方向,呈 形。
(4)写出C原子的电子排布式: ;写出E原子的简化电子排布式: 。
(5)写出F元素原子的价层电子排布式: 。
【答案】(1) (1分)(2)洪特规则 (1分)
(3)3(2分) 哑铃(2分)
(4)1s22s22p3(2分) [Ar]3d54s1(2分)
(5)3d104s1(2分)
【解析】A、B、C、D为短周期主族元素,原子序数依次增大,A元素原子的核外p电子数比s电子数少
3,电子排布式为1s22s22p1,即A为B元素;B元素形成的物质种类繁多,其形成的一种固体单质工业上常
用作切割工具,则B为C元素;C元素基态原子p轨道有3个未成对电子,价层电子排布式为ns2np3,D原
子核外所有p轨道全充满或半充满,结合原子序数可知,价层电子排布式为 3s23p3符合题意,即C为N元
素、D为P元素;E在该周期中未成对电子数最多,又E为第四周期元素,则其价层电子排布式为3d54s1,
9
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司则E为Cr元素;F能形成红色(或砖红色)的FO和黑色的FO两种氧化物,即F为Cu元素。
2
19.(19分)X、Y、Z、W为元素周期表前四周期的元素,原子序数依次增大,X原子核外有6种不同运
动状态的电子,Y原子基态时的2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧
化物可作涂料;W位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
(1)X 在元素周期表中的位置是 ;Y的最高价氧化物对应水化物与Y的最简单气态氢化
物反应的化学方程式 。
(2)X、Y最简单气态氢化物的稳定性:X Y(填“大于”或“小于”)。
(3)Z原子核外电子排布式为 。
(4)W位于元素周期表的 区,与W处于同一周期且最外层电子数相同的元素的基态原子共有
种,这些元素分别为 (填元素符号)。
(5)在发生焰色试验时,W的4s电子会跃迁到4p轨道,写出此激发态W原子的价层电子排布式:
。
(6)与钛位于同一周期且含有相同未成对电子数的过渡元素为 (填元素符号)。
(7)基态砷原子N电子层中的成对电子与单电子的数量比为 。
【答案】(1)第二周期ⅣA族(2分) HNO+NH NH NO (2分)
3 3 4 3
(2)小于(1分)
(3)1s22s22p63s23p63d64s2或[Ar]3d64s2(2分)
(4)ds(2分) 2(2分) K、Cr(2分)
(5)3d104p1(2分)
(6)Ni(2分)
(7)2∶3(2分)
【解析】X原子核外有6种不同运动状态的电子,则是碳元素;Y原子基态时的2p原子轨道上有3个未成
对的电子,是氮元素;Z有多种氧化物,其中一种红棕色氧化物可作涂料是氧化铁,则Z是铁元素;W位
于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态,符合条件的是铜元素。(1)Y的最
高价氧化物对应水化物是硝酸,Y的最简单气态氢化物是氨气,两者反应的化学方程式:HNO +NH
3 3
NH NO 。(2)X、Y最简单气态氢化物分别是甲烷、氨气,非金属性越强气态氢化
4 3
物越稳定,氮元素的非金属性大于碳元素,则它们的稳定性:X小于Y。(4)W是铜元素,位于元素周
期表的ds区,与W处于同一周期且最外层电子数相同的元素的基态原子共有两种:K、Cr。(5)在发生
焰色试验时,W的4s电子会跃迁到4p轨道,此激发态W原子的价层电子排布式:3d104p1。(6)与钛位
于同一周期即是第四周期,钛元素含有的未成对电子数是两个,则同周期且含有相同未成对电子数的过渡
元素为Ni。(7)基态砷原子价层电子排布式是 4s24p3,则N电子层中的成对电子与单电子的数量比为
2∶3。
10
原创精品资源学科网独家享有版权,侵权必究!
学学学科科科网网网(((北北北京京京)))股股股份份份有有有限限限公公公司司司