文档内容
课时检测(五) 离子共存与推断
1.(2023·广东汕头统考一模)离子鉴别能让我们感受微观世界的神奇。下列在透明溶液中能大量
共存的离子组是( )
A.Cu2+、SO、Na+、NO
B.MnO、Cl-、H+、I-
C.Al3+、S2-、NH、CO
D.Fe3+、SCN-、K+、ClO-
2.下列溶液中的离子一定能大量共存的是( )
A.c(ClO-)=1.0 mol·L-1的溶液中:Na+、K+、S2-、SO
B.c(Fe2+)=1 mol·L-1的溶液中:K+、Fe3+、Cl-、SO
C.0.1 mol·L-1 AgNO 溶液中:H+、K+、Cl-、Br-
3
D.c(Fe3+)=1 mol·L-1的溶液中:Na+、NH、SCN-、SO
3.常温下,下列各组离子在给定溶液中可能大量共存的是( )
A.酸性溶液中:Fe2+、Mg2+、SO、NO
B.0.1 mol·L-1 NaClO溶液中:H+、K+、SO、Cl-
C.能使酚酞变红的溶液中:Na+、Al3+、HCO、SO
D.加入铝片产生H 的溶液中:Na+、Ba2+、CH COO-、NO
2 3
4.(2023·湖南邵阳统考三模)常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1AlCl 溶液中:H+、Na+、K+、SO
3
B.0.1 mol·L-1FeCl 溶液中:H+、Al3+、SO、NO
2
C.能使紫色石蕊试纸变蓝的溶液中:Ag+、Fe3+、Br-、SO
D.由水电离产生的c(H+)=10-12mol·L-1的溶液中:NH、SO、HCO、Cl-
5.下列关于溶液中所含离子检验的说法正确的是( )
A.取少量某溶液于试管中,向其中先滴加稀硝酸,再滴加Ba(NO ) 溶液,有白色沉淀生成,说明
3 2
该溶液中含有SO
B.取少量某溶液于试管中,向其中加入少量新制氯水,再滴加KSCN溶液,若溶液变红,说明该
溶液中含有Fe3+
C.取少量某溶液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体,若
红色石蕊试纸变蓝,说明该溶液中含有NH
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶液中含有CO
6.下列各组澄清溶液中离子能大量共存,且滴入X试剂后发生的离子方程式书写正确的是( )
选项 离子组 X试剂 离子方程式
A NH、Fe3+、SO、Br- 过量HS 2Fe3++HS===2Fe2++S↓+2H+
2 2
4H++3Fe2++NO===3Fe3++NO↑
B Fe2+、K+、NO、Cl- 少量HI
+2HO
2
C NH、Fe3+、[Al(OH) ]-、Na+ 过量铜粉 2Fe3++Cu===2Fe2++Cu2+
4
D [Al(OH) 4 ]-、Na +、K+、HCO 少量HCl H++[Al(OH) 4 ]-===Al(OH) 3 ↓+HO
2
7.某白色粉末中可能含CuSO 、Na S、(NH)SO 、KHSO 和NaCl。某化学兴趣小组现取该白色粉
4 2 4 2 3 4
末进行如下实验:
步骤一:取少量白色粉末溶于水,没有气体逸出,得到无色透明溶液①;
步骤二:向溶液①中滴加稀硫酸,产生浅黄色固体和气体X;
步骤三:将气体X通入CuSO 溶液中,产生黑色沉淀。
4
根据上述现象可推知,该白色粉末中一定不含有的是( )
A.CuSO 、NaCl B.CuSO 、KHSO
4 4 4
C.Na S、(NH)SO D.CuSO 、Na S
2 4 2 3 4 2
8.X溶液中含有下表离子中的某5种,且浓度均为0.1 mol·L-1(不考虑水的电离与离子水解)。向
X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确
的是( )
阳离子 阴离子
Na+、Fe3+、Ca2+、Fe2+、Mg2+、Al3+ OH-、NO、HCO、CO、SO、Cl-
A.X溶液中含有2种阳离子和3种阴离子
B.X溶液中不可能含有HCO或CO
C.生成的无色气体是NO
D.根据电荷守恒,原溶液中一定含Ca2+
9.某溶液可能含有Cl-、SO、CO、NH、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,
加热,得到0.02 mol气体(已知:NH+OH-=====NH ↑+HO),同时产生2.14 g 红褐色沉淀;向上述滤
3 2
液中加足量BaCl 溶液,得到4.66 g不溶于盐酸的白色沉淀。由此可知原溶液中( )
2
A.至少存在4种盐
B.Cl-一定存在,且c(Cl-)等于0.4 mol·L-1
C.SO、NH、Fe3+一定存在,Cl-可能不存在
D.CO、Al3+一定不存在,K+可能存在
10.某溶液A中含有H+、Na+、Mg2+、Fe2+、SO、Cl-、CO和HCO中的若干种,取该溶液进行如下
实验(已知Ag SO 微溶于水,可溶于稀HNO ):
2 4 3
①向溶液中滴加几滴Ba(OH) 溶液,过滤,得到不溶于酸的白色沉淀和浅绿色滤液B;
2
②取滤液B,先用稀HNO 酸化,再滴加0.001 mol·L-1 AgNO 溶液,有白色沉淀生成。
3 3
下列说法不正确的是( )
A.溶液A中一定存在的离子是Fe2+、SO、H+和Cl-
B.溶液A中不存在CO和HCO,不能确定Na+、Mg2+的存在
C.第②步生成的白色沉淀中只有AgCl,没有Ag CO 和Ag SO
2 3 2 4
D.原溶液中存在的Fe2+可用KSCN溶液检验
11.某强酸性溶液中可能存在Al3+、Fe2+、NH、Ba2+、Cl-、CO、SO、NO中的若干种。为确定溶液
的组成进行了如下实验:
ⅰ.取100 mL原溶液,加入足量的Ba(NO ) 溶液,有白色沉淀a和无色气体b生成,过滤得滤液
3 2c。
ⅱ.往滤液c中加入足量的NaOH溶液并加热,可得气体d和沉淀e,过滤得滤液f。
ⅲ.取滤液f,通入少量的CO ,有白色沉淀g生成。
2
下列有关判断正确的是( )
A.原溶液中一定没有Ba2+、CO、NO、Cl-
B.原溶液中一定有Fe2+、NH、SO
C.气体b和气体d在一定条件下能反应生成盐
D.沉淀g中一定含有Al(OH) ,可能含有BaCO
3 3
12.某强酸性无色溶液中可能含表中的若干种离子。
阳离子 Mg2+、NH、Ba2+、Al3+、Fe2+
阴离子 SiO、MnO、Cl-、NO、SO
实验Ⅰ:取少量该溶液进行如图实验。
INCLUDEPICTURE "25YLCXHXⅡ1-45.TIF" \* MERGEFORMAT
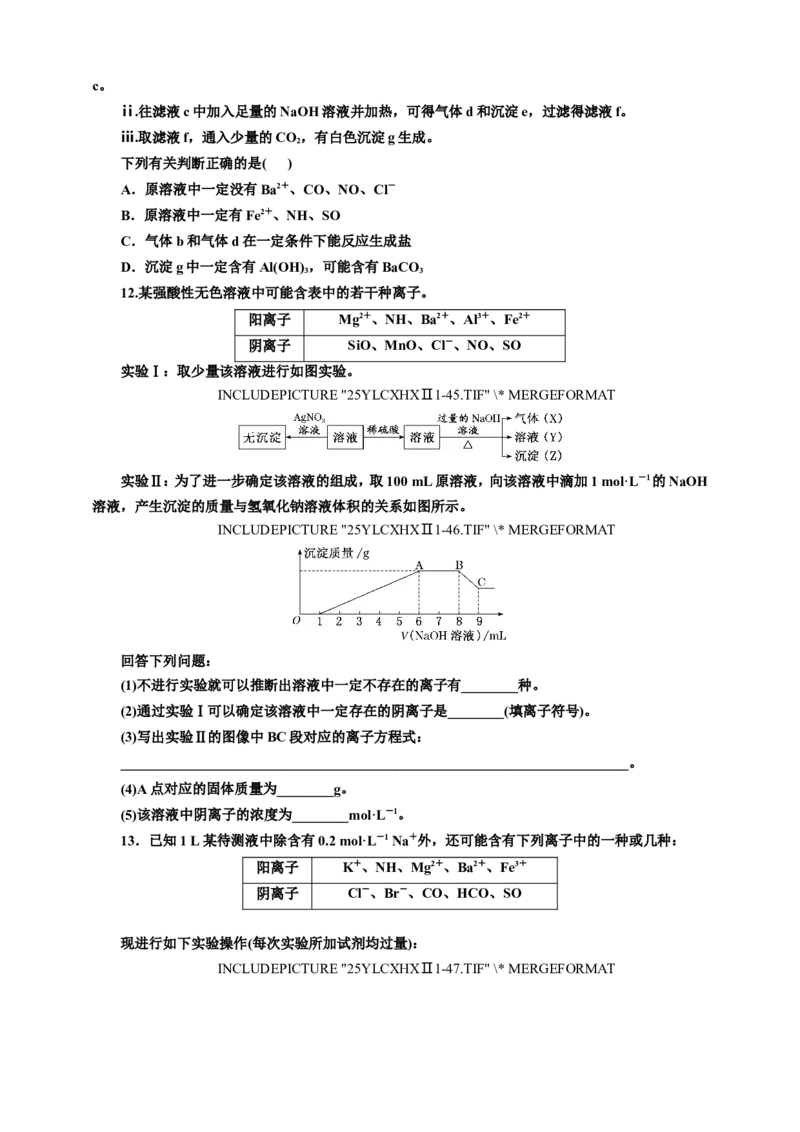
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液,向该溶液中滴加1 mol·L-1的NaOH
溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
INCLUDEPICTURE "25YLCXHXⅡ1-46.TIF" \* MERGEFORMAT
回答下列问题:
(1)不进行实验就可以推断出溶液中一定不存在的离子有________种。
(2)通过实验Ⅰ可以确定该溶液中一定存在的阴离子是________(填离子符号)。
(3)写出实验Ⅱ的图像中BC段对应的离子方程式:
________________________________________________________________________。
(4)A点对应的固体质量为________g。
(5)该溶液中阴离子的浓度为________mol·L-1。
13.已知1 L某待测液中除含有0.2 mol·L-1 Na+外,还可能含有下列离子中的一种或几种:
阳离子 K+、NH、Mg2+、Ba2+、Fe3+
阴离子 Cl-、Br-、CO、HCO、SO
现进行如下实验操作(每次实验所加试剂均过量):
INCLUDEPICTURE "25YLCXHXⅡ1-47.TIF" \* MERGEFORMAT(1)由气体B可确定待测液中含有的离子是
________________________________________________________________________。
(2)由沉淀D和沉淀E可确定待测液中一定含有的离子是________________,据此可排除的离子
是________________。
(3)由白色沉淀B可确定待测液中含有的离子是________。
(4)某同学读图后,认为待测液中一定不含溴离子,他判断的依据是
________________________________________________________________________
________________________________________________________________________。
(5)综合分析,待测液中K+的最小浓度为____________________。
课时检测(五)
1.A 该组离子彼此不发生反应,可以大量共存,故A正确;MnO与Cl-和I-均能发生氧化还原
反应,不能大量共存,故B错误;Al3+与S2-和CO均能发生相互促进的水解反应,不能大量共存,故C
错误;Fe3+与SCN-能发生络合反应生成Fe(SCN) ,SCN-能与ClO-发生氧化还原反应,不能大量共
3
存,故D错误。
2.B A项,ClO-具有强氧化性,与S2-不能大量共存;C项,Ag+与Cl-、Br-会生成AgCl、AgBr
沉淀,不能大量共存;D项,Fe3+与SCN-会生成Fe(SCN) 络合物,不能大量共存。
3
3.D 酸性溶液中,Fe2+、NO之间发生氧化还原反应,不能大量共存,A不符合题意;0.1 mol·L-1
NaClO溶液中,H+、ClO-、Cl-之间发生氧化还原反应,不能大量共存,B不符合题意;能使酚酞变红
的溶液显碱性,Al3+、HCO均与OH-反应,不能大量共存,C不符合题意;加入铝片产生H 的溶液可能
2
显酸性也可能显碱性,如果显碱性,Na+、Ba2+、CH COO-、NO之间不反应,可以大量共存,D符合题意。
3
4.A 0.1 mol·L-1AlCl 溶液显酸性,H+、Na+、K+、SO可以与其共存,故A 正确;酸性条件下,
3
NO具有强氧化性,可以将Fe2+氧化,故B错误;能使紫色石蕊试纸变蓝的溶液显碱性,Fe3+不能大量
存在,且Ag+和Br-不共存,故C错误;由水电离产生的c(H+)=10-12mol·L-1的溶液可能显酸性,也
可能显碱性,但都不可以和HCO共存,显碱性时也不能与NH大量共存,故D错误。
5.C 硝酸具有强氧化性,可以将SO氧化成SO,故检验SO不宜使用稀硝酸和硝酸钡,可以先向
溶液中加入稀盐酸,再滴加BaCl 溶液,有白色沉淀生成,说明该溶液中含有SO,A错误;先向溶液中
2
加入少量新制氯水,若溶液中含有Fe2+,则Fe2+会被氧化成Fe3+,影响Fe3+的检验,故只需向溶液中
加入KSCN溶液,若溶液变红,说明该溶液中含有Fe3+,B错误;将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,则产生的气体为CO 或SO ,说明该溶液中可能含有CO、HCO、SO
2 2
或HSO,D错误。
6.A Fe2+、K+、NO、Cl-能够大量共存,但I-的还原性大于Fe2+,加入少量HI后只有I-被氧化,
正确的离子方程式为8H++6I-+2NO===3I +2NO↑+4HO,故B错误;NH、Fe3+都与[Al(OH) ]-反
2 2 4
应,不能大量共存,故C错误;[Al(OH) ]-、HCO之间发生反应,不能大量共存,故D错误。
4
7.B 由步骤一可知,白色粉末中一定不含CuSO ;由步骤二可知,白色粉末中一定含Na S、
4 2
(NH)SO ,一定不含有KHSO ,酸性条件下发生反应2S2-+SO+6H+===3S↓+3HO;由步骤三可知,
4 2 3 4 2
X为HS;不能确定白色粉末中是否有NaCl,故选B。
2
8.D 向X溶液中加入足量稀盐酸,有无色气体生成,且反应前后阴离子种类没有发生改变,说
明X溶液中含有Cl-和NO,无色气体为NO;NO在酸中转化成NO,则X溶液中应含有还原性离子Fe2
+,根据电中性原则,X溶液中还含有Mg2+和SO,又因为Ca2+与SO会生成微溶物CaSO ,则X溶液中
4
一定不含有Ca2+。
9.A 取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol NH ,同时产生Fe(OH) 红褐
3 3
色沉淀,说明溶液中含有NH、Fe3+,n(NH)=0.02 mol,n(Fe3+)==0.02 mol,根据互斥性原则,溶液中
不存在CO;向上述滤液中加足量BaCl 溶液,得到4.66 g不溶于盐酸的白色沉淀,该沉淀是BaSO ,
2 4
n(BaSO )==0.02 mol,则n(SO)=n(BaSO )=0.02 mol,阳离子所带电荷>阴离子所带电荷,根据电
4 4
中性原则,溶液中还存在阴离子Cl- ,可能存在Al3+ 和K+。由分析可知,该溶液中至少存在Cl-、
SO、NH、Fe3+4种离子,至少存在4种盐,故A正确,C错误;该溶液中一定存在氯离子,假设溶液中只
有Cl- 、SO、NH、Fe3+,根据电中性原则,n(Cl-)=n(NH)+3n(Fe3+)-2n(SO)=0.02 mol+0.06 mol-
0.04 mol=0.04 mol,则c(Cl-)==0.4 mol·L-1,溶液中若还有其他阳离子,则 c(Cl-)≥0.4 mol·L-1,故
B错误;由分析可知,该溶液中一定存在Cl- 、SO、NH、Fe3+,可能存在Al3+和K+,故D错误。
10.D 根据步骤①可知原溶液中必然存在SO;根据浅绿色滤液B可知原溶液中存在H+和Fe2
+,则不可能存在CO和HCO;根据步骤②可知白色沉淀应该是AgCl,说明原溶液中含有Cl-;同时不
能推断出是否存在Na+、Mg2+,A、B、C正确;可用KSCN溶液检验Fe3+的存在而不能检验Fe2+的存
在,D错误。
11.B 强酸性溶液中,CO不能大量存在,Fe2+和NO不能共存,Ba2+和SO不能共存;根据实验
ⅰ可知,气体b为NO,沉淀a为BaSO ,则溶液中一定存在SO和Fe2+,则一定不存在Ba2+和NO;根
4
据实验ⅱ,气体d为NH ,沉淀e为Fe(OH) ,则溶液中一定存在NH,因为氢氧化铝溶于氢氧化钠,则
3 3
溶液中可能存在Al3+;根据实验ⅲ,又因为实验ⅰ中的硝酸钡是过量的,沉淀f可能为碳酸钡或碳酸钡
与氢氧化铝的混合物。原溶液中一定不存在Ba2+、CO、NO,A错误;原溶液中一定含有Fe2+、NH、
SO,B正确;气体b为NO,气体d为NH ,二者不能生成盐,C错误;沉淀g中可能含有氢氧化铝,D错
3
误。
12.解析:(1)强酸性无色溶液中Fe2+、SiO、MnO、SO一定不存在,即一定不存在的离子有4种。
(2)实验Ⅰ,向溶液中加入硝酸银溶液无沉淀生成,说明溶液中不存在Cl-;加入稀硫酸后得到溶液,说
明溶液中不存在Ba2+;加入过量的氢氧化钠溶液加热后有气体生成,说明溶液中存在NH,有沉淀生
成,说明存在Mg2+、Al3+或Mg2+、Al3+都有,根据(1)中判断,并结合电中性原则,溶液中肯定存在
NO。(3)实验Ⅱ的图像中BC段是Al(OH) 溶于过量NaOH溶液的过程,对应的离子方程式为Al(OH)
3 3
+OH-===[Al(OH) ]-。(4)BC段沉淀溶解发生反应:Al(OH) +OH-===[Al(OH) ]-,n(Al3+)=n(OH-)
4 3 4
=1×(9-8)×10-3 mol=10-3 mol,在沉淀生成过程中发生反应:Al3++ 3OH-===Al(OH) ↓,Mg2++
32OH-===Mg(OH) ↓,总共消耗氢氧化钠1×(6-1)×10-3 mol=5×10-3 mol,其中铝离子消耗氢氧根离
2
子3×10-3 mol,则镁离子消耗氢氧根离子2×10-3 mol,n(Mg2+)=10-3 mol,A点得到的固体是10-3
mol Al(OH) 和10-3 mol Mg(OH) ,质量为10-3×58 g+10-3×78 g=0.136 g。(5)根据上述分析,溶液中
3 2
存在的离子是Mg2+、NH、Al3+、NO、H+,图像开始阶段,NaOH中和H+,则溶液中n(H+)=1×(1-
0)×10-3 mol=10-3 mol;AB段发生反应消耗氢氧根离子的物质的量为 1×(8-6)×10-3 mol=2×10-3
mol,则溶液中n(NH)=2×10-3 mol;根据电荷守恒:n(NH)+n(H+)+2n(Mg2+)+3n(Al3+)=n(NO),解
得n(NO)=8×10-3 mol,则c(NO)= mol·L-1=0.08 mol·L-1。
答案:(1)4 (2)NO (3)Al(OH) +OH-===[Al(OH) ]-
3 4
(4)0.136 (5)0.08
13.解析:待测液与BaCl 溶液反应生成滤液A和沉淀A,沉淀A与稀硝酸反应生成白色沉淀D
2
和无色气体D,无色气体D与石灰水反应生成白色沉淀E,则待测液中一定含有SO和CO,结合离子
共存的条件可知待测液中一定不存在Mg2+、Ba2+、Fe3+;滤液A与NaOH溶液反应生成的气体B为
NH ,同时还生成了白色沉淀B,则待测液中一定含有NH和HCO;根据向溶液B中通入氯气,溶液呈
3
浅黄绿色和向溶液B中滴加硝酸酸化的硝酸银溶液,出现白色沉淀可知,待测液中一定不存在Br-;
由于实验过程中加入了BaCl 溶液,因此由白色沉淀C无法确定待测液中是否含有Cl-。(5)结合题中
2
数据可知,待测液中n(NH)==0.1 mol,n(HCO)=n(BaCO ) ==0.1 mol,n(CO)=n(CaCO )
3 沉淀B 3 沉淀E
==0.1 mol,n(SO)=n(BaSO ) ==0.05 mol,n(Na+)+n(NH)=1×0.2 mol+0.1 mol=0.3
4 沉淀D
mol,2n(CO)+2n(SO)+n(HCO)=0.4 mol,根据电中性原则可知,待测液中一定含有K+。若待测液中
不含Cl-,则n(K+)=0.1 mol;若待测液中含有Cl-,则n(K+)>0.1 mol,所以c(K+)≥0.1 mol·L-1。
答案:(1)NH (2)CO、SO Mg2+、Ba2+、Fe3+ (3)HCO
(4)向溶液B中通入氯气,溶液呈浅黄绿色(或向溶液B中滴加硝酸酸化的硝酸银溶液,出现白色
沉淀) (5)0.1 mol·L-1