文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04
(陕西、山西、宁夏、青海专用)
化 学
考情速递
高考·新动向:2025年的高考命题不仅可以引出考点的设问,让题设的问题与现实及生产联系更紧密,
也需要考生可以在题目中提取更多信息,不仅仅是选项知识的考察,也考察对整体题设的把握和理
解。比如此试卷第6题考查铜阳极泥提取碲,第8题考查工业上制硫酸的流程图,第10题考查烯烃一
定条件下转化为邻二醇的机理图;
高考·新考法:近年来,高考命题愈发重视对学生综合素质的评估。比如此试卷第13题考查制备醇类物
质,第14题考查以天然方沸石为引物探究元素周期规律;
高考·新情境:在科学与科技领域,题目设计将更加贴近当前科研动态和技术应用前沿,信息维度更加
丰富多元。比如此试卷第11题考查硫代硫酸钠(Na SO)的制备和应用相关流程图,第12题考查全固态
2 2 3
LiPON薄膜锂离子电池工作示意图;
命题·大预测:高考评价体系是指导高考命题的实践体系,有“四层”规定命题内容,“四翼”保障命
题水平,它将有力促进高考内容改革以及命题质量的提升。《国务院关于考试招生制度改革的实施意
见》明确提出深化高考考试内容改革,依据高校人才选拔要求和国家课程标准,科学设计命题内容,
增强基础性、综合性,着重考查学生独立思考和运用所学知识分析问题、解决问题的能力。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.下列对科学动态的解读错误的是
选项 最新科技动态 化学角度分析
A 研究人员研发出一种“火星化学电池” 该电池放电时将化学能转化成电能
B 我国首次发现罕见含金碲的叶碲金矿 叶碲金矿只含周期表前四周期元素
C 科学家发现水星钻石圈层 钻石(金刚石)与石墨烯互为同素异形体D 高效 (钯) 合金纳米颗粒催化甲酸制氢 (钯) 合金属于金属材料
A.A B.B C.C D.D
2.下列化学用语表示正确的是
A.乙炔分子的空间填充模型:
B.羟基的电子式:
C.CS 的VSEPR模型为:平面三角形
2
D.碳原子核外价电子的轨道表示式:
3.在人体中,大概含有60多种元素,其中含量前10的元素分别是氧、碳、氢、氮、钙、磷、硫、钾、钠、
氯。下列说法正确的是
A.酸性:HNO<HPO B.SO 通入紫色石蕊溶液中,溶液先变红后褪色
3 3 4 2
C.金属性:K<Na D.CO、SO 均属于酸性氧化物
2 3
4.设 为阿伏加德罗常数的值。下列叙述正确的是
A. 由 和 组成的混合气体中含原子总数为
B.一定条件下,将 置于密闭容器中充分分解,得到产物的分子总数为
C.在核反应方程 中, 含中子数为
D.标准状况下, (气体)与水完全反应(生成 和 )时转移电子数为
5.对于下列过程中发生的化学反应,相应离子方程式正确的是
A.向浓硝酸中加入少量氧化亚铜:
B.以热氢氧化钠溶液洗涤附着在试管内壁的少量硫:
C.醋酸铵的水解:
D.向碘酸钾溶液中滴加双氧水:
6.铜阳极泥(主要成分是 , )为原料提取碲的反应如下。下列说法不正确的是① ;
② 。
A. 中 元素的化合价是 价
B.反应①中氧化剂是 ,氧化产物是 和
C.每制备 理论上两个反应共转移
D.氧化性强弱顺序为
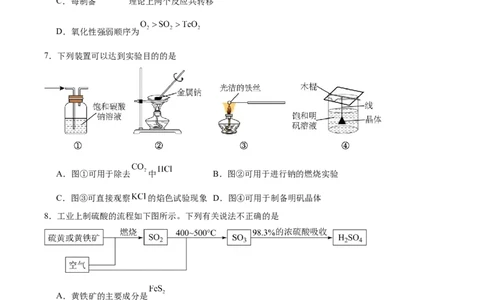
7.下列装置可以达到实验目的的是
A.图①可用于除去 中 B.图②可用于进行钠的燃烧实验
C.图③可直接观察 的焰色试验现象 D.图④可用于制备明矾晶体
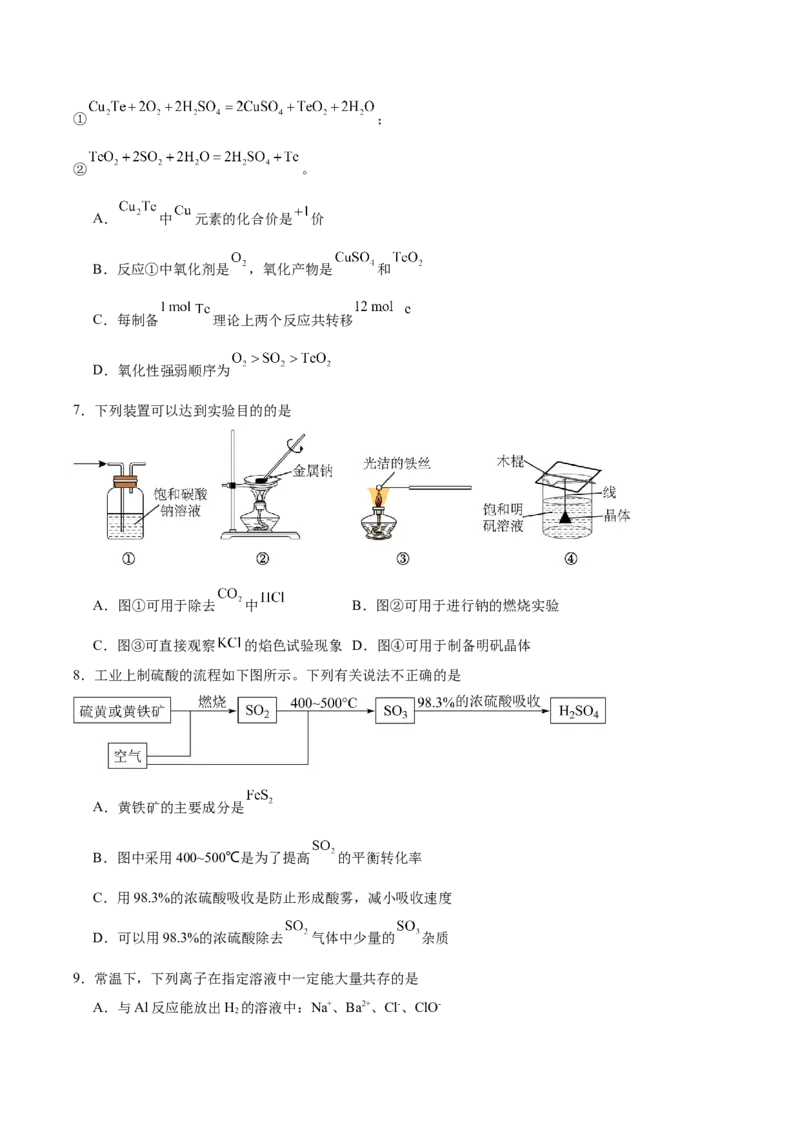
8.工业上制硫酸的流程如下图所示。下列有关说法不正确的是
A.黄铁矿的主要成分是
B.图中采用400~500℃是为了提高 的平衡转化率
C.用98.3%的浓硫酸吸收是防止形成酸雾,减小吸收速度
D.可以用98.3%的浓硫酸除去 气体中少量的 杂质
9.常温下,下列离子在指定溶液中一定能大量共存的是
A.与Al反应能放出H 的溶液中:Na+、Ba2+、Cl-、ClO-
2B.含大量NaHSO 的溶液中:K+、Fe2+、Cl-、
4
C.某中性溶液中:Fe3+、K+、 、
D.能使酚酞变红的溶液中:Na+、K+、 、
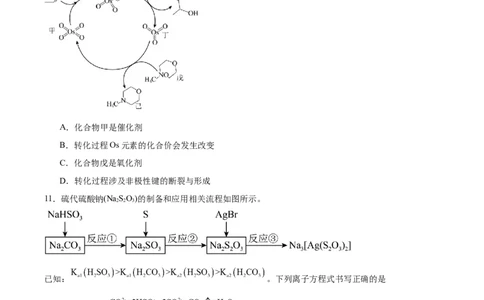
10.烯烃在一定条件下能转化为邻二醇,其机理如下图所示。下列说法错误的是
A.化合物甲是催化剂
B.转化过程Os元素的化合价会发生改变
C.化合物戊是氧化剂
D.转化过程涉及非极性键的断裂与形成
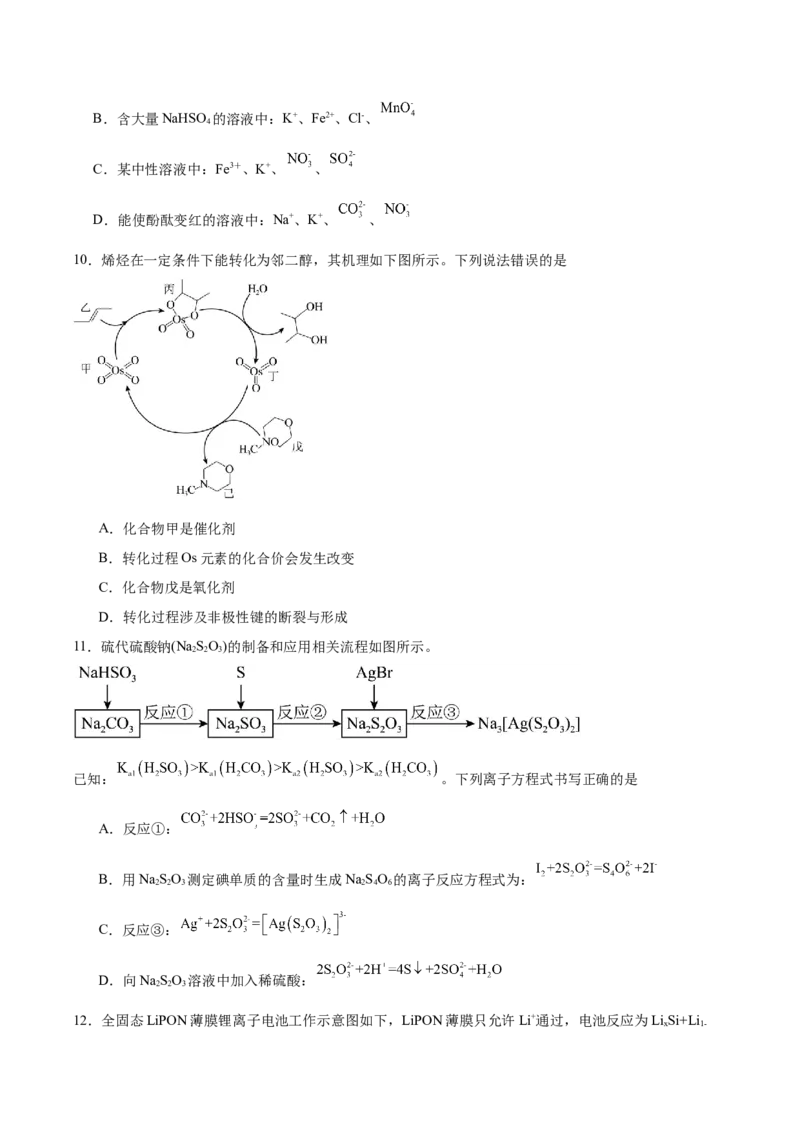
11.硫代硫酸钠(Na SO)的制备和应用相关流程如图所示。
2 2 3
已知: 。下列离子方程式书写正确的是
A.反应①:
B.用NaSO 测定碘单质的含量时生成NaSO 的离子反应方程式为:
2 2 3 2 4 6
C.反应③:
D.向NaSO 溶液中加入稀硫酸:
2 2 3
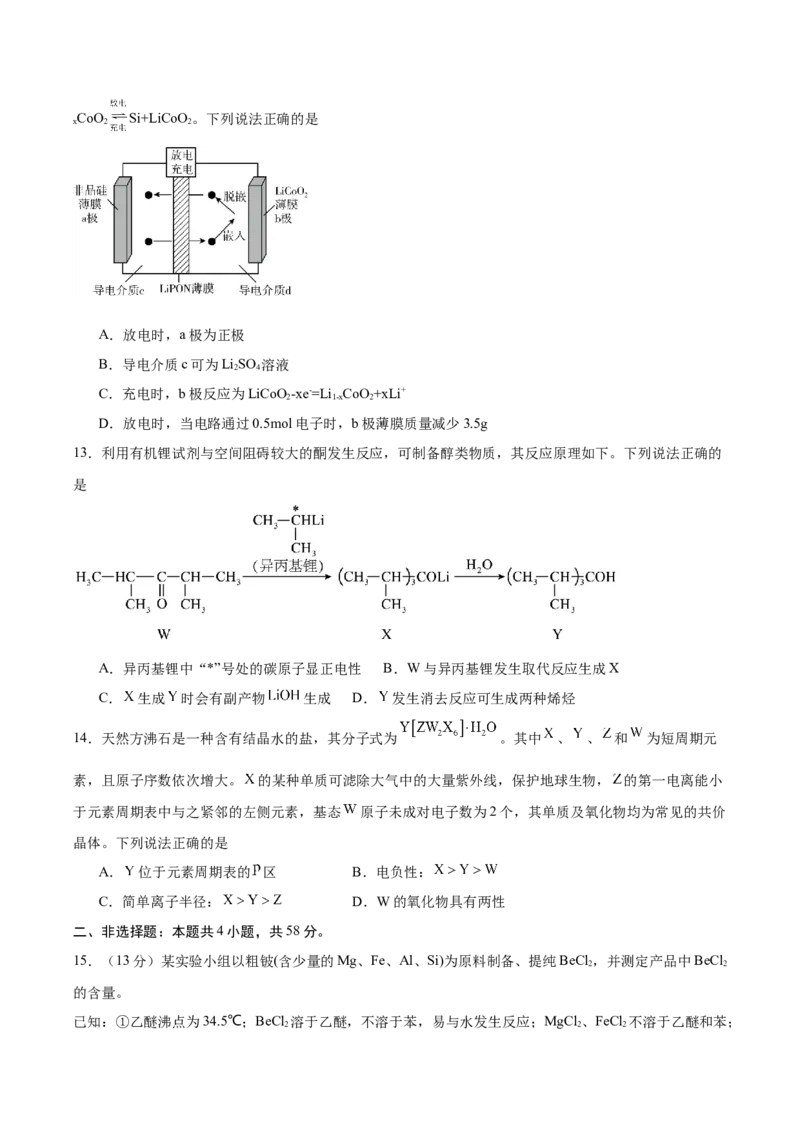
12.全固态LiPON薄膜锂离子电池工作示意图如下,LiPON薄膜只允许Li+通过,电池反应为LiSi+Li
x 1-CoO Si+LiCoO。下列说法正确的是
x 2 2
A.放电时,a极为正极
B.导电介质c可为LiSO 溶液
2 4
C.充电时,b极反应为LiCoO -xe-=Li CoO+xLi+
2 1-x 2
D.放电时,当电路通过0.5mol电子时,b极薄膜质量减少3.5g
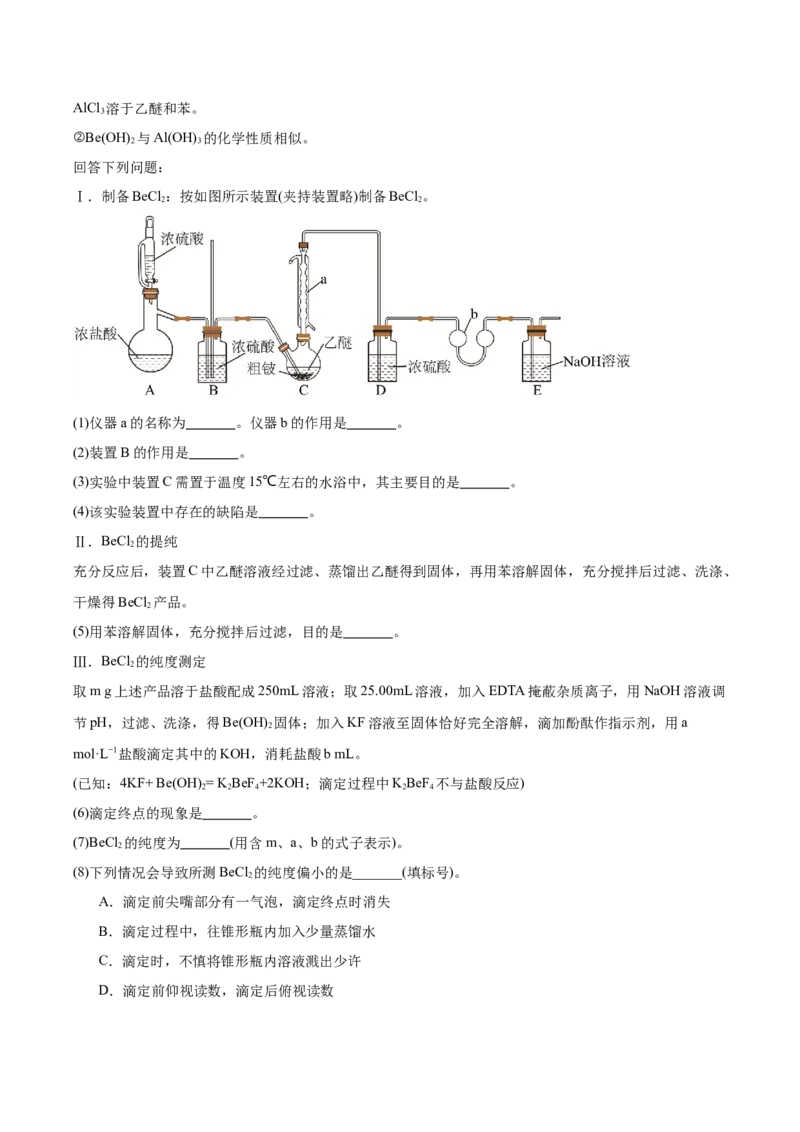
13.利用有机锂试剂与空间阻碍较大的酮发生反应,可制备醇类物质,其反应原理如下。下列说法正确的
是
A.异丙基锂中“*”号处的碳原子显正电性 B.W与异丙基锂发生取代反应生成X
C. 生成 时会有副产物 生成 D. 发生消去反应可生成两种烯烃
14.天然方沸石是一种含有结晶水的盐,其分子式为 。其中 、 、 和 为短周期元
素,且原子序数依次增大。 的某种单质可滤除大气中的大量紫外线,保护地球生物, 的第一电离能小
于元素周期表中与之紧邻的左侧元素,基态 原子未成对电子数为2个,其单质及氧化物均为常见的共价
晶体。下列说法正确的是
A. 位于元素周期表的 区 B.电负性:
C.简单离子半径: D.W的氧化物具有两性
二、非选择题:本题共4小题,共58分。
15.(13分)某实验小组以粗铍(含少量的Mg、Fe、Al、Si)为原料制备、提纯BeCl ,并测定产品中BeCl
2 2
的含量。
已知:①乙醚沸点为34.5℃;BeCl 溶于乙醚,不溶于苯,易与水发生反应;MgCl 、FeCl 不溶于乙醚和苯;
2 2 2AlCl 溶于乙醚和苯。
3
②Be(OH) 与Al(OH) 的化学性质相似。
2 3
回答下列问题:
Ⅰ.制备BeCl :按如图所示装置(夹持装置略)制备BeCl 。
2 2
(1)仪器a的名称为 。仪器b的作用是 。
(2)装置B的作用是 。
(3)实验中装置C需置于温度15℃左右的水浴中,其主要目的是 。
(4)该实验装置中存在的缺陷是 。
Ⅱ.BeCl 的提纯
2
充分反应后,装置C中乙醚溶液经过滤、蒸馏出乙醚得到固体,再用苯溶解固体,充分搅拌后过滤、洗涤、
干燥得BeCl 产品。
2
(5)用苯溶解固体,充分搅拌后过滤,目的是 。
Ⅲ.BeCl 的纯度测定
2
取m g上述产品溶于盐酸配成250mL溶液;取25.00mL溶液,加入EDTA掩蔽杂质离子,用NaOH溶液调
节pH,过滤、洗涤,得Be(OH) 固体;加入KF溶液至固体恰好完全溶解,滴加酚酞作指示剂,用a
2
mol·L−1盐酸滴定其中的KOH,消耗盐酸b mL。
(已知:4KF+ Be(OH) = K BeF +2KOH;滴定过程中KBeF 不与盐酸反应)
2 2 4 2 4
(6)滴定终点的现象是 。
(7)BeCl 的纯度为 (用含m、a、b的式子表示)。
2
(8)下列情况会导致所测BeCl 的纯度偏小的是_______(填标号)。
2
A.滴定前尖嘴部分有一气泡,滴定终点时消失
B.滴定过程中,往锥形瓶内加入少量蒸馏水
C.滴定时,不慎将锥形瓶内溶液溅出少许
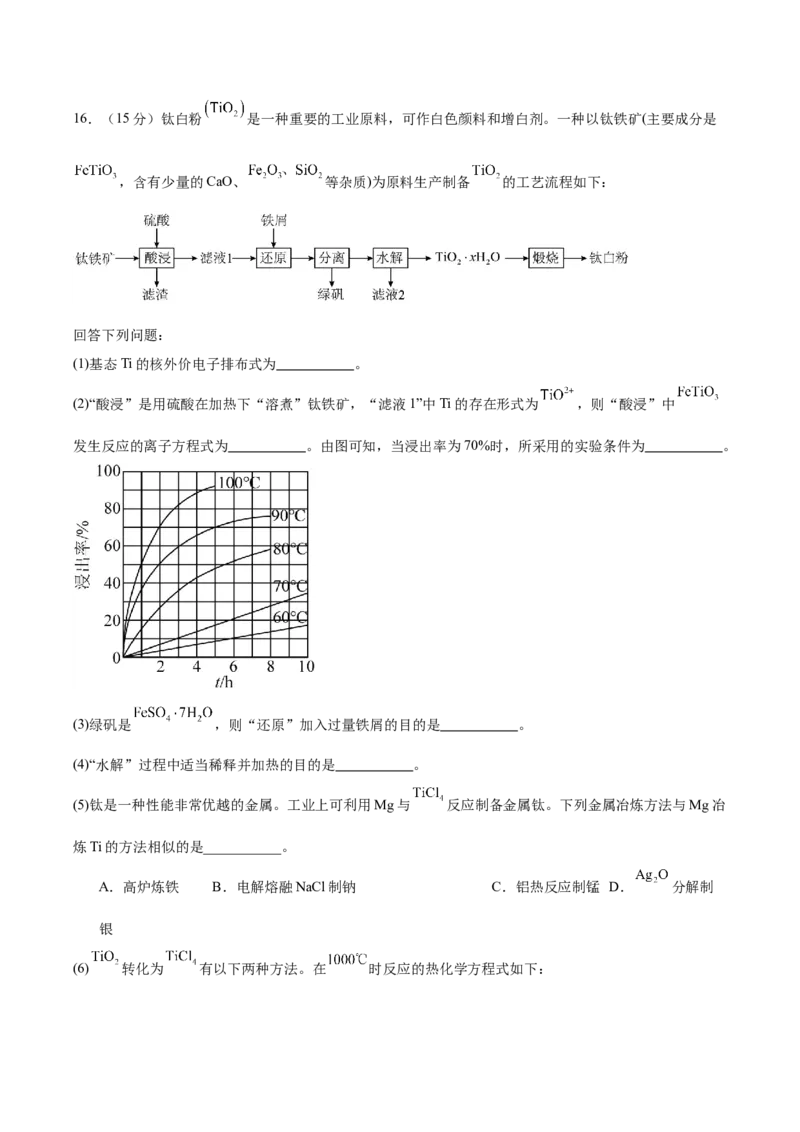
D.滴定前仰视读数,滴定后俯视读数16.(15分)钛白粉 是一种重要的工业原料,可作白色颜料和增白剂。一种以钛铁矿(主要成分是
,含有少量的CaO、 等杂质)为原料生产制备 的工艺流程如下:
回答下列问题:
(1)基态Ti的核外价电子排布式为 。
(2)“酸浸”是用硫酸在加热下“溶煮”钛铁矿,“滤液1”中Ti的存在形式为 ,则“酸浸”中
发生反应的离子方程式为 。由图可知,当浸出率为70%时,所采用的实验条件为 。
(3)绿矾是 ,则“还原”加入过量铁屑的目的是 。
(4)“水解”过程中适当稀释并加热的目的是 。
(5)钛是一种性能非常优越的金属。工业上可利用Mg与 反应制备金属钛。下列金属冶炼方法与Mg冶
炼Ti的方法相似的是___________。
A.高炉炼铁 B.电解熔融NaCl制钠 C.铝热反应制锰 D. 分解制
银
(6) 转化为 有以下两种方法。在 时反应的热化学方程式如下:①
②
请分析方法②加入C(s)的目的是 。
17.(15分)氨是重要化工原料,其工业合成原理为 。回答下列问题:
(1)已知:ⅰ. ;
ⅱ. (a、b都大于0)。
则反应 的 (用含a、b的代数式表示),利于该反应正向进行
的条件为 (填“低温”“高温”或“任意温度”)。
(2)向恒温恒容密闭容器中充入体积比 的 和 ,发生反应 。下列情况表
明该反应一定达到平衡状态的是___________(填字母,下同)。
A.气体密度不随时间变化 B.气体平均摩尔质量不随时间变化
C.气体总压强不随时间变化 D. 体积分数不随时间变化
(3)下列关于 的叙述正确的是 。
A. 生成速率等于 消耗速率的2倍
B.若加入高效催化剂,平衡常数和反应热都会增大
C.若起始按体积比 投入 和 ,则 和 的转化率相等
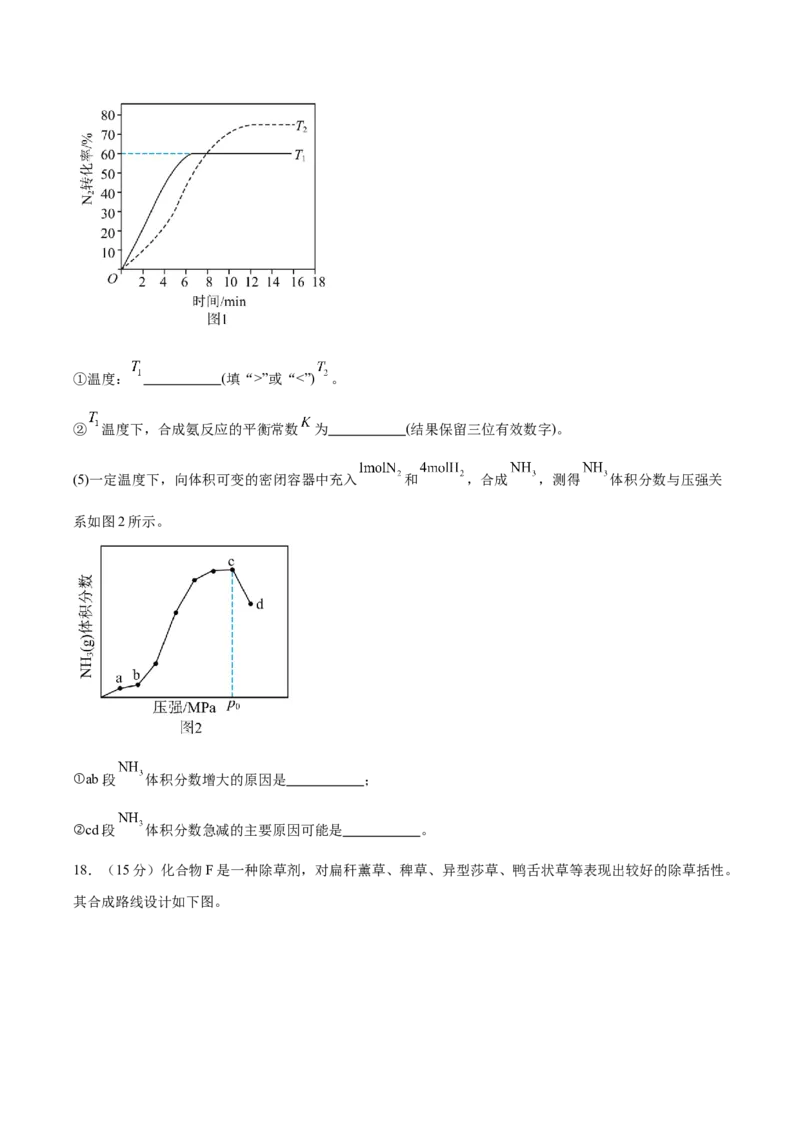
(4)向 刚性密闭容器中充入 和 合成氨,经历相同时间测得 转化率与温度及时间的关系
如图1所示。①温度: (填“>”或“<”) 。
② 温度下,合成氨反应的平衡常数 为 (结果保留三位有效数字)。
(5)一定温度下,向体积可变的密闭容器中充入 和 ,合成 ,测得 体积分数与压强关
系如图2所示。
①ab段 体积分数增大的原因是 ;
②cd段 体积分数急减的主要原因可能是 。
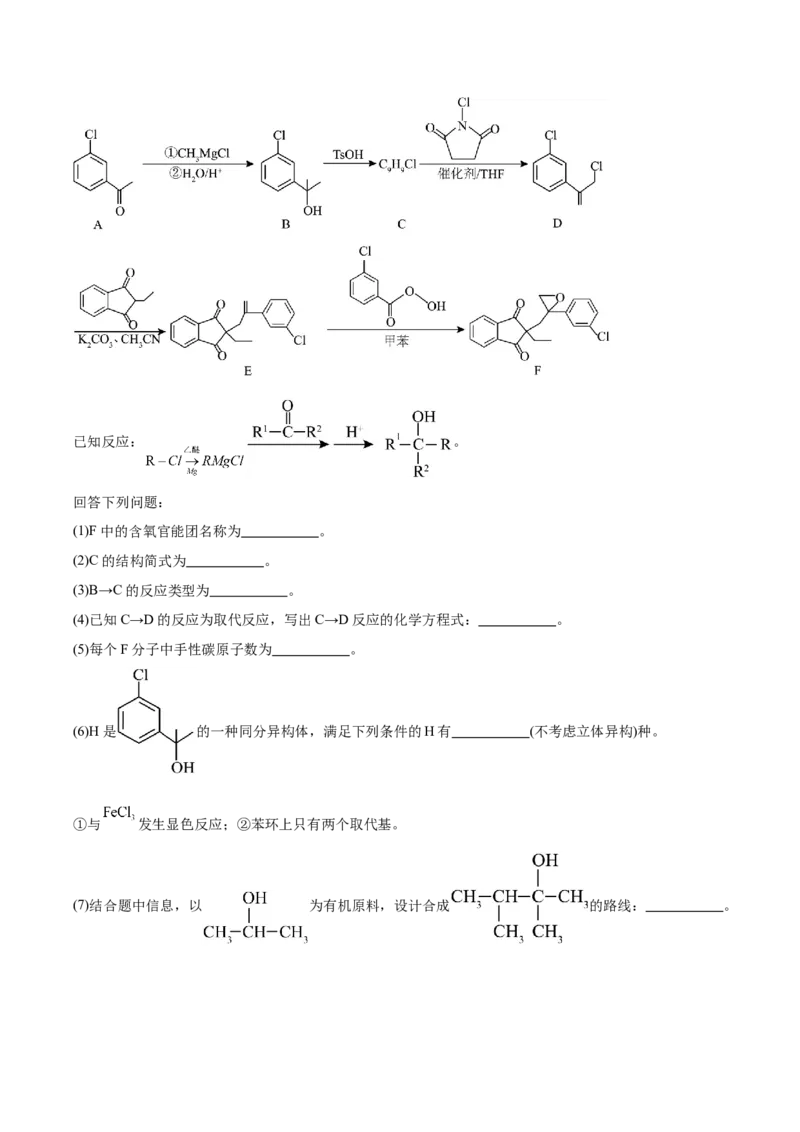
18.(15分)化合物F是一种除草剂,对扁秆薰草、稗草、异型莎草、鸭舌状草等表现出较好的除草括性。
其合成路线设计如下图。已知反应: 。
回答下列问题:
(1)F中的含氧官能团名称为 。
(2)C的结构简式为 。
(3)B→C的反应类型为 。
(4)已知C→D的反应为取代反应,写出C→D反应的化学方程式: 。
(5)每个F分子中手性碳原子数为 。
(6)H是 的一种同分异构体,满足下列条件的H有 (不考虑立体异构)种。
①与 发生显色反应;②苯环上只有两个取代基。
(7)结合题中信息,以 为有机原料,设计合成 的路线: 。