文档内容
微专题09 新情景中氧化还原反应方程式的配平与书写
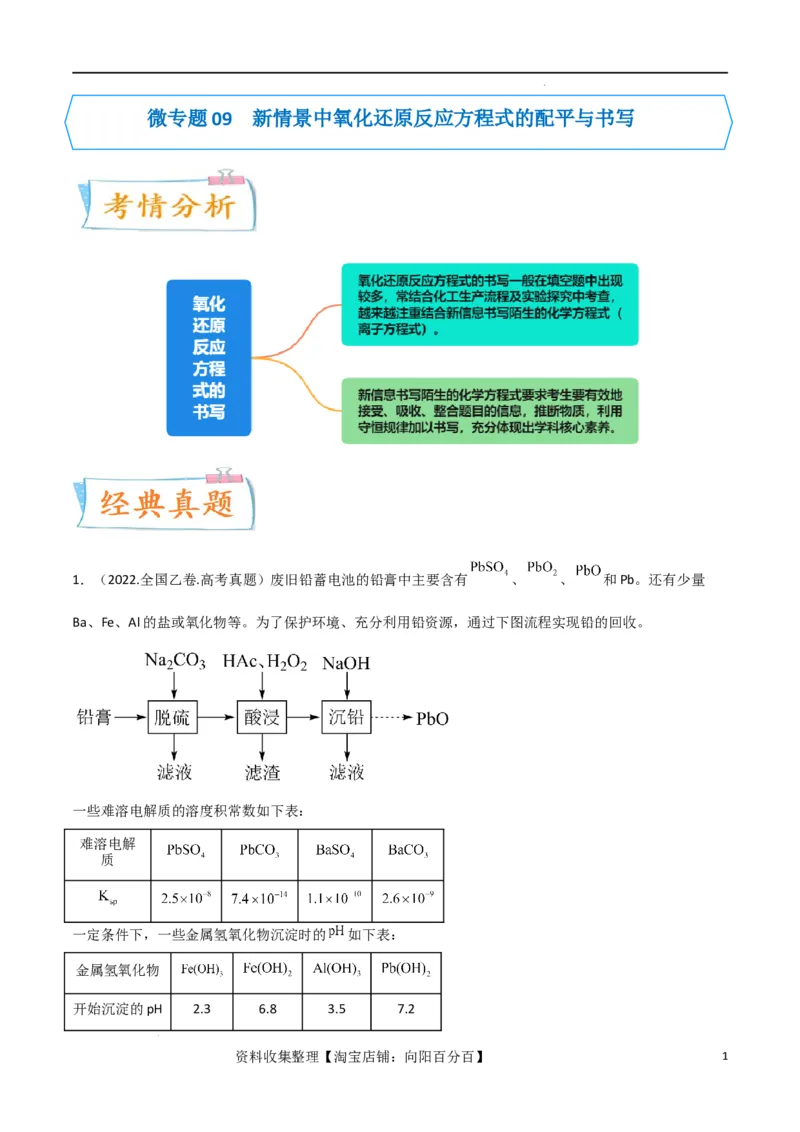
1.(2022.全国乙卷.高考真题)废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量
Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解
质
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
资料收集整理【淘宝店铺:向阳百分百】 1
学科网(北京)股份有限公司完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择 的原因
________。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。
(ⅰ)能被 氧化的离子是________;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
(ⅲ) 也能使 转化为 , 的作用是________。
【答案】(1) PbSO (s)+CO (aq)= PbCO (s)+SO (aq) 反应PbSO (s)+CO (aq)= PbCO (s)+SO (aq)的平
4 3 4 3
衡常数K= =3.4 105>105,PbSO 可以比较彻底的转化为PbCO
4 3
(3) Fe2+ Pb+H O +2HAc=Pb(Ac) +2H O 作还原剂
2 2 2 2
【解析】(1)“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:
PbSO (s)+CO (aq)= PbCO (s)+SO (aq),由一些难溶电解质的溶度积常数的数据可知,K (PbCO )=7.4 10-14,
4 3 sp 3
K (PbSO )=2.5 10-8,反应PbSO (s)+CO (aq)= PbCO (s)+SO (aq)的平衡常数K= = =
sp 4 4 3
= ≈3.4 105>105,说明可以转化的比较彻底,且转化后生成的碳酸铅可由酸浸进入溶
液中,减少铅的损失。
(3)(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发生氧还原反应生成Pb(Ac)
2 2
和H O,依据得失电子守恒和原子守恒可知,反应的化学方程式为:Pb+H O +2HAc=Pb(Ac) +2H O。
2 2 2 2 2
资料收集整理【淘宝店铺:向阳百分百】 2
学科网(北京)股份有限公司(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,PbO 是氧化剂,则过氧
2 2 2
化氢是还原剂。
一、工艺流程中的氧化还原方程式的书写
【归纳总结】
(1)细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的去除情况。
(2)确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
二、实验探究中的氧化还原方程式的书写
【归纳总结】
(1)细读题干寻找实验目的,通读题目中从实验步骤中了解操作步骤,结合装置分析实验过程,与实验
目的相对应。
(2)根据题意确定反应物和生成物,结合溶液环境配平方程式,注意质量守恒、电子守恒、电荷守恒。
三、电化学试题中氧化还原反应方程式的书写
【归纳总结】
(1)有关原电池原理的电极方程式的书写,负极失去电子,发生氧化反应;氧化剂在正极上得到电子,
发生还原反应。根据得失电子相等,从而配平电极方程式。
(2)有关电解原理的电极方程式的书写,还原剂在阳极上失去电子,发生氧化反应;氧化剂在阴极上得
到电子,发生还原反应。再根据得失电子相等,从而配平电极反应式。
资料收集整理【淘宝店铺:向阳百分百】 3
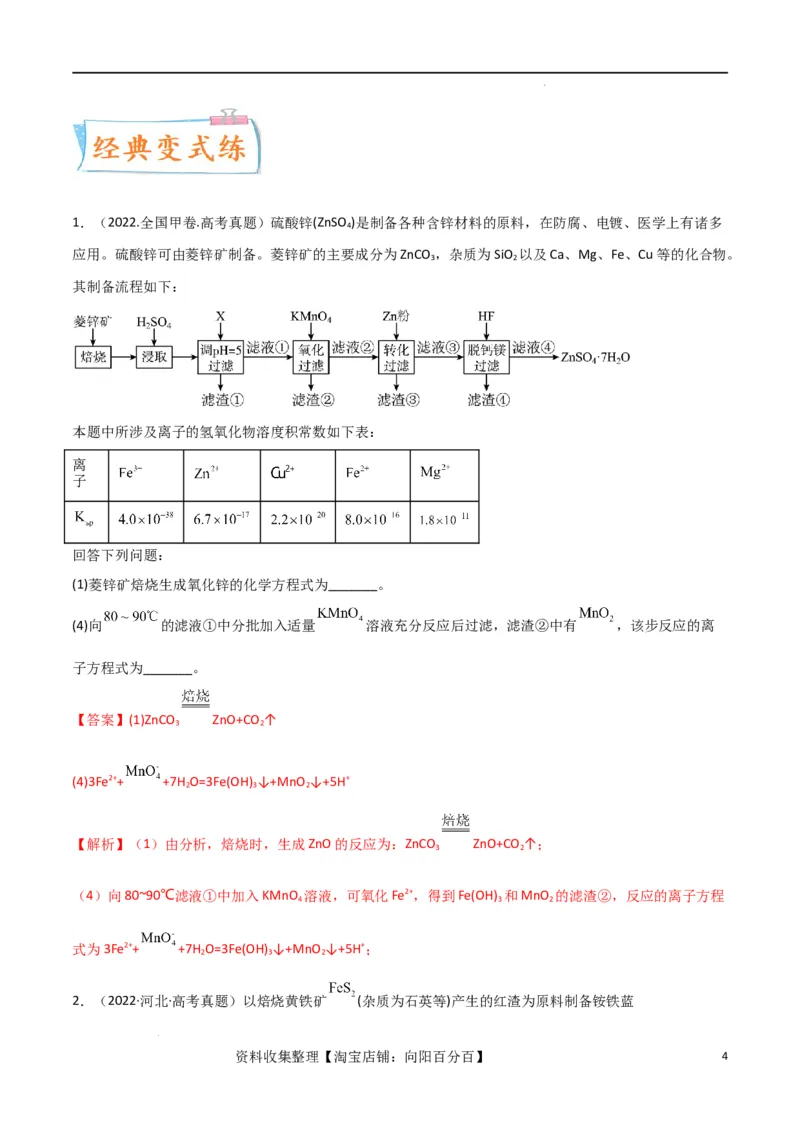
学科网(北京)股份有限公司1.(2022.全国甲卷.高考真题)硫酸锌(ZnSO )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多
4
应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。
3 2
其制备流程如下:
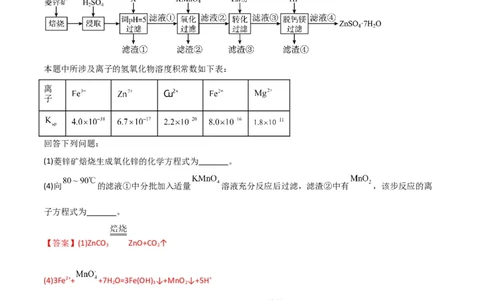
本题中所涉及离子的氢氧化物溶度积常数如下表:
离
子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的离
子方程式为_______。
【答案】(1)ZnCO ZnO+CO ↑
3 2
(4)3Fe2++ +7H O=3Fe(OH) ↓+MnO ↓+5H+
2 3 2
【解析】(1)由分析,焙烧时,生成ZnO的反应为:ZnCO ZnO+CO ↑;
3 2
(4)向80~90℃滤液①中加入KMnO 溶液,可氧化Fe2+,得到Fe(OH) 和MnO 的滤渣②,反应的离子方程
4 3 2
式为3Fe2++ +7H O=3Fe(OH) ↓+MnO ↓+5H+;
2 3 2
2.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
资料收集整理【淘宝店铺:向阳百分百】 4
学科网(北京)股份有限公司颜料。工艺流程如下:
回答下列问题:
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
【答案】(3)7Fe (SO ) +FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(5) +2; 6Fe(NH ) Fe(CN) + +6H+=6Fe(NH )Fe(CN) +3H O+Cl-+
4 2 6 4 6 2
【分析】已知黄铁矿高温煅烧生成Fe O ,反应原理为:4FeS +11O 2Fe O +8SO ,故产生的红渣主要成
2 3 2 2 2 3 2
分为Fe O 和SiO ,将红渣粉碎后加入足量的50%的H SO 溶液加热充酸浸,反应原理为:
2 3 2 2 4
Fe O +3H SO =Fe (SO ) +3H O,过滤出滤渣①,主要成分为SiO ,向滤液中加入黄铁矿进行还原,将Fe3+还
2 3 2 4 2 4 3 2 2
原为Fe2+,由(3)小问可知不生成S沉淀,则硫元素被氧化为 ,反应原理为:14Fe3++FeS +8H O=15Fe2++2
2 2
+16H+,然后进行工序①为蒸发浓缩、冷却结晶,得到FeSO 晶体和母液主要含有FeSO 溶液和H SO ,
4 4 2 4
加水溶解FeSO 晶体,向所得溶液中加入(NH ) SO 、K [Fe(CN) ]并用H SO 调节溶液的pH为3,进行沉铁过
4 4 2 4 4 6 2 4
程,反应原理为:Fe2++2 +[Fe(CN) ]3-=Fe(NH ) Fe(CN) ↓,然后过滤出沉淀,洗涤后加入H SO 和NaClO
6 4 2 6 2 4 3
进行氧化步骤,反应原理为:6Fe(NH ) Fe(CN) + +6H+=6Fe(NH )Fe(CN) +3H O+Cl-+6 ,过滤、洗涤干
4 2 6 4 6 2
燥即制得Fe(NH )Fe(CN) ,据此分析解题。
4 6
资料收集整理【淘宝店铺:向阳百分百】 5
学科网(北京)股份有限公司【解析】((3)由分析可知,还原工序中,不产生S单质沉淀,则硫元素被氧化为 ,反应原理为:
14Fe3++FeS +8H O=15Fe2++2 +16H+,故化学方程式为:7Fe (SO ) +FeS +8H O=15FeSO +8H SO ,故答案为:
2 2 2 4 3 2 2 4 2 4
7Fe (SO ) +FeS +8H O=15FeSO +8H SO ;
2 4 3 2 2 4 2 4
(5)沉铁工序中产生的白色沉淀Fe(NH ) Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,
4 2 6 6
氧化工序所发生的离子方程式为:6Fe(NH ) Fe(CN) + +6H+=6Fe(NH )Fe(CN) +3H O+Cl-+6 ,故答案为:
4 2 6 4 6 2
+2;6Fe(NH ) Fe(CN) + +6H+=6Fe(NH )Fe(CN) +3H O+Cl-+6 ;
4 2 6 4 6 2
1.(2022·湖南·高考真题)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,
含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗 中含有的几种物质的沸点:
物质
沸点/ 136 127 57 180
回答下列问题:
(2) 与C、 ,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
物质
分压
资料收集整理【淘宝店铺:向阳百分百】 6
学科网(北京)股份有限公司①该温度下, 与C、 反应的总化学方程式为_______;
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离 中含 、 杂质的方法是
_______。
【答案】(2) 5TiO +6C+10Cl 5TiCl +2CO+4CO 随着温度升高,CO 与C发生反应
2 2 4 2 2
(3) 3VOCl +Al=3VOCl +AlCl 蒸馏
3 2 3
【解析】钛渣中加入C、Cl 进行沸腾氯化,转化为相应的氯化物,降温收尘后得到粗TiCl ,加入单质Al除
2 4
钒,再除硅、铝得到纯TiCl ,加入Mg还原得到Ti。
4
(2)①根据表中数据可知,该温度下C主要生成CO和CO ,根据相同条件下气体的压强之比是物质的量
2
之比可知TiCl 、CO和CO 的物质的量之比约是5:2:4,所以TiO 与C、Cl 反应的总化学方程式为
4 2 2 2
5TiO +6C+10Cl 5TiCl +2CO+4CO ,故答案为:5TiO +6C+10Cl 5TiCl +2CO+4CO ;
2 2 4 2 2 2 4 2
②随着温度升高,CO 与C发生反应 ,导致CO含量升高,故答案为:随着温度升高,CO
2 2
与C发生反应 ;
(3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据得失电子守恒和元素守恒
3 2
配平方程式为3VOCl +Al=3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,“除硅、铝"过程中可采用蒸馏的
3 2 3 3 4 4
方法分离AlCl 、SiCl ,故答案为:3VOCl +Al=3VOCl +AlCl ;蒸馏;
3 4 3 2 3
2.(2022.辽宁.高考真题)某工厂采用辉铋矿(主要成分为 ,含有 、 杂质)与软锰矿(主要成
资料收集整理【淘宝店铺:向阳百分百】 7
学科网(北京)股份有限公司分为 )联合焙烧法制各 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(2) 在空气中单独焙烧生成 ,反应的化学方程式为_______。
(5)生成气体A的离子方程式为_______。
【答案】(2)
(5)
【解析】已知①焙烧时过量的 分解为 , 转变为 , 在空气中单独焙烧生成
和二氧化硫,经过酸浸,滤渣为二氧化硅, 与浓盐酸生成A氯气,滤液中含有Bi3+、Fe3+,加入Bi将
Fe3+转化为Fe2+,调节pH得到 ,据此分析解题。
资料收集整理【淘宝店铺:向阳百分百】 8
学科网(北京)股份有限公司(2) 在空气中单独焙烧生成 和二氧化硫,反应的化学方程式为 ;
(5)A为氯气,生成气体A的离子方程式为 ;
3.(2023·全国·高三专题练习)回答下列问题:
(1)利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中
(Ⅲ)的处理工艺流程如下:
已知:硫酸浸取液中的金属离子主要是 ,其次是 和 。
① 的作用是将滤液Ⅰ中的 转化为 ,写出此反应的离子方程式:_______。
②写出上述流程中用 进行还原时发生反应的离子方程式:_______。
(2) 常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为 ,还含少量
等杂质)通过如下方法制取:
已知: 能与烧碱反应生成可溶于水的 , 与酸反应生成 。
①“熔融”过程中, 发生反应的化学方程式为_______。
②滤渣Ⅲ的成分是 。“调 ”时,所发生反应的离子方程式为_______。滤渣Ⅲ
资料收集整理【淘宝店铺:向阳百分百】 9
学科网(北京)股份有限公司制备 的方法是_______。
【答案】(1)
(2)
高温焙烧
【解析】(1) 把 氧化为 , 被还原成水,结合电子转移守恒、电荷守恒、原子守恒
可得离子方程式为: ;
在调节pH=8的过程中会转化为 ,故通入SO 气体与 反应生成 和 ,
2
先用化合价升降法配平变价元素,再由电荷守恒确定生成 ;并确定 的系数,最后确定反应物中有
H O,并由原子守恒确定H O的系数,得反应的离子方程式为:
2 2
;答案为:
;
;
(2)① 与烧碱反应生成 , 元素的化合价均为 ,发生非氧化还原反应,另外生成
和 ;结合原子守恒可得化学方程式为:
;
②“调 ”时,反应生成 , 元素的化合价不变,根据原子守恒配平所发生反
应的离子方程式;结合电子转移守恒、电荷守恒、原子守恒可得离子方程式为
资料收集整理【淘宝店铺:向阳百分百】 10
学科网(北京)股份有限公司;滤渣Ⅲ 经
高温焙烧分解即可得到 ;
答案为: ;
;高温焙烧。
4.(2023·云南·校联考二模)六水合氯化镍(NiCl ·6H O)常用于电镀、陶瓷等工业。某实验室以镍矿渣(主要
2 2
含NiS、CuS、FeS)制备六水合氯化镍晶体,设计流程如图所示:
已知: K (NiS)= 1.07×10-21, K (CuS)= 1.27×10-26。
sp sp
回答下列问题:
(1)①写出“酸溶”时,NiS发生反应的离子方程式:_______。
②“酸溶”时,为减少生产过程对大气的污染,通常还需通入过量的_______(填气体名称)。
(3)“除铜”过程发生反应的离子方程式是_______,若要求溶液中Cu2+浓度小于1×10-5mol/L,则应控制溶液
中Ni2+浓度_______。(结果保留两位小数)
【答案】(1) 3NiS+8H++2 =3Ni2++3S+2NO↑+4H O 空气
2
(3) NiS+ Cu2+= CuS + Ni2+ 大于0.84mol/L
【解析】某实验室以镍矿渣(主要含NiS、CuS、FeS)制备六水合氯化镍晶体,加入稀硫酸和稀硝酸进行酸溶,
该过程中-2的S元素被氧化为S单质,过滤除去,滤液中的溶质为Ni2+、Cu2+和Fe3+,向滤液中加入试剂a
调节pH使Fe3+转化为Fe(OH) 沉淀,该过程不能引入新的杂质,试剂a为Ni(OH) ,过滤后向滤液中加入NiS
3 2
沉淀Cu2+,然后加入试剂b沉镍。
(1)①“酸溶”时,NiS和稀硝酸发生氧化还原反应生成S单质和NO,根据氧化还原反应的规律配平离子
方程式为:3NiS+8H++2 =3Ni2++3S+2NO↑+4H O;
2
②“酸溶”时会产生NO污染空气,可以先通入过量的空气氧化NiS,再加入稀硝酸酸化。
资料收集整理【淘宝店铺:向阳百分百】 11
学科网(北京)股份有限公司(3)“除铜”过程中NiS和Cu(NO ) 反应生成CuS和Ni(NO ) ,离子方程式为:NiS+ Cu2+= CuS + Ni2+;若要
3 2 3 2
求溶液中Cu2+浓度小于1×10-5mol/L,则溶液中c(S2-)= ,溶液
中Ni2+浓度c(Ni2+)= ,若要求溶液中Cu2+浓度小于1×10-5mol/L,则应
控制溶液中Ni2+浓度大于0.84mol/L。
5.(2023·海南海口·海南华侨中学校考二模)穿甲弹的弹芯用钨合金制造。工业上以黑钨矿(主要成分是
FeWO 、MnWO ,含少量的Fe O 、SiO )为原料冶炼钨的流程如图所示。
4 4 2 3 2
已知:钨酸H WO 难溶于水。
2 4
回答下列问题:
(1)浸取在加热、通空气条件下进行,FeWO 转化为Na WO 的化学方程式为________________。
4 2 4
【答案】(1)
【解析】黑钨矿(主要成分是FeWO 、MnWO ,含少量的Fe O 、SiO )中加入Na CO 浸取,生成Na WO 、
4 4 2 3 2 2 3 2 4
Na SiO 、Fe O 等,过滤分离出Fe O ;往滤液中加入HCl、调溶液的pH=8,Na SiO 转化为H SiO 等,过滤
2 3 2 3 2 3 2 3 2 3
得滤液;往滤液中加入CaCl 溶液,生成CaWO 等;加入盐酸发生反应,将CaWO 转化为H WO 沉淀;再
2 4 4 2 4
加氨水溶解,H WO 转化为(NH ) WO 进入溶液,过滤得滤液;将滤液经过系列操作X,使(NH ) WO 转化为
2 4 4 2 4 4 2 4
仲钨酸铵 析出并分离;煅烧后生成WO ;加入还原剂,将WO 还原为W。
3 3
(1)浸取在加热、通空气条件下进行,FeWO 转化为Na WO ,同时有O 参加反应,生成Fe O 等,化学
4 2 4 2 2 3
方程式为 。答案为:
;
资料收集整理【淘宝店铺:向阳百分百】 12
学科网(北京)股份有限公司6.(2023·安徽淮南·统考一模)锌的用途广泛,主要用于镀锌板及精密铸造等行业。以粗氧化锌(主要成分
为ZnO及少量Fe O 、CuO、MnO、SiO )为原料制备锌的工艺流程如图所示:
2 3 2
已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH ) ]2+、[Cu(NH ) ]2+进入溶液:
3 4 3 4
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中 ≤2.0×10-6
回答下列问题:
(2)“氧化除锰”时,H O 将Mn2+转化为难溶的MnO ,该反应的离子方程式为___________。
2 2 2
【答案】(2)Mn2++H O +2NH ·H O=MnO +2H O+2
2 2 3 2 2 2
【解析】粗氧化锌主要成分为ZnO及少量Fe O 、CuO、MnO、SiO ,加入NH -NH Cl的混合溶液,生成
2 3 2 3 4
[Zn(NH ) ]2+、[Cu(NH ) ]2+,同时生成Fe(OH) 、Mn(OH) 等,SiO 不溶解,进行操作1即过滤一起除去,得滤
3 4 3 4 3 2 2
渣1为Fe(OH) 、Mn(OH) 和SiO ,再向滤液中加入H O ,进行氧化除锰,反应的方程式为H O +Mn2+
3 2 2 2 2 2 2
+2NH •H O=MnO ↓+2H O+2 ,再加入(NH ) S,进行沉淀除铜,反应的方程式为[Cu(NH ) ]2++S2-
3 2 2 2 4 2 3 4
=CuS↓+4NH ,进行操作2即过滤,除去MnO 和CuS,即滤渣2为MnO 和CuS,向滤液中加入萃取剂,使
3 2 2
锌进入有机萃取剂中,进行操作3即分液后,再向有机萃取剂中加入硫酸,进行反萃取,得到硫酸锌溶液,
然后进行电解,得到锌,据此分析作答。
(2)由分析可知,“氧化除锰”时,H O 将Mn2+转化为难溶的MnO ,该反应的离子方程式为Mn2+
2 2 2
+H O +2NH ·H O=MnO +2H O+2 ,故答案为:Mn2++H O +2NH ·H O=MnO +2H O+2 ;
2 2 3 2 2 2 2 2 3 2 2 2
7.(2023·山西吕梁·统考二模)以萃铜余液为原料制备工业活性氧化锌,其生产工艺流程如图所示:
资料收集整理【淘宝店铺:向阳百分百】 13
学科网(北京)股份有限公司(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na S O )氧化法除锰,写出Mn2+被氧化成MnO 的离子方
2 2 8 2
程式___________ ; 采用石灰石粉中和除去铝和铁,则中和渣中主要成分为___________。
(3)用锌粉除镉(Cd2+ )的离子方程式为___________;沉锌生成碱式碳酸锌[2Zn(OH )·ZnCO ·H O]的化学方程式
2 3 2
为___________。
(5)煅烧炉中发生反应的化学方程式为___________,工艺流程设计中选用高效真空负压内转盘浓缩沉锌后
液一体化设备生产无水___________,蒸发生产过程可实现零排放。
【答案】(1) Mn2+ + +2H O= MnO +2 +4H+ MnO 、Al(OH) 、 Fe(OH)
2 2 2 3 3
(3) Zn+Cd2+=Zn2++Cd 3ZnSO + 3Na CO +3H O= 2Zn(OH) ·ZnCO ·H O↓+3Na SO + 2CO ↑
4 2 3 2 2 3 2 2 4 2
(5) 2Zn(OH) ·ZnCO ·H O 3ZnO+CO ↑+3H O Na SO 或硫酸钠
2 3 2 2 2 2 4
【解析】由流程可知,向萃铜余液中加入石灰石粉和氧化剂,余液中Mn2+、Fe2+被氧化生成MnO 、氢氧化
2
铁,反应过程中生成硫酸钙沉淀,过滤得到MnO 、氢氧化铁、硫酸钙,和“氧化除锰”的余液﹔向余液
2
中加入Zn, Zn与Cd2+发生置换反应生成Cd,过滤得到除去Cd2+的滤液;加入有机溶剂萃取,除去钴、镍,
分液得到硫酸锌溶液,向硫酸锌溶液中加入碳酸钠溶液﹐硫酸锌转化为ZnCO ·2Zn(OH) ·H O晶体,过滤得
3 2 2
到ZnCO ·2Zn(OH) ·H O晶体,煅烧、粉碎得到工业活性氧化性。
3 2 2
(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na S O )氧化法除锰,Mn2+被氧化成MnO ,过硫酸根
2 2 8 2
离子被还原为硫酸根离子,离子方程式为:Mn2+ + +2H O= MnO +2 +4H+;由分析可知,中和渣
2 2
中主要成分为MnO 、Al(OH) 、 Fe(OH) ;
2 3 3
(3)锌与镉离子发生取代反应生成锌离子和单质镉,离子方程式为:Zn+Cd2+=Zn2++Cd;向硫酸锌溶液中加
入碳酸钠溶液生成碱式碳酸锌,相应的方程式为:3ZnSO + 3Na CO +3H O= 2Zn(OH) ·ZnCO ·H O↓+3Na SO +
4 2 3 2 2 3 2 2 4
2CO ↑;
2
(5)由流程可知,工业碱式碳酸锌在煅烧炉中煅烧生成活性氧化锌,则相应的方程式为:
资料收集整理【淘宝店铺:向阳百分百】 14
学科网(北京)股份有限公司2Zn(OH) ·ZnCO ·H O 3ZnO+CO ↑+3H O;加入有机溶剂萃取,除去钴、镍,分液得到硫酸锌溶液,向
2 3 2 2 2
硫酸锌溶液中加入碳酸钠溶液﹐硫酸锌转化为ZnCO ·2Zn(OH) ·H O晶体,同时得到硫酸钠溶液,则工艺流
3 2 2
程设计中选用高效真空负压内转盘浓缩沉锌后液一体化设备生产无水Na SO 或硫酸钠。
2 4
1.(2023·山东潍坊·统考二模)钛及其合金具有密度小、比强度高、耐热、耐低温等特性,是制造飞机、
火箭等的优异材料。工业上以钛铁矿(主要成分为 ,含 的氧化物等杂质)制备钛和
的工艺流程如图:
已知:① 时相关物质的 见下表:
物质
②I. ,
Ⅱ. ,
回答下列问题:
(1)“酸浸”时 元素转化为 , 发生反应的离子方程式为___________。
(5)“沉铁”操作单元发生反应的化学方程式为________。
资料收集整理【淘宝店铺:向阳百分百】 15
学科网(北京)股份有限公司【答案】(1)
(5)
【解析】钛铁矿(主要成分为 ,含 的氧化物等杂质)加入硫酸酸浸,得到滤渣Ⅰ为二氧化
硅等;滤液加入过量铁粉将Fe3+还原为Fe2+,与硫酸反应,有利于 水解,除去滤渣Ⅱ为过量的铁粉,
所得滤液加入热水水解,滤液再加氨水调节pH除去滤渣Ⅲ为氢氧化铝,继续加入氨水并通入空气进行沉
铁,得到 ;水解后的 通入氯气,高温条件下与碳粉氯化,再蒸馏,与氯化钠、氯
化钾一样熔融后电解得到钛;
(1)“酸浸”时 元素转化为 , 发生反应生成硫酸亚铁、二氧化钛和水,反应的离子方程式
为 ;
(5)发生反应的化学方程式为 。
2.(2023·全国·模拟预测) 主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含
Co、Fe,还含有少量的CoO、FeO、 、CaO、 )制备氧化钴( )的工艺流程如图所示。
已知:i.黄钠铁矾的化学式为 ;
ii.金属钴与铁具有相似的化学性质;
iii.氧化性 。
回答下列问题:
资料收集整理【淘宝店铺:向阳百分百】 16
学科网(北京)股份有限公司(3)除铁时先加入NaClO溶液,主要反应的离子方程式为___________,
(5) 在空气中加热煅烧得到 的化学方程式是___________。
【答案】(3) 滴入几滴KSCN溶液,振荡,溶液不变红
(5)
【解析】含钴催化剂废料加入硫酸酸浸过滤后,滤渣主要为二氧化硅和硫酸钙;滤液含有Fe2+、Fe3+、
Co2+等;加入次所酸钠可将Fe2+氧为化Fe3+,加入碳酸钠溶液调节pH,除铁得到黄钠铁矾沉淀;继续加入碳
酸钠溶液沉钴1,得到滤液1和CoCO 沉淀,沉淀加入盐酸溶解,再加入草酸铵溶液进行沉钴2,得到滤液
3
2主要成分为氯化铵,沉淀为草酸钴晶体,煅烧得到Co O ;
2 3
(3)除铁时加入NaClO,可将 氧化为 [提示:黄钠铁矾中铁的化合价为+3],同时次氯酸根离子被
还原为氯离子,主要反应的离子方程式为 ;检验铁元素的离子即
已被完全沉淀的实验操作及现象为取少量待测液于试管中,滴入几滴KSCN溶液,振荡,溶液不变红;
((5) 在空气中加热煅烧,得到 ,Co由+2价升高到+3价,所以有 参加反应,
也被氧化为煅烧 ,故化学方程式为 ;
3.(2020春·北京海淀·高三人大附中阶段练习)铜银合金在现代工业中有广泛应用。从铜银合金切割废料
(不含其它金属)中回收银并制备铜化工产品的工艺如图。
资料收集整理【淘宝店铺:向阳百分百】 17
学科网(北京)股份有限公司(2)滤渣A溶于稀硝酸时产生无色气体,该反应的离子方程式为___________。
(3)在混料池中,将三种原料按一定的物质的量之比混合均匀,煮沸,过滤。将滤渣B在200℃下翻炒至质
量不再变化,得到固体C.C只含CuO、Al O ,物质的量之比为2:1。在惰性气体保护下,将C在煅烧釜
2 3
中高温灼烧,得到CuAlO 该反应的方程式为___________。
2.
(5)冷却银熔体得到的粗银可使用电解法精炼,精炼池中阳极的电极反应为___________。
【答案】(2)3Ag+ +4H+=3Ag++NO↑+2H O
2
(3)4CuO+2Al O =4CuAlO +O ↑
2 3 2 2
(5)Ag-e-=Ag+,Cu-2e-=Cu2+
【解析】由工艺流程图可知,废料在富氧空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣
中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫
酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al O ,二者反应得到CuAlO ,二者反应
2 3 2
得到CuAlO 。
2
(2)用稀硝酸溶解银,反应生成硝酸银、NO气体和水,离子方程式为:3Ag+NO ﹣+4H+═3Ag+
3
+NO↑+2H O,故答案为:3Ag+NO ﹣+4H+═3Ag++NO↑+2H O;
2 3 2
(3)由上述分析可知,CuO、Al O 反应得到CuAlO ,由电荷守恒可知,O元素化合价升高,有氧气生成,
2 3 2
反应前Cu为+2价,反应后为+1,化合价降低1,反应前氧为﹣2价,反应后为0,化合价升高2,两者的
最小公倍数是2,再根据原子守恒得:4CuO+2Al O =4CuAlO +O ↑,故答案为:
2 3 2 2
4CuO+2Al O =4CuAlO +O ↑;
2 3 2 2
(5)冷却银熔体得到的粗银中含有少量的铜,可使用电解法精炼,精炼池中阳极的电极反应为Ag﹣e﹣
=Ag+,Cu﹣2e﹣=Cu2+,故答案为:Ag﹣e﹣=Ag+,Cu﹣2e﹣=Cu2+;
4.(2021·广东·高考真题)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、
镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
资料收集整理【淘宝店铺:向阳百分百】 18
学科网(北京)股份有限公司已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
【答案】 + = ↓
【解析】(1)①滤液II中含有钼酸钠,加入氯化钡溶液后生成 沉淀,该反应的离子方程式为
+ = ↓。
5.(2020·全国·高考真题)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、
镁的铝硅酸盐,以及SiO 、Fe O 。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
资料收集整理【淘宝店铺:向阳百分百】 19
学科网(北京)股份有限公司回答下列问题:
(1)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有___________离子被氧化。写出VO+转化为 反
应的离子方程式___________。
(2)“沉淀转溶”中, 转化为钒酸盐溶解。滤渣③的主要成分是___________。
【答案】 (1) VO++MnO +2H+= +Mn2++H O
2 2
(2)NaAlO +HCl+H O=NaCl+Al(OH) ↓或Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O
2 2 3 4 3 2
【解析】(1)“酸浸氧化”中,钒矿粉中的Fe O 与硫酸反应生成FeSO 、Fe (SO ) 和水,MnO 具有氧化性,
3 4 4 2 4 3 2
Fe2+具有还原性,则VO+和VO2+被氧化成 的同时还有Fe2+被氧化,反应的离子方程式为MnO +2Fe2+
2
+4H+=Mn2++2Fe3++2H O;VO+转化为 时,钒元素的化合价由+3价升至+5价,1molVO+失去2mol电子,
2
MnO 被还原为Mn2+,Mn元素的化合价由+4价降至+2价,1molMnO 得到2mol电子,根据得失电子守恒、
2 2
原子守恒和电荷守恒,VO+转化为 反应的离子方程式为VO++MnO +2H+= +Mn2++H O,故答案为:
2 2
Fe2+,VO++MnO +2H+= +Mn2++H O;
2 2
(2)“调pH”中有沉淀生成,是NaAlO 与HCl反应生成Al(OH) 沉淀,生成沉淀反应的化学方程式是
2 3
NaAlO +HCl+H O=NaCl+Al(OH) ↓或Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O,故答案为:
2 2 3 4 3 2
NaAlO +HCl+H O=NaCl+Al(OH) ↓或Na[Al(OH) ]+HCl= NaCl+Al(OH) ↓+H O。
2 2 3 4 3 2
6.(2021·海南·高考真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废
铁屑(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
资料收集整理【淘宝店铺:向阳百分百】 20
学科网(北京)股份有限公司回答问题:
(1)反应 的化学方程式为___________。
【答案】(1)
【解析】(1)根据已知信息氯化亚砜( )熔点-101℃,沸点76℃,易水解,可得 与
SOCl 生成FeCl 的化学方程式为 。
2 3
资料收集整理【淘宝店铺:向阳百分百】 21
学科网(北京)股份有限公司