文档内容
微专题 43 常见物质的检验、分离和提纯
1.(2023·辽宁·统考高考真题)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别Na CO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验Na SO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
2.(2023·浙江·统考高考真题)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl
和泥沙)的提纯方案如下:
下列说法不正确的是
A.操作I中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹D.操作Ⅳ可用冷水洗涤晶体
1.常见阳离子检验
(1)常规检验法。
①用NaOH溶液能检验出Cu2+、Fe3+、Fe2+、Al3+、NH+
。
4
【答案】①蓝 红褐 白 灰绿 红褐 白 白 蓝
②焰色反应:用焰色反应可检验出溶液中的K+和Na+。
【答案】②紫 黄
(2)特殊检验法。
【答案】(2)红
[注意]①检验Fe2+和Fe3+时,一般应用特殊检验法。
②注意不能利用酸性KMnO 溶液检验FeCl 溶液中的Fe2+,因为KMnO (H+)会氧化Fe2+也会氧化Cl-。
4 2 4
2.常见阴离子检验
(1)利用酸碱指示剂检验。
【答案】(1)红 蓝(2)利用盐酸和其他试剂检验。
【答案】(2)白 无色无味 无色无味 白 白 刺激性 退色
(3)利用AgNO (HNO 酸化)溶液检验。
3 3
【答案】(3)白 浅黄 黄
(4)利用某些特征反应检验。
I-→滴入淀粉溶液和新制氯水,溶液变 色。
【答案】(4)蓝
[注意]①HC 与C 均会与盐酸反应产生CO ,所以要注意区分。②I-的特征反应检验方法中,氧化剂可以是
O- O2- 2
3 3
氯水,也可以是Fe3+或H O 等物质。
2 2
3.气体的检验
(1)可燃性气体的检验。
(2)酸性气体的检验。【答案】 (2)先变浑浊后变澄清 退去 出现红色 变红 白烟 白色沉淀
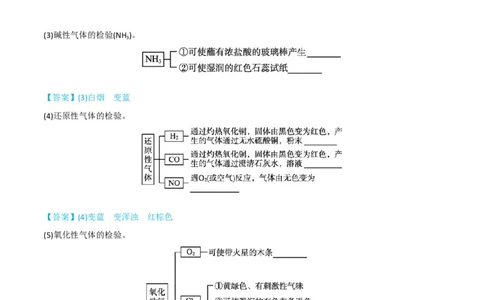
(3)碱性气体的检验(NH )。
3
【答案】(3)白烟 变蓝
(4)还原性气体的检验。
【答案】(4)变蓝 变浑浊 红棕色
(5)氧化性气体的检验。
【答案】(5)复燃 变蓝 变红 变蓝
4.有机化合物的检验物质 试剂与方法 现象与结论
饱和烃与 加入溴水或酸性
退色的是
不饱和烃 KMnO 溶液
4
苯与苯的
加酸性KMnO 溶液 退色的是
4
同系物
醛基 加银氨溶液、水浴加热 有 产生
化合物 加新制Cu(OH) 悬浊液、加热 煮沸后有 生成
2
醇 加乙酸、浓硫酸 有果香味液体生成
加Na CO 溶液 有气体逸出
2 3
羧酸
加紫色石蕊溶液 溶液显
淀粉 加碘水 溶液显
灼烧 有
蛋白质 显 (只用于检验部
加浓硝酸微热
分蛋白质)
【答案】不饱和烃 苯的同系物 银镜 砖红色沉淀 红色 蓝色 烧焦羽毛气味 黄色
5.物质分离、提纯常用的物理方法
(1)“固+固”混合物的分离(提纯)。
(2)“固+液”混合物的分离(提纯)。
(3)“液+液”混合物的分离(提纯)。
(4)物质分离、提纯常用物理方法的装置及注意事项。
方法、装置 适用范围 注意事项(1)一贴滤纸紧贴漏斗内壁
二低:滤纸低于滤纸液面低于漏斗边缘
把不溶性固体物质和液体进行分离
三靠:烧杯紧靠滤纸边缘,玻璃棒轻靠玻璃棒处,漏
斗下端紧靠三层滤纸
(2)若滤液浑浊,需烧杯内壁
过滤
(1)玻璃棒的作用:搅拌,防止局部温度过高造成再
分离溶于溶剂中的溶质 次过滤
(2)当液滴飞溅时,停止加热,用余热蒸干
蒸发
(1)溶质在萃取剂中的溶解度比在原溶剂中有大
(1)萃取:利用溶质在互不相溶的溶剂
量固体析出
里的溶解度不同,用一种溶剂把溶质
(2)萃取剂与原溶剂要大得多不互溶
从另一种溶剂里提取出来
(2)分液:两种液体互不相溶且易分层 (3)分液时,分液漏斗中的下层液体从下口流出,上
层液体从上口倒出
萃取和分液
(1)温度计的水银球在蒸馏烧瓶的支管口处
沸点相差较大的液体混合物 (2)蒸馏烧瓶要加沸石或碎瓷片
(3)冷凝管水流方向应为“下进上出”
应与物质的分解变化区分,如分解反应:NH Cl
4
某种组分易升华的混合物,利用物质
NH ↑+HCl↑
3
升华的性质在加热条件下分离的方法
升华
6.物质分离、提纯的化学方法
方 法 原 理 杂质成分
沉淀法 将杂质离子转化为沉淀
Cl-、SO2- 、CO2-
及能形成难溶性弱碱的金属阳离子
4 3
气化法 将杂质离子转化为气体
CO2-、HCO- 、SO2-、HSO- 、S2-、NH+
3 3 3 3 4
杂转 杂质中含不同价态的相同元素(加氧化剂或还原剂)、同一种
将杂质转化为需要提纯的物质
纯法 酸的正盐与酸式盐(加酸、酸酐或碱)
氧化还 用氧化剂(还原剂)除去具有还 如用酸性高锰酸钾溶液除去CO 中的SO ,用铜粉除去N 中
2 2 2
原法 原性(氧化性)的杂质 的O 2热分
加热使不稳定的物质分解除去 如除去NaCl中的NH Cl等
4
解法
酸碱溶 利用物质与酸或碱溶液混合后
如用过量的氢氧化钠溶液可除去Fe O 中的Al O
解法 的反应进行提纯 2 3 2 3
粗铜作为阳极、纯铜作为阴极,含Cu2+的盐溶液作电解质溶
电解法 利用电解原理除去杂质
液
加入试剂调节溶液pH,使溶液 如向含有Cu2+和Fe3+的溶液中加入CuO、CuCO 或
调pH法 3
中某种成分生成沉淀而分离 Cu (OH) CO 等调节pH使Fe3+转化为Fe (OH) 而除去
2 2 3 3
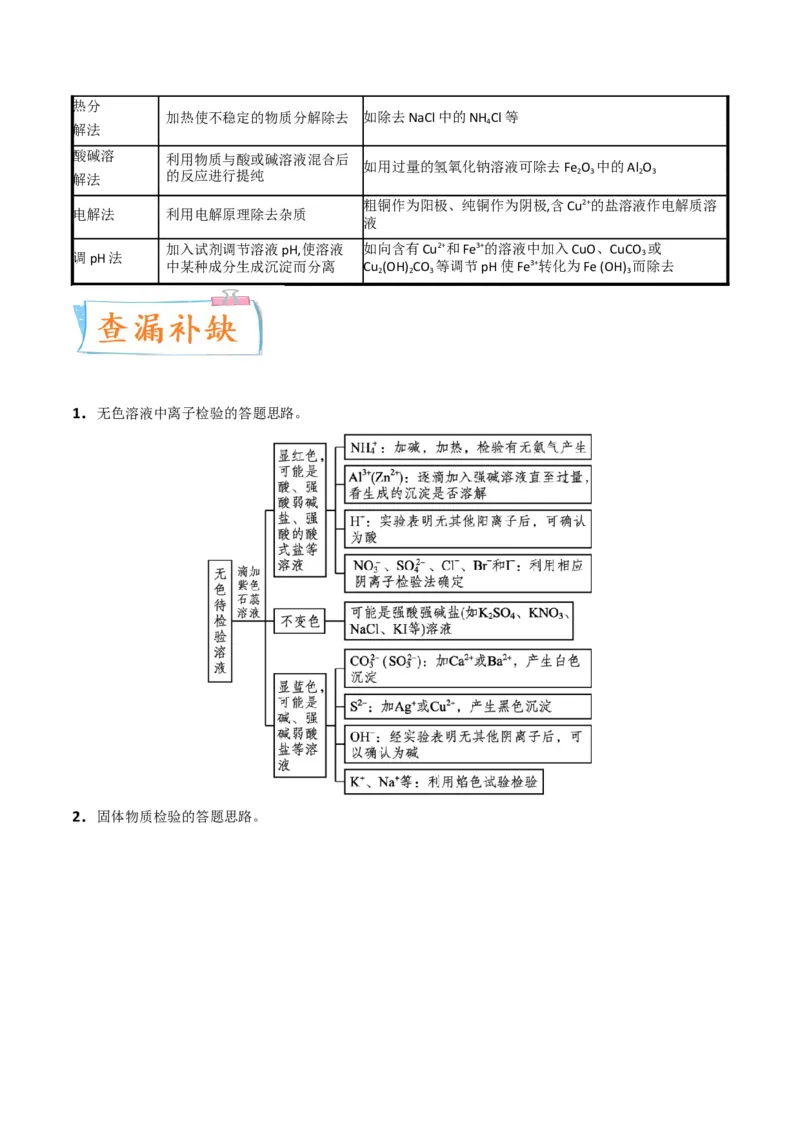
1.无色溶液中离子检验的答题思路。
2.固体物质检验的答题思路。3.物质分离、提纯的区别
(1)物质的分离。
将混合物中的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯。
将混合物中的杂质除去而得到纯净物的过程,又叫混合物的净化或除杂。
【易错提醒】
提纯的“四个原则”及“四个必须”
(1)“四个原则”:一是不增加新的杂质;二是不减少被提纯物质;三是被提纯物质与杂质易分离;四是被提纯物
质易复原。
(2)“四个必须”:一是除杂试剂必须过量;二是过量试剂必须除尽;三是除杂途径必须最佳;四是除去多种杂质
时必须考虑加入试剂的先后顺序。
4.分离、提纯题的答题步骤
第一步:确定被提纯物质与除杂对象
对比两者物理性质、化学性质的差异,利用差异性(溶解度差异、密度差异、熔沸点差异、与某些物质反应
的差异性等),选择合适的分离原理或除杂试剂;除杂试剂除去杂质的同时,不消耗被提纯物质,不引入新的杂质。
第二步:选择合适的分离或除杂装置
根据分离原理选择合适的分离装置(过滤、分液、蒸馏等);根据除杂试剂的状态及反应条件,选择合适的装置,
液体试剂一般选洗气瓶,固体试剂一般用干燥管或U形管。
第三步:综合分析,合理解答
综合分析物质分离是否完全,被提纯物质中的杂质是否被除去。
5.物质检验的基本原则和方法
物质检验的“三原则”:一看(颜色、状态)、二嗅(气味)、三实验(加试剂)。根据实验时生成物所表现的现象
不同,检验离子的方法可归纳为四类:(1)生成气体,如N
H+
、C
O2-
的检验;
4 3
(2)生成沉淀,如Cl-、S 的检验;
O2-
4
(3)显现特殊颜色,如Fe3+、苯酚的检验;
(4)焰色反应,如Na+、K+的检验。
(5)气体检验中干扰因素的排除。
气体检验中干扰因素的排除方法一般是先检验出一种可能会产生干扰的气体,并除去该气体,而且要确认该
气体已经除尽,再检验其余气体。如在SO 存在的条件下检验CO ,可设计如下检验思路:品红溶液检验SO →
2 2 2
酸性高锰酸钾溶液除去SO →品红溶液检验SO 是否除尽→澄清石灰水检验CO 。与此类似的还有检验实验
2 2 2
室制取的乙烯中含有SO 等。
2
1.(2023·湖南·统考高考真题)下列玻璃仪器在相应实验中选用不合理的是
A.重结晶法提纯苯甲酸:①②③ B.蒸馏法分离CH Cl 和CCl :③⑤⑥
2 2 4
C.浓硫酸催化乙醇制备乙烯:③⑤ D.酸碱滴定法测定NaOH溶液浓度:④⑥
2.(2022·广东·高考真题)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放
入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A.加入 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现 D.加入 溶液无蓝色沉淀生成1.(2023上·辽宁·高三校联考期中)下列离子检验所用试剂或实验现象错误的是
离子 试剂 现象
A 氯水和淀粉溶液 溶液显蓝色
B 稀盐酸和 溶液 加稀盐酸无现象,加 溶液后生成白色沉淀
浓NaOH溶液和湿润的蓝色 在加热条件下,产生有刺激性气味的气体,且气体能使湿润的
C
石蕊试纸 蓝色石蕊试纸变红
D KSCN溶液 溶液变为红色
A.A B.B C.C D.D
2.(2023下·全国·高三统考阶段练习)有一包白色粉末,可能含有 ,取少量样
品进行如下实验,该白色粉末一定含有的物质是
①将粉末加入水中,充分振荡,有白色沉淀;
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
③取少量②的溶液于试管中,滴加 溶液,有白色沉淀。
A. B.
C. D.
3.(2023上·黑龙江哈尔滨·高三哈九中校考阶段练习)某溶液中可能含有K+、 、Fe2+、Al3+、Cl-、
、 、 中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为0.1 mol/L。某同学进行了如
下实验,下列说法正确的是A.沉淀Ⅰ一定有BaSO ,可能含有BaCO B.沉淀Ⅲ具有两性
4 3
C.溶液中一定有 、Fe2+、Cl-、 D.需要通过焰色试验确定是否含有K+
4.(2023上·江西赣州·高三校联考期中)下列各组物质的鉴别方法错误的是
选项 物质 鉴别方法
A CO(g)和 分别通入澄清石灰水
B 和 分别取少许试剂加入金属钠
和 分别取少许试剂加入 溶
C
液
D 和 分别取少许固体加入盐酸中
A.A B.B C.C D.D
5.(2023上·辽宁沈阳·高三校联考期中)下列有关物质检验和鉴别的说法错误的是
A.用焰色试验检验溶液中是否含K元素
B.用湿润的蓝色石蕊试纸可鉴别Cl 和HCl
2
C.用氯化钡溶液可鉴别Na CO 和Na SO 粉末
2 3 2 3
D.用KSCN溶液检验FeSO 是否变质
4
6.(2023·辽宁鞍山·统考一模)下列鉴别或检验能达到实验目的的是
A.用金属钠检验乙醇中混有少量的水
B.用硝酸银溶液鉴别氯苯与溴苯
C.用酸性高锰酸钾溶液鉴别Vc水溶液与葡萄糖溶液
D.用BaCl 溶液鉴别SO 和SO
2 2 3
7.(2023上·黑龙江牡丹江·高三牡丹江市第二高级中学校考阶段练习)铍是非常重要的军工金属,也是非
常重要的战略资源。某工厂以含氟铍矿(主要成分是BeO、Fe O 、SiO 等)为原料,生产金属铍的工艺流程如
2 3 2
下:
已知:BeO是两性氧化物,Be(OH) 是两性氢氧化物。
2下列说法错误的是
A.实验室进行操作a用到三种玻璃仪器
B.碱溶时,BeO发生的离子反应为BeO+2OH-= +H O
2
C.“沉渣”和“浸渣”的成分分别为Fe(OH) 、H SiO
3 2 3
D.从该流程可知,BeO属于电解质
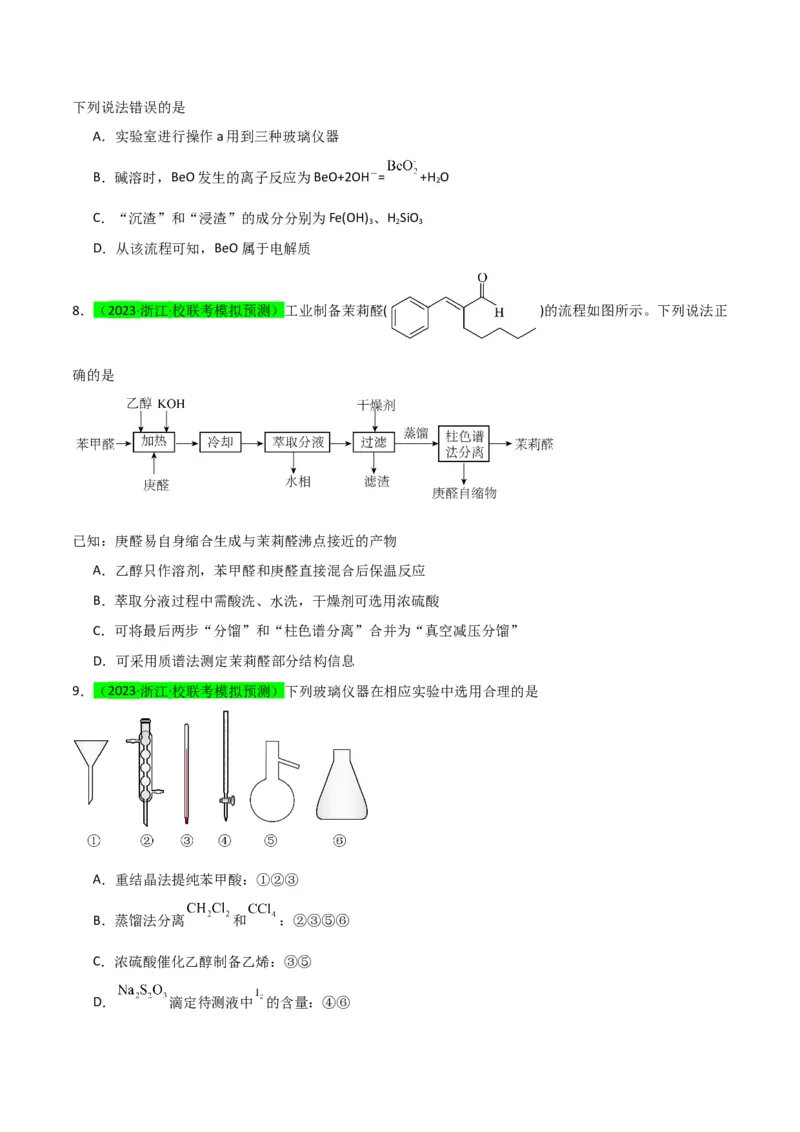
8.(2023·浙江·校联考模拟预测)工业制备茉莉醛( )的流程如图所示。下列说法正
确的是
已知:庚醛易自身缩合生成与茉莉醛沸点接近的产物
A.乙醇只作溶剂,苯甲醛和庚醛直接混合后保温反应
B.萃取分液过程中需酸洗、水洗,干燥剂可选用浓硫酸
C.可将最后两步“分馏”和“柱色谱分离”合并为“真空减压分馏”
D.可采用质谱法测定茉莉醛部分结构信息
9.(2023·浙江·校联考模拟预测)下列玻璃仪器在相应实验中选用合理的是
A.重结晶法提纯苯甲酸:①②③
B.蒸馏法分离 和 :②③⑤⑥
C.浓硫酸催化乙醇制备乙烯:③⑤
D. 滴定待测液中 的含量:④⑥10.(2023上·黑龙江齐齐哈尔·高三齐齐哈尔市恒昌中学校校考期中)以菱镁矿(主要成分为MgCO ,含少
3
量SiO 、Fe O 和Al O )为原料制备高纯镁砂的工艺流程如下:
2 2 3 2 3
已知浸出时产生的废渣中有SiO 、 和 。下列说法错误的是
2
A.流程中可循环使用的物质有NH 、NH Cl
3 4
B.浸出和沉镁的操作均不应在较高温度下进行
C.浸出镁的离子反应为
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物 的不同
1.(2023上·天津东丽·高三天津市第一百中学校考期中)对于某无色溶液中可能存在离子的检验及结论一
定正确的是
A.加入氢氧化钠溶液后用湿润的红色石蕊试纸靠近试管口,不显蓝色,一定不含
B.加入足量稀 后再滴入 溶液,有白色沉淀生成,原溶液中含有
C.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有
D.先通入 ,再加HCl溶液,有白色沉淀生成,一定有
2.(2023上·山东滨州·高三山东省滨州市沾化区第一中学校联考开学考试)下列鉴别的方法中,所用试剂、
操作或方法不正确的是
A.用Ca(OH) 溶液鉴别Na CO 溶液和NaHCO 溶液
2 2 3 3
B.用酚酞或氯水可鉴别NaI溶液和Na PO 溶液
3 4
C.鉴别NaNO 溶液和KNO 溶液;进行焰色试验
3 3
D.鉴别Fe(OH) 胶体和FeCl 溶液;利用丁达尔效应
3 33.(2023上·浙江·高三校联考开学考试)下列说法正确的是
A.可用新制氢氧化铜悬浊液鉴别甲酸甲酯、甲醛和甲酸
B.可用金属钠或无水硫酸铜检验乙醇中是否混有蒸馏水
C.氢氧化铁胶体和久置氯化铁溶液可用丁达尔效应区别
D.用Br 的CCl 溶液或酸性KMnO 溶液区别二烯烃和芳香烃
2 4 4
4.(2023·辽宁·统考高考真题)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别Na CO 与NaHCO
2 3 3
B.用KSCN溶液检验FeSO 是否变质
4
C.用盐酸酸化的BaCl 溶液检验Na SO 是否被氧化
2 2 3
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
5.(2023上·福建龙岩·高三福建省龙岩第一中学校联考期中)无水 常作为芳烃氯代反应的催化剂。
某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水 。
下列说法不正确的是
A.试剂 可以选用 溶液,其目的是氧化
B.操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗
C.操作②中,加热的同时通入 的目的是防止水解
D.反应 的化学方程式为
6.(2023上·浙江·高三慈溪中学校联考阶段练习)下述实验装置或试剂不正确的是A.分离 、 B.向容量瓶中 D.实验室制取
C.制备干燥纯净的
转移溶液
A.A B.B C.C D.D
7.(2023上·内蒙古赤峰·高三赤峰二中校考阶段练习)为提纯下列物质(括号内为杂质)选用的试剂和分离
方法都正确的是
序号 物质 试剂 分离方法
① 硝酸钾(氯化钠) 蒸馏水 重结晶
② 氨气(水蒸气) CaCl 干燥
2
③ NaCl溶液(Na S) AgCl 过滤
2
④ 乙醇(水) 金属钠 蒸馏
A.①④ B.①③ C.② D.③④
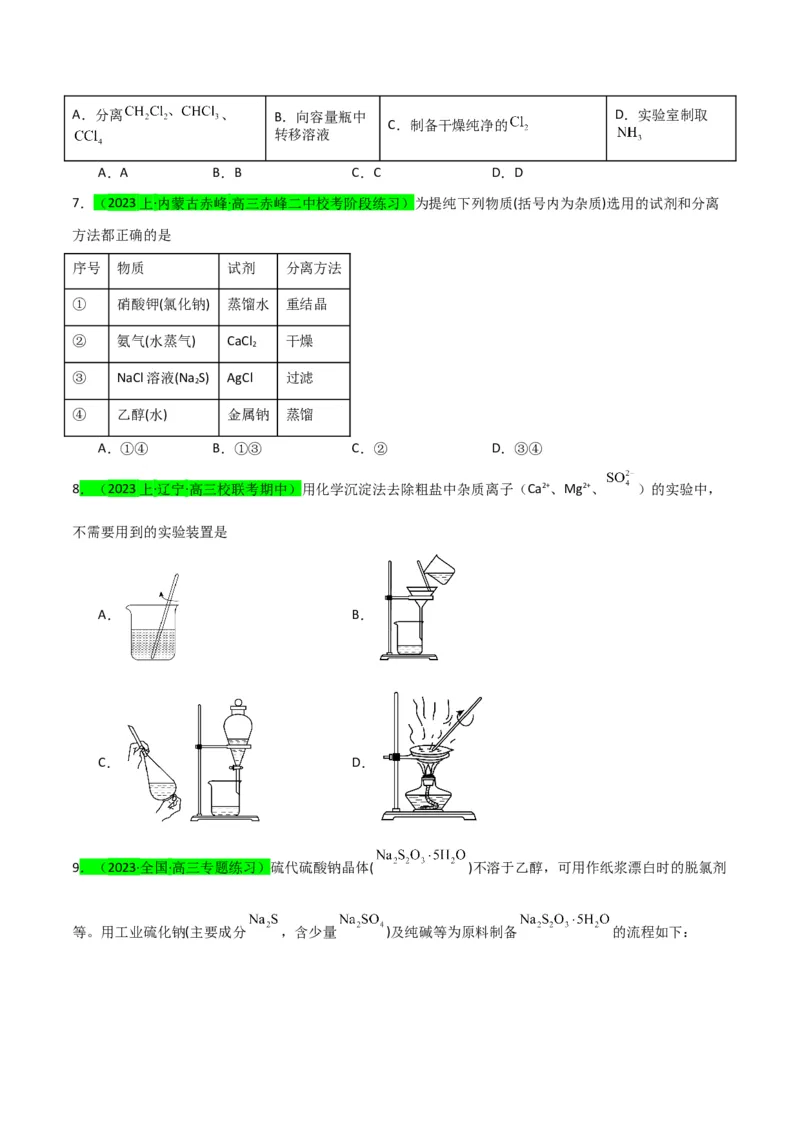
8.(2023上·辽宁·高三校联考期中)用化学沉淀法去除粗盐中杂质离子(Ca2+、Mg2+、 )的实验中,
不需要用到的实验装置是
A. B.
C. D.
9.(2023·全国·高三专题练习)硫代硫酸钠晶体( )不溶于乙醇,可用作纸浆漂白时的脱氯剂
等。用工业硫化钠(主要成分 ,含少量 )及纯碱等为原料制备 的流程如下:下列说法正确的是
A. 作脱氯剂时主要利用其还原性
B.“净化”时加入的试剂X可选用CaCl 溶液
2
C.“反应”过程中体系pH大小对产品产率无影响
D.提纯 时,应先用乙醇,再用水洗涤
10.(2023上·浙江嘉兴·高三统考阶段练习)一水硫酸四氨合铜(Ⅱ)的化学式为 是一
种重要的染料及农药中间体。某学习小组以废铜料(含少量铁及难溶性杂质)为主要原料合成该物质,合成
路线如下:
下列说法不正确的是
A.操作I中发生的主要反应为:
B.操作II中趁热过滤除去的是难溶性杂质和氢氧化铁
C.操作III中洗涤可用乙醇和水的混合液,干燥可采用减压干燥方式
D.设计操作IV的目的是为了提高乙醇的利用率