文档内容
(新高考)小题必练8:化学键与化学用语
化学用语是新高考中常常出现的考点,主要是以对同位素、原子结构、结构式、简单有机
物的命名、电子式为载体进行考查,同样化学键的类型判断也是经常涉及在元素周期推断题
中。熟练掌握相关概念定义。
1.【2020年江苏卷】反应8NH +3Cl=6NHCl+N 可用于氯气管道的检漏。下列表示相关微粒
3 2 4 2
的化学用语正确的是( )
A.中子数为9的氮原子: B.N 分子的电子式:
2
C.Cl 分子的结构式:Cl—Cl D.Cl−的结构示意图:
2
【答案】C
【解析】A项,N原子的质子数为7,中子数为9的氮原子的质量数为7+9=16,该氮原子表
示为 ,A错误;B项,N 分子中两个N原子间形成3对共用电子对,N 分子的电子式为
2 2
,B错误;C项,Cl 分子中两个Cl原子间形成1对共用电子对,Cl 分子的结构式
2 2
为Cl—Cl,C正确;D项,Cl−的核电荷数为17,核外有18个电子,Cl−的结构示意图为
,D错误;故选C。
【点睛】表示原子结构时,一定要分清中子数与质量数的区别。表示原子或者离子结构示
意图时,要看清微粒种类。
2.【2020年1月浙江省选考】有共价键的离子化合物是( )
A.NaO B.HSO C.CHCl D.SiC
2 2 2 4 2 2
【答案】A【解析】A项,NaO 中钠离子与过氧根之间为离子键,故为离子化合物,过氧根中氧原子
2 2
之间为共价价,故A正确;B项,硫酸为只含共价键的共价化合物,故B错误;C项,二氯甲烷
为只含共价键的共价化合物,故C错误;D项,碳化硅为只含共价键的共价化合物,故D错误;
故选A。
【点睛】含有离子键的化合物叫离子化合物,有些阳离子或者阴离子中也含有共价键,例
如铵根离子、氢氧根离子、酸根离子等。
3.【2020年浙江省选考】下列表示不正确的是( )
A.羟基的电子式: B.乙烯的结构简式:CHCH
2 2
C.氯原子的结构示意图: D.NH 分子的球棍模型:
3
【答案】B
【解析】A项,羟基中氧原子还有一个未成对的单电子,电子式为 ,故A正确;B项,
乙烯的官能团为碳碳双键,结构简式为CH=CH ,故B错误;C项,氯原子的核外有3个电子
2 2
层,最外层有7个电子,原子的结构示意图为 ,故C正确;D项,氨气为三角锥形的极
性分子,球棍模型为 ,故D正确;故选B。
【点睛】在书写有机物的结构简式时,要注意官能团是不能省略的。
4.【2020年浙江省选考】下列表示不正确的是( )
A.乙烯的结构式: B.甲酸甲酯的结构简式:C HO
2 4 2
C. 甲基丁烷的键线式: D.甲基的电子式:
【答案】B
【解析】A项,结构式是每一对共用电子对用一个短横来表示,乙烯分子中每个碳原子和
每个氢原子形成一对共用电子对,碳原子和碳原子形成两对共用电子对,故A正确;B项,结
构简式中需要体现出特殊结构和官能团,甲酸甲酯中要体现出酯基,其结构简式为
HCOOCH ,故B错误;C项,键线式中每个端点为一个C原子,省略C—H键,故C正确;D
3
项,甲基中碳原子和三个氢原子形成3对共用电子对,还剩一个成单电子,故D正确;故选B。
【点睛】区分清几个概念:结构式、结构简式、键线式、化学式、电子式。
1.下列关于化学键及晶体的说法中,不正确的是( )
A.Cl、Br 、I 的沸点逐渐升高,是因为分子间作用力越来越大
2 2 2
B.NaOH和NH Cl化学键类型相同
4
C.N 和CCl 两种分子中,每个原子的最外层都具有8电子稳定结构
2 4
D.石英晶体是原子晶体,其分子式为SiO
2
【答案】D
【解析】A项,Cl、Br 、I 均形成分子晶体,晶体中粒子间的作用为分子间作用力,且相对
2 2 2
分子质量逐渐增大,其分子间作用力增大,所以沸点逐渐升高,正确;B项,NaOH和NH Cl
4
中均含离子键和共价键,正确;C项,N 和CCl 的电子式分别为 ,
2 4
由此可看出分子中每个原子最外层均是8e-稳定结构,正确;D项,石英晶体为原子晶体,没
有分子,故不能说分子式,错误。
【点睛】判断化学键类型是否相同时,注意离子化合物中是否含有共价键。
2.对下列物质溶于水时破坏的作用力描述错误的是( )
A.氯化钠,破坏了离子键 B.氯化氢,破坏了共价键
C.蔗糖,破坏了分子间作用力 D.二氧化碳,没有破坏作用力
【答案】D
【解析】CO 溶于水,发生CO+HO HCO,破坏了分子间作用力,也破坏了共价键。
2 2 2 2 3
3.下列化学用语表示正确的是( )
A.HO分子的球棍模型:
2
B.三氟化氮的电子式:
C.原子核内有10个中子,8个质子的原子:D.C H 只有一种结构,甲烷分子或四氯化碳分子的比例模型表示为
3 8
【答案】C
【解析】HO分子模型中氧原子的体积相对较大,A项错误;B项F原子的未成键电子对没
2
有写出;C项质子数为6的元素是氧;C H 只能是CHCHCH,图中模型可以代表甲烷,但四
3 8 3 2 3
氯化碳不行,因为氯原子比碳原子大,D项错误。
4.下列化学用语的表示正确的是( )
A.HClO电子式: B.丙烯醛的结构简式:CH=CH-COH
2
C. 的结构示意图: D.CO 分子的比例模型:
2
【答案】C
【解析】A项,HClO中,H原子最外层有1个电子,达到稳定结构需要形成1对共用电子
对;O原子最外层有6个电子,达到稳定结构需要形成2对共用电子对;Cl原子最外层有7个
电子,达到稳定结构需要形成1对共用电子对;因此O分别和H、Cl形成一对共用电子对,其
电子式为 ,A错误;B项,醛基的结构简式为-CHO,则丙烯醛的结构简式为
CH=CHCHO,B错误;C项,S为16号元素,得到2个电子,形成S2-,其结构示意图为
2
,C正确;D项,CO 为直线型分子,其比例模型为 ,D错误;故选C。
2
【点睛】在写电子式时,可以先确定中心原子。
5.下列有关化学用语表示正确的是( )
A.质量数为31的磷原子: B.氟原子的结构示意图:
C.CaCl 的电子式: D.明矾的化学式:Al (SO )
2 2 4 3
【答案】A
【解析】A项,磷原子的质子数是15,质量数是31,故A正确;B项,氟原子是9号元素,核
外电子数为9,所以原子结构示意图: ,故B错误;C项,离子化合物中阴、阳离子间隔排列,其电子式中离子分开写,不能合并,CaCl 的电子式: ,故C错误;D项,
2
明矾是十二水合硫酸铝钾,即KAl(SO )·12H O,故D错误;故选A。
4 2 2
6.下列有关化学用语表示正确的是( )
A.中子数为143、质子数为92的铀(U)原子
B.CCl 的电子式:
4
C.乙炔的结构式:HC≡CH
D.丙烷的球棍模型:
【答案】D
【解析】A项,中子数为143、质子数为92,则质量数=143+92=235,该铀(U)原子表示为
,不是子 ,A错误;B项,CCl 的电子式: ,B错误;C项,乙炔的结构式:H-
4
C≡C-H,HC≡CH为乙炔的结构简式,C错误;D项,丙烷的球棍模型: ,D正确。故选
D。
7.下列说法不正确的是( )
A.HF比HCl稳定性更强,原因是HF分子间存在氢键
B.Na投入到水中,有共价键的断裂与形成
C.CCl 、N 和SiO 晶体中,各原子最外层都达到8电子稳定结构
4 2 2
D.NaHSO 晶体熔融时,离子键被破坏,共价键不受影响
4
【答案】A
【解析】A项,非金属性:F大于Cl,HF的键能较大,所以HF比HCl稳定性更强,故A错
误;B项,Na投入到水中,反应生成氢氧化钠和氢气,反应过程中有共价键H-O键的断裂与
H-H的形成,故B正确;C项,CCl 、N 和SiO 晶体中,各原子通过形成共用电子对,最外层
4 2 2
都达到8电子稳定结构,故C正确;D项,NaHSO 晶体熔融时,NaHSO=Na++
4 4
HSO,Na+与HSO间离子键被破坏,HSO中共价键不受影响,故D正确;故选A。
8.下列说法不正确的是( )A.有化学键断裂的过程不一定是化学过程
B.NH Cl和NaSO 晶体中含有的化学键类型相同
4 2 4
C.HO比HS更稳定,是因为氧的非金属性更强
2 2
D.离子晶体中一定含有离子键,分子晶体中一定含有共价键
【答案】D
【解析】A项,化学反应一定有旧键的断裂和新键的形成,有化学键断裂过程中,不一定发
生了化学变化,如氯化氢溶于水,只破坏共价键,没有形成化学键,故A正确;B项,NH Cl中
4
铵根离子与氯离子之间存在离子键,N与H之间存在共价键,NaSO 晶体钠离子与硫酸根离
2 4
子之间存在离子键,O与S之间存在共价键,所以二者中均含有共价键和离子键,化学键类
型相同,故B正确;C项,元素的非金属性越强,其氢化物越稳定,非金属性:O>S,所以HO
2
比HS更稳定,故C正确;D项,单原子分子中没有化学键,如稀有气体为单原子分子,则形
2
成的晶体中没有共价键,离子晶体中一定含有离子键,故D错误;故选D。
9.下列说法正确的是( )
A.食盐与石英熔化时,克服微粒间的作用力相同
B.SiHFBr 分子中所有原子的最外层均为8个稳定结构
2
C.重水在3.8℃时就变成了“热冰”,可能与重水分子间存在氢键有关
D.NaHSO 加热融化时破坏了该物质中的离子键和共价键
4
【答案】C
【解析】A项,食盐是离子晶体,熔化时破坏离子键,石英是原子晶体,熔融时破坏共价键,
故A错误;B项,SiHFBr 中氢原子最外层有1个电子,其化合价是+1价,所以不能满足最外
2
层8电子结构,故B错误;C项,重水在3.8℃时就变成了“热冰”,是因为重水分子间存在
氢键,故C正确;D项,NaHSO 加热融化电离得到钠离子和硫酸氢根离子,破坏了离子键,故
4
D错误;故选C。
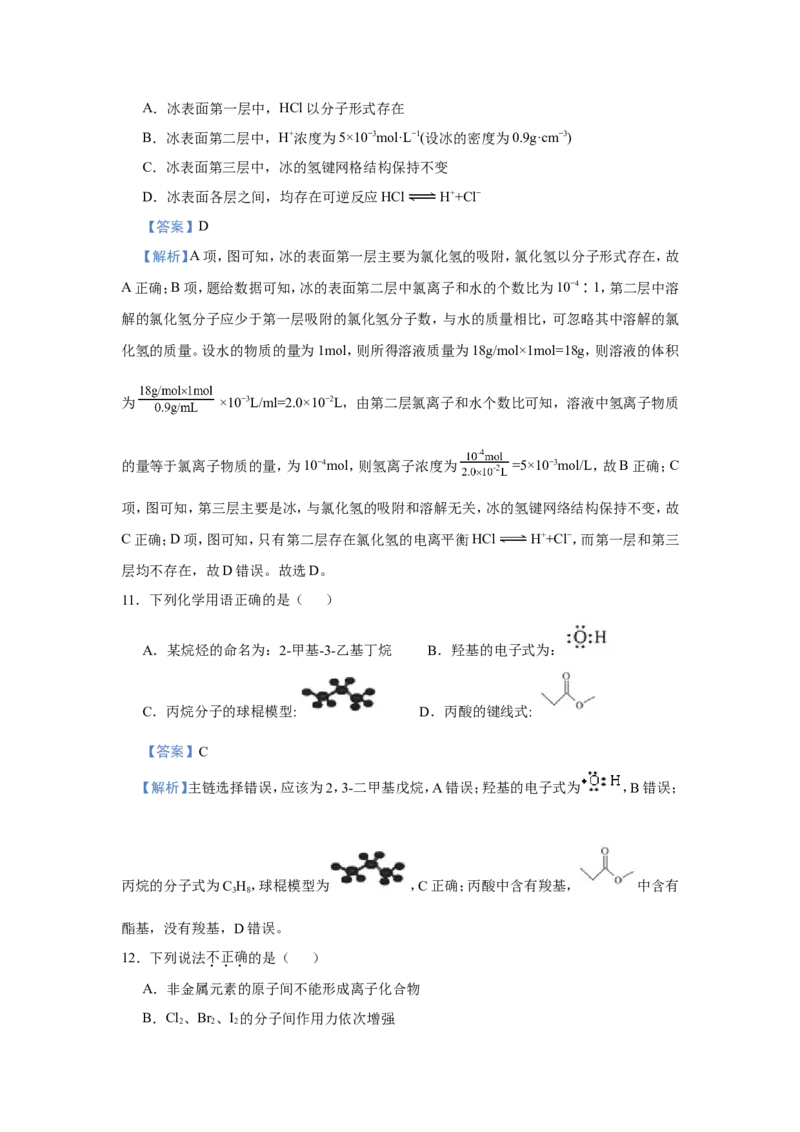
10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课
题。下图为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图。下列叙述错误的
是( )A.冰表面第一层中,HCl以分子形式存在
B.冰表面第二层中,H+浓度为5×10−3mol·L−1(设冰的密度为0.9g·cm−3)
C.冰表面第三层中,冰的氢键网格结构保持不变
D.冰表面各层之间,均存在可逆反应HCl H++Cl−
【答案】D
【解析】A项,图可知,冰的表面第一层主要为氯化氢的吸附,氯化氢以分子形式存在,故
A正确;B项,题给数据可知,冰的表面第二层中氯离子和水的个数比为10−4∶1,第二层中溶
解的氯化氢分子应少于第一层吸附的氯化氢分子数,与水的质量相比,可忽略其中溶解的氯
化氢的质量。设水的物质的量为1mol,则所得溶液质量为18g/mol×1mol=18g,则溶液的体积
为 ×10−3L/ml=2.0×10−2L,由第二层氯离子和水个数比可知,溶液中氢离子物质
的量等于氯离子物质的量,为10−4mol,则氢离子浓度为 =5×10−3mol/L,故B正确;C
项,图可知,第三层主要是冰,与氯化氢的吸附和溶解无关,冰的氢键网络结构保持不变,故
C正确;D项,图可知,只有第二层存在氯化氢的电离平衡HCl H++Cl−,而第一层和第三
层均不存在,故D错误。故选D。
11.下列化学用语正确的是( )
A.某烷烃的命名为:2-甲基-3-乙基丁烷 B.羟基的电子式为:
C.丙烷分子的球棍模型: D.丙酸的键线式:
【答案】C
【解析】主链选择错误,应该为2,3-二甲基戊烷,A错误;羟基的电子式为 ,B错误;
丙烷的分子式为C H,球棍模型为 ,C正确;丙酸中含有羧基, 中含有
3 8
酯基,没有羧基,D错误。
12.下列说法不正确的是( )
A.非金属元素的原子间不能形成离子化合物
B.Cl、Br 、I 的分子间作用力依次增强
2 2 2C.氯化氢气体溶于水共价键被破坏
D.干冰、NaCl固体、石英晶体的熔沸点逐渐升高
【答案】A
【解析】A项,由非金属元素形成的化合物大部分是共价化合物,但也可形成离子化合物,
如铵盐,故A错误;B项,Cl、Br 、I 都是结构相似的双原子分子,随着相对分子质量增大,分
2 2 2
子间作用力依次增强,故B正确;C项,氯化氢为共价化合物,溶于水共价键被破坏,电离出
氢离子和氯离子,故C正确;D项,干冰为分子晶体,熔沸点低,NaCl固体为离子晶体,具有
较高的熔沸点,石英晶体是原子晶体,具有很高的熔沸点,则干冰、NaCl固体、石英晶体的熔
沸点逐渐升高,故D正确;故选A。