文档内容
专题 九
电解质溶液中的平衡
××
命 题 趋 势
1.理解弱电解质在水溶液中的电离平衡,能利用电离平衡常数进行相关计算。
2.了解水的电离,离子积常数。
3.了解溶液pH的定义及测定方法,能进行pH的简单计算。
4.了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。
5.了解难溶电解质的溶解平衡。理解溶度积的定义,能进行相关计算。
Ⅰ.客观题
(1)以拼盘式选择题考查电解质溶液基本知识的辨析。
(2)以图像题考查强弱电解质的判断、微粒浓度的比较、溶度积常数的应用。
(3)与化工生产流程相结合以客观题形式呈现,考查盐类水解、溶解平衡知识的应用。
Ⅱ.主观题
(1)强弱电解质、溶液酸碱性与pH的关系、盐类水解等基本概念、理论的分析判断。
(2)电离平衡、水解平衡、溶解平衡的影响规律及应用。
(3)电离常数、水解常数、溶度积常数的表达式及应用。
考 点 清 单
一、溶液中的“三大平衡”及影响因素
电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡。这三种平衡都遵循勒夏特列原理——当只改
变体系的一个条件时,平衡向能够减弱这种改变的方向移动。
1.电离平衡、水解平衡与沉淀溶解平衡的比较
水解平衡(如CHCOONa
电离平衡CHCOOH 3 沉淀溶解平衡AgCl(s)
3 溶液)CHCOO−+HO
CHCOO-+H+ 3 2 Ag+(aq)+Cl−(aq)
3 CHCOOH+OH−
3
弱电解质(包括弱酸、弱 盐溶液(包括强酸弱碱
研究 难溶电解质(如难溶的
碱、水、多元弱酸的酸 盐、弱酸强碱盐、弱酸弱
对象 酸、碱、盐等)
式酸根) 碱盐)
升高 促进电离,离子浓度增 K 可能增大,也可能减
促进水解,K 增大 sp
影响 温度 大,K 增大 h 小
a
因素 加水 促进电离,离子浓度(除 促进水解,离子浓度(除
促进溶解,K 不变
稀释 OH−外)减小,K 不变 H+外)减小,K 不变 sp
a h加入 加入CHCOONa固体或 加入CHCOOH或
3 3 加入AgNO 溶液或NaCl
相应 盐酸,抑制电离,K 不 NaOH,抑制水解,K 不 3
a h 溶液抑制溶解,K 不变
离子 变 变 sp
加入
加入NaOH,促进电 加入盐酸,促进水解,K 加入氨水,促进溶解,
反应 h
离,K 不变 不变 K 不变
离子 a sp
2.“电离平衡”分析判断中的常见误区
(1)误认为电离平衡正向移动,弱电解质的电离程度一定增大。如向醋酸溶液中加入少量冰醋酸,平衡向
电离方向移动,但醋酸的电离程度减小。
(2)误认为弱电解质在加水稀释的过程中,溶液中离子浓度都减小。如氨水加水稀释时,c(H+)增大。
(3)误认为由水电离出的c(H+)=1.0×10−13mol·L−1的溶液一定呈碱性。如25℃,0.1mol·L−1盐酸或氢氧化钠
溶液中由水电离的c(H+)都为1.0×10−13mol·L−1。
(4)弱电解质溶液在加水稀释的过程中,判断某些微粒浓度的关系式是否发生变化时,首先要考虑该关系
式是否是电离常数、离子积常数或者是它们的变形。
二、溶液中离子浓度关系判断
1.理解溶液中的“三个守恒”关系
(1)电荷守恒:电解质溶液中阴离子所带电荷总数等于阳离子所带电荷总数,根据电荷守恒可准确、快速
地解决电解质溶液中许多复杂的离子浓度问题。
(2)物料守恒:物质发生变化前后,有关元素的存在形式不同,但元素的种类和原子数目在变化前后保持
不变,根据物料守恒可准确、快速地解决电解质溶液中复杂离子、分子、物质的量浓度或物质的量的关系。
(3)质子守恒:在电离或水解过程中,会发生质子(H+)转移,但质子转移过程中其数量保持不变。
将混合溶液中的电荷守恒式和物料守恒式相联立,通过代数运算消去其中未参与平衡移动的离子,即可
推出溶液中的质子守恒式。
2.三个守恒的综合应用
应用三种守恒关系解决电解质溶液中离子浓度关系时,要清楚电解质溶液中微粒存在的变化(水解或电
离),抓住守恒的实质,将由守恒所得的关系结合起来使用。综合运用三种守恒关系,理清一条思路,掌握分
析方法。如图所示:三、结合图像判断溶液中粒子浓度的变化
结合图像分析电离平衡、水解平衡、溶解平衡,判断离子浓度的关系是全国卷考查的重点,常考图像类
型总结如下:
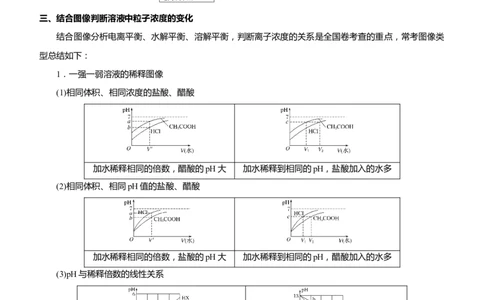
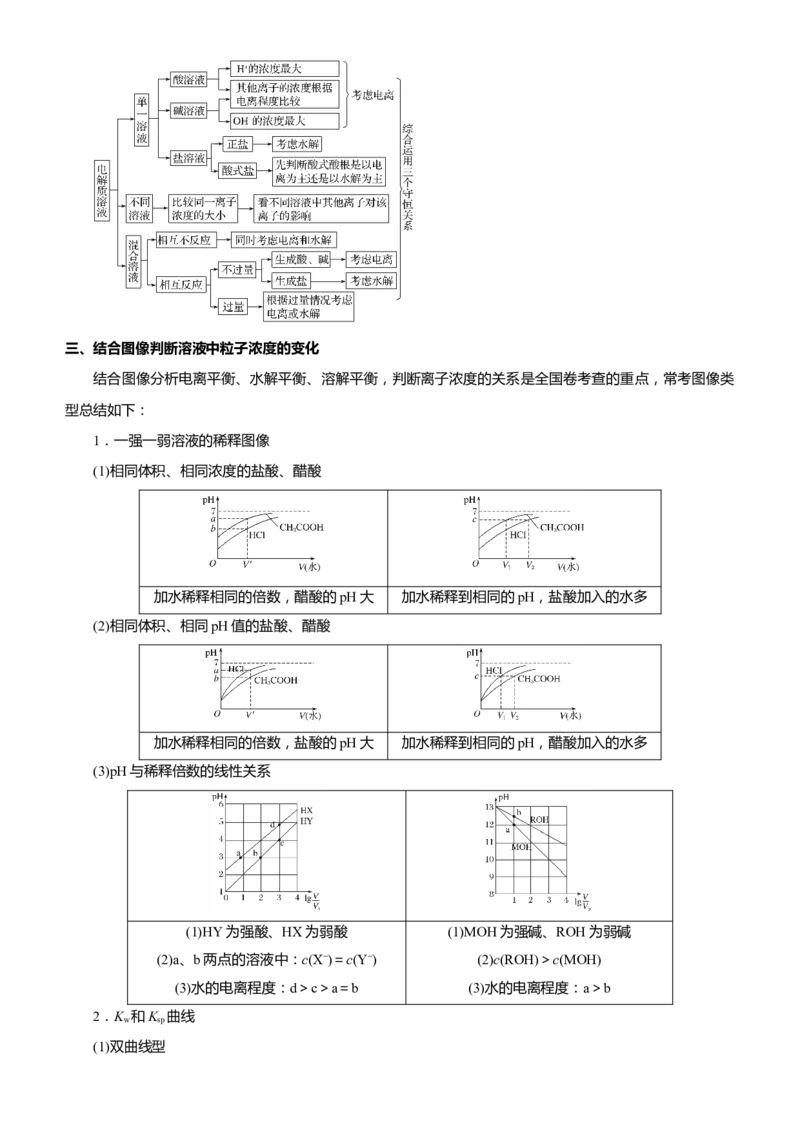
1.一强一弱溶液的稀释图像
(1)相同体积、相同浓度的盐酸、醋酸
加水稀释相同的倍数,醋酸的pH大 加水稀释到相同的pH,盐酸加入的水多
(2)相同体积、相同pH值的盐酸、醋酸
加水稀释相同的倍数,盐酸的pH大 加水稀释到相同的pH,醋酸加入的水多
(3)pH与稀释倍数的线性关系
(1)HY为强酸、HX为弱酸 (1)MOH为强碱、ROH为弱碱
(2)a、b两点的溶液中:c(X−)=c(Y−) (2)c(ROH)>c(MOH)
(3)水的电离程度:d>c>a=b (3)水的电离程度:a>b
2.K 和K 曲线
w sp
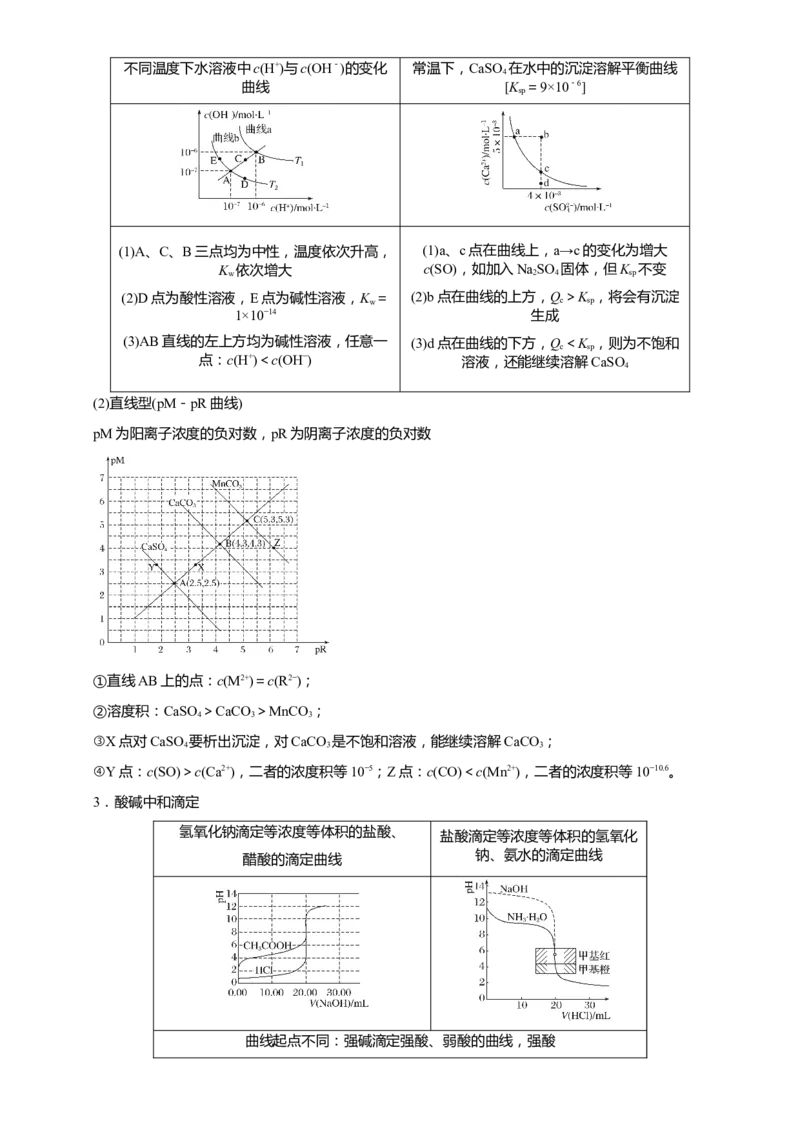
(1)双曲线型不同温度下水溶液中c(H+)与c(OH-)的变化 常温下,CaSO 在水中的沉淀溶解平衡曲线
4
曲线 [K =9×10-6]
sp
(1)A、C、B三点均为中性,温度依次升高, (1)a、c点在曲线上,a→c的变化为增大
K w 依次增大 c(SO),如加入Na 2 SO 4 固体,但K sp 不变
(2)D点为酸性溶液,E点为碱性溶液,K w = (2)b点在曲线的上方,Q c >K sp ,将会有沉淀
1×10−14 生成
(3)AB直线的左上方均为碱性溶液,任意一 (3)d点在曲线的下方,Q<K ,则为不饱和
c sp
点:c(H+)<c(OH−) 溶液,还能继续溶解CaSO
4
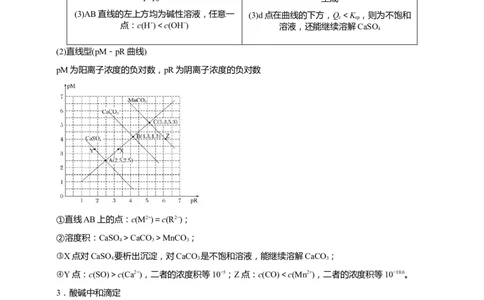
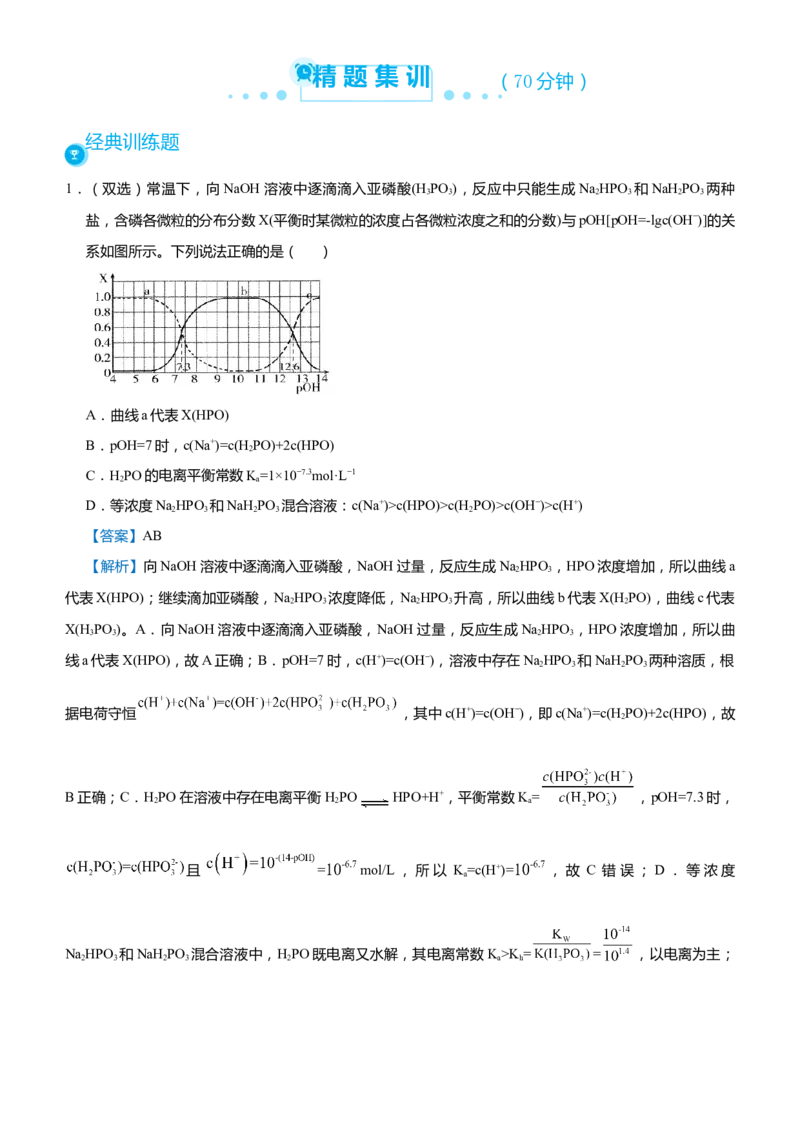
(2)直线型(pM-pR曲线)
pM为阳离子浓度的负对数,pR为阴离子浓度的负对数
①直线AB上的点:c(M2+)=c(R2−);
②溶度积:CaSO>CaCO >MnCO ;
4 3 3
③X点对CaSO 要析出沉淀,对CaCO 是不饱和溶液,能继续溶解CaCO ;
4 3 3
④Y点:c(SO)>c(Ca2+),二者的浓度积等10−5;Z点:c(CO)<c(Mn2+),二者的浓度积等10−10.6。
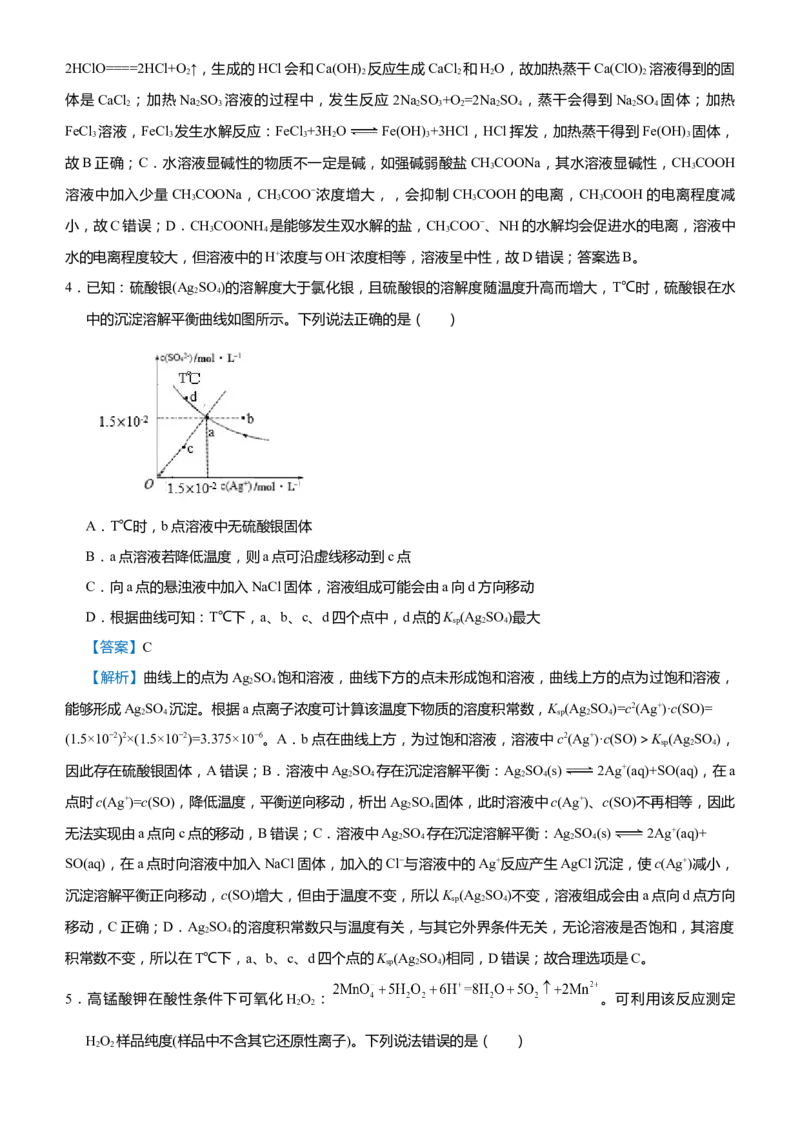
3.酸碱中和滴定
氢氧化钠滴定等浓度等体积的盐酸、
盐酸滴定等浓度等体积的氢氧化
钠、氨水的滴定曲线
醋酸的滴定曲线
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的
突跃点变化范围大于强碱与弱酸反应(强酸与弱碱反应)
室温下pH=7不一定是终点:强碱与强酸反应时,终点是pH=7;强碱与弱
酸(强酸与弱碱)反应时,终点不是pH=7(强碱与弱酸反应终点是pH>7,强酸
与弱碱反应终点是pH<7)精 题 集 训
(70分钟)
经典训练题
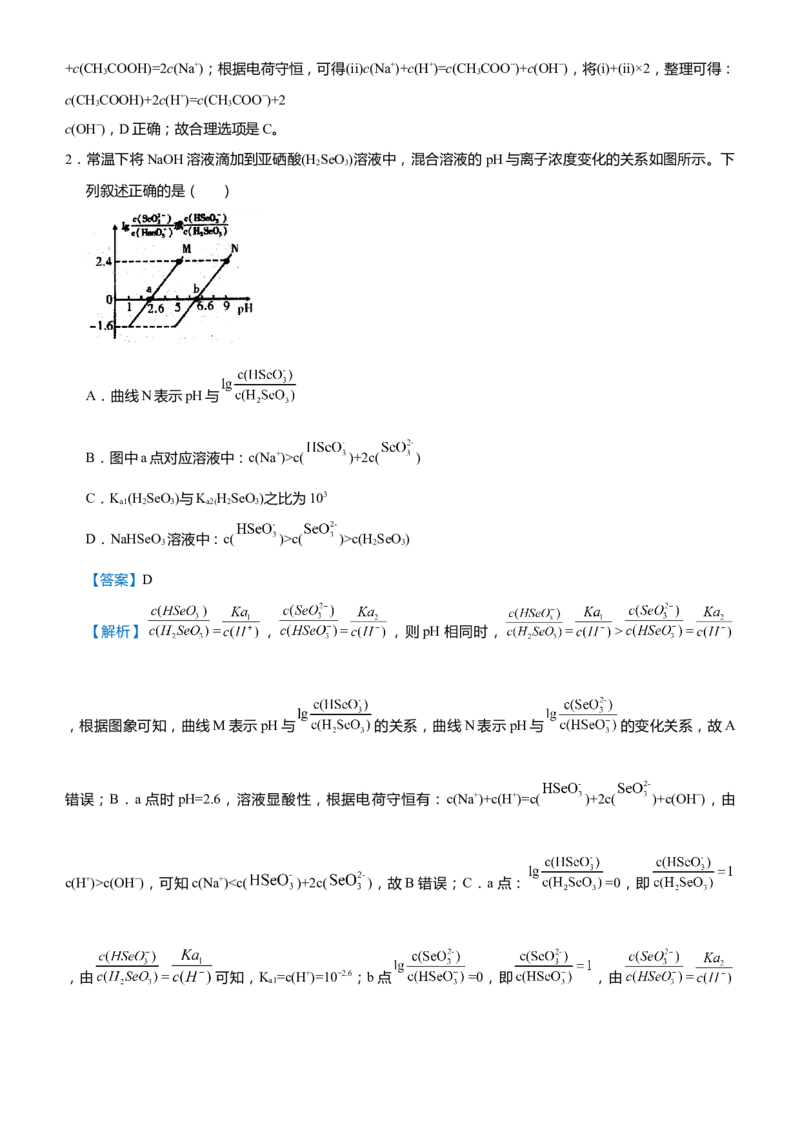
1.(双选)常温下,向NaOH溶液中逐滴滴入亚磷酸(H PO ),反应中只能生成NaHPO 和NaH PO 两种
3 3 2 3 2 3
盐,含磷各微粒的分布分数X(平衡时某微粒的浓度占各微粒浓度之和的分数)与pOH[pOH=-lgc(OH−)]的关
系如图所示。下列说法正确的是( )
A.曲线a代表X(HPO)
B.pOH=7时,c(Na+)=c(H PO)+2c(HPO)
2
C.HPO的电离平衡常数K=1×10−7.3mol·L−1
2 a
D.等浓度NaHPO 和NaH PO 混合溶液:c(Na+)>c(HPO)>c(H PO)>c(OH−)>c(H+)
2 3 2 3 2
【答案】AB
【解析】向NaOH溶液中逐滴滴入亚磷酸,NaOH过量,反应生成NaHPO ,HPO浓度增加,所以曲线a
2 3
代表X(HPO);继续滴加亚磷酸,NaHPO 浓度降低,NaHPO 升高,所以曲线b代表X(H PO),曲线c代表
2 3 2 3 2
X(H PO )。A.向NaOH溶液中逐滴滴入亚磷酸,NaOH过量,反应生成NaHPO ,HPO浓度增加,所以曲
3 3 2 3
线a代表X(HPO),故A正确;B.pOH=7时,c(H+)=c(OH−),溶液中存在NaHPO 和NaH PO 两种溶质,根
2 3 2 3
据电荷守恒 ,其中c(H+)=c(OH−),即c(Na+)=c(H PO)+2c(HPO),故
2
B正确;C.HPO在溶液中存在电离平衡HPO HPO+H+,平衡常数K= ,pOH=7.3时,
2 2 a
且 = mol/L,所以 K=c(H+)= ,故 C 错误;D.等浓度
a
NaHPO 和NaH PO 混合溶液中,HPO既电离又水解,其电离常数K>K = = ,以电离为主;
2 3 2 3 2 a hHPO只水解,其水解常数K= = c(HPO)>c(H PO)>c(H+)>c(OH−),故D错误;故选AB。
2
【点评】把pOH换算成pH计算,pOH增大,碱性减弱,是解题的基本前提,依次推出各曲线代表的粒
子变化情况。
2.(双选)下列实验操作、现象和结论都正确的是( )
选项 实验操作和现象 结论
向盛有少量PbI 固体的试管中,加入3mL蒸馏
2
A 水振荡后静置,待上层液体变澄清后,向上层清 上层清液中存在Pb2+
液中滴加几滴0.1mol·L−1 KI液中有黄色沉淀生成
用盛有盐酸和醋酸的烧杯分别做导电性实验,盛
B 醋酸是弱电解质
有醋酸的烧杯所连灯泡亮度较暗
向盛有0.01mol·L−1的CHCOONa溶液的小试管
3 CHCOO−+H O
C 中滴加一滴酚酞溶液,将小试管在酒精灯上微微 3 2
CHCOOH+OH−是吸热反应
3
加热,溶液红色变深
向盛有2ml 0.1mol·L−1 NaS溶液的试管中,加入
2
D 2滴ZnSO 溶液,生成白色沉淀,再加入适量 K (ZnS)>K (CuS)
4 sp sp
0.1mol·L−1 CuSO 溶液,有黑色沉淀生成
4
【答案】AC
【解析】A.上层清液中滴加KI溶液,有黄色沉淀生成,表明生成 PbI ,则上层清液中含有Pb2+,A正
2
确;B.用盐酸和醋酸做导电性实验,虽然盛有醋酸的烧杯所连灯泡亮度较暗,但二者的浓度关系未知,不
能说明醋酸是弱电解质,B不正确;C.CHCOONa溶液中滴加酚酞后溶液变红色,表明溶液显碱性,加热
3
溶液,红色加深,表明c(OH−)增大,CHCOO−的水解平衡正向移动,从而得出CHCOO−的水解是吸热反应,
3 3
C正确;D.NaS溶液中滴加几滴ZnSO 溶液,产生ZnS白色沉淀,再加入CuSO 溶液,又生成黑色CuS沉
2 4 4
淀,因为溶液中加入 ZnSO 后 S2−有剩余,所以并不能说明 ZnS 转化为 CuS,也就不能得出 K (ZnS)>
4 sp
K (CuS)的结论,D不正确;故选AC。
sp
3.下列有关电解质溶液的说法正确的是( )
A.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解
B.将Ca(ClO) 、NaSO 、FeCl 溶液蒸干均得不到原溶质
2 2 3 3
C.室温下,向0.1mol/L的CHCOOH溶液中加入少量水溶液显碱性的物质,CHCOOH的电离程度一定
3 3
增大
D.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同
3 4
【答案】B
【解析】A.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止 Fe2+被氧化为Fe3+,故A错误;B.
Ca(ClO) 在 水 中 发 生 水 解 : Ca(ClO) +2H O Ca(OH) +2HClO , HClO 不 稳 定 , 受 热 分 解 :
2 2 2 22HClO====2HCl+O ↑,生成的HCl会和Ca(OH) 反应生成CaCl 和HO,故加热蒸干Ca(ClO) 溶液得到的固
2 2 2 2 2
体是CaCl ;加热NaSO 溶液的过程中,发生反应 2NaSO +O =2Na SO ,蒸干会得到NaSO 固体;加热
2 2 3 2 3 2 2 4 2 4
FeCl 溶液,FeCl 发生水解反应:FeCl +3H O Fe(OH) +3HCl,HCl挥发,加热蒸干得到Fe(OH) 固体,
3 3 3 2 3 3
故B正确;C.水溶液显碱性的物质不一定是碱,如强碱弱酸盐CHCOONa,其水溶液显碱性,CHCOOH
3 3
溶液中加入少量CHCOONa,CHCOO−浓度增大,,会抑制 CHCOOH的电离,CHCOOH的电离程度减
3 3 3 3
小,故C错误;D.CHCOONH 是能够发生双水解的盐,CHCOO−、NH的水解均会促进水的电离,溶液中
3 4 3
水的电离程度较大,但溶液中的H+浓度与OH−浓度相等,溶液呈中性,故D错误;答案选B。
4.已知:硫酸银(Ag SO )的溶解度大于氯化银,且硫酸银的溶解度随温度升高而增大,T℃时,硫酸银在水
2 4
中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A.T℃时,b点溶液中无硫酸银固体
B.a点溶液若降低温度,则a点可沿虚线移动到c点
C.向a点的悬浊液中加入NaCl固体,溶液组成可能会由a向d方向移动
D.根据曲线可知:T℃下,a、b、c、d四个点中,d点的K (Ag SO )最大
sp 2 4
【答案】C
【解析】曲线上的点为Ag SO 饱和溶液,曲线下方的点未形成饱和溶液,曲线上方的点为过饱和溶液,
2 4
能够形成Ag SO 沉淀。根据a点离子浓度可计算该温度下物质的溶度积常数,K (Ag SO )=c2(Ag+)·c(SO)=
2 4 sp 2 4
(1.5×10−2)2×(1.5×10−2)=3.375×10−6。A.b点在曲线上方,为过饱和溶液,溶液中c2(Ag+)·c(SO)>K (Ag SO ),
sp 2 4
因此存在硫酸银固体,A错误;B.溶液中Ag SO 存在沉淀溶解平衡:Ag SO (s) 2Ag+(aq)+SO(aq),在a
2 4 2 4
点时c(Ag+)=c(SO),降低温度,平衡逆向移动,析出Ag SO 固体,此时溶液中c(Ag+)、c(SO)不再相等,因此
2 4
无法实现由a点向c点的移动,B错误;C.溶液中Ag SO 存在沉淀溶解平衡:Ag SO (s) 2Ag+(aq)+
2 4 2 4
SO(aq),在a点时向溶液中加入NaCl固体,加入的Cl−与溶液中的Ag+反应产生AgCl沉淀,使c(Ag+)减小,
沉淀溶解平衡正向移动,c(SO)增大,但由于温度不变,所以K (Ag SO )不变,溶液组成会由a点向d点方向
sp 2 4
移动,C正确;D.Ag SO 的溶度积常数只与温度有关,与其它外界条件无关,无论溶液是否饱和,其溶度
2 4
积常数不变,所以在T℃下,a、b、c、d四个点的K (Ag SO )相同,D错误;故合理选项是C。
sp 2 4
5.高锰酸钾在酸性条件下可氧化HO : 。可利用该反应测定
2 2
HO 样品纯度(样品中不含其它还原性离子)。下列说法错误的是( )
2 2A.将高锰酸钾溶液装入酸式滴定管中
B.打开酸式滴定管的活塞,迅速放液以赶出气泡
C.滴定过程中,眼睛要时刻注意锥形瓶中溶液颜色的变化
D.滴定中盛放HO 的锥形瓶内壁有水,所测定的HO 纯度变小
2 2 2 2
【答案】D
【解析】A.高锰酸钾溶液具有强氧化性,会腐蚀碱式滴定管的橡胶管,因此应该装入酸式滴定管中,A
正确;B.如果滴定管尖嘴有气泡,需要赶走气泡,使尖嘴充满液体,所以就应打开酸式滴定管的活塞,迅
速放液以赶出气泡,B正确;C.滴定过程中,左手控制滴定管的活塞,右手摇动锥形瓶,使溶液混合均
匀,眼睛要时刻注意锥形瓶中溶液颜色的变化,C正确;D.滴定中盛放HO 的锥形瓶内壁有水,由于不影
2 2
响HO 的物质的量,因此不影响标准溶液的消耗,对所测定的 HO 纯度无影响,其纯度测定值不变,D错
2 2 2 2
误;故合理选项是D。
高频易错题
1.25℃时,对于浓度均为0.1mol/L的三种溶液:①醋酸、②氢氧化钠、③醋酸钠溶液,下列说法错误的是
( )
A.c(CHCOO−):③>①
3
B.水电离出的c(H+):③>①>②
C.25℃时,①和②等体积混合后的溶液:
D.25℃时,①和③等体积混合后的溶液:
【答案】C
【解析】A.①醋酸是弱酸,主要以电解质分子存在,电离产生的离子浓度很小,而③醋酸钠是盐,属于
强电解质,完全电离产生离子,因此等浓度的①、③溶液中c(CHCOO−):③>①,A正确;B.①是醋酸,
3
酸电离产生H+会抑制水的电离;②是氢氧化钠,属于碱,碱电离产生OH−也会抑制水的电离,由于②电离产
生的OH−大于①产生的H+的浓度,因此水电离程度:①>②;③醋酸钠,该盐是强碱弱酸盐,水解使溶液显
碱性,水解会促进水的电离,水的电离程度增大,因此其中水的电离程度比酸或碱都大,故③中水电离程度
最大。则三种溶液中水电离程度:③>①>②。水电离程度越大,水电离产生的H+的浓度就越大,故三种溶
液中水电离出的 c(H+):③>①>②,B 正确;C.25℃时,①和②等体积混合后,二者恰好反应产生
CHCOONa,该盐是强碱弱酸盐,水解使溶液显碱性,c(OH−)>c(H+);CHCOO−水解消耗,则溶液中c(Na+)
3 3
>c(CHCOO−);盐电离产生的离子浓度大于水电离产生的离子浓度,故c(CHCOO−)>c(OH−),因此该溶液中
3 3
各种离子浓度大小关系为:c(Na+)>c(CHCOO−)>c(OH−)>c(H+),C错误;D.①和③等体积混合后,溶液为
3
CHCOOH 与 CHCOONa 等 物 质 的 量 的 比 混 合 溶 液 , 根 据 物 料 守 恒 可 得 (i)c(CHCOO−)
3 3 3+c(CHCOOH)=2c(Na+);根据电荷守恒,可得(ii)c(Na+)+c(H+)=c(CHCOO−)+c(OH−),将(i)+(ii)×2,整理可得:
3 3
c(CHCOOH)+2c(H+)=c(CHCOO−)+2
3 3
c(OH−),D正确;故合理选项是C。
2.常温下将NaOH溶液滴加到亚硒酸(H SeO)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下
2 3
列叙述正确的是( )
A.曲线N表示pH与
B.图中a点对应溶液中:c(Na+)>c( )+2c( )
C.K (H SeO)与K HSeO)之比为103
a1 2 3 a2( 2 3
D.NaHSeO 溶液中:c( )>c( )>c(H SeO)
3 2 3
【答案】D
【解析】 = , = ,则pH相同时, = > =
,根据图象可知,曲线M表示pH与 的关系,曲线N表示pH与 的变化关系,故A
错误;B.a点时pH=2.6,溶液显酸性,根据电荷守恒有:c(Na+)+c(H+)=c( )+2c( )+c(OH−),由
c(H+)>c(OH−),可知c(Na+)c(
a2 3
)>
c(HSeO),故D正确;故选D。
2 3
【点评】考查酸碱混合的定性判断、弱电解质的电离,明确图象曲线变化的意义为解答关键,注意掌握溶
液酸碱性与溶液pH的关系。
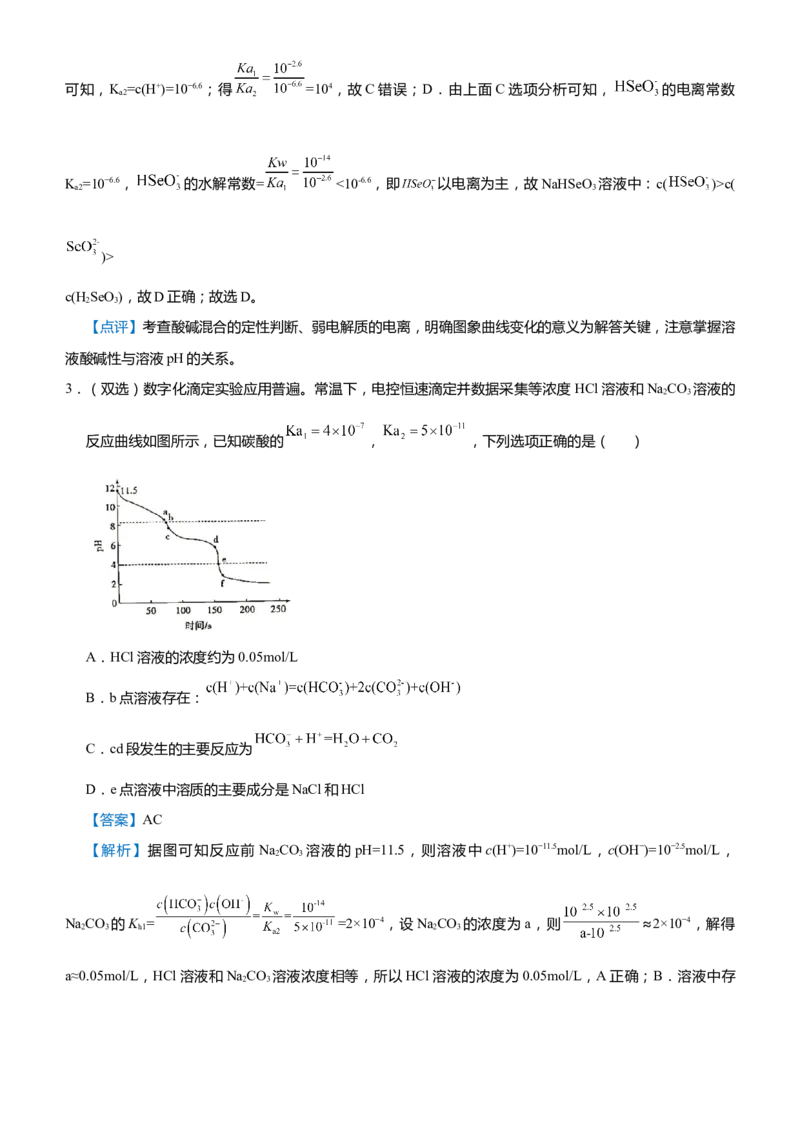
3.(双选)数字化滴定实验应用普遍。常温下,电控恒速滴定并数据采集等浓度HCl溶液和NaCO 溶液的
2 3
反应曲线如图所示,已知碳酸的 , ,下列选项正确的是( )
A.HCl溶液的浓度约为0.05mol/L
B.b点溶液存在:
C.cd段发生的主要反应为
D.e点溶液中溶质的主要成分是NaCl和HCl
【答案】AC
【解析】据图可知反应前 NaCO 溶液的 pH=11.5,则溶液中 c(H+)=10−11.5mol/L,c(OH−)=10−2.5mol/L,
2 3
NaCO 的K = =2×10−4,设NaCO 的浓度为a,则 ≈2×10−4,解得
2 3 h1 2 3
a≈0.05mol/L,HCl溶液和NaCO 溶液浓度相等,所以HCl溶液的浓度为0.05mol/L,A正确;B.溶液中存
2 3在电荷守恒 ,B 错误;C.碳酸的 K =
a2
=5×10−11,所以当c(CO)=c(HCO)时c(H+)=5×10−11mol/L,溶液的pH<11,而c点溶液pH<8,所以C元素主要
以HCO的形式存在,c~d段pH下降时发生的反应为HCO+H+=H O+CO ,C正确;D.据图可知e点之后继
2 2
续滴加盐酸,溶液的pH变化较大,说明e点HCO还未完全反应,继续滴加盐酸会继续反应,从而导致pH
突变,所以溶质不可能有HCl,溶液显酸性是因为含有HCO,D错误;综上所述答案为AC。
2 3
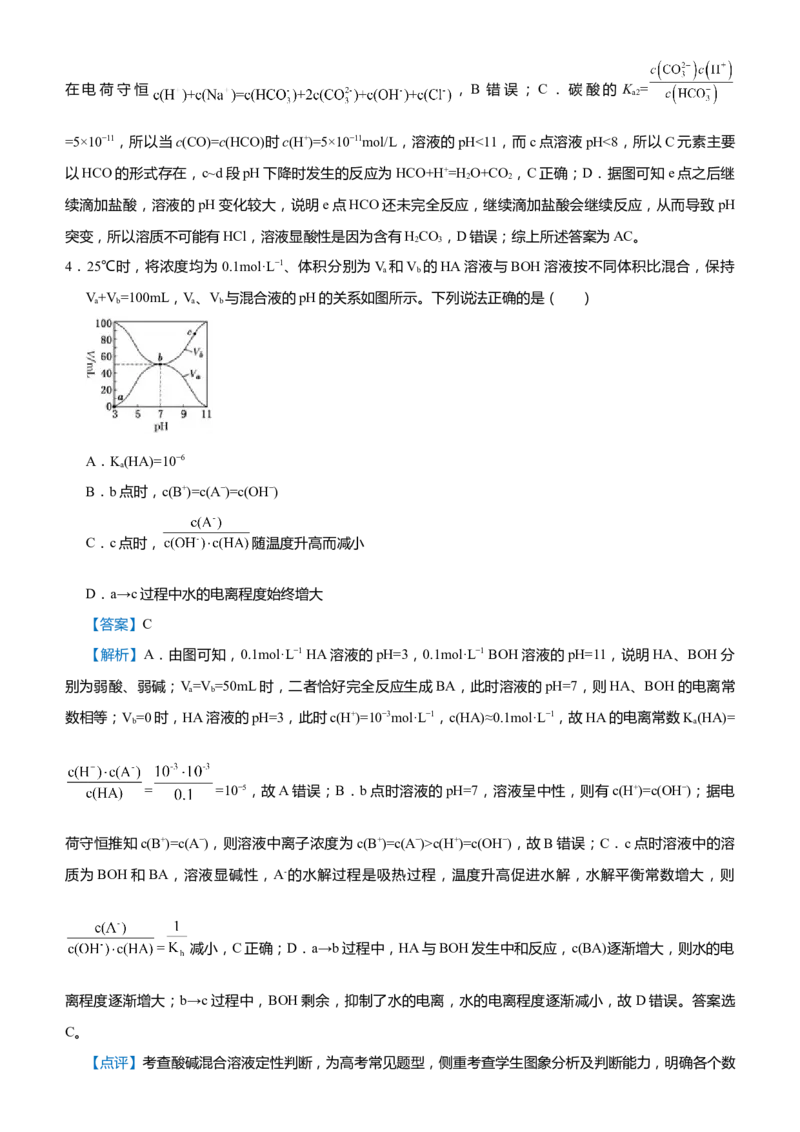
4.25℃时,将浓度均为0.1mol·L−1、体积分别为V 和V 的HA溶液与BOH溶液按不同体积比混合,保持
a b
V+V=100mL,V、V 与混合液的pH的关系如图所示。下列说法正确的是( )
a b a b
A.K(HA)=10−6
a
B.b点时,c(B+)=c(A−)=c(OH−)
C.c点时, 随温度升高而减小
D.a→c过程中水的电离程度始终增大
【答案】C
【解析】A.由图可知,0.1mol·L−1 HA溶液的pH=3,0.1mol·L−1 BOH溶液的pH=11,说明HA、BOH分
别为弱酸、弱碱;V=V=50mL时,二者恰好完全反应生成BA,此时溶液的pH=7,则HA、BOH的电离常
a b
数相等;V=0时,HA溶液的pH=3,此时c(H+)=10−3mol·L−1,c(HA)≈0.1mol·L−1,故HA的电离常数K(HA)=
b a
= =10−5,故A错误;B.b点时溶液的pH=7,溶液呈中性,则有c(H+)=c(OH−);据电
荷守恒推知c(B+)=c(A−),则溶液中离子浓度为c(B+)=c(A−)>c(H+)=c(OH−),故B错误;C.c点时溶液中的溶
质为BOH和BA,溶液显碱性,A-的水解过程是吸热过程,温度升高促进水解,水解平衡常数增大,则
= 减小,C正确;D.a→b过程中,HA与BOH发生中和反应,c(BA)逐渐增大,则水的电
离程度逐渐增大;b→c过程中,BOH剩余,抑制了水的电离,水的电离程度逐渐减小,故D错误。答案选
C。
【点评】考查酸碱混合溶液定性判断,为高考常见题型,侧重考查学生图象分析及判断能力,明确各个数据含义及各点溶液中溶质成分及其性质是解本题关键。
5.下列有关滴定的说法正确的是( )
A.用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL
B.用未知浓度的HCl溶液滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯
视,会导致测定结果偏高
C.用标准的KOH溶液滴定未知浓度的HCl溶液,配制标准溶液的固体KOH中混有NaOH杂质,则结果
偏高
D.将KMnO 标准溶液加入碱式滴定管中,滴定未知浓度的HC O 溶液
4 2 2 4
【答案】B
【解析】A.滴定管为精量器,读数读到0.01mL,用25mL滴定管进行中和滴定时,用去标准液的体积为
21.70mL,故A错误;B.用未知浓度的HCl溶液滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰
视,滴定到终点后俯视,导致消耗盐酸溶液的体积偏小,测定结果偏高,故B正确;C.所用固体KOH中混
有NaOH,相同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾的物质的量,故所配得溶液
中氢氧根离子浓度偏大,造成滴定时消耗标准溶液的体积会偏小,所测结果偏低,故C错误;D.高锰酸钾
溶液具有强氧化性,会腐蚀碱式滴定管中的橡胶管,应将高锰酸钾溶液装入酸式滴定管中,故 D错误;故选
B。
精准预测题
1.下列说法正确的是( )
A.向AgCl浊液中加入KBr溶液,沉淀颜色变为浅黄色,即可证明K (AgCl)>K (AgBr)
sp sp
B.常温下向NaOH溶液中滴入HCOOH溶液至pH=5时:c(HCOO−)>c(Na+)
C.常温下等物质的量浓度的四种溶液①NH ·H O ②NH HSO ③(NH )CO ④NH Cl,c(NH)的关系为
3 2 4 4 4 2 3 4
②>④>③>①
D.等物质的量浓度的NaHCO 与NaCO 混合溶液:3c(Na+)=2[c(CO)+c(HCO)+c(H CO)]
3 2 3 2 3
【答案】B
【解析】A.向AgCl浊液中加入KBr溶液,沉淀颜色变为浅黄色,则有AgBr生成,AgCl转变为AgBr,
只要 即有AgBr沉淀,若溴化钾浓度很大,即使K (AgBr)>K (AgCl)也可实现,故不可
sp sp
证明K (AgCl)>K (AgBr),A错误;B.常温下向NaOH溶液中滴入HCOOH溶液至pH=5时,溶液呈酸性,
sp sp
,根据电荷守恒, ,则有 :c(HCOO−)>c(Na+),B正
确;C.常温下等物质的量浓度的四种溶液①NH ·H O ②NH HSO ③(NH )CO ④NH Cl,①NH ·H O是弱
3 2 4 4 4 2 3 4 3 2
电解质,其余都是强电解质,因此 c(NH)最小的是①,根据能够电离出的 NH 的个数可分为两类,③(NH )CO 是二元铵盐,虽然碳酸铵溶液中,碳酸根和铵根相互促进水解,但水解不彻底,铵离子浓度较
4 2 3
大,②NH HSO 和④NH Cl一元铵盐,②NH HSO 中电离产生的氢离子抑制铵离子水解,故② NH HSO 和
4 4 4 4 4 4 4
④ NH Cl 比较,c(NH)较大的是②;则,c(NH)的关系为③>②>④>①,C 错误;D.等物质的量浓度的
4
NaHCO 与NaCO 混合溶液:根据物料守恒可知:2c(Na+)=3[c(CO)+c(HCO)+c(H CO)],D错误;答案选B。
3 2 3 2 3
2.叠氮酸(HN )与NaOH溶液反应生成NaN 。已知NaN 溶液呈碱性,下列叙述正确的是( )
3 3 3
A.0.01mol·L−1 HN 溶液的pH=2
3
B.HN 溶液的pH随温度升高而减小
3
C.NaN 的电离方程式:NaN =Na++3N
3 3
D.0.01mol·L−1 NaN 溶液中:c(H+)+c(Na+)=c(N)+c(HN )
3 3
【答案】B
【解析】A.由题意,NaN 溶液呈碱性,则叠氮酸根(N)会发生水解,说明HN 为弱酸,在水溶液中不能
3 3
完全电离,故0.01mol·L−1 HN 溶液的pH>2,A错误;B.HN 为弱酸,电离方程式为HN H++N,电离
3 3 3
是吸热过程,升高温度促进HN 的电离,c(H+)增大,pH减小,B正确;C.NaN 是强电解质,完全电离出
3 3
Na+和N,电离方程式为NaN =Na++N,C选项错误;D.0.01mol·L−1 NaN 溶液中:由物料守恒c(Na+)=c(N)
3 3
+c(HN ),故D错误;故答案选B。
3
3.下列说法中不正确的有( )
①水是一种极弱的电解质,在常温下平均每n个水分子只有1个分子发生电离,n的值是5.56×108
②两种醋酸的物质的量浓度分别为c 和c,pH分别为a和a+1,则c=10c
1 2 1 2
③常温下pH=4的醋酸加水稀释过程中,所有离子浓度都降低
④蒸干AlCl 溶液可得纯净的无水氯化铝
3
A.1个 B.2个 C.3个 D.4个
【答案】C
【解析】①1L水在常温下质量约为1000g,物质的量为: ≈55.6mol,1L水在常温下含有氢离子
物质的量为:10−7mol,平均每n个水分子中只有一个水分子发生电离,则n mol水分子中会有1mol水分子电
离出1mol氢离子,即: = ,解得n=5.56×108,故正确;②醋酸是弱电解质,在水溶液中只有部
分电离,所以醋酸的浓度大于氢离子浓度;两种醋酸溶液的物质的量浓度分别为 c 和c ,pH分别为a和a+1
1 2
的两种醋酸溶液中氢离子浓度之比=10∶1,当两种酸的电离度相同时,则c=10c ,实际上,两种酸的浓度不
1 2
等,且浓度越大,酸的电离度越小,所以两种酸的浓度关系为c >10c ,故错误;③酸溶液稀释时,c(H+)减
1 2
小,由于K 不变,则c(OH−)增大,故错误;④水解生成的HCl易挥发,蒸干不会得到氯化铝,而是氢氧化
w
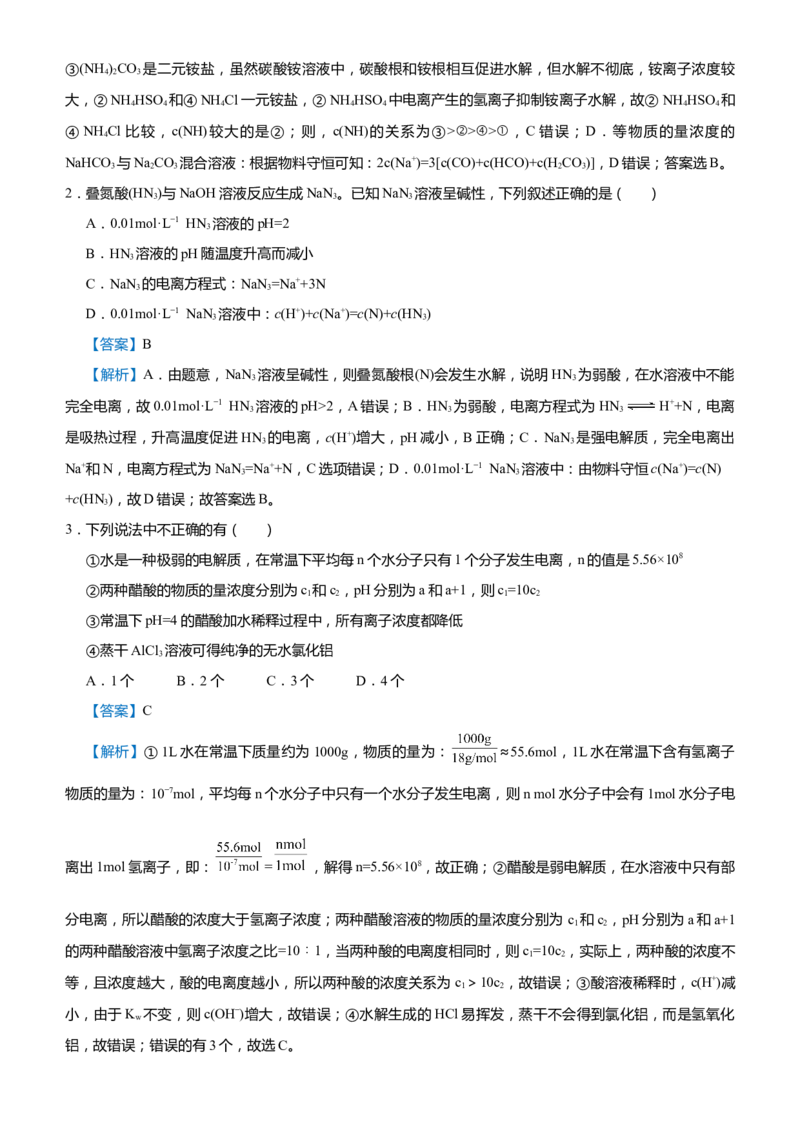
铝,故错误;错误的有3个,故选C。4.25℃时,向20mL 0.1mol/L HAuCl 溶液中滴加0.1mol/L NaOH溶液,滴定曲线如图所示,则下列说法不正
4
确的是( )
A.b点对应溶液中:c(HAuCl )>c( )
4
B.d点对应溶液中:c(OH−)-c(H+)=c(HAuCl )
4
C.HAuCl 的电离平衡常数K 约为10−5
4 a
D.滴定过程中,n(HAuCl )与n( )之和保持不变
4
【答案】A
【解析】a点时,0.1mol/L HAuCl 溶液的pH=3,即c(H+)=10−3mol/L,则HAuCl 为弱酸,故溶液pH=7
4 4
时,加入NaOH溶液的体积小于20mL。A.b点对应溶液中的溶质为等量的 HAuCl 、NaAuCl ,溶液显酸
4 4
性,则HAuCl 电离程度大于NaAuCl 的水解程度,即c(HAuCl )<c( ),A说法错误;B.d点对应溶液
4 4 4
中的溶质为NaAuCl ,根据质子守恒可得c(OH−)=c(HAuCl )+c(H+),则c(OH−)-c(H+)=c(HAuCl )成立,B说法
4 4 4
正确;C.HAuCl 的电离平衡常数K= =10-5,C说法正确;D.滴定过程中,根据物料守恒,
4 a
n(HAuCl )+n( )=20mL×0.1mol/L,保持不变,D说法正确;答案为A。
4
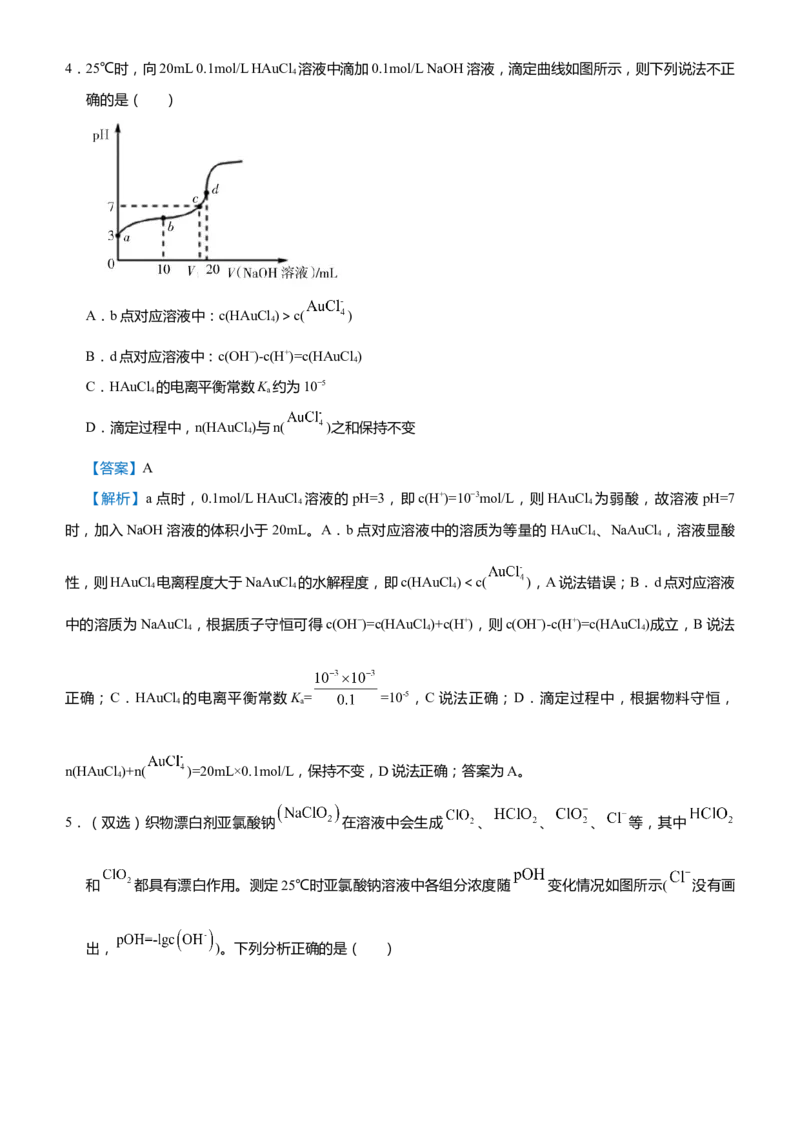
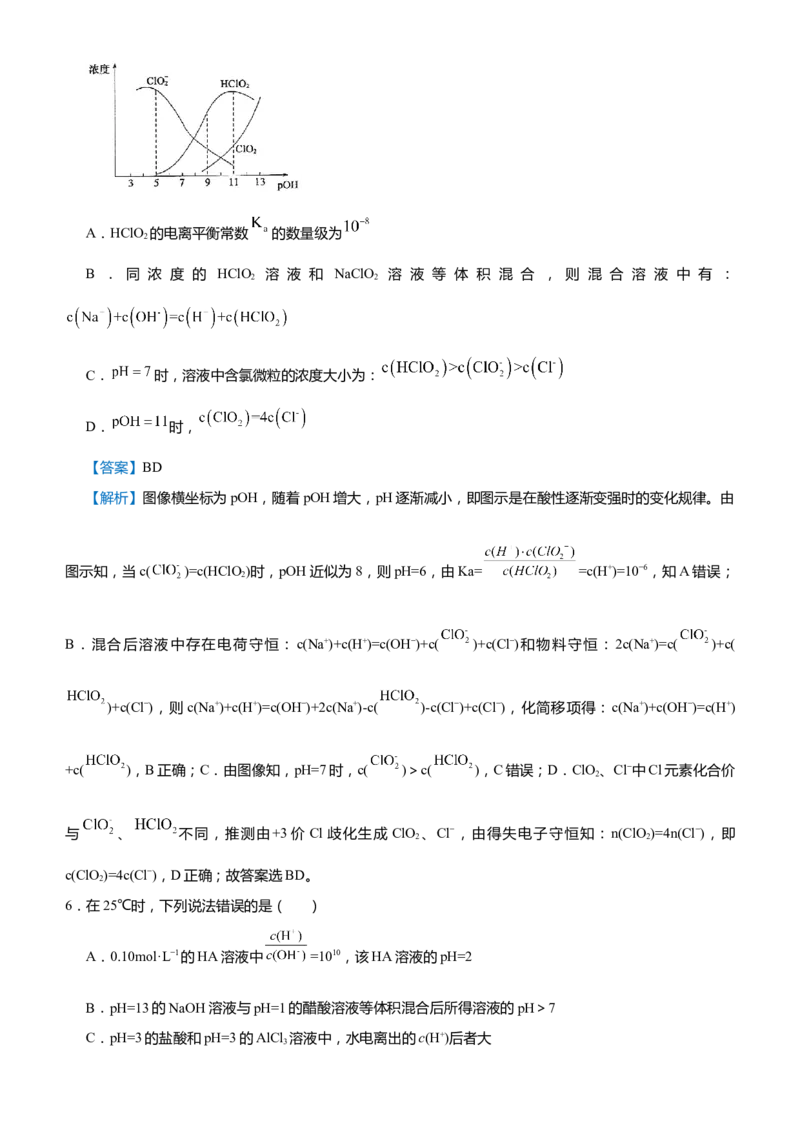
5.(双选)织物漂白剂亚氯酸钠 在溶液中会生成 、 、 、 等,其中
和 都具有漂白作用。测定25℃时亚氯酸钠溶液中各组分浓度随 变化情况如图所示( 没有画
出, )。下列分析正确的是( )A.HClO 的电离平衡常数 的数量级为
2
B . 同 浓 度 的 HClO 溶 液 和 NaClO 溶 液 等 体 积 混 合 , 则 混 合 溶 液 中 有 :
2 2
C. 时,溶液中含氯微粒的浓度大小为:
D. 时,
【答案】BD
【解析】图像横坐标为pOH,随着pOH增大,pH逐渐减小,即图示是在酸性逐渐变强时的变化规律。由
图示知,当c( )=c(HClO)时,pOH近似为8,则pH=6,由Ka= =c(H+)=10−6,知A错误;
2
B.混合后溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH−)+c( )+c(Cl−)和物料守恒:2c(Na+)=c( )+c(
)+c(Cl−),则c(Na+)+c(H+)=c(OH−)+2c(Na+)-c( )-c(Cl−)+c(Cl−),化简移项得:c(Na+)+c(OH−)=c(H+)
+c( ),B正确;C.由图像知,pH=7时,c( )>c( ),C错误;D.ClO 、Cl−中Cl元素化合价
2
与 、 不同,推测由+3 价 Cl 歧化生成 ClO 、Cl−,由得失电子守恒知:n(ClO )=4n(Cl−),即
2 2
c(ClO )=4c(Cl−),D正确;故答案选BD。
2
6.在25℃时,下列说法错误的是( )
A.0.10mol·L−1的HA溶液中 =1010,该HA溶液的pH=2
B.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7
C.pH=3的盐酸和pH=3的AlCl 溶液中,水电离出的c(H+)后者大
3D.10mL pH=3的盐酸与1mL pH=12的NaOH混合后溶液呈中性
【答案】B
【 解 析 】 A . 0.10mol·L−1 的 HA 溶 液 中 =1010 , 又 , 则
,该HA溶液的pH=2,故A正确;B.pH=1的醋酸溶液的物质的量浓度比pH=13的
NaOH溶液的物质的量浓度大的多,则二者等体积混合后所得溶液显酸性,pH<7,故B错误;C.盐酸抑制
水的电离,AlCl 溶液中铝离子水解促进水的电离,则水电离出的 c(H+)后者大,故C正确;D.pH=3的盐酸
3
中 ,pH=12 的NaOH 溶液中 ,则10mL pH=3 的盐酸与 1mL pH=12 的
NaOH混合后,恰好反应生成氯化钠,则溶液呈中性,故D正确;故选B。
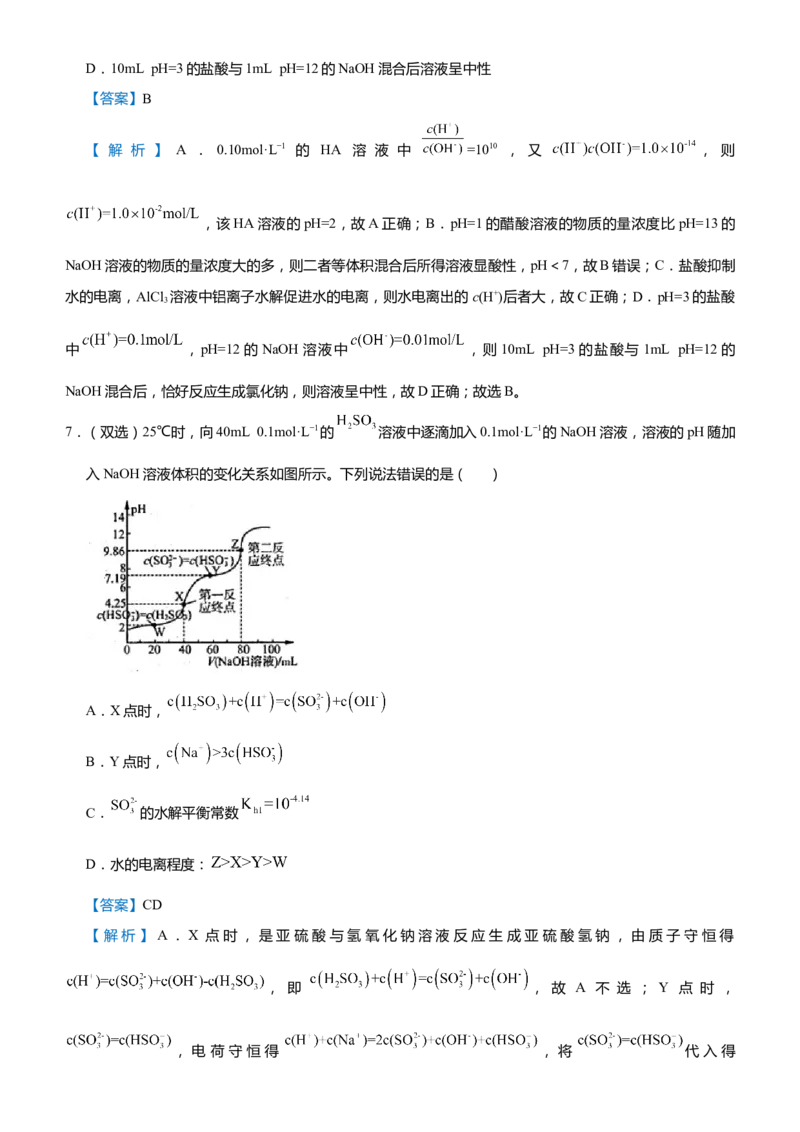
7.(双选)25℃时,向40mL 0.1mol·L−1的 溶液中逐滴加入0.1mol·L−1的NaOH溶液,溶液的pH随加
入NaOH溶液体积的变化关系如图所示。下列说法错误的是( )
A.X点时,
B.Y点时,
C. 的水解平衡常数
D.水的电离程度:
【答案】CD
【解析】A.X 点时,是亚硫酸与氢氧化钠溶液反应生成亚硫酸氢钠,由质子守恒得
, 即 , 故 A 不 选 ; Y 点 时 ,
, 电 荷 守 恒 得 , 将 代 入 得,因为 pH=7.19,所以 ,所以 ,故 B 不
选 ; C . 的 水 解 平 衡 常 数 , 在 Y 点 , , 代 入 得
,故C选;D.水的电离程度与氢离子浓度或者氢氧根浓度有关,当
只有亚硫酸时,水的电离程度最小,随着氢氧根的加入,到 X点,相当于亚硫酸氢钠,其电离大于水解,抑
制水的电离,只不过抑制程度减少,Y点接近水的正常电离,到Z点生成亚硫酸钠,促进水的电离,电离程
度最大,则水的电离程度: ,故D选;故选:CD。
8.室温下,①将浓度均为0.1mol/L的盐酸与氨水等体积混合,混合液 pH=a;②将浓度为b mol/L盐酸与
0.3mol/L氨水等体积混合,混合液pH=7(忽略溶液体积变化)。下列判断错误的是( )
A.a<7,b<0.3
B.常温下氨水的电离平衡常数
C.②中混合液存在:c(NH)+c(NH ·H O)+c(Cl−)=0.3mol/L
3 2
D.将①与②混合液混合,则混合后溶液中存在:c(Cl−)>c(NH)
【答案】C
【解析】A.①将浓度均为0.1mol/L的盐酸与氨水等体积混合,二者恰好完全反应生成氯化铵和水,氯化
铵水解显酸性,故混合液 pH=a<7;②将浓度为 b mol/L盐酸与 0.3mol/L氨水等体积混合,因该混合液
,故必须盐酸少量即b<0.3,A正确;B.由题意列电荷守恒得: ,因
室温下混合液 ,说明溶液显中性, ,所以 ,因等体积混合故
= mol/L。常温下氨水中一水合氨的电离方程式为NH ·H O NH+OH−,故其电离平衡常
3 2
数 ,B 正确;C.②中混合液存在物料守恒 c(NH)+c(NH ·H O)=
3 2, < ,故c(NH)+c(NH
3
·H
2
O)+c(Cl−)≠0.3mol/L,C错误;D.因①溶
液显酸性,②溶液显中性,故将①与②混合液混合显酸性, > ,由电荷守恒得:
,故 ,D正确;故选C。
9.I.25℃时,部分物质的电离平衡常数如表所示:
弱酸或弱碱 电离常数
NH ·H O K=2×10−5
3 2 b
HClO K=3×10−8
a
HCO K =4×10−7 K =4×10−11
2 3 a1 a2
HSO K =1.3×10−2 K =6.3×10−8
2 3 a1 a2
(1)0.1mol·L−1 NH ClO溶液中离子浓度由大到小的顺序是_____________________。
4
(2)等浓度的NaSO 、NaClO、NaCO、NaHCO 溶液,pH由大到小的顺序是________。
2 3 2 3 3
(3)某小组同学探究饱和NaClO和KAl(SO ) 溶液混合反应的实验,发现两种溶液混合后产生大量的白色胶
4 2
状沉淀。出现上述现象的原因是____________________(请用反应的离子方程式表示)。
II.用沉淀滴定法快速测定NaI溶液中c(I−),实验过程包括准备标准溶液和滴定待测溶液。
i.准备标准溶液
a.准确称取AgNO 基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保
3
存,备用。
b.配制并标定100mL 0.1000mol·L−1 NH SCN标准溶液,备用。
4
ii.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 0.1000mol·L−1 AgNO 溶液(过量),使I−完全转化为AgI沉淀。
3
c.加入NH Fe(SO ) 溶液作指示剂。
4 4 2
d.用0.1000mol·L−1 NH SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红
4
色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗NH SCN标准溶液体积/mL 10.24 10.02 9.98
4
f.数据处理。
回答下列问题:(4)滴定应在pH<0.5的条件下进行,其原因是____________________________。
(5)若在配制AgNO 标准溶液时,烧杯中的溶液有少量溅出,会导致 c(I−)测定结果___________(填“偏
3
高”、“偏低”或“不影响”)。
(6)测得c(I−)=__________mol·L−1。
【答案】(1)c(NH)>c(ClO−)>c(OH−)>c(H+)
(2)NaCO>NaClO>NaSO >NaHCO
2 3 2 3 3
(3)Al3++3ClO−+3H O=Al(OH) ↓+3HClO
2 3
(4)防止因Fe3+水解而影响滴定终点的判断
(5)偏高
(6)0.0600
【解析】(1)根据电离平衡常数NH ·H O的K=2×10−5,HClO的K=3×10−8,次氯酸根水解显碱性,铵根水
3 2 b a
解显酸性,根据越弱越水解,次氯酸根水解程度大于铵根水解程度,溶液显碱性,因此0.1mol·L−1 NH ClO溶
4
液中离子浓度由大到小的顺序是c(NH)>c(ClO−)>c(OH−)>c(H+);故答案为:c(NH)>c(ClO−)>c(OH−)>
c(H+)。(2)根据电离平衡常数得到酸强弱顺序:HSO >HCO > >HClO> ,根据对应的酸越
2 3 2 3
弱,其水解程度越大,碱性越强,因此等浓度的NaSO 、NaClO、NaCO 、NaHCO 溶液,pH由大到小的顺
2 3 2 3 3
序是NaCO>NaClO>NaSO >NaHCO ;故答案为:NaCO>NaClO>NaSO >NaHCO 。(3)根据题意说明
2 3 2 3 3 2 3 2 3 3
Al3+和ClO−发生双水解生成氢氧化铝沉淀和次氯酸,其离子方程式为Al3++3ClO−+3H O=Al(OH) ↓+3HClO;故
2 3
答案为:Al3++3ClO−+3H O=Al(OH) ↓+3HClO。(4)由于铁离子发生水解而影响滴定终点的判断,因此滴定应
2 3
在pH<0.5的条件下进行;故答案为:防止因Fe3+水解而影响滴定终点的判断。(5)若在配制AgNO 标准溶液
3
时,烧杯中的溶液有少量溅出,则配制出的硝酸银浓度偏低,取等量的硝酸银,物质的量减少,则消耗的
NH SCN溶液的体积偏低,得到碘离子的量增大,因此会导致c(I−)测定结果偏高;故答案为:偏高。(6)根据
4
三次数据得出第一次数据是错误的数据,因此消耗NH SCN标准溶液平均体积为10.00mL,根据Ag+~I−~
4
AgI,则 n(I−)=0.1000mol·L−1×0.025L-0.1000mol·L−1×0.01L =0.0015mol,
;故答案为:0.0600。
10.用硫酸分解磷尾矿[主要成分为Ca (PO )F]可制得中强酸磷酸。已知:25℃时,HPO 的电离平衡常数:
5 4 3 3 4
K=7.1×10−3;K=6.3×10−8;K=4.2×10−13.请回答:
1 2 3
(1)NaH PO 溶液中c(HPO)________c(HPO )(填“>”“<”或“=”)。
2 4 3 4
(2)25℃时,HPO(aq)+OH−(aq) HPO(aq)+H O(l)的平衡常数K=___________。
2 2
(3)Ca (PO )F(s)+OH−(aq) Ca (PO )(OH)(s)+F−(aq),溶液中c(F−)随溶液的pH和温度(T)的变化曲线如
5 4 3 5 4 3
图所示。则:pH_______pH(填“>”“<”或“=”,下同);A、B 两点的溶液中用 F−表示的反应速率
1 2
υ(A)________υ(B)。
(4)下列说法正确的是___________
A.磷酸溶液中存在3个平衡
B.向pH=2的磷酸溶液中加入NaH PO 固体,溶液酸性降低
2 4
C.向NaHPO 溶液中滴加稀盐酸的过程中 的值增大
2 4
D.向NaH PO 溶液中滴加NaOH至过量,水的电离程度先增大后减小
2 4
【答案】(1)>
(2)6.3×106
(3)< >
(4)BD
【解析】(1)NaH PO 溶液中HPO既要电离又要水解,水解常数 ,因此说明
2 4 2
电离占主要,所以c(HPO)>c(HPO );故答案为:>。(2)25℃时,HPO(aq)+OH−(aq) HPO(aq)+H O(l)的
3 4 2 2
平衡常数 ;故答案为:6.3×106。
(3)作过B点与y轴的平行线,从下到上c(F−)增大,说明平衡正向移动,则说明向反应中增加了OH−浓度,因
此A点碱性更强即pH <pH ;A点的c(F−)比B点高,且A点的温度比B点温度高,因此两点的溶液中用F-
1 2
表示的反应速率υ(A)>υ(B);故答案为:<;>。(4)A.磷酸溶液中存在4个平衡即磷酸第一步电离平衡、
第二步电离平衡、第三步电离平衡和水的电离,故A错误;B.向pH=2的磷酸溶液中加入NaH PO 固体,
2 4
增加了HPO浓度,致使磷酸电离平衡逆向移动,氢离子浓度减低,因此溶液酸性降低,故B正确;C.向
2
NaHPO 溶液中滴加稀盐酸的过程中,氢离子浓度增大,因此 的值减小,故C错误;D.向
2 4
NaH PO 溶液中滴加NaOH至过量,先生成NaPO ,磷酸根水解,水的电离程度先增大,后来NaOH过量,
2 4 3 4
溶质是NaPO 和NaOH的混合溶液,NaOH抑制水的电离,水的电离程度减小,故D正确;综上所述,答案
3 4为BD。
11.某兴趣小组用废铝合金(成分为Al、Zn、Fe、Si)制备Al O 和Fe O、ZnSO·7H O,流程如图:
2 3 2 3 4 2
已知:①ZnSO·7H O晶体易溶于水,易风化。
4 2
②已知25℃常见离子沉淀的pH范围如下:
开始沉淀 完全沉淀
Fe3+ 1.5 3.7
Fe2+ 6.5 9.7
Al3+ 3.3 5.2
Zn2+ 5.4 8.2
回答下列问题:
(1)下列操作或描述正确的是___。
A.加入试剂A目的是将Fe2+氧化为Fe3+
B.调节pH=5.3,可用试剂ZnO
C.操作②中用玻璃棒在过滤器上搅拌以加快过滤速度
D.为制备ZnSO·7H O,可蒸发ZnSO 溶液至有大量晶体析出,再停止加热,用余热蒸干
4 2 4
(2)调节pH=2的目的是 。
(3)写出滤液③中加入碳酸氢钠溶液生成沉淀④的反应的离子方程式 。
(4)为了得到纯净的沉淀③,需要将沉淀③进行洗涤。洗涤沉淀的具体操作是 。
(5)判断滤液②是否有铁元素残留的简要实验方案为 。
【答案】(1)AB
(2)抑制Zn2+水解,提高晶体纯度
(3)AlO+HCO+H O=Al(OH) ↓+CO
2 3
(4)向漏斗中加入蒸馏水浸没沉淀物,使水自然流出后,重复2~3次
(5)取样,滴加KSCN溶液,显血红色说明残留Fe3+
【解析】废铝合金(成分为Al、Zn、Fe、Si)加入足量稀盐酸得到滤液①和沉淀①,滤液①中含有 Al3+、
Zn2+、Fe2+,沉淀①为Si;滤液①中加入试剂A,调节pH=5.3,得到滤液②和沉淀②,滤液②经一系列操作最终得到ZnSO·7H O,表明滤液②中含有Zn2+,根据离子沉淀的pH范围可知,pH=5.3时,Al3+、Fe3+会沉淀,
4 2
由此判定沉淀②中的成分为 Fe(OH) 、Al(OH) ;加入试剂 A则是为了使 Fe2+转化为Fe3+;沉淀②中加入
3 3
NaOH溶液,得到滤液③和沉淀③,滤液③的成分为NaAlO ,沉淀③为Fe(OH) ;沉淀④是Al(OH) 。(1)A.
2 3 3
加入试剂A的目的是,将Fe2+转化为Fe3+,A项正确;B.铝合金和足量稀硫酸反应得到滤液①,滤液①显酸
性,可以用碱或碱性氧化物调节pH,使pH=5.3,可用试剂ZnO并且不会引入杂质,B项正确;C.滤纸上用
玻璃棒搅拌会导致滤纸破损,从而导致漏液,C项错误;D.蒸发ZnSO 溶液至有大量晶体析出,再停止加
4
热,用余热蒸干,最终会得到ZnSO 固体,D项错误;答案选AB。(2)Zn2+易水解,调节pH=2是为了抑制
4
Zn2+水解,提高晶体纯度;(3)滤液③中加入碳酸氢钠溶液生成沉淀④,这一过程是NaAlO 和碳酸氢钠反应生
2
成Al(OH) 沉淀,离子方程式为:AlO+HCO+H O=Al(OH) ↓+CO;(4)洗涤沉淀的具体操作是:向漏斗中加入
3 2 3
蒸馏水浸没沉淀物,使水自然流出后,重复 2~3次;(5)滤液②中的Fe元素以Fe3+形式存在,所以只需验证
Fe3+是否存在即可判断滤液②是否有铁元素残留,简要的实验方案为:取样,滴加KSCN溶液,显血红色说
明残留Fe3+。
7.