文档内容
3.2019年12月以来,我国部分地区突发的新冠肺炎疫情严重威胁着人们的身体健康。研究发现洛匹
(新高考)2021 届高考考前冲刺卷
那韦对新冠病毒有较好抑制作用,洛匹那韦能溶于水,其结构如图所示,下列说法不正确的是
化 学(二)
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴
在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写 A.洛匹那韦的分子式为C H NO
37 48 4 5
在试题卷、草稿纸和答题卡上的非答题区域均无效。 B.洛匹那韦的水解产物之一遇Fe3+可显紫色
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和
C.洛匹那韦能发生取代、加成、消去、氧化、还原反应
答题卡上的非答题区域均无效。
D.洛匹那韦能溶于水与氢键作用有关
4.考试结束后,请将本试题卷和答题卡一并上交。
【答案】B
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
【解析】A.根据结构简式,洛匹那韦的分子式为C H NO,故A正确;B.洛匹那韦的水解产物中
37 48 4 5
没有酚羟基,遇Fe3+不能发生显色反应而显紫色,故B错误;C.洛匹那韦中含有羟基能发生取代反应、
一、选择题:每小题2分,共20分。每小题给出的四个选项中,只有一项是符合题目要求的。
1.手工制作工艺在我国有着悠长的历史,下列有关叙述不正确的是 苯环能发生加成反应、羟基的邻碳上有氢、能发生氧化反应能发生消去反应、羰基能发生还原反应,
A.北京糖人所用饴糖属于天然高分子化合物 故C正确;D.洛匹那韦能与水分子间形成氢键,增大分子间作用力,故D正确;故选B。
B.苏绣又称丝绣,所用蚕丝的主要成分为蛋白质 4.设N 为阿伏加德罗常数的数值,下列说法正确的是
A
C.秦朝兵马俑用陶土烧制而成,属于无机非金属材料 A.将0.1mol H 和0.2mol I 充入密闭容器中充分反应后,生成HI的分子数为0.2N
2 2 A
D.芜湖铁画属于铁制品,属于合金材料 B.1.0mol/L的CHCOONa溶液中所含CHCOO−的数目小于N
3 3 A
【答案】A C.标准状况下,2.24L CHCl 中所含C-Cl键的数目为0.2N
2 2 A
【解析】A.饴糖是低聚糖,不是高分子化合物,A错误;B.苏绣又称丝绣,所用材料是蚕丝,蚕丝的 D.1mol硝基(-NO )与46g二氧化氮(NO )所含的电子数均为23N
2 2 A
主要成分为蛋白质,B正确;C.秦朝兵马俑用陶土烧制而成,因此属于硅酸盐产品,硅酸盐产品属于 【答案】D
【解析】A.碘和氢气的反应为可逆反应,故不能进行彻底,则生成的HI分子个数小于2N 个,A项
无机非金属材料,C正确;D.芜湖铁画所用材料是铁合金,属于铁制品,D正确;故合理选项是A。 A
2.生活处处有化学,下列说法正确的是 错误;B.溶液体积未知,所以溶液中醋酸根离子数目无法确定,B项错误;C.二氯甲烷标况下为液态,
A.食品中的淀粉和纤维素的组成都可用(C H O) 表示,它们互为同分异构体 不能用气体摩尔体积计算C-Cl键的数目,C项错误;D.1mol硝基(-NO )含有23N 电子,46g二氧
6 10 5 n 2 A
B.棉、麻、丝、毛的燃烧产物都只有CO 和HO
2 2
C.在紫外线、饱和CuSO 溶液、福尔马林等作用下,蛋白质均会发生变性
4
化氮(NO )摩尔数为 所含的电子数也为23N ,D项正确;答案选D。
2 A
D.煎炸食物的花生油和牛油都是可皂化的饱和酯类
【答案】C 5.短周期元素W、X、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X最外层电子数的2倍,
【解析】A.聚合度n不同,二者不是同分异构体,故A错误;B.丝、毛的成分为蛋白质,含N元素,
Z最外层电子数等于最内层电子数,X、Y、Z简单离子的电子层结构相同,W的单质是空气中体积
燃烧有含氮物质生成,而棉、麻的燃烧产物都只有CO 和HO,故B错误;C.强酸、强碱、紫外线、饱
2 2 分数最大的气体。下列说法正确的是
和CuSO 4 溶液等重金属盐、福尔马林均使蛋白质发生变性,故C正确;D.花生油为不饱和高级脂肪酸 A.元素非金属性由强到弱的顺序:Y、X、W
甘油酯,牛油为饱和酯类,均可发生皂化反应,故D错误;答案选C。 B.W的简单气态氢化物比Y的简单气态氢化物稳定
封密不订装只卷此
号位座
号场考
号证考准
名姓
级班C.原子半径由大到小的顺序:Z、Y、X、W
A. 晶体中存在I离子,I离子的空间构型为V形
D.WX与ZX中的化学键类型相同
B.三氯化氮(NCl )是一种极性分子,NCl 还能再以配位键与Cl−结合
【答案】A 3 3
C.PH 和NH 分子中均含有孤电子对,且PH 提供孤电子对的能力强于NH
【解析】W的单质是空气中体积分数最大的气体可知W是N元素,W、X、Y、Z的原子序数依次增 3 3 3 3
D.BeO的晶格能大于MgO,可推测BeCO 的分解温度低于MgCO
3 3
大,Z最外层电子数等于最内层电子数,可知Z为Mg元素,W与Y最外层电子数之和为X最外层电
【答案】B
子数的2倍,且X、Y、Z简单离子的电子层结构相同,可知X为O元素,Y为F元素。A.同周期自左
向右非金属性逐渐增强,则元素非金属性由强到弱的顺序为F>O>N,A正确;B.非金属性越强,氢 【解析】A.I离子中心I原子价层电子对数为:2+ =4,由于I原子上有2对共用电子对,
化物越稳定,则Y的简单气态氢化物比W的简单气态氢化物稳定,B错误;C.同周期自左向右原子
所以其空间构型为V形,A正确;B.NCl 分子中的中性N原子以及Cl−没有空轨道可以容纳孤电子对,
3
半径逐渐减小,同主族自上而下原子半径逐渐增大,原子半径由大到小的顺序:Z、W、X、Y,C错误;
所以NCl 不能再以配位键与Cl−结合,B错误;C.P、N原子最外层都是由5个电子,其中含有1对孤
3
D.NO与MgO中的化学键类型不相同,其中是共价键,后者是离子键,D错误;答案选A。
电子对,3个成单电子与H原子形成共价键,都能提供孤电子对,由于N的电负性比P大,所以对孤
6.根据下列实验操作过程中颜色变化所得出的结论正确的是
电子对吸引能力N比P强,因此PH 提供孤电子对的能力比NH 强,C正确;D.BeO的晶格能大于
3 3
选项 实验操作和现象 结论
MgO,可知阳离子半径越小对氧的吸引力越大,夺取氧的能力越强,所以碳酸铍分解生成氧化铍比碳
将NaClO溶液滴入品红溶液中,品红溶液缓慢褪 酸镁分解生成氧化镁容易,则可推测出BeCO 的分解温度低于MgCO ,D正确;故合理选项是B。
A ClO−的氧化性随pH的减小而增强 3 3
色;若同时加入食醋,红色很快褪去
8.现用如下实验装置在实验室制取溴苯(夹持装置已略去),反应引发后,扎紧软橡胶袋口。下列说法
将石油分馏的产品石蜡加热,产生的气体通入酸
B 石油中含有烯烃 不正确的是
性高锰酸钾溶液中,溶液紫红色逐渐褪去
向滴有酚酞的氨水中加入CHCOONH 固体,溶
C 3 4 CHCOONH 溶液呈酸性
液的红色变浅 3 4
向含AgCl和AgBr的饱和溶液中加入足量浓
D 溶液中c(Cl−)/c(Br−)减小
AgNO 溶液,产生两种颜色沉淀,但以白色为主
3
【答案】A
【解析】A.将NaClO溶液滴入品红溶液中,品红溶液缓慢褪色;若同时加入食醋,红色很快褪去,
A.托起A中软橡胶袋使铁粉落下引发反应
说明溶液酸性越强,反应速率越快,酸性越强pH越小,所以ClO−的氧化性随pH的减小而增强,A符
B.B中双球管中液体颜色逐渐变为橙色
合题意;B.石蜡加热,产生的气体通入酸性高锰酸钾溶液中,溶液紫红色逐渐褪去,只能说明石蜡的
C.若CCl 过量,则C中无明显现象
4
分解产物中含有不饱和烃,但不一定是烯烃,B不符题意;C.CHCOONH 电离生成的铵根离子抑制
3 4 D.D中倒置的漏斗可增大吸收面积防止倒吸
一水合氨的电离,溶液中的氢氧根离子减少,溶液碱性减弱,红色变浅,而CH 3 COONH 4 溶液呈中性, 【答案】C
【解析】A.铁粉沿导管落下,与溴生成溴化铁,催化引发反应,故A正确;B.B中装CCl 的双球管
4
吸收苯和溴蒸气,溶液颜色变为橙色,故B正确;C.苯与溴反应为取代反应生成HBr,C中生成AgBr
C不符题意;D. ,由于温度不变,则K (AgCl)、K (AgBr)
sp sp
浅黄色沉淀,故C错误;D.倒置的漏斗可增大吸收面积防止倒吸,故D正确;故选C。
9.在2L恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g) 2C(g)+D(s),所得实验数据如下
c(Cl—)
表:
不变,所以c(Br—)不变,D不符题意;答案选A。
起始时物质的量/
平衡时物质的量/mol
实验编 mol
7.下列说法不正确的是 号
温度/℃
n(A) n(B) n(C)子从负极移向正极,即H+由左室通过质子交换膜进入右室,故B错误;C.b极上N元素的化合价降低,
b是正极,发生还原反应,电极反应式为:2NO+10e−+12H+=N↑+6H O,故C正确;D.原电池中电流从
① 600 0.30 0.20 0.30 2 2
正极流向负极,电流由b电极沿导线流向a电极,故D错误;故选C。
② 700 0.20 0.30 0.24
二、选择题:本题共5小题,每小题4分,共20分。在每小题给出的四个选项中,有1个或2个选项符
③ 800 0.10 0.10 a
合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
下列说法不正确的是
11.我国科研人员通过控制光沉积的方法构建Cu O-Pt/SiC/IrO 型复合材料光催化剂,其中Fe2+和
2 x
A.实验①中,若5min时测得n(B)=0.050mol,则0至5min时间内平均反应速率v(A)=0.015
Fe3+离子渗透Nafion膜可协同CO、HO分别反应,构建了一个人工光合作用体系,其反应机理如
2 2
mol/(L·min)
图:
B.实验②中达到平衡后,增大压强,A的转化率不变,平衡常数不变
C.700℃时该反应的平衡常数K=4.0
D.实验③中,达到平衡时,a>0.10
【答案】D
【解析】实验①中,若5min时测得n(B)=0.050mol,则0至5min时间内消耗B 0.150mol,平均反应
速率v(A)=v(B)=0.015mol/(L·min),故A正确;B.该反应气体物质的量不变化,实验②中达到平衡后,
增大压强,平衡不移动,A的转化率不变,平衡常数不变,故B正确;C.700℃时各物质平衡浓度:
下列说法正确的是
A.该反应为2CO+2H O=========2HCOOH+O
2 2 2
B.该反应能量转化形式为光能→化学能
c(A)=0.04mol/L,c(B)=0.09mol/L,c(C)=0.12mol/L,该反应的平衡常数K= =4.0,故C正确;
C.图中a、b分别代表Fe3+、Fe2+
D.实验①平衡时n(C)>实验②平衡时n(C),表明升温平衡左移,平衡常数随温度升高而减小。实验③ D.反应过程中涉及到非极性键、极性键的断裂和形成
中,达到平衡时,若a>0.10,则c(A)<0.025mol/L,c(B)<0.025mol/L,c(C)>0.05mol/L,该反应的平衡常 【答案】AB
数K>4.0,故D不正确。故选D。 【解析】A.根据图示可知,反应物为二氧化碳和水,生成物为甲酸和氧气,因此该反应方程式为
8.一种微生物燃料电池如图所示,下列关于该电池的说法正确的是 2CO+2H O=========2HCOOH+O ,故A正确;B.由“人工光合作用体系”可知,该反应能量转化
2 2 2
形式为光能→化学能,故B正确;C.观察图中物质转化关系可知,b代表Fe3+,用于氧化HO,a代表
2
Fe2+,用于还原CO,故C错误;D.根据A项总反应可知,反应过程中不涉及到非极性共价键的断裂,
2
故D错误;答案选AB。
12.配合物[Cu(En) ]SO 的名称是硫酸二乙二胺合铜,是铜的一种重要化合物。其中En是乙二胺
2 4
(H N-CH -CH-NH )的简写。有关说法中正确的是
2 2 2 2
A.a电极发生还原反应 A.该配合物中含有离子键、极性共价键、非极性共价键、配位键、氢键等化学键
B.H+由右室通过质子交换膜进入左室 B.配体乙二胺分子中氮原子、碳原子轨道的杂化类型不同
C.b电极反应式为2NO+10e−+12H+=N ↑+6H O C.该配合物中金属离子的价电子构型为3d10
2 2
D.电池工作时,电流由a电极沿导线流向b电极 D.乙二胺和三甲胺[N(CH )]均属于胺,乙二胺比三甲胺的沸点高
3 3
【答案】C 【答案】D
【解析】A.b极上N元素的化合价降低,所以b是正极发生还原反应,故A错误;B.原电池中阳离 【解析】A.[Cu(En)]2+、SO之间是离子键;Cu2+与HN-CH-CH-NH 通过配位键结合;HN-
2 2 2 2 2 2CH-CH-NH 中存在极性共价键和非极性共价键、SO中存在极性共价键和配位键,但是氢键不属
2 2 2
=c(H+),则由X点处的pH,可计算K (HS)的值,故C错误;D.NaHS溶液中加入
a2 2
于化学键,选项A错误;B.乙二胺分子中氮原子形成3个σ键,价电子对数是 =4,氮原子轨道 CuSO 溶液,硫化铜难溶于稀酸,发生反应:Cu2++HS−=CuS↓+H+,溶液显示强酸性,故D正确;故选
4
D。
14.钛酸钡(BaTiO )在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子
3
的杂化类型为sp3;碳原子形成4个σ键,价电子对数是 =4,碳原子轨道的杂化类型为sp3,二者 元件。以下是生产钛酸钡的一种工艺流程图:
杂化类型相同,选项B错误;C.En是乙二胺,分子整体显0价,硫酸根显-2价,则根据“正负化合价
的代数和等于零”可以判断铜显+2价,其价电子构型为3d9,选项C错误;D.由于乙二胺分子之间可
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C O)·4H O;
2 4 2 2
以形成氢键,三甲胺分子之间不能形成氢键,所以乙二胺比三甲胺的沸点高得多,选项D正确。答案
②25℃时,BaCO 的溶度积K =2.58×10−9。
3 sp
选D。
下列说法错误的是
13.向等物质的量浓度的NaS、NaOH混合溶液中滴加稀盐酸至过量。其中主要含硫物种(H S、HS−、
2 2
A.BaTiO 中Ti元素的化合价为+4
3
S2−)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示
B.在“酸浸”过程中为加快反应速率可用浓硫酸代替浓盐酸
(忽略滴加过程中HS气体的逸出)。下列说法不正确的是
2 C.流程中可以通过过滤得到草酸氧化钛钡晶体
D.若浸出液中c(Ba2+)=0.1mol/L,则c(CO)在浸出液中的最大浓度为2.58×10−8mol/L
【答案】B
【解析】由制备流程可知,BaCO 用盐酸酸浸得到氯化钡溶液,再向氯化钡混合液中加入TiCl 溶液
3 4
和草酸溶液得到草酸氧化钛钡晶体和HCl,生成的HCl可循环利用,最后通过洗涤、干燥、煅烧草酸
氧化钛钡晶体得到BaTiO 。A.BaTiO 中O为-2价,Ba为+2价,则Ti元素的化合价为2×3-2=4,即+4
3 3
价,故A正确;B.如用浓硫酸代替浓盐酸,可生成硫酸钡沉淀,消耗钡离子,难以得到钛酸钡,故B错
A.含硫物种B表示HS−
误;C.由流程可知,加入草酸,得到草酸氧化钛钡晶体,可用过滤的方法得到,故C正确;D.若浸出液
B.在滴加盐酸过程中,溶液中c(Na+)与含硫物种浓度的关系为c(Na+)=2[c(HS)+c(HS−)+c(S2−)]
2
C.X、Y为曲线的两交叉点,若能知道X点处的pH,就可以计算出HS的K
2 a1
D.NaHS溶液呈碱性,若向该溶液中加入CuSO 溶液,恰好完全反应时所得溶液呈强酸性,其原 中c(Ba2+)=0.1mol/L,则c(CO)在浸出液中的最大浓度为 mol/L=2.58×
4
因是Cu2++HS−=CuS↓+H+
10−8mol/L,故D正确;故选B。
【答案】BC
15.CuSO 是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法正确的是
4
【解析】向等物质的量浓度NaS、NaOH混合溶液中滴加稀盐酸,盐酸和氢氧化钠先反应,然后和
2
硫化钠反应,A表示含硫微粒浓度减小,则A为S2−;B先增加后减少,则B为HS−;C开始时几乎不存
在,之后逐渐增大,则C为HS。A.B先增加后减少,则B为HS−,故A正确;B.向等物质的量浓度
2
NaS、NaOH混合溶液中滴加稀盐酸,若忽略滴加过程HS气体的逸出,根据混合液Na、S物料守恒
2 2
A.相对于途径①,途径②更好地体现了绿色化学思想
可得:c(Na+)=3[c(HS)+c(HS−)+c(S2−)],故 B 错误;C.X 点为 S2−和 HS−浓度相同,K (HS)=
2 2 2
B.将CuSO 溶液蒸发,利用余热蒸干,可制得胆矾晶体
4
C.X可能是SO 和SO 的混合气体
2 3D.Y可以是蔗糖溶液 (5)除去所得金属钛中少量的金属镁可用的试剂是___________。
【答案】A 【答案】(1)+4 FeTiO +2HSO (浓)=TiOSO +FeSO +2HO
3 2 4 4 4 2
【解析】A.Cu和浓硫酸加热反应生成CuSO 、SO 、HO,途径①产生了有毒气体,相对于途径①, (2)防止Fe2+被氧化
4 2 2
途径②更好地体现了绿色化学思想,A项正确;B.将CuSO 溶液蒸发,利用余热蒸干,会导致开始得 (3)9 TiO2++2HO=TiO(OH) ↓+2H+或TiO2++2HO=HTiO ↓+2H+ FeSO ·7H O 烧杯、漏斗、
4 2 2 2 2 3 4 2
到的胆矾晶体失去结晶水,故无法得到胆矾,B项错误;C.CuSO 热分解生成两种产物,其中一种为 玻璃棒
4
(4)隔绝空气
Cu O,Cu化合价降低,则必有元素的化合价升高,CuSO 中只有O元素的化合价能升高,故X中必有
2 4
(5)稀盐酸或稀硫酸
O,C项错误;D.CuSO 与过量NaOH溶液反应会生成Cu(OH) 悬浊液,蔗糖不是还原性的糖,不能
2 4 2
【解析】向钛铁矿(主要成分为钛酸亚铁)中加浓硫酸使其转化为可溶性的硫酸亚铁等;然后加水和
还原新制Cu(OH) 悬浊液生成Cu O,D项错误;答案选A。
2 2
加铁粉除消耗多于的氢离子外还可防止亚铁离子被氧化成铁离子;沉降分离后得到TiOSO 以及硫酸
三、非选择题:本题共5小题,共60分。 4
亚铁的混合溶液,然后冷却结晶,过滤得到硫酸亚铁晶体和溶液II,向溶液II中加水并加热过滤得到
16.金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料。以钛铁矿(主要
钛酸和回收硫酸;将钛酸煅烧得到二氧化钛,在高温条件下与碳和氯气反应生成四氯化钛,然后四氯
成分为钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如图所示。
化钛与镁在高温下反应生成钛单质。(1)根据2R+C=====2Fe+2TiO+CO ↑以及原子守恒,可得钛酸亚
2 2
铁的化学式为FeTiO ,根据化合物中各元素化合价代数和为零可得FeTiO 中Ti的化合价为+4价;钛
3 3
酸亚铁和浓HSO 反应的产物之一是TiOSO,反应中无气体生成,则该反应为非氧化还原反应,则其
2 4 4
反应为:FeTiO +2HSO (浓)=TiOsO +FeSO +2HO;(2)由分析可知,加铁粉的主要目的是为了防止亚
3 2 4 4 4 2
铁离子被氧化,故答案为:防止Fe2+被氧化;(3)① ,所以有
请回答下列问题:
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为:2R+C=====2Fe+2TiO+CO ↑,钛酸亚
2 2
,pOH=5,则pH=14-pOH=9,故答案为9;②若将含有Fe2+、
铁中钛元素的化合价为___________,钛酸亚铁和浓HSO 反应的产物之一是TiOSO,反应中无气体
2 4 4
生成,该反应的化学方程式为___________。
TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,结合表中K 数据可知TiO(OH) 的K 最小,
sp 2 sp
(2)上述生产流程中加入铁屑的目的是___________。
则所得该白色沉淀为氢氧化氧钛,则该反应的方程式为:TiO2++2HO=TiO(OH) ↓+2H+或 TiO2+
2 2
(3)溶液I中含有Fe2+、TiO2+和少量Mg2+等阳离子,常温下,其对应氢氧化物的K 如表所示。
sp
+2HO=HTiO ↓+2H+;③由分析可知,溶液I经冷却、结晶、过滤,得到的副产物甲是为FeSO ·7H O,
2 2 3 4 2
氢氧化物 Fe(OH) TiO(OH) Mg(OH)
2 2 2 过滤时所需的玻璃仪器有漏斗、玻璃棒以及烧杯,故答案为:FeSO ·7H O;漏斗、玻璃棒、烧杯;(4)Mg
4 2
为活泼金属,容易被氧气氧化,所以Mg还原TiCl 过程除必须在1070K的温度下进行外还应隔绝空
K 8.0×10−16 1.0×10−29 1.8×10−11 4
sp
气,故答案为:隔绝空气;(5)常温时耐酸碱腐蚀,所以除去所得金属钛中少量的金属镁可用的试剂为
①常温下,若所得溶液中Mg2+的物质的量浓度为0.18mol·L−1,当溶液的pH等于___________时,
稀硫酸或稀盐酸,故答案为:稀硫酸或稀盐酸。
Mg(OH) 开始沉淀。
2
17.钴及其化合物在催化剂、磁性材料、电池等领域应用十分广泛。回答下列问题:
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为
(1)纳米氧化钴可以在室温下将甲醛完全催化氧化为CO 和HO。
2 2
___________。
①基态钴原子的核外电子排布式为[Ar]_______。
③溶液I经冷却、结晶、过滤,得到的副产物甲是___________,过滤需要的主要玻璃仪器是
②甲醛分子中三种元素电负性由大到小的顺序为_______(填元素符号);甲醛分子的立体构型为
___________。
_______;分子中σ键与π键数目比为_______。
(4)Mg还原TiCl 过程必须在1070K的温度下进行,你认为还应该控制的反应条件是___________。
4
(2)[Co(NH )]Cl 是橙黄色晶体,该配合物中提供空轨道接受孤对电子的微粒是_______,NH 分子
3 6 3 3中氮原子的杂化轨道类型为_______,NH 是_______(填“极性”或“非极性”)分子。
3
g·cm−3。
(3)LiCoO 可用作锂离子电池的电极材料。在元素周期表中,与Li的化学性质最相似的邻族元素
2
是_______(填元素符号),该元素基态原子核外M层电子的自旋状态_______(填“相同”或“相反”);
18.水合肼(N H·H O)是一种重要的化工原料,工业上用尿素[CO(NH)]、NaOH和NaClO溶液反应
2 4 2 2 2
LiF的熔点为848℃,属于_______晶体,LiF的熔点高于LiCl熔点(605℃)的原因是_______。
制备水合肼的实验流程如图:据此某化学兴趣小组设计了下列实验制备NH·H O。
2 4 2
(4)某钴化合物纳米粉可以提高碱性电池的性能。该化合物晶胞结构如图所示,已知晶胞参数为a
nm,则此晶体的密度为(列出计算式即可)_______g·cm−3。
查阅资料:①3NaClO====2NaCl+NaClO ;②NH·H O易溶于水,熔点-40℃,沸点为118℃,具有
3 2 4 2
强还原性,能与NaClO剧烈反应生成N;属于二元弱碱,在空气中可吸收CO 而产生烟雾。
2 2
【答案】(1)3d74s2 O>C>H 平面三角形 3∶1
[实验一]制备NaClO溶液
(2)Co3+ sp3 极性
(3)Mg 相反 离子 LiF、LiCl均为离子晶体,F−半径小于Cl−,且所带电荷数相等,则LiF
的晶格能大于LiCl
(4)
【解析】(1)①基态钴原子为27号元素,则核外电子排布式为[Ar]3d74s2;②甲醛分子中含有C、H、O
三种元素,非金属性越强,电负性越大,则电负性由大到小的顺序为O>C>H;甲醛分子中心碳原子
回答下列问题:
有3条键,无孤电子对,为sp2杂化,则空间构型为平面三角形;分子中含有3个σ键,1个π键,则σ
(1)盛装浓盐酸仪器的名称是_______,加入实验药品之前必须进行的操作是_______。
键与π键数目比为3∶1;(2)[Co(NH )]Cl 是配合物,Co3+提供空轨道;NH 分子中氮原子含有3条共
3 6 3 3 (2)装置II中为了提高NaClO的产率,用冰水浴控制温度在30℃以下,其主要原因是_______。
价键,1对孤电子对,则杂化轨道类型为sp3杂化;空间构型为三角锥型,则为由极性键构成的极性分
(3)装置III的作用是_______。
子;(3)根据对角线原则,在元素周期表中,与Li的化学性质最相似的邻族元素是Mg;该元素基态原
[实验二]制备水合肼
子核外M层电子为3s2,自旋状态相反;LiF的熔点为848℃,属于离子晶体;LiF、LiCl均为离子晶体,
F−半径小于Cl−,且所带电荷数相等,则LiF的晶格能大于LiCl,故LiF的熔点高于LiCl熔点(605℃);
(4)根据晶胞的结构,Co在晶胞的顶点个数=8× =1,Ti在晶胞的体内个数为1,O在晶胞的面心,个
(4)装置中的直形冷凝管_______(填“能”或“不能”)用球形冷凝管代替。
数=6× =3,则1mol晶胞的质量=(59+48+16×3)g,1mol晶胞的体积=(a nm)3×N ,则此晶体的密度=
A
(5)三颈烧瓶中生成水合肼的化学反应方程式:_______。
(6)滴加NaClO溶液时不能过快、过多的原因是_______。
(7)有同学认为该实验收集装置有缺陷,请你写出改进措施_______。【答案】(1)分液漏斗 检查装置气密性
(2)防止温度高,使NaClO分解
(3)吸收尾气,防止污染空气
(4)不能
(5)NaClO+CO(NH )+2NaOH=NH∙H O+NaCl+Na CO
2 2 2 4 2 2 3
(6)防止水合肼被NaClO氧化
(7)在锥形瓶导管上连接装有碱石灰的干燥管,防止空气中二氧化碳进入收集装置 A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液
【解析】实验一:装置I中浓盐酸与二氧化锰共热制备氯气,氯气通入冰水浴中的30%的NaOH溶 C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H++2e−=H↑
2
液中,生成NaCl、NaClO,防止温度过高生成氯酸钠;氯气有毒,装置III中用NaOH吸收未反应的氯 (3)将不同量的CO(g)和H 2 O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H 2 O(g)
CO(g)+H(g),得到如下三组数据:
气。实验二:三颈烧瓶中NaClO与尿素反应生成水合肼,控制温度,使水合肼变为蒸汽溢出,水合肼具 2 2
有强还原性,能与NaClO剧烈反应生成N 2 ,则滴加NaClO溶液时不能过快、过多;利用冷凝管冷凝水 起始量/mol 平衡量/mol 达到平衡所需时间/min
实验组 温度/℃
合肼,在锥形瓶中收集;水合肼在空气中可吸收CO 而产生烟雾,则需在锥形瓶后加装有碱石灰的干
2
HO CO CO
2 2
燥管,防止空气中二氧化碳进入收集装置。(1)根据装置特点,盛装浓盐酸仪器的名称是分液漏斗;连
1 650 2 4 1.6 5
接装置后,应先检验装置的气密性;(2)已知加热NaClO溶液可生成氯酸钠,则用冰水浴控制温度在
2 900 1 2 0.4 3
30℃以下,可防止温度过高NaClO分解;(3)氯气有毒,则装置III的作用是吸收未反应的氯气,防止污
3 900 1 2 0.4 1
染空气;(4)球形冷凝管一般用于合成装置中的冷凝回流,直形冷凝管用于蒸馏实验的冷凝,则装置中
①该反应的正反应为_____(填“吸”或“放”)热反应。
的直形冷凝管不能用球形冷凝管代替;(5)三颈烧瓶中NaClO、NaOH与尿素反应生成水合肼和碳酸钠,
②实验2中,平衡常数K=_____。
化学反应方程式为NaClO+CO(NH )+2NaOH=NH∙H O+NaCl+Na CO
2 2 2 4 2 2 3
③实验3跟实验2相比,改变的条件可能是_____(答一种情况即可)。
;(6)水合肼具有强还原性,能与NaClO剧烈反应生成N,滴加NaClO溶液时不能过快、过多;(7)水合
2
(4)将2.4g碳在足量氧气中燃烧,所得气体通入100mL 3.0mol/L的氢氧化钠溶液中,完全吸收后,
肼在空气中可吸收CO 而产生烟雾,则需在锥形瓶后加装有碱石灰的干燥管,防止空气中二氧化碳进
2
溶液中所含离子的物质的量浓度由大到小的顺序_____。
入收集装置。
【答案】(1)Fe O(s)+3CO(g)=2Fe(s)+3CO (g) ΔH=-28.5kJ/mol PdCl +CO+H O=Pd+CO+2HCl
19.碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生 2 3 2 2 2 2
(2)C H+26OH−-20e−=3CO+17H O ABD
3 8 2
活”不再只是一种理想,更是一种值得期待的新的生活方式。
(3)放热 0.167 使用了催化剂或增大了压强
(1)将CO 与焦炭作用生成CO,CO可用于炼铁等.
2
(4)c(Na+)>c(HCO)>c(CO)>c(OH−)>c(H+)
①已知:Fe O(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=+489.0kJ/mol
2 3 1
【解析】(1)①Fe O(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH =+489.0kJ/mol ①;C(石墨)+CO (g)=
2 3 1 2
C(石墨)+CO (g)=2CO(g) ΔH=+172.5kJ/mol
2 2
2CO(g) ΔH=+172.5kJ/mol ②;由①-②×3,得到热化学方程式:Fe O(s)+3CO(g)=2Fe(s)+3CO (g)
则CO还原Fe O 的热化学方程式为 。 2 2 3 2
2 3
ΔH=-28.5kJ/mol,故答案为:Fe O(s)+3CO(g)=2Fe(s)+3CO (g) ΔH=-28.5kJ/mol,②氧化还原反应
②氯化钯(PdCl )溶液常被应用于检测空气中微量CO、PdCl 被还原成单质,反应的化学方程式为 2 3 2
2 2
规律,CO与PdCl 溶液反应,PdCl 被还原成单质,则CO被氧化成CO,根据质量守恒定律,有水参与
。 2 2 2
反应同时生成氯化氢,反应的化学方程式为:PdCl +CO+H O=Pd+CO+2HCl,故答案为:
(2)将两个石墨电极插入KOH溶液中,向两极分别通入C H 和O 构成丙烷燃料电池。 2 2 2
3 8 2
①负极电极反应式是: 。 PdCl 2 +CO+H 2 O=Pd+CO 2 +2HCl;(2)C 3 H 8 和 O 2 构成丙烷燃料电池的总反应:C 3 H 8 +5O 2 +6OH−=
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH) 的实验装置(如图所示),通电后,溶液 3CO+7H O,正极发生还原反应,电极反应式为:O+4e−+2H O=4OH−,负极发生氧化反应,电极反应
2 2 2 2
中产生大量的白色沉淀,且较长时间不变色.下列说法中正确的是_____(填序号)。 式为:C H+26OH−-20e−=3CO+17H O;故答案为:C H+26OH−-20e−=3CO+17H O;②A.因为生成的
3 8 2 3 8 2氢气将装置中原有氧气溢出,所以氢气从B端阴极析出,A电极则是铁做阳极失去电子生成亚铁离子,
电源中的a与A相连,则a为正极,b与B相连,则b为负极,选项A正确;B.电解池中阳极是铁失去 已知: +R-OH
电子发生氧化反应生成亚铁离子,阴极是溶液中的氢离子得电子发生还原反应,所以电解质溶液中的
阴离子不会在阳极失电子,所以选用NaCl溶液不影响实验,选项B正确;C.阳极应该用铁电极,阴极 回答下列问题:
可以是铁也可以是其他惰性电极,选项C错误;D.阴极氢离子放电,其电极反应为2H++2e−=H↑,选 (1)D的名称是______。
2
(2)D→E反应①的化学方程式是_______。
项D正确;答案选ABD;(3)①实验1中CO的转化率为 ×100%=40%,实验2中CO的转化 (3)E→F的反应类型为_______。
(4)J中的含氧官能团除硝基外还有_______(填官能团名称)。
率为 ×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动, (5)化合物X是H的同系物,其分子式为C HON,其核磁共振氢谱有3组峰,则X的结构简式可
8 9 3
能为_______(写一种即可)。
正反应放热,故答案为:放热;
(6)D的同分异构体中能发生水解反应有 种(不考虑立体异构),其中核磁共振氢谱有4组
CO(g) + H O(g) CO(g)+H(g)
2 2 2
峰,峰面积之比为1∶2∶2∶3的结构简式为_______。
②起始量(mol/L) 0.5 1 0 0
变化量(mol/L) 0.2 0.2 0.2 0.2
(7)参照题中合成路线图,设计以2-甲基-1-丙烯和 为原料来合成 的
平衡量(mol/L) 0.3 0.8 0.2 0.2
合成路线_______。
根据K= = =0.167;③实验3跟实验2相比,温度相同,浓度相同,但实
【答案】(1)2-甲基-2-羟基丙醛
验3达到平衡所用时间少,反应速率更大,但平衡状态没有发生移动,应是使用了催化剂,又由于反
(2) +2Cu(OH) +NaOH――→ +Cu O↓+3HO
应前后气体体积不变,则增大了压强,平衡也不移动,也可能为压强的增大,故答案为:使用了催化剂 2 2 2
或增大了压强;(4)2.4g碳是0.2mol,燃烧生成0.2mol CO,与0.3mol NaOH反应的化学方程式为:
2
(3)取代反应
2CO+3NaOH=NaHCO +Na CO+H O,生成0.1mol NaCO、0.1mol NaHCO ,在含等物质的量的碳
2 3 2 3 2 2 3 3
(4)醚键、羧基
酸钠、碳酸氢钠的溶液中,c(Na+)最大,碳酸根离子水解大于碳酸氢根离子的水解,则 c(HCO)>
c(CO),水解使溶液显碱性,则c(OH−)>c(H+),显性离子大于隐性离子,所以c(HCO)>c(CO)>c(OH−)
(5) 或
>c(H+),即离子浓度大小为:c(Na+)>c(HCO)>c(CO)>c(OH−)>c(H+),故答案为:c(Na+)>c(HCO)>
c(CO)>c(OH−)>c(H+)。
(6)4 HCOOCH CHCH
2 2 3
20.有机物J在有机化工领域具有十分重要的价值。2018年我国首次使用α-溴代羰基化合物合成了
J,其合成路线如下:
(7)
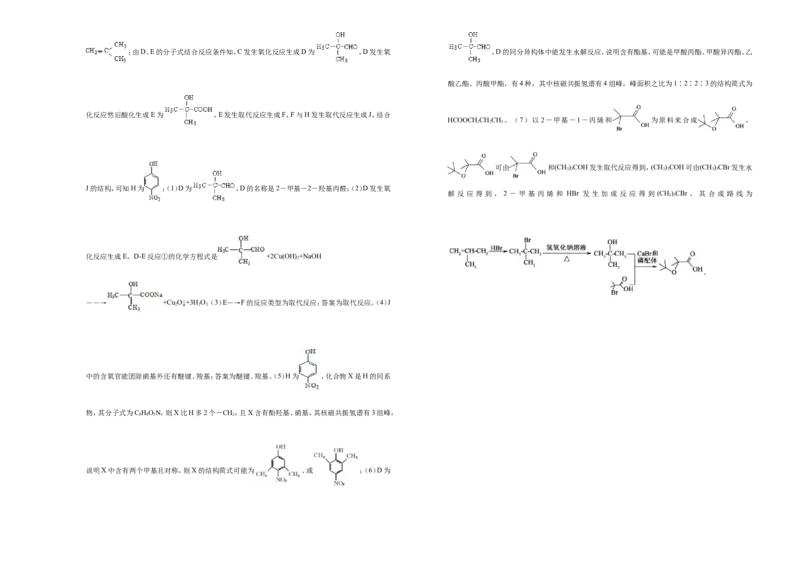
【解析】A发生加成反应生成B,B水解生成C,由C的结构逆推可知B为 ,A为;由D、E的分子式结合反应条件知,C发生氧化反应生成D为 ,D发生氧 ,D的同分异构体中能发生水解反应,说明含有酯基,可能是甲酸丙酯、甲酸异丙酯、乙
酸乙酯、丙酸甲酯,有4种,其中核磁共振氢谱有4组峰,峰面积之比为1∶2∶2∶3的结构简式为
化反应然后酸化生成E为 ,E发生取代反应生成F,F与H发生取代反应生成J,结合
HCOOCH CHCH 。(7)以 2-甲基-1-丙烯和 为原料来合成 ,
2 2 3
可由 和(CH)COH发生取代反应得到,(CH)COH可由(CH)CBr发生水
3 3 3 3 3 3
J的结构,可知H为 ;(1)D为 ,D的名称是2-甲基-2-羟基丙醛;(2)D发生氧
解 反 应 得 到 , 2 - 甲 基 丙 烯 和 HBr 发 生 加 成 反 应 得 到 (CH)CBr , 其 合 成 路 线 为
3 3
化反应生成E,D-E反应①的化学方程式是 +2Cu(OH) +NaOH
2
。
――→ +Cu O↓+3HO;(3)E―→F的反应类型为取代反应;答案为取代反应。(4)J
2 2
中的含氧官能团除硝基外还有醚键、羧基;答案为醚键、羧基。(5)H为 ,化合物X是H的同系
物,其分子式为C HON,则X比H多2个-CH,且X含有酚羟基、硝基,其核磁共振氢谱有3组峰,
8 9 3 2
说明X中含有两个甲基且对称,则X的结构简式可能为 、或 ;(6)D为