文档内容
第 20 讲 硫酸 硫酸盐
[复习目标] 1.掌握浓硫酸的三大特性及应用。2.熟知常见的硫酸盐,掌握SO的检验方法。
3.能依据信息,控制条件制取硫的复杂含氧酸盐并探究其性质。
考点一 硫酸及其工业制法
1.硫酸的物理性质
HSO 是无色液体,能与水以任意比互溶,稀释时放出大量的热,浓HSO 稀释的方法是
2 4 2 4
_______________________________________________________________________________
_______________________________________________________________________________
。
2.浓硫酸的三大特性
3.硫酸的工业制法
(1)制备流程
完成相关反应的化学方程式:
①____________________________________________________________________________,
_______________________________________________________________________________
;②____________________________________________________________________________。
(2)常考问题
①SO 进入催化反应室前净化、干燥的目的是________________________________________
2
______________________________________________________________________________。
②工业生产SO 采用常压的原因:_________________________________________________
2
_______________________________________________________________________________
。
③用98.3%的浓硫酸吸收SO 而不用水的原因:_____________________________________。
3
1.浓硫酸具有强氧化性,所以浓硫酸不可用于干燥H 和CO( )
2
2.少量胆矾加入浓硫酸中,蓝色晶体变白,体现浓硫酸的吸水性( )
3.用玻璃棒蘸取浓硫酸滴在滤纸上,滤纸变黑,体现浓硫酸的脱水性( )
4.将铜片加入盛有浓硫酸的试管中,加热铜片逐渐溶解,产生无色、有刺激性气味的气体,
体现浓硫酸的强氧化性、酸性( )
5.将少量铜加入浓硫酸中加热,很快能观察到溶液变为蓝色( )
6.一定量浓硫酸中加入足量锌粒加热,产生的气体为SO 和H 的混合气体( )
2 2
7.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化( )
8.工业上可用稀硫酸洗去锅炉中的水垢( )
一、浓HSO 的特性及应用
2 4
1.下列有关硫酸的实验或用途中利用了硫酸的哪些性质?
(1)用浓硫酸作干燥剂干燥CO、SO 、Cl 等气体:____________________________________。
2 2
(2) 分 别 用 浓 硫 酸 与 NaCl(s) 、 NaNO (s) 反 应 制 取 HCl 、 HNO :
3 3
____________________________
_______________________________________________________________________________
。
(3)用铝或铁制容器贮存或运输浓硫酸:_____________________________________________
_______________________________________________________________________________
。
(4)工业上用硫酸与磷酸钙反应制取磷酸:___________________________________________
________________________。
(5)实验室用铜与浓硫酸反应制取SO :_____________________________________________
2
________________________。
(6)实验室用甲酸与浓硫酸作用制取CO:HCOOH――――→CO+HO:__________________
2______________________________________________________________________________。
(7)浓硫酸与蔗糖制取“黑面包”的实验:__________________________________________。
2.下列有机反应中都要使用硫酸。其中使用浓硫酸的是____________(填序号,下同),使
用稀硫酸的是________________。
(1)苯的硝化 (2)乙醇的消去
(3)乙醇与乙酸的酯化 (4)乙酸乙酯的水解
(5)糖类物质的水解 (6)蛋白质的水解
(7)油脂的水解
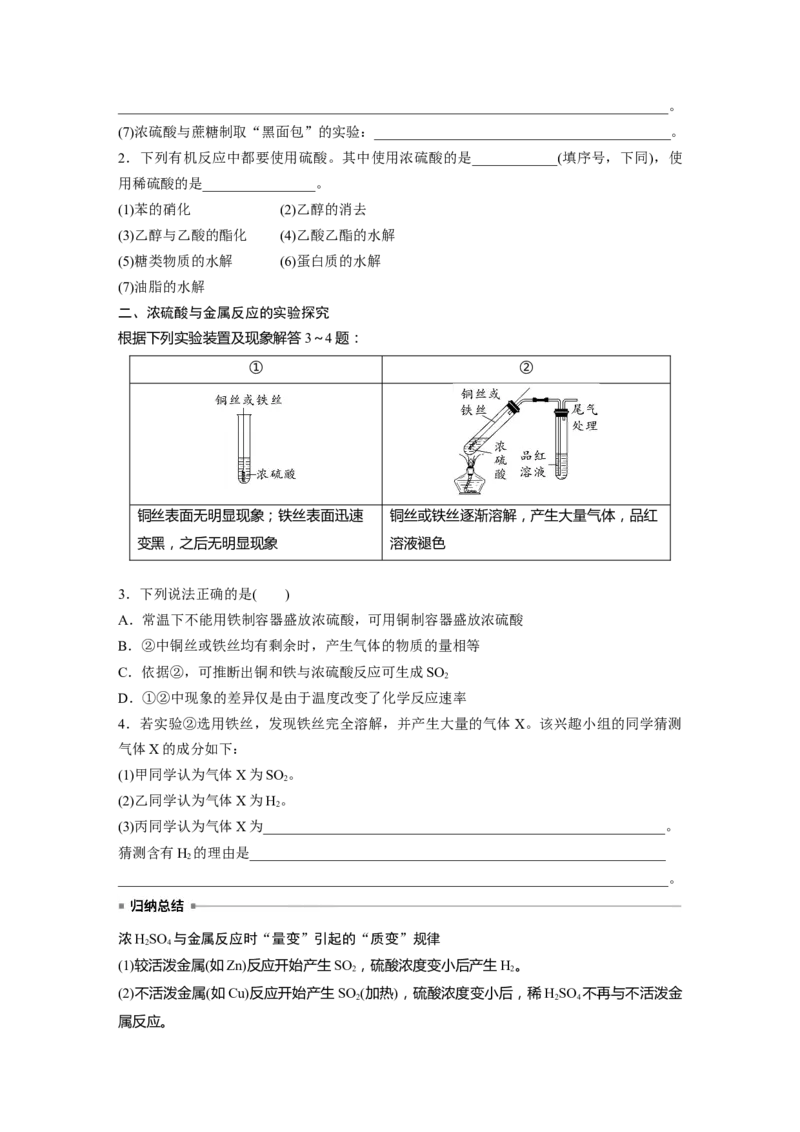
二、浓硫酸与金属反应的实验探究
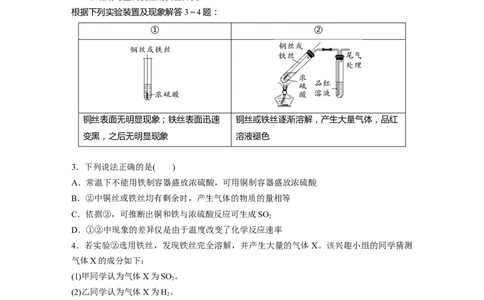
根据下列实验装置及现象解答3~4题:
① ②
铜丝表面无明显现象;铁丝表面迅速 铜丝或铁丝逐渐溶解,产生大量气体,品红
变黑,之后无明显现象 溶液褪色
3.下列说法正确的是( )
A.常温下不能用铁制容器盛放浓硫酸,可用铜制容器盛放浓硫酸
B.②中铜丝或铁丝均有剩余时,产生气体的物质的量相等
C.依据②,可推断出铜和铁与浓硫酸反应可生成SO
2
D.①②中现象的差异仅是由于温度改变了化学反应速率
4.若实验②选用铁丝,发现铁丝完全溶解,并产生大量的气体X。该兴趣小组的同学猜测
气体X的成分如下:
(1)甲同学认为气体X为SO 。
2
(2)乙同学认为气体X为H。
2
(3)丙同学认为气体X为_________________________________________________________。
猜测含有H 的理由是___________________________________________________________
2
______________________________________________________________________________。
浓HSO 与金属反应时“量变”引起的“质变”规律
2 4
(1)较活泼金属(如Zn)反应开始产生SO ,硫酸浓度变小后产生H。
2 2
(2)不活泼金属(如Cu)反应开始产生SO (加热),硫酸浓度变小后,稀HSO 不再与不活泼金
2 2 4
属反应。考点二 SO 的检验 硫的复杂含氧酸盐
1.常见的硫酸盐
名称 化学式 用途
重晶石 白色颜料、胃肠镜的内服药剂等
石膏 医学、工业、建筑等使用的材料
胆矾 媒染剂、杀虫剂、消毒剂、饲料添加剂和镀铜电解液等
明矾 净水剂、灭火剂、膨化剂、药物等
2.SO的检验
检验SO的正确操作方法:被检液――――――――→取清液――――――→有无白色沉淀产生(判断有无
SO)。
先加稀盐酸的目的是________________________________,再加BaCl 溶液,有白色沉淀产
2
生 。 整 个 过 程 中 可 能 发 生 反 应 的 离 子 方 程 式 : ________________________ 、
____________________________、_______________________________________________、
_____________________________________________________________________________。
一、SO检验实验方案设计
1.下列过程中,最终的白色沉淀物不一定是BaSO 的是( )
4
A.Fe(NO ) 溶液――――――――――――――→白色沉淀
3 2
B.Ba(NO ) 溶液―――――――――――――→白色沉淀
3 2
C.无色溶液―――――――――→白色沉淀
D.无色溶液―――――→无色溶液―――――→白色沉淀
2.有一瓶NaSO 溶液,试设计实验探究NaSO 的氧化程度。
2 3 2 3
________________________________________________________________________
________________________________________________________________________
二、硫的复杂含氧酸盐的制备
3.硫代硫酸钠(Na SO)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用
2 2 3
反应2NaS+NaCO +4SO ===3NaSO +CO 制得。实验室模拟该工业过程的装置如图所
2 2 3 2 2 2 3 2
示。回答下列问题:
(1)b中反应的离子方程式为_______________________________________________________
________________________________________________________________________,c 中试
剂为______________________________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________(写化学式)。
(3)d中的试剂为________________。
(4) 实 验 中 要 控 制 SO 生 成 速 率 , 可 以 采 取 的 措 施 有
2
____________________________________
______________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO 不能过量,原因是___________________
2
_______________________________________________________________________________
。
4.[2018·全国卷Ⅰ,27(1)(2)]焦亚硫酸钠(Na SO)在医药、橡胶、印染、食品等方面应用广
2 2 5
泛。回答下列问题:
(1)生产NaSO ,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式:
2 2 5 3
______________________________________________________________________________。
(2)利用烟道气中的SO 生产NaSO 的工艺:
2 2 2 5
①pH=4.1时,Ⅰ中为____________(写化学式)溶液。
②工艺中加入NaCO 固体,并再次充入SO 的目的是_______________________________。
2 3 2
5.连二亚硫酸钠(Na SO)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白
2 2 4
剂。NaSO 易溶于水,不溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。回答下列
2 2 4
问题:
(1)Na SO 在潮湿空气中被氧化,生成的两种常见酸式盐是____________________________
2 2 4
____________________________________________________________________(填化学式)。
(2)锌粉法制备NaSO 的工艺流程如图所示:
2 2 4①工业上常将锌块进行预处理得到锌粉-水悬浊液,其目的是__________________________。
②步骤Ⅰ中发生反应的化学方程式为______________________________________________
______________________________________________________________________________。
③在步骤Ⅲ中得到的NaSO 固体要用乙醇洗涤,其优点是__________________________,
2 2 4
“后续处理”最终要加入少量的NaCO 固体,其原因是_____________________________。
2 3
(3)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将 HCOONa和烧碱加入乙
醇水溶液中,然后通入 SO 发生反应,有 CO 气体放出,总反应的离子方程式是
2 2
______________________________________________________________________________
______________________________________________________________________________。
几种硫的复杂含氧酸盐
(1)硫代硫酸钠(Na SO) 俗名大苏打,它是无色透明的晶体,易溶于水,溶于水后溶液呈碱
2 2 3
性。它受热、遇酸易分解,其与酸反应的离子方程式:SO+2H+===S↓+SO ↑+HO。它
2 2 2
具有较强的还原性,可用作分析试剂及鞣革还原剂。
(2)连二亚硫酸钠(Na SO)能溶于冷水,在热水中分解,不溶于乙醇。其水溶液有很强的还
2 2 4
原性,在碱性介质中较稳定,在空气中易被氧化。
(3)焦亚硫酸钠(Na SO) 具有还原性,温度高于150 ℃易分解,在食品加工中常作防腐剂、
2 2 5
漂白剂、疏松剂。
(4)过二硫酸钠(Na SO)中S元素的化合价是+6价,其阴离子SO结构中含有1个过氧键(—
2 2 8 2
O—O—),性质与过氧化氢相似,具有氧化性,是一种强氧化剂。
1.正误判断,正确的打“√”,错误的打“×”。
(1)工业上煅烧黄铁矿(FeS )生产SO (2023·浙江1月选考,5B)( )
2 2
(2)浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化(2023·河北,10A)( )
2 4
(3)稀硫酸具有酸性,可用于除去铁锈(2019·江苏,3B)( )
(4)向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸,有刺激性气味气体产生,溶液变浑浊
(2019·全国卷Ⅱ,10C)( )
(5)用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:SO +2OH-===SO+HO(2022·福
3 2
建,8C)( )2.(2019·上海等级考试,12)证明亚硫酸钠部分变质所需要的试剂是( )
A.硝酸钡,稀硫酸 B.稀盐酸,氯化钡
C.稀硫酸,氯化钡 D.稀硝酸,氯化钡
3.(2022·广东,5)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的
探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
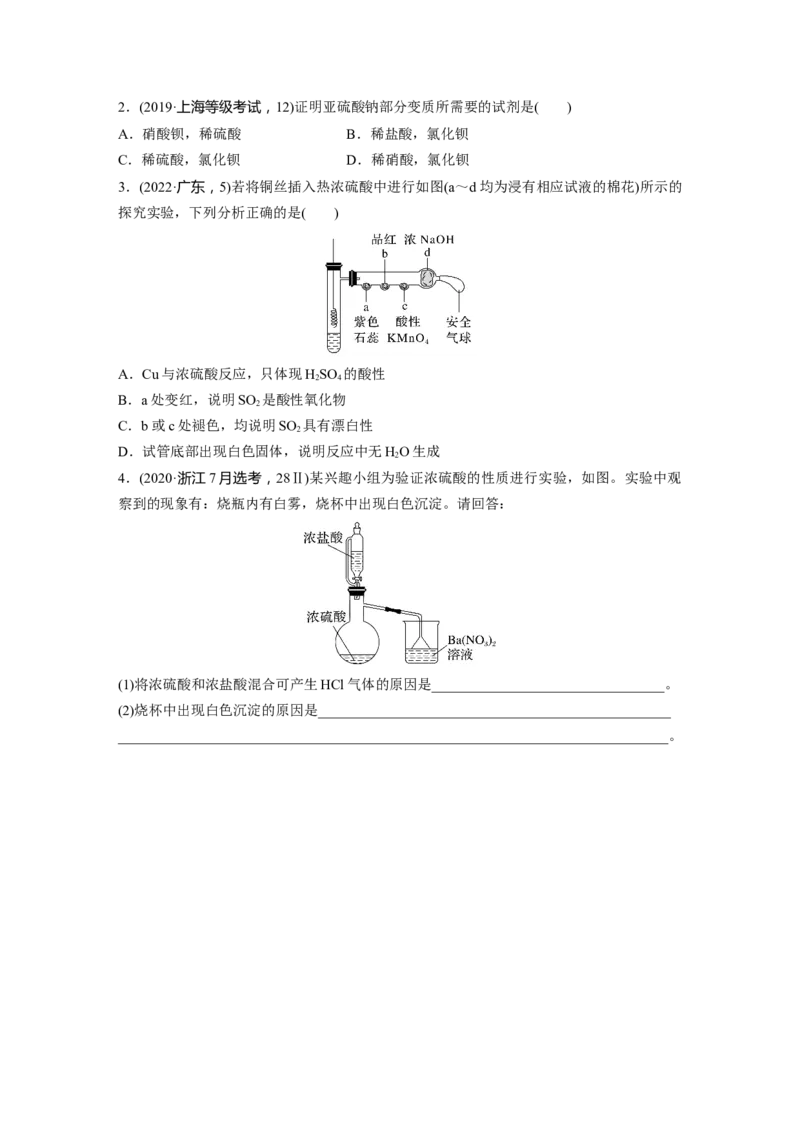
4.(2020·浙江7月选考,28Ⅱ)某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观
察到的现象有:烧瓶内有白雾,烧杯中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生HCl气体的原因是_________________________________。
(2)烧杯中出现白色沉淀的原因是__________________________________________________
______________________________________________________________________________。