文档内容
闵行区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2020.1
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Ca-40
一、选择题
1.硅是制成光伏电池的重要材料,硅的元素符号是( )
A. Se B. Si C. Sl D. Sn
2.70 周年庆典活动中属于化学变化的是( )
A. 变化的队形 B. 雄壮的军乐 C. 行进的检阅车 D. 威武的礼炮
3.属于可回收垃圾的是( )
A. 饮料瓶 B. 废弃的树叶 C. 烟头 D. 废旧荧光灯
4.将少量下列调味品加入水中,不能形成溶液的是
A. 食盐 B. 蔗糖 C. 味精 D. 芝麻油
5.属于氧化物的是( )
A. 空气 B. 液氧 C. 水 D. 碳酸钙
6.互为同素异形体 的物质是( )
A. 干冰与冰 B. 金刚石和石墨 C. 水银与银 D. 氢气与液氢
7.触摸屏的材料之一是氧化铟。氧化铟(InO)中铟元素(In)的化合价为
2 3
A. 0 B. +2 C. +3 D. +6
8.化学符号中“3”的含义表述正确的是( )
A. 3H:3 个氢元素 B. O:3 个氧原子
3
C. 3N:3 个氮分子 D. CO :三氧化碳
2 3
9.氨气(NH )燃烧反应的化学方程式为:4NH + 3O 点燃 6HO + 2 X,则X的化学式为
3 3 2 2
A. H B. O C. N D. NO
2 2 2 2
10.用途利用其物理性质的是( )
A. 金刚石作钻探机钻头 B. 氧气用于炼钢
C. 稀有气体用作保护气 D. 二氧化碳用作气体肥料
11.氧气变成液氧时,分析正确的是( )A. 分子从运动到静止 B. 分子间隔变小
C. 分子种类发生变化 D. 分子体积增小
12.实验操作和目的对应关系错误的是( )
A 测定空气中氧气体积分数时,首先要检查气密性 使实验结果更准确
B 配制一定浓度的 NaCl 溶液时,仰视量筒刻度读数 导致溶液浓度偏大
C 铁丝在氧气中燃烧时,集气瓶底部放少量水 放置炸裂瓶底
D 用双氧水制氧气时,加入少量二氧化锰 加快氧气生成速度
A. A B. B C. C D. D
13.不随水的质量改变的是( )
A. 物质的溶解度 B. 溶质质量分数
C. 溶液的 pH 值 D. 饱和溶液的状态
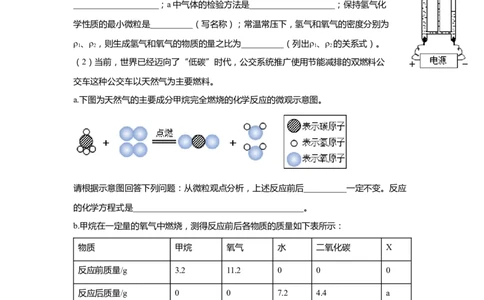
14.具有启普发生器工作原理的装置是( )
A. B.
C. D.
15.有关柠檬酸(C HO)的说法正确的是( )
6 8 7
A. 式量为 192g
B. 该物质中碳元素的质量分数最大
C. 分子中碳、氢、氧三种原子的物质的量之比是 6:8:7
D. 该物质由 6 个碳原子、8 个氢原子和 7 个氧原子构成
16.不能达到实验目的是( )选项 实验目的 实验方法
A 鉴别 CO 和 CO 通过灼热的氧化铜
2
B 除去 CO 中的少量 CO 通过灼热的氧化铜
2
C 鉴别 CuO 和 C 通入 CO,并加热
D 除去 CuO 中的少量 C 通入 CO,并加热
A. A B. B C. C D. D
17.下列说法正确的是( )
A. 0.5mol O 含 6.02×1023 个氧
2
B. 0.5mol NH 中含 1.204×1023 个原子
3
C. 等物质的量的 O 比 O 多 1 个氧原子
3 2
D. 等质量的 CO 和 N 所含原子数一样
2
18.在室温下将少量氧化钙加入到一定量的饱和氢氧化钙溶液中,搅拌并恢复到室温。图像
中 x 代表时间,则 y 代表的是( )
A. 溶剂的质量 B. 溶质的溶解度
C. 溶质的质量 D. 溶质的质量分数
19.已知某物质的以下数据,不能计算出该物质摩尔质量的是( )
A. 微粒个数和质量 B. 一个分子的真实质量
C. 物质的量和质量 D. 物质的量和微粒个数
20.有关“不一定”的说法正确的是( )
①冷却热饱和溶液,不一定有晶体析出
②在一定的条件下碳与氧气反应,不一定生成二氧化碳
③能使紫色石蕊试液变蓝色的溶液,不一定是碱性溶液
④化合物中的某种元素转变为单质,不一定要通过分解反应
A. ①②④ B. ①②③ C. ②③④ D. ①②③④
二、填空题
21.要使世界更美好,必须学好好学。
Ⅰ.化学使生活更健康。(1)自来水往往通过沉淀、__________、吸附、消毒杀菌等方法净化获得。
(2)为了预防碘缺乏症的发生,我国提倡食用加碘食盐,其中的“碘”是指__________。
A单质 B分子 C原子 D元素
(3)柚子皮可以吸附室内异味,写出一种具有同样性质的化学物质的名称__________。
Ⅱ.化学使能源更环保。
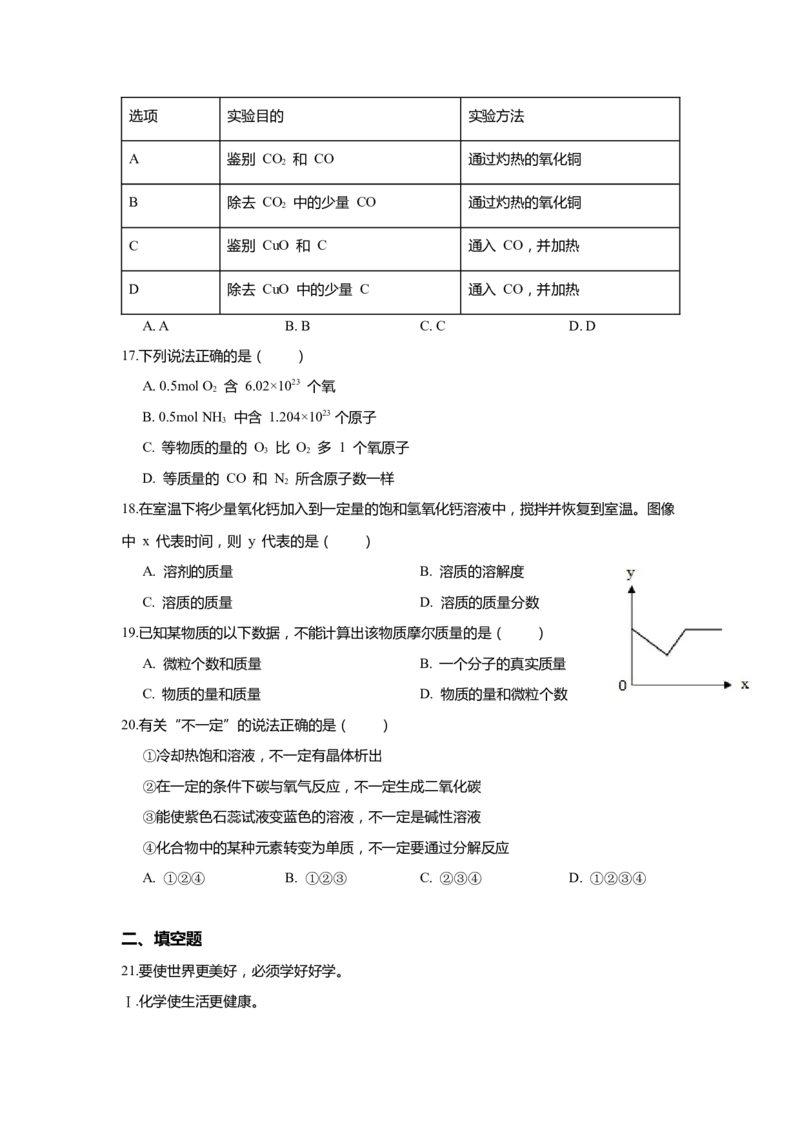
(1)绿色能源氢气可由如图电解水实验装置得到。该反应的化学方程式是
____________________,基本反应类型____________________。通电后观察到的现象
____________________;a中气体的检验方法是____________________;保持氢气化
学性质的最小微粒是__________(写名称);常温常压下,氢气和氧气的密度分别为
、,则生成氢气和氧气的物质的量之比为__________(列出、 的关系式)。
1 2 1 2
(2)当前,世界已经迈向了“低碳”时代,公交系统推广使用节能减排的双燃料公
交车这种公交车以天然气为主要燃料。
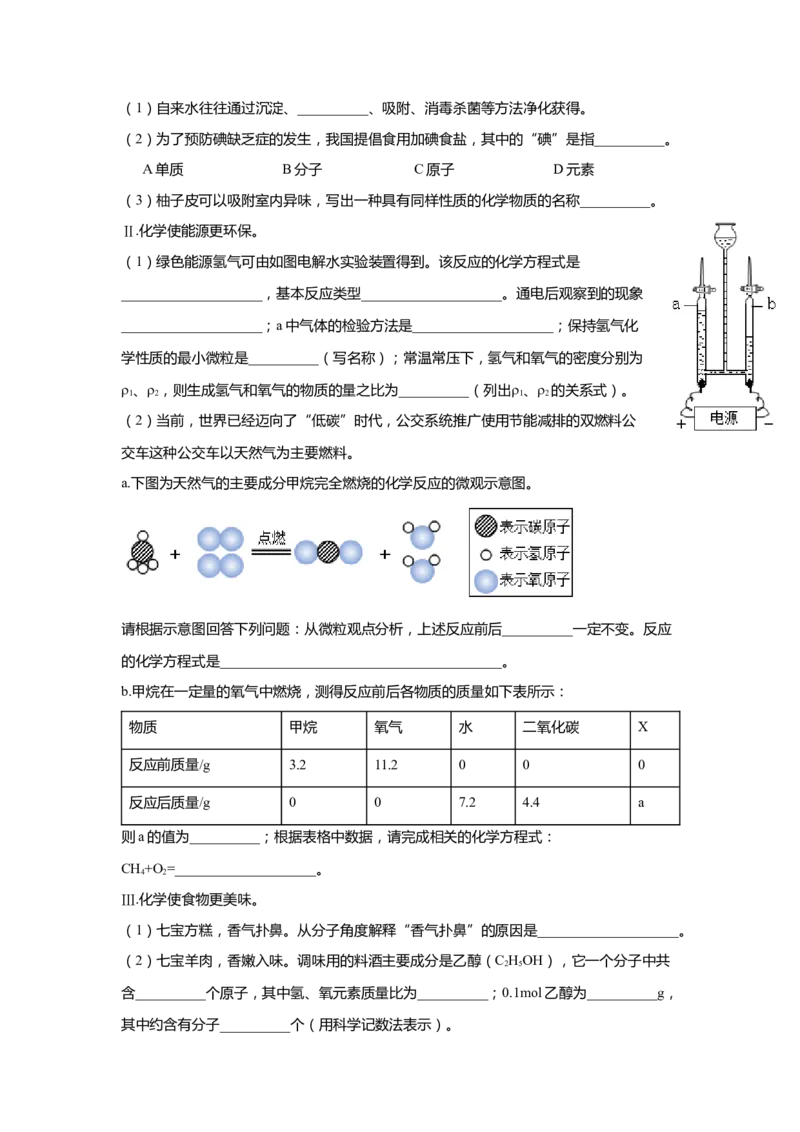
a.下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图。
请根据示意图回答下列问题:从微粒观点分析,上述反应前后__________一定不变。反应
的化学方程式是________________________________________。
b.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 甲烷 氧气 水 二氧化碳 X
反应前质量/g 3.2 11.2 0 0 0
反应后质量/g 0 0 7.2 4.4 a
则a的值为__________;根据表格中数据,请完成相关的化学方程式:
CH+O =____________________。
4 2
Ⅲ.化学使食物更美味。
(1)七宝方糕,香气扑鼻。从分子角度解释“香气扑鼻”的原因是____________________。
(2)七宝羊肉,香嫩入味。调味用的料酒主要成分是乙醇(C HOH),它一个分子中共
2 5
含__________个原子,其中氢、氧元素质量比为__________;0.1mol乙醇为__________g,
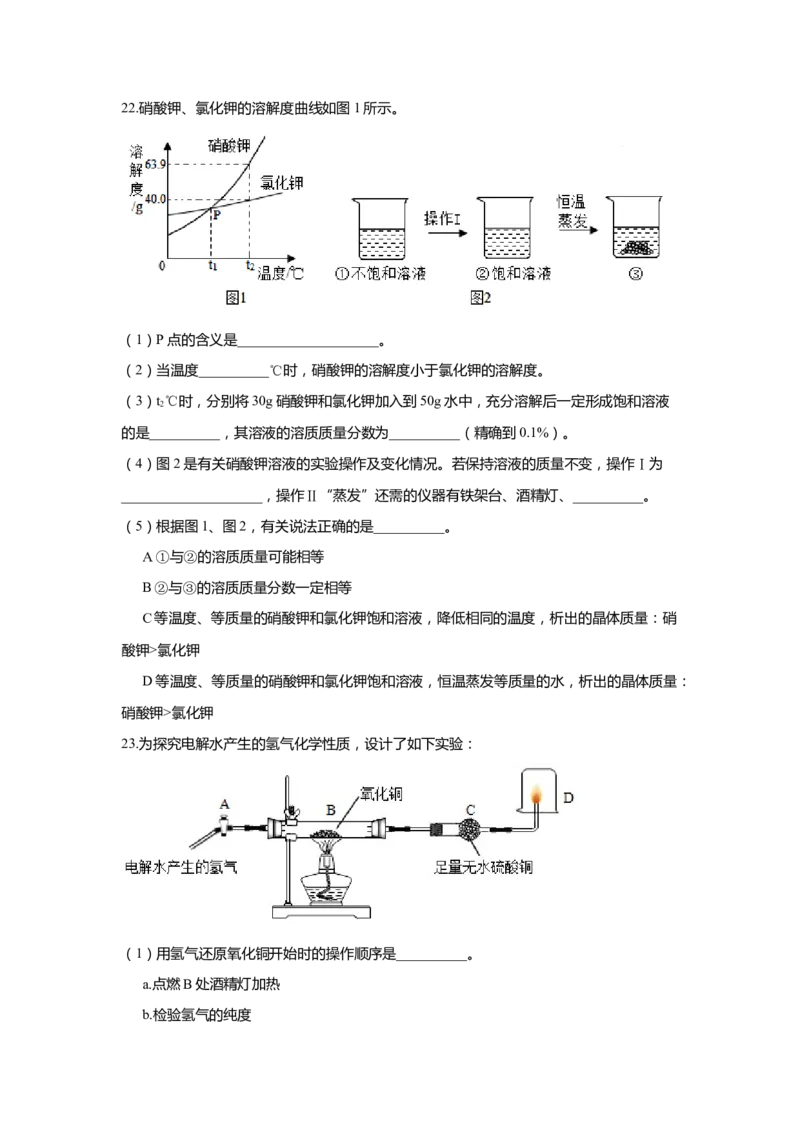
其中约含有分子__________个(用科学记数法表示)。22.硝酸钾、氯化钾的溶解度曲线如图1所示。
(1)P点的含义是____________________。
(2)当温度__________℃时,硝酸钾的溶解度小于氯化钾的溶解度。
(3)t℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液
2
的是__________,其溶液的溶质质量分数为__________(精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为
____________________,操作Ⅱ“蒸发”还需的仪器有铁架台、酒精灯、__________。
(5)根据图1、图2,有关说法正确的是__________。
A①与②的溶质质量可能相等
B②与③的溶质质量分数一定相等
C等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝
酸钾>氯化钾
D等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:
硝酸钾>氯化钾
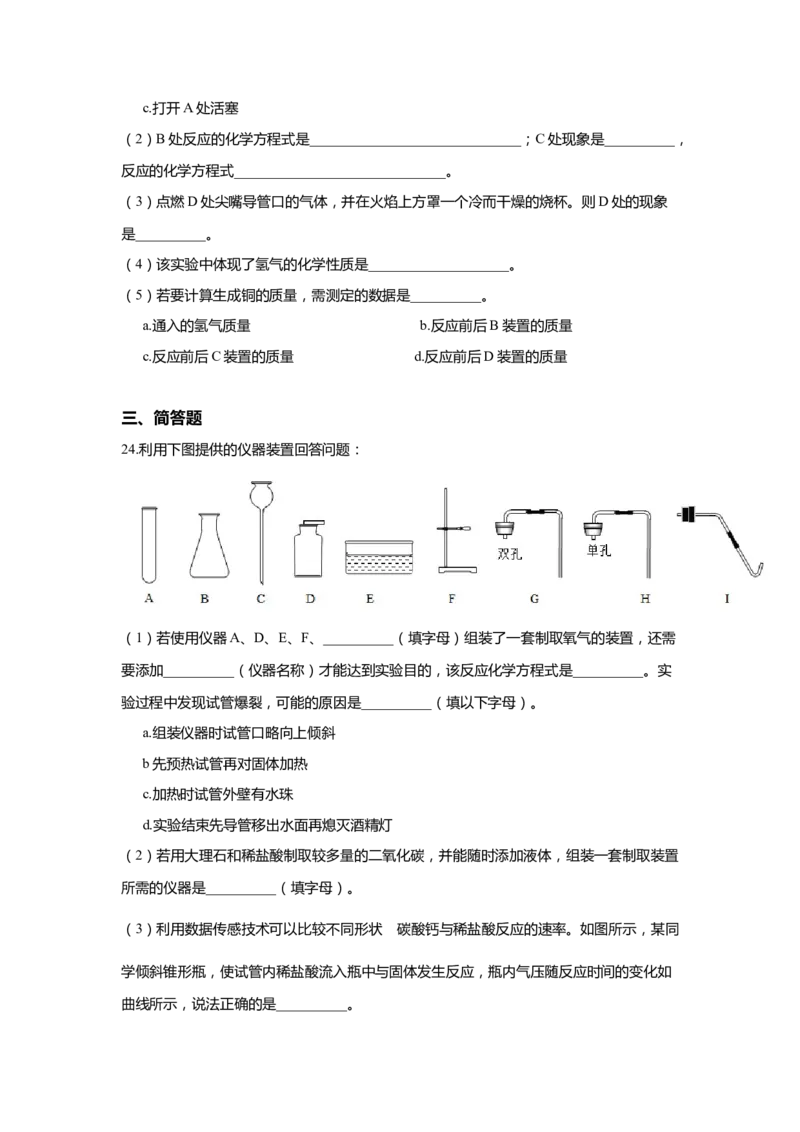
23.为探究电解水产生的氢气化学性质,设计了如下实验:
(1)用氢气还原氧化铜开始时的操作顺序是__________。
a.点燃B处酒精灯加热
b.检验氢气的纯度c.打开A处活塞
(2)B处反应的化学方程式是______________________________;C处现象是__________,
反应的化学方程式______________________________。
(3)点燃D处尖嘴导管口的气体,并在火焰上方罩一个冷而干燥的烧杯。则D处的现象
是__________。
(4)该实验中体现了氢气的化学性质是____________________。
(5)若要计算生成铜的质量,需测定的数据是__________。
a.通入的氢气质量 b.反应前后B装置的质量
c.反应前后C装置的质量 d.反应前后D装置的质量
三、简答题
24.利用下图提供的仪器装置回答问题:
(1)若使用仪器A、D、E、F、__________(填字母)组装了一套制取氧气的装置,还需
要添加__________(仪器名称)才能达到实验目的,该反应化学方程式是__________。实
验过程中发现试管爆裂,可能的原因是__________(填以下字母)。
a.组装仪器时试管口略向上倾斜
.
b先预热试管再对固体加热
c.加热时试管外壁有水珠
d.实验结束先导管移出水面再熄灭酒精灯
(2)若用大理石和稀盐酸制取较多量的二氧化碳,并能随时添加液体,组装一套制取装置
所需的仪器是__________(填字母)。
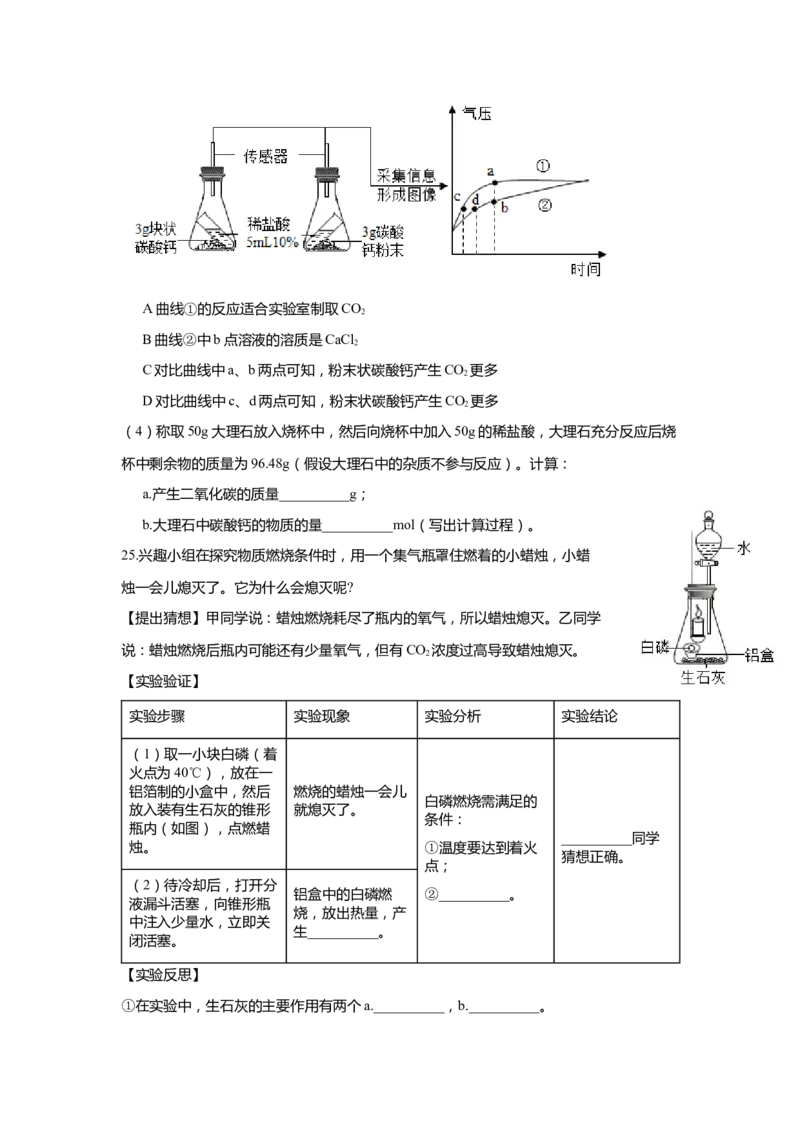
(3)利用数据传感技术可以比较不同形状 的碳酸钙与稀盐酸反应的速率。如图所示,某同
学倾斜锥形瓶,使试管内稀盐酸流入瓶中与固体发生反应,瓶内气压随反应时间的变化如
曲线所示,说法正确的是__________。A曲线①的反应适合实验室制取CO
2
B曲线②中b点溶液的溶质是CaCl
2
C对比曲线中a、b两点可知,粉末状碳酸钙产生CO 更多
2
D对比曲线中c、d两点可知,粉末状碳酸钙产生CO 更多
2
(4)称取50g大理石放入烧杯中,然后向烧杯中加入50g的稀盐酸,大理石充分反应后烧
杯中剩余物的质量为96.48g(假设大理石中的杂质不参与反应)。计算:
a.产生二氧化碳的质量__________g;
b.大理石中碳酸钙的物质的量__________mol(写出计算过程)。
25.兴趣小组在探究物质燃烧条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡
烛一会儿熄灭了。它为什么会熄灭呢?
【提出猜想】甲同学说:蜡烛燃烧耗尽了瓶内的氧气,所以蜡烛熄灭。乙同学
说:蜡烛燃烧后瓶内可能还有少量氧气,但有CO 浓度过高导致蜡烛熄灭。
2
【实验验证】
实验步骤 实验现象 实验分析 实验结论
(1)取一小块白磷(着
火点为40℃),放在一
铝箔制的小盒中,然后 燃烧的蜡烛一会儿
白磷燃烧需满足的
放入装有生石灰的锥形 就熄灭了。
条件:
瓶内(如图),点燃蜡
__________同学
烛。 ①温度要达到着火
猜想正确。
点;
(2)待冷却后,打开分
铝盒中的白磷燃 ②__________。
液漏斗活塞,向锥形瓶
烧,放出热量,产
中注入少量水,立即关
生__________。
闭活塞。
【实验反思】
①在实验中,生石灰的主要作用有两个a.__________,b.__________。②实验结束后,同学们对集气瓶底部的含钙固体又产生了兴趣并设计了如下实验:
实验过程 现象 结论
实验1:取样,__________ 放出大量热 该固体中含有__________
实验2:取样,滴加无色酚酞 __________ 该固体中含有氢氧化钙
实验3:取样,滴加足量
有气泡冒出 该固体中含有碳酸钙
__________
经小组讨论发现,实验__________(填序号)的结论错误,理由是__________。
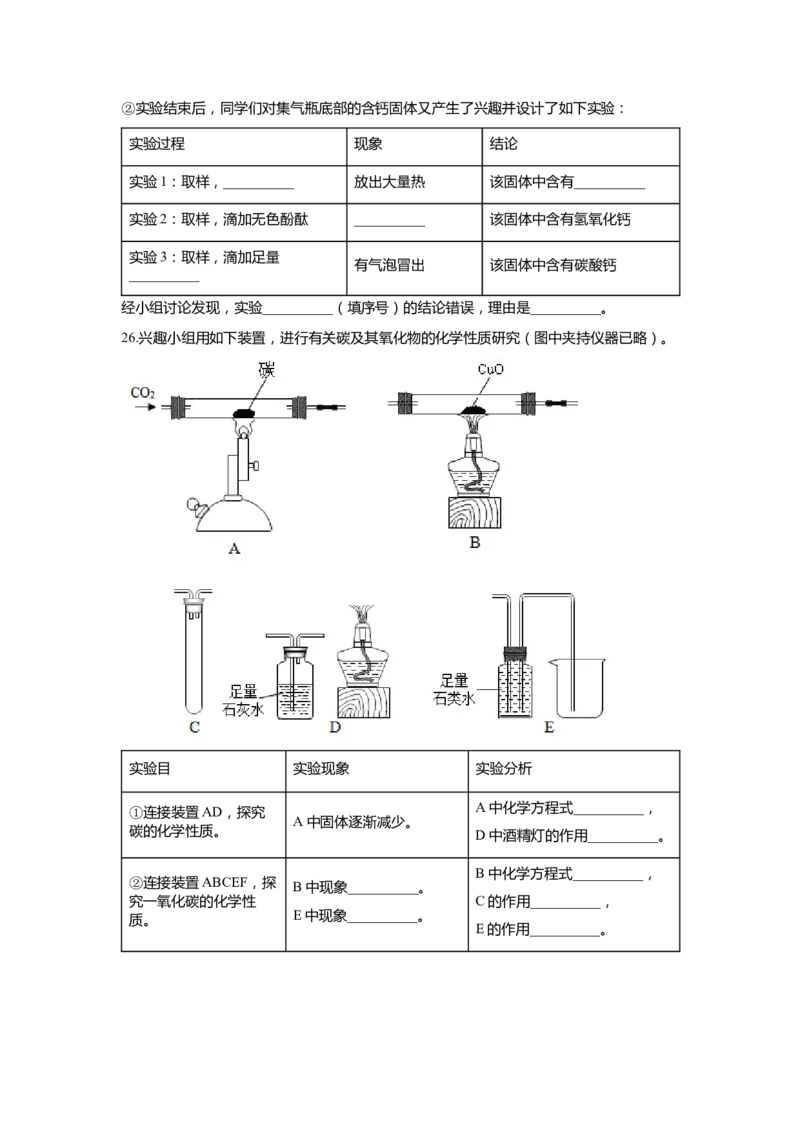
26.兴趣小组用如下装置,进行有关碳及其氧化物的化学性质研究(图中夹持仪器已略)。
实验目 的实验现象 实验分析
①连接装置AD,探究
A中化学方程式__________,
A中固体逐渐减少。
碳的化学性质。 D中酒精灯的作用__________。
B中化学方程式__________,
②连接装置ABCEF,探
B中现象__________。
究一氧化碳的化学性 C的作用__________,
E中现象__________。
质。
E的作用__________。