文档内容
2022-2023第一学期期末测试
高三化学
一、选择题;本题共12小题,每小题3分,共36分.在每小题给出的四个选项中,
只有一项是符合题目要求的.
1.下列说法不正确的是 ( )
A.泡沫灭火器可用于一般的起火,但不适用于活泼金属引起的火灾
B.纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,
其本质是纳米铁粉对重金属离子较强的物理吸附
C.储热材料是一类重要的能量存储物质,单位质量的储热材料在发生熔融或结晶时会
吸收或释放较大的热量
D.Ge (32号元素)的单晶可以作为光电转换材料用于太阳能电池
2.下列说法不正确的是
A.煤的液化和气化均为物理变化
B.工业酒精中往往含有甲醇
C.液化石油气是混合物
D.许多水果和花卉有芳香气味是因为含有酯
3.在重结晶法提纯苯甲酸的实验中不需要用到的仪器有
A. B. C. D.
4.下列各组物质融化或升华时,所克服的粒子间作用力属于同种类型的是
A.NaOH和 熔化 B.镁和硫的熔化
C.氯化钠和蔗糖熔化 D.碘和干冰升华
5.前4周期元素X、Y、Z、W的原子序数依次增大。X和Y的基态原子的2p能级上
各有两个未成对电子,Z与Y同族,W原子核内有29个质子,下列说法正确的是
A.W与Y形成的化合物晶胞如图所示,该化合物的化学式为WY
B.元素第一电离能:I(Z)>I (Y)
1 1
C.气态氢化物的热稳定性:Y>ZD.原子半径:
6.下列实验内容可以达到预期实验目的的是
选
实验内容 实验目的
项
配制1 的 溶
A 将1 mol 溶解在1 L水中
液
B 将 通入酸性 溶液中 证明 具有漂白性
除去 溶液中的少量
C 加入足量铁屑,充分反应后,过滤
将木炭与浓硫酸共热,得到的气体通入澄清石灰
D 检验木炭的氧化产物是
水
A.A B.B C.C D.D
7.有人设计出利用CH 和O 反应,用铂电极在KOH溶液中构成原电池。电池的总反
4 2
应类似于CH 在O 中燃烧,则下列说法中正确的是
4 2
①每消耗1molCH 可以向外电路提供8mol e—
4
②电池放电时,溶液pH不断升高
③负极上是O 获得电子,电极反应式为:O+2H O+4e—=4OH—
2 2 2
④负极上CH 失去电子,电极反应式为:CH+10OH——8e—= +7H O
4 4 2
A.①④ B.①③ C.①② D.③④
8.下列各选项中两种粒子所含电子数不相等的是
A.羟甲基(-CHOH)和甲氧基(CHO-) B.亚硝酸(HNO)和亚硝酸根
2 3 2
(NO )
C.硝基(-NO )和二氧化氮(NO ) D.羟基(-OH)和氢氧根(OH-)
2 2
9.下列指定反应的离子方程式正确的是
A.双氧水使酸性KMnO 溶液褪色:2MnO +5H O=2Mn2++5O ↑+6OH-+2H O
4 2 2 2 2
B.过量的铁粉溶于稀硝酸:Fe+4H++NO =Fe3++NO↑+2HO
2
C.用NaSO 溶液吸收水中的Cl:4Cl+S O +5H O=10H++2SO +8Cl-
2 2 3 2 2 2 2
D.向NaAlO 溶液中通入过量CO:2AlO +CO +3H O=2Al(OH) ↓+CO
2 2 2 2 310.在理论上不能用于设计成原电池的化学反应是
①HSO (aq)+Ba(OH) (aq)=2HO(l)+BaSO(s);△H<0
2 4 2 2 4
②CH CHOH(l)+3O(g) 2CO(g)+3HO(l) ;△H<0
3 2 2 2 2
③2FeCl (aq)+Cu(s)=2FeCl (aq)+CuCl (aq);△H<0
3 2 2
④C(s)+CO(g)=2CO(g) ;△H>0
2
A.④ B.①④ C.①② D.②③
11.下列说法正确的是
A.同位素之间或同素异形体之间的相互转化均属于化学变化
B.油酸和硬脂酸互为同系物
C. 和 互为同分异构体
D.由H、D、T、 、 这几种核素组成的水分子共有12种
12.分类法在化学学科发展中起到了非常重要的作用,下列分类依据合理的是
①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据水溶液溶液能否导电将物质分为电解质和非电解质
A.②④⑤ B.②③④ C.①③⑤ D.①②④
二、多选题;本题共3小题,每小题4分,共12分.
13.根据实验操作和现象所得出的结论正确的是
选
实验操作和现象 结论
项
向Fe(NO ) 溶液中滴入HI和淀粉混合溶液,溶液变
A 3 2 氧化性:Fe2+>I
蓝 2
向3 mL KI溶液中滴加几滴氯水,振荡,再滴加1mL
B Cl 的氧化性比I 的强
淀粉溶液,溶液显蓝色 2 2
向Ag CO 白色悬浊液中滴加少量NaS溶液,出现黑
C 2 3 2 K (Ag S)<K (Ag CO)
色沉淀 sp 2 sp 2 3
苯和液溴在FeBr 的催化下发生反应,将得到的气体
D 3 苯和液溴发生取代反应
直接通入AgNO 溶液中,产生淡黄色沉淀
3A.A B.B C.C D.D
14.三甲胺N(CH ) 是重要的化工原料。我国科学家实现了在铜催化剂条件下将N,N-
3 3
二甲基甲酰胺[(CH )NCHO,简称DMF]转化为三甲胺[N(CH )]。计算机模拟单个
3 2 3 3
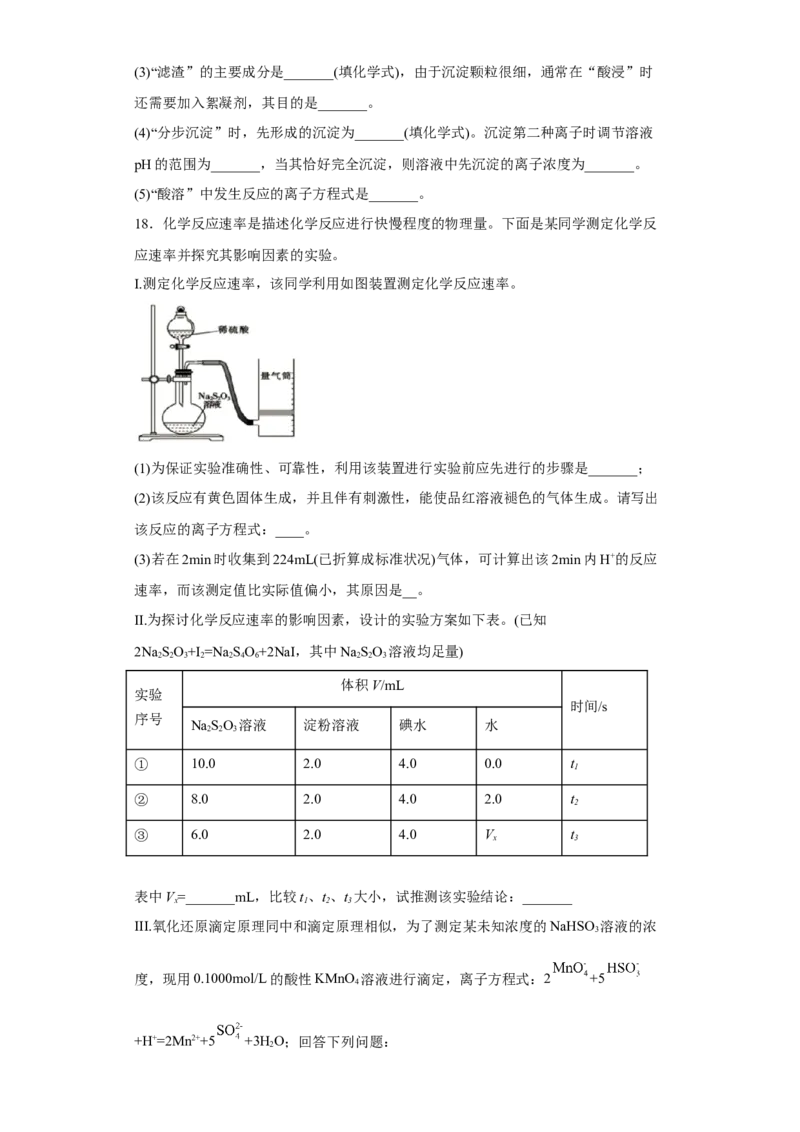
DMF分子在铜催化剂表面的反应历程如图所示(*表示物质吸附在铜催化剂上),下列说
法正确的是
A.该历程中决速步骤为
B.该历程中的最大能垒(活化能)为1.19eV
C.升高温度可以加快反应速率,并提高DMF的平衡转化率
D.若1molDMF完全转化为三甲胺,则会释放出1.02eV·N 的能量
A
15.下列溶液中有关物质的量浓度关系正确的是
A.0.1 mol·L-1NaHCO 溶液:c(Na+)>c(HCO-)>c(CO 2-)>c(H CO)
3 3 3 2 3
B.0.1 mol·L-1NaHCO 溶液与0.1 mol·L-1NaOH溶液等体积混合:c(Na+)=2c(CO2-)
3 3
+c(HCO -)+2c(HCO)
3 2 3
C.0.1 mol·L-1NaHCO 溶液与0.2 mol·L-1NaOH溶液等体积混合:c(Na+)>c(OH
3
-)>0.05 mol·L-1>c(CO 2-)>c(HCO-)
3 3
D.0.2 mol·L-1NaHCO 溶液与0.1 mol·L-1NaOH溶液等体积混合:c(CO2-)+2c(OH-)
3 3
=c(HCO -)+3c(HCO)+2c(H+)
3 2 3
三、填空题:52分
16.已知A、B、R、D都是周期表中前四周期的元素,它们的原子系数依次增大。其
中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L
层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式__________。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上
生产高纯度R的单质过程如下:写出过程③的反应方程式___________,已知RHCl 的沸点是31.5oC,则该物质的晶体
3
类型是__________,中心原子的轨道杂化类型为__________,该物质的空间构型是
______。
(3)A的第一电离能比B的第一电离能大的原因是_________,A、B两元素分别与R形
成的共价键中,极性较强的是________。A、B两元素间能形成多种二元化合物,其中
与A-互为等电子体的物质的化学式为_______。
3
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为______,一个D的晶胞质
量为____,已知D原子半径为r pm,则该晶胞的空间利用率为_____________ (写出计
算过程)。
17.铊(T1)在工业中的用途非常广泛。从某铅锌厂的电尘(主要成分为PbO、ZnO还含
有少量Fe O、T1O)中回收铊的工艺流程如图所示:
2 3 2
已知:①Zn(OH) 为两性氢氧化物,溶液pH=10.0时开始溶解。
2
②常温下,相关离子开始沉淀和沉淀完全时的pH如下表所示:
离子 Fe3+ Zn2+
开始沉淀的pH 2.7 6.4
沉淀完全的pH 3.7 8.0
回答下列问题:
(1)为提高“酸浸”效率,可采取的措施有_______(写出一种)。
(2)为提高电尘的转化率,利用洗涤后的滤渣检验“酸浸”是否充分,其实验操作
__________。(3)“滤渣”的主要成分是_______(填化学式),由于沉淀颗粒很细,通常在“酸浸”时
还需要加入絮凝剂,其目的是_______。
(4)“分步沉淀”时,先形成的沉淀为_______(填化学式)。沉淀第二种离子时调节溶液
pH的范围为_______,当其恰好完全沉淀,则溶液中先沉淀的离子浓度为_______。
(5)“酸溶”中发生反应的离子方程式是_______。
18.化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反
应速率并探究其影响因素的实验。
I.测定化学反应速率,该同学利用如图装置测定化学反应速率。
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是_______;
(2)该反应有黄色固体生成,并且伴有刺激性,能使品红溶液褪色的气体生成。请写出
该反应的离子方程式:____。
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应
速率,而该测定值比实际值偏小,其原因是__。
II.为探讨化学反应速率的影响因素,设计的实验方案如下表。(已知
2NaSO+I =Na SO+2NaI,其中NaSO 溶液均足量)
2 2 3 2 2 4 6 2 2 3
体积V/mL
实验
时间/s
序号
NaSO 溶液 淀粉溶液 碘水 水
2 2 3
① 10.0 2.0 4.0 0.0 t
1
② 8.0 2.0 4.0 2.0 t
2
③ 6.0 2.0 4.0 V t
x 3
表中V=_______mL,比较t、t、t 大小,试推测该实验结论:_______
x 1 2 3
III.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO 溶液的浓
3
度,现用0.1000mol/L的酸性KMnO 溶液进行滴定,离子方程式:2 +5
4
+H+=2Mn2++5 +3H O;回答下列问题:
2(1)用KMnO 进行滴定时,判断滴定终点的现象是_______。
4
(2)下列操作会导致测定结果偏低的是_______。
A.酸式滴定管水洗后未用待测液润洗
B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定管尖嘴部分有气泡,滴定后消失
D.观察读数时,滴定前仰视,滴定后俯视
(3)根据下表中测定的实验数据,计算NaHSO 溶液的物质的量浓度(写出计算过程,结
3
果保留4位有效数字)_________。
实验编号 待测NaHSO 溶液的体积/mL KMnO 溶液的体积/mL
3 4
1 20.00 15.98
2 20.00 17.00
3 20.00 16.02
19.乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品工业和食品工业,下图是乙
酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。已知A是果实的催熟
剂。
(1)A分子的电子式为________;C的分子式为________;D中官能团结构简式为
________。
(2)A→B反应类型为_____________,反应F→G反应类型___________。
(3)G的同分异构体有多种,遇FeCl 溶液显紫色的共有_____种;
3
苯环上一氯代物有2种的物质的结构简式______________。
(4)写出下列反应的化学方程式:
B→C:_____________________;
F→G:______________________;
G→H:___________________;
C的银镜反应方程式为:____________________。
20.三氯化硅 是制备硅烷、多晶硅的重要原料。已知 在催化剂作用下发生反应: 。一定条件下,向容积为1L的恒容
密闭容器中充入 ,分别在温度为 、 条件下反应,测得反应体系
中 的物质的量分数随时间变化的关系如图所示。
(1)在 温度下, 的平衡转化率 _______%。若想进一步提高
的转化率,除改变温度外还可以采取的措施是_______。
(2)在 温度下,经 后反应达到平衡。
① 内, 的反应速率 _______ 。
②在 温度下,该反应的平衡常数 _______(已知,压强平衡常数 用各气体组
分的分压代替物质的量浓度计算)。
(3)下列不能判断该反应达到平衡状态的是_______(填标号)。
a.
b.混合气体的密度不再发生变化
c. 与 的浓度之比不再改变
d.混合气体的平均摩尔质量不再发生变化
(4)已知:反应速率 , 、 分别表
示正、逆反应速率常数, 为组分B的物质的量分数。①a、b点的正反应速率之比 _______(填“>”、“<”或“=”)1。
②b点的 _______(保留三位有效数字)。参考答案
1.B 2.A 3.C 4.D 5.C 6.C 7.A 8.D 9.C 10.B 11.D 12.D 13.BC
14.BD 15.CD
16. [Ar]3d64s2 SiHCl + H Si + 3HCl 分子晶体 sp3
3 2
四面体形 N原子的2p能级处于较稳定的半充满状态 Si-O键
NO 8 晶胞中铁原子占据的体积为两个铁原子的体积,铁原子的半径为r
2
pm,如图所示,晶胞的棱长为= ,晶胞的体积=( )3,空间利用率= =
100%=68%
×
17.(1)适当增大硫酸浓度
(2)取滤渣于干燥洁净的试管中,加入硫酸溶液,再滴加KSCN溶液,若溶液不变红,则已
充分酸浸
(3) PbSO 吸附 PbSO 沉淀,使沉淀颗粒变大,便于过滤除杂
4 4
(4) Fe(OH) 8.0≤pH<10.0 10-17.9 mol/L
3
(5)2H++Tl S= H S↑+2TI+
2 2
18. 检查装置的气密性 SO 会
2
部分溶于水,导致所测得的SO 的体积偏小 4 增大反应物浓度,可加快反应速
2
率 当加入最后一滴酸性KMnO 溶液时,溶液由无色变为浅红色,且半分钟内不
4
褪色 D 0.219. C HO -COOH 加成反应 取代反应
2 4
(水解反应) 有3种 2C HOH + O
2 5 2
2CHCHO + 2H O; + NaOH
3 2
+NaCl CHCOOH +
3
+ H O C的银镜反应方程式为:CHCHO+2Ag(NH )OH
2 3 3 2
CHCOONH+H O+2Ag↓+ 3NH ↑
3 4 2 3
20.(1) 20 及时移去产物
(2)
(3)bd
(4) > 2.01