文档内容
失 2e-
微专题 08 新情景中氧化还原反应方程式的
配平与书写
氧化还原反应方程式的书写一般在填空题中出现较多,常结合化工生产流程及实验
探究中考查,越来越注重结合新信息书写陌生的化学方程式(离子方程式)。要求考生
要有效地接受、吸收、整合题目的信息,推断物质,利用守恒规律加以书写,充分体现
出学科核心素养:电子得失——变化观念与守恒思想;方程式配平——模型认知;而氧
化性(还原性)体现宏观辨识与微观探析。具体解题可用以下方法:
“四步法”突破新情景下氧化还原方程式的书写
第一步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物。
第二步:按“氧化剂+还原剂——氧化产物+还原产物”写出方程式,根据得失电子守恒
对方程式进行配平。
第三步:根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充H+、OH-或H2O等。
第四步:根据质量守恒配平反应方程式。
【典例精析】
KMnO4能与热的硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程
式为
分析第一步:依题意,锰元素的化合价降低,故 KMnO4是氧化剂,Mn2+是还原产物;
碳元素的化合价升高,故Na2C2O4(碳元素化合价为+3价)是还原剂,CO2是氧化产物。
第二步:按“氧化剂+还原剂——氧化产物+还原产物”把离子方程式初步写成:
,由MnO - 2+,锰元素降了5价,由C O2-
4 Mn 2 4
CO ,碳元素升了1价,1molC O2-共失去2mole-,故在C O2-前配5,在氧化产物
2 2 4 2 4
CO 前 配 10 , 在 MnO - 前 配 2 , 在 还 原 产 物 Mn2 + 前 配 2 , 即
2 4
。
第三步:反应在硫酸中进行,故在左边补充H+,右边补充HO,2MnO -+5C O2-+H+
2 4 2 4
2Mn2++10CO↑+HO
2 2第四步:依据电荷守恒及H、O原子守恒配平如下:
2MnO -+5C O2-+16H+ △ 2Mn2++10CO↑+8HO
4 2 4 2 2
一、工艺流程中的氧化还原方程式的书写
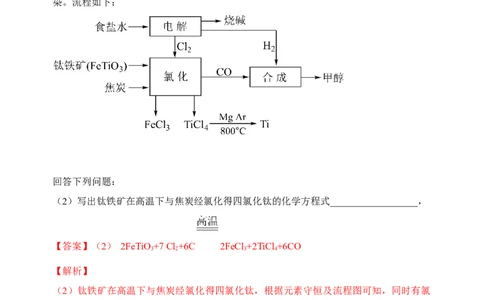
1.某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污
染。流程如下:
回答下列问题:
(2)写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式__________________,
【答案】(2) 2FeTiO+7 Cl +6C 2FeCl +2TiCl +6CO
3 2 3 4
【解析】
(2)钛铁矿在高温下与焦炭经氯化得四氯化钛,根据元素守恒及流程图可知,同时有氯
化铁、CO生成,化学方程式为2FeTiO+7Cl+6C 2FeCl +2TiCl +6CO;
3 2 3 4
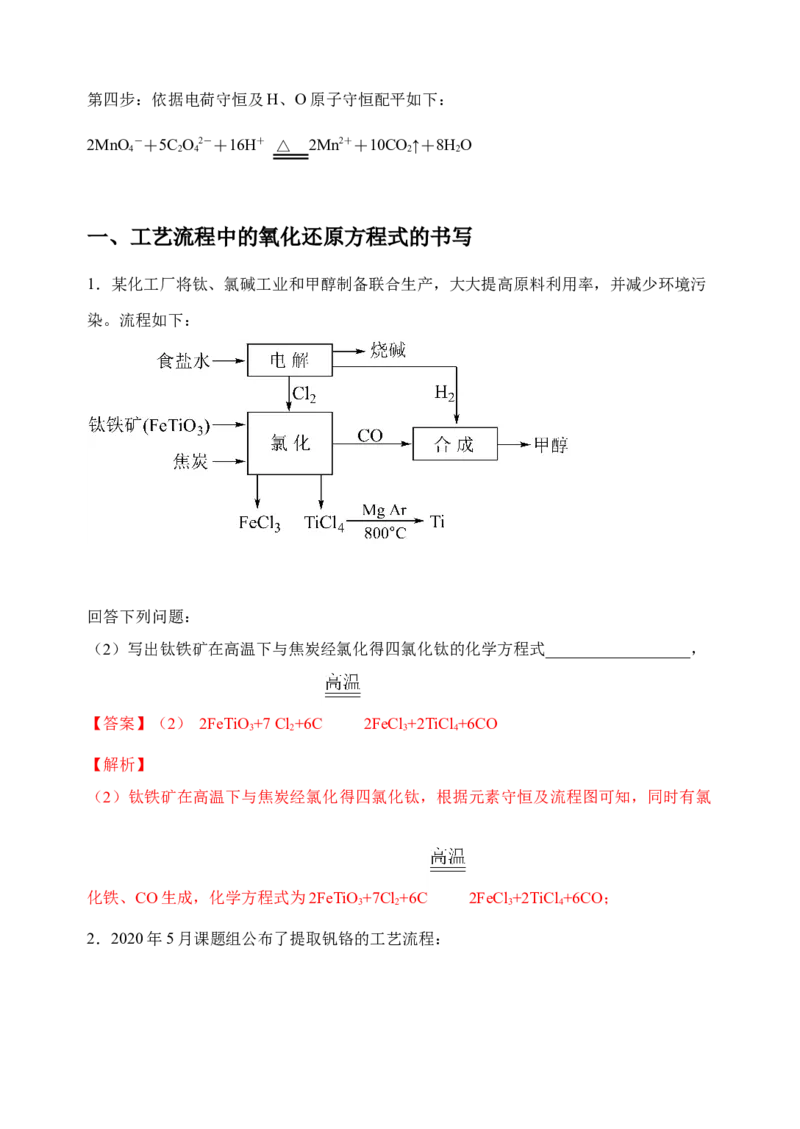
2.2020年5月课题组公布了提取钒铬的工艺流程:已知:
①钒铬渣中含有 ,及 等;
② 时, 的溶度积常数为 ; 。
回答下列问题:
(4)写出“煅烧”时反应的化学方程式______(已知“沉钒”时析出正五价钒的含氧酸铵盐)。
(5)“还原”溶液中的 时发生反应的离子方程式为______,
【答案】
(4) (5)
【解析】
(4)由分析可知,正五价钒的含氧酸铵盐为 ,“煅烧”时反应的化学方程式为
,故答案为:
;
(5) 由 分 析 可 知 , “ 还 原 ” 溶 液 中 的 时 发 生 反 应 的 离 子 方 程 式 为;
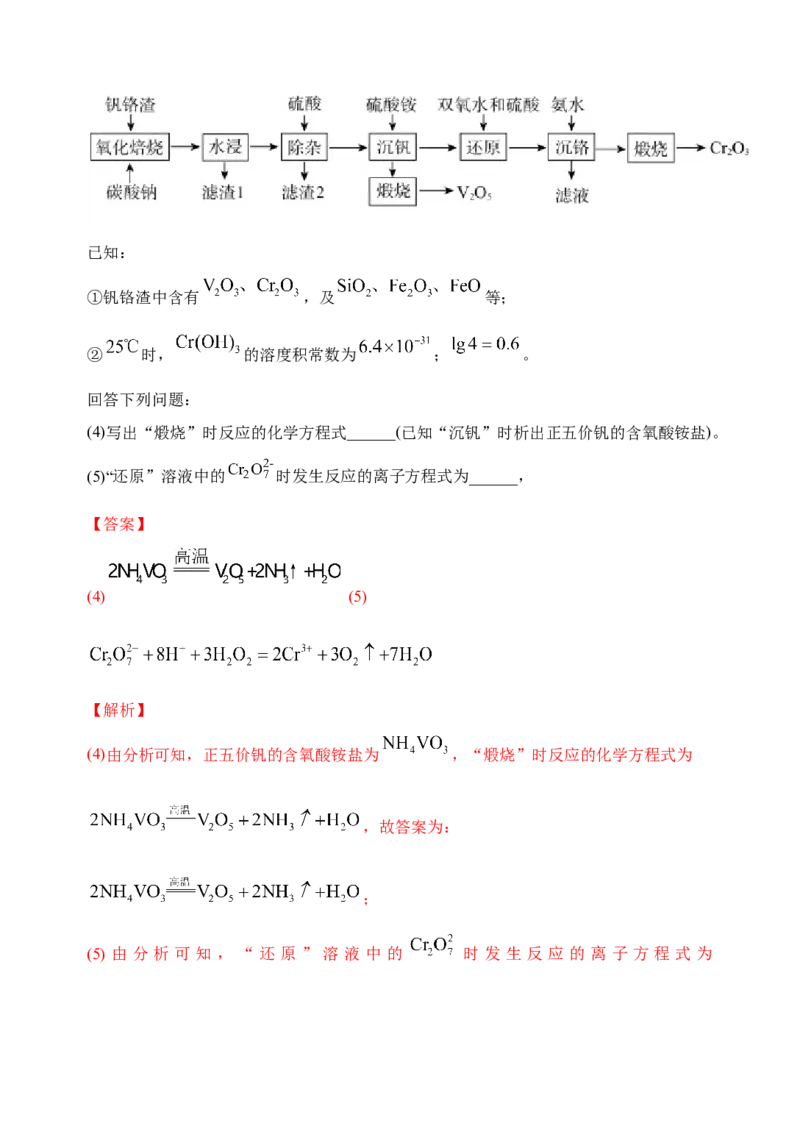
3.Cr(Ⅵ)对A体具有致癌、致突变作用。铁氧体法(铁氧体是组成类似于Fe O 的复合氧
3 4
化物,其中部分Fe(Ⅲ)可被Cr(Ⅲ)等所代换)是目前处理Cr(Ⅵ)废水的常见方法之一,其工
艺流程如下:
(2)铁氧体法处理含Cr O 废水的工艺流程中:
2
①“反应槽”中发生反应的离子方程式为______。
【答案】Cr O +6Fe2++14H+=2Cr3++6Fe3++7H O
2 2
【解析】
(2)①反应槽中,Cr O 在酸性条件下氧化Fe2+,生成Fe3+和Cr3+,根据Fe和Cr得失电子
2
守恒,用H+平衡电荷,则离子方程式为Cr O +6Fe2++14H+=2Cr3++6Fe3++7H O。
2 2
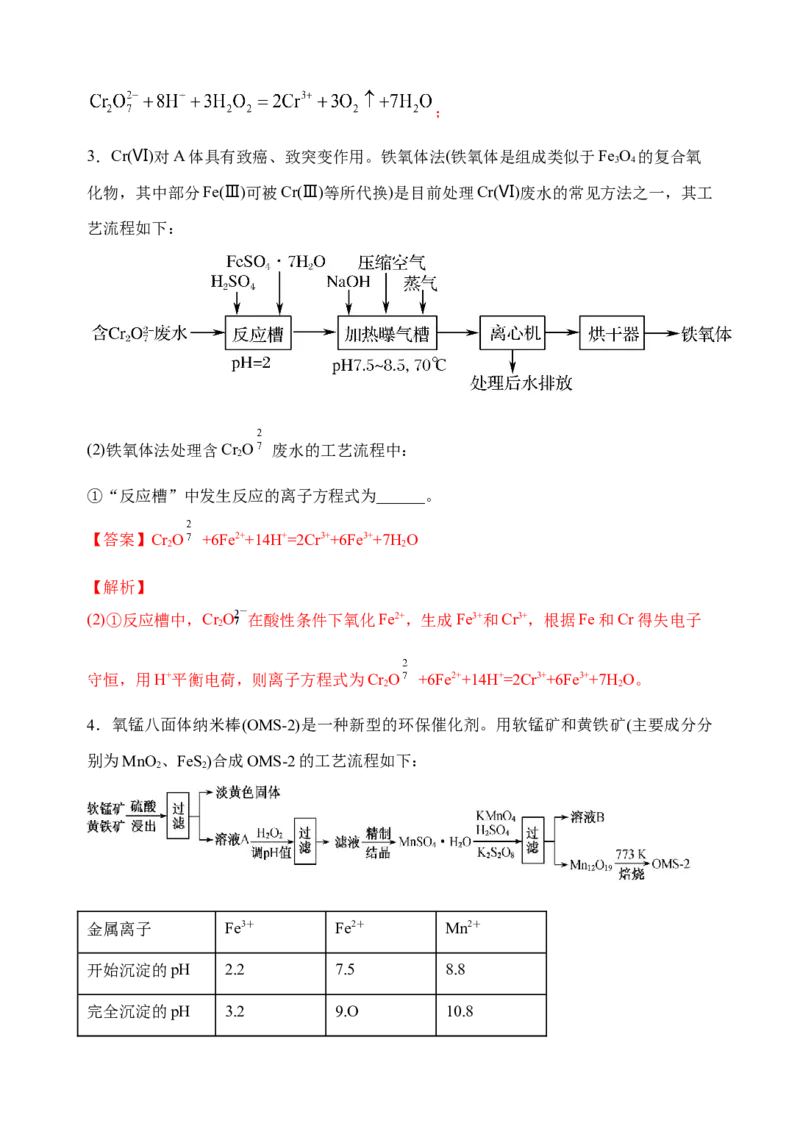
4.氧锰八面体纳米棒(OMS-2)是一种新型的环保催化剂。用软锰矿和黄铁矿(主要成分分
别为MnO 、FeS)合成OMS-2的工艺流程如下:
2 2
金属离子 Fe3+ Fe2+ Mn2+
开始沉淀的pH 2.2 7.5 8.8
完全沉淀的pH 3.2 9.O 10.8(3)生产过程中的原料KMnO 、KSO、MnSO ·H O按物质的量比1︰1︰5反应,产物中
4 2 2 8 4 2
硫元素全部以 的形式存在,该反应的离子方程式为___________。
【答案】
【解析】
(3)生产过程中的原料KMnO 、KSO、MnSO ▪H O按物质的量比1:1:5反应,产物中硫
4 2 2 8 4 2
元素全部以 的形式存在,Mn全部转化为Mn O ,根据质量守恒和电荷守恒,可写
12 19
出反应的化学方程式为2 +2 +10Mn2++11H O=Mn O ↓+4 +22H+。
2 12 19
5.草酸钴是一种重要的化工材料,广泛应用于有机合成。一种以铜钴矿粉(主要成分为
,还含一定量 )为原料,生产草酸钴晶体( )的工艺流程
如下:
已知:①“浸出”液含有的离子主要有 、 、 、 、 ;
②草酸钴晶体难溶于水。
回答下列问题:
(3)“氧化”过程中发生的主要反应的离子方程式为____________________。
【答案】
【解析】
(3)由流程梳理可知,“氧化”过程中,过氧化氢与亚铁离子发生氧化还原反应生成2Fe2 H O 2H O 2FeOOH4H
2 2 2
FeOOH
,反应的离子方程式为 ;“
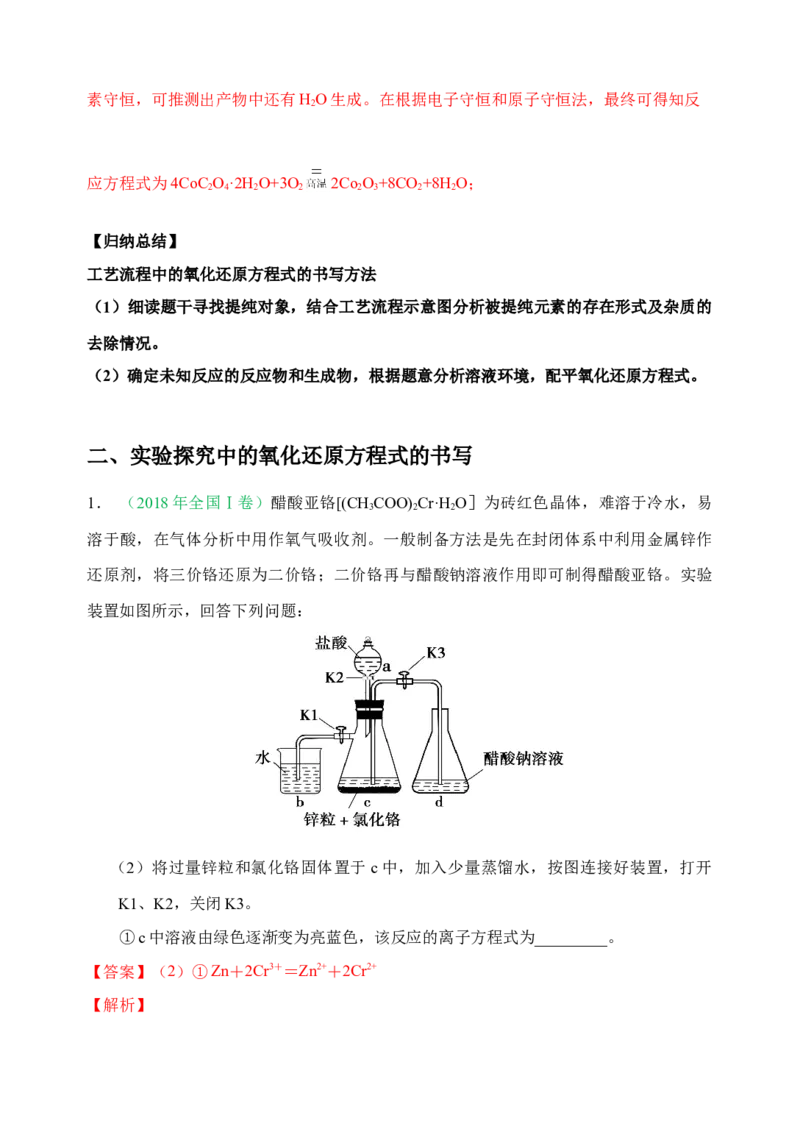
6.三氧化二镍是一种重要的电子元件材料、蓄电池材料。工业上利用含镍废料(以镍、铁、
钙、镁合金为主)制取草酸镍(NiC O·2H O),再高温煅烧草酸镍制取三氧化二镍。已知草
2 4 2
酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
(5)NiC O·2H O高温煅烧制取三氧化二镍时会产生CO、CO、水蒸气等混合气体,发生
2 4 2 2
反应的化学方程式为___________。
【答案】2NiC O·2H O Ni O+3CO↑+CO↑+4HO
2 4 2 2 3 2 2
【解析】
(5)NiC O·2H O高温煅烧生成三氧化二镍、CO、CO、水蒸气,根据得失电子守恒,发
2 4 2 2
生反应的化学方程式为2NiC O·2H O Ni O+3CO↑+CO↑+4HO;
2 4 2 2 3 2 2
7.三氧化二钴主要用作颜料、釉料及磁性材料,利用铜钴矿石制备 的工艺流程如
图所示。已知:铜钴矿石主要含有 、 、 ,其中还含有一定量的
、 和 等。请回答下列问题:
(4)向“沉铜”后的滤液中加入 溶液,写出滤液中的金属离子与 反应的
离子方程式_______。
(6) 在空气中高温煅烧得到 的化学方程式是_______。
【答案】(4)
(6)
【解析】
(4) “沉铜”后的滤液中含有Fe2+,向其中加入NaClO 溶液,NaClO 会将Fe2+氧化为
3 3
Fe3+,则根据电子守恒、电荷守恒及原子守恒,可知滤液中的Fe2+与NaClO 反应的离子方
3
程式为:ClO -+6Fe2++6H+=Cl-+6Fe3++3H O;
3 2
(6) 由题中可知CoC O•2H O在空气中高温煅烧得到Co O,CoC O 中Co的化合价为+2
2 4 2 2 3 2 4
价,生成Co O(Co的化合价为+3价),化合价升高,说明空气中的O 作为氧化剂参与了
2 3 2
反应,而C O2-具有一定还原性也被O 氧化成CO,故产物分别为Co O 和CO,根据元
2 4 2 2 2 3 2素守恒,可推测出产物中还有HO生成。在根据电子守恒和原子守恒法,最终可得知反
2
应方程式为4CoC O·2H O+3O 2Co O+8CO +8H O;
2 4 2 2 2 3 2 2
【归纳总结】
工艺流程中的氧化还原方程式的书写方法
(1)细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的
去除情况。
(2)确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
二、实验探究中的氧化还原方程式的书写
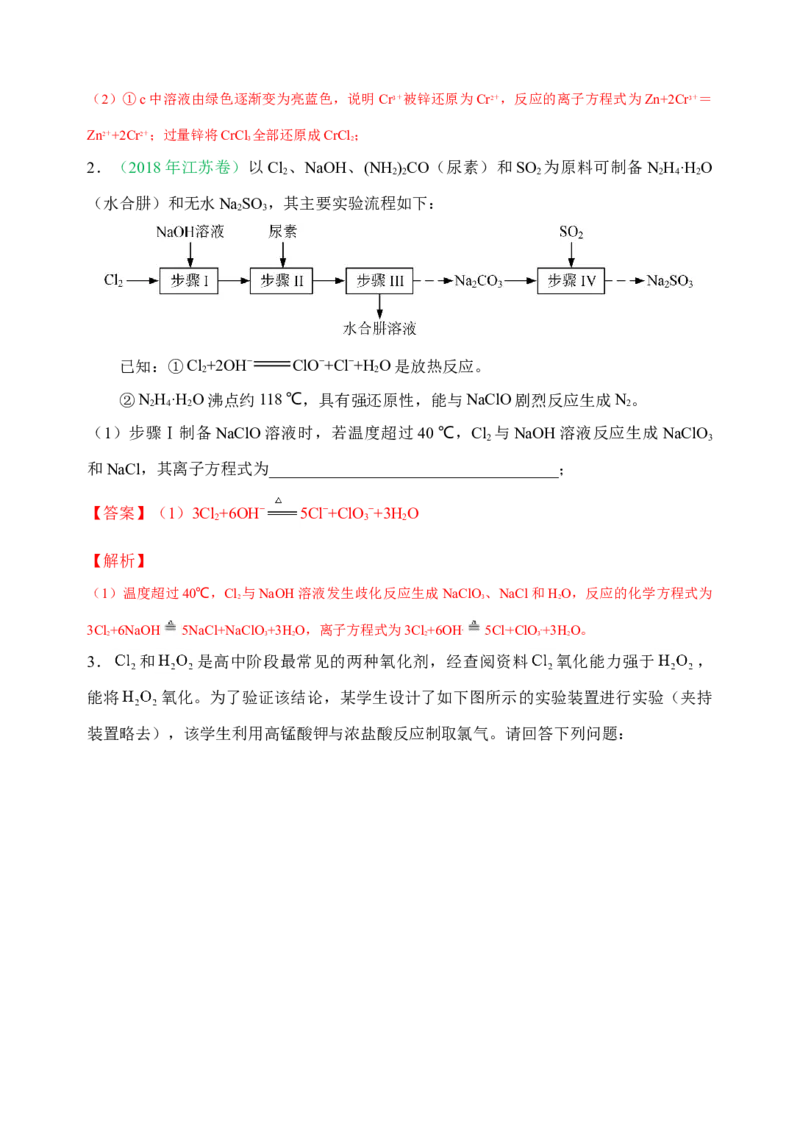
1. (2018年全国Ⅰ卷)醋酸亚铬[(CH COO) Cr·H O]为砖红色晶体,难溶于冷水,易
3 2 2
溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作
还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验
装置如图所示,回答下列问题:
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开
K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________。
【答案】(2)①Zn+2Cr3+=Zn2++2Cr2+
【解析】(2)①c中溶液由绿色逐渐变为亮蓝色,说明Cr3+被锌还原为Cr2+,反应的离子方程式为Zn+2Cr3+=
Zn2++2Cr2+;过量锌将CrCl全部还原成CrCl;
3 2
2.(2018年江苏卷)以Cl 、NaOH、(NH )CO(尿素)和SO 为原料可制备NH·H O
2 2 2 2 2 4 2
(水合肼)和无水NaSO ,其主要实验流程如下:
2 3
已知:①Cl+2OH− ClO−+Cl−+H O是放热反应。
2 2
②NH·H O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N。
2 4 2 2
(1)步骤Ⅰ制备NaClO溶液时,若温度超过40 ℃,Cl 与NaOH溶液反应生成NaClO
2 3
和NaCl,其离子方程式为____________________________________;
【答案】(1)3Cl+6OH− 5Cl−+ClO −+3H O
2 3 2
【解析】
(1)温度超过40℃,Cl 与NaOH溶液发生歧化反应生成NaClO、NaCl和HO,反应的化学方程式为
2 3 2
3Cl+6NaOH 5NaCl+NaClO+3HO,离子方程式为3Cl+6OH- 5Cl-+ClO-+3HO。
2 3 2 2 3 2
3. 和 是高中阶段最常见的两种氧化剂,经查阅资料 氧化能力强于 ,
能将 氧化。为了验证该结论,某学生设计了如下图所示的实验装置进行实验(夹持
装置略去),该学生利用高锰酸钾与浓盐酸反应制取氯气。请回答下列问题:(1)圆底烧瓶A中发生反应的化学方程式是_______________。
【答案】(1)
【解析】
(1)A是制取氯气的装置,其中高锰酸钾被还原为 。
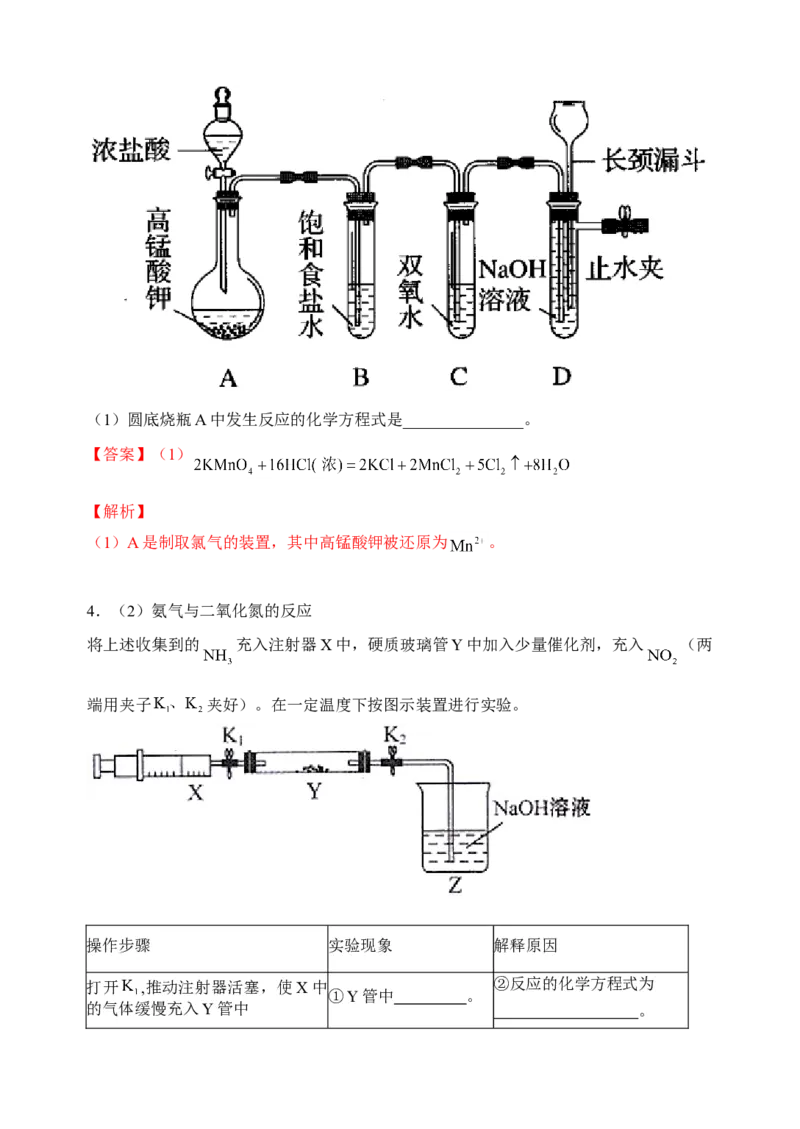
4.(2)氨气与二氧化氮的反应
将上述收集到的 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入 (两
端用夹子 夹好)。在一定温度下按图示装置进行实验。
操作步骤 实验现象 解释原因
打开 ,推动注射器活塞,使X中 ②反应的化学方程式为
①Y管中 。
的气体缓慢充入Y管中 。将 注 射 器 活 塞 退 回 原处并同
Y管中有少量水珠 生成的气态水凝 聚
定,待装置恢复到室温
打开 ③ 。 ④ 。
【答案】(2)①红棕色气体慢慢变浅
②
③Z中NaOH溶液产生倒吸现象
④反应后气体分子数减少,Y管中压强小于外界大气压
【解析】
(2)由题干内容“工业上在一定温度和催化剂条件下用 将 还原生成 ,结合
实验条件可知反应为 , 为红棕色气体,发生反应后变
成无色气体,因此现象为红棕色气体逐渐变浅。反应后气体分子数减少,Y管中的压强小
于外界大气压,因此产生倒吸现象。
5.(2019年北京卷)化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不
含干扰测定的物质)。
Ⅰ.用已准确称量的KBrO 固体配制一定体积的a mol·L−1 KBrO 标准溶液;
3 3
Ⅱ.取v mL上述溶液,加入过量KBr,加HSO 酸化,溶液颜色呈棕黄色;
1 2 4
Ⅲ.向Ⅱ所得溶液中加入v mL废水;
2
Ⅳ.向Ⅲ中加入过量KI;
Ⅴ.用b mol·L−1 NaSO标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定
2 2 3
至终点,共消耗NaSO溶液v mL。
2 2 3 3
已知:I+2Na SO=2NaI+ Na SO
2 2 2 3 2 4 6
NaSO和NaSO溶液颜色均为无色
2 2 3 2 4 6
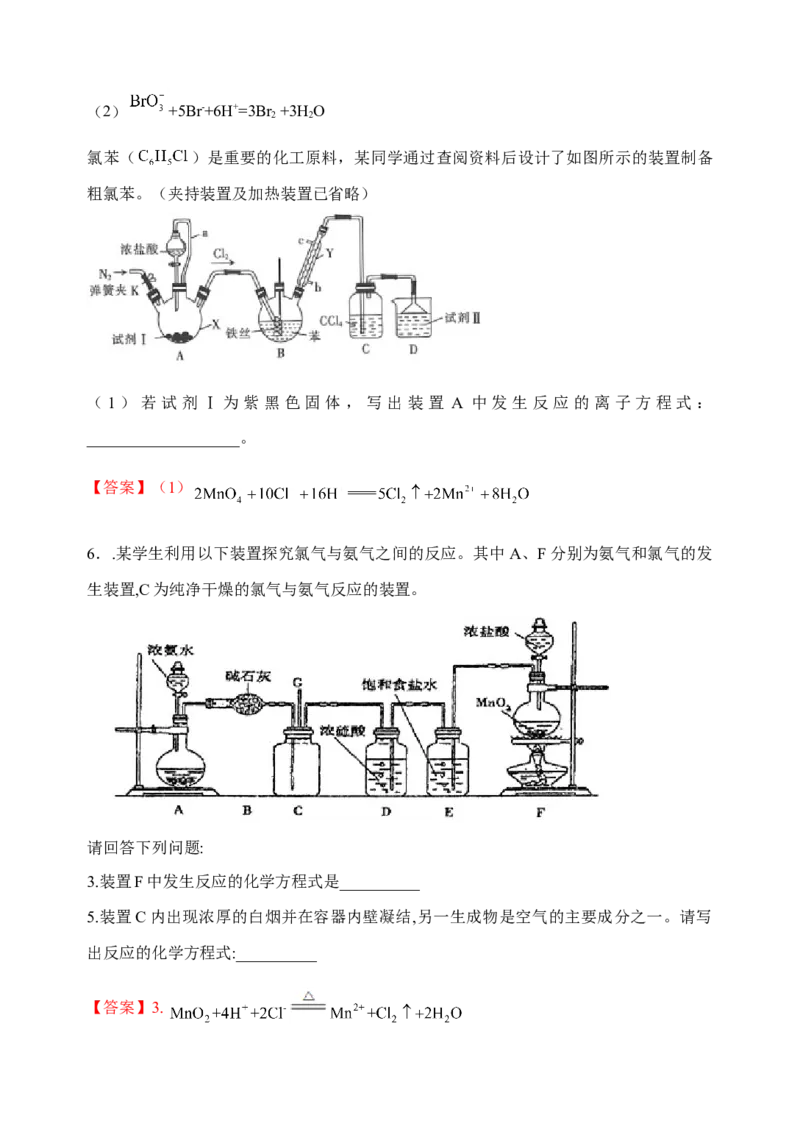
(2)Ⅱ中发生反应的离子方程式是_______________________________。(2) +5Br-+6H+=3Br +3H O
2 2
氯苯( )是重要的化工原料,某同学通过查阅资料后设计了如图所示的装置制备
粗氯苯。(夹持装置及加热装置已省略)
(1)若试剂Ⅰ为紫黑色固体,写出装置 A 中发生反应的离子方程式:
___________________。
【答案】(1)
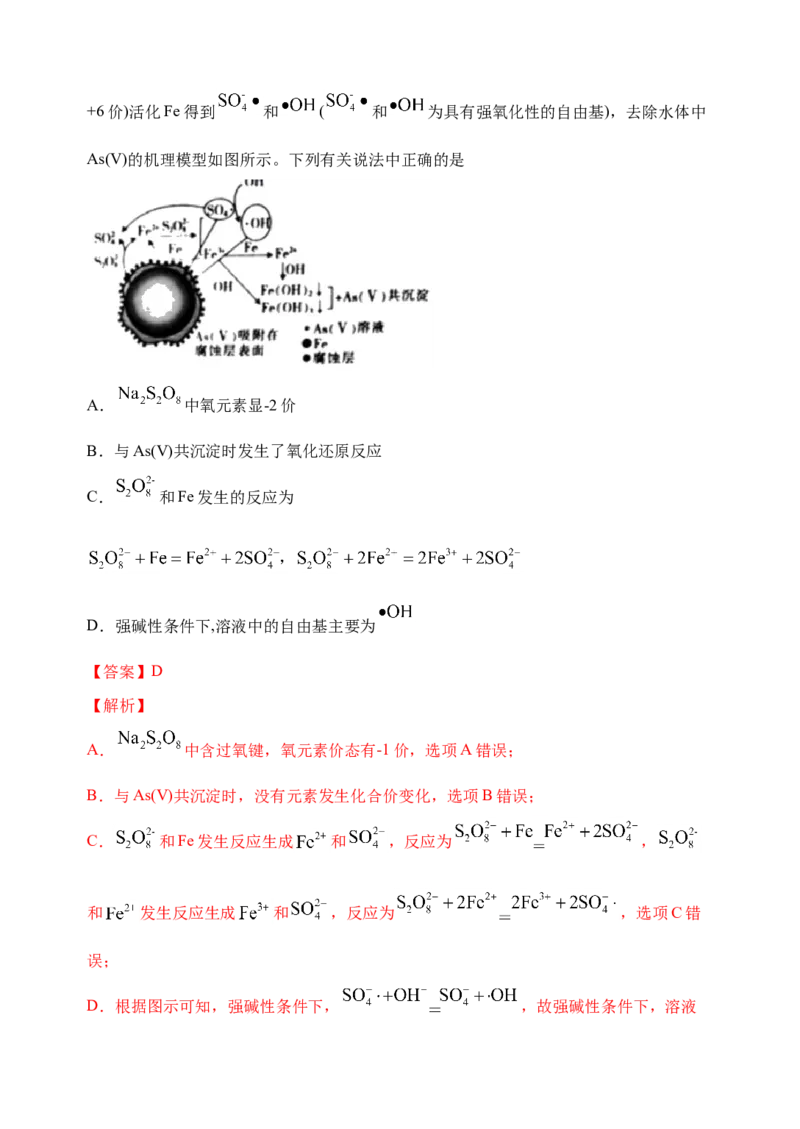
6..某学生利用以下装置探究氯气与氨气之间的反应。其中 A、F分别为氨气和氯气的发
生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
3.装置F中发生反应的化学方程式是__________
5.装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写
出反应的化学方程式:__________
【答案】3.5.3Cl+8NH=N +6NHCl
2 3 2 4
【解析】
3.F装置中发生
5.C中的反应物是NH 与Cl,产生的白烟是固体NH Cl,另一生成物是空气的主要成分N,反
3 2 4 2
应方程式为3Cl+8NH=N +6NHCl
2 3 2 4
【归纳总结】
(1)细读题干寻找实验目的,通读题目中从实验步骤中了解操作步骤,结合装置分析实
验过程,与实验目的相对应。
(2)根据题意确定反应物和生成物,结合溶液环境配平方程式,注意质量守恒、电子守
恒、电荷守恒。
【实战演练】
1.( )是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓
或浓 反应生成 以回收 。在回收过程中涉及如下化学反应:
① ;
② 。
下列有关叙述不正确的是
A.反应①中 是还原产物, 是氧化产物
B. 、 (浓)、 的氧化性由强到弱的顺序是 (浓)
C.反应②中浓 既体现其酸性又体现强氧化性
D.反应①中每有 生成,转移电子数目为【答案】C
【解析】
A.反应①中氧化剂是 ,还原剂是 ,则 是还原产物, 是氧化产物,A正确。
B.同一个氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,反应①中氧化剂是
,氧化产物是 ,反应②中氧化剂是浓硫酸,氧化产物是 ,所以氧化性:
(浓) ,B正确。
C.反应②中浓 只体现其强氧化性,而不体现酸性,C错误。
D.反应①中每生成 转移 电子,则每有 生成,转移电子 ,
即转移电子数目为 ,D正确。
故选:C。
2.用Cu S、FeS处理酸性废水中的Cr O ,发生的反应如下:
2 2
反应①:Cu S+Cr O +H+→Cu2++SO +Cr3++H O(未配平)
2 2 2
反应②:FeS+Cr O +H+→Fe3++SO +Cr3++H O(未配平)
2 2
下列判断错误的是
A.反应①中还原剂与氧化剂的物质的量之比为3:5
B.用相同物质的量的Cu S和FeS处理Cr O 时,Cu S消耗更多Cr O
2 2 2 2
C.处理等物质的量的Cr O 时,反应①和②中消耗H+的物质的量相等
2
D.用FeS处理废水不仅可以除去Cr O ,还可吸附悬浮杂质
2【答案】C
【分析】
根据得失电子守恒、电荷守恒、元素守恒配平两个方程式如下:反应①:3Cu S+5
2
+46H+=6Cu2++3 +10Cr3++23H O;反应②:6FeS+9 +78H+=6Fe3++6 +18Cr3+
2
+39H O。
2
【解析】
A. 由分析知,还原剂所含元素化合价升高,失电子,氧化剂所含元素化合价降低,得
电子,则Cu S为还原剂, 为氧化剂,则反应①中还原剂与氧化剂的物质的量之比
2
为3:5,A正确;
B. 1molCu S参与反应失去10mol电子,1molFeS参与反应失去9mol电子,根据得失电
2
子守恒可知,用相同物质的量的Cu S和FeS处理 时,Cu S消耗更多 ,B正
2 2
确;
C. 由分析知,处理等物质的量的 时,反应①②中消耗H+的物质的量不等,C错
误;
D. 用FeS处理废水不仅可以除去Cr O ,且该反应还可以生成Fe3+,Fe3+能水解生成
2
氢氧化铁胶体,其具有吸附性,可吸附悬浮杂质,D正确;
故选C。
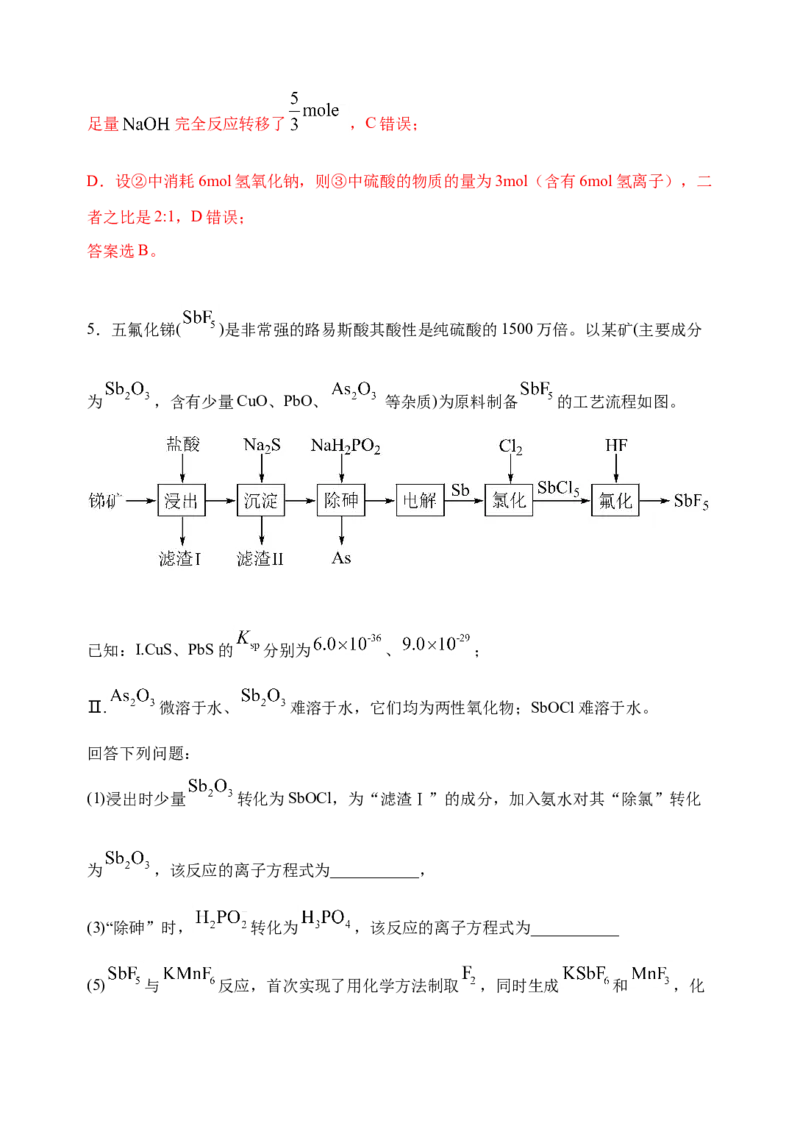
3.硫酸根自由基( )是具有较高氧化还原电位的自由基,可以氧化很多物质。通常
利用分解过硫酸盐的方式产生硫酸根自由基。碱性条件下,过硫酸钠( 硫元素为+6价)活化Fe得到 和 ( 和 为具有强氧化性的自由基),去除水体中
As(V)的机理模型如图所示。下列有关说法中正确的是
A. 中氧元素显-2价
B.与As(V)共沉淀时发生了氧化还原反应
C. 和Fe发生的反应为
D.强碱性条件下,溶液中的自由基主要为
【答案】D
【解析】
A. 中含过氧键,氧元素价态有-1价,选项A错误;
B.与As(V)共沉淀时,没有元素发生化合价变化,选项B错误;
C. 和Fe发生反应生成 和 ,反应为 ,
和 发生反应生成 和 ,反应为 ,选项C错
误;
D.根据图示可知,强碱性条件下, ,故强碱性条件下,溶液中的自由基主要是 ,选项D正确。
答案选D。
4.实验室模拟工业回收碘水中的碘,其操作流程如下:
下列判断正确的是
A. 在 中的溶解度小于在 中的
B.②、③中涉及的分离操作分别为分液和过滤
C.②中 与足量 完全反应转移了
D.②中反应消耗的 和③中反应消耗的 的物质的量之比为
【答案】B
【分析】
根据已知,②中发生的反应是 ,③中发生的反应是
;
【解析】
A.卤素在四氯化碳中溶解度大于水中溶解度,A错误;
B.②是将四氯化碳与水溶液分离,二者互不相容,且为液态混合物,故是分液;③是将
固体与液体分离,故为过滤,B正确;
C.由方程式可以看出,每 与足量 完全反应转移了 ,故 与足量 完全反应转移了 ,C错误;
D.设②中消耗6mol氢氧化钠,则③中硫酸的物质的量为3mol(含有6mol氢离子),二
者之比是2:1,D错误;
答案选B。
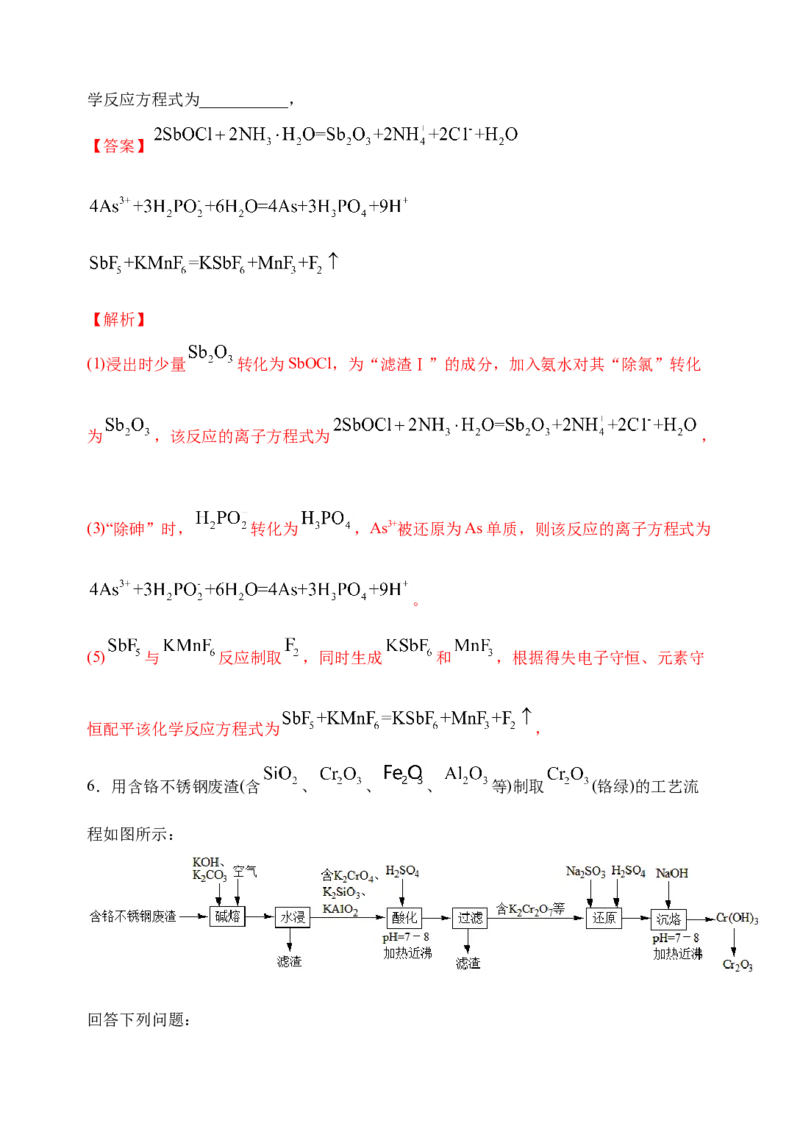
5.五氟化锑( )是非常强的路易斯酸其酸性是纯硫酸的1500万倍。以某矿(主要成分
为 ,含有少量CuO、PbO、 等杂质)为原料制备 的工艺流程如图。
已知:I.CuS、PbS的 分别为 、 ;
Ⅱ. 微溶于水、 难溶于水,它们均为两性氧化物;SbOCl难溶于水。
回答下列问题:
(1)浸出时少量 转化为SbOCl,为“滤渣Ⅰ”的成分,加入氨水对其“除氯”转化
为 ,该反应的离子方程式为___________,
(3)“除砷”时, 转化为 ,该反应的离子方程式为___________
(5) 与 反应,首次实现了用化学方法制取 ,同时生成 和 ,化学反应方程式为___________,
【答案】
【解析】
(1)浸出时少量 转化为SbOCl,为“滤渣Ⅰ”的成分,加入氨水对其“除氯”转化
为 ,该反应的离子方程式为 ,
(3)“除砷”时, 转化为 ,As3+被还原为As单质,则该反应的离子方程式为
。
(5) 与 反应制取 ,同时生成 和 ,根据得失电子守恒、元素守
恒配平该化学反应方程式为 ,
6.用含铬不锈钢废渣(含 、 、 、 等)制取 (铬绿)的工艺流
程如图所示:
回答下列问题:(2) 、KOH、 反应生成 的化学方程式为___________。
(5)“还原”时发生反应的离子方程式为___________。
【答案】
【解析】
(2) 失去 , 、 得到 ,依据得失电子
数相等,配平得 ;
(5) 得到 , 失去 ,依据得失电子数相等,配
平得 ;
7.自然界中锰是含量较高的元素,分布在海洋深处与地壳中,它有多种化合价,如
KMnO (Ⅶ)、KMnO (Ⅵ)、MnO (Ⅳ)等具有氧化性,MnSO (Ⅱ)等具有还原性。
4 2 4 2 4
(1)工业上常用锰酸钾溶液电解制备高锰酸钾,写出离子方程式___。
【答案】2MnO +2H O 2MnO +2OH-+H ↑
2 2
【解析】
(1)根据题意,电解锰酸钾溶液制备高锰酸钾,则阳极锰酸根失电子转化为高锰酸根,阴极水电离的氢离子得电子转化为氢气,反应的离子方程式为2MnO +2H O 2MnO
2
+2OH-+H ↑;
2
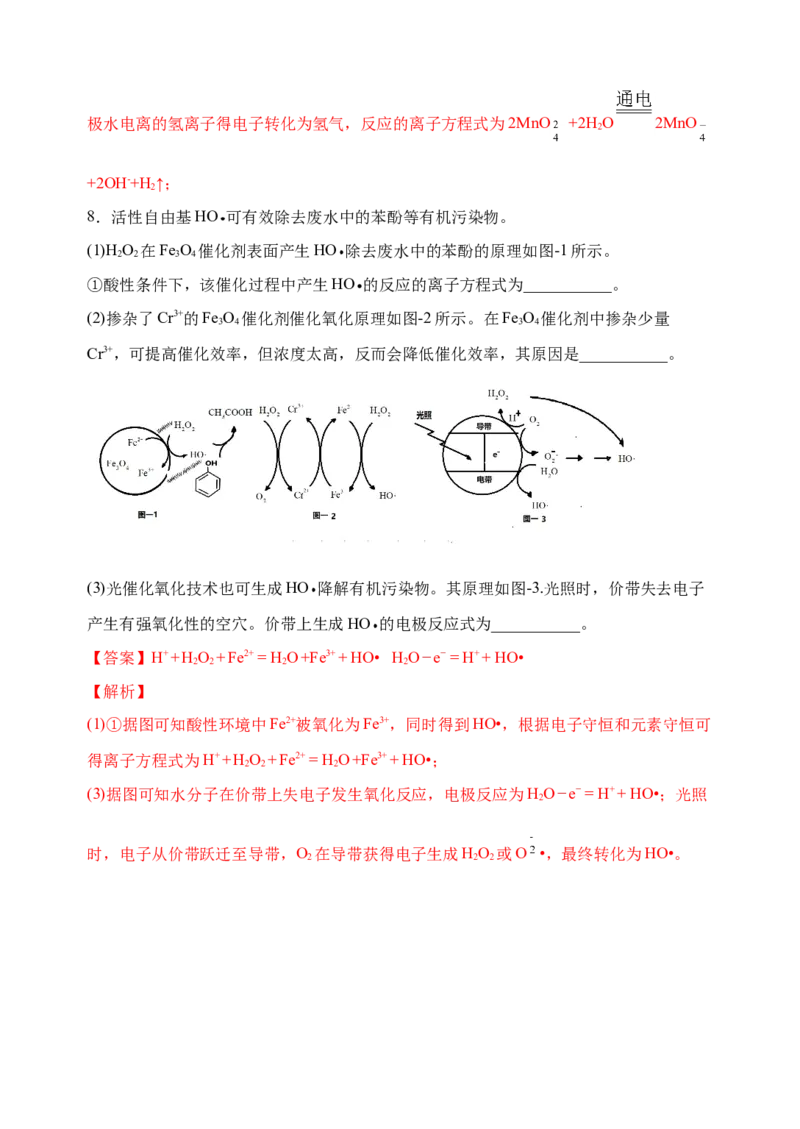
8.活性自由基HO 可有效除去废水中的苯酚等有机污染物。
(1)H O 在Fe O 催化剂表面产生HO 除去废水中的苯酚的原理如图-1所示。
2 2 3 4
①酸性条件下,该催化过程中产生HO 的反应的离子方程式为___________。
(2)掺杂了Cr3+的Fe O 催化剂催化氧化原理如图-2所示。在Fe O 催化剂中掺杂少量
3 4 3 4
Cr3+,可提高催化效率,但浓度太高,反而会降低催化效率,其原因是___________。
(3)光催化氧化技术也可生成HO 降解有机污染物。其原理如图-3.光照时,价带失去电子
产生有强氧化性的空穴。价带上生成HO 的电极反应式为___________。
【答案】H+ +HO +Fe2+ = H O+Fe3+ + HO• H O−e− = H+ + HO•
2 2 2 2
【解析】
(1)①据图可知酸性环境中Fe2+被氧化为Fe3+,同时得到HO•,根据电子守恒和元素守恒可
得离子方程式为H+ +HO +Fe2+ = H O+Fe3+ + HO•;
2 2 2
(3)据图可知水分子在价带上失电子发生氧化反应,电极反应为HO−e− = H+ + HO•;光照
2
时,电子从价带跃迁至导带,O 在导带获得电子生成HO 或O •,最终转化为HO•。
2 2 2