文档内容
微专题23 新型含硫化合物的制备与性质探究
(Na S O Na S O Na S O )
2 2 3 2 2 4 2 4 6
近年来高考的知识面不断扩大,灵活性不断增加,对新型含硫化合物的制备与性质探究
的考查逐渐增多,下面把常考的新型含硫化合物归纳整理如下:
硫的含氧酸应该按以下分类:
正酸系列:次硫酸HSO 、亚硫酸HSO 、硫酸HSO
2 2 2 3 2 4
过酸系列:过硫酸HSO 、过二硫酸HSO
2 5 2 2 8
焦酸系列:焦亚硫酸HSO、焦硫酸HSO
2 2 5 2 2 7
硫代硫酸系列:硫代亚硫酸HSO、硫代硫酸HSO
2 2 2 2 2 3
连酸系列:连二亚硫酸HSO 连多硫酸HS O
2 2 4 2 (2-6) 6
硫能形成多种含氧酸,其含氧酸的种类数,在常见元素中可以说是排名靠前的(含碳的
有机酸除外),究其原因,主要是S—S键键能较高,文献记载可达268kJ/mol。众所周
知,含碳的有机物种类极多的主要原因是C—C键键能高(文献记载332kJ/mol),碳原
子之间能形成碳链,而S—S键的键能并不比C—C键低很多,比Si—Si键或者N—N键
都要高得多,硫原子也有一定的形成较长硫链能力,例如多硫化钠(NaS)和多硫化氢
2 x
(HS,也称为硫烷)都是比较稳定的,单质硫通常以S 分子晶体的形式存在,都是硫
2 x 8
原子能形成硫链能力的一种表现。
硫的含氧酸种类较多,与很多硫含氧酸结构中都存在S—S键有关,除了众所周知的亚硫
酸(HSO )和硫酸(HSO )之外,很多其它硫含氧酸的盐,在工业上或者实验室中有
2 3 2 4
着广泛的用途,这里列举出几种:
1、硫代硫酸钠(Na S O )
2 2 3
硫代硫酸钠是硫代硫酸(HSO)的钠盐,硫代硫酸的结构简式可写作HO—SSO—OH,
2 2 3
可看作硫酸(HO—SO—OH)中的一个氧原子被硫原子取代后得到的化合物,自由的硫
2
代硫酸是不稳定的,易分解为S、SO 和HO,但硫代硫酸的盐可以是稳定的。
2 2含有5个结晶水的硫代硫酸钠,即NaSO·5H O,也就是俗称的“大苏打”或者“海
2 2 3 2
波”,是一种常见的工业品或者化学试剂。硫代硫酸根离子有较强的配位能力,能与一
价银离子Ag+生成稳定的络离子[Ag(S O)]3-,其稳定常数Kf比常见的银氨络离子
2 3 2
[Ag(NH)]+高好几个数量级,因此过去常作为照相底片或者相纸的定影剂,以溶解底片或
3 2
者相纸上未感光的卤化银(以溴化银为主):
AgBr + 2Na SO → Na [Ag(S O)] + NaBr
2 2 3 3 2 3 2
硫代硫酸钠有较强的还原性,可以与卤素单质反应,其中与碘的反应是定量的:
2NaSO + I = Na SO + 2NaI
2 2 3 2 2 4 6
NaSO 是连四硫酸钠,即连四硫酸(HSO)的钠盐,连四硫酸的结构简式是HO—SO
2 4 6 2 4 6 2
—S—S—SO —OH,分子中存在S—S—S—S硫链。该反应在分析化学中用于测定碘的含
2
量,滴定时可用淀粉作为指示剂。用5%的硫代硫酸钠溶液浸渍口罩,可防护低浓度的氯
气,对皮肤的刺激性要比NaOH等强碱小得多。
硫代硫酸钠还可以作为氰化物中毒的解毒剂,在体内可以将剧毒的氰离子CN-转化为毒性
很低的硫氰酸根离子SCN-,以解除CN-的毒性。
NaSO·5H O加热到约48℃时,NaSO 溶解在自身的结晶水中,成为溶液,继续加热则
2 2 3 2 2 2 3
逐渐失去结晶水得到无水物,如果再继续高温加热,NaSO 开始分解,分解产物中有少
2 2 3
量单质硫成为硫蒸气放出,遇空气可能燃烧发出蓝色火焰,分解产物中还含有SO 等气体
2
2、连二亚硫酸钠(Na S O )
2 2 4
连二亚硫酸(HSO)的结构简式可写作HO—SO—SO—OH,与亚硫酸(HO—SO—
2 2 4
OH)有相似之处,分子中存在S—S键。
虽然亚硫酸是中强酸,但将锌粉放在水中,通入二氧化硫,主要并不生成亚硫酸锌,而
是二氧化硫被锌粉还原,生成连二亚硫酸锌:Zn + 2SO → ZnS O
2 2 4
工业上,用锌粉还原亚硫酸氢钠(NaHSO)溶液,即可制取连二亚硫酸钠:
3
,有强烈的刺激性气味,因此工业品硫代硫酸钠也要注意防火。
2NaHSO + Zn → Na SO + Zn(OH) ↓
3 2 2 4 2
可见,连二亚硫酸可看作亚硫酸的还原产物,因此其还原性比亚硫酸更强,在碱性条件
下连二亚硫酸钠(或者连二亚硫酸根离子)是很强的还原剂,碱性条件下标准电极电势
可低到-1.12V,比某些较活泼金属的还原性还要强。
天然染料靛蓝(吲哚衍生物)不溶于水,古代用发酵法将靛蓝还原为水溶性的靛白,然
后将靛白水溶液置于瓮中,放进需要染色的织物,使得靛白水溶液浸入织物纤维,最后
将织物置空气中,织物上的靛白与氧气接触,重新被氧化为不溶于水的靛蓝,染色牢固,
经久耐用。因为在染色过程中存在还原和氧化过程,靛蓝这样的染料就被称为还原染料,
也称为“瓮染料(Vat dyes)”。今天工业上还原靛蓝这类还原染料,不再使用效率低的
发酵还原法,都是使用化学还原剂,主要使用的就是有着强还原性的连二亚硫酸钠。
连二亚硫酸钠也很容易被空气中的氧气氧化,特别是在水溶液中,可以作为一种强的抗
氧化剂,能够保护某些易氧化物质不被氧化,因此工业上连二亚硫酸钠俗称“保险粉”。
连二亚硫酸钠是强还原剂,与氧气的反应是放热的,一旦连二亚硫酸钠固体遇少量水或
者受潮,就容易与空气中氧气反应放热,如果积热不散,达到一定温度连二亚硫酸钠会
剧烈分解,生成单质硫等易燃产物,最终引起自燃,因此保险粉是属于遇湿易燃物品的
危险品,在消防安全上是不“保险”的。一旦保险粉受潮发生火灾,如果扑救用水量不
足,反而会加剧燃烧,干粉、二氧化碳、干砂等灭火剂只能压住表面燃烧的火焰,不能
阻止已经受潮保险粉的氧化分解,只有用大量水扑救,使得保险粉溶解于水,才能彻底灭火。保险粉发生火灾时会产生二氧化硫等有毒产物,消防人员和抢险人员必须做好自
身防护,也要防止有毒产物污染环境。
有趣的是,4价硫的化合物和4价碳的化合物,有时却有一定的相似性,例如二氧化硫和
二氧化碳都是酸性氧化物,二氧化硫也能像二氧化碳一样使得澄清石灰水变浑浊等,草
酸(HOOC—COOH)可以看作“连二碳酸”,草酸和草酸盐也具有明显的还原性。
3、焦亚硫酸钠(Na S O )
2 2 5
焦亚硫酸(HSO)又称为一缩二亚硫酸,形式上看是两分子亚硫酸失去一分子水的产物,
2 2 5
但其结构简式一般认为并不是HO—SO—O—SO—OH,而是HO—SO—SO —OH,分子
2
中同样存在S—S键。
在氢氧化钠或者碳酸钠的浓溶液(工业上一般使用碳酸钠)中通入过量的二氧化硫,通
常认为最终生成亚硫酸氢钠(NaHSO)的浓溶液:
3
2NaOH + SO → Na SO + H O(或者NaCO + SO → Na SO + CO ↑)
2 2 3 2 2 3 2 2 3 2
NaSO + H O + SO → 2NaHSO
2 3 2 2 3
亚硫酸氢钠又称重亚硫酸钠,系英文习惯名称Sodium bisulfite的直译,酸根前的bi-前缀
即“重”,例如Sodium bicarbonate重碳酸钠即碳酸氢钠。
但实际上,在存在高浓度亚硫酸氢根离子的水溶液中,存在下列平衡:
2HSO SO + H O
2 2
SO 即焦亚硫酸根离子,结构简式为[O—SO—SO —O]2-,而不是[O—SO—O—SO—
2 2
O]2-。因此从浓溶液中结晶析出亚硫酸氢钠时,很容易结晶析出Na2S2O5,可以看作两分子亚
硫酸氢钠失去一分子水的产物,Na2S2O5的英文习惯名称在酸根前再加meta-前缀,即
Sodium metabisulfite,meta-前缀可译作“偏”,即“失水”,例如Metaphosphoric acid偏
磷酸,因此中文名可译作“偏重亚硫酸钠”。
但是NaSO 也可以直接看作焦亚硫酸的钠盐,因此英文名称又可以写作Sodium
2 2 5
pyrosulfite,酸根前缀pyro-是“焦”,中文名“焦亚硫酸钠”。
这样一来,NaSO 这种化合物中英文名称都有两种,分别是偏重亚硫酸钠(Sodium
2 2 5
metabisulfite)和焦亚硫酸钠(Sodium pyrosulfite),试剂品多使用前一名称,而工业品多
使用后一名称,命名的混乱导致了很多不懂化学者的误译,例如“偏亚硫酸氢钠”,甚
至看到有将KSO 误称为“偏硫代硫酸钾”的情况。
2 2 5
商品固体亚硫酸氢钠和固体焦亚硫酸钠实际上都是NaHSO 和NaSO 的混合物,只是主
3 2 2 5
要成分不同,工业品多生产焦亚硫酸钠固体,而亚硫酸氢钠可以溶液形式供应商品。焦
亚硫酸钠溶于水后又发生水解反应,最终还是得到亚硫酸氢钠溶液,因此在实际应用中
二者基本可以通用。
焦亚硫酸钠和亚硫酸氢钠都是还原剂,虽然还原性不如连二亚硫酸钠,但较稳定,还原
作用也较温和,工业上也广泛作为还原剂和抗氧化保护剂。
亚硫酸氢根离子的硫原子上还有一对孤对电子,硫原子亲核性强于氧原子,因此亚硫酸
氢根离子是较强的亲核试剂,在有机化学反应中可看作“磺酸基负离子”,能与醛或者
酮羰基发生亲核加成反应,生成α-羟基磺酸(或者α-羟基磺酸的盐),这一特性使得亚
硫酸氢钠或者焦亚硫酸钠在有机合成上也有广泛用途。焦亚硫酸钠和亚硫酸氢钠也可以作为食品添加剂,有二氧化硫漂白、抗氧化等作用,二
氧化硫是红酒的常见添加剂,目前常将NaSO 或者KSO 添加到红酒中作为二氧化硫产
2 2 5 2 2 5
生剂。
4、焦硫酸钠(Na S O )
2 2 7
将硫酸氢钠(NaHSO)加热到熔点以上,就发生与亚硫酸氢钠失水得到焦亚硫酸钠相似
4
的反应,两分子硫酸氢钠失去一分子水,得到焦硫酸钠:
2NaHSO → Na SO + H O↑
4 2 2 7 2
如果继续加热,焦硫酸钠还会进一步分解放出SO :
3
NaSO → Na SO + SO↑
2 2 7 2 4 3
在焦硫酸钠未明显分解之前,将熔体冷却,趁凝固未完全冷却时破碎成小块,即得商品
焦硫酸钠。
焦硫酸钠在工业生产上用途不大,但在分析化学,特别是工业分析中是很有用的试剂。
很多天然氧化物矿石虽然有一定的碱性氧化物性质,但并不容易溶解于酸,例如天然的
铁矿石,特别是磁铁矿(Fe O)在酸中即使加热也很难溶解,但与焦硫酸钠或者焦硫酸
3 4
钾共熔,在高温和SO 的作用下,即可转化为易溶的化合物。因此焦硫酸钠常在实验室分
3
析中用作酸性熔矿剂。
5、过硫酸钠(Na S O )
2 2 8
过硫酸钠是过二硫酸(HSO)的钠盐,过二硫酸的结构简式可以写作HO—SO—O—O
2 2 8 2
—SO —OH,分子中存在过氧链,可看作过氧化氢中的氢原子被磺酸基(—SO —OH或
2 2
者—SO H)取代的产物。过硫酸钠、过硫酸钾和过硫酸铵都是重要的过硫酸盐,工业生
3产过硫酸铵或者过硫酸钠较为容易,用途也较广,过硫酸钾溶解度远小于过硫酸铵和过
硫酸钠,但稳定性较好,容易重结晶提纯,常作为实验室试剂。
过硫酸铵和过硫酸钠在工业上常缩写为APS和SPS,系英文习惯名称Ammonium
persulfate和Sodium persulfate的缩写,酸根前加per-前缀表示酸根中心原子的“形式化合
价”高于通常酸根中心原子化合价,例如过硫酸根离子中,硫形式上是+7价,但这一前
缀并不表示酸根的真实结构,翻译成中文时要注意。过去一般将per-前缀直接翻译成
“过”,例如Ammonium persulfate过硫酸铵、Potassium perchlorate过氯酸钾、Potassium
permanganate过锰酸钾等,直到上世纪60年代中文化学资料上一般还是这样翻译的,但
今天则要注意酸根结构,酸根中有过氧链才能用“过”字,否则应该用“高”字,因此
Potassium perchlorate和Potassium permanganate今天应该翻译成“高氯酸钾”和“高锰酸
钾”。
过硫酸钠或者过硫酸根离子在水溶液中是一种极强的氧化剂,标准电极电势高达2.01V,
氧化性强于过氧化氢、高锰酸钾、重铬酸钾等常见强氧化剂,但过硫酸根离子有较高的
稳定性,低温和不加催化剂的情况下,氧化反应速率很慢,接近惰性,因此固体过硫酸
盐相对硝酸钾、氯酸钾、高锰酸钾等固体强氧化剂,储运和使用反而要安全一些。
使用过硫酸盐作为氧化剂时,需要升温或者加入适当的催化剂,Ag+、Cu2+等金属离子可
作为催化剂。目前印刷电路板(PCB)行业中常用过硫酸铵或者过硫酸钠作为PCB铜箔
的腐蚀剂,市售的一些小包装白色粉末状PCB腐蚀剂,实际上就是以过硫酸盐为主要成
分的,当铜箔浸入过硫酸盐浓溶液时,即发生下列反应(以过硫酸钠为例):
NaSO + Cu → Na SO + CuSO
2 2 8 2 4 4
未加温情况下,一开始腐蚀速率极慢,但少量铜箔被腐蚀后,Cu2+进入溶液,成为了过硫
酸盐的催化剂,起到了自催化作用,反应速率逐渐加快,因此不需要额外添加催化剂,待腐蚀剂反复使用一段时间后,腐蚀效果下降,可补加一定量的过硫酸盐,仍可继续使
用一段时间。
过硫酸盐腐蚀剂无需使用硫酸、盐酸等强酸腐蚀性危险品,也不使用过氧化氢等危险氧
化剂,较为安全。固体过硫酸盐储运也较安全,但固体过硫酸盐仍然严禁与强还原剂混
存,否则一旦二者发生接触同样有燃烧爆炸危险,1993年深圳清水河危险品仓库大爆炸
事故,起火原因正是过硫酸铵与硫化钠(强还原剂)混存接触发生自燃。
【专题精练】
1.硫代硫酸钠(Na SO)可作为还原剂,已知25.0mL 0.0100mol/L Na SO 溶液恰好把
2 2 3 2 2 3
22.4mL Cl (标准状况下)完全转化为Cl-离子,则 将转化成
2
A.S2- B.S C. D.
2.硫代硫酸钠(NaSO)可作为脱氯剂,已知1mol Na SO 溶液恰好把4mol Cl 完全转
2 2 3 2 2 3 2
化为Cl-离子,则SO2-将转化成
2 3
A.SO 2- B.S C.SO 2- D.S2-
4 3
3.连二亚硫酸钠(Na SO)俗称保险粉,还原性比 Naso3更强,工业上广泛用于纺织品漂
2 2 4
白及作脱氧剂等。工业上可用惰性电极电解 NaHSO 溶液得到连二亚硫酸钠(Na SO),
3 2 2 4
如下图所示。下列说法不正确的是
A.得到连二亚硫酸钠产品电极反应式为2HSO -+2e-=S O2-+2OH-
3 2 4
B.a为阳极
C.连二亚硫酸钠产品在阴极得到
D.若不加隔膜,则得不到连二亚硫酸钠4.连二亚硫酸钠(Na SO)俗称保险粉,工业上可用于纸浆漂白,该物质还原性比NaSO
2 2 4 2 3
强,其水溶液能被空气中的氧气氧化,在碱性介质中相对稳定。下列说法不正确的是
2
A.连二亚硫酸钠可以用于除去废水中的重铬酸根离子,使Cr O7 转化为Cr3+
2
B.连二亚硫酸钠溶液敞口可能会发生的化学方程式为:2NaSO+O +2H O=4NaHSO
2 2 4 2 2 3
C.连二亚硫酸钠用于纸浆漂白的原理与ClO 的漂白原理相同
2
D.在包装保存“保险粉”时加入少量NaCO 固体,可以提高“保险粉”的稳定性
2 3
5.《环境科学》曾刊发我国科研部门采用零价铁活化过硫酸钠(NaSO 其中S为+6
2 2 7
价)去除废水中的正五价砷的研究成果,其反应机理模型如图,(N 为阿伏加德罗常数
A
的值)下列说法正确的是
A.1 molSO -· (自由基)中含50N 个电子
4 A
B.pH越大,越不利于去除废水中的正五价砷
C.1 mol过硫酸钠中含N 个过氧键
A
D.转化过程中,若共有1 mol S O2-被还原,则参加反应的Fe为56 g
2 8
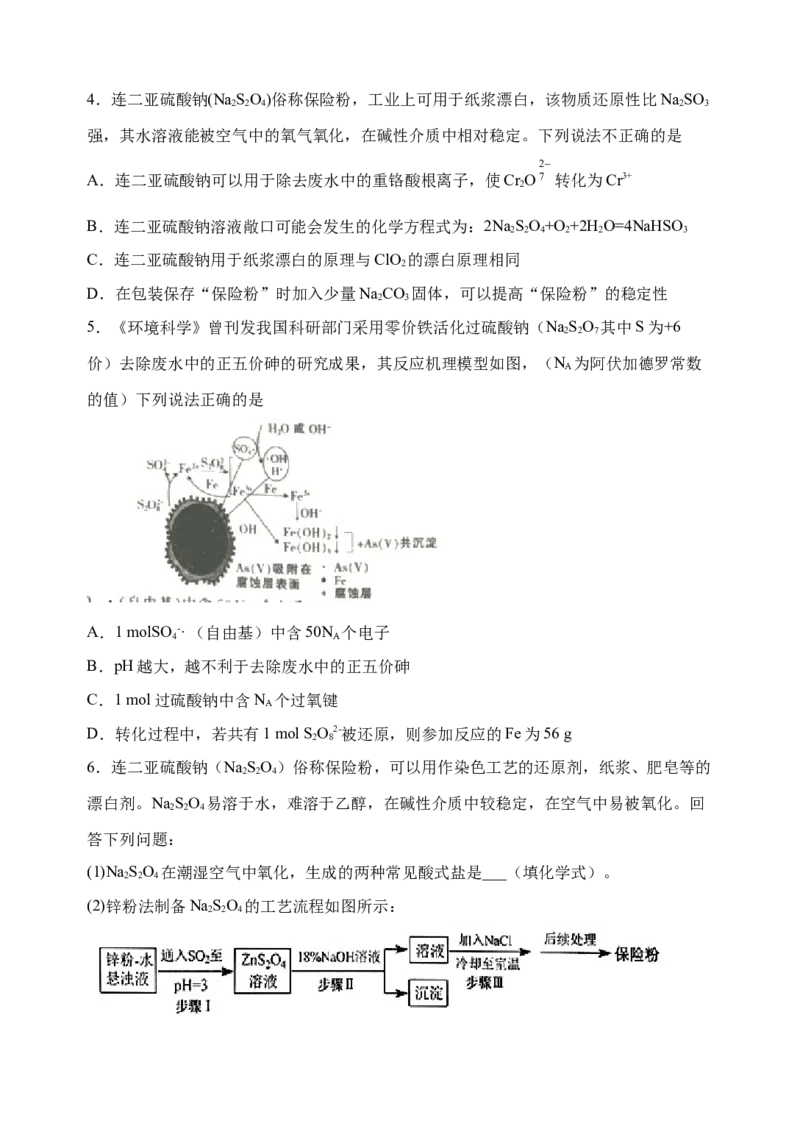
6.连二亚硫酸钠(NaSO)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的
2 2 4
漂白剂。NaSO 易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。回
2 2 4
答下列问题:
(1)NaSO 在潮湿空气中氧化,生成的两种常见酸式盐是___(填化学式)。
2 2 4
(2)锌粉法制备NaSO 的工艺流程如图所示:
2 2 4①工业上常将锌块进行预处理得到锌粉-水悬浊液,其目的是__。
②步骤Ⅰ中发生反应的化学方程式为__。
③在步骤Ⅲ中得到的NaSO 固体要用乙醇洗涤,其优点是__,“后续处理”最终要加入
2 2 4
少量的NaCO 固体,其原因是__。
2 3
(3)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将HCOONa和烧碱加入
乙醇水溶液中,然后通入SO 发生反应,有CO 气体放出,总反应的离子方程式是___。
2 2
(4)有人设计了图示方法同时制备连二亚硫酸钠和过二硫酸钠(NaSO),并获得中国专
2 2 8
利。电解过程中,阴极室生成NaSO,a极的电极反应式为__,通过阳离子交换膜的离
2 2 4
子主要是Na+,其迁移方向是__(填“a到b”或“b到a”)。
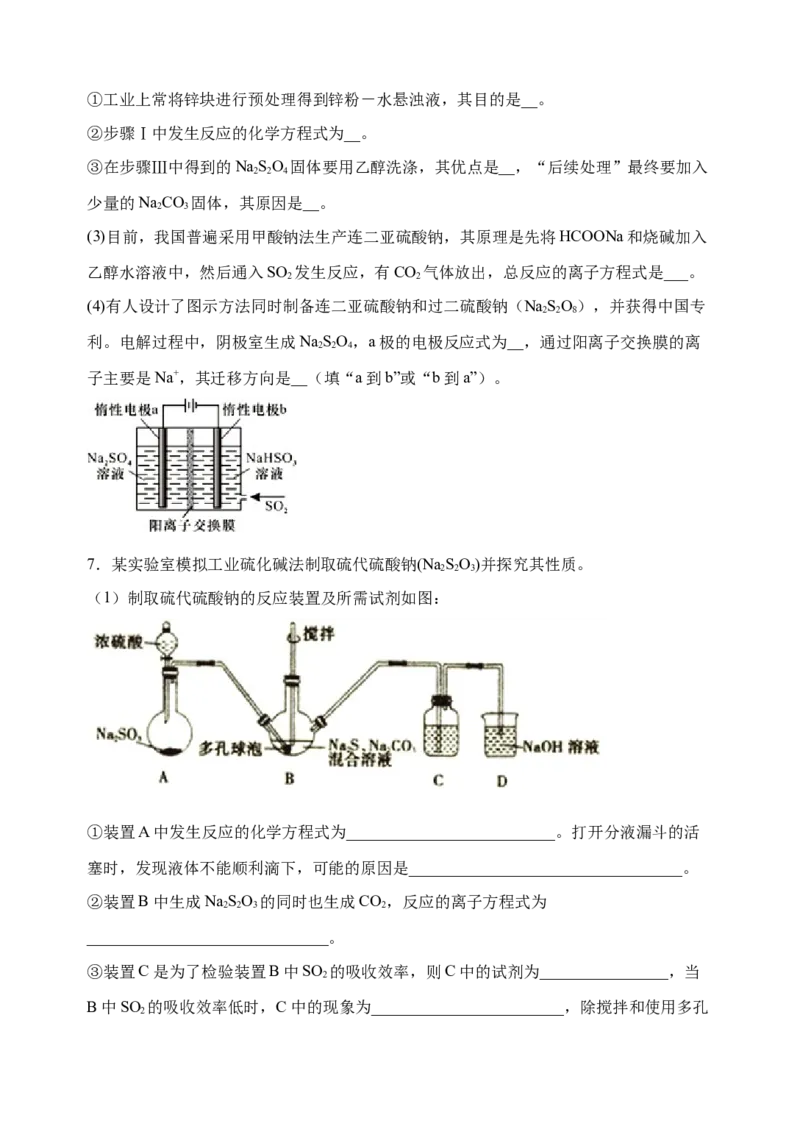
7.某实验室模拟工业硫化碱法制取硫代硫酸钠(Na SO)并探究其性质。
2 2 3
(1)制取硫代硫酸钠的反应装置及所需试剂如图:
①装置A 中发生反应的化学方程式为__________________________。打开分液漏斗的活
塞时,发现液体不能顺利滴下,可能的原因是__________________________________。
②装置B 中生成NaSO 的同时也生成CO,反应的离子方程式为
2 2 3 2
______________________________。
③装置C 是为了检验装置B中SO 的吸收效率,则C中的试剂为________________,当
2
B中SO 的吸收效率低时,C 中的现象为________________________,除搅拌和使用多孔
2球泡外,再写出一种提高B中SO 的吸收效率的方法:
2
______________________________。
(2)预测并探究硫代硫酸钠的性质(反应均在溶液中进行):
预测 实验操作 实验现象
探究1 NaSO 溶液呈碱性 _________ pH=8
2 2 3
探究2 NaSO 具有还原性 向新制氯水中滴加NaSO ______
2 2 3 2 2 3
①探究1中的实验操作为________________________。
②探究2 中的实验现象为_____________________,反应的离子方程式为_____________。
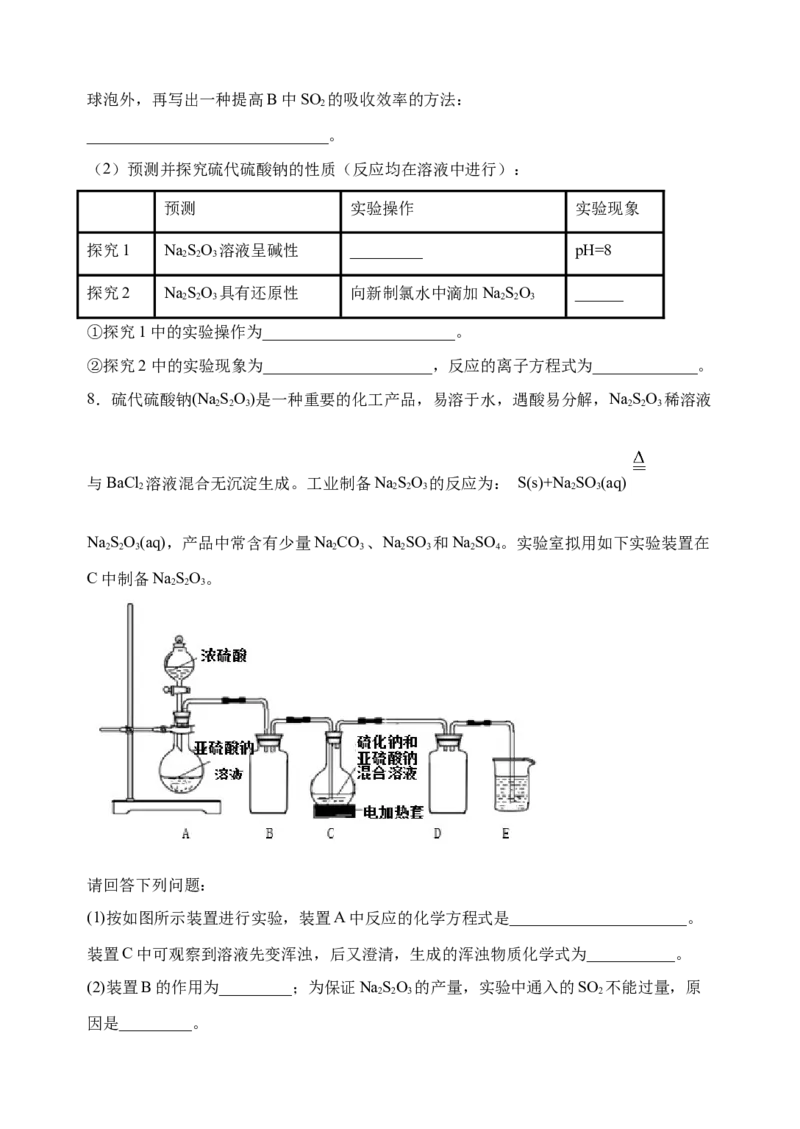
8.硫代硫酸钠(Na SO)是一种重要的化工产品,易溶于水,遇酸易分解,NaSO 稀溶液
2 2 3 2 2 3
与BaCl 溶液混合无沉淀生成。工业制备NaSO 的反应为: S(s)+Na SO (aq)
2 2 2 3 2 3
NaSO(aq),产品中常含有少量NaCO 、NaSO 和NaSO 。实验室拟用如下实验装置在
2 2 3 2 3 2 3 2 4
C中制备NaSO。
2 2 3
请回答下列问题:
(1)按如图所示装置进行实验,装置A中反应的化学方程式是______________________。
装置C中可观察到溶液先变浑浊,后又澄清,生成的浑浊物质化学式为___________。
(2)装置B的作用为_________;为保证NaSO 的产量,实验中通入的SO 不能过量,原
2 2 3 2
因是_________。(3)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:
①实验装置的连接顺序依次________________(填装置的字母代号),装置C中的试剂为
____________。
②能证明固体中含有碳酸钠的实验现象是__________________。
(4)若要检验固体硫代硫酸钠工业产品中含有NaSO ,需先加水配成稀溶液,再依次加入
2 3
的试剂为_____________________和品红溶液。
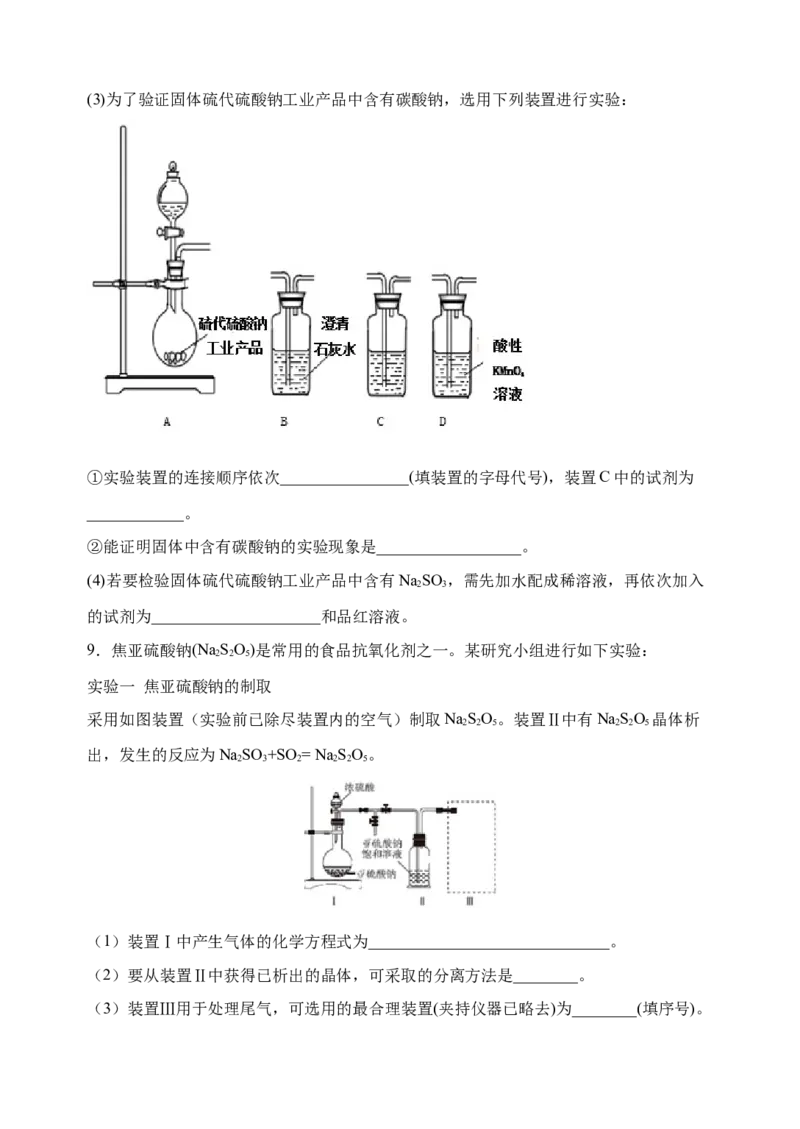
9.焦亚硫酸钠(Na SO)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
2 2 5
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取NaSO。装置Ⅱ中有NaSO 晶体析
2 2 5 2 2 5
出,发生的反应为NaSO +SO= Na SO。
2 3 2 2 2 5
(1)装置Ⅰ中产生气体的化学方程式为______________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是________。
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。实验二 焦亚硫酸钠的性质
已知:NaSO 溶于水即生成NaHSO。
2 2 5 3
(4)检测NaSO 晶体在空气中已被氧化的实验方案是 ____________________。
2 2 5
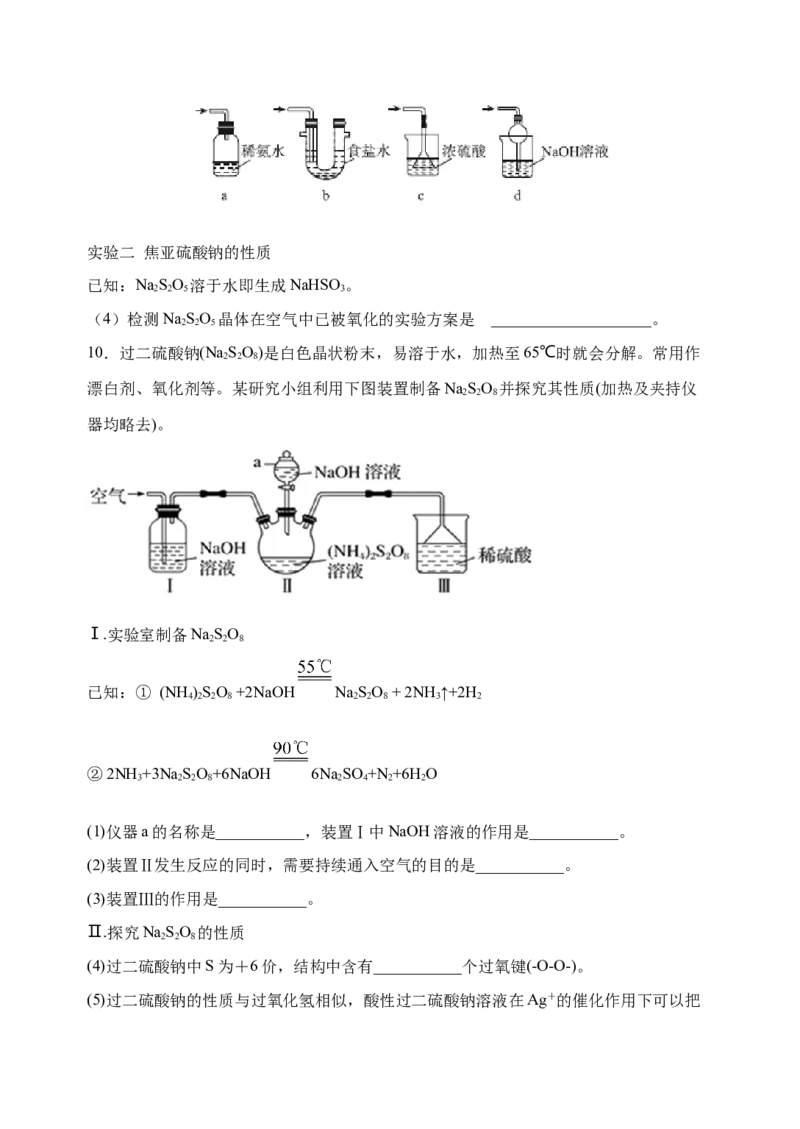
10.过二硫酸钠(Na SO)是白色晶状粉末,易溶于水,加热至65℃时就会分解。常用作
2 2 8
漂白剂、氧化剂等。某研究小组利用下图装置制备NaSO 并探究其性质(加热及夹持仪
2 2 8
器均略去)。
Ⅰ.实验室制备NaSO
2 2 8
已知:① (NH )SO +2NaOH NaSO + 2NH↑+2H
4 2 2 8 2 2 8 3 2
②2NH +3Na SO+6NaOH 6NaSO +N +6H O
3 2 2 8 2 4 2 2
(1)仪器a的名称是___________,装置Ⅰ中NaOH溶液的作用是___________。
(2)装置Ⅱ发生反应的同时,需要持续通入空气的目的是___________。
(3)装置Ⅲ的作用是___________。
Ⅱ.探究NaSO 的性质
2 2 8
(4)过二硫酸钠中S为+6价,结构中含有___________个过氧键(-O-O-)。
(5)过二硫酸钠的性质与过氧化氢相似,酸性过二硫酸钠溶液在Ag+的催化作用下可以把Mn2+氧化为MnO ,该法可用于检验Mn2+,所得溶液除去Ag+后加入BaCl 溶液可以产
2
生白色沉淀。写出该反应的离子方程式___________。
Ⅲ.测定产品纯度
(6)称取0.2500g样品,用蒸馏水溶解,加入过量KI,充分反应后,再滴加几滴指示剂,
用0.1000mol/L Na SO 标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为20.00
2 2 3
mL。
已知:I+2SO =S O +2I-。
2 2 4
①选用的指示剂是___________;达到滴定终点的现象是___________。
②样品的纯度为___________。