文档内容
微专题突破8 化学反应速率与化学平衡
生命是一张弓,那弓弦是梦想
目标定位
1.能应用化学反应速率和化学平衡移动原理解释生活、生产中的相关问题。
2.能判断反应的熵变、反应是否达到平衡状态,能计算平衡常数。
3.能根据图示判断反应机理。
教学重点难点
1.温度的影响规范答题。
2.催化剂与反应机理。
教学方法
讨论、归纳
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.三不混同,二原则
①不要将平衡的移动和速率的变化混同起来。
三个
如平衡正向移动,不一定是正反应速率增加,逆反应速率减小
不要
②不要将平衡的移动与浓度的变化混同起来。如平衡右移生成物的浓度不一定增加
混同
③不要将平衡的移动与反应物的转化率提高等同起来。如平衡右移,反应物的转化率不一定提高
二个 “ ” 可逆反应中反应物的量不为0(确定取值范围)
原则 “ 一” 把生成物的量全部转化为反应物的量(处理等效平衡)
2.反应速率理论在实际生产中的运用
对于受热不稳定性的物质(如HO 、HNO )或受易挥发的物质(如浓硝酸),在采用升高温
温度 2 2 3
度加快反应速率时,要描述为“适当升高温度”
接触面积 不同相之间的反应,若增大接触面积对于固体用粉碎的方法,而液体则用喷洒的方法
接触机会 增大接触机会的措施为直接搅拌、通气体搅拌
催化剂 有机反应、混合气体的反应,常使用催化剂加快反应速率
3.传统速率、平衡图象题的解答方法及思路——一看、二想、三判断
①一看面:即横坐标、纵坐标的量;②二看线:即线的斜率,平与陡的含义,函数的增减
性(先拐先平:如在转化率——时间图上,先出现拐点的曲线先达到平衡,此时逆向推理
一看图象 可得该变化的温度高、浓度大、压强高);③看点:即起点、转折点、拐点、交叉点;④
四看要不要画辅助线:等温线、等压线等(定一议二:当图象中有三个量时,先确定一个
量不变再讨论另外两个量的关系);⑤看量:定量图象中有关量的多少
联想外界条件改变对化学反应速率和化学平衡的影响,紧扣可逆反应的特征,搞清正反应
二想规律
方向吸热还是放热,体积是增大、减少,还是不变,有无固体参加或生成等
三判断 认准某些关键数据在解题中的特定作用,全面准确地从图中找出直接或隐含的相关信息
3.陌生平衡图像的分析方法
(1)题型特点
化学反应原理综合题在非选择题中的陌生图像打破了传统的速率、平衡图像模式,反应体系不再局限于气
相反应,引入了更多的液相反应,纵坐标和横坐标不再局限于时间、温度、压强、速率、转化率等物理量,而
是引入了更多的变量,如两种物质的物质的量之比、气体分压的负对数等,使得图像更新颖、信息容量更大、
题目难度更大。微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
(2)复杂(竞争、连续)反应图像的解题流程
①找准竞争(或连续)反应在反应特点方面的异同
第一步 审反应方程式
②分清主、副反应
提取研究状态 ①非平衡状态量,其变化与反应速率有关
第二步
(平衡、非平衡) ②平衡状态量,则与平衡移动有关
依据图中横坐标、纵坐标的内容,找出图中曲线中的“点”、“线”的含义
第三步 析图
和变化趋势,并用平衡移动原理解答具体问题
位位位位位
1.(2024·江苏卷)下列说法正确的是
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能
B.C H 与O 反应中,Ag催化能提高生成CHCHO的选择性
2 4 2 3
C.HO 制O 反应中,MnO 能加快化学反应速率
2 2 2 2
D.SO 与O 反应中,VO 能减小该反应的焓变
2 2 2 5
【答案】C
【解析】A项,固氮酶是豆科植物固氮过程的催化剂,能降低该反应的活化能,错误;B项,根据题意,
催化剂有选择性,如C H 与O 反应用Ag催化生成 (环氧乙烷)、用CuCl /PdCl 催化生成CHCHO,
2 4 2 2 2 3
则判断Ag催化不能提高生成CHCHO的选择性,错误;C项,MnO 是HO 制O 反应的催化剂,能加快化学
3 2 2 2 2
反应速率,正确;D项,VO 是SO 与O 反应的催化剂,能加快反应速率,但不能改变该反应的焓变,错误。
2 5 2 2
2.(2023·江苏卷)金属硫化物(MS)催化反应CH(g)+2HS(g)=CS(g)+4H(g),既可以除去天然
x y 4 2 2 2
气中的HS,又可以获得H。下列说法正确的是
2 2
A.该反应的ΔS<0
B.该反应的平衡常数K=
C.题图所示的反应机理中,步骤Ⅰ可理解为HS中带部分负电荷的S与催化剂中的M之间发生作用
2
D.该反应中每消耗1 mol H S,转移电子的数目约为2×6.02×1023
2
【答案】C
【解析】A项,左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5,ΔS>0,错误;B项,
由方程式知,K=,错误;C项,由图可知,步骤Ⅰ发生的反应为硫化氢中硫原子与催化剂MS 中的M原子结
x y
合形成了M—S键,正确;D项,由方程式知,消耗 1 mol H S同时生成2 mol H ,转移4 mol e-,数目为
2 2
4×6.02×1023,错误。
3.(2024·江苏卷)二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)为:
①CO(g)+H(g)=CO(g)+HO(g) ∆H=41.2 kJ·mol-1
2 2 2 1
②CO(g)+2H(g)=CHOH(g) ∆H
2 3 2
225℃、8×106 Pa下,将一定比例CO、H 混合气匀速通过装有催化剂的绝热反应管。装置及L、L、L…
2 2 1 2 3
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找位点处(相邻位点距离相同)的气体温度、CO和CHOH的体积分数如图所示。下列说法正确的是
3
A.L 处与L 处反应①的平衡常数K相等
4 5
B.反应②的焓变∆H>0
2
C.L 处的HO的体积分数大于L 处
6 2 5
D.混合气从起始到通过L 处,CO的生成速率小于CHOH的生成速率
1 3
【答案】C
【解析】A项,L 处与L 处的温度不同,故反应①的平衡常数K不相等,错误;B项,由图像可知,L -
4 5 1
L 温度在升高,该装置为绝热装置,反应①为吸热反应,所以反应②为放热反应,ΔH <0,错误;C项,从L
3 2 5
到L,甲醇的体积分数逐渐增加,说明反应②在向右进行,反应②消耗CO,而CO体积分数没有明显变化,说
6
明反应①也在向右进行,反应①为气体分子数不变的反应,其向右进行时,n(H₂O)增大,反应②为气体分子数
减小的反应,且没有HO的消耗与生成,故n总减小而n(H₂O)增加,即HO的体积分数会增大,故L 处的
2 2 6
HO的体积分数大于L 处,正确;D项,L 处CO的体积分数大于CHOH,说明生成的CO的物质的量大于
2 5 1 3
CHOH,两者反应时间相同,说明CO的生成速率大于CHOH的生成速率,错误。
3 3
【问题解决1】
1.(2024·江苏南京市、盐城市一模)“碳中和”目标如期实现的关键技术之一是CO 的再资源化利用。
2
(1)氨的饱和食盐水捕获CO 是其利用的方法之一,反应原理为:NaCl(aq)+NH (g)+CO(g)+HO(l)
2 3 2 2
=NaHCO (s)+NH Cl(aq)。该反应常温下能自发进行的原因是__________________________。
3 4
【答案】反应∆H<0
【解析】反应NaCl(aq)+NH (g)+CO(g)+HO(l)=NaHCO (s)+NH Cl(aq)为熵减的反应,该反应常
3 2 2 3 4
温下能自发进行,反应∆H<0,故答案为反应∆H<0。
2.(2024·淮安市高三上学期开学考)以废旧锂电池的正极材料[活性物质为LiCoO(x≤1)、附着物为炭
x 2
黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和Co O。
3 4
(1)浸出:将煅烧后的粉末(含LiCoO 和少量难溶杂质)与HSO 溶液、HO 溶液中的一种配成悬浊液,
x 2 2 4 2 2
加入图所示的烧瓶中。75℃下通过滴液漏斗缓慢滴加另一种溶液;充分反应后,滤去少量固体残渣。得到
LiSO 、Co O 和硫酸的混合溶液。
2 4 3 4
①滴液漏斗中的溶液是__________。微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
②为了提高浸出过程中钴的浸出率,实验中可采取的措施有_______。(填字母)
A.增加预处理后材料投入量 B.将预处理后材料粉碎并适当加快搅拌
C.缩短浸出时间 D.适当提高浸出温度
【答案】①HO ②BD
2 2
【解析】①硫酸用于和煅烧后的粉末(含LiCoO 和少量难溶杂质)反应,HO 用以还原钴元素以得到
x 2 2 2
LiSO 、CoSO 和硫酸,当气体不再产生时可停止加入,且反应温度控制为75℃,实验中需防止HO 分解,故
2 4 4 2 2
需将HO 通过分液漏斗滴加;②A项,增加预处理后材料投入量,不利于增大接触面积,不利于提高钴的浸出
2 2
率,不符合题意;B项,将预处理后材料粉碎并适当加快搅拌,增大了接触面积,有利于提高钴的浸出率,符
合题意;C项,缩短浸出时间,生成物的物质的量减小,不利于提高钴的浸出率,不符合题意;D项,适当提
高浸出温度,增大反应速率,生成物的物质的量增大,有利于提高钴的浸出率,符合题意。
化学反应速率与化学反应的方向
加快反应速率 浓度、压强、温度、催化剂,固体大小、原电池、通气体搅拌、气液逆流操作、液体喷
洒
规范 将固体粉碎,增大接触面积,加快反应速 格式 操作——原理——目的
率
注意 对于受热不稳定的物质(如HO、HNO)是:适当升高温度,防止HNO、HO 分解
2 2 3 3 2 2
化学反应的方向 ΔG=ΔH-TΔS ΔG<0,可自发进行
考点精练
1.(2024·镇江市丹阳市上学期开学考)MnO -CeO 催化剂能催化NH 脱除烟气中的NO,反应为
2 2 3
4NH (g)+4NO(g)+O(g)=4N(g)+6HO(g),其机理如图所示。下列说法正确的是
3 2 2 2
A.该反应∆S<0
B.该反应的平衡常数K=
C.步骤Ⅰ可描述为NH 吸附到MnO 表面与表面吸附氧反应生成-NH 和HO,同时MnO 被还原为
3 2 2 2 2
MnO;烟气中的NO和-NH 反应生成N 和HO
2 3 2 2 2
D.该反应中每消耗1 mol O,转移电子的数目约为4×6.02×1023
2
【答案】C
【解析】A项,该反应是气体分子数增加的反应,故该反应ΔS>0,错误;B项,化学平衡常数的表达式
为各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积,即该反应的平衡常数 K
=,错误;C项,如图所示,步骤Ⅰ可描述为NH 吸附到MnO 表面与表面吸附氧反应生成—NH 和HO,同时
3 2 2 2
MnO 被还原为MnO ;烟气中的NO和—NH 反应生成N 和HO,正确;D项,该反应中,NO、O 作氧化剂,
2 2 3 2 2 2 2
NH 作还原剂,每消耗1 mol O,就有4 mol NH 反应,转移电子的数目约为12×6.02×1023,错误。
3 2 3
2.(2024·南通一模)一种燃煤烟气中CO 的捕集和资源再利用技术可通过如下转化过程实现。
2
转化I是利用风/太阳能电厂过剩电力,将CO 转化为C H 等高值产品。
2 2 4
转化II是利用风/太阳能电厂过剩电力驱动压缩机压缩CO。
2
转化III是风/太阳能电厂发电低谷时,利用压缩CO 推动汽轮机,带动发电机发电。
2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找(2)在金属催化剂表面发生*CO— \s\up 0()*C H 转化的过程可能为*CO— \s\up 0()*COOH— \s\up
2 → 2 4 2 → →
0()*CO— \s\up 0()*OCCO— \s\up 0()*C H(*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构
→ → 2 4
型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的Cu-Cs复合催化剂更有
利于C H 的形成,可能原因是________________
2 4
_______________________________________________________________________________________________。
(3)从物质转化与资源综合利用角度分析,本工艺中CO 的捕集和资源再利用技术的优点是
2
__________________________________________________________________________________________。
【答案】(2)Cu-Cs复合催化剂可提供更多的活性位点(Cu-Cs复合催化剂更有利于CO等中间体的吸
附),且能降低反应的活化能,因此更有利于C H 的形成 (3)有利于将CO 转化为更有价值的C H 等产品;
2 4 2 2 4
使用风能、太阳能有利于减排CO;能实现能量的储存和转化,调控电力过剩或电力不足
2
【解析】(2)从图甲中可以看出Cu-Cs复合催化剂可提供更多的活性位点,有利于CO等中间体的吸附,
故掺杂了Cs的Cu-Cs复合催化剂更有利于C H 的形成,可能原因是:Cu-Cs复合催化剂可提供更多的活性
2 4
位点(Cu-Cs复合催化剂更有利于CO等中间体的吸附),且能降低反应的活化能,因此更有利于C H 的形成;
2 4
(3)从物质转化与资源综合利用角度分析,本工艺中CO 的捕集和资源再利用技术的优点是:有利于将CO 转
2 2
化为更有价值的C H 等产品;使用风能、太阳能有利于减排CO ;能实现能量的储存和转化,调控电力过剩或
2 4 2
电力不足等。
【问题解决2】
1.(2024·江苏省南通市三模)下列关于反应2SO (g)+O(g) 2SO (g) ∆H<0的说法正确的是
2 2 3
A.基态V原子核外电子排布为3d34s2
B.反应达到平衡状态时,υ (SO )=2υ (O)
逆 3 正 2
C.使用VO 的目是为了增大SO 的平衡转化率
2 5 2
D.其他条件相同,增大压强,平衡常数增大
【答案】B
【解析】A项,V为第23号元素,基态V原子核外电子排布为1s22s22p63d34s2,不符合题意;B项,反应达
到平衡状态时,υ (SO )=2υ (O),符合题意;C项,催化剂可以增大化学反应速率,不能使平衡移动,不能
逆 3 正 2
改变平衡转化率,不符合题意;D项,化学平衡常数只受温度的影响,温度改变,平衡常数才会改变,不符合
题意。
2.(2024·镇江市丹阳市上学期开学考)科学家利用CO 在Ru(与Fe同族)基催化剂上加氢成功制得甲酸,
2
其过程如下图所示。
①CO 与Ru-H通过加成形成中间体X,画出中间体X的结构式:___________________。
2
②反应过程中加入NaOH或NH 的目的是_________________________________________________。
3微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
【答案】① ②降低HCOOH浓度,CO+H HCOOH正向进行程度增大
2 2
【解析】①氧化碳与Ru—H发生加成反应生成 HCOORu,则X的结构式为 ,故答案为:
;②二氧化碳与氢气反应生成甲酸的方程式为 CO +H HCOOH,反应过程中加入氢氧化钠
2 2
或氨气可以将甲酸转化为HCOO—离子,使反应正向进行程度增大,故答案为:降低HCOOH浓度,CO +H
2 2
HCOOH正向进行程度增大。
化学平衡状态与平衡移动
1.平衡状态判断:
根据“变量不变”判断。
2.平衡移动判断:
根据反应条件结合移动原理,判断平衡移动方向及其量的改变。
考点精练
1.(2024·南通市海安市高三上学期开学考)在新型催化剂RuO 作用下,O 氧化HCl可获得Cl:
2 2 2
4HCl(g)+O(g) 2Cl(g)+2HO(g)。对于该反应下列说法正确的是
2 2 2
A.该反应∆H>0 B.RuO 的使用能降低该反应的焓变
2
C.该条件下,氧化性:O>Cl D.反应的平衡常数为K=
2 2
【答案】C
【解析】A项,该反应是熵减反应,该反应在一定条件下能发生,说明该反应的焓变小于0,错误;B项,
催化剂可以加快反应速率,但不能改变反应的焓变,错误;C项,O 氧化HCl得到Cl,氧化剂的氧化性强于氧
2 2
化产物,则该条件下,氧化性:O>Cl,正确;D项,反应中各物种状态均为气态,平衡常数K=,错误。
2 2
2.(2024·泰州市下学期一模)利用碳氮化反应TiO(s)+2Cl(g)+2C(s) TiCl (g)+2CO(g) ∆H=
2 2 4
-51 kJ·mol-1,可将TiO 转化为TiCl ,再进一步还原得到金属钛,下列说法正确的是
2 4
A.碳氯化反应在高温下不能自发进行
B.加压、降温均可增大生成TiCl 的速率
4
的
C.反应中每消耗1 mol TiO,转移电子 数目约为4×6.02×1023
2
D.将TiO(s)与C(s)粉碎并混合均匀后反应可提高Cl 的平衡转化率
2 2
【答案】C
【解析】A项,碳氯化反应是放热反应,熵增的反应,根据 ,则该反应在任意温度下能
自发进行,错误;B项,加压,速率增大;降温,速率降低,因此不能增大生成TiCl 的速率,错误;C项,根
4
据方程式分析,消耗 1 mol TiO ,转移 4 mol 电子,反应中每消耗 1 mol TiO ,转移电子的数目约为
2 2
4×6.02×1023,正确;D项,将TiO(s)与C(s)粉碎并混合均匀后反应可提高Cl 的反应速率,是由于增大接触面
2 2
积,但不能提高平衡转化率,错误。
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找3.(2024·无锡上学期期中)CO 氧化乙苯脱氢制苯乙烯的反应方程式是: (g)+
2
CO(g) (g)+HO(g)+CO(g),其反应历程如图所示。下列有关说法正确的是
2 2
A.该反应的∆S<0
B.该反应的平衡常数表达式为K=(C H-表示苯基)
6 5
C.催化剂表面酸性越强,苯乙烯的产率越高
D.过程③可能生成副产物
【答案】D
【解析】A项,由题干反应方程式可知,该反应正反应是一个气体体积增大的方向,故该反应的∆S>0,错
误;B项,由题干反应方程式可知,产物中HO为气态,故该反应的平衡常数表达式为K=(C H -表示苯基),
2 6 5
错误;C项,根据反应历程可知,催化剂表面需要活化吸附 ,该微粒带负电荷,如果催化剂表面酸性较强,
则带负电荷的氢氧根离子较少,有利于 的吸附,且酸性物质不会和二氧化碳反应,从而提高了乙苯的转化率,
但酸性太强,催化剂表面吸附大量的带正电的H+,导致 的吸附能力减弱,不利乙苯转化率的提
高,故并不是催化剂表面酸性越强,苯乙烯的产率越高,错误;D项,由题干反应历程图示信息可知,过程③
中存在 和 中间体微粒,故可能生成副产物 ,正确。
4.(2023·江苏)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
合成尿素[CO(NH )]是利用CO 的途径之一、尿素合成主要通过下列反应实现:
2 2 2
反应Ⅰ:2NH (g)+CO(g)=NH COONH(l)
3 2 2 4
反应Ⅱ:NH COONH(l)=CO(NH )(l)+HO(l)
2 4 2 2 2
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如图甲所示,反应Ⅰ的ΔH______(填“=0”“>0”或
“<0”)。
②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH CO)NH]和尿素转化
2 2
为氰酸铵(NH OCN)等副反应。尿素生产中实际投入NH 和CO 的物质的量之比为n(NH )∶n(CO)=4∶1,其
4 3 2 3 2
实际投料比值远大于理论值的原因是_______________________________________________________________。
【答案】①<0 ②适当抑制副反应的发生,尿素中氮碳比小于副产物中缩二脲的氮碳比,氨气与二氧化碳
的投料比越大,二氧化碳转化率越高
【解析】①由图甲可知升高温度反应Ⅰ的lgK减小,说明温度升高平衡逆向移动,故正反应为放热反应,微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
其ΔH<0。
【问题解决3】
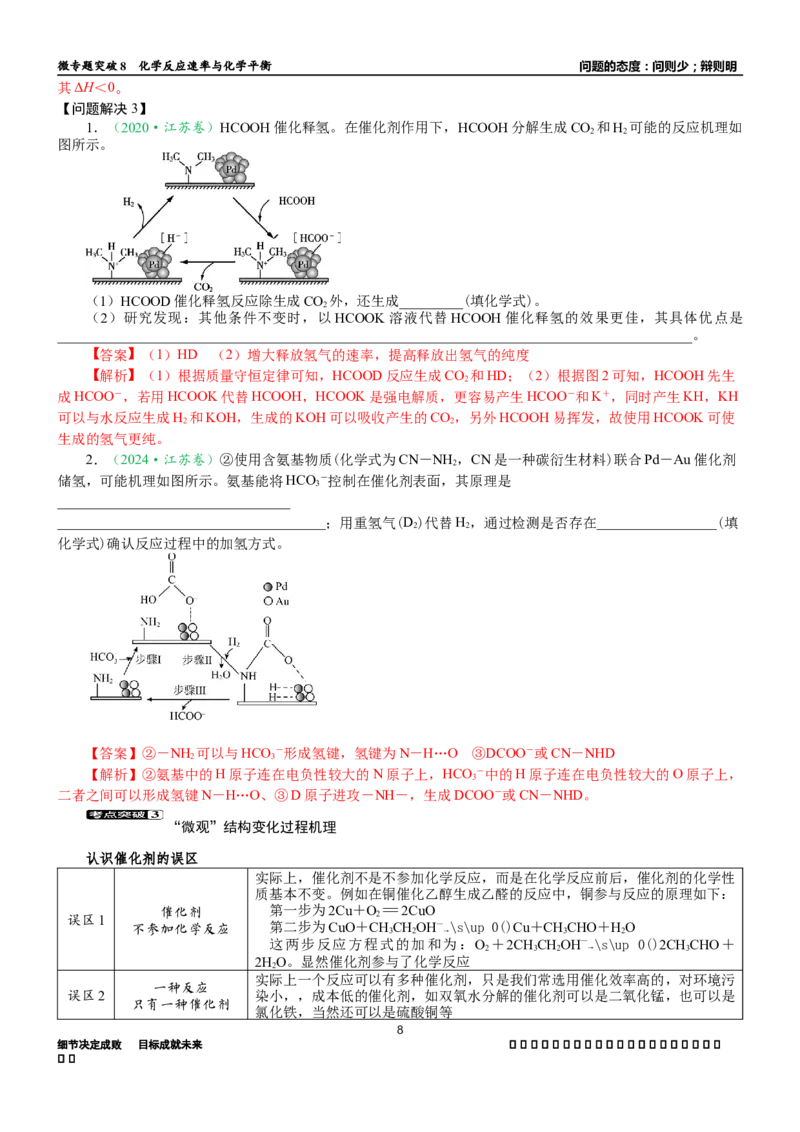
1.(2020·江苏卷)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO 和H 可能的反应机理如
2 2
图所示。
(1)HCOOD催化释氢反应除生成CO 外,还生成_________(填化学式)。
2
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是
__________________________________________________________________________________________。
【答案】(1)HD (2)增大释放氢气的速率,提高释放出氢气的纯度
【解析】(1)根据质量守恒定律可知,HCOOD反应生成CO 和HD;(2)根据图2可知,HCOOH先生
2
成HCOO-,若用HCOOK代替HCOOH,HCOOK是强电解质,更容易产生HCOO-和K+,同时产生KH,KH
可以与水反应生成H 和KOH,生成的KOH可以吸收产生的CO,另外HCOOH易挥发,故使用HCOOK可使
2 2
生成的氢气更纯。
2.(2024·江苏卷)②使用含氨基物质(化学式为CN-NH ,CN是一种碳衍生材料)联合Pd-Au催化剂
2
储氢,可能机理如图所示。氨基能将HCO -控制在催化剂表面,其原理是
3
_________________________________
______________________________________;用重氢气(D)代替H,通过检测是否存在_________________(填
2 2
化学式)确认反应过程中的加氢方式。
【答案】②-NH 可以与HCO -形成氢键,氢键为N-H…O ③DCOO-或CN-NHD
2 3
【解析】②氨基中的H原子连在电负性较大的N原子上,HCO -中的H原子连在电负性较大的O原子上,
3
二者之间可以形成氢键N-H…O、③D原子进攻-NH-,生成DCOO-或CN-NHD。
“微观”结构变化过程机理
认识催化剂的误区
实际上,催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化学性
质基本不变。例如在铜催化乙醇生成乙醛的反应中,铜参与反应的原理如下:
催化剂 第一步为2Cu+O=2CuO
误区1 2
不参加化学反应 第二步为CuO+CHCHOH— \s\up 0()Cu+CHCHO+HO
3 2 → 3 2
这两步反应方程式的加和为:O +2CHCHOH— \s\up 0()2CHCHO+
2 3 2 → 3
2HO。显然催化剂参与了化学反应
2
实际上一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环境污
一种反应
误区2 染小,,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也可以是
只有一种催化剂
氯化铁,当然还可以是硫酸铜等
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找催化剂都是 实际上,催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负催化
误区3
加快化学反应速率 剂是减慢化学反应速率的
实际上,催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂的表
催化剂的效率
误区4 面积,催化剂的浓度大小必然影响化学反应速率。比如用酵母催化剂做食品,
与催化剂的量无关
酵母量大自然面就膨大快。催化剂的用量是会改变催化效率的
考点精练
1.(2022·江苏卷)随着反应进行,FeCO 迅速转化为活性Fe O ,活性Fe O 是HCO -转化为HCOO
3 3 4-x 3 4-x 3
-的催化剂,其可能反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ可描述为
_________________________________________________________________________________________________
_______________________________________________________________________________________________。
【答案】H的电负性大于Fe,小于O,在活性Fe O 表面,H 断裂为H原子,一个吸附在催化剂的铁离
3 4-x 2
子上,略带负电,一个吸附在催化剂的氧离子上,略带正电,前者与HC 中略带正电的碳结合,后者与HC
O−
3
中略带负电的羟基氧结合生成HO,HCO -转化为HCOO-
O− 2 3
3
2.NaBH 是一种应用广泛的强还原剂,在热水中生成硼酸钠和氢气,反应如下:
4
NaBH +4HO=NaB(OH) +4H↑。NaBH 在催化剂作用下与水反应获得H 的微观过程如题图所示,若将
4 2 4 2 4 2
HO中的H全部用D(重氢原子)代替,请根据下图结合相关方程式描述生成 D 气体这一步的微观过程:
2 2
_____________
_________________________________________________________________________________________________
。
【答案】BH +HO— \s\up 0()H ,HBO+HO— \s\up 0()H ,2HO— \s\up 0()H ,DO代替HO时生
3 2 → 2 3 2 → 2 2 → 2 2 2
成的氢气反应为2DO— \s\up 0()D 有D 生成
2 → 2 2
【问题解决4】
1.(2024·南通市海安市)捕集并转化CO 可以有效实现碳达峰、碳中和。
2
Ⅰ.工业上利用两种温室气体CH 和CO 催化重整制取H 和CO,主要反应为
4 2 2
反应①:CH(g)+CO(g) 2CO(g)+2H(g) ∆H=+247.4 kJ·mol-1
4 2 2 1
过程中还发生三个副反应:
反应②:CO(g)+H(g) CO(g)+HO(g) ∆H=+41.2 kJ·mol-1
2 2 2 2
反应③:2CO(g) CO(g)+C(s) ∆H=-171.0 kJ·mol-1
2 3
反应④:CH(g) 2H(g)+C(s) ∆H
4 2 4
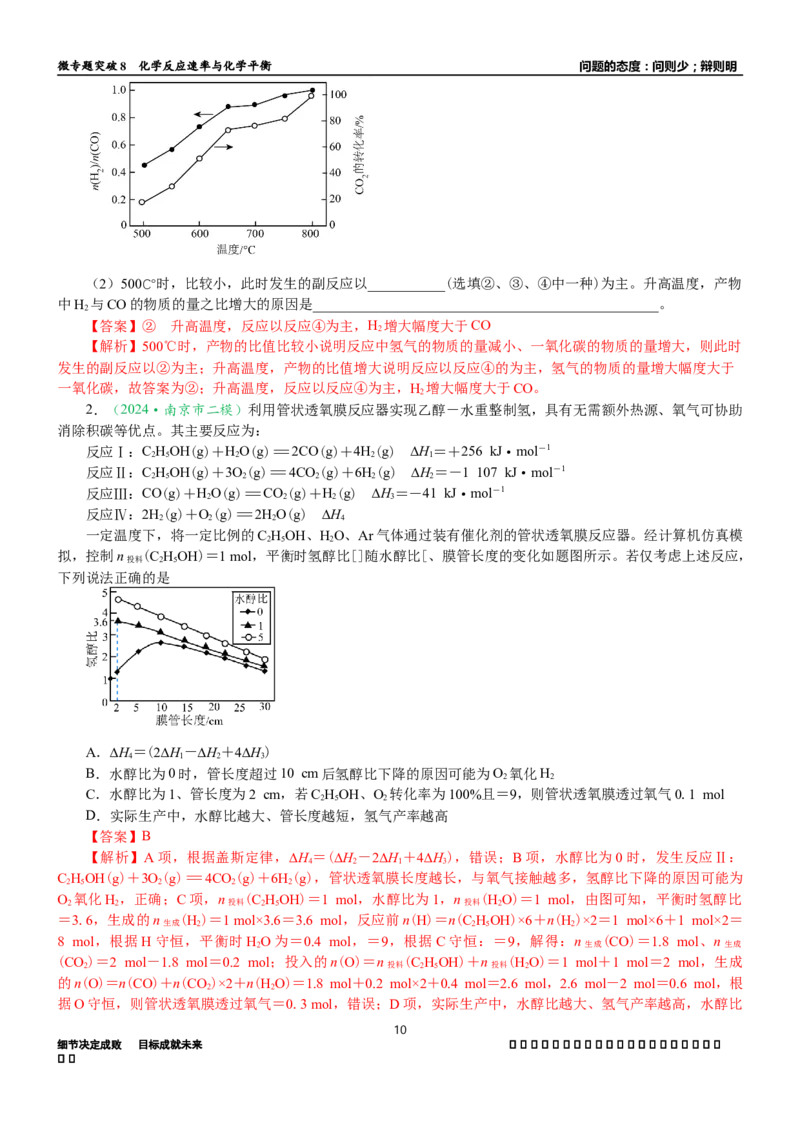
将CH 与CO(体积比为1∶1)的混合气体以一定流速通过催化剂,产物中H 与CO的物质的量之比、CO
4 2 2 2
的转化率与温度的关系如图所示:微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
(2)500℃时,比较小,此时发生的副反应以___________(选填②、③、④中一种)为主。升高温度,产物
中H 与CO的物质的量之比增大的原因是_________________________________________________。
2
【答案】② 升高温度,反应以反应④为主,H 增大幅度大于CO
2
【解析】500℃时,产物的比值比较小说明反应中氢气的物质的量减小、一氧化碳的物质的量增大,则此时
发生的副反应以②为主;升高温度,产物的比值增大说明反应以反应④的为主,氢气的物质的量增大幅度大于
一氧化碳,故答案为②;升高温度,反应以反应④为主,H 增大幅度大于CO。
2
2.(2024·南京市二模)利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助
消除积碳等优点。其主要反应为:
反应Ⅰ:C HOH(g)+HO(g)=2CO(g)+4H(g) ∆H=+256 kJ·mol-1
2 5 2 2 1
反应Ⅱ:C HOH(g)+3O(g)=4CO(g)+6H(g) ∆H=-1 107 kJ·mol-1
2 5 2 2 2 2
反应Ⅲ:CO(g)+HO(g)=CO(g)+H(g) ∆H=-41 kJ·mol-1
2 2 2 3
反应Ⅳ:2H(g)+O(g)=2HO(g) ∆H
2 2 2 4
一定温度下,将一定比例的C HOH、HO、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模
2 5 2
拟,控制n (C HOH)=1 mol,平衡时氢醇比[]随水醇比[、膜管长度的变化如题图所示。若仅考虑上述反应,
投料 2 5
下列说法正确的是
A.∆H=(2∆H-∆H+4∆H)
4 1 2 3
B.水醇比为0时,管长度超过10 cm后氢醇比下降的原因可能为O 氧化H
2 2
C.水醇比为1、管长度为2 cm,若C HOH、O 转化率为100%且=9,则管状透氧膜透过氧气0.1 mol
2 5 2
D.实际生产中,水醇比越大、管长度越短,氢气产率越高
【答案】B
【解析】A项,根据盖斯定律,∆H =(∆H -2∆H +4∆H),错误;B项,水醇比为0时,发生反应Ⅱ:
4 2 1 3
C HOH(g)+3O(g)=4CO(g)+6H(g),管状透氧膜长度越长,与氧气接触越多,氢醇比下降的原因可能为
2 5 2 2 2
O 氧化H ,正确;C项,n (C HOH)=1 mol,水醇比为1,n (HO)=1 mol,由图可知,平衡时氢醇比
2 2 投料 2 5 投料 2
=3.6,生成的n (H)=1 mol×3.6=3.6 mol,反应前n(H)=n(C HOH)×6+n(H)×2=1 mol×6+1 mol×2=
生成 2 2 5 2
8 mol,根据H守恒,平衡时HO为=0.4 mol,=9,根据C守恒:=9,解得:n (CO)=1.8 mol、n
2 生成 生成
(CO)=2 mol-1.8 mol=0.2 mol;投入的n(O)=n (C HOH)+n (HO)=1 mol+1 mol=2 mol,生成
2 投料 2 5 投料 2
的n(O)=n(CO)+n(CO)×2+n(HO)=1.8 mol+0.2 mol×2+0.4 mol=2.6 mol,2.6 mol-2 mol=0.6 mol,根
2 2
据O守恒,则管状透氧膜透过氧气=0.3 mol,错误;D项,实际生产中,水醇比越大、氢气产率越高,水醇比
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找为0时,管长度在10 cm左右氢气产率最高,小于10 cm或大于10 cm均氢气产率最低,错误。
速率与平衡图象
1.化学反应速率与平衡图像中信息的处理方法
2.化学平衡移动的定性分析与定量计算
3.化工生产中最佳反应条件的选择
化工生产中反应条件的选择,除应考虑反应速率、反应限度等反应本身的因素外,还必须考虑生产成本,
如动力设备要求、原料和能量的充分利用等。
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
从化学反应限度分析 既要注意外界条件对速率和平衡影响的一致性,又要注意二者影响的矛盾性
从原料的利用率分析 增加易得廉价原料,提高难得高价原料的利用率,从而降低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意温度对催化剂活性的限制
4.创新速率、平衡图象题
(1)关注题中物质的选择性、平衡转化率与实际转化率,注意图中双坐标的含义。
(2)有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
①如果主反应的生成物又与主反应的某一反应物发生另一个可逆反应,那么该反应物的平衡转化率就会增
大。
②在一定温度下,特定起始浓度的混合体系,其多重平衡选择性为定值,催化剂不能提高某一物质的平衡
转化率。
③如果在同一条件下,两种物质同时可以发生几个可逆反应,那么催化剂的选用就可以使其中某一反应的
选择性提高。
④多重平衡体系中,随着温度的升高,如果两种物质的选择性之和等于100%,那么二者的选择性变化曲线
呈镜像对称(如2022·江苏卷13题)。
(2022·江苏卷)乙醇水催化重整可获得H 。其主要反应为C HOH(g)+3HO(g)=2CO(g)+6H(g)
2 2 5 2 2 2
ΔH=173.3 kJ·mol-1,CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2 kJ·mol-1,在 1.0×105 Pa、n
2 2 2 始
(C HOH)∶n (HO)=1∶3时,若仅考虑上述反应,平衡时CO 和CO的选择性及H 的产率随温度的变化如
2 5 始 2 2 2
图所示。微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
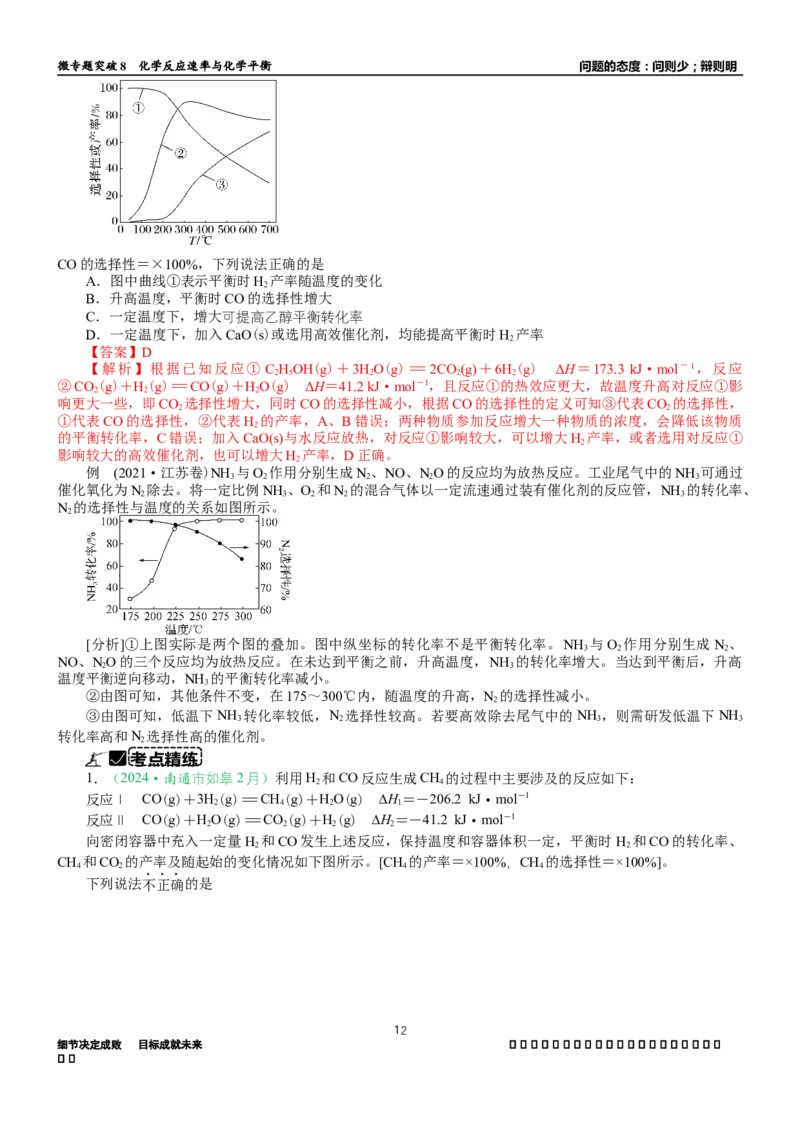
CO的选择性=×100%,下列说法正确的是
A.图中曲线①表示平衡时H 产率随温度的变化
2
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大可提高乙醇平衡转化率
D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H 产率
2
【答案】D
【解析】根据已知反应① C HOH(g)+3HO(g)=2CO(g)+6H(g) ΔH=173.3 kJ·mol-1,反应
2 5 2 2 2
②CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2 kJ·mol-1,且反应①的热效应更大,故温度升高对反应①影
2 2 2
响更大一些,即CO 选择性增大,同时CO的选择性减小,根据CO的选择性的定义可知③代表CO 的选择性,
2 2
①代表CO的选择性,②代表H 的产率,A、B错误;两种物质参加反应增大一种物质的浓度,会降低该物质
2
的平衡转化率,C错误;加入CaO(s)与水反应放热,对反应①影响较大,可以增大H 产率,或者选用对反应①
2
影响较大的高效催化剂,也可以增大H 产率,D正确。
2
例 (2021·江苏卷)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可通过
3 2 2 2 3
催化氧化为N 除去。将一定比例NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,NH 的转化率、
2 3 2 2 3
N 的选择性与温度的关系如图所示。
2
[分析]①上图实际是两个图的叠加。图中纵坐标的转化率不是平衡转化率。NH 与O 作用分别生成N 、
3 2 2
NO、NO的三个反应均为放热反应。在未达到平衡之前,升高温度,NH 的转化率增大。当达到平衡后,升高
2 3
温度平衡逆向移动,NH 的平衡转化率减小。
3
②由图可知,其他条件不变,在175~300℃内,随温度的升高,N 的选择性减小。
2
③由图可知,低温下NH 转化率较低,N 选择性较高。若要高效除去尾气中的NH ,则需研发低温下NH
3 2 3 3
转化率高和N 选择性高的催化剂。
2
考点精练
1.(2024·南通市如皋2月)利用H 和CO反应生成CH 的过程中主要涉及的反应如下:
2 4
反应Ⅰ CO(g)+3H(g)=CH(g)+HO(g) ∆H=-206.2 kJ·mol-1
2 4 2 1
反应Ⅱ CO(g)+HO(g)=CO(g)+H(g) ∆H=-41.2 kJ·mol-1
2 2 2 2
向密闭容器中充入一定量H 和CO发生上述反应,保持温度和容器体积一定,平衡时 H 和CO的转化率、
2 2
CH 和CO 的产率及随起始的变化情况如下图所示。[CH 的产率=×100%,CH 的选择性=×100%]。
4 2 4 4
下列说法不正确的是
12
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
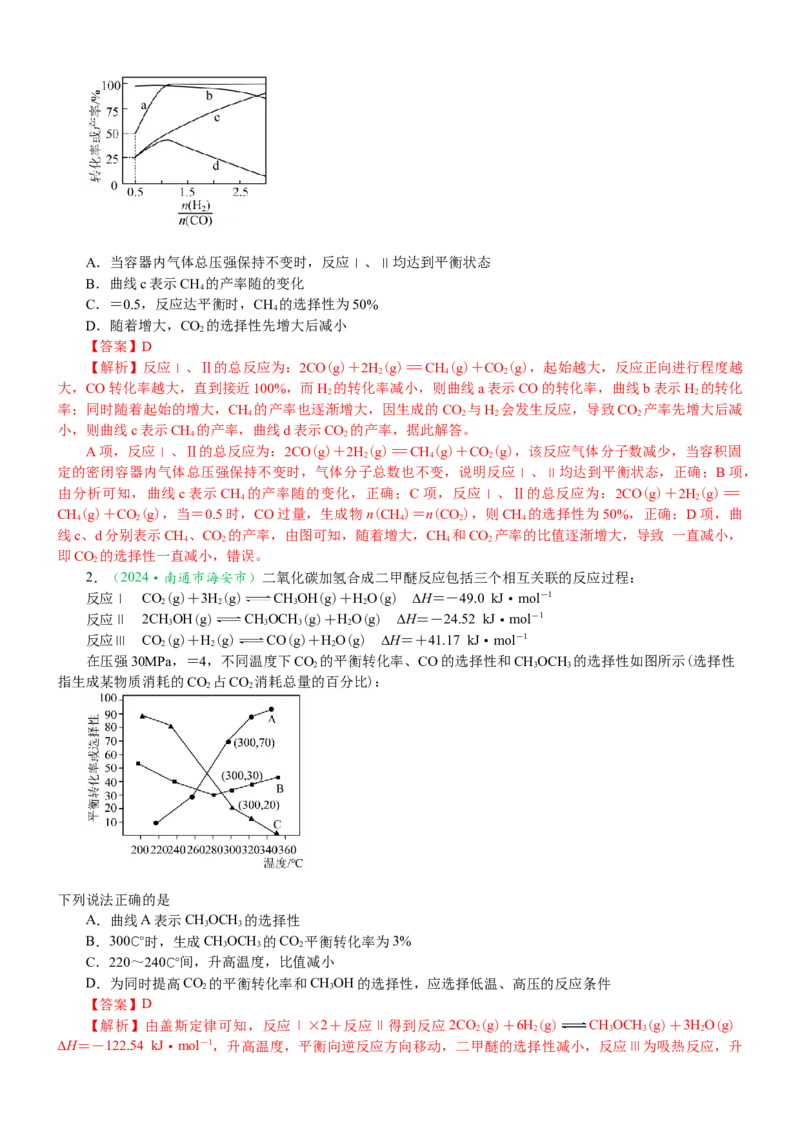
找找A.当容器内气体总压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态
B.曲线c表示CH 的产率随的变化
4
C.=0.5,反应达平衡时,CH 的选择性为50%
4
D.随着增大,CO 的选择性先增大后减小
2
【答案】D
【解析】反应Ⅰ、Ⅱ的总反应为:2CO(g)+2H(g)=CH(g)+CO(g),起始越大,反应正向进行程度越
2 4 2
大,CO转化率越大,直到接近100%,而H 的转化率减小,则曲线a表示CO的转化率,曲线b表示H 的转化
2 2
率;同时随着起始的增大,CH 的产率也逐渐增大,因生成的CO 与H 会发生反应,导致CO 产率先增大后减
4 2 2 2
小,则曲线c表示CH 的产率,曲线d表示CO 的产率,据此解答。
4 2
A项,反应Ⅰ、Ⅱ的总反应为:2CO(g)+2H(g)=CH(g)+CO(g),该反应气体分子数减少,当容积固
2 4 2
定的密闭容器内气体总压强保持不变时,气体分子总数也不变,说明反应Ⅰ、Ⅱ均达到平衡状态,正确;B项,
由分析可知,曲线c表示CH 的产率随的变化,正确;C项,反应Ⅰ、Ⅱ的总反应为:2CO(g)+2H(g)=
4 2
CH(g)+CO(g),当=0.5时,CO过量,生成物n(CH)=n(CO),则CH 的选择性为50%,正确;D项,曲
4 2 4 2 4
线c、d分别表示CH 、CO 的产率,由图可知,随着增大,CH 和CO 产率的比值逐渐增大,导致 一直减小,
4 2 4 2
即CO 的选择性一直减小,错误。
2
2.(2024·南通市海安市)二氧化碳加氢合成二甲醚反应包括三个相互关联的反应过程:
反应Ⅰ CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49.0 kJ·mol-1
2 2 3 2
反应Ⅱ 2CHOH(g) CHOCH (g)+HO(g) ∆H=-24.52 kJ·mol-1
3 3 3 2
反应Ⅲ CO(g)+H(g) CO(g)+HO(g) ∆H=+41.17 kJ·mol-1
2 2 2
在压强30MPa,=4,不同温度下CO 的平衡转化率、CO的选择性和CHOCH 的选择性如图所示(选择性
2 3 3
指生成某物质消耗的CO 占CO 消耗总量的百分比):
2 2
下列说法正确的是
A.曲线A表示CHOCH 的选择性
3 3
B.300℃时,生成CHOCH 的CO 平衡转化率为3%
3 3 2
C.220~240℃间,升高温度,比值减小
D.为同时提高CO 的平衡转化率和CHOH的选择性,应选择低温、高压的反应条件
2 3
【答案】D
【解析】由盖斯定律可知,反应Ⅰ×2+反应Ⅱ得到反应2CO(g)+6H(g) CHOCH (g)+3HO(g)
2 2 3 3 2
∆H=-122.54 kJ·mol-1,升高温度,平衡向逆反应方向移动,二甲醚的选择性减小,反应Ⅲ为吸热反应,升微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
高温度,平衡向正反应方向移动,一氧化碳的选择性增大,则曲线 A表示一氧化碳的选择性、曲线B表示二氧
化碳的转化率、曲线C表示二甲醚的选择性。
A项,由分析可知,曲线C表示二甲醚的选择性,错误;B项,由图可知,300℃平衡时,二氧化碳的转化
率为30%、二甲醚的选择性为20%,设二氧化碳的起始物质的量为1 mol,则反应生成二甲醚消耗二氧化碳的
物质的量为1 mol×30%×20%×2=0.12 mol,则生成二甲醚的二氧化碳的转化率为×100%=12%,错误;C
项,反应Ⅰ为放热反应、反应Ⅲ为吸热反应,220~240℃间,升高温度,反应Ⅰ的平衡向正反应方向移动,反
应生成二氧化碳和氢气的物质的量比为1∶3,反应Ⅲ的平衡向正反应方向移动,消耗二氧化碳和氢气的物质的
量比为1∶1,则比值增大,错误;D项,反应Ⅰ为气体体积减小的放热反应,反应Ⅲ为气体体积不变吸热反应,
增大压强,反应Ⅰ的平衡向正反应方向移动、反应Ⅲ的平衡不移动,则二氧化碳的转化率和甲醇的选择性都增
大,降低温度,反应Ⅰ的平衡向正反应方向移动、反应Ⅲ的平衡向逆反应方向移动,则二氧化碳的转化率和甲
醇的选择性都增大,所以为同时提高二氧化碳的平衡转化率和甲醇的选择性,应选择低温、高压的反应条件,
正确。
成功体验
1.(2023·苏州上学期期末)压强0.7MPa、温度370℃,化合物WS 催化反应HS+CHOH=HO+
2 2 3 2
CHSH用于制备甲硫醇。下列说法正确的是
3
A.该反应的平衡常数K=
B.过程I存在反应物吸附,S-H键没有断裂
C.图中“ ”代表S原子
D.若用CHOD代替CHOH,则生成CHSD
3 3 3
【答案】B
【解析】A项,反应在370℃下进行,水为气态,所以该反应的平衡常数为K=,错误;B项,由图可知,
过程I中S-H键没有断裂,正确;C项,W为第六周期过渡金属元素,可以与O、S形成化学键,所以图中“
”代表W原子,错误;D项,根据反应过程可知,CHOD代替CHOH,仍然生成CHSH,错误。
3 3 3
2.(2024·南通市海门市第一次调研)周期表中VIA族元素及其化合物应用广泛。186O、187O、188O是氧元素
3种核素,可以形成多种重要的化合物。亚硫酰氯(SOCl )为黄色液体,其结构式为( ),遇水发生
2
的
水解。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],过二硫酸铵与双氧水中都含有
2 4 4 2 4 4 2 2 8
过氧键(-O-O-)。硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol
2 2 3
-1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列有关NO (g)+SO (g)=SO (g)+NO(g) ∆H
2 3 2 2 3
=+41.8 kJ·mol-1,下列说法正确的
14
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.该反应中反应物的总能量低于生成物的总能量
B.反应达平衡后,分离出少量SO ,正反应速率加快
3
C.其他条件不变,平衡后继续充入NO ,平衡常数将减小
2
D.该反应中消耗22.4 LNO ,转移电子的数目为2×6.02×1023
2
【答案】A
【解析】A项,根据焓变可知,该反应为吸热反应,则反应中反应物的总能量低于生成物的总能量,正确;
B项,反应达平衡后,分离出少量SO ,平衡正向移动,反应物浓度开始减小,正反应速率开始减慢,错误;C
3
项,其他条件不变,平衡后继续充入NO ,平衡正向移动,但平衡常数不变,错误;D项,NO 的状态未知,
2 2
无法计算其物质的量,无法计算转移电子的数目,错误。
3.(2024·南京市二模)制备光电子功能材料ZnS可通过自发反应ZnO(s)+HS(g) ZnS(s)+HO(g)
2 2
∆H>0。下列说法正确的是
A.该反应的ΔS<0
B.其他条件相同,缩小容器体积,达到新平衡时减小
C.其他条件相同,升高体系温度,HS的平衡转化率增大
2
D.其他条件相同,使用催化剂加快正反应速率,减慢逆反应速率
【答案】C
【解析】A项,反应ZnO(s)+HS(g) ZnS(s)+HO(g)能自发进行,其∆H>0,则ΔS>0,不正确;B
2 2
项,反应前后气体分子数相等,其他条件相同,缩小容器体积,相当于加压,平衡不发生移动,则不变,不正
确;C项,其他条件相同,升高体系温度,由于正反应为吸热反应,则平衡正向移动,HS的平衡转化率增大,
2
正确;D项,其他条件相同,使用催化剂,可降低反应的活化能,加快正反应速率,同时加快逆反应速率,不
正确。
4.(2023·江苏卷)二氧化碳加氢制甲烷过程中的主要反应为
CO(g)+4H(g)=CH(g)+2HO(g) ΔH=-164.7 kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2 kJ·mol-1
2 2 2
在密闭容器中,1.01×105 Pa、n (CO)∶n (H)=1∶4时,CO 平衡转化率、在催化剂作用下反应相
起始 2 起始 2 2
同时间所测得的CO 实际转化率随温度的变化如图所示。CH 的选择性可表示为×100%。下列说法正确的是
2 4
A.反应2CO(g)+2H(g)=CO(g)+CH(g)的焓变ΔH=-205.9 kJ·mol-1
2 2 4
B.CH 的平衡选择性随着温度的升高而增加
4
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450 ℃时,提高的值或增大压强,均能使CO 平衡转化率达到X点的值
2
【答案】D
【解析】A项,由盖斯定律可知反应2CO(g)+2H(g)=CO(g)+CH(g)的焓变ΔH=-2×41.2 kJ·mol-
2 2 4
1-164.7 kJ·mol-1=-247.1 kJ·mol-1,错误;B项,CO(g)+4H(g)=CH(g)+2HO(g)为放热反应,升高
2 2 4 2
温度平衡逆向移动,CH 的含量降低,故CH 的平衡选择性随着温度的升高而降低,错误;C项,由图可知,
4 4
400℃时CO 实际转化率最大,用该催化剂催化CO 反应的最佳温度范围为350~400℃,错误;D项,450℃时,
2 2
提高的值可提高二氧化碳的平衡转化率,增大压强第一个反应平衡正向移动,可提高二氧化碳的平衡转化率,
均能使CO 平衡转化率达到X点的值,正确。
2
4.(2024·淮安市高三上学期开学考)利用H 和CO反应生成CH 的过程中主要涉及的反应如下:
2 4
反应Ⅰ CO(g)+3H(g) CH(g)+HO(g) ∆H=-206.2 kJ·mol-1
2 4 2 1
反应Ⅱ CO(g)+HO(g) CO(g)+H(g) ∆H=-41.2 kJ·mol-1
2 2 2 2微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
[CH 的产率×100% n(CH) ,CH 的选择性×100%]。保持温度一定,在固定容积的密闭容器中进行上述
4 4 生成 4
反应,平衡时CH 和CO 的产率及CO和HO的转化率随的变化情况如图所示。下列说法不正确的是
4 2 2
A.当容器内气体总压不变时,反应Ⅱ达到平衡状态
B.曲线c表示CH 的产率随的变化
4
C.=0.5,反应达平衡时,CH 的选择性为50%
4
D.随着增大,CO 的选择性先增大后减小
2
【答案】D
【解析】A项,反应I是气体体积缩小的反应,当固定密闭容器内总压不变时,反应 I达到平衡状态,则
CO、HO的浓度保持不变,所以反应Ⅱ也达到平衡状态,正确;B项,增大H 的浓度,CO的转化率增大、H
2 2 2
的转化率降低,b表示H 的转化率,CO的转化率为甲烷、二氧化碳产率的和,根据a、c、d起点的数值,可知
2
a表示CO的转化率,根据反应Ⅰ,持续增大H 的浓度,反应1正向移动,甲烷的产率会持续增大,c表示CH
2 4
的产率随的变化;H 的浓度增大到一定程度,反应Ⅱ逆向移动,CO 的产率先增大后减小,d表示CO 的产率,
2 2 2
正确;C项,根据B分析,c表示CH 的产率随的变化,当=0.5时,生成物n(CH)=n(CO),故CH 的选择性
4 4 4
为50%,正确;D项,根据图像,随着的不断增加,甲烷的产率大于CO 的产率,所以CO 选择性先减小,错
2 2
误。
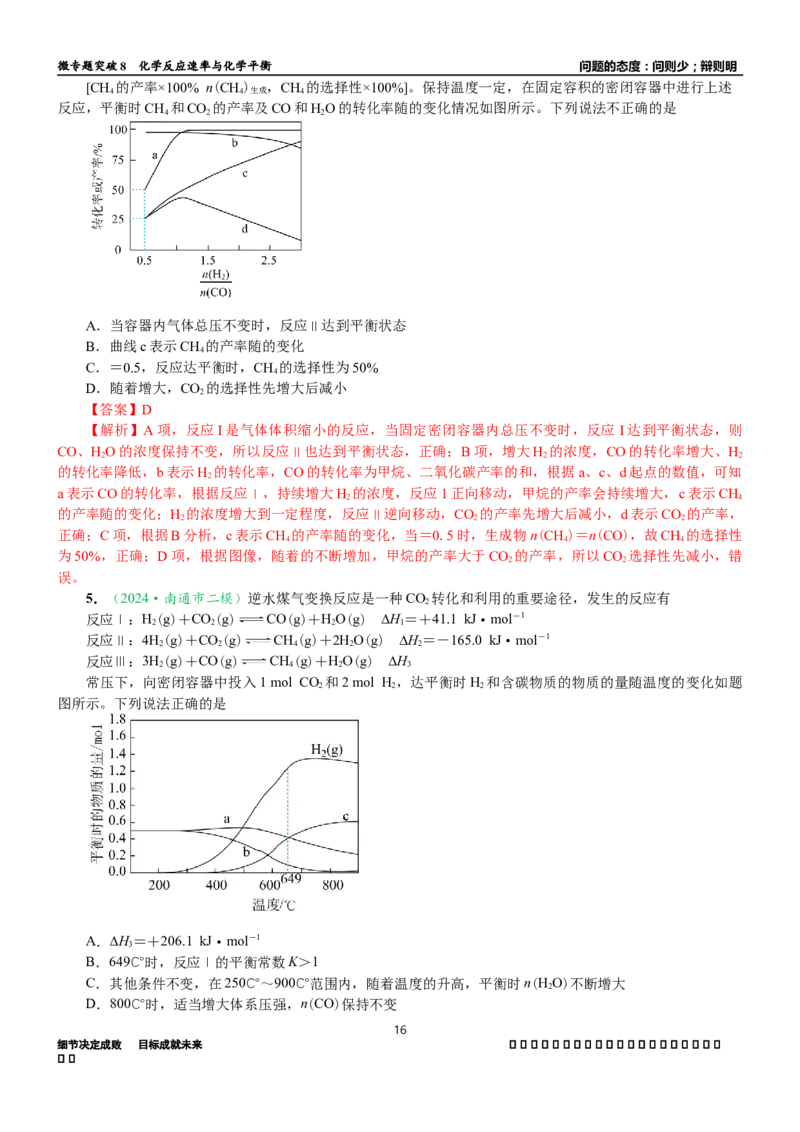
5.(2024·南通市二模)逆水煤气变换反应是一种CO 转化和利用的重要途径,发生的反应有
2
反应Ⅰ:H(g)+CO(g) CO(g)+HO(g) ∆H=+41.1 kJ·mol-1
2 2 2 1
反应Ⅱ:4H(g)+CO(g) CH(g)+2HO(g) ∆H=-165.0 kJ·mol-1
2 2 4 2 2
反应Ⅲ:3H(g)+CO(g) CH(g)+HO(g) ∆H
2 4 2 3
常压下,向密闭容器中投入1 mol CO 和2 mol H ,达平衡时H 和含碳物质的物质的量随温度的变化如题
2 2 2
图所示。下列说法正确的是
A.∆H=+206.1 kJ·mol-1
3
B.649℃时,反应Ⅰ的平衡常数K>1
C.其他条件不变,在250℃~900℃范围内,随着温度的升高,平衡时n(HO)不断增大
2
D.800℃时,适当增大体系压强,n(CO)保持不变
16
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找【答案】D
【解析】A项,根据盖斯定律,反应Ⅲ=反应Ⅱ-反应Ⅰ,则∆H =∆H -∆H =-206.1 kJ·mol-1,错误;
3 2 1
B项,温度升高,反应Ⅰ正向移动,反应Ⅱ和Ⅲ逆向移动,可知c线为CO,a为CO ,b为CH ,649℃时,反
2 4
应平衡时n(H)=1.2 mol,消耗的氢气为2 mol-1.2 mol=0.8 mol,因为还生成CH ,则生成的HO小于0.8
2 4 2
mol,n(CO)=n(CO),反应Ⅰ(H(g)+CO(g) CO(g)+HO(g))平衡常数:K==<=<1,错误;C项,
2 2 2 2
由图像可知,250℃~649℃范围内,随着温度的升高,平衡时n(H)增大,平衡逆向移动,则平衡时n(HO)不
2 2
断减小;649℃~900℃范围内,随着温度的升高,平衡时n(H)减小,平衡正向移动,则平衡时n(HO)不断增
2 2
大,错误;D项,高温时反应I进行程度很大,反应II、III程度很小,CH 含量很少,平衡不受压强影响,适当
4
增大体系压强,n(CO)保持不变,正确。