文档内容
微专题突破8 化学反应速率与化学平衡
生命是一张弓,那弓弦是梦想
目标定位
1.能应用化学反应速率和化学平衡移动原理解释生活、生产中的相关问题。
2.能判断反应的熵变、反应是否达到平衡状态,能计算平衡常数。
3.能根据图示判断反应机理。
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
1.三不混同,二原则
①不要将平衡的移动和速率的变化混同起来。
三个
如平衡正向移动,不一定是正反应速率增加,逆反应速率减小
不要
②不要将平衡的移动与浓度的变化混同起来。如平衡右移生成物的浓度不一定增加
混同
③不要将平衡的移动与反应物的转化率提高等同起来。如平衡右移,反应物的转化率不一定提高
二个 “ ” 可逆反应中反应物的量不为0(确定取值范围)
原则 “ 一” 把生成物的量全部转化为反应物的量(处理等效平衡)
2.反应速率理论在实际生产中的运用
对于受热不稳定性的物质(如HO 、HNO )或受易挥发的物质(如浓硝酸),在采用升高温
温度 2 2 3
度加快反应速率时,要描述为“适当升高温度”
接触面积 不同相之间的反应,若增大接触面积对于固体用粉碎的方法,而液体则用喷洒的方法
接触机会 增大接触机会的措施为直接搅拌、通气体搅拌
催化剂 有机反应、混合气体的反应,常使用催化剂加快反应速率
3.传统速率、平衡图象题的解答方法及思路——一看、二想、三判断
①一看面:即横坐标、纵坐标的量;②二看线:即线的斜率,平与陡的含义,函数的增减
性(先拐 先平:如在转化率——时间图上,先出现拐点的曲线先达到平衡,此时逆向推理
一看图象 可得该变化的温度高、浓度大、压强高);③看点:即起点、转折点、拐点、交叉点;④
四看要不要画辅助线:等温线、等压线等(定一议二:当图象中有三个量时,先确定一个
量不变再讨论另外两个量的关系);⑤看量:定量图象中有关量的多少
联想外界条件改变对化学反应速率和化学平衡的影响,紧扣可逆反应的特征,搞清正反应
二想规律
方向吸热还是放热,体积是增大、减少,还是不变,有无固体参加或生成等
三判断 认准某些关键数据在解题中的特定作用,全面准确地从图中找出直接或隐含的相关信息
3.陌生平衡图像的分析方法
(1)题型特点
化学反应原理综合题在非选择题中的陌生图像打破了传统的速率、平衡图像模式,反应体系不再局限于气
相反应,引入了更多的液相反应,纵坐标和横坐标不再局限于时间、温度、压强、速率、转化率等物理量,而
是引入了更多的变量,如两种物质的物质的量之比、气体分压的负对数等,使得图像更新颖、信息容量更大、
题目难度更大。
(2)复杂(竞争、连续)反应图像的解题流程
①找准竞争(或连续)反应在反应特点方面的异同
第一步 审反应方程式
②分清主、副反应
提取研究状态 ①非平衡状态量,其变化与反应速率有关
第二步
(平衡、非平衡) ②平衡状态量,则与平衡移动有关
依据图中横坐标、纵坐标的内容,找出图中曲线中的“点”、“线”的含义
第三步 析图
和变化趋势,并用平衡移动原理解答具体问题微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
位位位位位
1.(2024·江苏卷)下列说法正确的是
A.豆科植物固氮过程中,固氮酶能提高该反应的活化能
B.C H 与O 反应中,Ag催化能提高生成CHCHO的选择性
2 4 2 3
C.HO 制O 反应中,MnO 能加快化学反应速率
2 2 2 2
D.SO 与O 反应中,VO 能减小该反应的焓变
2 2 2 5
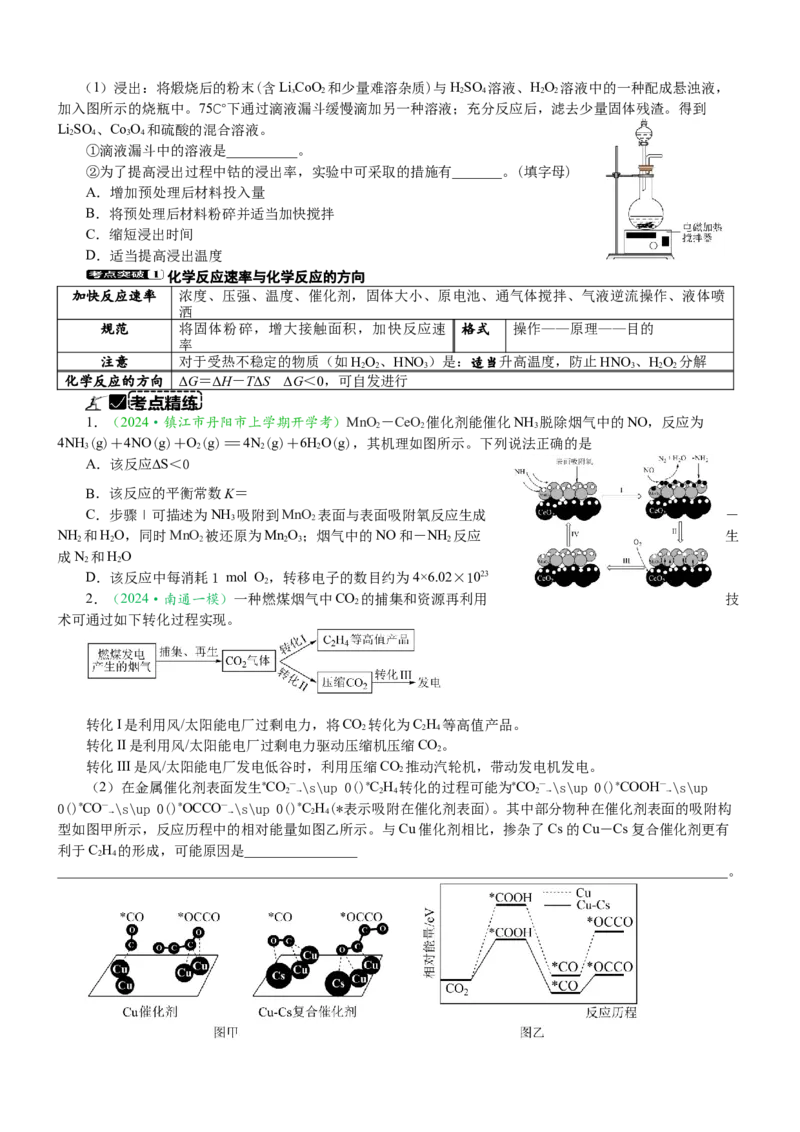
2.(2023·江苏卷)金属硫化物(MS)催化反应CH(g)+2HS(g)=CS(g)+4H(g),既可以除去天然
x y 4 2 2 2
气中的HS,又可以获得H。下列说法正确的是
2 2
A.该反应的ΔS<0
B.该反应的平衡常数K=
C.右图所示的反应机理中,步骤Ⅰ可理解为HS中带部分负电荷的S与催
2
化剂中的M之间发生作用
D.该反应中每消耗1 mol H S,转移电子的数目约为2×6.02×1023
2
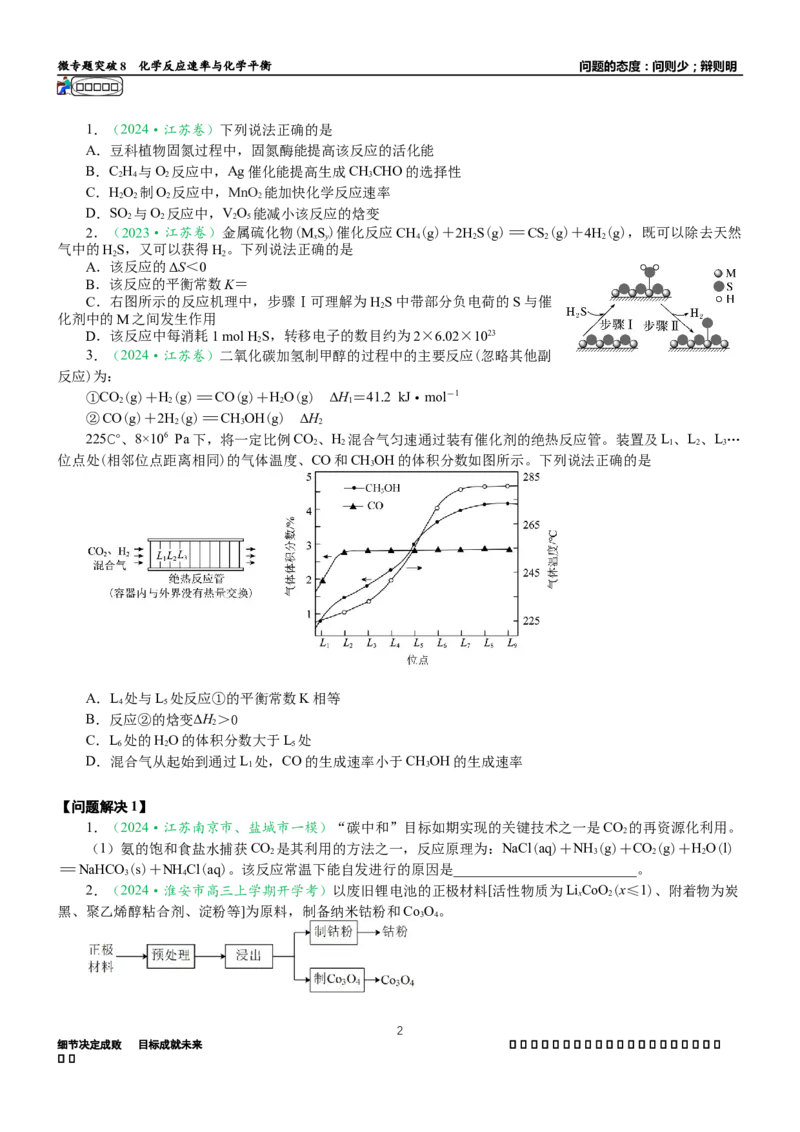
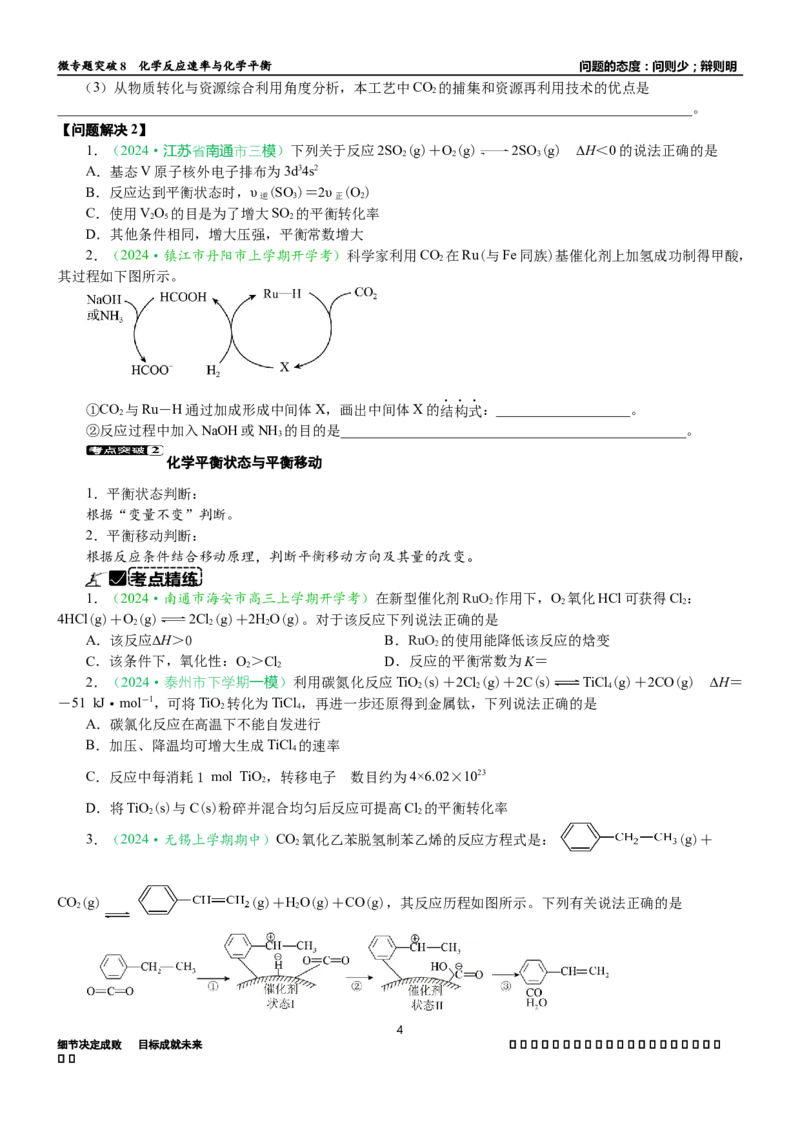
3.(2024·江苏卷)二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副
反应)为:
①CO(g)+H(g)=CO(g)+HO(g) ∆H=41.2 kJ·mol-1
2 2 2 1
②CO(g)+2H(g)=CHOH(g) ∆H
2 3 2
225℃、8×106 Pa下,将一定比例CO、H 混合气匀速通过装有催化剂的绝热反应管。装置及L、L、L…
2 2 1 2 3
位点处(相邻位点距离相同)的气体温度、CO和CHOH的体积分数如图所示。下列说法正确的是
3
A.L 处与L 处反应①的平衡常数K相等
4 5
B.反应②的焓变∆H>0
2
C.L 处的HO的体积分数大于L 处
6 2 5
D.混合气从起始到通过L 处,CO的生成速率小于CHOH的生成速率
1 3
【问题解决1】
1.(2024·江苏南京市、盐城市一模)“碳中和”目标如期实现的关键技术之一是CO 的再资源化利用。
2
(1)氨的饱和食盐水捕获CO 是其利用的方法之一,反应原理为:NaCl(aq)+NH (g)+CO(g)+HO(l)
2 3 2 2
=NaHCO (s)+NH Cl(aq)。该反应常温下能自发进行的原因是__________________________。
3 4
2.(2024·淮安市高三上学期开学考)以废旧锂电池的正极材料[活性物质为LiCoO(x≤1)、附着物为炭
x 2
黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和Co O。
3 4
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找(1)浸出:将煅烧后的粉末(含LiCoO 和少量难溶杂质)与HSO 溶液、HO 溶液中的一种配成悬浊液,
x 2 2 4 2 2
加入图所示的烧瓶中。75℃下通过滴液漏斗缓慢滴加另一种溶液;充分反应后,滤去少量固体残渣。得到
LiSO 、Co O 和硫酸的混合溶液。
2 4 3 4
①滴液漏斗中的溶液是__________。
②为了提高浸出过程中钴的浸出率,实验中可采取的措施有_______。(填字母)
A.增加预处理后材料投入量
B.将预处理后材料粉碎并适当加快搅拌
C.缩短浸出时间
D.适当提高浸出温度
化学反应速率与化学反应的方向
加快反应速率 浓度、压强、温度、催化剂,固体大小、原电池、通气体搅拌、气液逆流操作、液体喷
洒
规范 将固体粉碎,增大接触面积,加快反应速 格式 操作——原理——目的
率
注意 对于受热不稳定的物质(如HO、HNO)是:适当升高温度,防止HNO、HO 分解
2 2 3 3 2 2
化学反应的方向 ΔG=ΔH-TΔS ΔG<0,可自发进行
考点精练
1.(2024·镇江市丹阳市上学期开学考)MnO -CeO 催化剂能催化NH 脱除烟气中的NO,反应为
2 2 3
4NH (g)+4NO(g)+O(g)=4N(g)+6HO(g),其机理如图所示。下列说法正确的是
3 2 2 2
A.该反应∆S<0
B.该反应的平衡常数K=
C.步骤Ⅰ可描述为NH 吸附到MnO 表面与表面吸附氧反应生成 -
3 2
NH 和HO,同时MnO 被还原为MnO;烟气中的NO和-NH 反应 生
2 2 2 2 3 2
成N 和HO
2 2
D.该反应中每消耗1 mol O,转移电子的数目约为4×6.02×1023
2
2.(2024·南通一模)一种燃煤烟气中CO 的捕集和资源再利用 技
2
术可通过如下转化过程实现。
转化I是利用风/太阳能电厂过剩电力,将CO 转化为C H 等高值产品。
2 2 4
转化II是利用风/太阳能电厂过剩电力驱动压缩机压缩CO。
2
转化III是风/太阳能电厂发电低谷时,利用压缩CO 推动汽轮机,带动发电机发电。
2
(2)在金属催化剂表面发生*CO— \s\up 0()*C H 转化的过程可能为*CO— \s\up 0()*COOH— \s\up
2 → 2 4 2 → →
0()*CO— \s\up 0()*OCCO— \s\up 0()*C H(*表示吸附在催化剂表面)。其中部分物种在催化剂表面的吸附构
→ → 2 4
型如图甲所示,反应历程中的相对能量如图乙所示。与Cu催化剂相比,掺杂了Cs的Cu-Cs复合催化剂更有
利于C H 的形成,可能原因是________________
2 4
_______________________________________________________________________________________________。微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
(3)从物质转化与资源综合利用角度分析,本工艺中CO 的捕集和资源再利用技术的优点是
2
__________________________________________________________________________________________。
【问题解决2】
1.(2024·江苏省南通市三模)下列关于反应2SO (g)+O(g) 2SO (g) ∆H<0的说法正确的是
2 2 3
A.基态V原子核外电子排布为3d34s2
B.反应达到平衡状态时,υ (SO )=2υ (O)
逆 3 正 2
C.使用VO 的目是为了增大SO 的平衡转化率
2 5 2
D.其他条件相同,增大压强,平衡常数增大
2.(2024·镇江市丹阳市上学期开学考)科学家利用CO 在Ru(与Fe同族)基催化剂上加氢成功制得甲酸,
2
其过程如下图所示。
①CO 与Ru-H通过加成形成中间体X,画出中间体X的结构式:___________________。
2
②反应过程中加入NaOH或NH 的目的是_________________________________________________。
3
化学平衡状态与平衡移动
1.平衡状态判断:
根据“变量不变”判断。
2.平衡移动判断:
根据反应条件结合移动原理,判断平衡移动方向及其量的改变。
考点精练
1.(2024·南通市海安市高三上学期开学考)在新型催化剂RuO 作用下,O 氧化HCl可获得Cl:
2 2 2
4HCl(g)+O(g) 2Cl(g)+2HO(g)。对于该反应下列说法正确的是
2 2 2
A.该反应∆H>0 B.RuO 的使用能降低该反应的焓变
2
C.该条件下,氧化性:O>Cl D.反应的平衡常数为K=
2 2
2.(2024·泰州市下学期一模)利用碳氮化反应TiO(s)+2Cl(g)+2C(s) TiCl (g)+2CO(g) ∆H=
2 2 4
-51 kJ·mol-1,可将TiO 转化为TiCl ,再进一步还原得到金属钛,下列说法正确的是
2 4
A.碳氯化反应在高温下不能自发进行
B.加压、降温均可增大生成TiCl 的速率
4
的
C.反应中每消耗1 mol TiO,转移电子 数目约为4×6.02×1023
2
D.将TiO(s)与C(s)粉碎并混合均匀后反应可提高Cl 的平衡转化率
2 2
3.(2024·无锡上学期期中)CO 氧化乙苯脱氢制苯乙烯的反应方程式是: (g)+
2
CO(g) (g)+HO(g)+CO(g),其反应历程如图所示。下列有关说法正确的是
2 2
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.该反应的∆S<0
B.该反应的平衡常数表达式为K=(C H-表示苯基)
6 5
C.催化剂表面酸性越强,苯乙烯的产率越高
D.过程③可能生成副产物
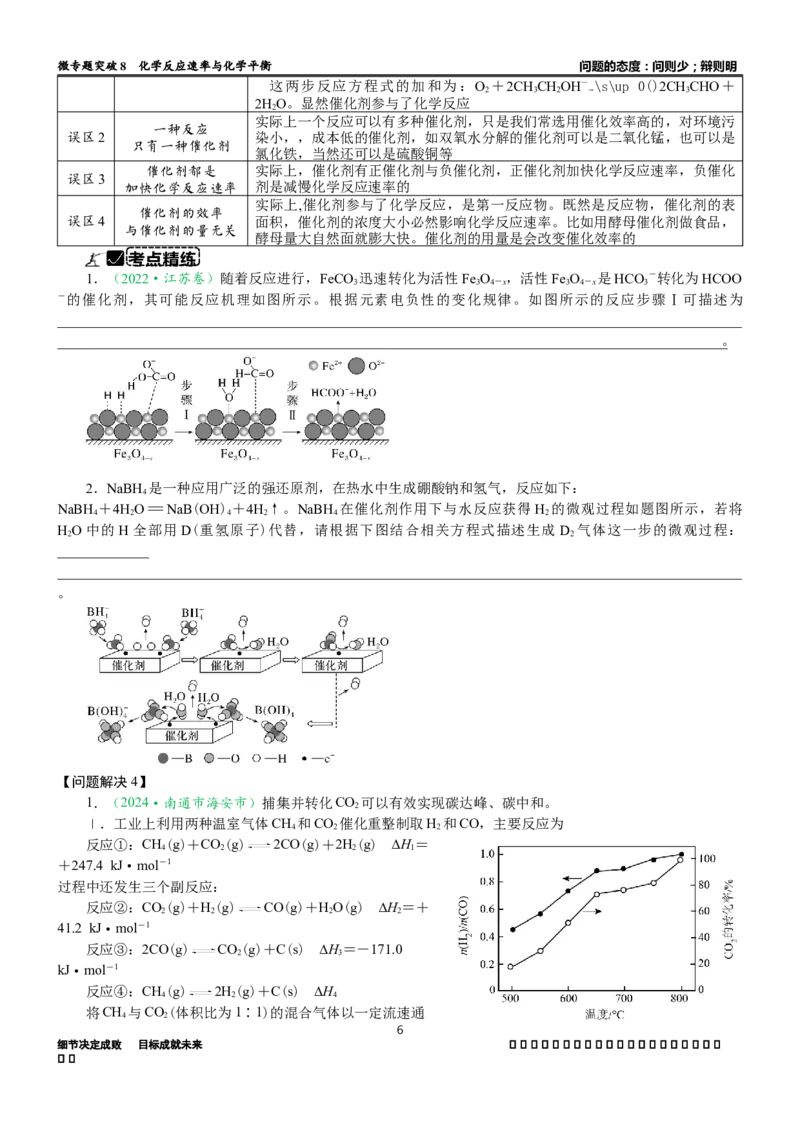
4.(2023·江苏)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
合成尿素[CO(NH )]是利用CO 的途径之一、尿素合成主要通过下列反应实现:
2 2 2
反应Ⅰ:2NH (g)+CO(g)=NH COONH(l)
3 2 2 4
反应Ⅱ:NH COONH(l)=CO(NH )(l)+HO(l)
2 4 2 2 2
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如右图所示,反应Ⅰ的
ΔH______(填“=0”“>0”或“<0”)。
②反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲
[(NH CO)NH]和尿素转化为氰酸铵(NH OCN)等副反应。尿素生产中实际投入NH 和CO 的物质的量之比为
2 2 4 3 2
n(NH )∶n(CO) = 4∶1 , 其 实 际 投 料 比 值 远 大 于 理 论 值 的 原 因 是
3 2
_______________________________________________________________。
【问题解决3】
1.(2020·江苏卷)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO 和H 可能的反应机理如
2 2
图所示。
(1)HCOOD催化释氢反应除生成CO 外,还生成_________(填化学式)。
2
(2)研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是
__________________________________________________________________________________________。
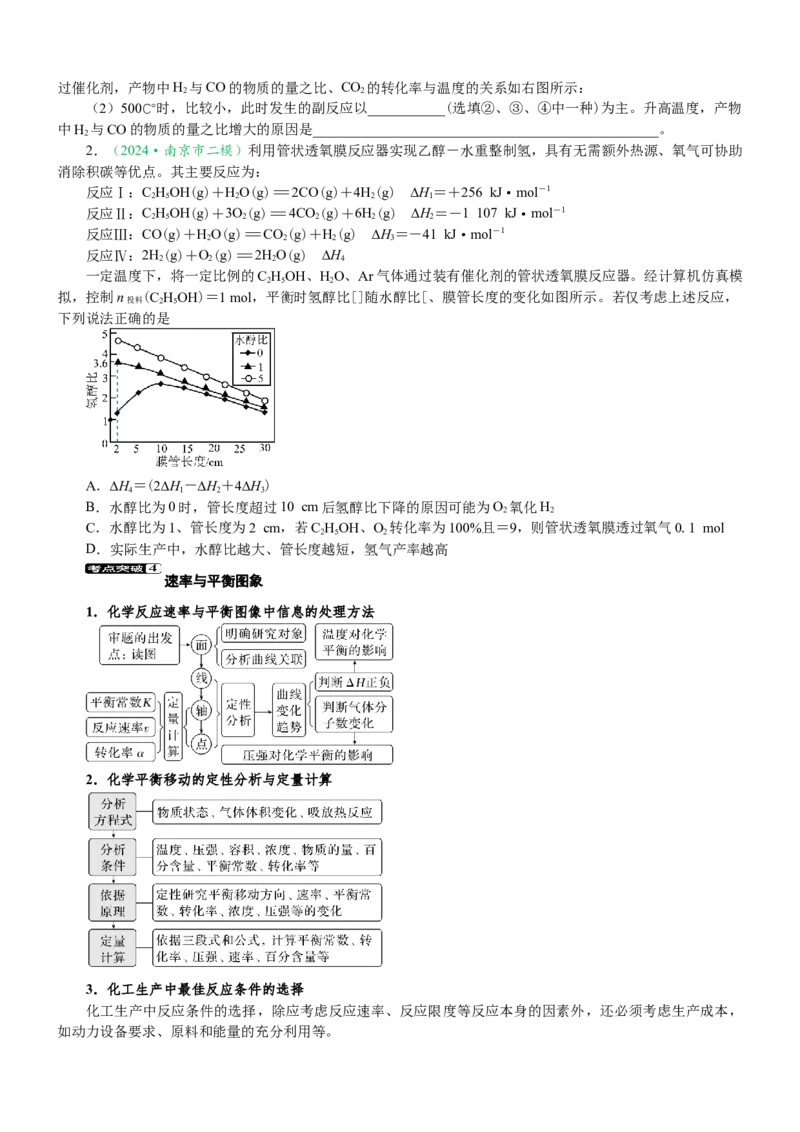
2.(2024·江苏卷)②使用含氨基物质(化学式为CN-NH ,CN是一种碳衍生材料)联合Pd-Au催化剂
2
储氢,可能机理如图所示。氨基能将HCO -控制在催化剂表面,其原理是
3
_________________________________
______________________________________;用重氢气(D)代替H,通过检测是否存在_________________(填
2 2
化学式)确认反应过程中的加氢方式。
“微观”结构变化过程机理
认识催化剂的误区
实际上,催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化学性
催化剂 质基本不变。例如在铜催化乙醇生成乙醛的反应中,铜参与反应的原理如下:
误区1
不参加化学反应 第一步为2Cu+O=2CuO
2
第二步为CuO+CHCHOH— \s\up 0()Cu+CHCHO+HO
3 2 → 3 2微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
这两步反应方程式的加和为:O +2CHCHOH— \s\up 0()2CHCHO+
2 3 2 → 3
2HO。显然催化剂参与了化学反应
2
实际上一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环境污
一种反应
误区2 染小,,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也可以是
只有一种催化剂
氯化铁,当然还可以是硫酸铜等
催化剂都是 实际上,催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负催化
误区3
加快化学反应速率 剂是减慢化学反应速率的
实际上,催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂的表
催化剂的效率
误区4 面积,催化剂的浓度大小必然影响化学反应速率。比如用酵母催化剂做食品,
与催化剂的量无关
酵母量大自然面就膨大快。催化剂的用量是会改变催化效率的
考点精练
1.(2022·江苏卷)随着反应进行,FeCO 迅速转化为活性Fe O ,活性Fe O 是HCO -转化为HCOO
3 3 4-x 3 4-x 3
-的催化剂,其可能反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ可描述为
_________________________________________________________________________________________________
_______________________________________________________________________________________________。
2.NaBH 是一种应用广泛的强还原剂,在热水中生成硼酸钠和氢气,反应如下:
4
NaBH +4HO=NaB(OH) +4H↑。NaBH 在催化剂作用下与水反应获得H 的微观过程如题图所示,若将
4 2 4 2 4 2
HO中的H全部用D(重氢原子)代替,请根据下图结合相关方程式描述生成 D 气体这一步的微观过程:
2 2
_____________
_________________________________________________________________________________________________
。
【问题解决4】
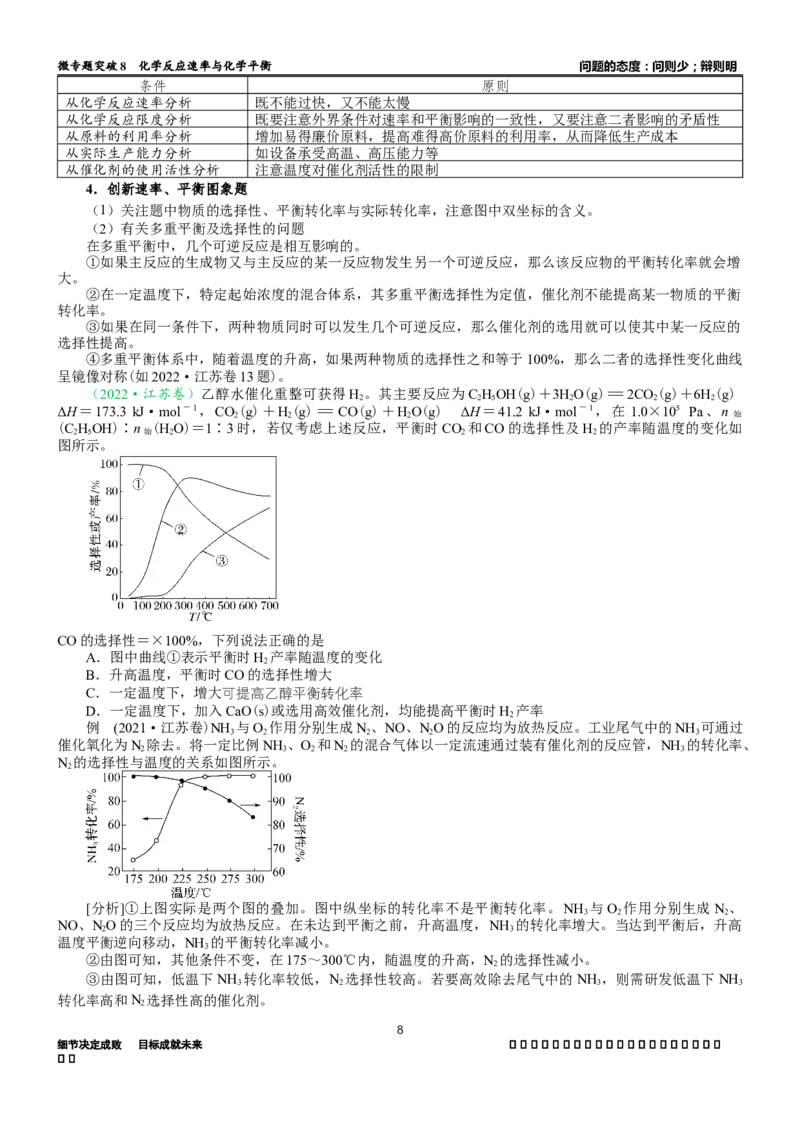
1.(2024·南通市海安市)捕集并转化CO 可以有效实现碳达峰、碳中和。
2
Ⅰ.工业上利用两种温室气体CH 和CO 催化重整制取H 和CO,主要反应为
4 2 2
反应①:CH(g)+CO(g) 2CO(g)+2H(g) ∆H=
4 2 2 1
+247.4 kJ·mol-1
过程中还发生三个副反应:
反应②:CO(g)+H(g) CO(g)+HO(g) ∆H=+
2 2 2 2
41.2 kJ·mol-1
反应③:2CO(g) CO(g)+C(s) ∆H=-171.0
2 3
kJ·mol-1
反应④:CH(g) 2H(g)+C(s) ∆H
4 2 4
将CH 与CO(体积比为1∶1)的混合气体以一定流速通
4 2
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找过催化剂,产物中H 与CO的物质的量之比、CO 的转化率与温度的关系如右图所示:
2 2
(2)500℃时,比较小,此时发生的副反应以___________(选填②、③、④中一种)为主。升高温度,产物
中H 与CO的物质的量之比增大的原因是_________________________________________________。
2
2.(2024·南京市二模)利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助
消除积碳等优点。其主要反应为:
反应Ⅰ:C HOH(g)+HO(g)=2CO(g)+4H(g) ∆H=+256 kJ·mol-1
2 5 2 2 1
反应Ⅱ:C HOH(g)+3O(g)=4CO(g)+6H(g) ∆H=-1 107 kJ·mol-1
2 5 2 2 2 2
反应Ⅲ:CO(g)+HO(g)=CO(g)+H(g) ∆H=-41 kJ·mol-1
2 2 2 3
反应Ⅳ:2H(g)+O(g)=2HO(g) ∆H
2 2 2 4
一定温度下,将一定比例的C HOH、HO、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模
2 5 2
拟,控制n (C HOH)=1 mol,平衡时氢醇比[]随水醇比[、膜管长度的变化如图所示。若仅考虑上述反应,
投料 2 5
下列说法正确的是
A.∆H=(2∆H-∆H+4∆H)
4 1 2 3
B.水醇比为0时,管长度超过10 cm后氢醇比下降的原因可能为O 氧化H
2 2
C.水醇比为1、管长度为2 cm,若C HOH、O 转化率为100%且=9,则管状透氧膜透过氧气0.1 mol
2 5 2
D.实际生产中,水醇比越大、管长度越短,氢气产率越高
速率与平衡图象
1.化学反应速率与平衡图像中信息的处理方法
2.化学平衡移动的定性分析与定量计算
3.化工生产中最佳反应条件的选择
化工生产中反应条件的选择,除应考虑反应速率、反应限度等反应本身的因素外,还必须考虑生产成本,
如动力设备要求、原料和能量的充分利用等。微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
从化学反应限度分析 既要注意外界条件对速率和平衡影响的一致性,又要注意二者影响的矛盾性
从原料的利用率分析 增加易得廉价原料,提高难得高价原料的利用率,从而降低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意温度对催化剂活性的限制
4.创新速率、平衡图象题
(1)关注题中物质的选择性、平衡转化率与实际转化率,注意图中双坐标的含义。
(2)有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
①如果主反应的生成物又与主反应的某一反应物发生另一个可逆反应,那么该反应物的平衡转化率就会增
大。
②在一定温度下,特定起始浓度的混合体系,其多重平衡选择性为定值,催化剂不能提高某一物质的平衡
转化率。
③如果在同一条件下,两种物质同时可以发生几个可逆反应,那么催化剂的选用就可以使其中某一反应的
选择性提高。
④多重平衡体系中,随着温度的升高,如果两种物质的选择性之和等于100%,那么二者的选择性变化曲线
呈镜像对称(如2022·江苏卷13题)。
(2022·江苏卷)乙醇水催化重整可获得H 。其主要反应为C HOH(g)+3HO(g)=2CO(g)+6H(g)
2 2 5 2 2 2
ΔH=173.3 kJ·mol-1,CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2 kJ·mol-1,在 1.0×105 Pa、n
2 2 2 始
(C HOH)∶n (HO)=1∶3时,若仅考虑上述反应,平衡时CO 和CO的选择性及H 的产率随温度的变化如
2 5 始 2 2 2
图所示。
CO的选择性=×100%,下列说法正确的是
A.图中曲线①表示平衡时H 产率随温度的变化
2
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大可提高乙醇平衡转化率
D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H 产率
2
例 (2021·江苏卷)NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可通过
3 2 2 2 3
催化氧化为N 除去。将一定比例NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,NH 的转化率、
2 3 2 2 3
N 的选择性与温度的关系如图所示。
2
[分析]①上图实际是两个图的叠加。图中纵坐标的转化率不是平衡转化率。NH 与O 作用分别生成N 、
3 2 2
NO、NO的三个反应均为放热反应。在未达到平衡之前,升高温度,NH 的转化率增大。当达到平衡后,升高
2 3
温度平衡逆向移动,NH 的平衡转化率减小。
3
②由图可知,其他条件不变,在175~300℃内,随温度的升高,N 的选择性减小。
2
③由图可知,低温下NH 转化率较低,N 选择性较高。若要高效除去尾气中的NH ,则需研发低温下NH
3 2 3 3
转化率高和N 选择性高的催化剂。
2
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找考点精练
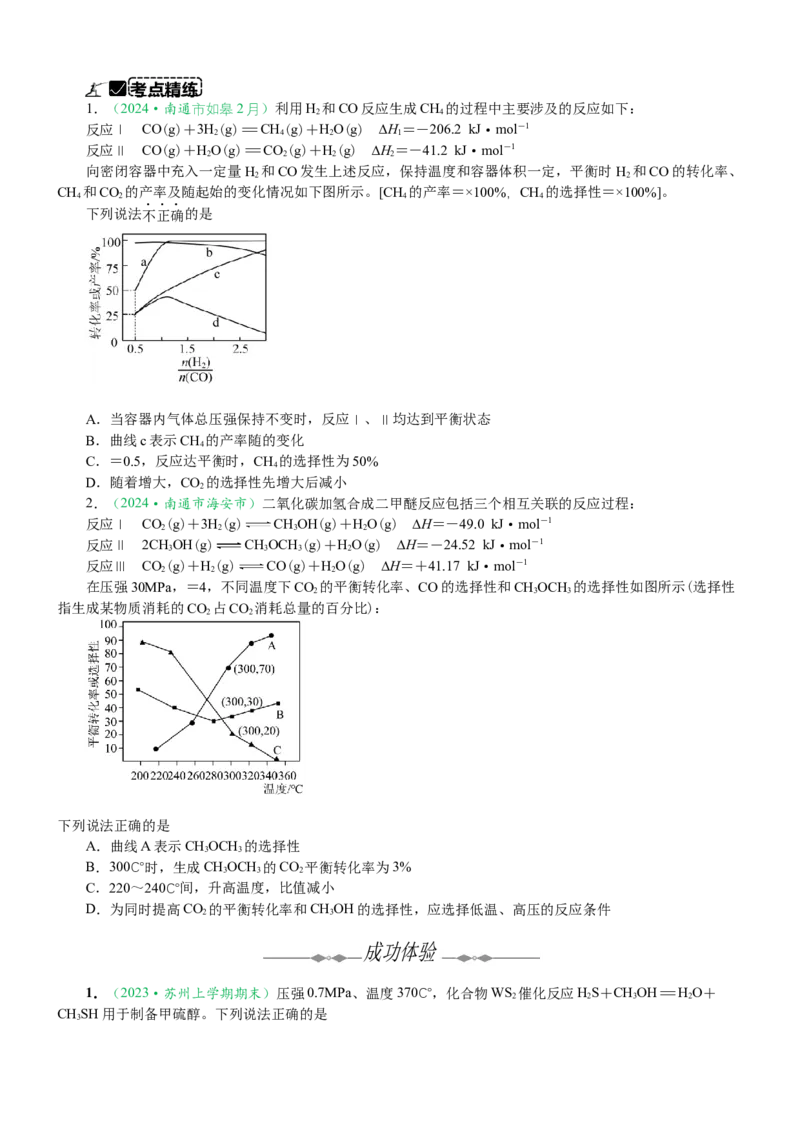
1.(2024·南通市如皋2月)利用H 和CO反应生成CH 的过程中主要涉及的反应如下:
2 4
反应Ⅰ CO(g)+3H(g)=CH(g)+HO(g) ∆H=-206.2 kJ·mol-1
2 4 2 1
反应Ⅱ CO(g)+HO(g)=CO(g)+H(g) ∆H=-41.2 kJ·mol-1
2 2 2 2
向密闭容器中充入一定量H 和CO发生上述反应,保持温度和容器体积一定,平衡时 H 和CO的转化率、
2 2
CH 和CO 的产率及随起始的变化情况如下图所示。[CH 的产率=×100%,CH 的选择性=×100%]。
4 2 4 4
下列说法不正确的是
A.当容器内气体总压强保持不变时,反应Ⅰ、Ⅱ均达到平衡状态
B.曲线c表示CH 的产率随的变化
4
C.=0.5,反应达平衡时,CH 的选择性为50%
4
D.随着增大,CO 的选择性先增大后减小
2
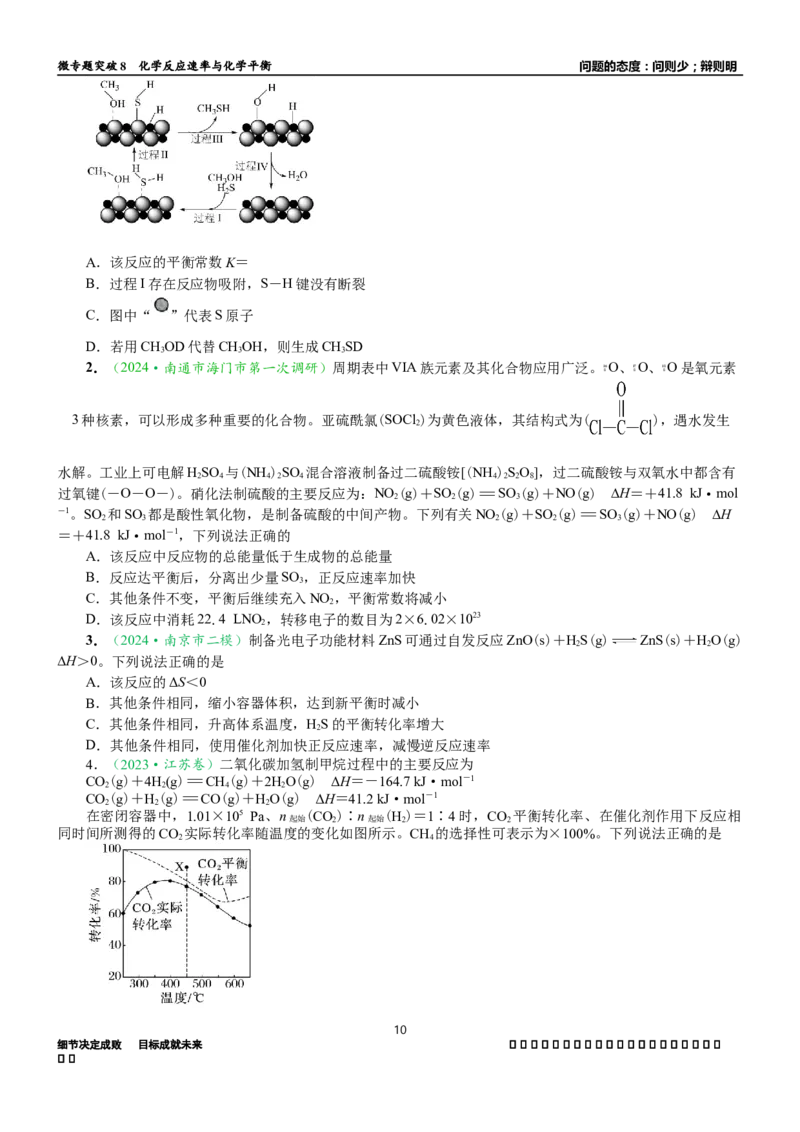
2.(2024·南通市海安市)二氧化碳加氢合成二甲醚反应包括三个相互关联的反应过程:
反应Ⅰ CO(g)+3H(g) CHOH(g)+HO(g) ∆H=-49.0 kJ·mol-1
2 2 3 2
反应Ⅱ 2CHOH(g) CHOCH (g)+HO(g) ∆H=-24.52 kJ·mol-1
3 3 3 2
反应Ⅲ CO(g)+H(g) CO(g)+HO(g) ∆H=+41.17 kJ·mol-1
2 2 2
在压强30MPa,=4,不同温度下CO 的平衡转化率、CO的选择性和CHOCH 的选择性如图所示(选择性
2 3 3
指生成某物质消耗的CO 占CO 消耗总量的百分比):
2 2
下列说法正确的是
A.曲线A表示CHOCH 的选择性
3 3
B.300℃时,生成CHOCH 的CO 平衡转化率为3%
3 3 2
C.220~240℃间,升高温度,比值减小
D.为同时提高CO 的平衡转化率和CHOH的选择性,应选择低温、高压的反应条件
2 3
成功体验
1.(2023·苏州上学期期末)压强0.7MPa、温度370℃,化合物WS 催化反应HS+CHOH=HO+
2 2 3 2
CHSH用于制备甲硫醇。下列说法正确的是
3微专题突破8 化学反应速率与化学平衡 问题的态度:问则少;辩则明
A.该反应的平衡常数K=
B.过程I存在反应物吸附,S-H键没有断裂
C.图中“ ”代表S原子
D.若用CHOD代替CHOH,则生成CHSD
3 3 3
2.(2024·南通市海门市第一次调研)周期表中VIA族元素及其化合物应用广泛。186O、187O、188O是氧元素
3种核素,可以形成多种重要的化合物。亚硫酰氯(SOCl )为黄色液体,其结构式为( ),遇水发生
2
的
水解。工业上可电解HSO 与(NH )SO 混合溶液制备过二硫酸铵[(NH )SO],过二硫酸铵与双氧水中都含有
2 4 4 2 4 4 2 2 8
过氧键(-O-O-)。硝化法制硫酸的主要反应为:NO (g)+SO (g)=SO (g)+NO(g) ∆H=+41.8 kJ·mol
2 2 3
-1。SO 和SO 都是酸性氧化物,是制备硫酸的中间产物。下列有关NO (g)+SO (g)=SO (g)+NO(g) ∆H
2 3 2 2 3
=+41.8 kJ·mol-1,下列说法正确的
A.该反应中反应物的总能量低于生成物的总能量
B.反应达平衡后,分离出少量SO ,正反应速率加快
3
C.其他条件不变,平衡后继续充入NO ,平衡常数将减小
2
D.该反应中消耗22.4 LNO ,转移电子的数目为2×6.02×1023
2
3.(2024·南京市二模)制备光电子功能材料ZnS可通过自发反应ZnO(s)+HS(g) ZnS(s)+HO(g)
2 2
∆H>0。下列说法正确的是
A.该反应的ΔS<0
B.其他条件相同,缩小容器体积,达到新平衡时减小
C.其他条件相同,升高体系温度,HS的平衡转化率增大
2
D.其他条件相同,使用催化剂加快正反应速率,减慢逆反应速率
4.(2023·江苏卷)二氧化碳加氢制甲烷过程中的主要反应为
CO(g)+4H(g)=CH(g)+2HO(g) ΔH=-164.7 kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2 kJ·mol-1
2 2 2
在密闭容器中,1.01×105 Pa、n (CO)∶n (H)=1∶4时,CO 平衡转化率、在催化剂作用下反应相
起始 2 起始 2 2
同时间所测得的CO 实际转化率随温度的变化如图所示。CH 的选择性可表示为×100%。下列说法正确的是
2 4
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找A.反应2CO(g)+2H(g)=CO(g)+CH(g)的焓变ΔH=-205.9 kJ·mol-1
2 2 4
B.CH 的平衡选择性随着温度的升高而增加
4
C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃
D.450 ℃时,提高的值或增大压强,均能使CO 平衡转化率达到X点的值
2
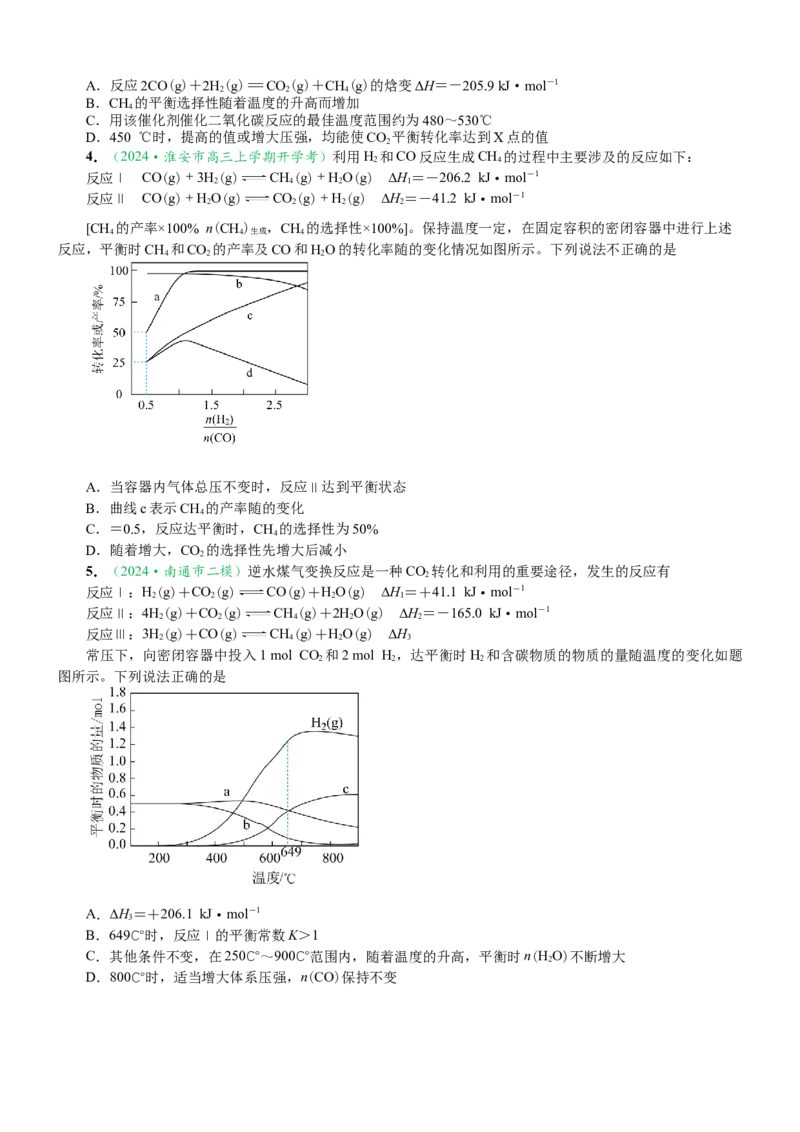
4.(2024·淮安市高三上学期开学考)利用H 和CO反应生成CH 的过程中主要涉及的反应如下:
2 4
反应Ⅰ CO(g)+3H(g) CH(g)+HO(g) ∆H=-206.2 kJ·mol-1
2 4 2 1
反应Ⅱ CO(g)+HO(g) CO(g)+H(g) ∆H=-41.2 kJ·mol-1
2 2 2 2
[CH 的产率×100% n(CH) ,CH 的选择性×100%]。保持温度一定,在固定容积的密闭容器中进行上述
4 4 生成 4
反应,平衡时CH 和CO 的产率及CO和HO的转化率随的变化情况如图所示。下列说法不正确的是
4 2 2
A.当容器内气体总压不变时,反应Ⅱ达到平衡状态
B.曲线c表示CH 的产率随的变化
4
C.=0.5,反应达平衡时,CH 的选择性为50%
4
D.随着增大,CO 的选择性先增大后减小
2
5.(2024·南通市二模)逆水煤气变换反应是一种CO 转化和利用的重要途径,发生的反应有
2
反应Ⅰ:H(g)+CO(g) CO(g)+HO(g) ∆H=+41.1 kJ·mol-1
2 2 2 1
反应Ⅱ:4H(g)+CO(g) CH(g)+2HO(g) ∆H=-165.0 kJ·mol-1
2 2 4 2 2
反应Ⅲ:3H(g)+CO(g) CH(g)+HO(g) ∆H
2 4 2 3
常压下,向密闭容器中投入1 mol CO 和2 mol H ,达平衡时H 和含碳物质的物质的量随温度的变化如题
2 2 2
图所示。下列说法正确的是
A.∆H=+206.1 kJ·mol-1
3
B.649℃时,反应Ⅰ的平衡常数K>1
C.其他条件不变,在250℃~900℃范围内,随着温度的升高,平衡时n(HO)不断增大
2
D.800℃时,适当增大体系压强,n(CO)保持不变