文档内容
押新高考卷第 15 题
工艺流程综合题
化学工艺流程题一般是陌生复杂的情境,多以工业流程图的形式呈现,试题主要特点:源于生产实际,问
题情境真实;试题内容丰富,既考查化学知识的掌握和应用,同时也考查迁移推理能力;试题新颖,阅读
量、思维含量较大,考查考生的信息提取加工、处理、应用表达能力。分析近年的高考试题,可以预测
2024年的高考考查中,主要考查以下知识点:
(1)常见的工艺操作方法措施(研磨、焙烧、水浸、酸(碱)浸等);
(2)常见的工艺操作控制条件(调节溶液pH、控制温度等);
(3)物质分离、提纯的方法及要点;
(4)流程中陌生的反应方程式的书写;
(5)流程中有关Ksp的计算;
(6)流程中有关物质的纯度、转化率、产品的产率的计算等。
另外,在新高考中,常将晶胞分析与计算内容放在工艺流程题中考查,这点需要考生特别注意。
考向一 物质的制备类
1.(2023·湖南卷)超纯 是制备第三代半导体的支撑源材料之一,近年来,我国科技工作者开发
了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯 方面取得了显著成果,工业上以
粗镓为原料,制备超纯 的工艺流程如下:
已知:①金属 的化学性质和 相似, 的熔点为 ;
② (乙醚)和 (三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:物质
沸点/ 55.7 34.6 42.4 365.8
回答下列问题:
(1)晶体 的晶体类型是_______;
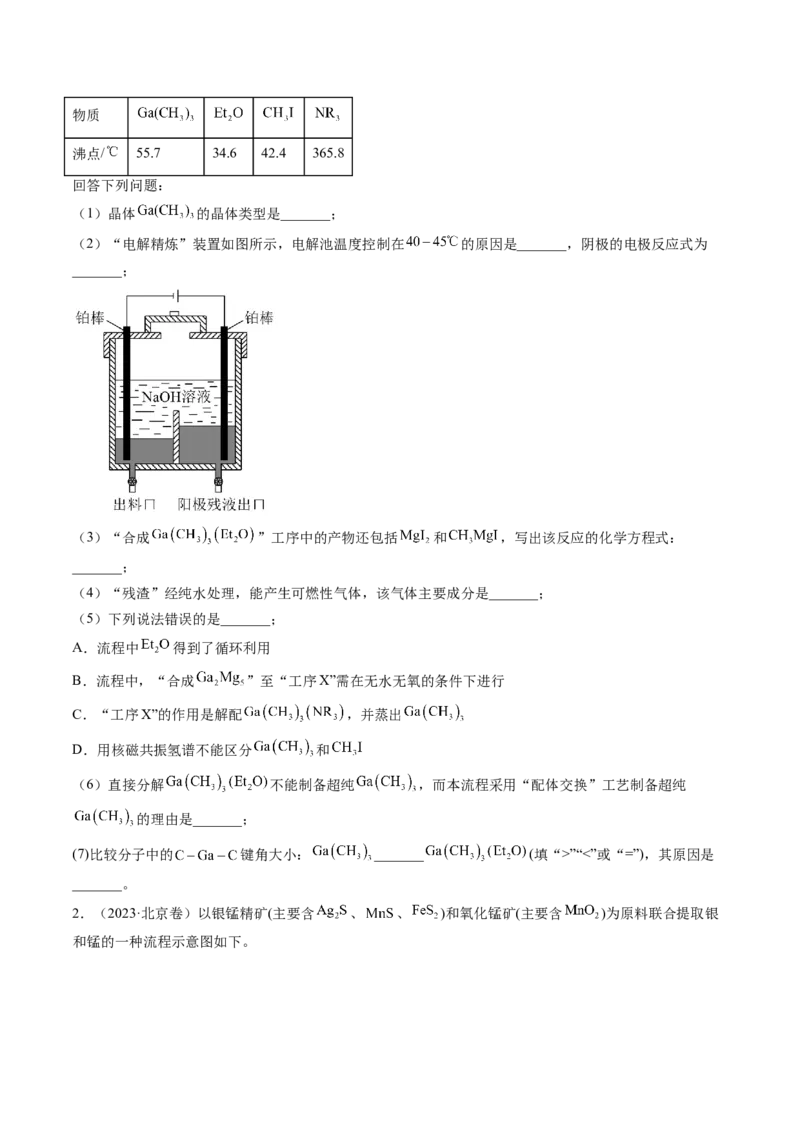
(2)“电解精炼”装置如图所示,电解池温度控制在 的原因是_______,阴极的电极反应式为
_______;
(3)“合成 ”工序中的产物还包括 和 ,写出该反应的化学方程式:
_______;
(4)“残渣”经纯水处理,能产生可燃性气体,该气体主要成分是_______;
(5)下列说法错误的是_______;
A.流程中 得到了循环利用
B.流程中,“合成 ”至“工序X”需在无水无氧的条件下进行
C.“工序X”的作用是解配 ,并蒸出
D.用核磁共振氢谱不能区分 和
(6)直接分解 不能制备超纯 ,而本流程采用“配体交换”工艺制备超纯
的理由是_______;
(7)比较分子中的 键角大小: _______ (填“>”“<”或“=”),其原因是
_______。
2.(2023·北京卷)以银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )为原料联合提取银
和锰的一种流程示意图如下。已知:酸性条件下, 的氧化性强于 。
(1) “浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿
石中的银以 的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断: __________(填“>”或
“<”) 。
②在 溶液中,银锰精矿中的 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
__________。
(2) “浸银”时,使用过量 和 的混合液作为浸出剂,将 中的银以 形式浸
出。
①将“浸银”反应的离子方程式补充完整:__________。
②结合平衡移动原理,解释浸出剂中 的作用:____________________。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有______________________________。
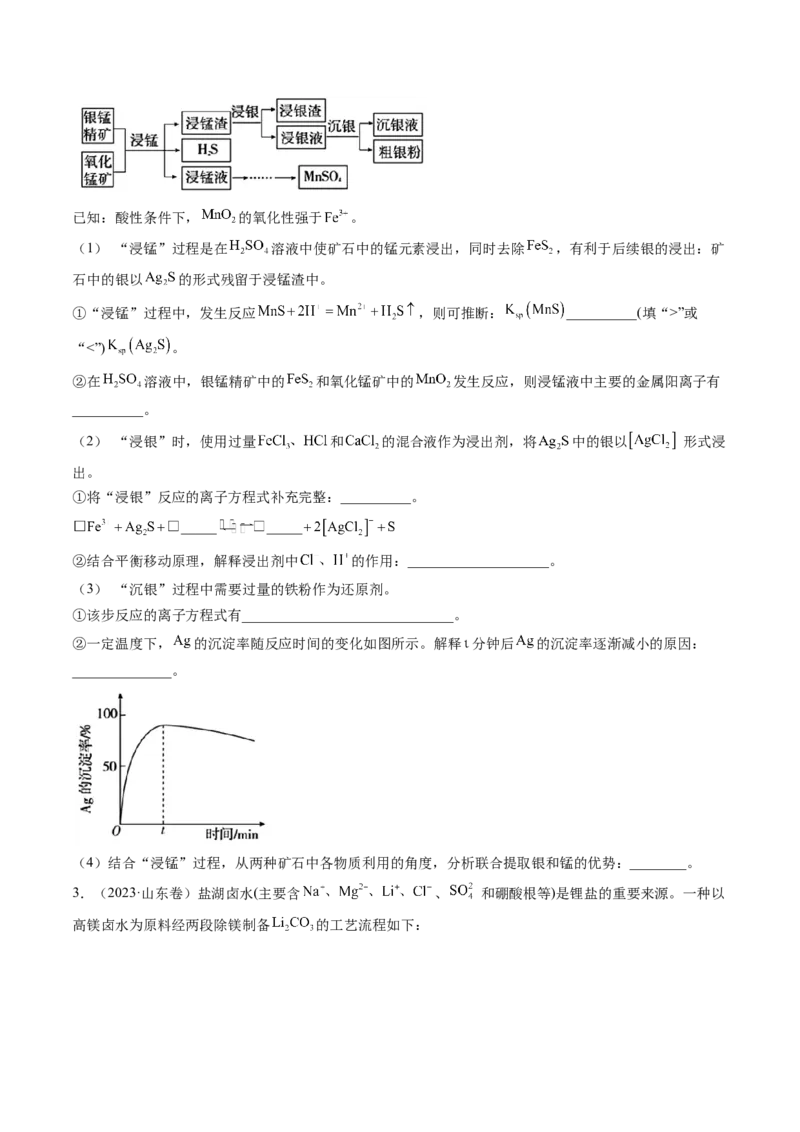
②一定温度下, 的沉淀率随反应时间的变化如图所示。解释 分钟后 的沉淀率逐渐减小的原因:
______________。
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:________。
3.(2023·山东卷)盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一种以
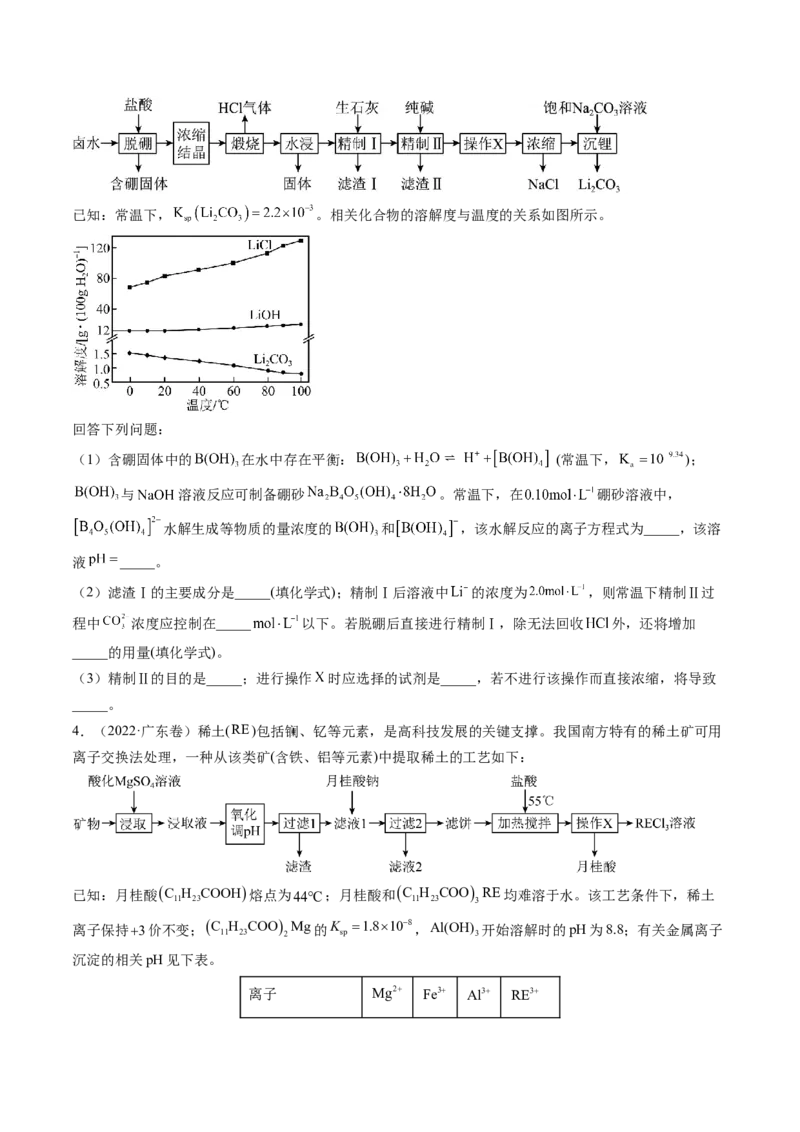
高镁卤水为原料经两段除镁制备 的工艺流程如下:已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为_____,该溶
液 _____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过
程中 浓度应控制在_____ 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加
_____的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作 时应选择的试剂是_____,若不进行该操作而直接浓缩,将导致
_____。
4.(2022·广东卷)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用
离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 C H COOH 熔点为44C;月桂酸和 C H COO RE均难溶于水。该工艺条件下,稀土
11 23 11 23 3
离子保持3价不变; C
11
H
23
COO
2
Mg的K
sp
1.8108 ,Al(OH)
3
开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子 Mg2 Fe3 Al3 RE3开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。(2)“过滤1”前,用NaOH溶液调pH至
_______的范围内,该过程中Al3发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到Mg元素,滤液2中Mg2浓度为2.7gL1。为尽可能多地提取RE3,
可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中c
C
11
H
23
COO-
低于_______molL1(保留两位有
效数字)。
(4)①“加热搅拌”有利于加快RE3溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3
①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1molPt Y转移_______mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O 的还原,发生的电极反应为
3 2
_______。
考向二 物质的提纯类
5.(2023·湖北卷) 是生产多晶硅的副产物。利用 对废弃的锂电池正极材料 进行氯化处
理以回收Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第_______周期,第_______族。
(2)烧渣是LiCl、 和 的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大
量烟雾,用化学方程式表示其原因_______。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是_______。
(4)已知 ,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为_______
。“850℃煅烧”时的化学方程式为_______。(5)导致 比 易水解的因素有_______(填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
6.(2023·辽宁卷)某工厂采用如下工艺处理镍钴矿硫酸浸取液含( 和
)。实现镍、钴、镁元素的回收。
已知:
物质
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_______(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸 , 中
过氧键的数目为_______。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为_______(
的电离第一步完全,第二步微弱);滤渣的成分为 、_______(填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。 体积分数为_______时,
(Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率减小的原因是_______。
(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为_______。
(6)“沉镁”中为使 沉淀完全 ,需控制 不低于_______(精确至0.1)。
7.(2022·湖南卷)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为TiO ,含少量
2V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1)已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化。若
ΔG<0,则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。
A.C(s)O (g)CO (g)
2 2
B.2C(s)O (g)2CO(g)
2
C.TiO (s)2Cl (g)TiCl (g)O (g)
2 2 4 2
D.TiO (s)C(s)2Cl (g)TiCl (g)CO (g)
2 2 4 2
(2)TiO 与C、Cl ,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压MPa 4.59102 1.84102 3.70102 5.98109
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2
②随着温度升高,尾气中CO的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl
4
中含Si、Al杂质的方法
是_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰 D.氧化汞分解制汞
8.(2022·湖北卷)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水
进行浓缩和初步除杂后,得到浓缩卤水(含有Na+、Li+、Cl-和少量Mg2+、Ca2+),并设计了以下流程通过制
备碳酸锂来提取锂。
25℃时相关物质的参数如下:
LiOH的溶解度:12.4g/100gH O
2
化合物 K
sp
MgOH 5.61012
2
CaOH 5.5106
2
CaCO 2.8109
3
Li CO 2.5102
2 3
回答下列问题:
(1)“沉淀1”为___________。(2)向“滤液1”中加入适量固体Li CO 的目的是___________。
2 3
(3)为提高Li CO 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
2 3
(4)有同学建议用“侯氏制碱法”的原理制备Li CO 。查阅资料后,发现文献对常温下的Li CO 有不同的
2 3 2 3
描述:①是白色固体;②尚未从溶液中分离出来。为探究LiHCO 的性质,将饱和LiCl溶液与饱和
3
NaHCO 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述
3
现象说明,在该实验条件下LiHCO ___________(填“稳定”或“不稳定”),有关反应的离子方程式为
3
___________。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入Na CO 改为通入CO 。这一改动能否达
2 3 2
到相同的效果,作出你的判断并给出理由___________。
一、常见的工艺操作方法措施和条件控制
方法措施或
思考角度
条件控制
固体原料粉 将块状或颗粒状的物质磨成粉末或将液体雾化,增大反应物接触面积,以加快反应速率
碎或研磨、 或使反应更充分。
液体原料雾 目的:提高原料转化率、利用率、浸取率,提高产品的产率等
化 增大接触面积的方法:固体——粉碎、研磨;液体——喷洒;气体——用多孔分散器等
①除去硫、碳单质;
②有机物转化、除去有机物;
焙烧或灼烧
③高温下原料与空气中氧气反应;
④除去热不稳定的杂质(如碳酸盐沉淀)等。
煅烧 改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解,如煅烧高岭土。
①溶解转变成可溶物进入溶液中,以达到与难溶物分离的目的;
酸浸
②去氧化物(膜)
①除去金属表面的油污;
碱溶
②溶解两性化合物(AlO、ZnO等),溶解铝、二氧化硅等
2 3
水浸 与水接触反应或溶解,使原料变成离子进入溶液中
醇浸 提取有机物,常采用有机溶剂(乙醚,二氯甲烷等)浸取的方法提取有机物
①加快反应速率或溶解速率;
②促进平衡向吸热反应方向移动(一般是有利于生成物生成的方向);如:促进水解生成
加热
沉淀。
③除杂,除去热不稳定的杂质,如:HO 、氨水、铵盐(NH Cl)、硝酸盐、NaHCO 、
2 2 4 3Ca(HCO )、KMnO 等物质;
3 2 4
④使沸点相对较低或易升华的原料气化;
⑤煮沸时促进溶液中的气体(如氧气)挥发逸出等
①防止某物质在高温时溶解(或分解);
②使化学平衡向着题目要求的方向(放热反应方向)移动;
降温
③使某个沸点较高的产物液化,使其与其他物质分离等;
④降低某些晶体的溶解度,使其结晶析出,减少损失等
温度过低:反应速率过慢或溶解速率小
温度过高:** 错误的表达式 **催化剂逐渐失活,化学反应速率急剧下降
控制温度在
** 错误的表达式 **物质分解,如:NaHCO 、NH HCO 、HO、浓HNO 等
3 4 3 2 2 3
一定范围(综
** 错误的表达式 **物质会挥发,如:浓硝酸、浓盐酸、醋酸、液溴、乙醇等
合考虑)
** 错误的表达式 **物质氧化,如:NaSO 等
2 3
** 错误的表达式 **物质升华,如:I 升华
2
①防止副反应的发生
②使化学平衡移动;控制化学反应的方向
③控制固体的溶解与结晶
控制温度(常 ④控制反应速率;使催化剂达到最大活性
用水浴、冰 ⑤升温:促进溶液中的气体逸出,使某物质达到沸点挥发
浴或油浴) ⑥加热煮沸:促进水解,聚沉后利于过滤分离
⑦趁热过滤:减少因降温而析出的溶质的量
⑧降温:防止物质高温分解或挥发;降温(或减压)可以减少能源成本,降低对设备的要
求
①酸浸时提高酸的浓度可提高矿石中某金属元素的浸取率;
反应物用量
②增大便宜、易得的反应物的浓度,可以提高其他物质的利用率,使反应充分进行;
或浓度
③增大物质浓度可以加快反应速率,使平衡发生移动等
①氧化(或还原)某物质,转化为目标产物的价态;
加入氧化剂
②除去杂质离子[如把Fe2+氧化成Fe3+,而后调溶液的pH,使其转化为Fe(OH) 沉淀除
3
(或还原剂)
去]
①生成硫化物沉淀(如加入硫化钠、硫化铵、硫化亚铁等);
加入沉淀剂 ②加入可溶性碳酸盐,生成碳酸盐沉淀;
③加入氟化钠,除去Ca2+、Mg2+
(1)调节溶液的酸碱性,使金属离子形成氢氧化物沉淀析出,以达到除去金属离子的目
的;
** 错误的表达式 **原理:加入的物质能与溶液中的H+反应,降低了H+的浓度,使溶液
pH控制
pH值增大
** 错误的表达式 **pH控制的范围:杂质离子完全沉淀时pH值~主要离子开始沉淀时
pH (注意两端取值)** 错误的表达式 **需要的物质:含主要阳离子(不引入新杂质即可)的难溶性氧化物或
氢氧化物或碳酸盐,即能与H+反应,使pH增大的物质,如MgO、Mg(OH) 、MgCO 等
2 3
类型的物质
** 错误的表达式 **实例:除去 CuSO 溶液中少量 Fe3+,可向溶液中加入 CuO、
4
Cu(OH) 、Cu (OH) CO 、CuCO ,调节pH至3~4,使Fe3+转化为Fe(OH) 沉淀除去。
2 2 2 3 3 3
Fe3+溶液中存在水解平衡:Fe3++3HO Fe(OH) +3H+,加入CuO后,溶液中H+浓度
2 3
降低,平衡正向移动,Fe(OH) 越聚越多,最终形成沉淀
3
a.加入CuO的作用:调节溶液的pH,使Fe3+转化为Fe(OH)
3
b.加热的目的:促进Fe3+水解
(2)抑制盐类水解;
像盐酸盐、硝酸盐溶液,通过结晶方法制备晶体或加热脱水结晶水合物制备相对应的无
水盐时,由于水解生成的盐酸或硝酸挥发,促使了金属离子水解(水解反应为吸热反应)
导致产品不纯
如:由MgCl ·6H O制无水MgCl 要在HCl气流中加热,否则:
2 2 2
MgCl ·6H O Mg(OH) +2HCl↑+4HO
2 2 2 2
(3)促进盐类水解生成沉淀,有利于过滤分离
(4)“酸作用”还可除去氧化物(膜)
(5)“碱作用”还可除去油污,除去铝片氧化膜,溶解铝、二氧化硅等
(6)特定的氧化还原反应需要的酸性条件(或碱性条件)
【注意】调节pH的试剂选取:
①选取流程中出现的物质;
②未学习过的物质且题目又无信息提示的一般不做考虑;
③已学的常见酸碱(NaOH、NaCO、HCl、HSO 、NH ·H O、HNO)。
2 3 2 4 3 2 3
①水洗:通常是为了除去晶体表面水溶性的杂质
②冰水洗涤:能洗去晶体表面的杂质离子,且防止晶体在洗涤过程中的溶解损耗
③用特定有机试剂清洗晶体:洗去晶体表面的杂质,降低晶体的溶解度、有利于析出,
洗涤晶体
减少损耗等
④洗涤沉淀的方法:往漏斗中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作
2~3次
在空气中或
在其他气体 要考虑O、HO、CO 或其他气体是否参与反应;或能否达到隔绝空气、防氧化、防水
2 2 2
中进行的反 解、防潮解等目的
应或操作
判断能否加
要考虑是否引入杂质(或影响产物的纯度)等
其他物质
提高原子利
绿色化学(物质的循环利用、废物处理、原子利用率、能量的充分利用)
用率过滤、蒸发、萃取、分液、蒸馏等常规操作
分离、提纯
从溶液中得到晶体的方法:蒸发浓缩―→冷却结晶―→过滤―→洗涤、干燥
二、物质分离、提纯的方法及要点
不相溶液体 分液
相溶性液体 蒸馏
分
难溶性固体 过滤
离
易溶性固体 蒸发浓缩、冷却结晶
提
趁热过滤 防止温度降低,某物质析出
纯
冰水洗涤 减少晶体的溶解损失
乙醇、有机溶剂洗涤 减少晶体的水溶性损失
三、工艺流程中的物质确定及方程式书写方法
1.工艺流程中的物质确定
首先分析题干信息,明确原料成分,看清流程图中的箭头指向,根据物质性质写出相关的化学反应(离子方
程式或化学方程式),最后根据题干信息确定滤液中物质的成分。滤液中物质的成分确定的思维模型如图所
示:
循环物质的确定
副产品的确定
①过量的反应物。
②原料中不参与反应的物质。
滤渣成分的确定
③由原料转化的生成物。
④由杂质转化的沉淀物。
2.工艺流程中的方程式书写
(1)明确一些特殊物质中元素的化合价
CuFeS:Cu为+2,Fe为+2,S为-2; C O:C为+3;
2 2
KFeO:Fe为+6; HCN:C为+2;N为-3;
2 4
FePO :Fe为+3; CuH:Cu为+1,H为-1;
4LiFePO :Fe为+2; BH:B为+3、H为-1;
4
LiNH、LiNH、AlN:N为-3; FeO:Fe为+(8-n);
2 2
NH:N为-2; Si N:Si为+4,N为-3;
2 4 3 4
NaSO:S为+2; MnO(OH):Mn为+3;
2 2 3
SO:S为+6; CrO:Cr为+6;
2
VO:V为+5;
(2)认识并掌握常见的氧化剂、还原剂。
①强氧化性物质或离子:
NaO 、Fe3+、NO 、HNO(浓)、HNO(稀)、O 、O 、HO 、HSO (浓)、Cl 、Br 、HClO、NaClO、
2 2 2 3 3 2 3 2 2 2 4 2 2
Ca(ClO) 、KMnO (H+)。
2 4
②强还原性物质或离子:
Fe2+、Fe(OH) 、SO (H SO 、NaSO 、NaHSO、SO)、HS(Na S、NaHS、S2-)、HI(NaI、I-)等。
2 2 2 3 2 3 3 2 2
(3)书写关键——识记常见氧化剂、还原剂及产物预测
①常见的氧化剂及还原产物预测
氧化剂 还原产物
KMnO Mn2+(酸性);MnO (中性);MnO(碱性)
4 2
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
HSO (浓) SO
2 4 2
X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO)
2 2 2 3
Cl Cl-
2
HClO、NaClO、Ca(ClO) (或ClO
2
Cl-、Cl
2
-)
NaClO Cl、ClO 、Cl-
3 2 2
PbO Pb2+
2
Fe3+ Fe2+
②常见的还原剂及氧化产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或HSO 、SO、NaHSO) SO
2 2 3 3
S2-(或HS、NaHS) S、SO (或SO)、SO
2 2
HC O、C O CO、CO
2 2 4 2 2HO O
2 2 2
I-(或HI、NaI) I、IO
2
CO CO
2
金属单质(Zn、Fe、Cu等) Zn2+、Fe2+(与强氧化剂反应生成Fe3+)、Cu2+
H H+(酸性)、HO(碱性)
2 2
四、工艺流程中有关溶度积的计算
1.溶度积(K )的有关计算
sp
(1)已知溶度积,求溶液中的某种离子的浓度,如K =a的饱和AgCl溶液中c(Ag+)= mol·L-1。
sp
(2)已知溶度积、溶液中某离子的浓度,求溶液中另一种离子的浓度,如某温度下,AgCl的K =a,在
sp
0.1 mol·L-1 NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
(3)计算反应的平衡常数,如反应 Cu2+(aq)+MnS(s) CuS(s)+Mn2+(aq),K (MnS)=c(Mn2+)·c(S2
sp
-),K (CuS)=c(Cu2+)·c(S2-),平衡常数K==。
sp
(4)求解开始沉淀和沉淀完全时的pH,如判断M(OH) (s) Mn+(aq)+nOH-(aq)开始沉淀与沉淀完全
n
时的pH。
①开始沉淀时pH的求法:c(OH-)=,c(H+)=,从而确定pH。
②沉淀完全时pH的求法:当Mn+的浓度小于或等于1.0×10-5 mol·L-1时,认为该离子已经沉淀完全,
c(OH-)= mol·L-1,结合K 求出c(H+),从而确定pH。
w
注意:有关K 的计算往往与pH的计算结合,要注意pH与c(OH-)关系的转换;难溶电解质的悬浊液即其
sp
沉淀溶解平衡状态,满足相应的K 。
sp
2.溶度积常数的考查角度及思路分析
考查角度 思路分析
①根据离子浓度数据求得Q,若Q>K ,则有沉淀生成;
sp
判断沉淀的生成或沉淀是
②利用K 的数值计算某一离子浓度,若该离子浓度小于10-5 mol·L-
sp
否完全
1,则该离子沉淀完全
①根据氢氧化物的K 以及开始沉淀时金属阳离子的初始浓度,计算溶
sp
常温下,计算氢氧化物沉
液中c(OH-),再求得溶液的pH;
淀开始和沉淀完全时的
②金属阳离子沉淀完全时的离子浓度为10-5 mol·L-1,根据K 可计算
sp
pH
金属阳离子沉淀完全时溶液中的c(OH-),进而求得pH
计算沉淀转化反应的平衡
根据沉淀的转化反应和K ,计算该反应的平衡常数,K的值越大,转
sp
常数,并判断沉淀转化的
化反应越易进行,转化程度越大
程度
①沉淀类型相同,则K 小的化合物先沉淀;
sp
沉淀先后的计算与判断 ②沉淀类型不同,则需要根据K 计算出沉淀时所需离子浓度,所需离
sp
子浓度小的先沉淀五、工艺流程中有关物质的纯度、转化率、产品的产率的计算
化工流程题中涉及的计算主要有:样品的质量分数或纯度的计算,物质的转化率或产率、物质的量浓度、
物质的质量的计算。
1.计算公式
(1)n=,n=,n=cV(aq)
(2)=×100%
(3)产品产率=×100%
(4)物质的转化率=×100%
考向一 物质的制备类
1.(2024·山东济南一模)工业上常用软锰矿(主要成分为MnO ,含少量Fe O、Al O、SiO)和LiCO 合
2 2 3 2 3 2 2 3
成电极材料LiMn O 并回收净水剂明矾,其工艺流程如图所示。
2 4
已知:①Mn2+在酸性条件下比较稳定,pH高于5.5时易被O 氧化;
2
②当溶液中某离子浓度 时,可认为该离子沉淀完全;常温下,几种沉淀的 如
下表所示:
③lg5=0.7。
回答下列问题:
(1)“酸浸”时,通入稍过量SO 的目的是 ,一定温度下,软锰矿与不同浓度的硫酸反应
2
60min时结果如下表所示:
c(HSO )/mol·L-1 1.0 5.0 10.0 16.0 18.0
2 4
Mn浸出率/% 25 78 95 85 55
Al浸出率/% 35 90 83 5 0
则“酸浸”时,选择c(HSO )为 mol·L-1。
2 4(2)加入MnCO “调pH”时,若c(Mn2+)=1.0mol·L-1,其他金属阳离子浓度为0.001mol·L-1,则调pH的范围
3
为 ,若“滤渣Ⅲ”主要成分为FeOOH,则“氧化”操作中主反应的离子方程式为
。
(3)“焙烧”操作中,为了提高LiCO 利用率,加入稍过量的MnO ,加热至600℃~750℃便制得
2 3 2
LiMn O,则反应的化学方程式为 ,整个流程中,可以循环使用的物质有 。
2 4
(4)获取明矾 的“一系列操作”是 。
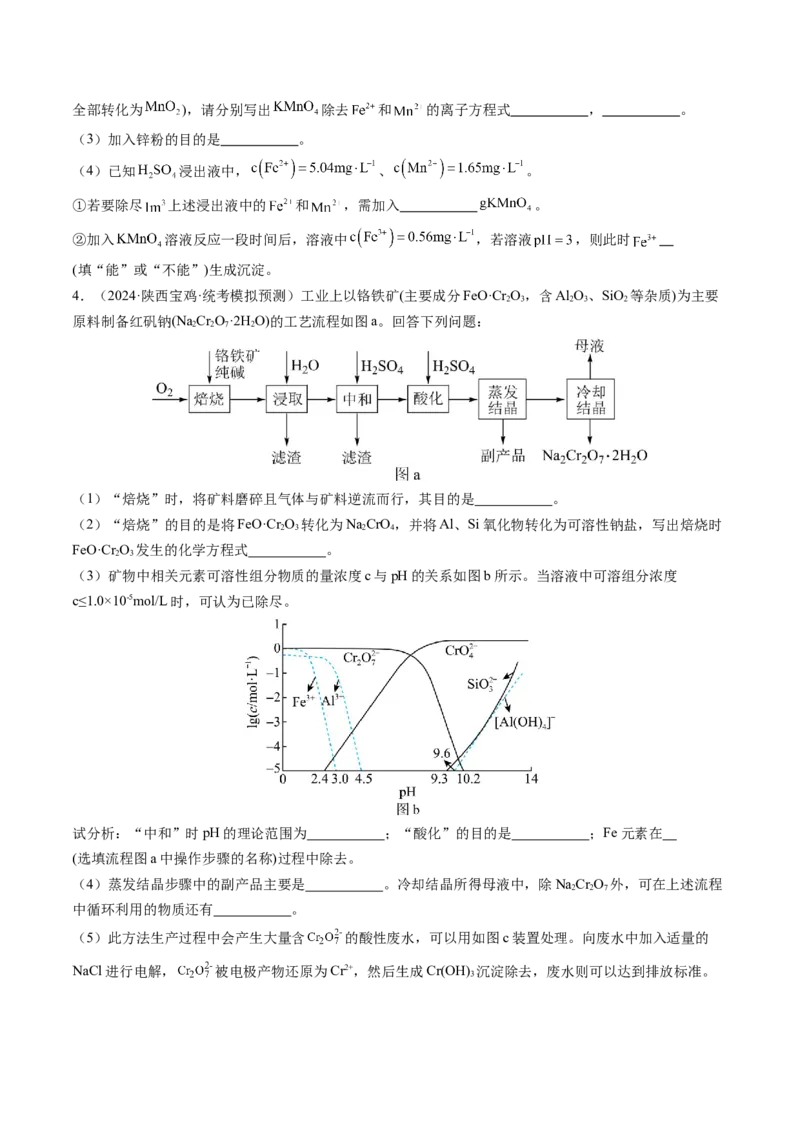
2.(2024·广西·统考模拟预测)层状结构 薄膜能用于制作电极材料。 薄膜由辉钼矿(主要含
及少量FeO、 )制得 后再与S经气相反应并沉积得到,其流程如下。
回答下列问题:
(1)“焙烧”产生的 用 溶液吸收生成 的离子方程式为 。
(2)“焙烧”后的固体用氨水“浸取”得到重钼酸铵 溶液,为提高“浸取”速率,可采
用的措施是 (举一例)。
(3)“灼烧”过程中需回收利用的气体是 (填化学式)。
(4)在650℃下“气相沉积”生成 的反应需在特定气流中进行,选用Ar而不选用 形成该气流的
原因是 。
(5)层状 晶体与石墨晶体结构类似,层状 的晶体类型为 。将 嵌入层状 充
电后得到的 可作电池负极,该负极放电时的电极反应式为 。结合原子结构分析,
能嵌入 层间可能的原因是 。
半径小。
3.(2024·黑龙江哈尔滨·高三一模)高纯活性氧化锌可用于光催化、光电极、彩色显影等领域。以工业级
氧化锌(含 等)为原料,用硫酸浸出法生产高纯活性氧化锌的工艺流程如下:
已知 。
回答下列问题:
(1)浸出时,为了提高浸出效率可采取的措施有(写两种): 。
(2)氧化时,加入 溶液是为了将浸出液中的 和 均转化为沉淀而除去,(溶液中 元素全部转化为 ),请分别写出 除去 和 的离子方程式 , 。
(3)加入锌粉的目的是 。
(4)已知 浸出液中, 、 。
①若要除尽 上述浸出液中的 和 ,需加入 。
②加入 溶液反应一段时间后,溶液中 ,若溶液 ,则此时
(填“能”或“不能”)生成沉淀。
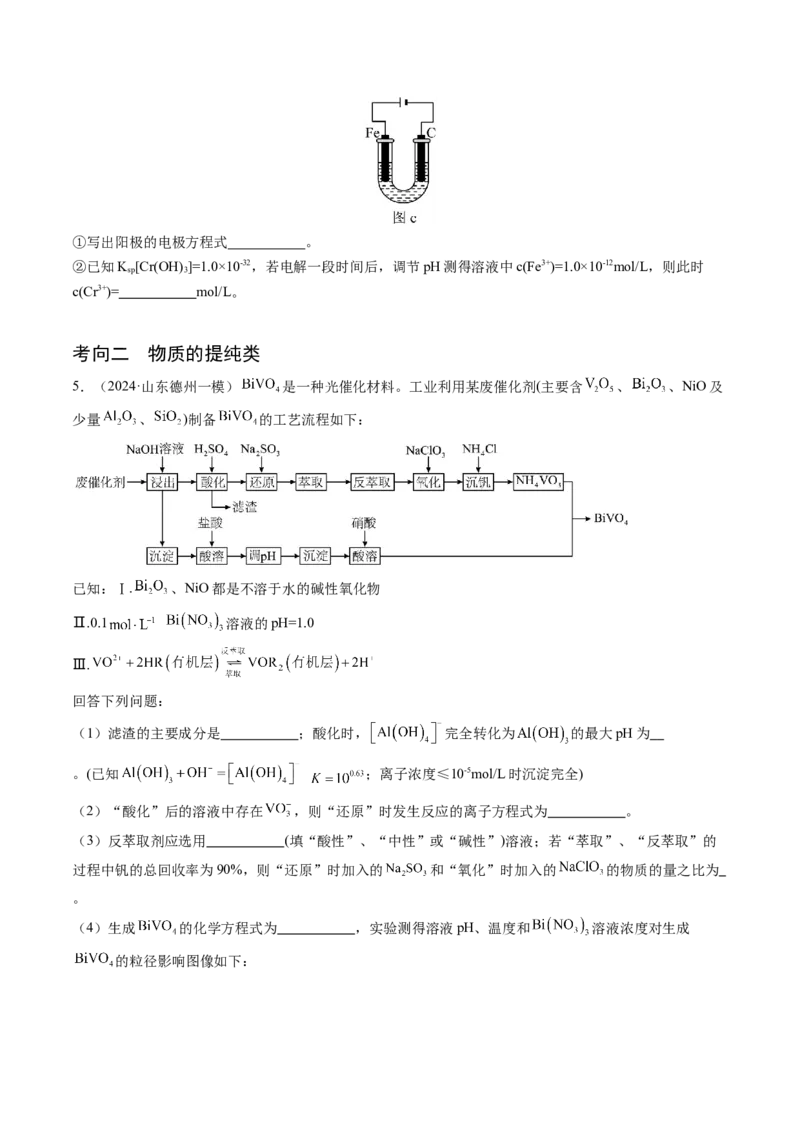
4.(2024·陕西宝鸡·统考模拟预测)工业上以铬铁矿(主要成分FeO·Cr O,含Al O、SiO 等杂质)为主要
2 3 2 3 2
原料制备红矾钠(Na Cr O·2H O)的工艺流程如图a。回答下列问题:
2 2 7 2
(1)“焙烧”时,将矿料磨碎且气体与矿料逆流而行,其目的是 。
(2)“焙烧”的目的是将FeO·Cr O 转化为NaCrO,并将Al、Si氧化物转化为可溶性钠盐,写出焙烧时
2 3 2 4
FeO·Cr O 发生的化学方程式 。
2 3
(3)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图b所示。当溶液中可溶组分浓度
c≤1.0×10-5mol/L时,可认为已除尽。
试分析:“中和”时pH的理论范围为 ;“酸化”的目的是 ;Fe元素在
(选填流程图a中操作步骤的名称)过程中除去。
(4)蒸发结晶步骤中的副产品主要是 。冷却结晶所得母液中,除NaCr O 外,可在上述流程
2 2 7
中循环利用的物质还有 。
(5)此方法生产过程中会产生大量含 的酸性废水,可以用如图c装置处理。向废水中加入适量的
NaCl进行电解, 被电极产物还原为Cr2+,然后生成Cr(OH) 沉淀除去,废水则可以达到排放标准。
3①写出阳极的电极方程式 。
②已知K [Cr(OH) ]=1.0×10-32,若电解一段时间后,调节pH测得溶液中c(Fe3+)=1.0×10-12mol/L,则此时
sp 3
c(Cr3+)= mol/L。
考向二 物质的提纯类
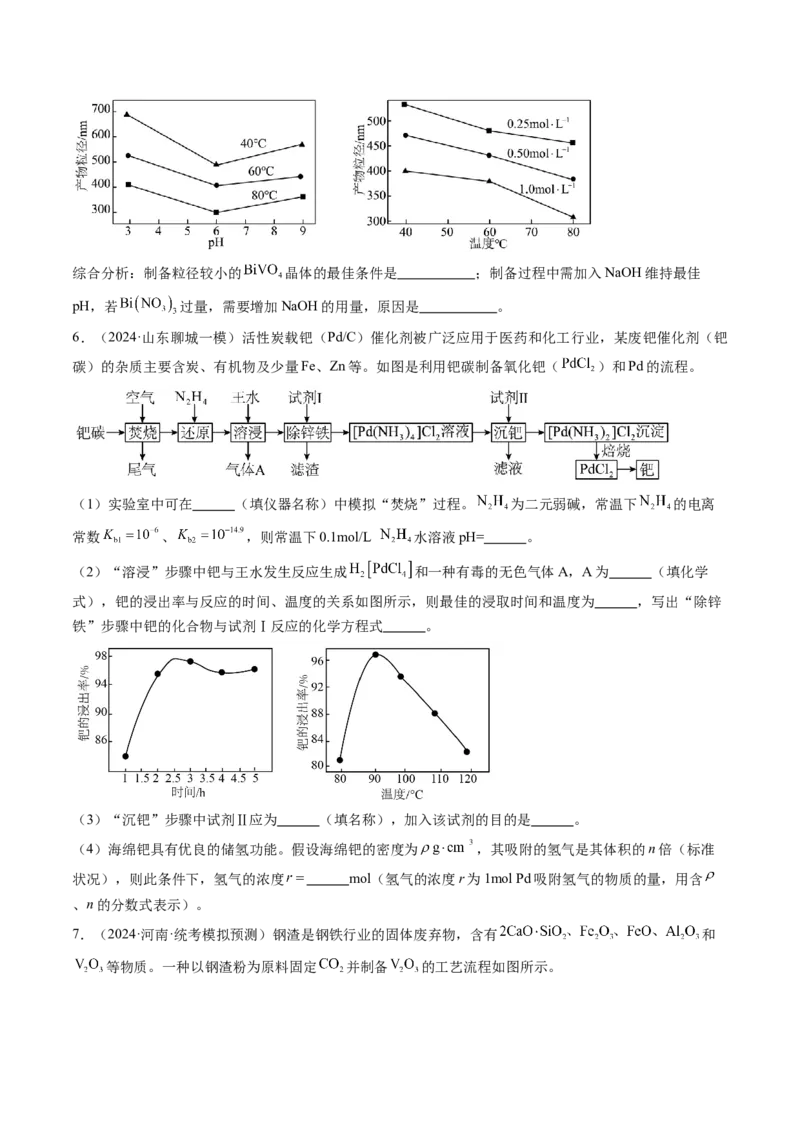
5.(2024·山东德州一模) 是一种光催化材料。工业利用某废催化剂(主要含 、 、NiO及
少量 、 )制备 的工艺流程如下:
已知:Ⅰ. 、NiO都是不溶于水的碱性氧化物
Ⅱ.0.1 溶液的pH=1.0
Ⅲ.
回答下列问题:
(1)滤渣的主要成分是 ;酸化时, 完全转化为 的最大pH为
。(已知 ;离子浓度≤10-5mol/L时沉淀完全)
(2)“酸化”后的溶液中存在 ,则“还原”时发生反应的离子方程式为 。
(3)反萃取剂应选用 (填“酸性”、“中性”或“碱性”)溶液;若“萃取”、“反萃取”的
过程中钒的总回收率为90%,则“还原”时加入的 和“氧化”时加入的 的物质的量之比为
。
(4)生成 的化学方程式为 ,实验测得溶液pH、温度和 溶液浓度对生成
的粒径影响图像如下:综合分析:制备粒径较小的 晶体的最佳条件是 ;制备过程中需加入NaOH维持最佳
pH,若 过量,需要增加NaOH的用量,原因是 。
6.(2024·山东聊城一模)活性炭载钯(Pd/C)催化剂被广泛应用于医药和化工行业,某废钯催化剂(钯
碳)的杂质主要含炭、有机物及少量Fe、Zn等。如图是利用钯碳制备氧化钯( )和Pd的流程。
(1)实验室中可在 (填仪器名称)中模拟“焚烧”过程。 为二元弱碱,常温下 的电离
常数 、 ,则常温下0.1mol/L 水溶液pH= 。
(2)“溶浸”步骤中钯与王水发生反应生成 和一种有毒的无色气体A,A为 (填化学
式),钯的浸出率与反应的时间、温度的关系如图所示,则最佳的浸取时间和温度为 ,写出“除锌
铁”步骤中钯的化合物与试剂Ⅰ反应的化学方程式 。
(3)“沉钯”步骤中试剂Ⅱ应为 (填名称),加入该试剂的目的是 。
(4)海绵钯具有优良的储氢功能。假设海绵钯的密度为 ,其吸附的氢气是其体积的n倍(标准
状况),则此条件下,氢气的浓度 mol(氢气的浓度r为1mol Pd吸附氢气的物质的量,用含
、n的分数式表示)。
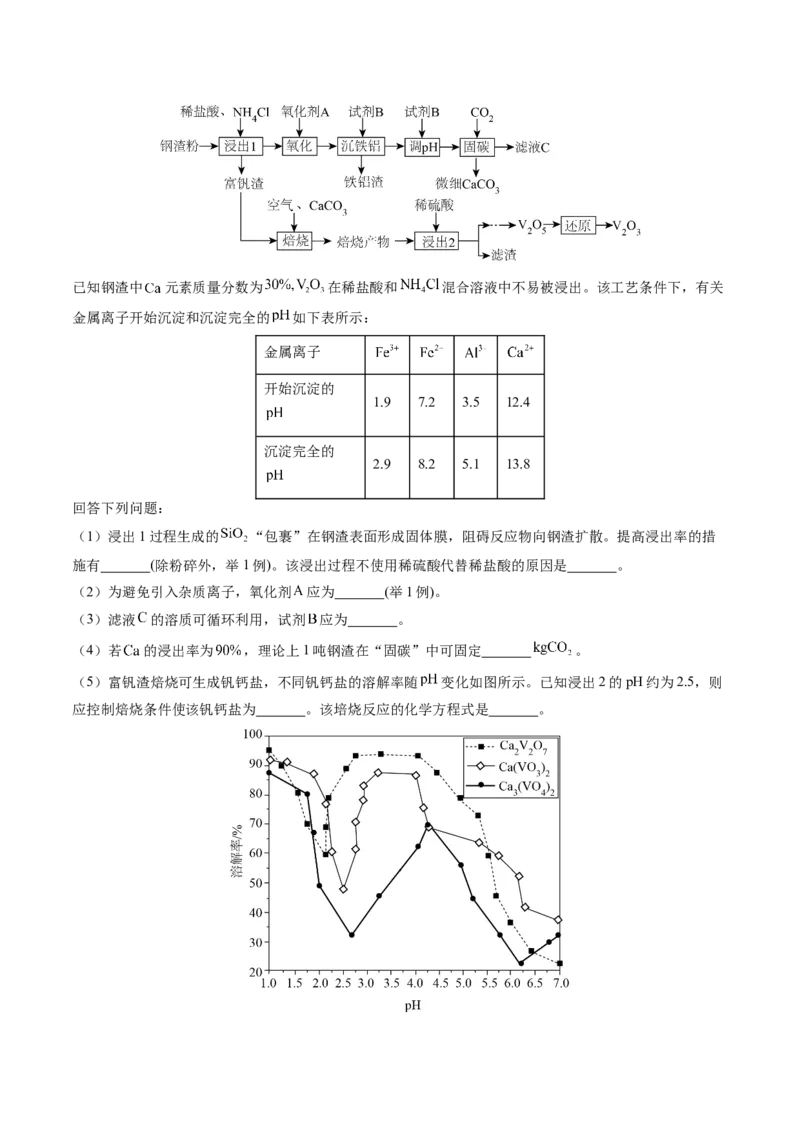
7.(2024·河南·统考模拟预测)钢渣是钢铁行业的固体废弃物,含有 和
等物质。一种以钢渣粉为原料固定 并制备 的工艺流程如图所示。已知钢渣中 元素质量分数为 在稀盐酸和 混合溶液中不易被浸出。该工艺条件下,有关
金属离子开始沉淀和沉淀完全的 如下表所示:
金属离子
开始沉淀的
1.9 7.2 3.5 12.4
沉淀完全的
2.9 8.2 5.1 13.8
回答下列问题:
(1)浸出1过程生成的 “包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措
施有 (除粉碎外,举1例)。该浸出过程不使用稀硫酸代替稀盐酸的原因是 。
(2)为避免引入杂质离子,氧化剂 应为 (举1例)。
(3)滤液 的溶质可循环利用,试剂 应为 。
(4)若 的浸出率为 ,理论上1吨钢渣在“固碳”中可固定 。
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随 变化如图所示。已知浸出2的pH约为2.5,则
应控制焙烧条件使该钒钙盐为 。该培烧反应的化学方程式是 。(6)微细碳酸钙广泛应用于医药、食品等领域,某种碳酸钙晶胞如图所示。已知
,该晶体密度为 (列出计算式,阿伏加德罗常数的值
为 )。
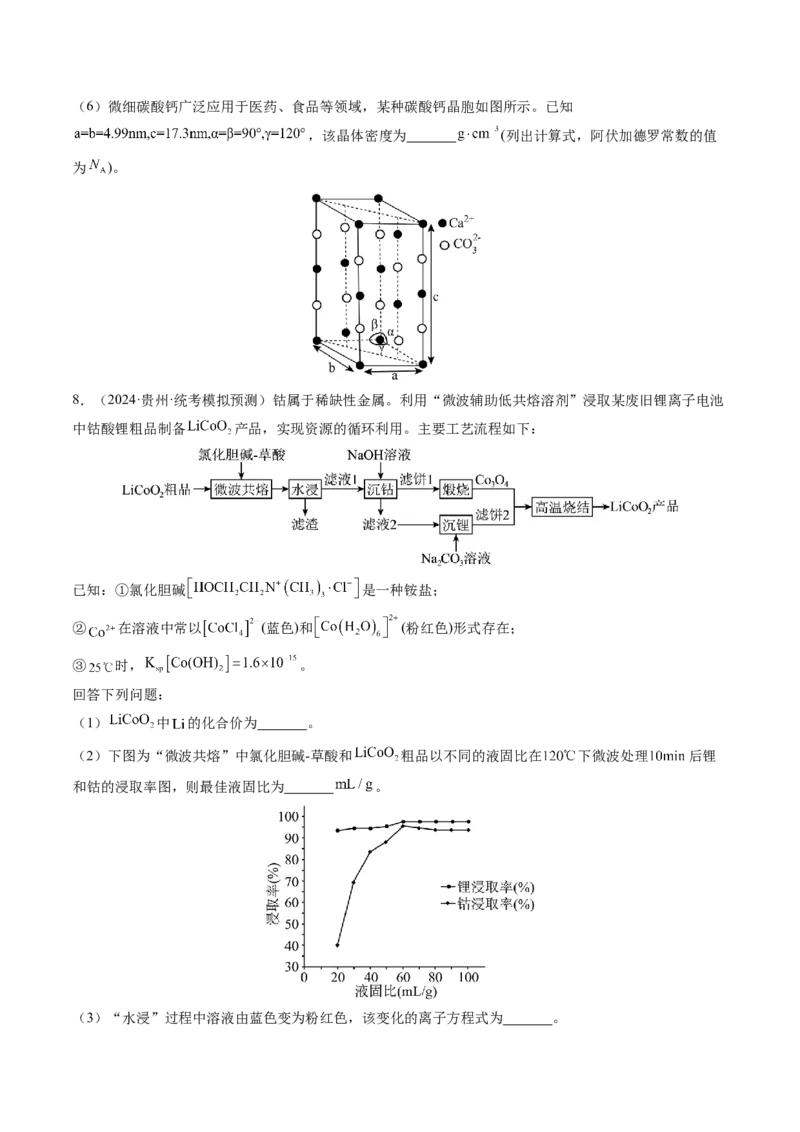
8.(2024·贵州·统考模拟预测)钴属于稀缺性金属。利用“微波辅助低共熔溶剂”浸取某废旧锂离子电池
中钴酸锂粗品制备 产品,实现资源的循环利用。主要工艺流程如下:
已知:①氯化胆碱 是一种铵盐;
② 在溶液中常以 (蓝色)和 (粉红色)形式存在;
③ 时, 。
回答下列问题:
(1) 中 的化合价为 。
(2)下图为“微波共熔”中氯化胆碱-草酸和 粗品以不同的液固比在 下微波处理 后锂
和钴的浸取率图,则最佳液固比为 。
(3)“水浸”过程中溶液由蓝色变为粉红色,该变化的离子方程式为 。(4) 时,“沉钴”反应完成后,溶液 ,此时 。
(5)“滤饼2”在高温烧结前需要洗涤、干燥,检验“滤饼2”是否洗涤干净的操作及现象是 。
(6)“高温烧结”中需要通入空气,其作用是 。
(7)锂离子电池正极材料 在多次充放电后由于可循环锂的损失,结构发生改变生成 ,导致电
化学性能下降。
① 晶体(常式尖晶石型)的晶胞示意图如图所示,则顶点上的离子为 (用离子符号表示)。
②使用 和 溶液可以实现 的修复,则修复过程中的化学反应方程式为 。
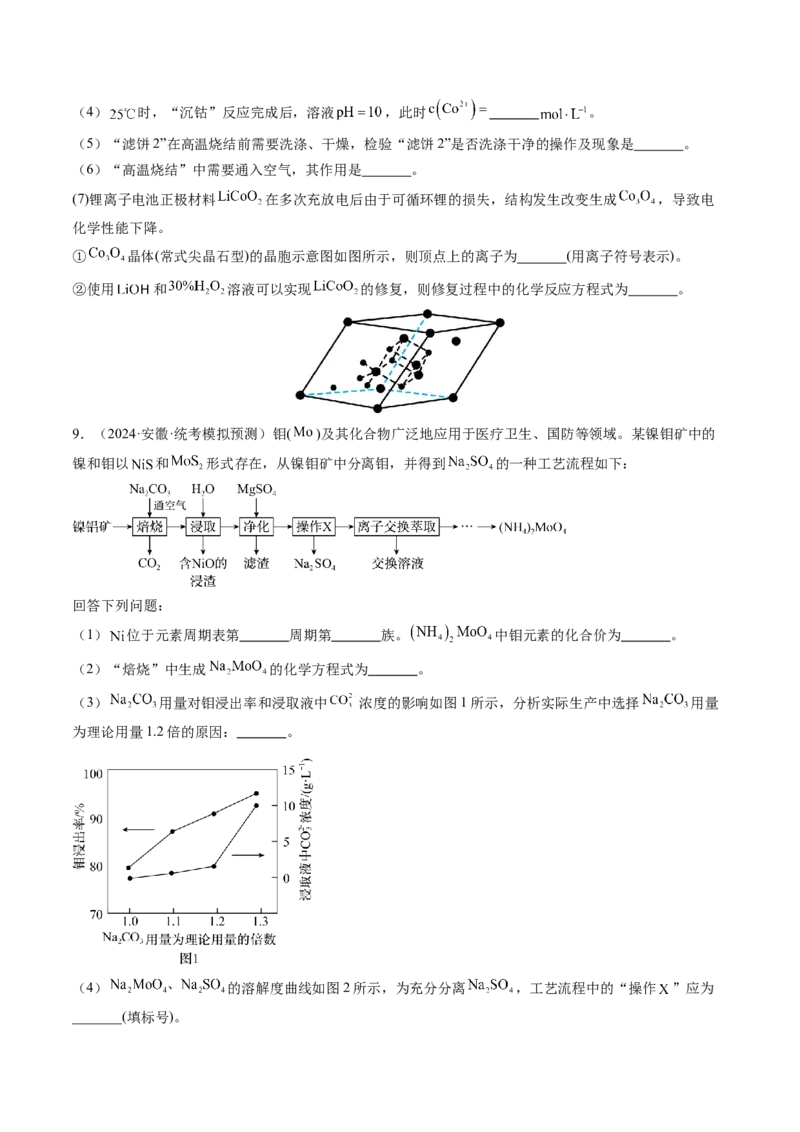
9.(2024·安徽·统考模拟预测)钼( )及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的
镍和钼以 和 形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
回答下列问题:
(1) 位于元素周期表第 周期第 族。 中钼元素的化合价为 。
(2)“焙烧”中生成 的化学方程式为 。
(3) 用量对钼浸出率和浸取液中 浓度的影响如图1所示,分析实际生产中选择 用量
为理论用量1.2倍的原因: 。
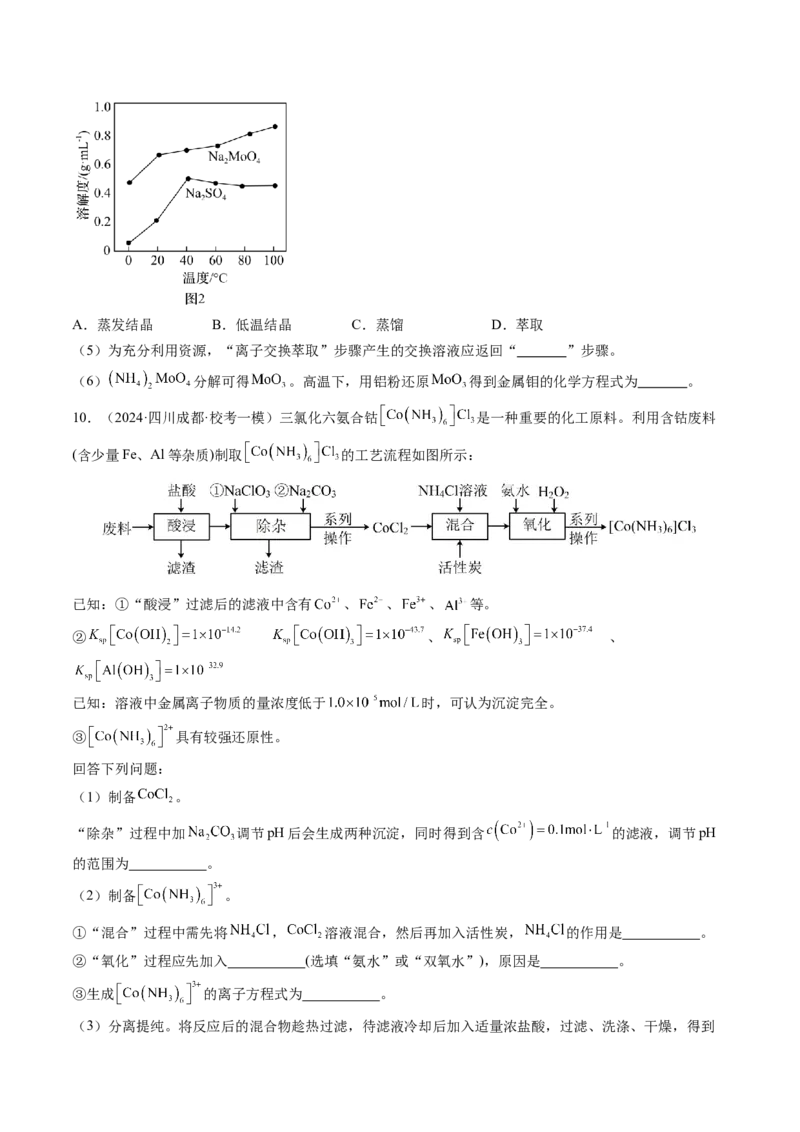
(4) 的溶解度曲线如图2所示,为充分分离 ,工艺流程中的“操作 ”应为
_______(填标号)。A.蒸发结晶 B.低温结晶 C.蒸馏 D.萃取
(5)为充分利用资源,“离子交换萃取”步骤产生的交换溶液应返回“ ”步骤。
(6) 分解可得 。高温下,用铝粉还原 得到金属钼的化学方程式为 。
10.(2024·四川成都·校考一模)三氯化六氨合钴 是一种重要的化工原料。利用含钴废料
(含少量Fe、Al等杂质)制取 的工艺流程如图所示:
已知:①“酸浸”过滤后的滤液中含有 、 、 、 等。
② 、 、
已知:溶液中金属离子物质的量浓度低于 时,可认为沉淀完全。
③ 具有较强还原性。
回答下列问题:
(1)制备 。
“除杂”过程中加 调节pH后会生成两种沉淀,同时得到含 的滤液,调节pH
的范围为 。
(2)制备 。
①“混合”过程中需先将 , 溶液混合,然后再加入活性炭, 的作用是 。
②“氧化”过程应先加入 (选填“氨水”或“双氧水”),原因是 。
③生成 的离子方程式为 。
(3)分离提纯。将反应后的混合物趁热过滤,待滤液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到晶体。该过程中加入浓盐酸的目的是 。
(4)含量测定。通过碘量法可测定产品中的钴元素的含量。称取0.10g产品加入稍过量的NaOH溶液并加
热,将Co完全转化为难溶的 ,过滤洗涤后将滤渣完全溶于盐酸中,向所得的溶液中加入过量的
KI和2~3滴淀粉溶液,再用 溶液滴定(反应原理: 、
),达到滴定终点时消耗 溶液24.00mL,则产品中钴元素的含量 。