文档内容
押江苏卷第 10 题
反应原理小综合
核心考点 考情统计 考向预测 备考策略
2023·江苏卷,10 1.重点关注化学反应的方向、化
反应原理小综
2022·江苏卷,10 结
数
合
、
化
化
学
学
反
反
应
应
与
进
能
行
量
的
、
方
化
向
学
等
平
角
衡
度
常
综
学
粒浓
平
度
衡
比
常
值
数
的
的
方
应
法
用
等
、
;
判断溶液中微
合
2021·江苏卷,8 合考查 2.利用键能计算焓变、能量图像
分析等
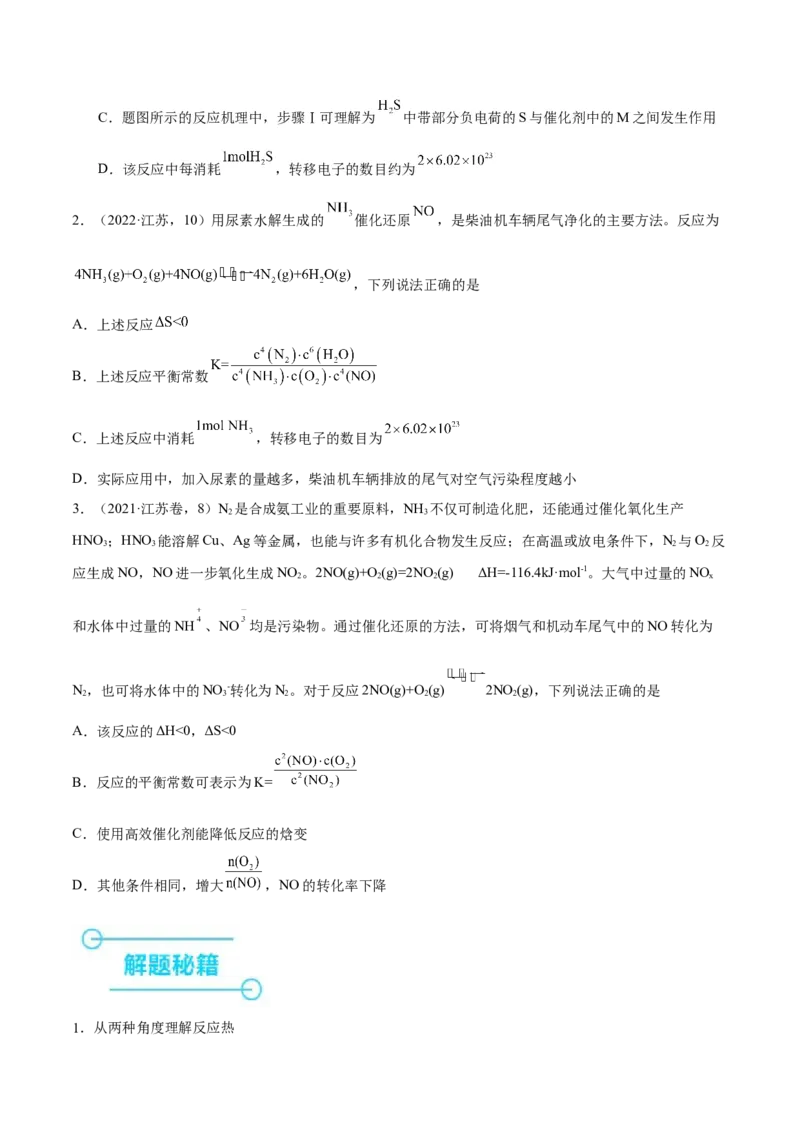
1.(2023·江苏卷,10)金属硫化物( )催化反应 ,既可以除去天
然气中的 ,又可以获得 。下列说法正确的是
A.该反应的
B.该反应的平衡常数C.题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用
D.该反应中每消耗 ,转移电子的数目约为
2.(2022·江苏,10)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
3.(2021·江苏卷,8)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产
2 3
HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反
3 3 2 2
应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO
2 2 2 x
和水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为
N,也可将水体中的NO -转化为N。对于反应2NO(g)+O (g) 2NO (g),下列说法正确的是
2 3 2 2 2
A.该反应的ΔH<0,ΔS<0
B.反应的平衡常数可表示为K=
C.使用高效催化剂能降低反应的焓变
D.其他条件相同,增大 ,NO的转化率下降
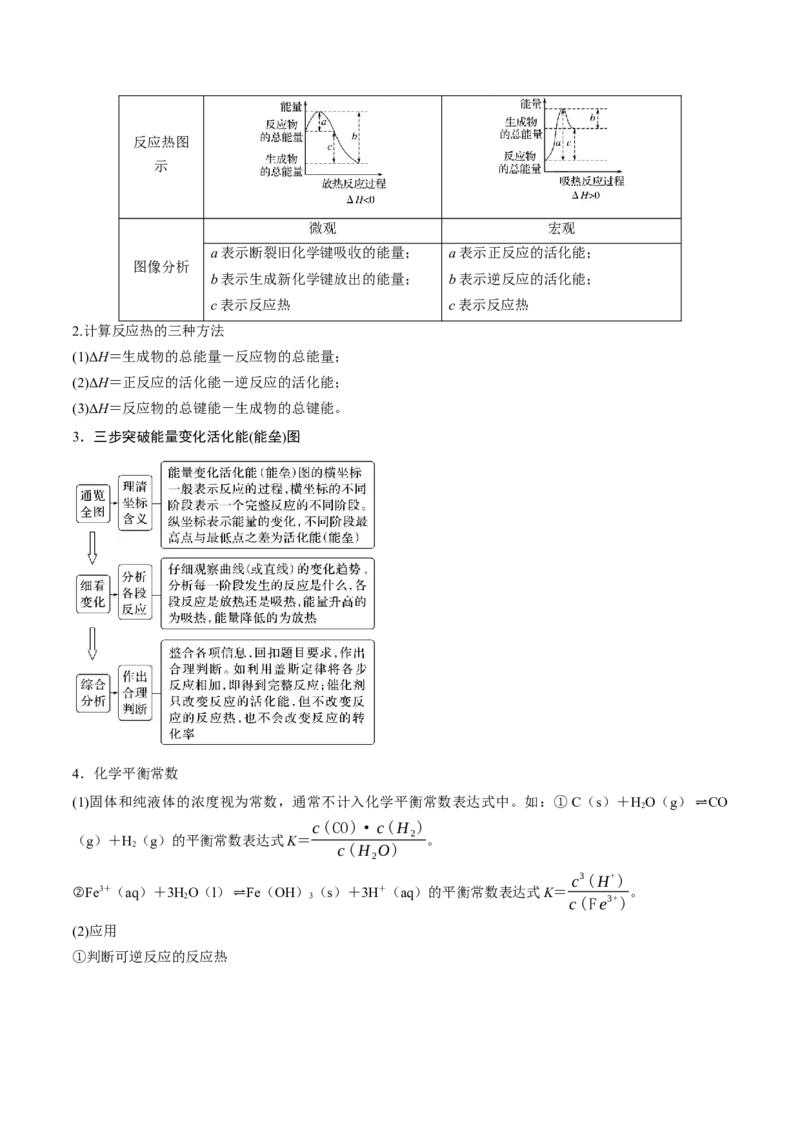
1.从两种角度理解反应热反应热图
示
微观 宏观
a表示断裂旧化学键吸收的能量; a表示正反应的活化能;
图像分析
b表示生成新化学键放出的能量; b表示逆反应的活化能;
c表示反应热 c表示反应热
2.计算反应热的三种方法
(1)ΔH=生成物的总能量-反应物的总能量;
(2)ΔH=正反应的活化能-逆反应的活化能;
(3)ΔH=反应物的总键能-生成物的总键能。
3.三步突破能量变化活化能(能垒)图
4.化学平衡常数
(1)固体和纯液体的浓度视为常数,通常不计入化学平衡常数表达式中。如:①C(s)+H
2
O(g)⇌CO
c(CO)·c(H )
2
(g)+H(g)的平衡常数表达式K= 。
2 c(H O)
2
c3(H+)
②Fe3+(aq)+3H
2
O(l)⇌Fe(OH)
3
(s)+3H+(aq)的平衡常数表达式K=
c(Fe3+)
。
(2)应用
①判断可逆反应的反应热②判断化学平衡移动的方向
分析浓度商(Qc)与平衡常数的大小关系,
当Qc<K时,反应向正反应方向进行,直至达到平衡状态;
当Qc=K时,反应处于平衡状态;
当Qc>K时,反应向逆反应方向进行,直至达到平衡状态。
5.判断化学反应方向的判据(ΔG=ΔH-TΔS)
ΔG<0时,反应能自发进行;
ΔG=0时,反应处于平衡状态;
ΔG>0时,反应不能自发进行。
6.判断溶液中微粒浓度比值的方法
(1)将浓度之比转化为物质的量之比进行比较,这样分析起来可以忽略溶液体积的变化,只需分析微粒数目
的变化即可。如同一溶液中,溶液体积相同,=,NH ·H O溶液稀释过程中,n(NH)增大,n(NH ·H O)减
3 2 3 2
小,故的值增大。
c(F−)
(2)“假设法”,如上述D项,假设无限稀释,c(F-)趋近于0,c(H+)趋于10-7mol·L-1,故 变小。
c(H+)
(3)“凑常数”,解题时将某些粒子的浓度比值乘以或除以某种粒子的浓度,转化为一个常数与某种粒子浓
度的乘积或相除的关系。如CHCOOH溶液加水稀释后,判断溶液中 的变化,将式子的分子、
3
分母同乘以c(H+)得 ,CHCOOH在稀释时,c(H+)减小,Ka不变,则该比值增
3
大。
1.(2024·江苏泰州高三一模,11)利用碳氮化反应
,可将 转化为 ,再进一步还原得到金属钛,下列说法正确的是
A.碳氯化反应在高温下不能自发进行B.加压、降温均可增大生成 的速率
C.反应中每消耗 ,转移电子的数目约为
D.将 与 粉碎并混合均匀后反应可提高 的平衡转化率
2.(2024·江苏无锡高三期终教学质量调研测试,10)电催化是利用催化剂电极进行电解以实现物质转变
的前沿方法。使用单原子催化剂电催化将CO 转化为CO的部分机理如图所示。下列说法正确的是( )
2
A. 该催化过程在电解池的阳极进行 B. 该催化过程CO 发生了氧化反应
2
C. 甲、乙中的C原子的杂化类型不同 D. 催化剂原子吸附CO 中带负电的部分
2
3.(2024·江苏淮安市5校高三10月份联考,7)对于反应2NO (g) NO(g),下列说法正确的是
2 2 4
A.该反应的 H>0 S<0
B.该反应的平衡常数表达式为
C.升高温度, 该反应的 (正)增大, (逆)减小
D.将容器体积压缩为原来一半,气体颜色比压缩前深
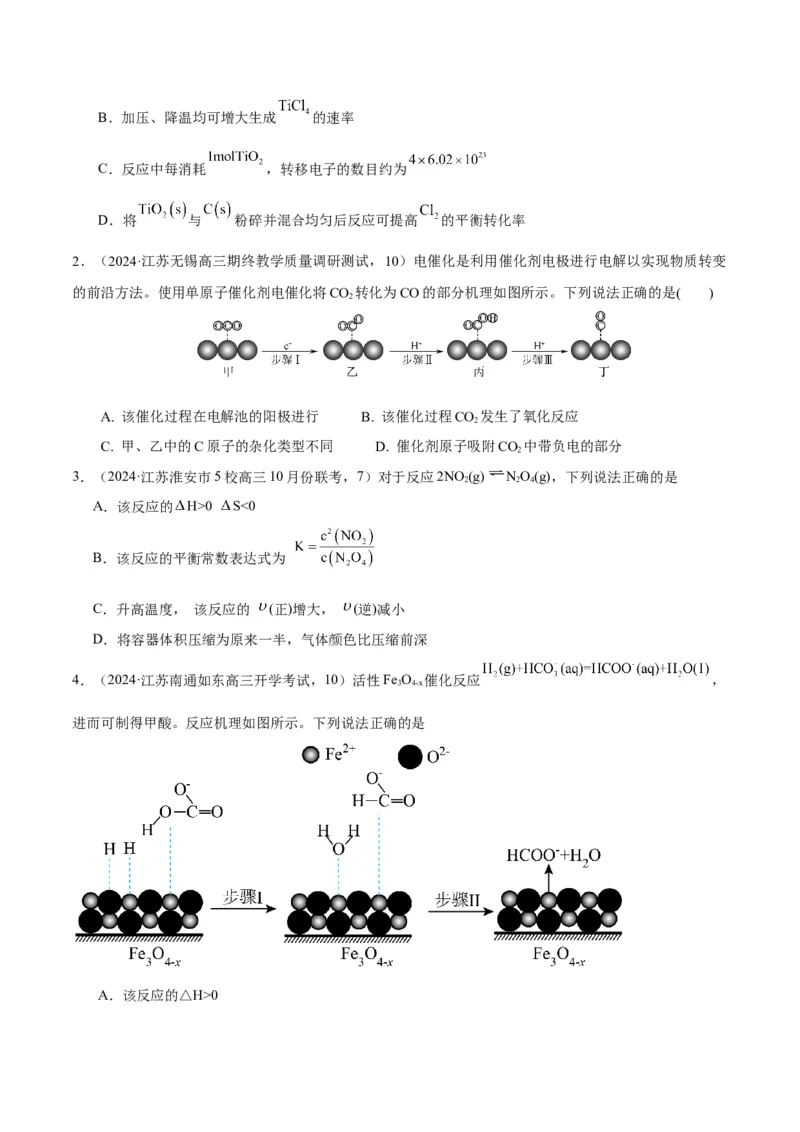
4.(2024·江苏南通如东高三开学考试,10)活性Fe O 催化反应 ,
3 4-x
进而可制得甲酸。反应机理如图所示。下列说法正确的是
A.该反应的△H>0B.该反应的平衡常数
C.反应前后,碳原子的杂化方式和化合价均没有发生变化
D.题图所示的反应机理中,步骤Ⅰ可理解为带部分负电荷的氢与HCO 中带部分正电荷的碳结合,
带部分正电荷的氢与带部分负电荷的羟基氧结合生成水,HCO 转化为的HCOO-
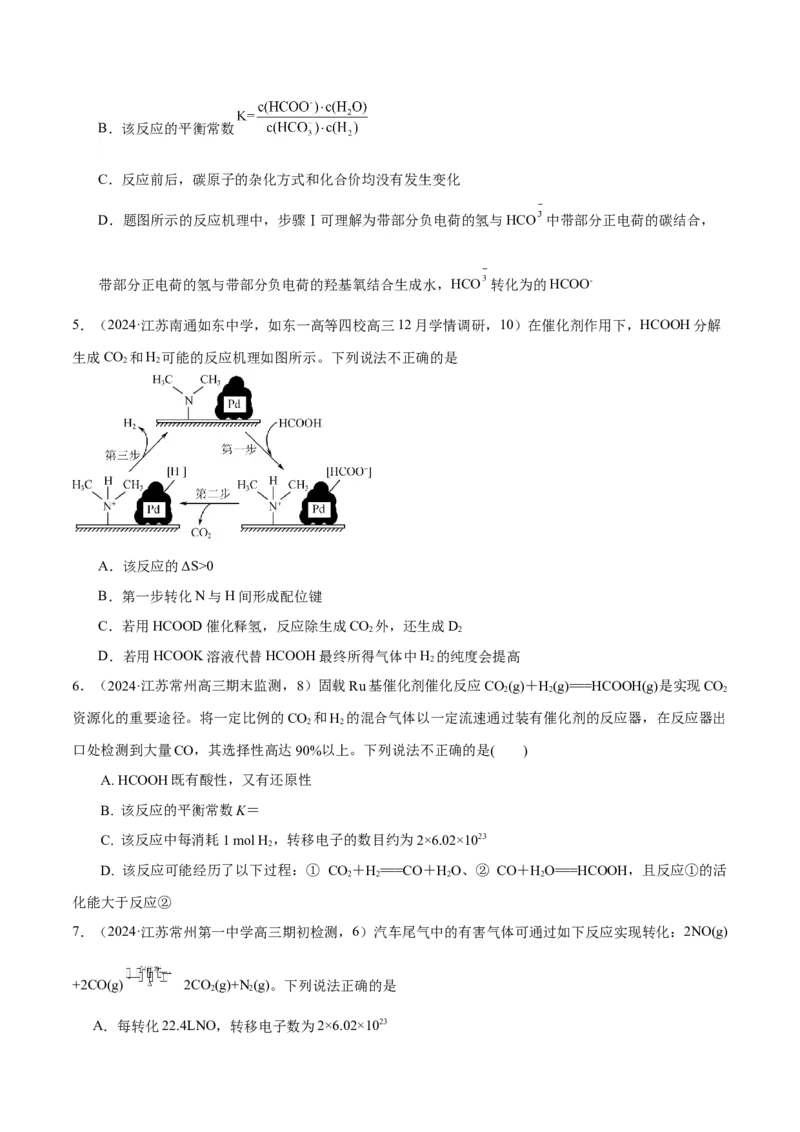
5.(2024·江苏南通如东中学,如东一高等四校高三12月学情调研,10)在催化剂作用下,HCOOH分解
生成CO 和H 可能的反应机理如图所示。下列说法不正确的是
2 2
A.该反应的ΔS>0
B.第一步转化N与H间形成配位键
C.若用HCOOD催化释氢,反应除生成CO 外,还生成D
2 2
D.若用HCOOK溶液代替HCOOH最终所得气体中H 的纯度会提高
2
6.(2024·江苏常州高三期末监测,8)固载Ru基催化剂催化反应CO(g)+H(g)===HCOOH(g)是实现CO
2 2 2
资源化的重要途径。将一定比例的CO 和H 的混合气体以一定流速通过装有催化剂的反应器,在反应器出
2 2
口处检测到大量CO,其选择性高达90%以上。下列说法不正确的是( )
A. HCOOH既有酸性,又有还原性
B. 该反应的平衡常数K=
C. 该反应中每消耗1 mol H ,转移电子的数目约为2×6.02×1023
2
D. 该反应可能经历了以下过程:① CO +H===CO+HO、② CO+HO===HCOOH,且反应①的活
2 2 2 2
化能大于反应②
7.(2024·江苏常州第一中学高三期初检测,6)汽车尾气中的有害气体可通过如下反应实现转化:2NO(g)
+2CO(g) 2CO(g)+N(g)。下列说法正确的是
2 2
A.每转化22.4LNO,转移电子数为2×6.02×1023B.其他条件相同,使用催化剂,可提高活化分子百分数,降低反应的焓变
C.反应的平衡常数K=
D.该反应ΔH<0
8.(2024·江苏常州八校10月调研,8)以NaCl为原料,可制取Na、NaO、NaOH和NaCO 等。
2 2 2 3
NaCO,可用侯氏制碱法制取,主要涉及如下反应:
2 3
N(g)+3H(g) 2NH (g) ΔH=-92.4kJ·mol-1
2 2 3
NaCl+NH +CO +H O=NaHCO ↓+NHCl
3 2 2 3 4
2NaHCO NaCO+CO ↑+H O
3 2 3 2 2
对于反应N(g)+3H(g) 2NH (g),下列说法正确的是
2 2 3
A.该反应的ΔS>0
B.该反应的平衡常数可表示为
C.其他条件相同,增大 ,H 转化率减小
2
D.使用催化剂能降低该反应的焓变
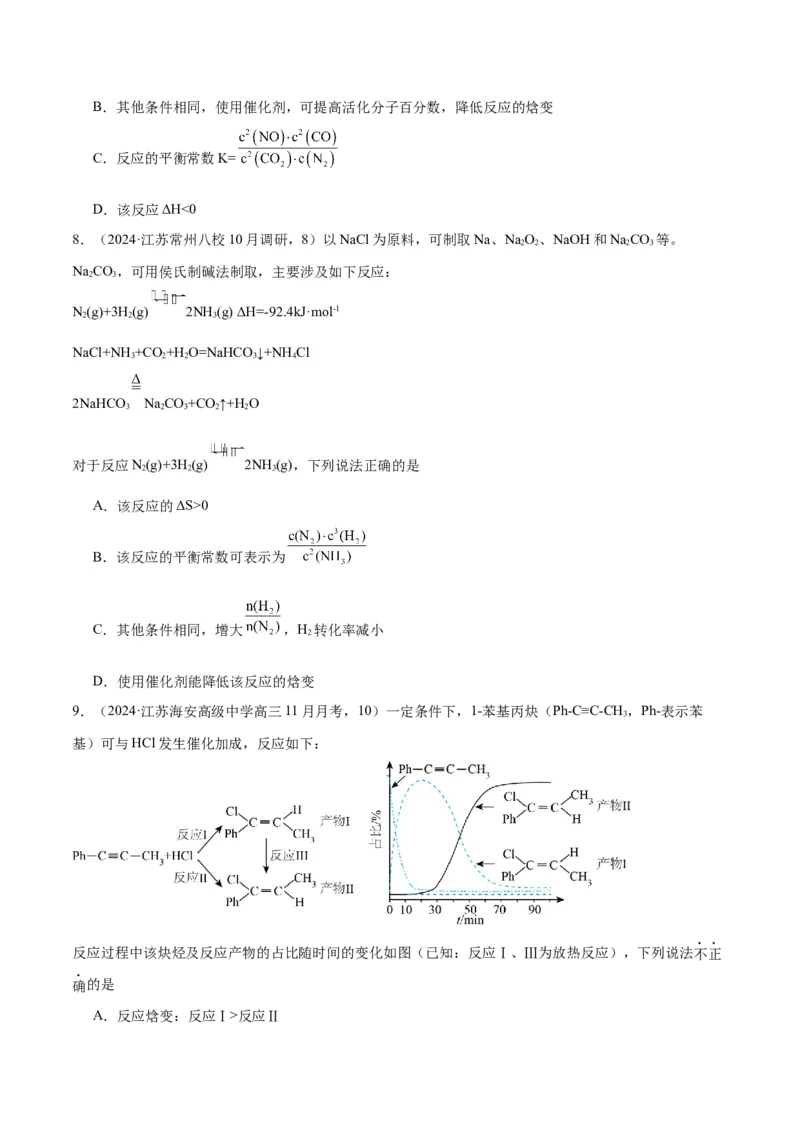
9.(2024·江苏海安高级中学高三11月月考,10)一定条件下,1-苯基丙炔(Ph-C≡C-CH ,Ph-表示苯
3
基)可与HCl发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应Ⅰ、Ⅲ为放热反应),下列说法不正
确的是
A.反应焓变:反应Ⅰ>反应ⅡB.反应活化能:反应Ⅰ<反应Ⅱ
C.增加 浓度可使平衡时产物Ⅱ比产物Ⅰ的值增加
D.选择相对较短的反应时间,及时分离可获得高产率的产物I
10.(2024·江苏华罗庚中学高三测试,
)在恒温恒容的密闭容器中发生 △H<0,T℃时,平衡常数为
K,下列说法正确的是
A.该反应在任何温度下都可自发进行
B.T℃时,若 K
1 2
B.反应①②的ΔH均小于0
C.CO中的C原子提供孤电子对与Fe2⁺配位
D.用高压氧舱治疗CO中毒时,平衡②逆向移动
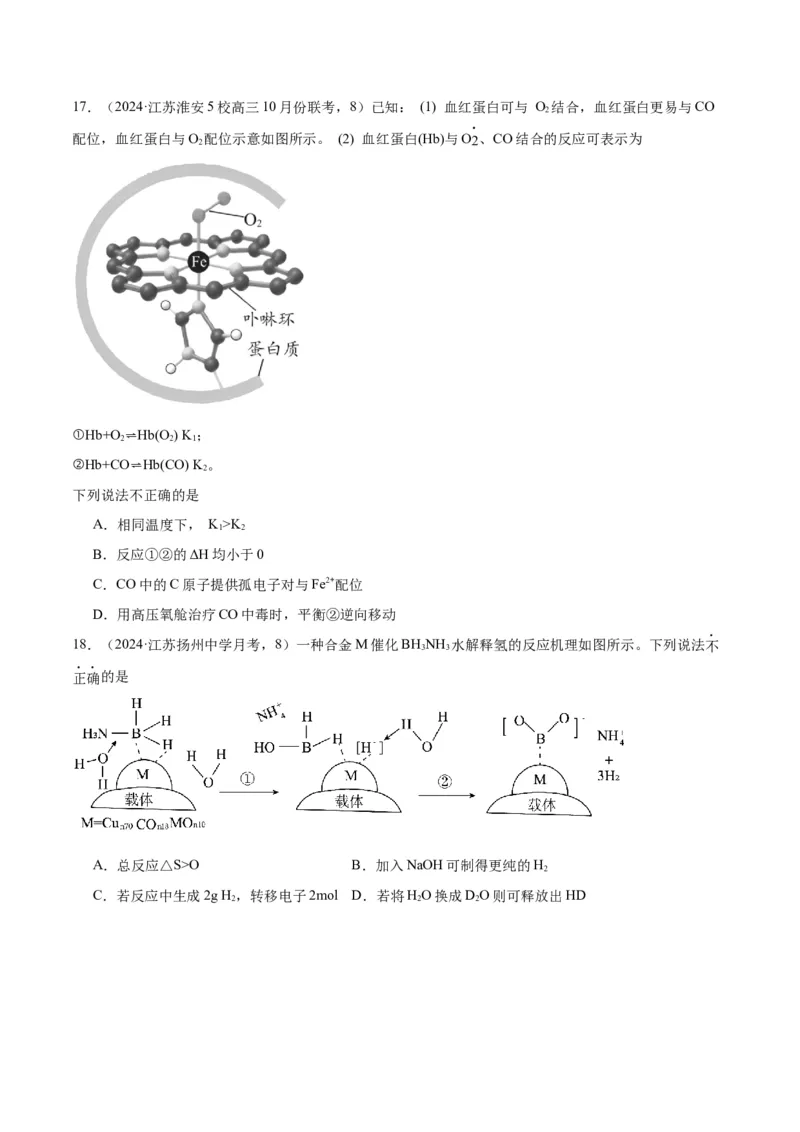
18.(2024·江苏扬州中学月考,8)一种合金M催化BHNH 水解释氢的反应机理如图所示。下列说法不
3 3
正确的是
A.总反应△S>O B.加入NaOH可制得更纯的H
2
C.若反应中生成2g H ,转移电子2mol D.若将HO换成DO则可释放出HD
2 2 2