文档内容
素养说明:高考中的新型化学电源,一般具有高能环保、经久耐用、电压稳定、比
能量(单位质量释放的能量)高等特点。由于该类试题题材广、信息新、陌生度大,
因此许多考生感觉难度大。但应用的解题原理仍然还是原电池的基础知识,只要
细心分析,实际上得分相对比较容易。
1.新型燃料电池(Fuel Cell)
燃料电池是利用氢气、碳、甲醇、硼氢化物、天然气等为燃料与氧气或空气进行反
应,将化学能直接转化成电能的一类原电池。其特点是:(1)有两个相同的多孔电
极,同时电极不参与反应(掺杂适当的催化剂)。(2)不需要将还原剂和氧化剂全
部储藏在电池内。(3)能量转换率较高,超过80%(普通燃烧能量转换率30%多)。
【解题模板】
2.可充电电池
对于一般的电池而言,充电电池具有一定的可逆性,在放电时,它是原电池装置;
在充电时,它是电解过程,是一种经济、环保、电量足、适合大功率、长时间使用的
电器。
【模型示例】 镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高且
平稳,因此成为人们研制绿色电池所关注的重点。有一种镁二次电池的反应为
xMg+Mo S Mg Mo S 。下列说法错误的是( )
3 4 x 3 4
A.放电时Mg2+向正极移动
B.放电时正极的电极反应式为Mo S +2xe-===Mo S
3 4 3
C.放电时Mo S 发生氧化反应
3 4
D.充电时阴极的电极反应为xMg2++2xe-===xMg
【解题模板】答案 C
[题型专练]
1.(2016·课标全国Ⅲ,11)锌—空气燃料电池可用作电动车动力电源,电池的电
解质溶液为KOH溶液,反应为2Zn+O +4OH-+2H O===2Zn(OH)。下列说法
2 2
正确的是( )
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-)逐渐减小
C.放电时,负极反应为:Zn+4OH--2e-===Zn(OH)
D.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况)
解析 A项,充电时,电解质溶液中K+向阴极移动,错误;B项,充电时,总反应
方程式为2Zn(OH)=====2Zn+O ↑+4OH-+2H O,所以电解质溶液中c(OH
2 2
-)逐渐增大,错误;C项,在碱性环境中负极Zn失电子生成的Zn2+将与OH―结
合生成Zn(OH),正确;D项,O ~4e-,故电路中通过2 mol电子,消耗氧气0.5
2
mol,在标准状况时体积为11.2 L,错误。
答案 C
2.(2015·江苏化学,10)一种熔融碳酸盐燃料电池原理示意如图。下列有关该电
池的说法正确的是( )A.反应CH +H O=====3H +CO,每消耗1 mol CH 转移12 mol电子
4 2 2 4
B.电极A上H 参与的电极反应为H +2OH--2e-===2H O
2 2 2
C.电池工作时,CO向电极B移动
D.电极B上发生的电极反应为O +2CO +4e-===2CO
2 2
解析 A项, ,则该反应中每消耗1 mol CH 转移6 mol电子,
4
错误;该电池的传导介质为熔融的碳酸盐,所以A电极即负极上H 参与的电极反
2
应为H -2e-+CO===CO +H O,错误;C项,原电池工作时,阴离子移向负极,
2 2 2
而B极是正极,错误;D项,B电极即正极上O 参与的电极反应为O +4e-+
2 2
2CO ===2CO,正确。
2
答案 D
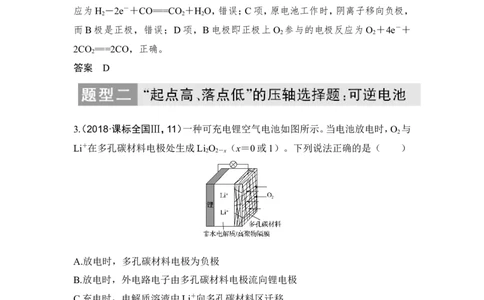
3(. 2018·课标全国Ⅲ,11)一种可充电锂空气电池如图所示。当电池放电时,O 与
2
Li+在多孔碳材料电极处生成Li O (x=0或1)。下列说法正确的是( )
2 2-x
A.放电时,多孔碳材料电极为负极
B.放电时,外电路电子由多孔碳材料电极流向锂电极
C.充电时,电解质溶液中Li+向多孔碳材料区迁移
D.充电时,电池总反应为Li O ===2Li+O
2 2-x 2
解析 根据电池工作原理,多孔碳材料吸附O ,O 在此获得电子,所以多孔碳材
2 2
料电极为电池的正极,A项错误;放电时电子从负极(锂电极)流出,通过外电路
流向正极(多孔碳材料电极),B项错误;Li+带正电荷,充电时,应该向电解池的
阴极(锂电极)迁移,C项错误;充电时,电池总反应为Li O ===2Li+O ,D项正
2 2-x 2
确。答案 D
4(. 2018·课标全国Ⅲ,11)全固态锂硫电池能量密度高、成本低,其工作原理如图
所示,其中电极a常用掺有石墨烯的S 材料,电池反应为:16Li+xS ===8Li S
8 8 2 x
(2≤x≤8)。下列说法错误的是( )
A.电池工作时,正极可发生反应:2Li S +2Li++2e-===3Li S
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中Li S 的量越多
2 2
解析 A项,原电池电解质中阳离子移向正极,根据全固态锂硫电池工作原理图
示中Li+移动方向可知,电极a为正极,正极发生还原反应,由总反应可知正极依
次发生S →Li S →Li S →Li S →Li S 的还原反应,正确;B项,电池工作时负极
8 2 8 2 6 2 4 2 2
电极方程式为:Li-e-===Li+,当外电路中流过0.02 mol电子时,负极消耗的Li
的物质的量为0.02 mol,其质量为0.14 g,正确;C项,石墨烯具有良好的导电性,
故可以提高电极a的导电能力,正确;D项,电池充电时为电解池,此时电解总反
应为8Li S 16Li+xS (2≤x≤8),故Li S 的量会越来越少,错误。
2 x 8 2 2
答案 D
5.(2016·课标全国Ⅱ,11)MgAgCl电池是一种以海水为电解质溶液的水激活电
池。下列说法错误的是( )
A.负极反应式为Mg-2e-===Mg2+
B.正极反应式为Ag++e-===Ag
C.电池放电时Cl-由正极向负极迁移D.负极会发生副反应Mg+2H O===Mg(OH) +H ↑
2 2 2
解析 首先从题干信息“Mg-AgCl电池”所提供的电极材料判断电池类型,属
于Cu-Zn型原电池,应用模型思想推断出电池电化学原理:活泼金属Mg做负
极,含金属阳离子的AgCl做正极,电池反应式为:Mg+2AgCl===MgCl +2Ag;
2
其次,判断各选项正误: B错误,因为AgCl难溶于水,正极发生还原反应的Ag+
存在形式为AgCl,因而正极反应式:AgCl+e-===Ag+Cl-。
答案 B
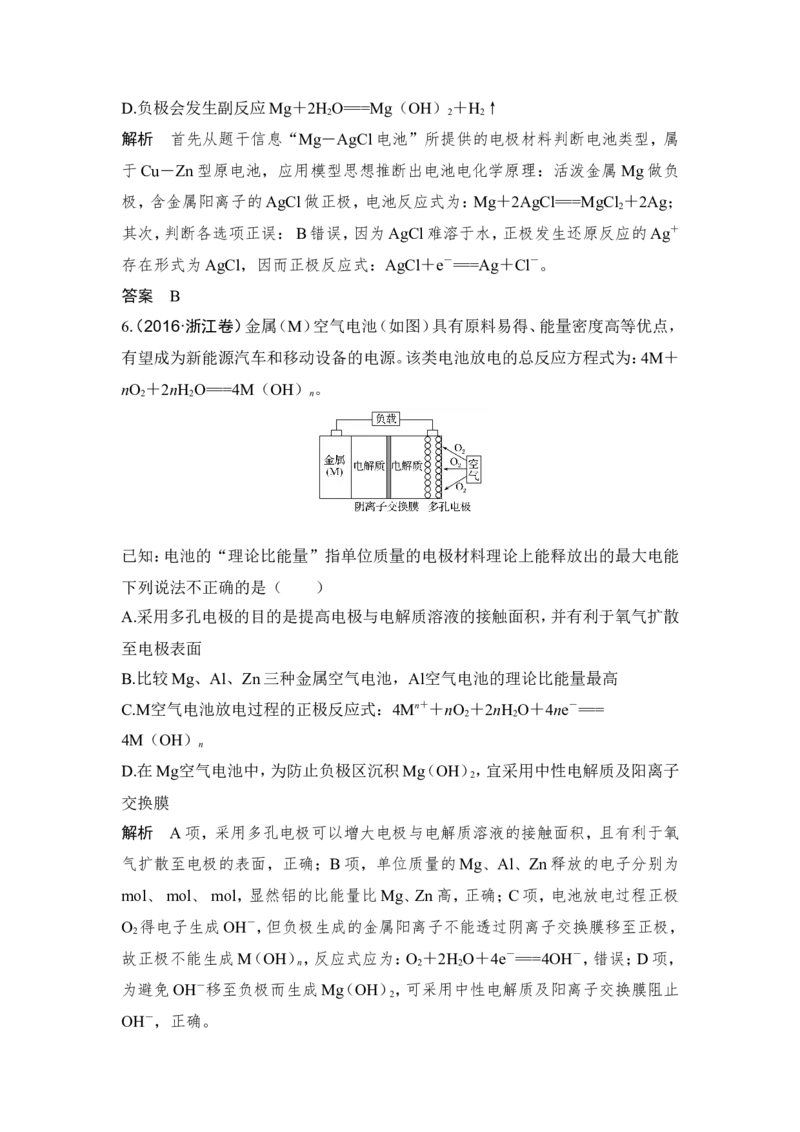
6(. 2016·浙江卷)金属(M)空气电池(如图)具有原料易得、能量密度高等优点,
有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+
nO +2nH O===4M(OH) 。
2 2 n
已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能
下列说法不正确的是( )
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散
至电极表面
B.比较Mg、Al、Zn三种金属空气电池,Al空气电池的理论比能量最高
C.M空气电池放电过程的正极反应式:4Mn++nO +2nH O+4ne-===
2 2
4M(OH)
n
D.在Mg空气电池中,为防止负极区沉积Mg(OH),宜采用中性电解质及阳离子
2
交换膜
解析 A项,采用多孔电极可以增大电极与电解质溶液的接触面积,且有利于氧
气扩散至电极的表面,正确;B项,单位质量的Mg、Al、Zn释放的电子分别为
mol、 mol、 mol,显然铝的比能量比Mg、Zn高,正确;C项,电池放电过程正极
O 得电子生成OH-,但负极生成的金属阳离子不能透过阴离子交换膜移至正极,
2
故正极不能生成M(OH),反应式应为:O +2H O+4e-===4OH-,错误;D项,
n 2 2
为避免OH-移至负极而生成Mg(OH),可采用中性电解质及阳离子交换膜阻止
2
OH-,正确。答案 C