文档内容
2022 年湖北省孝感新高考联考协作体 9 月高二考试
高二化学试卷
命题学校:孝感一中 命题教师:丁祖闯 审题学校:应城一中
考试时间:2022年9月9日下午14:30−17:05 试卷满分:100分
注意事项:
1.答卷前,考生务必将自己的姓名、考号等填写在答题卡和试卷指定的位置上。
2.回答选择题时,选出每题答案后,用铅笔把答案卡对应题目的答案标号涂黑。如需要改动,先用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷上无效。
可能用到的相对原子质量:H 1 Li 7 C 12 O 16 Na 23 Al 27 Ca 40
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1. 化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是
A.炖排骨汤时加点醋味道更鲜
B.加入明矾后泥水变澄清
C.北京冬奥会场馆使用CO 跨临界直冷制冰
2
D.科学家成功将CO 转化为淀粉或葡萄糖
2
2. 下列离子方程式正确的是
A.Cl 通入冷的NaOH溶液: Cl +6OH− =5Cl−+ClO−+3H O
2 2 3 2
B.用醋酸和淀粉-KI溶液检验加碘盐中的IO−:IO−+5I−+6H+ =3I +3H O
3 3 2 2
C.FeSO 溶液中加入H O 若产生沉淀:2Fe2++H O +4H O=2Fe(OH) ↓+4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO−+Ba2++OH− =BaCO ↓+H O
3 2 3 3 2
3. 室温下,下列实验探究方案不能达到探究目的的是
..
选项 探究方案 探究目的
向盛有FeSO 溶液的试管中滴加几滴KSCN溶液,振荡,再
4
A Fe2+具有还原性
滴加几滴新制氯水,观察溶液颜色变化
向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,加热
2
B SO 具有氧化性
2
试管,观察溶液颜色变化
向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶
C Br 的氧化性比I 的强
2 2
液颜色变化
用pH计测量相同条件下,同浓度醋酸、盐酸的pH,比较
D CH COOH是弱电解质
3
溶液pH大小
A.A B.B C.C D.D
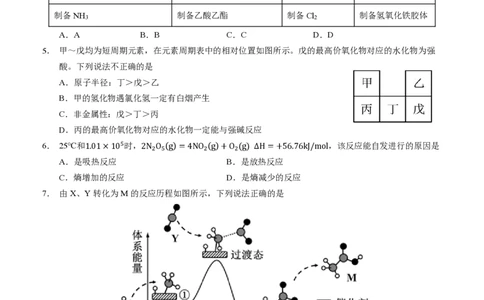
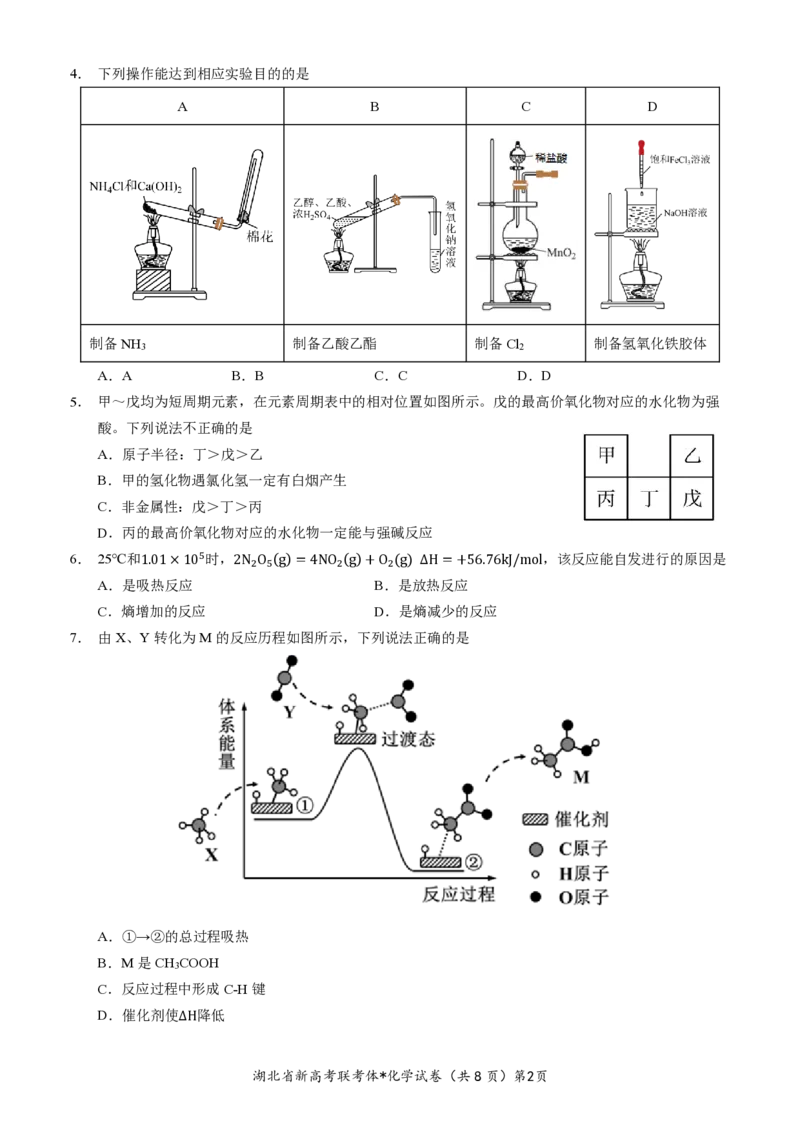
湖北省新高考联考体*化学试卷(共8页)第1页4. 下列操作能达到相应实验目的的是
A B C D
制备NH 制备乙酸乙酯 制备Cl 制备氢氧化铁胶体
3 2
A.A B.B C.C D.D
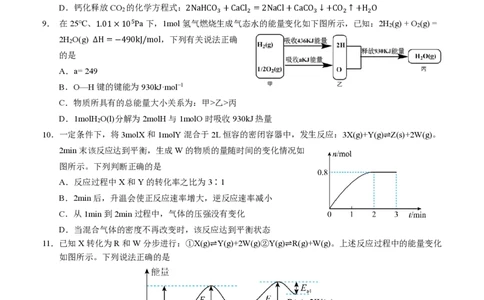
5. 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强
酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.甲的氢化物遇氯化氢一定有白烟产生
C.非金属性:戊>丁>丙
D.丙的最高价氧化物对应的水化物一定能与强碱反应
6. 25℃和1.01×105时,2N O (g)=4NO (g)+O (g) ∆H=+56.76kJ/mol,该反应能自发进行的原因是
2 5 2 2
A.是吸热反应 B.是放热反应
C.熵增加的反应 D.是熵减少的反应
7. 由X、Y转化为M的反应历程如图所示,下列说法正确的是
A.①→②的总过程吸热
B.M是CH COOH
3
C.反应过程中形成C-H键
D.催化剂使∆H降低
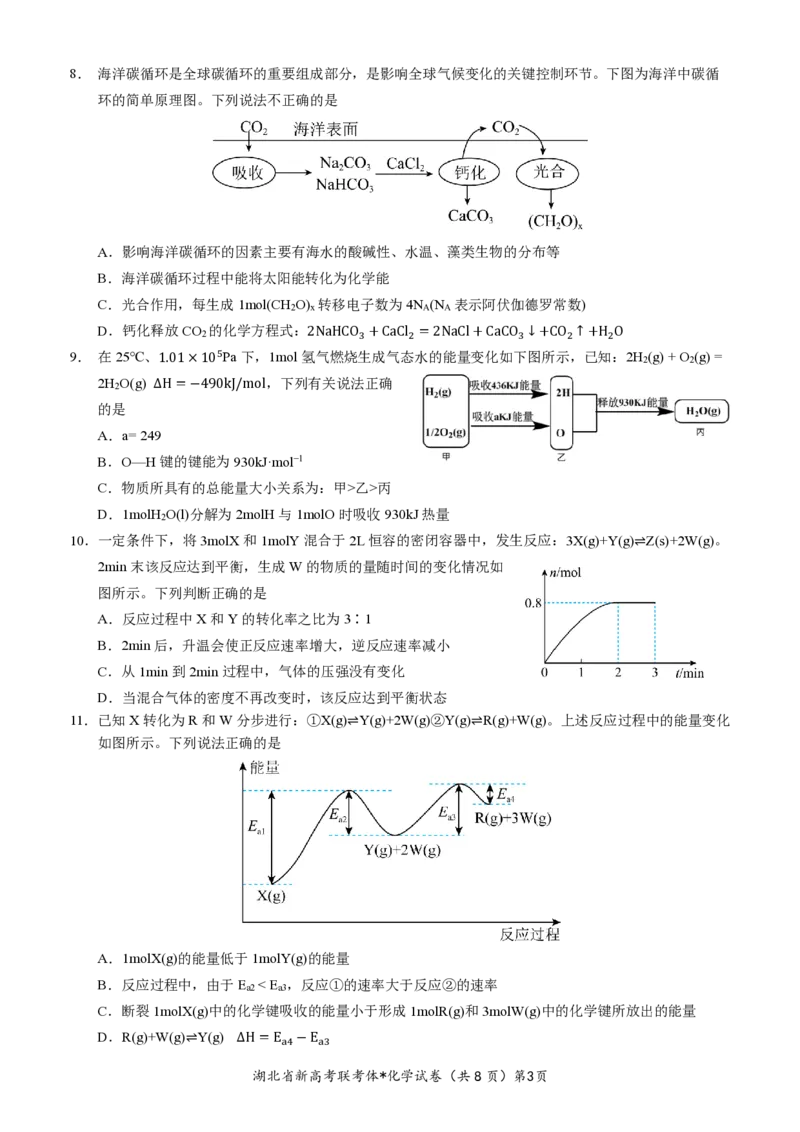
湖北省新高考联考体*化学试卷(共8页)第2页8. 海洋碳循环是全球碳循环的重要组成部分,是影响全球气候变化的关键控制环节。下图为海洋中碳循
环的简单原理图。下列说法不正确的是
A.影响海洋碳循环的因素主要有海水的酸碱性、水温、藻类生物的分布等
B.海洋碳循环过程中能将太阳能转化为化学能
C.光合作用,每生成1mol(CH O) 转移电子数为4N (N 表示阿伏伽德罗常数)
2 x A A
D.钙化释放CO 的化学方程式:2NaHCO +CaCl =2NaCl+CaCO ↓+CO ↑+H O
2 3 2 3 2 2
9. 在25℃、1.01×105Pa下,1mol氢气燃烧生成气态水的能量变化如下图所示,已知:2H (g) + O (g) =
2 2
2H O(g) ∆H=−490kJ/mol,下列有关说法正确
2
的是
A.a= 249
B.O—H键的键能为930kJ·mol−1
C.物质所具有的总能量大小关系为:甲>乙>丙
D.1molH O(l)分解为2molH与1molO时吸收930kJ热量
2
10.一定条件下,将3molX和1molY混合于2L恒容的密闭容器中,发生反应:3X(g)+Y(g)⇌Z(s)+2W(g)。
2min末该反应达到平衡,生成W的物质的量随时间的变化情况如
图所示。下列判断正确的是
A.反应过程中X和Y的转化率之比为3∶1
B.2min后,升温会使正反应速率增大,逆反应速率减小
C.从1min到2min过程中,气体的压强没有变化
D.当混合气体的密度不再改变时,该反应达到平衡状态
11.已知X转化为R和W分步进行:①X(g)⇌Y(g)+2W(g)②Y(g)⇌R(g)+W(g)。上述反应过程中的能量变化
如图所示。下列说法正确的是
A.1molX(g)的能量低于1molY(g)的能量
B.反应过程中,由于E < E ,反应①的速率大于反应②的速率
a2 a3
C.断裂1molX(g)中的化学键吸收的能量小于形成1molR(g)和3molW(g)中的化学键所放出的能量
D.R(g)+W(g)⇌Y(g) ∆H=E −E
a4 a3
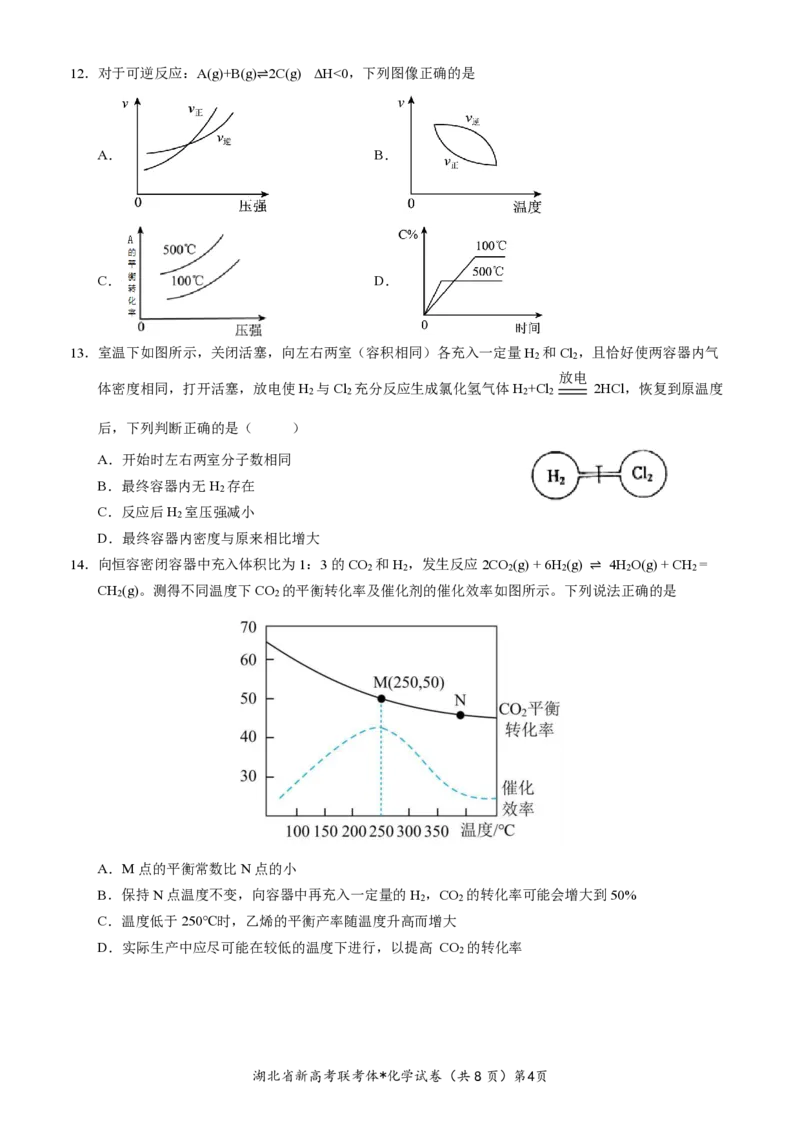
湖北省新高考联考体*化学试卷(共8页)第3页12.对于可逆反应:A(g)+B(g)⇌2C(g) ∆H<0,下列图像正确的是
A. B.
C. D.
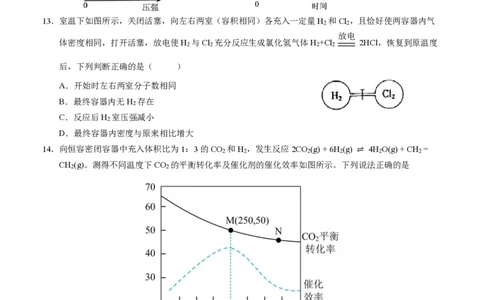
13.室温下如图所示,关闭活塞,向左右两室(容积相同)各充入一定量H 和Cl ,且恰好使两容器内气
2 2
放电
体密度相同,打开活塞,放电使H 与Cl 充分反应生成氯化氢气体H +Cl 2HCl,恢复到原温度
2 2 2 2
后,下列判断正确的是( )
A.开始时左右两室分子数相同
B.最终容器内无H 存在
2
C.反应后H 室压强减小
2
D.最终容器内密度与原来相比增大
14.向恒容密闭容器中充入体积比为1:3的CO 和H ,发生反应2CO (g) + 6H (g) ⇌ 4H O(g) + CH =
2 2 2 2 2 2
CH (g)。测得不同温度下CO 的平衡转化率及催化剂的催化效率如图所示。下列说法正确的是
2 2
A.M点的平衡常数比N点的小
B.保持N点温度不变,向容器中再充入一定量的H ,CO 的转化率可能会增大到50%
2 2
C.温度低于250℃时,乙烯的平衡产率随温度升高而增大
D.实际生产中应尽可能在较低的温度下进行,以提高 CO 的转化率
2
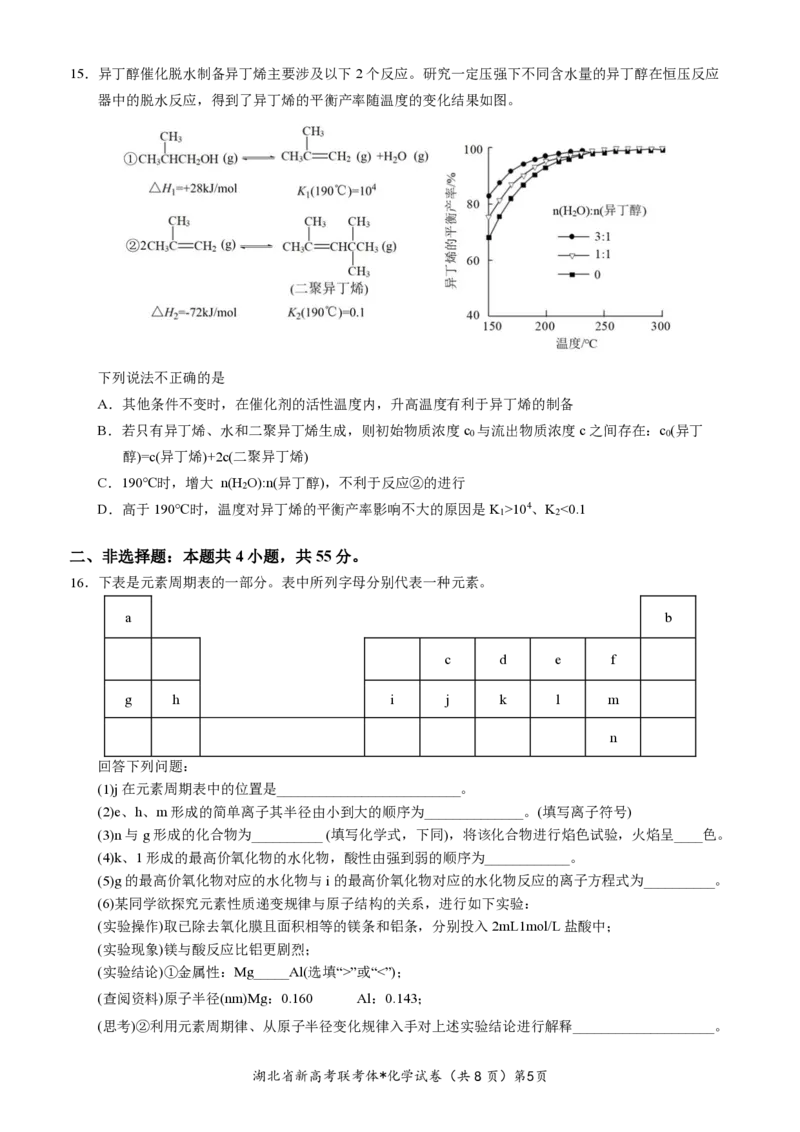
湖北省新高考联考体*化学试卷(共8页)第4页15.异丁醇催化脱水制备异丁烯主要涉及以下2个反应。研究一定压强下不同含水量的异丁醇在恒压反应
器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如图。
下列说法不正确的是
A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备
B.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度c 与流出物质浓度c之间存在:c (异丁
0 0
醇)=c(异丁烯)+2c(二聚异丁烯)
C.190℃时,增大 n(H O):n(异丁醇),不利于反应②的进行
2
D.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是K >104、K <0.1
1 2
二、非选择题:本题共 4小题,共 55分。
16.下表是元素周期表的一部分。表中所列字母分别代表一种元素。
a b
c d e f
g h i j k l m
n
回答下列问题:
(1)j在元素周期表中的位置是__________________________。
(2)e、h、m形成的简单离子其半径由小到大的顺序为______________。(填写离子符号)
(3)n与g形成的化合物为__________ (填写化学式,下同),将该化合物进行焰色试验,火焰呈____色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为____________。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为__________。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律、从原子半径变化规律入手对上述实验结论进行解释____________________。
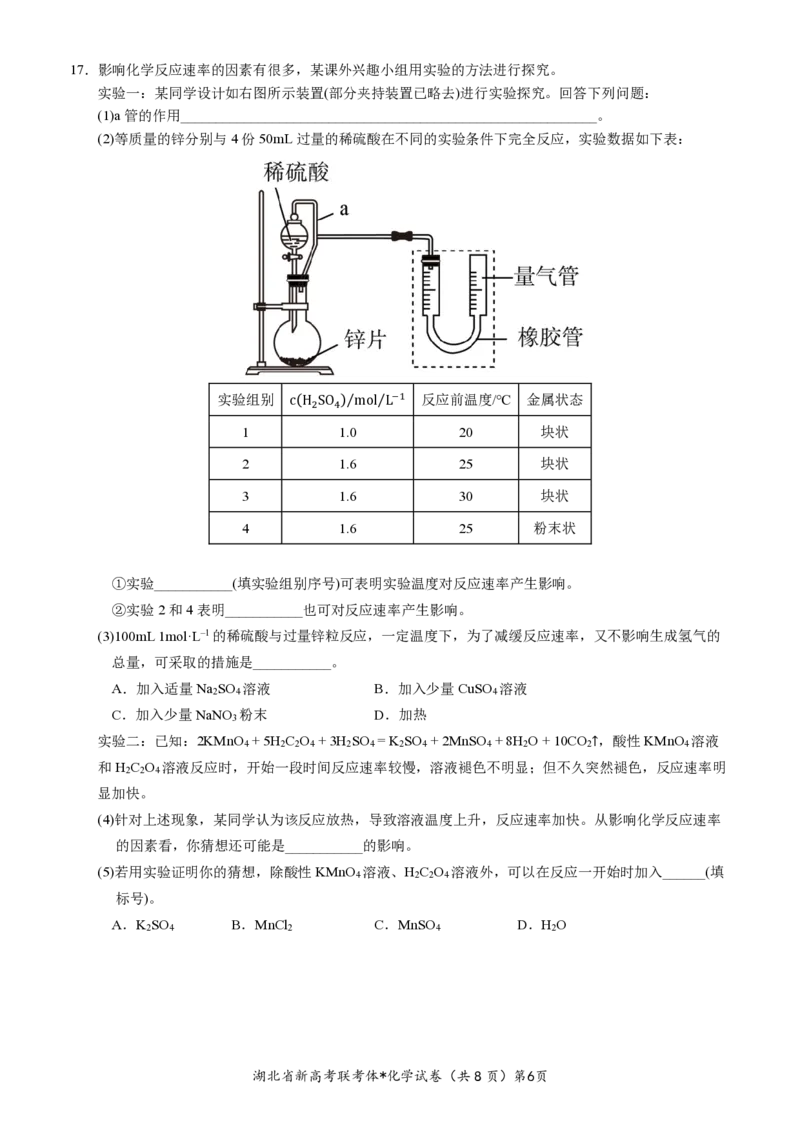
湖北省新高考联考体*化学试卷(共8页)第5页17.影响化学反应速率的因素有很多,某课外兴趣小组用实验的方法进行探究。
实验一:某同学设计如右图所示装置(部分夹持装置已略去)进行实验探究。回答下列问题:
(1)a管的作用___________________________________________________________。
(2)等质量的锌分别与4份50mL过量的稀硫酸在不同的实验条件下完全反应,实验数据如下表:
实验组别 c(H SO )⁄mol⁄L−1 反应前温度/℃ 金属状态
2 4
1 1.0 20 块状
2 1.6 25 块状
3 1.6 30 块状
4 1.6 25 粉末状
①实验___________(填实验组别序号)可表明实验温度对反应速率产生影响。
②实验2和4表明___________也可对反应速率产生影响。
(3)100mL 1mol·L‒1的稀硫酸与过量锌粒反应,一定温度下,为了减缓反应速率,又不影响生成氢气的
总量,可采取的措施是___________。
A.加入适量Na SO 溶液 B.加入少量CuSO 溶液
2 4 4
C.加入少量NaNO 粉末 D.加热
3
实验二:已知:2KMnO + 5H C O + 3H SO = K SO + 2MnSO + 8H O + 10CO ↑,酸性KMnO 溶液
4 2 2 4 2 4 2 4 4 2 2 4
和H C O 溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明
2 2 4
显加快。
(4)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快。从影响化学反应速率
的因素看,你猜想还可能是___________的影响。
(5)若用实验证明你的猜想,除酸性KMnO 溶液、H C O 溶液外,可以在反应一开始时加入______(填
4 2 2 4
标号)。
A.K SO B.MnCl C.MnSO D.H O
2 4 2 4 2
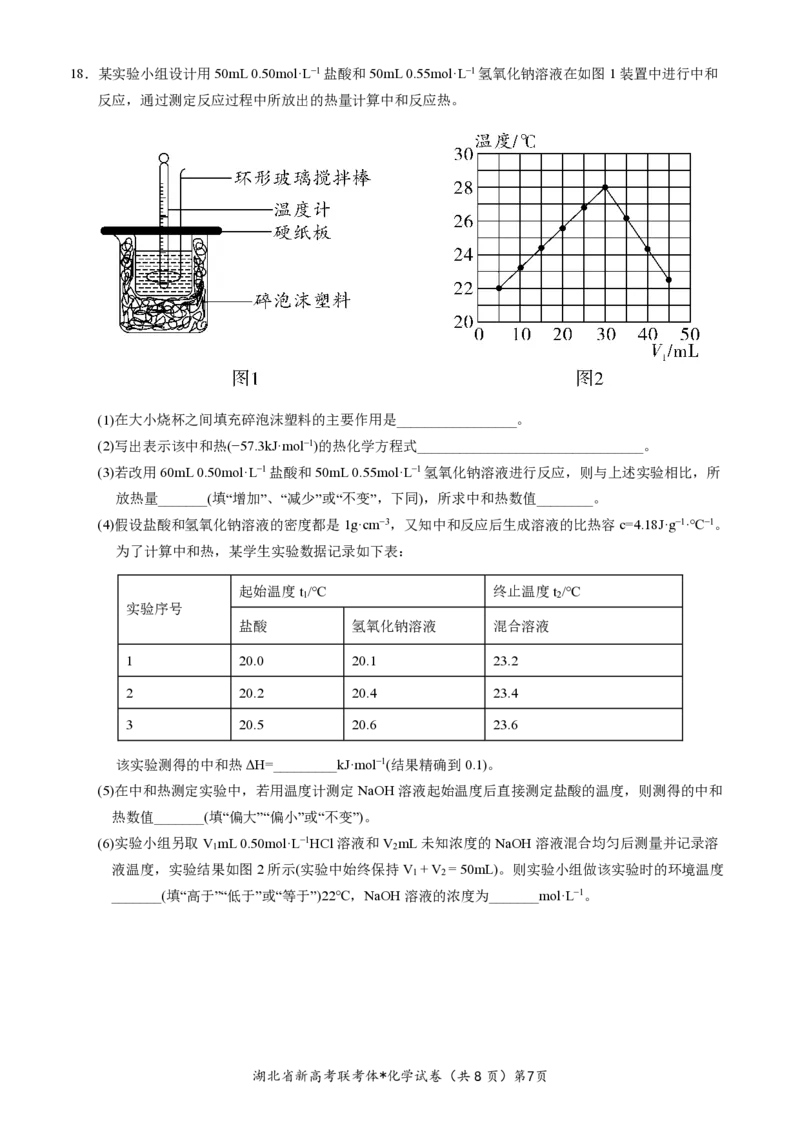
湖北省新高考联考体*化学试卷(共8页)第6页18.某实验小组设计用50mL 0.50mol·L−1盐酸和50mL 0.55mol·L−1氢氧化钠溶液在如图1装置中进行中和
反应,通过测定反应过程中所放出的热量计算中和反应热。
(1)在大小烧杯之间填充碎泡沫塑料的主要作用是_________________。
(2)写出表示该中和热(−57.3kJ·mol−1)的热化学方程式________________________________。
(3)若改用60mL 0.50mol·L−1盐酸和50mL 0.55mol·L−1氢氧化钠溶液进行反应,则与上述实验相比,所
放热量_______(填“增加”、“减少”或“不变”,下同),所求中和热数值________。
(4)假设盐酸和氢氧化钠溶液的密度都是1g·cm−3,又知中和反应后生成溶液的比热容c=4.18J·g−1·℃−1。
为了计算中和热,某学生实验数据记录如下表:
起始温度t /℃ 终止温度t /℃
1 2
实验序号
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
该实验测得的中和热ΔH=_________kJ·mol−1(结果精确到0.1)。
(5)在中和热测定实验中,若用温度计测定NaOH溶液起始温度后直接测定盐酸的温度,则测得的中和
热数值_______(填“偏大”“偏小”或“不变”)。
(6)实验小组另取V mL 0.50mol·L−1HCl溶液和V mL未知浓度的NaOH溶液混合均匀后测量并记录溶
1 2
液温度,实验结果如图2所示(实验中始终保持V + V = 50mL)。则实验小组做该实验时的环境温度
1 2
_______(填“高于”“低于”或“等于”)22℃,NaOH溶液的浓度为_______mol·L−1。
湖北省新高考联考体*化学试卷(共8页)第7页19.2022年冬奥会的国家速滑馆“冰丝带”采用二氧化碳跨临界制冰,CO 的资源化可以推动经济高质量发
2
展和生态环境质量的持续改善。
Ⅰ. 二氧化碳催化加氢可合成低碳烯烃,合成乙烯(C H )的反应为:
2 4
2CO
2
(g)+6H
2
(g)⇌C
2
H
4
(g)+4H
2
O(g) ∆H, 该过程分两步进行:
第一步:CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g) ∆H
1
= +41.3 kJ·mol−1
第二步:2CO(g)+4H
2
(g)⇌C
2
H
4
(g)+2H
2
O(g) ∆H
2
= −210.5 kJ·mol−1
(1)∆H=_______kJ/mol,该反应在_______(填“高温”“低温”或“任何温度”)下能自发进行。
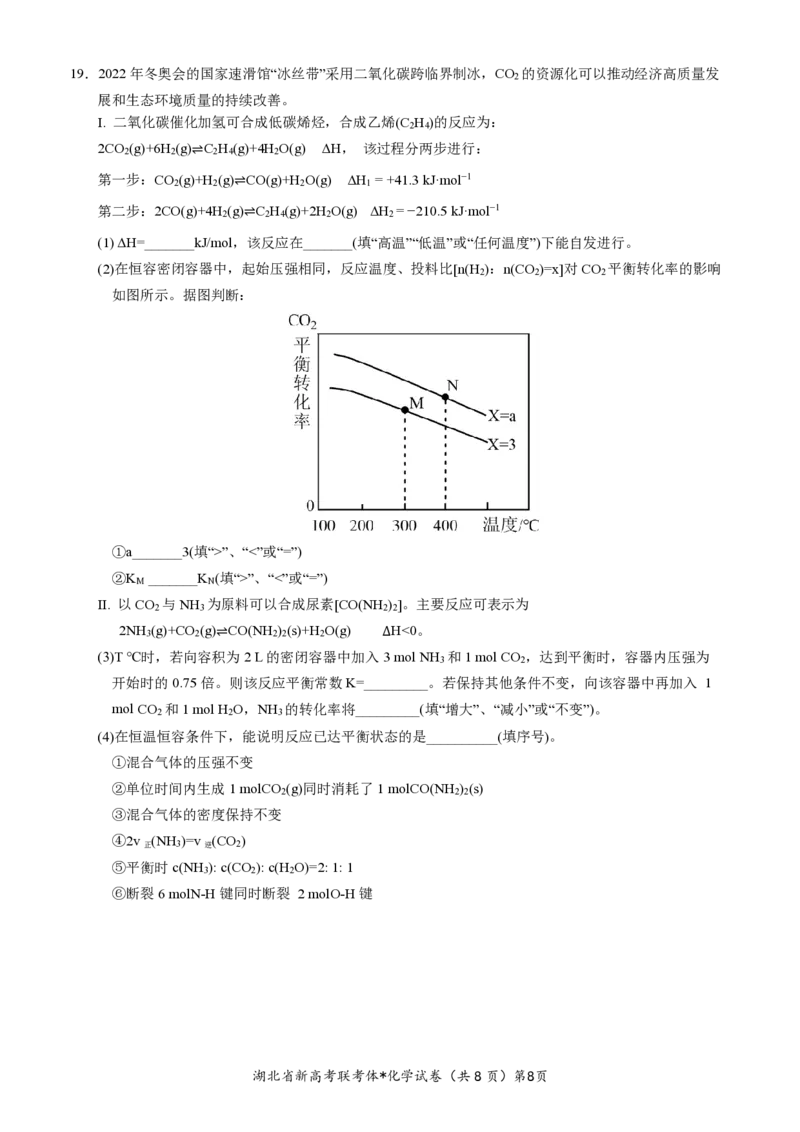
(2)在恒容密闭容器中,起始压强相同,反应温度、投料比[n(H ):n(CO )=x]对CO 平衡转化率的影响
2 2 2
如图所示。据图判断:
①a_______3(填“>”、“<”或“=”)
②K _______K (填“>”、“<”或“=”)
M N
Ⅱ. 以CO 与NH 为原料可以合成尿素[CO(NH ) ]。主要反应可表示为
2 3 2 2
2NH (g)+CO (g)⇌CO(NH ) (s)+H O(g) ∆H<0。
3 2 2 2 2
(3)T ℃时,若向容积为2 L 的密闭容器中加入3 mol NH
3
和1 mol CO
2
,达到平衡时,容器内压强为
开始时的0.75 倍。则该反应平衡常数K=_________。若保持其他条件不变,向该容器中再加入 1
mol CO 和1 mol H O,NH 的转化率将_________(填“增大”、“减小”或“不变”)。
2 2 3
(4)在恒温恒容条件下,能说明反应已达平衡状态的是__________(填序号)。
①混合气体的压强不变
②单位时间内生成1 molCO (g)同时消耗了1 molCO(NH ) (s)
2 2 2
③混合气体的密度保持不变
④2v
正
(NH
3
)=v
逆
(CO
2
)
⑤平衡时c(NH ): c(CO ): c(H O)=2: 1: 1
3 2 2
⑥断裂6 molN-H 键同时断裂 2 molO-H 键(cid:1)
湖北省新高考联考体*化学试卷(共8页)第8页