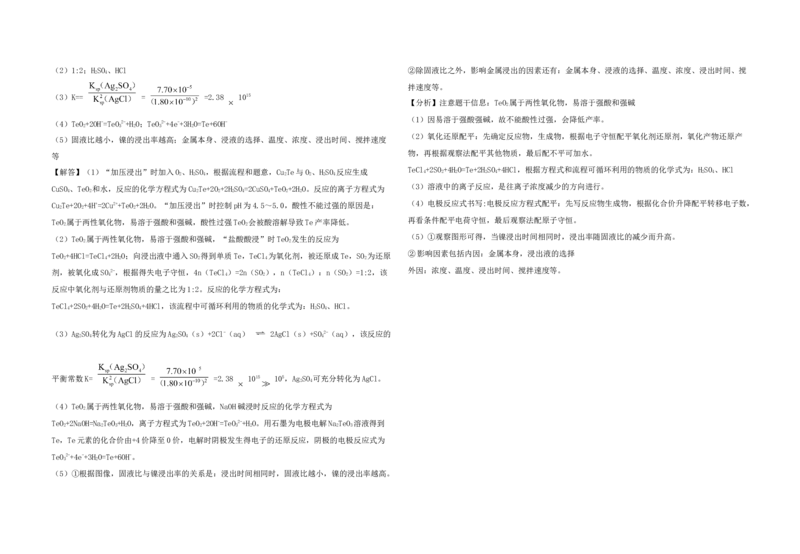文档内容
C.96 D.124
湖北高考模拟测试卷
4.下列指定反应的离子方程式正确的是( )
化学
A.酸化的NaIO 和NaI的溶液混合:I- +IO +6H+=I +3HO
3 2 2
可能用到的相对原子质量:H-1 C-12 N-14 0-16 F-19 S-32 C1-35.5 K-39 B.实验室用氯化铝溶液和氨水制备氢氧化铝:Al3++3OH-=Al(OH)↓
3
Ga-70 In-115 Sb-122
C.饱和NaCO 溶液与CaSO 固体反应:CO (aq)+CaSO(s) CaCO(s)+SO (aq)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有 2 3 4 4 3
一项是符合题目要求的。
D.(NH)Fe(SO) 溶液与过量NaOH溶液反应制Fe(OH) :Fe2++2OH-=Fe(OH) ↓
4 2 4 2 2 2
1.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工发展水平。下列说
5.下列有机物分子中所有原子一定不在同一平面内的是( )
法正确的是( )
A.乙烯
A.乙烯可作果实催熟剂
B.石油裂解气属于纯净物 B.苯乙烯( )
C.乙烯可使酸性高锰酸钾溶液褪色,说明乙烯具有漂白性
C.异戊烷
D.PE(聚乙烯)是由乙烯单体聚合而成,说明PE中含有碳碳双键
D.氯乙烯(CH=CHCl)
2
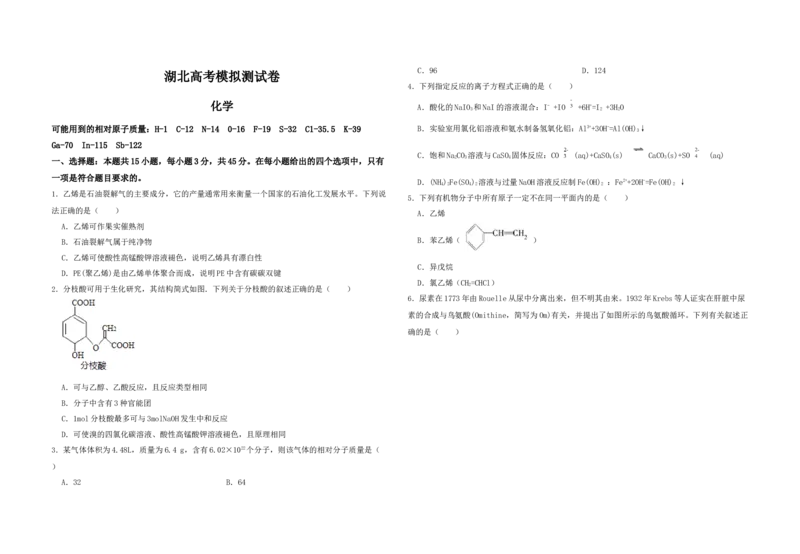
2.分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )
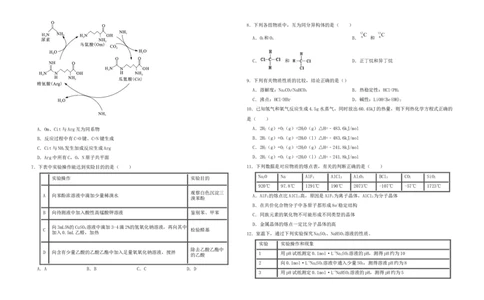
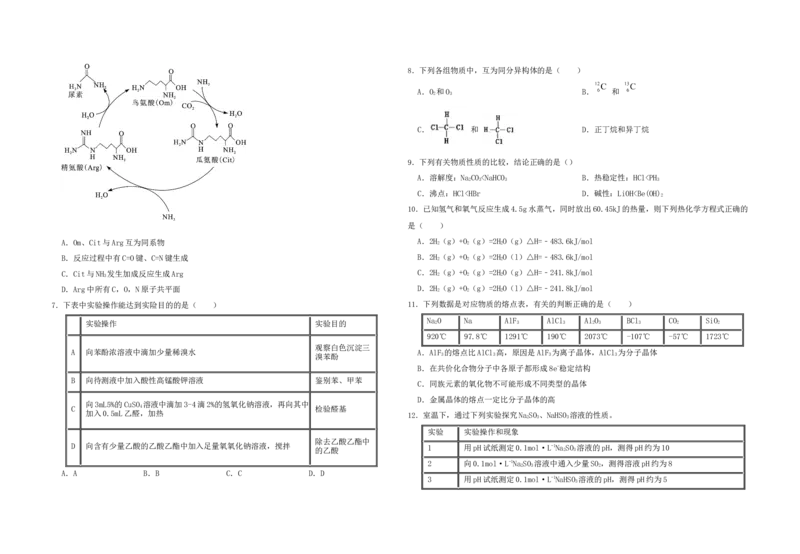
6.尿素在1773年由Rouelle从尿中分离出来,但不明其由来。1932年Krebs等人证实在肝脏中尿
素的合成与鸟氨酸(Omithine,简写为Om)有关,并提出了如图所示的鸟氨酸循环。下列有关叙述正
确的是( )
A.可与乙醇、乙酸反应,且反应类型相同
B.分子中含有3种官能团
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
3.某气体体积为4.48L,质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量是(
)
A.32 B.648.下列各组物质中,互为同分异构体的是( )
A.O 和O B. 和
2 3
C. 和 D.正丁烷和异丁烷
9.下列有关物质性质的比较,结论正确的是()
A.溶解度:NaCO c(HSO )+2c(SO )
C.实验3可以得出:K (HSO)·K (HSO) > K
a1 2 3 a2 2 3 w
D.实验4中反应后的溶液中存在:c(SO )+3c(SO )=c(HSO)
2 3
13.碳酸锶(SrCO)被广泛应用于电子工业、彩色显像管、陶瓷等行业,工业上以天青石矿(SrSO)
3 4
A.该电池隔膜左侧的电解液a可选用水性电解液
为原料制备碳酸锶的操作流程如下图:
B.放电时,若消耗1.5molCO 时,转移2mol电子
2
C.放电时,电子从锂电极流出,通过电解液流回锂电极,构成闭合回路
D.充电时,锂电极与外接电源的正极相连
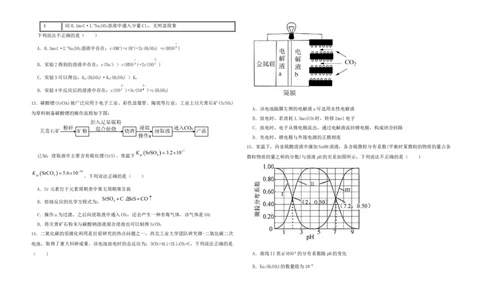
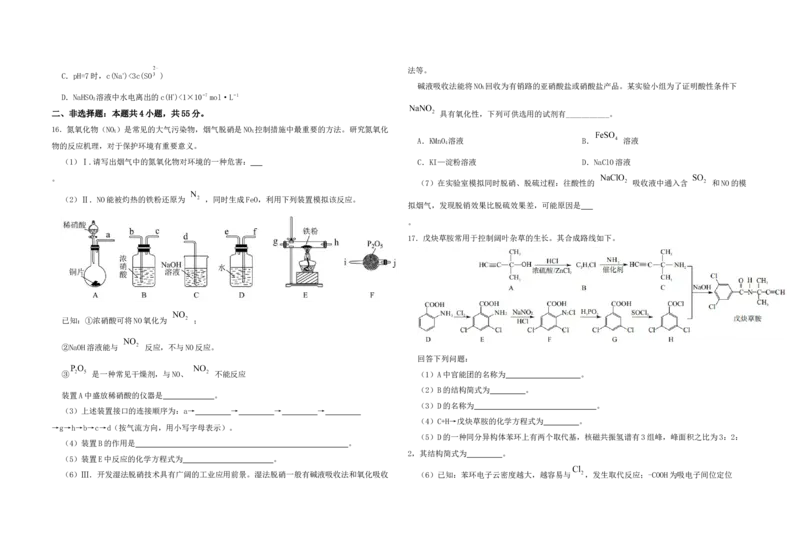
15.室温下,向亚硫酸溶液中滴加NaOH溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各
已知:浸取液中主要含有硫化锶(SrS)。常温下 微粒物质的量之和的分数)与溶液pH的关系如图所示。下列说法不正确的是( )
,下列说法正确的是( )
A.Sr元素位于元素周期表中第五周期第Ⅱ族
B.焙烧反应的化学方程式为:
C.操作a为过滤,之后向浸取液中通入CO,还会产生一种有毒气体,该气体是SO
2 2
D.将天青矿石粉末与碳酸钠溶液混合浸泡也可以制得SrCO
3
14.二氧化碳的资源化利用是目前研究的热点问题之一,西北工业大学团队研究锂-二氧化碳二次
电池,取得了重大科研成果。该电池放电时的总反应为:3CO+4Li=2LiCO+C,下列说法正确的是
2 2 3
( ) A.曲线II表示HSO 的分布系数随pH的变化
B.Ka(HSO)的数量级为10−8
2 2 3法等。
C.pH=7时,c(Na+)<3c(SO )
碱液吸收法能将NO 回收为有销路的亚硝酸盐或硝酸盐产品。某实验小组为了证明酸性条件下
X
D.NaHSO 溶液中水电离出的c(H+)<1×10−7 mol·L−1
3
二、非选择题:本题共4小题,共55分。 具有氧化性,下列可供选用的试剂有___________。
16.氮氧化物(NO)是常见的大气污染物,烟气脱硝是NO 控制措施中最重要的方法。研究氮氧化
X X
A.KMnO 溶液 B. 溶液
物的反应机理,对于保护环境有重要意义。 4
(1)Ⅰ.请写出烟气中的氮氧化物对环境的一种危害: C.KI—淀粉溶液 D.NaClO溶液
。
(7)在实验室模拟同时脱硝、脱硫过程:往酸性的 吸收液中通入含 和NO的模
(2)Ⅱ.NO能被灼热的铁粉还原为 ,同时生成FeO,利用下列装置模拟该反应。
拟烟气,发现脱销效果比脱硫效果差,可能原因是
。
17.戊炔草胺常用于控制阔叶杂草的生长。其合成路线如下。
已知:①浓硝酸可将NO氧化为 ;
②NaOH溶液能与 反应,不与NO反应。
回答下列问题:
③ 是一种常见干燥剂,与NO、 不能反应 (1)A中官能团的名称为 。
(2)B的结构简式为 。
装置A中盛放稀硝酸的仪器是 。
(3)D的名称为 。
(3)上述装置接口的连接顺序为:a→ → → →
(4)C+H→戊炔草胺的化学方程式为 。
→g→h→b→c→d(按气流方向,用小写字母表示)。
(5)D的一种同分异构体苯环上有两个取代基,核磁共振氢谱有3组峰,峰面积之比为3:2:
(4)装置B的作用是 。
2,其结构简式为 。
(5)装置E中反应的化学方程式为 。
(6)Ⅲ.开发湿法脱硝技术具有广阔的工业应用前景。湿法脱硝一般有碱液吸收法和氧化吸收 (6)已知:苯环电子云密度越大,越容易与 ,发生取代反应;-COOH为吸电子间位定位基,-NH 为给电子邻对位定位基。不直接使用苯甲酸而使用D合成G的原因是
2
。
18.在起始温度相同(T℃)的条件下,分别向容积相同的密闭容器甲、乙、丙中加入等量NHI(s),
4
发生反应:NHI(s) NH(g)+HI(g) ΔH>0,2HI(g) I(g)+H(g) ΔH>0,容器如图所示。
4 3 2 2
回答下列问题:
已知:在T℃时,2HI(g) I(g)+H(g)的平衡常数K= 。
2 2
(1)在甲容器中,不能作为2HI(g) I(g)+H(g)达到平衡的依据是 (填标号)。
2 2
①曲线b代表的变化曲线 (填化学式);
a.气体颜色不变 b.气体压强不变
②2min内,用NH 表示的反应速率为 ,HI的分解率为 。
3
c.气体温度不变 d.混合气体的平均相对分子质量不变
③T℃时,若在丙容器中加入I(g)和H(g)各1mol;反应达平衡后,放出7.6kJ的热量,则I(g)
2 2 2
(2)乙容器中反应达平衡后,再充入He,则反应2HI(g) I(g)+H(g)的平衡
2 2 与H(g)反应的热化学方程式为 。
2
(4)甲、乙、丙三个容器中反应均达到平衡时,I(g)的体积分数由大到小的顺序是
移动(填“正反应方向”“逆反应方向”或“不”)。 2
。
(3)在反应过程中,测得丙容器中HI、H 的物质的量(c)随时间(t)变化如图所示。
2
19.碲(Te)是一种第VIA族分散稀有元素,主要伴生于铜、镍、铅等金属矿藏中。TeO 属于两性氧
2
化物,难溶于水,易溶于强酸和强碱。工业上可从电解精炼铜的阳极泥(主要成分CuTe,还有少量
2
的Ag、Au)中提取碲。其工艺流程如下:(1)“加压浸出”生成TeO 的离子方程式为 ,“加压浸
2
出”时控制pH为4.5~5.0,酸性不能过强的原因是 。
(2)“盐酸酸浸”后将SO 通入浸出液即可得到单质碲,该反应中氧化剂与还原剂物质的量之
2
比为 ,该流程中可循环利用的物质是 (填化学式)。
(3)已知:K (AgSO)=7.70×10-5,K (AgCl)=1.80×10-10。盐酸酸浸时,“浸出渣1”中AgSO
sp 2 4 sp 2 4
可充分转化为AgC1。通过计算说明为什么可以实现充分转化
。
(4)NaOH碱浸时反应的离子方程式为 。流程中,电解过程用石墨
为电极得到碲,阴极的电极反应式为 。
(5)浸出法是工业提取金属常用的方法,某实验小组用1.0mol· L-1的草酸在75℃时浸出镍。
随时间变化,不同固液比对镍浸出率的影响曲线如图所示。
①由图可知,固液比与镍浸出率的关系是 。
②除固液比之外,你认为影响金属浸出率的因素还有
(至少两项)。1.A 量即可。
【解答】A.乙烯可用作水果催熟剂,A符合题意; 4.C
B.石油裂解气中含有多种物质,属于混合物,B不符合题意;
【解答】A.选项所给离子方程式电荷不守恒,符合题意离子方程式为5I- +IO +6H+=3I +3HO,
2 2
C.酸性KMnO 溶液具有氧化性,能将C=C氧化,因此乙烯能使酸性KMnO 溶液褪色,但不能说明乙烯
4 4
A不符合题意;
具有漂白性,C不符合题意;
D.聚乙烯是由乙烯发生加聚反应后生成的,聚乙烯中不含有碳碳双键,D不符合题意; B.一水合氨为弱电解质,不能拆,符合题意离子方程式为Al3++3NH·HO=Al(OH)↓+3NH ,B不
3 2 3
故答案为:A
符合题意;
C.饱和NaCO 溶液与CaSO 固体反应,硫酸钙转化为碳酸钙沉淀,离子方程式为CO (aq)
【分析】A、乙烯可用作水果催熟剂; 2 3 4
B、石油裂解气中含有多种物质;
C、乙烯不具有漂白性;
+CaSO(s) CaCO(s)+SO (aq),C符合题意;
4 3
D、聚乙烯中不含有碳碳双键;
2.A
D.NaOH过量,铵根也会反应,符合题意离子方程式为2NH +Fe2++4OH-=Fe(OH) ↓+2NH·HO,D
2 3 2
【解答】解:A.可与乙醇、乙酸反应,均为酯化反应,反应类型相同,故A正确;
B.含﹣COOH、碳碳双键、﹣OH、醚键四种官能团,故B错误; 不符合题意;
C.只有﹣COOH与NaOH反应,则1mol分枝酸最多可与2molNaOH发生中和反应,故C错误; 故答案为C。
D.含碳碳双键,与溴发生加成反应,与高锰酸钾发生氧化反应,原理不同,故D错误;
故选A. 【分析】A.得失电子不守恒
【分析】由结构可知,分子中含﹣COOH、碳碳双键、﹣OH、醚键,结合羧酸、烯烃、醇的性质来解 B.考查的是氨水是弱碱,不拆
答. C.考查的是难溶性物质的转换
3.B
D.考查的反应物的量对反应的影响
【解答】6.02×1022个分子的物质的量为6.02×1022÷6.02×1022=0.1moL分子,6.4g该气体的物质
的量0.1mol,该气体的摩尔质量为=64g/mol,当摩尔质量以g/mol作单位,数值上等于其相对分子
5.C
质量,所以该气体的相对分子质量为64,
【解答】A. 乙烯分子中所有原子一定共平面,A不符合;
故答案为:B。
B. 苯乙烯( )分子中所有原子有可能共平面,B不符合;
【分析】根据阿伏加德罗常数的数值计算其物质的量,再计算摩尔质量,得出该气体的相对分子质C. 异戊烷分子内碳原子都是四面体结构,分子中所有原子一定不能共平面,C符合; 【分析】A.根据相似相溶原理进行判断;
D. 氯乙烯(CH=CHCl) 分子中所有原子一定共平面,D不符合; B.苯的同系物能与酸性高锰酸钾溶液发生氧化还原反应而使其褪色;
2
故答案为:C。
C.检验醛基时需要碱过量;
D.乙酸乙酯在氢氧化钠溶液中会发生水解反应。
【分析】苯环上以及乙烯中的所有的原子都在同一平面上,主要是和碳原子的成键方式有关,饱和
8.D
碳原子中的所有原子均不在同一平面 【解答】A.O 和O 同种元素组成的不同单质为同素异形体,故A不选;
2 3
6.B
B. 和 具有相同质子数、不同中子数,互为同位素,故B不选;
【解答】A.Orn(鸟氨酸)、Cit(瓜氨酸)与Arg(精氨酸)的氮原子数目均不相同,分子组成不是相差
CH 原子团,因此它们不能互为同系物,A不符合题意;
2
C. 和 组成、结构均相同的为同种物质,故C不选;
B.根据图示物质结构简式可知:在反应反应过程中有C=O键、C=N键生成,B符合题意;
C.Cit与NH 发生反应除生成Arg外,还有HO生成,因此反应类型不是加成反应,C不符合题意;
3 2
D.正丁烷和异丁烷分子式相同CH 、结构不同,互为同分异构体,故D选;
D.Arg中的a-碳处于四面体构型的中心,其结合的羧基碳、β-碳、氨基氮处于四面体顶点,不可 4 10
故答案为:D。
能全部共面,即所有C、O、N原子不可能都共平面,D不符合题意;
【分析】结构相似、组成相差n个CH 原子团的有机物为同系物;
故答案为:B。 2
分子式相同、结构不同的化合物互为同分异构体;
同种元素组成的不同单质为同素异形体;
【分析】A、三者氮原子数不相同,分子式不是相差CH,不属于同系物;
2
同种元素的不同原子具有相同质子数、不同中子数,互为同位素;
C、反应生成Arg和HO,不是加成反应;
2
组成、结构均相同的为同种物质。
D、结构中存在空间四面体构型,不可能所有原子共面。
9.C
7.B
【解答】A.碳酸钠的溶解度大于碳酸氢钠,A不符合题意;
【解答】A.苯酚和溴反应生成三溴苯酚,但三溴苯酚溶于苯中,所以用苯酚的浓溶液与少量溴水反
B.同周期由左向右非金属的气态氢化物的稳定性逐渐增强,所以稳定性应该是:HCl>PH,B不符
3
应时不能看到白色沉淀,故不符合题意;
合题意;
B.甲苯能使酸性高锰酸钾溶液褪色,而苯不能,故符合题意;
C.氯化氢和溴化氢形成的均是分子晶体,沸点随分子间作用力的增大而升高,相对分子质量越大,
C.检验醛基时需要在碱性条件下,实验过程中氢氧化钠为少量,故不符合题意;
分子间作用力越大,则沸点:HCl<HBr,C符合题意;
D.乙酸乙酯与氢氧化钠反应,不能除去乙酸,故不符合题意。
D.同周期由左向右最高价氧化物的水化物的碱性逐渐减弱,所以碱性应该是:LiOH>Be(OH),D不
2
故答案为:B。
符合题意;
故答案为:C【分析】A.相同条件下,NaCO 的溶解度大于NaHCO; 题意;
2 3 3
B.结合非金属性的递变规律分析氢化物的稳定性; 故答案为:A。
C.氢化物的沸点受分子间作用力影响,分子间作用力随相对分子质量增大而增大;
【分析】A.离子晶体熔点较高,分子晶体熔点较低;
D.根据金属性的强弱确定碱性强弱;
10.A B. BCl
3
为共价化合物,B原子最外层电子数为6;
C.根据二氧化碳和二氧化硅的晶体类型分析;
【解答】解:n(HO)= =0.25mol,同时放出60.45kJ的热量,则生成1mol蒸气,同时
2
D. Na的熔点比AlCl 低。
3
12.D
放出热量为 =241.8kJ,则该反应的热化学方程式为H(g)+ O(g)=HO(g)△H=﹣
2 2 2 【解答】A.NaSO 是强碱弱酸盐,水解显碱性,溶液中存在质子守恒,c(OH-)=c(H+)+2c(HSO)
2 3 2 3
241.8kJ/mol或2H(g)+O(g)=2HO(g)△H=﹣483.6kJ/mol,
2 2 2 +c(HSO ),故A不符合题意;
故选A.
B. 0.1mol·L-1NaSO 溶液中通入少量SO,存在电荷守恒,c(Na+)+ c(H+) = c(OH-)+c(HSO )
2 3 2
【分析】n(HO)= =0.25mol,同时放出60.45kJ的热量,则生成1mol蒸气,同时放出
2
+2c(SO ),测得溶液pH约为8,所以c(H+) c(HSO )+2c(SO ),故B不
符合题意;
热量为 =241.8kJ,结合物质的状态、焓变书写热化学方程式.
C.由 的电离平衡 可得 ,由 的水解平衡
11.A
【解答】A.由于Al和Cl的电负性差值小于1.7,故氯化铝为分子晶体,而F元素的电负性大于Cl
元素,铝与氟电负性差值大于1.7,氟化铝为离子晶体,离子晶体熔化须克服离子键,而分子晶体
可得 ,因为
熔化只需要克服分子间作用力,故离子晶体的熔点更高,所以AlF 熔点高于AlCl,A符合题意;
3 3
B.BCl 为共价化合物,B原子最外层电子数为6,B不符合题意;
3
C.C和Si同主族,但氧化物的晶体类型不同,CO 和SiO 分别属于分子晶体和共价晶体,所以同族
2 2
NaHSO 溶液中显酸性,说明电离大于水解,所以 ,即K (HSO)·K (HSO) > K,故C不
元素的氧化物可能形成不同类型的晶体,C不符合题意; 3 a1 2 3 a2 2 3 w
D.金属晶体Na的熔点比分子晶体AlCl 低,所以金属晶体的熔点不一定比分子晶体的高,D不符合
3
符合题意;故答案为:D。
D. NaSO 溶液中通入少量Cl,会发生反应 ,
2 3 2
【分析】A.根据质子数以及核外电子排布规律即可判断位置
,即总式为 ,所以溶液为NaCl、NaSO、NaHSO 和NaSO 的混
2 4 3 2 3
B.书写方程式需要配平方程式
C.根据反应物浸泡即可得出生成物
合物,由C知对于NaHSO 来说电离大于水解,所以 ,且通入少量Cl,混合液中
3 2
D.根据给出的溶度积即可实现难溶沉淀转化
14.B
一定满足 ,所以c(SO )+3c(SO )>c(HSO),故D符合题意;
2 3
【解答】A.锂能与水反应生成氢氧化锂和氢气,所以电池隔膜左侧的电解液a不能选用水性电解
故答案为:D
液,故A不符合题意;
B.放电时,右侧电极为正极,在锂离子作用下,二氧化碳在正极得到电子发生还原反应生成碳酸
【分析】A.根据质子守恒即可判断
锂和碳,电极反应式为3CO+2Li++4e-=2LiCO+C,由电极反应式可知,消耗1.5mol二氧化碳时,转
2 2 3
B.根据电荷守恒结合pH判断
C.根据给出pH判断水解和电离的程度大小判断
移电子的物质的量为 =2mol,故B符合题意;
D.根据元素守恒即可判断
13.D
C.放电时,电子从锂电极流出通过导线和灯泡流回锂电极构成闭合回路,故C不符合题意;
D.由分析可知,充电时,金属锂电极与直流电源的负极相连做阴极,故D不符合题意;
故答案为:B。
【解答】A.Sr为38号元素,原子结构示意图为 ,其位于第五周期第ⅡA族,A
【分析】根据图示,放电时金属锂做负极,二氧化碳做正极材料,锂极易与水反应,因此不能用水
不符合题意;
做电解液,充电时,锂与负极连接,结合选项即可判断
B.焙烧时,碳酸锶与足量碳粉反应,生成SrS和CO,反应的化学方程式为:
15.C
,B不符合题意; 【解答】A.根据前面分析曲线II表示HSO 的分布系数随pH的变化,故A不符合题意;
C.向浸取液中通入CO,SrS、CO、HO发生反应,生成SrCO 和HS,C不符合题意; B.在pH=7.2时,亚硫酸氢根物质的量浓度和亚硫酸根物质的量浓度相等,则Ka(HSO)=
2 2 2 3 2 2 2 3
c(H+)=1×10−7.2=100.8×10−8,因此Ka(HSO)的数量级为10−8,故B不符合题意;
D.常温下 、 ,由于SrCO 比SrSO 更难溶, 2 2 3
3 4
C.pH=7时,根据电荷守恒和pH=7得到c(Na+)=2c(SO )+c(HSO ),又由于pH=7时c(SO )<
所以将天青矿石粉末与碳酸钠溶液混合浸泡可以制得SrCO,D符合题意;
3Δ
c(HSO ),因此c(Na+)>3c(SO ),故C符合题意;
(5)装置E中Fe粉还原NO生成FeO和氮气,反应的化学方程式为 2NO+2Fe ¿2FeO ¿ +N ;
2
¿
D.根据图中信息得到NaHSO 溶液pH大约为4,说明溶液显酸性,是亚硫酸氢根电离占主要,抑制
3
水的电离,因此溶液中水电离出的c(H+)<1×10−7 mol·L−1,故D不符合题意。 (6)根据氧化还原反应规律,为了证明酸性条件下 具有氧化性,选择还原性试剂,
故答案为C。
具有还原性, 和 溶液混合,若 溶液由浅绿色变为黄色,说明
【分析】向亚硫酸中加入氢氧化钠,先生成亚硫酸氢钠,在生成亚硫酸钠,I表示的亚硫酸,II表
示的是亚硫酸氢钠,III表示的是亚硫酸钠,根据交点即可计算出常数,结合选项即可判断 具有氧化性; KI具有还原性, 和KI—淀粉溶液混合,若KI—淀粉溶液由无色变为蓝色,
16.(1)造成酸雨、造成光化学烟雾、破坏臭氧层(任写一种)
说明具有氧化性;
(2)分液漏斗
故答案为:BC。
(3)f;e;j;i
(7)往酸性的 吸收液中通入含 和NO的模拟烟气,脱销效果比脱硫效果差,可能
(4)将NO氧化为 ,进而被NaOH溶液吸收,防止污染环境
Δ
原因是NO在水中的溶解度比 的要小(或 更容易被亚氯酸钠氧化)。
(5)2NO+2Fe
¿2FeO
¿
+N
2
¿ 【分析】(1)氮氧化物主要是造成硝酸型酸雨或者是破坏臭氧层等等
(6)B;C
(2)根据仪器连接即可判断出名称
(7)NO在水中的溶解度比 的要小(或 更容易被亚氯酸钠氧化) (3)根据题意先利用A制取一氧化氮,将产生的气体进入D中,除去可能产生的二氧化氮,再将
气体利用F进行干燥得到干燥的一氧化氮与E作用通过B在通过C即可进行实验
【解答】(1)氮氧化物能形成酸雨、造成光化学烟雾、破坏臭氧层;
(4)多于的一氧化氮被硝酸氧化便于吸收
(2)根据图示,装置A中盛放稀硝酸的仪器是分液漏斗;
(5)根据反应物和生成物即可写方程式
(3)A中的铜与稀硝酸反应生成NO,用D中的水除去NO中的 (长进短出),用F中的PO
2 5
(6)根据证明酸性条件下 具有氧化性,因此需要找具有还原性物质且现象明显的物质,结
干燥NO(粗进细出),E中Fe粉还原NO,用B中浓硝酸把NO氧化为 ,最后用C中氢氧化钠
合选项即可判断
溶液吸收NO,防止污染;所以装置接口的连接顺序为a→f→e→j→i→g→h→b→c→d;
2 (7)收集一氧化氮是利用排水法,可能是一氧化氮难溶于水
(4)装置B中的浓硝酸将NO氧化为 ,进而被NaOH溶液吸收,防止污染环境; 17.(1)羟基、碳碳三键(5)D的一种同分异构体苯环上有两个取代基,核磁共振氢谱有3组峰,说明含有3种环境的氢原子,
(2) 又因为苯环上有两个取代基,核磁共振氢谱有3组峰,峰面积之比为3:2:2,则两个取代基应处
于对位,此时苯环上已经有两种环境的氢原子,且满足2:2,则两个取代基只有一种环境的氢原子,
(3)邻氨基苯甲酸或2-氨基苯甲酸 且含有3个氢原子,则其中一个取代基为甲基,从而确定另一个取代基为硝基,因此符合条件的结
(4)
构简式为 。
(6)苯环电子云密度越大,越容易与氯气发生取代反应,氨基是给电子基,可增大苯环电子云密度,
有利于氯代反应的发生,因此不直接使用苯甲酸而使用邻氨基苯甲酸合成G。
(5)
(6)氨基是给电子基,可增大苯环电子云密度,有利于氯代反应的发生
【分析】(1)根据结构简式解答,注意官能团要求写名称。
【解答】(1)由A的结构简式可知,A中含有的官能团为羟基和碳碳三键;
(2)通过对比A、B的分子式及A→B的反应条件进行分析。
(2)根据A和C的结构简式可推知,A→B的过程中,A中含有羟基被氯原子取代生成B,结合B的分
(3)根据有机物的系统命名规则解答。
(4)注意反应物处理两种有机物外,还有NaOH,产物中别丢掉HO。
2
(5)同分异构体就是含有相同的分子式、不同结构的化合物。核磁共振氢谱有3组峰表示有3种
子式可知,B的结构简式为 ;
氢原子,峰面积之比就是不同氢原子的个数之比,据此分析。
(6)氨基是给电子基,可增大苯环电子云密度,有利于氯代反应的发生。
18.(1)d
(3)D为 ,其名称为邻氨基苯甲酸或2-氨基苯甲酸;
(2)正反应方向
(3)H;2.5mol/(L•min);20%;I(g)+H(g) 2HI(g) △H=-9.5kJ/mol
2 2
(4)由图可知,C、H和氢氧化钠反应生成戊炔草胺,反应的化学方程式为
(4)乙>丙>甲
【解答】(1)甲容器为绝热恒容,发生2HI(g) I(g)+H(g):
2 2
a.气体颜色不变,则I(g)的浓度不变,说明反应已达平衡,a不符合题意;
2
;
b.2HI(g) I(g)+H(g) ΔH>0,反应吸热,未平衡时,容器内温度降低,气体分子数不变,压强
2 2减小,则气体压强不变,说明反应已达平衡,b不符合题意; ⇌
¿
+
c.2HI(g) I(g)+H(g) ΔH>0,反应吸热,未平衡时,容器内温度降低,气体温度不变,说明反
2 2 2HI(g) ¿
¿开始(mol/L) I (g)
0 2 H (g)
③设体积为1L,列三段式变化(mol/L) 1 2 ,T℃时K= ,则 ,
应已达平衡,c不符合题意; 2x ¿ 1
平衡(mol/L) x ¿
2x x
1−x
d.2HI(g) I(g)+H(g)是气体总物质的量不变,总质量不变的反应,故混合气体的平均相对分子 1−x
2 2
¿
¿
质量始终不变,不能说明反应已达平衡,d符合题意;
故答案为:d;
(2)乙容器是恒温恒压容器,反应达平衡后,再充入He,体积增大,相当于减小压强,反应NHI(s) 解得x=0.8或 (舍去),因为体积为1L,则0.8molI(g)和0.8molH(g)反应生成1.6molHI(g)放出
4 2 2
NH(g)+HI(g)正向移动,使体系温度降低,但乙容器恒温,相当于升高温度,则2HI(g)
3
I(g)+H(g) ΔH>0向正反应方向移动; 7.6kJ的热量,则1molI(g)和1molH(g)反应生成2molHI(g)放出的热量为 kJ=9.5kJ,则I(g)
2 2 2 2 2
(3)①NHI(s) NH(g)+HI(g) ΔH>0,2HI(g) I(g)+H(g) ΔH>0,HI(g)是第一个反应的生成
4 3 2 2
与H(g)反应的热化学方程式为I(g)+H(g) 2HI(g) △H=-9.5kJ/mol;
2 2 2
物,第二个反应的反应物,则开始阶段HI(g)浓度增大程度大于H(g),故曲线b代表HI的变化曲
2
线; (4)甲是恒容绝热容器,乙是恒温恒压,丙是恒温恒容,以丙为基础,甲相比于丙是降温,平衡逆
向移动,I(g)的体积分数比丙小,乙相比于丙是降压,平衡正向移动,I(g)的体积分数比丙大,
2 2
②结合①可知,2min内,H(g)浓度增大0.5mol/L,则反应2HI(g) I(g)+H(g) 中HI减小
2 2 2
则甲、乙、丙三个容器中反应均达到平衡时,I(g)的体积分数由大到小的顺序是乙>丙>甲。
2
1mol/L,HI在该2min内增大4mol/L,则反应NHI(s) NH(g)+HI(g)中NH(g)浓度增大4mol/
4 3 3
【分析】(1)对弈前后系数不变的反应可以通过气体颜色,压强以及温度等作为判断平衡依据
L+1mol/L=5mol/L,用NH 表示的反应速率为v(NH)=5mol/L÷2min=2.5mol/(L·min);
3 3 (2)对于乙,平衡后加入氦气,体积增大,压强减小,平衡向右移动,温度降低,对于甲相当于
温度升高,正向移动
HI的分解率= =20%;
(3)①根据反应即可得出a为H2,b为HI
②根据氢气和HI的浓度即可计算出反应速率和分解速率
③根据数据结合常数计算出热量
(4)根据温度高低即可判断
19.(1)CuTe+2O+4H+=2Cu2++TeO+2HO;酸性过强TeO 会被酸溶解导致Te产率降低
2 2 2 2 2(2)1:2;HSO、HCl ②除固液比之外,影响金属浸出的因素还有:金属本身、浸液的选择、温度、浓度、浸出时间、搅
2 4
拌速度等。
(3)K== = =2.38 1015
【分析】注意题干信息:TeO 属于两性氧化物,易溶于强酸和强碱
2
(1)因易溶于强酸强碱,故不能酸性过强,会降低产率。
(4)TeO+2OH-=TeO2-+HO;TeO2-+4e-+3HO=Te+6OH-
2 3 2 3 2
(2)氧化还原配平:先确定反应物,生成物,根据电子守恒配平氧化剂还原剂,氧化产物还原产
(5)固液比越小,镍的浸出率越高;金属本身、浸液的选择、温度、浓度、浸出时间、搅拌速度
物,再根据观察法配平其他物质,最后配不平可加水。
等
TeCl+2SO+4HO=Te+2HSO+4HCl,根据方程式和流程可循环利用的物质的化学式为:HSO、HCl
【解答】(1)“加压浸出”时加入O、HSO,根据流程和题意,CuTe与O、HSO 反应生成 4 2 2 2 4 2 4
2 2 4 2 2 2 4
(3)溶液中的离子反应,是往离子浓度减少的方向进行。
CuSO、TeO 和水,反应的化学方程式为CuTe+2O+2HSO=2CuSO+TeO+2HO。反应的离子方程式为
4 2 2 2 2 4 4 2 2
CuTe+2O+4H+=2Cu2++TeO+2HO。“加压浸出”时控制pH为4.5~5.0,酸性不能过强的原因是: (4)电极反应式书写:电极反应方程式配平:先写反应物生成物,根据化合价升降配平转移电子数,
2 2 2 2
再看条件配平电荷守恒,最后观察法配原子守恒。
TeO 属于两性氧化物,易溶于强酸和强碱,酸性过强TeO 会被酸溶解导致Te产率降低。
2 2
(5)①观察图形可得,当镍浸出时间相同时,浸出率随固液比的减少而升高。
(2)TeO 属于两性氧化物,易溶于强酸和强碱,“盐酸酸浸”时TeO 发生的反应为
2 2
②影响因素包括内因:金属本身,浸出液的选择
TeO+4HCl=TeCl+2HO;向浸出液中通入SO 得到单质Te,TeCl 为氧化剂,被还原成Te,SO 为还原
2 4 2 2 4 2
剂,被氧化成SO2-,根据得失电子守恒,4n(TeCl)=2n(SO),n(TeCl):n(SO)=1:2,该 外因:浓度、温度、浸出时间、搅拌速度等。
4 4 2 4 2
反应中氧化剂与还原剂物质的量之比为1:2。反应的化学方程式为:
TeCl+2SO+4HO=Te+2HSO+4HCl,该流程中可循环利用的物质的化学式为:HSO、HCl。
4 2 2 2 4 2 4
(3)AgSO 转化为AgCl的反应为AgSO(s)+2Cl-(aq) 2AgCl(s)+SO2-(aq),该反应的
2 4 2 4 4
平衡常数K= = =2.38 1015 105,AgSO 可充分转化为AgCl。
2 4
(4)TeO 属于两性氧化物,易溶于强酸和强碱,NaOH碱浸时反应的化学方程式为
2
TeO+2NaOH=NaTeO+HO,离子方程式为TeO+2OH-=TeO2-+HO。用石墨为电极电解NaTeO 溶液得到
2 2 3 2 2 3 2 2 3
Te,Te元素的化合价由+4价降至0价,电解时阴极发生得电子的还原反应,阴极的电极反应式为
TeO2-+4e-+3HO=Te+6OH-。
3 2
(5)①根据图像,固液比与镍浸出率的关系是:浸出时间相同时,固液比越小,镍的浸出率越高。