文档内容
热点 04 物质结构与性质(选择题)
物质结构与性质的选择题是江苏高考的必考内容,属于热点问题,本题考查化学选修
3《物质结构与性质》的相关知识,常涉及如下高频考点:原子结构与元素的性质(基态微
粒的电子排布式、电离能及电负性的比较)、元素周期律;分子结构与性质(化学键类型、
原子的杂化方式、分子空间构型的分析与判断);晶体结构与性质(晶体类型、性质及与粒
子间作用的关系、以晶胞为单位的密度、微粒间距与微粒质量的关系计算及化学式分析等)
命题形式有两种:一是直接给出元素,围绕给出元素的原子结构、形成的物质等进行考
查;二是给出元素的原子的一些结构特点等,首先判断出元素,然后再进行相应的考查。
一、有关基态原子的核外电子排布
1. 四种表示方法
表示方法 举例
电子排布式 Cr:1s22s22p63s23p63d54s1
简化表示式 Cu:[Ar]3d104s1
价电子
Fe:3d64s2
排布式
电子排布图 S:
2. 排布三原则
能量最低原理 原子核外电子总是先占有能量最低的原子轨道
泡利原理 每个原子轨道上最多只能容纳2个自旋方向相反的电子
洪特规则 当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单
独占据一个轨道,而且自旋方向相同
3. 有关第一电离能和电负性的两种递变性
同周期(从左到右) 同主族(从上到下)
第一电离能 增大(注意ⅡA、ⅤA的特殊性) 依次减小
电负性 依次增大 依次减小
二、根据价层电子对互斥模型判断分子的空间构型
1. 价层电子对互斥模型说的是价层电子对的空间构型,而分子的空间构型指的是成键电子
对的空间构型,不包括孤电子对。
①当中心原子无孤电子对时,两者的构型一致。②当中心原子有孤电子对时,两者的构型不一致。
电子 价层电子
成键数 孤电子对数 分子立体构型 实例
对数 对立体构型
2 2 0 直线形 直线形 CO
2
3 0 三角形 BF
3
3 三角形
2 1 V 形 SO
2
4 0 正四面体形 CH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V形 HO
2
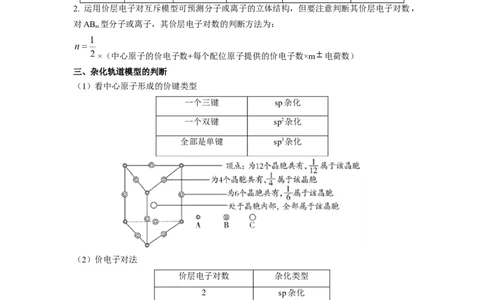
2. 运用价层电子对互斥模型可预测分子或离子的立体结构,但要注意判断其价层电子对数,
对AB 型分子或离子,其价层电子对数的判断方法为:
m
×(中心原子的价电子数+每个配位原子提供的价电子数×m 电荷数)
三、杂化轨道模型的判断
(1)看中心原子形成的价键类型
一个三键 sp杂化
一个双键 sp2杂化
全部是单键 sp3杂化
(2)价电子对法
价层电子对数 杂化类型
2 sp杂化
3 sp2杂化
4 sp3杂化
四、“两角度”比较晶体熔、沸点的高低
1. 不同类型晶体熔、沸点的比较
(1)不同类型晶体的熔、沸点高低一般规律:原子晶体>离子晶体>分子晶体。
(2)金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。
2. 同种类型晶体熔、沸点的比较
(1)原子晶体→→→
如熔点:金刚石>碳化硅>硅。
(2)离子晶体
①一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力越强,其晶体
的熔、沸点越高,如熔点:MgO>MgCl ,NaCl>CsCl。
2
②衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔点越
高,硬度越大。
(3)分子晶体
①分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常高。如
HO>HTe>HSe>HS。
2 2 2 2
②组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如 SnH >GeH >SiH
4 4 4
>CH。
4
③组成和结构不相似的分子晶体(相对分子质量接近),其分子的极性越大,熔、沸点越
高,如CHOH>CHCH。
3 3 3
④同分异构体,支链越多,熔、沸点越低。
如:CHCHCHCHCH>
3 2 2 2 3
(4)金属晶体
金属离子半径越小,离子电荷数越多,其金属键越强,金属晶体的熔、沸点越高,如熔、
沸点:Na<Mg<Al。
考向 物质结构与性质的分析判断
1.(2023·山东·统考高考真题)下列分子属于极性分子的是
A. B. C. D.
【答案】B
【解析】A.CS 中C上的孤电子对数为 ×(4-2×2)=0,σ键电子对数为2,价层电子对数为
2
2,CS 的空间构型为直线形,分子中正负电中心重合,CS 属于非极性分子,A项不符合
2 2
题意;
B.NF 中N上的孤电子对数为 ×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,NF
3 3
的空间构型为三角锥形,分子中正负电中心不重合,NF 属于极性分子,B项符合题意;
3
C.SO 中S上的孤电子对数为 ×(6-3×2)=0,σ键电子对数为3,价层电子对数为3,SO
3 3
的空间构型为平面正三角形,分子中正负电中心重合,SO 属于非极性分子,C项不符合题
3意;
D.SiF 中Si上的孤电子对数为 ×(4-4×1)=0,σ键电子对数为4,价层电子对数为4,SiF
4 4
的空间构型为正四面体形,分子中正负电中心重合,SiF 属于非极性分子,D项不符合题
4
意;
答案选B。
2.(2023·浙江·高考真题)共价化合物 中所有原子均满足8电子稳定结构,一定条
件下可发生反应: ,下列说法不正确的是
A. 的结构式为 B. 为非极性分子
C.该反应中 的配位能力大于氯 D. 比 更难与 发生反应
【答案】D
【解析】A.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,故A正确;
B.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子的结构式为
,则双聚氯化铝分子为结构对称的非极性分子,故B正确;
C.由反应方程式可知,氨分子更易与具有空轨道的铝原子形成配位键,配位能力大于氯
原子,故C正确;
D.溴元素的电负性小于氯元素,原子的原子半径大于氯原子,则铝溴键弱于铝氯键,所
以双聚溴化铝的铝溴键更易断裂,比双聚氯化铝更易与氨气反应,故D错误;
故选D。
3.(2023·湖北·统考高考真题)物质结构决定物质性质。下列性质差异与结构因素匹配错
误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 熔点: (1040℃)远高于 (178℃升华) 晶体类型
C 酸性: ( )远强于 ( ) 羟基极性
D 溶解度(20℃): (29g)大于 (8g) 阴离子电荷A.A B.B C.C D.D
【答案】D
【解析】A.正戊烷和新戊烷形成的晶体都是分子晶体,由于新戊烷支链多,对称性好,
分子间作用力小,所以沸点较低,故A正确;
B.AlF 为离子化合物,形成的晶体为离子晶体,熔点较高,AlCl 为共价化合物,形成的
3 3
晶体为分子晶体,熔点较低,则 熔点远高于 ,故B正确;
C.由于电负性F>H,C-F键极性大于C-H键,使得羧基上的羟基极性增强,氢原子更容
易电离,酸性增强,故C正确;
D.碳酸氢钠在水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中HCO 间存在氢键,与
晶格能大小无关,即与阴离子电荷无关,故D错误;
答案选D。
4.(2023·湖南·统考高考真题)科学家合成了一种高温超导材料,其晶胞结构如图所示,
该立方晶胞参数为 。阿伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
【答案】C
【解析】A.根据晶胞结构可知,其中K个数:8× =1,其中Ca个数:1,其中B个数:
12× =6,其中C个数:12× =6,故其最简化学式为 ,A正确;
B.根据晶胞结构可知, 位于晶胞顶点,Ca2+位于体心,每个 为8个晶胞共用,则晶
体中与 最近且距离相等的 有8个,B正确;C.根据晶胞结构可知,晶胞中B和C原子构成的多面体有14个面,C错误;
D.根据选项A分析可知,该晶胞最简化学式为 ,则1个晶胞质量为: ,晶
胞体积为a3×10-30cm3,则其密度为 ,D正确;
故选C。
5.(2023·辽宁·统考高考真题)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导
体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料
(图2)。下列说法错误的是
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【解析】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个
晶胞的质量为 g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密
度为 g÷(a3×10-30cm3)= g/cm3,A项正确;
B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配位数为6,B项正
确;
C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4× =1,
Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错
x 1-x
误;
D.进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生
的空位有利于Li+的传导,D项正确;
答案选C。(建议用时:45分钟)
1.(2023上·江苏盐城·高二盐城中学校考期中)第三周期元素的单质及其化合物有重要用
途。如在熔融状态下可用金属钠制备金属钾: 上可制备多种镁产品:铝―空气电池
具有较高的比能量,在碱性电解液中总反应为 。高
纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷( ),再经氢气还
原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为 )、单斜硫等。 可除去
废水中 等重金属离子, 水溶液在空气中会缓慢氧化生成S而变浑浊。下列说法不
正确的是
A.斜方硫和单斜硫互为同素异形体 B.1mol 中含有4molσ键
C. 的空间构型为V形 D.Si―Si键的键能小于Si―O键的键能
【答案】B
【解析】A.斜方硫、单斜硫均为硫单质,且为不同物质,则斜方硫和单斜硫互为同素异
形体,A正确;
B. 中1个氢氧根含有1个σ键,氧原子又与铝原子形成1个配位键,故1mol
中含有8molσ键,B错误;
C. 分子中中心S原子价层电子对数为2+ =4,采用sp3杂化,S原子上含有2对
孤电子对,分子是V形分子,C正确;
D.氧原子半径小于硅原子,Si-Si键的键长大于Si-O键的键长,导致Si-Si键的键能
小于Si-O键的键能,D正确;
故选B。
2.(2023上·河南洛阳·高三孟津县第一高级中学校考阶段练习)对氮氧化物进行催化还原
的一步反应为 +NO= +N +NH +H O。下列有关说法不正确的是
2 2
A.若 为平面结构,则离子中 为 杂化
B. 的VSEPR模型结构相同
C.反应中Cu(NH ) 既是氧化剂又是还原剂
3
D.每生成 ,反应生成2molπ键
【答案】A
【解析】A.若离子中 为 杂化, 应为正四面体结构,A错误;B. 和 中的氮原子、 中的氧原子价层电子对数都为4,所以
的VSEPR模型结构相同,都是四面体形,B正确;
C.由方程式可知,反应中NO中氮元素、铜元素的化合价降低,被还原,NO和
是反应的氧化剂,部分 中氮元素的化合价升高,被氧化,
是反应的还原剂,C正确;
D.氮气分子中含氮氮三键,一个三键中有2个π键,则每生成 ,反应生成2 mol π
键,D正确;
故选A。
3.(2023上·湖南长沙·高三长郡中学校考阶段练习)我国长征系列运载火箭采用偏二甲肼
(C HN)和 作发动机推进剂,产物为氨气、二氧化碳和水,无污染。下列有关说法不
2 8 2
正确的是
A.基态N的价电子排布图为
B.N、O的电负性较大,其单质通常比较活泼
C.偏二甲肼分子间存在氢键,沸点较高
D.二氧化碳为非极性分子,水分子和偏二甲肼为极性分子
【答案】B
【解析】A.氮为7号元素,故价电子排布图为 ,故A正确;
B.氮原子半径小,氮氮三键键长短,键能大, 化学性质稳定,故B错误;
C.类比氨分子可知偏二甲肼分子间存在氢键,沸点较高,故C正确;
D.二氧化碳为直线形分子,结构对称,为非极性分子,水分子和偏二甲肼分子结构不对
称,为极性分子,故D正确。
答案选B。
4.(2023上·江苏盐城·高二盐城中学校考期中)非金属氟化物在生产、生活和科研中应用
广泛。下列说法正确的是
A.基态F原子核外电子的空间运动状态有9种
B.金刚石与石墨烯中的C―C―C夹角都为120°
C. 分子的空间构型为V形, 的熔、沸点低于
D.Xe是第五周期的稀有气体元素,与F形成的 室温下易升华。 中心原子的
价层电子对数为4
【答案】C
【解析】A.把电子在原子核外的一个空间运动状态称为一个原子轨道,因而空间运动状态个数等于轨道数;基态F原子电子排布为1s22s22p5,所以核外电子的空间运动状态有5
种,A错误;
B.金刚石中碳以正四面体形结构结合,C―C―C夹角不是120°,B错误;
C.OF 的中心原子O的价层电子对数为2+ =4,含有2个孤电子对,则OF 分子的
2 2
空间结构是V形;OF 和ClO都是分子晶体,结构相似,ClO的相对分子质量大,范德华
2 2 2
力大,故ClO的熔、沸点高,C正确;
2
D.XeF 是分子晶体,熔沸点低,易升华,其中心原子的价层电子对数为2+ =5,D
2
错误;
故选C。
5.(2023·全国·高三专题练习)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图所
示,已如其晶体密度为 , 表示阿伏加德罗常数。下列有关说法不正确的是
A.磷化硼(BP)的晶体类型为分子晶体
B.磷化硼(BP)晶体的熔点比金刚石低
C.该晶胞中所含的硼原子和磷原子个数均为4
D.经计算,B—P键的键长为
【答案】A
【解析】A.磷化硼(BP)是通过共价键形成的晶体,晶体类型为共价晶体,A错误;
B.磷、硼原子半径大于碳,则B-P键键长大于C-C键键长,B-P键键能小于C-C键键能,
故金刚石的熔点更高,B正确;
C.根据“均摊法”,晶胞中含 个P、4个B,该晶胞中所含的硼原子和磷原
子个数均为4,C正确;
D.设晶胞边长为acm,结合C分析可知,晶体密度为 = ,,B—P键的键长为体对角线的四分之一,故为 ,D正确;
故选A。
6.(2023上·北京·高三北京师大附中校考阶段练习)三氟化氮( )常用于微电子工业,
可用以下反应制备: ,下列说法中,正确的是
A. 的电子式为 B. 中仅含离子键
C.在制备 的反应中, 表现出还原性 D. 比 的键角小
【答案】C
【解析】A. 的电子式为 ,故A错误;
B. 中铵根离子和氟离子间存在离子键,铵根离子中N、H原子间存在共价键,故B
错误;
C.在制备 的反应中,N元素化合价升高, 表现出还原性,故C正确;
D. 成键电子对偏向N原子,成键电子对的斥力增大, 中成键电子对偏向F原子,
成键电子对的斥力减小,所以 比 的键角大,故D错误;
选C。
7.(2023上·浙江嘉兴·高二嘉兴高级中学校考阶段练习)下列说法或有关化学用语的表达
正确的是
A.能级能量大小关系:
B.基态铜原子( Cu)的价层电子排布式:
29
C. 处于激发态的电子排布式可能为:
D.基态 的轨道表示式:
【答案】C
【解析】A.由构造原理可知,4f的能力低于5d,故A错误;
B.铜元素的原子序数为29,基态原子的价层电子排布式为3d104s1,故B错误;
C.钙元素的原子序数为20,基态原子的电子排布式为1s22s22p63s23p64s2,则发态的电子排
布式可能为 ,故C正确;
D.钠元素的原子序数为11,基态钠离子的电子排布式为1s22s22p6,轨道表示式为
,故D错误;故选C。
8.(2023上·云南曲靖·高三曲靖一中校考阶段练习)联氨(N H)为二元弱碱,在水中的电
2 4
离方式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如
图所示。下列说法正确的是
A.每个NH 分子中有一个π键
2 4
B.H-N-H键角:[Cu(NH )]²+>NH₃
3 4
C.2mol NH 最多能处理44.8L O
2 4 2
D.[Cu(NH )]2+和[Cu(NH )]+的配体均为N原子
3 4 3 2
【答案】B
【解析】A.NH 分子各原子以单键相连接,不含π键,A错误;
2 4
B.[Cu(NH )]²+中N原子孤电子对形成配位键, 中含1对孤电子对,导致孤电子对与
3 4
成键电子对间的斥力大,键角小,B正确;
C.未指明气体是否处于标准状况,无法计算,C错误;
D.N原子是配位原子,配体是 ,D错误;
答案选B。
9.(2023上·安徽阜阳·高二阜阳市第三中学校考期中)侯氏制碱法制取NaHCO 的原理为
3
。下列说法正确的是
A.NH 是含有极性共价键的非极性分子
3
B.CO 的空间填充模型:
2
C.氧原子核外电子的空间运动状态有8种
D.NaCl的晶胞:
【答案】B
【解析】A.NH 是含有极性共价键的极性分子,A项错误;
3
B.CO 的空间填充模型: ,B项正确;
2
C.基态氧原子的电子排布式为1s22s22p4,存在电子的轨道有5个,核外电子的空间运动状
态有5种,C项错误;D.NaCl的晶胞为 ,D项错误;
故选B。
10.(2023上·黑龙江哈尔滨·高三哈师大附中校考期中)氮化硼(BN)晶体有多种结构。六
方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂;立方相
氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示,关于这两种晶体的说法
正确的是
A.两种晶体中B原子的杂化方式均为
B.两种晶体均为共价晶体
C.六方相氮化硼层间共价键键能较小,所以可做高温润滑剂
D.每个立方氮化硼晶胞中含有4个B原子和4个N原子
【答案】D
【解析】A.立方氮化硼中硼原子形成4个共价键,所以立方氮化硼中硼原子采用的是sp3
杂化,六方相氮化硼中硼原子采用的是sp2杂化,A错误;
B.六方相氮化硼与石墨相似是混合晶体,立方相氮化硼是共价晶体,B错误;
C.六方相氮化硼层间分子间作用力较小,所以可做高温润滑剂,C错误;
D.根据立方氨化硼的晶胞示意图,每个晶胞中B原子个数是8 +6 =4,N原子个数
为4,故每个立方氮化硼晶胞中含有4个B原子和4个N原子,D正确;
故选D。
11.(2023上·安徽阜阳·高二阜阳市第三中学校考期中)立方砷化硼(BAs)是一种优良的半
导体材料,BAs的晶胞结构如图所示。若晶胞参数为apm,下列说法正确的是
A.As位于第五周期VA族B.1号砷的坐标为
C.BAs晶体中存在着配位键
D.晶体BAs的摩尔体积为
【答案】C
【解析】A.As为33号元素,则As位于第四周期VA族,A错误;
B.1号砷在体对角线的四分之一处,其坐标为( ),B错误;
C.B最外层有三个电子,易形成三个共价键,根据图中结构BAs晶体中B有四个价键,
说明BAs晶体中存在着配位键,C正确;
D.根据晶体BAs的结构分析可知,1个晶胞中含有4个BAs,其摩尔体积为
,D错误;
故选C。
12.(2021下·内蒙古赤峰·高一统考期末)氰气的化学式为(CN),结构式为
2
,性质与卤素相似,下列叙述正确的是
A.在一定条件下可发生加成反应
B.分子中 键的键长大于 键的键长
C.分子中含有2个σ键和4个π键
D.不和氢氧化钠溶液发生反应
【答案】A
【解析】A.该分子中含三键,可以发生加成反应,A正确;
B.氮原子半径小于碳原子半径,故 键的键长小于 键的键长,B错误;
C.单键全部是σ键,三键中含1个σ键和2个π键,故该分子中含有3个σ键和4个π键,
C错误;
D.氰气性质与卤素相似,能与氢氧化钠溶液反应,D错误;
故选A。
13.(2023·全国·高三专题练习)LiS属立方晶体,晶胞边长为dpm,晶胞截面图如图所
2
示。则下列关于该晶胞的描述正确的是
A.每个晶胞中含有的 数目为8
B.与Li+最近且等距离的 有4个C.该晶胞中两个距离最近的Li+和 的核间距的计算表达式为
D.LiS晶体的密度为
2
【答案】B
【分析】由晶胞截面图可知,硫离子位于晶胞的顶点和面心,其离子个数为 ,
锂离子位于晶胞内,其离子个数为8。
【解析】A.由以上分析可知,每个晶胞中含有的S2-数目为4,A错误;
B.Li+位于立方晶胞体对角线四分之一处,与其最近且等距离的S2-有4个,B正确;
C.该晶胞中两个距离最近的Li+和S2-的核间距恰好为该立方晶胞体对角线的四分之一,该
晶胞边长为dpm,则核间距的计算表达式为 dpm,C错误;
D.由以上分析可知,一个晶胞中含有4个S2-和8个Li+,晶胞边长为d×10-10cm,则LiS晶
2
体的密度为 ,D错误;
故选B。
14.(2024上·浙江绍兴·高三阶段练习)X、Y、Z、Q、T、W为前36号元素,原子序数
依次增大。其中仅X、Y、Z为短周期主族元素,且分占三个周期。基态Y元素原子价层p
轨道上的电子数比s轨道多,且第一电离能小于同周期的相邻元素;在同周期元素中,Z
的电负性最大;基态W元素原子的4p轨道半充满;Q和T既处于同一周期又位于同一族,
且原子序数T比Q多2。下列说法正确的是
A.基态Y原子核外电子有8种空间运动状态
B. 为非极性分子
C.与X形成的简单化合物沸点:
D. 有2个未成对电子
【答案】D
【分析】X、Y、Z原子序数依次增大,且为短周期主族元素,分占三个周期,则X是H,
Y在第二周期,Z在第三周期。基态Y元素原子价层p轨道上的电子数比s轨道多,且第一
电离能小于同周期的相邻元素,则Y在第ⅥA族,Y是O。Z是第三周期电负性最大的元
素,Z是Cl;基态W元素原子的4p轨道半充满,W是As;Q和T既处于同一周期又位于
同一族,且原子序数T比Q多2,则Q、T在第四周期Ⅷ族,是Fe和Ni。综上,X、Y、
Z、Q、T、W分别为H、O、Cl、Fe、Ni、As。
【解析】A.基态O原子核外电子轨道表示式为 ,则氧原子的空间运
动状态有5种,故A错误;B.WZ 为AsCl ,中心原子As有一个孤电子对,空间构型为三角锥形,为极性分子,故B
3 3
错误;
C.Y与X形成的简单化合物是HO,W与X形成的简单化合物是AsH ,水分子间有氢键,
2 3
沸点高于AsH ,故C错误;
3
D.Ni2+价层电子轨道表示式为 ,有2个未成对电子,故D正确;
答案选D。
15.(2023上·江苏盐城·高二盐城市第一中学校考期中)CrSi、Ge—GaAs、ZnGeAs 和碳
2
化硅都是重要的半导体化合物,下列说法错误的是
A.基态铬原子的价电子排布式为3d54s1
B.酸性:HSiOGe>Zn
2
D.Ge—GaAs中元素Ge、Ga、As的第一电离能由大到小的顺序为As>Ga>Ge
【答案】D
【解析】A.铬是第24号元素,基态铬原子的价电子排布式为3d54s1,A正确;
B.根据同主族从上到下元素非金属性减弱,最高价氧化物水化物酸性减弱,故碳酸的酸
性比硅酸的强,B正确;
C.Zn、Ge、As同为第四周期元素,同周期元素从左到右电负性增强,Zn、Ge、As的电
负性由大到小的顺序为As>Ge>Zn,C正确;
D.同周期元素的第一电离能总体呈现从左到右增大的变化,但第ⅡA、ⅤA族元素反常
大,故元素Ge、Ga、As的第一电离能由大到小的顺序为As>Ge >Ga,D错误;
故选D。
16.(2023上·湖南·高三湖南师大附中校联考阶段练习)下列有关物质结构与性质的说法
正确的是
A. 和 均为非极性分子 B. 与 的键角相等
C. 、 中心原子均采取 杂化 D. 和 的空间结构均为三角锥形
【答案】C
【解析】A. 为直线型非极性分子, 为V型极性分子,A错误;
B.XeF 的价层电子对数=2+ =5,XeO 的价层电子对数=2+ =4,孤电子对数不等,
2 2
键角不相等,B错误;
C. 、 中心原子价电子对数都为4,中心原子都均采取 杂化,C正确;
D. 价电子对数为4,无孤对电子,空间结构为平面三角形, 价电子对数为4,
有一孤电子对,空间结构为三角锥形,D错误;
故选C。17.(2023上·重庆荣昌·高三重庆市荣昌中学校校考阶段练习)干冰(固态二氧化碳)在﹣
78℃时可直接升华为气体,其晶胞结构如下图所示。下列说法不正确的是
A.干冰升华时需克服分子间作用力
B.每个晶胞中含有4个CO 分子
2
C.每个CO 分子周围有12个紧邻CO 分子
2 2
D.CO 中有C=O键,中心原子C是sp2杂化
2
【答案】D
【解析】A.干冰为分子晶体,升华时需要克服分子间作用力,A正确;
B.根据均摊法,一个晶胞中含有CO 分子数为 =4,B正确;
2
C.以顶点处的分子为例,每个CO 分子周围与其紧邻的CO 分子位于面心,一个面上有4
2 2
个这样的CO 分子,共有3个这样互相垂直的面,因此每个CO 分子周围有12个紧邻的
2 2
CO 分子,C正确;
2
D.CO 中C与O形成C=O键,中心碳原子有2条σ键,无孤电子对,价层电子对数为
2
2,为sp杂化,D错误;
故答案选D。
18.(2023·全国·高三专题练习)科学家合成了一种高温超导材料,其晶胞结构如图所示,
该立方晶胞参数为 。阿伏加德罗常数的值为 。下列说法错误的是
A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有6个
C.晶胞中B和C原子构成的多面体有14个面
D.晶体的密度为
【答案】B【解析】A.晶胞中K位于顶点,每个晶胞中含K原子 个,Ca位于体心,每个晶胞
中含Ca原子1个,B和C位于面心,每个晶胞中含B原子和C原子各 个,则晶体
最简化学式为 ,A正确;
B.晶体中与 位于顶点, 位于体心,则晶体中与 最近且距离相等的 有8个,
B错误;
C.晶胞中B和C原子构成的多面体,有6个面位于晶胞的六个面上,上半部分和下半部
分还各有4个面,故该多面体共有14个面,C正确;
D. 的摩尔质量为217g/mol,一个晶胞的质量为 ,体积为 ,故
晶体的密度为 ,D正确;
故选B。
19.(2023上·湖南·高三湖南师大附中校考阶段练习)下列有关物质结构的说法正确的是
A.图①中18-冠-6通过离子键与 作用,体现了超分子“分子识别”的特征
B.图②物质相较 摩尔质量更大,具有更高的熔沸点
C.图③中, 表示硅氧四面体,则该多硅酸根结构的通式为
D.图④表示氮化铝晶胞,则该晶体中存在共价键和配位键,且铝的配位数为6
【答案】C
【解析】A.①中18-冠-6通过配位键与K+作用,体现了超分子“分子识别”的特征,故
A错误;
B.②物质阳离子基团较大,离子键较弱,熔沸点更低NaBF4,故B错误;
C.将③中左边环补齐,则得到两个完整环,则两环共用的氧原子有左边7个、右边7个共
14个;独立成个体的氧原子有10个,同时两个环都有独立的硅原子,则硅原子和氧原子
个数比为(4+4×0.5):(14×0.5+10)=6:17,结合硅化合价为+4,氧化合价为-2,可得到
通式为: ,故C正确;
D.④表示氮化铝晶胞,则该晶体中存在共价键和配位键,且铝的配位数为4,故D错误;
故选C。
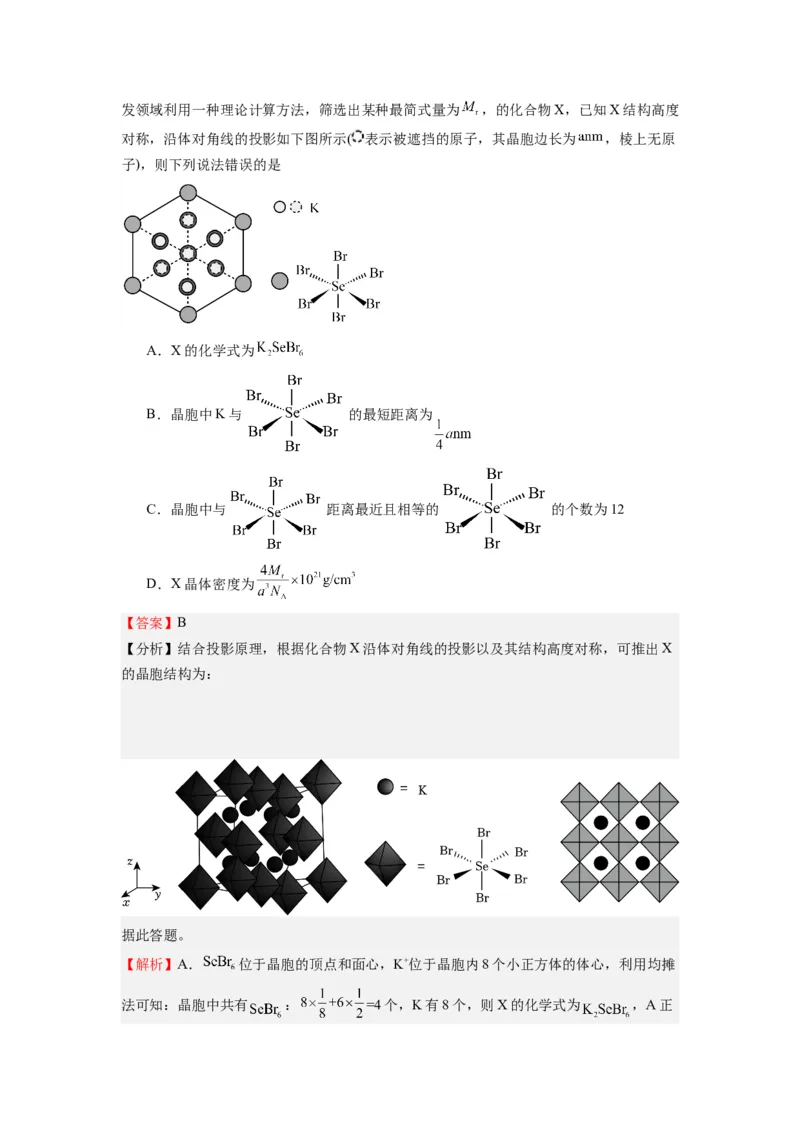
20.(2023上·湖南·高三湖南师大附中校联考阶段练习)我国科学家在新型热电材料的研发领域利用一种理论计算方法,筛选出某种最简式量为 ,的化合物X,已知X结构高度
对称,沿体对角线的投影如下图所示( 表示被遮挡的原子,其晶胞边长为 ,棱上无原
子),则下列说法错误的是
A.X的化学式为
B.晶胞中K与 的最短距离为
C.晶胞中与 距离最近且相等的 的个数为12
D.X晶体密度为
【答案】B
【分析】结合投影原理,根据化合物X沿体对角线的投影以及其结构高度对称,可推出X
的晶胞结构为:
据此答题。
【解析】A. 位于晶胞的顶点和面心,K+位于晶胞内8个小正方体的体心,利用均摊
法可知:晶胞中共有 : =4个,K有8个,则X的化学式为 ,A正确;
B.晶胞中K与 最短距离为晶胞体对角线的 ,其晶胞边长为 ,则体对角线为
nm,晶胞中K与 最短距离为 nm,B错误;
C. 位于晶胞的顶点和面心,以顶点为例,距离其最近的 是相邻面心的3个
,则距离 最近且相等的 的总数为 ,C正确;
D.晶胞中含有4个 ,其最简式量为 ,其晶胞边长为 ,根据 ,则X
晶体密度为 ,D正确;
故选B。