文档内容
热点 10 化学反应的方向与限度
化学反应的方向与限度是江苏高考的必考内容,属于热点问题,主要考查根据ΔH,
ΔS判断反应方向及根据自发或非自发判断ΔH,ΔS,平衡常数的表表达式、影响化学反应
的因素、平衡移动的判定等相关知识点,备考时关注核心考点的掌握至关重要。
一、化学反应的方向与焓变的关系
1.下列反应进行的方向与ΔH之间的关系
(1)H (g)+O(g)===H O(l),燃烧反应是放热反应,ΔH<0,常温下能自发进行。
2 2 2
(2)Zn(s)+CuSO (aq)===ZnSO (aq)+Cu(s),该反应是放热反应,ΔH<0,常温下能自发进行。
4 4
(3)(NH )CO(s)===NHHCO (s)+NH (g) ΔH=+56.7 kJ·mol-1,该反应在常温下能自发进
4 2 3 4 3 3
行。
(4)CaCO(s)===CaO(s)+CO(g) ΔH>0,该反应在常温下不能自发进行,但在较高温度下
3 2
能自发进行。
2.自发反应与焓变的关系
大多数放热反应是可以自发进行的,但也有很多吸热反应能自发进行,因此,反应焓变是
与反应进行的方向有关的因素之一,但不是决定化学反应能否自发进行的唯一因素。
二、化学反应的方向与熵变的关系
1.熵的含义
自发过程的体系趋向于由有序转变为无序,体系的混乱度增大。体系的混乱度常用熵来描
述,熵的概念是表示体系的混乱或无序程度的物理量,其符号为S。熵值越大,体系的混
乱度越大。
2.影响熵大小的因素
(1)同一条件下,不同的物质熵值不同。
(2)同一物质的熵与其聚集状态及外界条件有关,如对同一种物质不同状态时熵值大小为
S(g)>S(l)>S(s)。
(3)物质的量越大,分子数越多,熵值越大。
物质由固态到液态、由液态到气态或由固态到气态的过程,熵变为正值,是熵增加的过程。
气体体积增大的反应,熵变通常都是正值,是熵增加的反应。气体体积减小的反应,熵变
通常都是负值,是熵减小的反应。
3.反应熵变与反应方向
(1)二者关系
—(2)结论:不能仅用反应熵变来判断反应能否自发进行。
反应熵变是与反应进行的方向有关的因素之一,但不是决定反应能否自发进行的唯一因素
如:2Al(s)+Fe O(s)===AlO(s)+2Fe(s) ΔS=-39.35 J·mol-1·K-1,上述反应为熵减少的
2 3 2 3
反应,但在一定条件下,该反应也能自发进行。说明“熵判据”也具有一定的局限性。
4.复合判据
(1)判据
(2)温度对反应方向的影响
考向 化学反应的方向与限度的分析判断
1. (2023江苏卷)金属硫化物( )催化反应 ,
既可以除去天然气中的 ,又可以获得 。下列说法正确的是
A. 该反应的
B. 该反应的平衡常数
C. 题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用
D. 该反应中每消耗 ,转移电子的数目约为
【答案】C
【解析】
A.左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5, ,A错误;
B.由方程形式知, ,B错误;
C.由题图知,经过步骤Ⅰ后, 中带部分负电荷的S与催化剂中的M之间形成了作用
力,C正确;
D . 由 方 程 式 知 , 消 耗 同 时 生 成 , 转 移 , 数 目 为
,D错误;
故选C。
2. (2022江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要
方法。反应为 ,下列说法正确的是
A. 上述反应
B. 上述反应平衡常数
C. 上述反应中消耗 ,转移电子的数目为
D. 实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】
A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,
故A错误;
B.由方程式可知,反应平衡常数 ,故B正确;
C.由方程式可知,反应每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气
转移电子的数目为3mol×4× ×6.02×1023=3×6.02×1023,故C错误;
D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气
对空气污染程度增大,故D错误;
故选B。
3. (2021江苏卷)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化
2 3生产HNO;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放
3 3
电条件下,N 与O 反应生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g)
2 2 2 2 2
ΔH=-116.4kJ·mol-1。大气中过量的NO 和水体中过量的NH 、NO 均是污染物。通过催化
x
还原的方法,可将烟气和机动车尾气中的NO转化为N,也可将水体中的NO -转化为N。
2 3 2
对于反应2NO(g)+O (g) 2NO (g),下列说法正确的是
2 2
A. 该反应的ΔH<0,ΔS<0
B. 反应的平衡常数可表示为K=
C. 使用高效催化剂能降低反应的焓变
D. 其他条件相同,增大 ,NO的转化率下降
【答案】A
【解析】
A.2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1,反应气体物质的量减少,ΔS<0,故A
2 2
正确;
B.2NO(g)+O (g) 2NO (g)反应的平衡常数可表示为K= ,故B错误;
2 2
C.使用高效催化剂,反应的焓变不变,故C错误;
D.其他条件相同,增大 ,NO的转化率增大,故D错误;
选A。
(建议用时:45分钟)
1.(2023上·江苏扬州·高三扬州中学校考期中)下列说法正确的是
A.常温下,反应2NO(g)+O (g)=2NO (g)能自发进行,该反应的ΔH>0
2 2
B.2 mol SO 与1 mol O 混合反应生成SO ,转移电子数为4×6.02×1023
2 2 3
C.常温下,0.1 mol·L-1氨水稀释后,溶液中 的值增大
D.用pH均为11的NaOH溶液和氨水分别中和等体积等物质的量浓度的盐酸,消耗氨
水的体积更大
【答案】C
【解析】A.常温下2NO(g)+O (g)=2NO (g)能够自发进行,说明 H-T△S<0,已知该反应
2 2
的 S<0,所以其 H<0,故A错误;
△
△ △B.2 mol SO 与1 mol O 混合,由于该反应为可逆反应,反应生成SO 的物质的量小于
2 2 3
1mol,则转移电子的物质的量小于4mol,所以转移电子数小于4×6.02×1023,故B错误;
C.常温下,0.1 mol•L-1氨水稀释后氢氧根离子浓度减小,温度不变一水合氨的电离平衡常
数不变,则 的比值增大,故C正确;
D.用pH均为11的NaOH溶液和氨水分别中和等体积等物质的量浓度的盐酸,由于氨水
的浓度较大,则消耗NaOH溶液的的体积更大,故D错误;
故选:C。
2.(2023上·江苏苏州·高三阶段练习)催化氧化法制取SO 的反应如下:2SO (g)+O(g)
3 2 2
2SO (g) △H=-196.6kJ/mol,下列关于工业上制取浓硫酸的说法正确的是
3
A.催化氧化法制取SO 能够自发进行的原因是△S>0
3
B.2molSO (g)和1molO (g)所含化学键的键能总和比2molSO (g)大196.6kJ/mol
2 2 3
C.工业上用浓硫酸吸收SO 时是将SO 从吸收塔底部通入,浓硫酸从塔顶喷淋下来,
3 3
这样操作的目的是为了提高SO 的吸收率
3
D.1molSO 与足量O 反应,放出的热量为98kJ
2 2
【答案】C
【解析】A. 在一定条件下可自发进行,则 G=△H-T•△S<0,该反应的 H<0, S<
0,只有在低温下才能使△G<0,能够自发进行的原因不是△S>0,故A错误;
△ △ △
B.2mol SO 和1mol O 中的化学键键能总和小于2mol SO 中的化学键键能总和,故B错误;
2 2 3
C. 工业上用浓硫酸吸收SO 时是将SO 从吸收塔底部通入,浓硫酸从塔顶喷淋下来,使
3 3
浓硫酸和三氧化硫充分接触,增大接触面积,提高吸收效率,这样操作的目的是为了提高
SO 的吸收率,故C正确;
3
D. 反应是可逆反应,1molSO 与足量O 反应,放出的热量少于98kJ,故D错误;
2 2
故选C。
3.(2023上·江苏苏州·高三江苏省苏州实验中学阶段练习)下列有关说法正确的是
A.银质奖牌久置后表面变暗是因为发生了电化学腐蚀
B.因为二氧化碳普遍存在,所以钢铁的电化学腐蚀以析氢腐蚀为主
C.常温常压下,氢氧燃料电池放电过程中消耗 ,转移电子的数目为
D.一定温度下,反应 能自发进行,该反应的
【答案】D
【解析】A.银在空气中被氧气氧化发生化学腐蚀,和电化学腐蚀无关,A错误;
B.钢铁的电化学腐蚀是铁与氧气反应,以吸氧腐蚀为主,B错误;
C.常温常压下11.2L氢气的物质的量无法计算,也就无法计算出转移电子的数目,C错误;
D.根据ΔH-TΔS<0反应能自发进行,该反应ΔS<0,则一定温度下该反应能自发进行,说
明ΔH<0,D正确;故答案选D。
4.(2023上·江苏南通·高三统考期中)下列说法正确的是
A.反应 在常温下可自发进行,则该反应的
B.反应 达到平衡时,
C. 具有还原性,因此可用作氢氧燃料电池的燃料
D.一定温度下,增大反应 容器的体积,平衡不移动
【答案】C
【解析】A.根据△G=△H-T·△S<0反应可以自发进行,该反应的△S<0,室温下能发生,
则应满足△H<0,A错误;
B.反应 达到平衡时, ,B错误;
C. 具有还原性,因此可用作氢氧燃料电池的燃料,C正确;
D.一定温度下,增大反应 容器的体积,平衡向气体体积增加
的方向移动,向正向移动,D错误;
答案选C。
5.(2023上·江苏扬州·高三统考期中)将CO 转化为有机燃料是实现碳资源可持续利用的
2
有效途径。CO 催化加氢合成CHOH总反应为CO(g)+3H(g) CHOH(g)+
2 3 2 2 3
HO(g) ΔH=-49.4kJ/mol。我国学者提出该反应的机理如图(其中吸附在催化剂表面的物种
2 1
用“*”标注)所示。下列说法正确的是
A.CO 催化加氢合成CHOH总反应的ΔS<0,反应高温自发
2 3
B.提高CO 转化为CHOH的平衡转化率,需要研发在低温区高效的催化剂
2 3
C.反应④中存在共价键的断裂和共价键的生成
D.反应①②过程中,碳元素化合价不断降低
【答案】D【解析】A.由图可知,总反应为CO+3H =CH OH+H O,气体的量减少,总反应的△S<
2 2 3 2
0,已知ΔH<0,根据自发反应的判据ΔG=ΔH-TΔS<0可知,反应低温自发,故A错误;
1
B.催化剂不能使平衡发生移动,不能提高CO 的平衡转化率,故B错误;
2
C.根据机理图可判断反应④中只存在O-H共价键的生成,故C错误;
D.CO
2
中碳元素化合价为+4,∗HCOO中碳为+3价,∗CH
3
O中碳为-1价,反应①②过程
中,碳元素化合价不断降低,故D正确;
故选:D。
6.(2023上·江苏淮安·高三统考期中)在强碱中氢氧化铁可被一些氧化剂氧化为高铁酸根
离子(FeO ),FeO 在酸性条件下氧化性极强且不稳定, Fe O 中铁元素有2、3价;
3 4
HO 可在催化剂Fe O 或Fe O 作用下产生OH,OH能将烟气中的NO、SO 氧化。OH产
2 2 2 3 3 4 2
生机理如下:
反应Ⅰ: Fe3 HO = Fe2 + OOH H (慢反应)
2 2
反应Ⅱ:Fe2 HO = Fe3 OH OH- (快反应)
2 2
对于HO 脱除SO 反应:SO g HO l =H SO l ,下列有关说法不正确的是
2 2 2 2 2 2 2 4
A.该反应能自发进行,则该反应的ΔH 0
B.加入催化剂 Fe O,可提高SO 的脱除效率
2 3 2
C.向固定容积的反应体系中充入氦气,反应速率加快
D.与Fe O 作催化剂相比,相同条件下Fe O 作催化剂时SO 脱除效率可能更高
2 3 3 4 2
【答案】C
【解析】A.SO g HO l =H SO l 熵减,该反应能自发进行,
2 2 2 2 4
时自发,则该反应的ΔH 0,A正确;
B.已知:HO 可在催化剂Fe O 或Fe O 作用下产生OH,或结合反应机理:Fe O 催化剂
2 2 2 3 3 4 2 3
表面仅存在Fe3+,Fe3+通过慢反应Ⅰ产生Fe2+再通过快反应Ⅱ产生•OH,总反应速率由慢反
应Ⅰ决定,生成的OH能将烟气中的NO、SO 氧化,则加入催化剂 Fe O,可提高SO 的
2 2 3 2
脱除效率,B正确;
C. 向固定容积的反应体系中充入氦气,反应相关的物质浓度不发生变化,则反应速率不
变,C不正确;
D. 与Fe O 作催化剂相比,相同条件下Fe O 作催化剂时SO 脱除效率可能更高,D正
2 3 3 4 2
确;
答案选C。
7.(2023上·江苏南京·高三南京市第九中学校考阶段练习)下列有关说法正确的是
A.向 氨水中加入少量水,pH减小, 减小
B.常温下,反应 能自发发生反应,则该反应
C.以铁作阳极、铂作阴极,电解饱和食盐水可以制备烧碱D.电解熔融氧化铝时反应的离子方程式为:
【答案】D
【解析】A.向 氨水中加入少量水,根据勒夏特列原理溶液中 减小,
只受温度影响不变,则 增大,故A错误;
B.该反应气态反应物生成固态产物, ,常温下能自发 则 ,
故B错误;
C.以铁作阳极、铂作阴极,阳极是活泼电极,Fe自身放电,电解饱和食盐水无法制得氢
氧化钠,故C错误;
D.熔融态下氧化铝电离为铝离子和氧负离子,电解熔融态的氧化铝离子方程为:
,故D正确;
故答案为:D。
8.(2023上·江苏扬州·高三统考期中)下列有关说法正确的是
A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀
B.合成氨生产中,使用高效催化剂可提高原料平衡转化率
C.反应 在室温下可自发进行,则该反应的
D.10mLpH=2的 溶液加水稀释至100mL,测得溶液的pH=3
【答案】C
【解析】A.若在海轮外壳上附着一些铜块,铁比铜活泼,形成原电池后,铁作负极,则
会加快海轮外壳的腐蚀,A项错误;
B.催化剂只能改变化学反应的速率,不能使化学平衡移动,不能提高原料平衡转化率,B
项错误;
C.由于该反应是两种气体生成一种固体,所以该反应的ΔS<0,若该反应可自发,需满
足ΔG=ΔH-TΔS<0,由于ΔS<0,T>0,所以该反应必须满足ΔH<0才能使ΔG<0,C项
正确;
D.CHCOOH是弱酸,pH=2的CHCOOH由10ml稀释到100ml,稀释10倍,pH应小于
3 3
3,D项错误;
故选C。
9.(2023上·江苏常州·高三常州市第一中学校考期中)750℃时,NH 和O 发生以下两个
3 2
反应:
①4NH (g)+5O(g) 4NO(g)+6H O(g) △H
3 2 2 1
②4NH (g)+3O(g) 2N(g)+6HO(g) △H
3 2 2 2 2下列说法正确的是
A.反应①的平衡常数可表示为K=
1
B.反应②的△S<0
C.反应①中每生成2molNO,转移电子数约为6.02×1024
D.反应②的△H=2E(N≡N)+12E(H-O)-12E(N-H)-3E(O=O)
2
【答案】C
【解析】A.反应①的平衡常数可表示为K= ,A错误;
1
B.反应②反应物生成物均为气态,系数之和反应物小于生成物,所以反应②的△S大于
0,B错误;
C.由方程式可知生成1molNO时电子转移5mol,所以反应①中每生成2molNO,转移电子
10mol约为6.02×1024,C正确;
D.反应②的△H=-2E(N≡N) ,D错误;
2
故选C。
10.(2023上·江苏南通·高三海安高级中学校考阶段练习)下列说法或表示方法正确的是
A.用一定浓度的NaOH溶液滴定未知浓度的 时,可用甲基橙作为终点判断
的指示剂
B.25℃时,0.1 溶液加水稀释,溶液中所有离子浓度均减小
C.已知 的燃烧热是283.0kJ/mol,则
D.一定温度下,某容器中发生反应:
,则该反应
【答案】D
【解析】A.用NaOH标准溶液滴定未知浓度的CHCOOH溶液时,所得醋酸钠溶液显碱
3
性,应该用酚酞作指示剂,故A错误;
B.25℃时,0.1 溶液加水稀释,醋酸、氢离子和醋酸根的浓度减小,但
K =c(H+)c(OH-) =10-14,则溶液中氢氧根离子浓度增大,故B错误;
W ·
C.燃烧热是1mol可燃物完全燃烧产生稳定的物质时放出的热量,CO(g)的燃烧热是
283.0kJ·mol-1,则2molCO燃烧放出热量是(2×283.0 )kJ,由于反应物、生成物的能量相同,
所以则 2CO(g) =2CO(g)+O (g)反应的ΔH=+(2×283.0 )kJ·mol-1 ,故C错误;
2 2
D.一定温度下,某容器中发生反应: ,
当ΔH-TΔS<0时可自发,则该反应 ,故D正确;
故选D。11.(2023上·江苏泰州·高三姜堰中学校考期中)含硫矿物是多种化工生产的原料,主要
有硫黄、黄铁矿 、辉铜矿 、明矾 、绿矾 、
胆矾 、重晶石 等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜
矿煅烧可制备Cu单质: 。 直接排放会造成环境污染,可将
其转化,或用石灰乳、 等物质进行回收再利用,对于自发反应
,下列说法正确的是
A.该反应的
B.该反应的化学平衡常数
C.其他条件不变,增大容器的体积可以增大 的平衡转化率
D.容器体积一定,当混合气体的密度不变时说明该反应到达化学平衡状态
【答案】D
【解析】A.由方程式可知,硫化氢气体回收二氧化硫的反应为熵减的反应,由该反应能
自发反应可知,反应ΔH—TΔS<0,则该反应为焓变小于0的放热反应,A错误;
B.由方程式可知,硫化氢气体回收二氧化硫反应的化学平衡常数 ,B
错误;
C.由方程式可知,硫化氢气体回收二氧化硫的反应为气体体积减小的反应,其他条件不
变,增大容器的体积,气体压强减小,平衡向逆反应方向移动,二氧化硫的平衡转化率减
小,C错误;
D.由质量守恒定律可知,反应前后气体的质量不相等,在体积一定的容器中混合气体的
密度会发生变化,则混合气体的密度保持不变能说明正逆反应速率相等,可以判断反应达
到平衡,D正确;
故选D。
12.(2023上·江苏南京·高三南京师大附中校考期中)用尿素水解生成的 催化还原
NO,是柴油机车辆尾气净化的主要方法。反应为
,下列说法不正确的是
A.该反应的
B.该反应的平衡常数
C.该反应中每消耗1mol NO,转移电子的数目约为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小【答案】D
【解析】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应
的 ,A正确;
B.由方程式可知,反应平衡常数 ,B正确;
C.由方程式可知,反应过程中NH 中N元素化合价升高,O 中O元素和NO中N元素化
3 2
合价降低,反应每消耗4mol NH ,即消耗4mol NO,反应转移12mol电子,则反应中消耗
3
1mol NO转移电子的数目约为 ,C正确;
D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气
对空气污染程度增大,D错误;
故选C。
13.(2023上·江苏徐州·高三徐州市第一中学校联考阶段练习)以 Cl、 SO 和 PCl 为原
2 2 3
料, 制备 POCl 和氯化亚砜(SOCl )的原理为:
3 2 3 2 2 3
。下列说法正确的是
2
A.该反应在任意温度下均可自发进行
B.反应平衡常数
C.反应达到平衡状态时,移走部分 POCl ,可以增大正反应速率
3
D.反应中每消耗2.24L Cl ,转移的电子数为0.2×6.02×10²³
2
【答案】B
【解析】A. 该反应 S小于0,如 H小于0,在低温度下才可自发进行,如 H大于
0,在任意温度下均不可自发进行,故A错误;
B. POCl 是固态,反应平衡常数 ,故B正确;
3
C. POCl 是固态,反应达到平衡状态时,移走部分 POCl ,对正反应速率没有影响,故
3 3
C错误;
D. 氯气的状态不能确定,反应中每消耗2.24L Cl ,无法计算转移的电子数,故D错误;
2
故选B。
14.(2023上·江苏淮安·高三马坝高中校考阶段练习)对于反应
,下列有关说法正确的是
A.该反应只有在高温条件下能自发进行
B.该反应的还原产物是 和 ,氧化产物是
C.达到平衡时,升高温度, (正)减小、 (逆)增加
D. 时,说明反应达到平衡【答案】B
【解析】A.反应的∆H<0,∆S>O,根据吉布斯自由能 ∆G=∆H-T∆S<0,该反应在任何温
条件下都能自发进行,A错误;
B.反应中N的化合价升高,O的化合价降低,故还原产物是 和 ,氧化产物是
,B正确;
C.升高温度, (正)和 (逆)均增加,C错误;
D.各物质的浓度不再变化达到平衡,浓度之比等于化学计量数之比不能说明达到平衡,D
错误;
故选B。
15.(2023上·江苏徐州·高三徐州市第七中学校考阶段练习) 在催化剂CuCl 作用下,通
2
过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为
。对于反应
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.其他条件相同,增大 ,能提高HCl的转化率
D.上述反应中消耗1molHCl,转移电子的数目为6.02×1023
【答案】D
【解析】A.由题干反应方程式可知,反应物的气体系数和比生成物的气体系数和大,故
上述反应 ,A错误;
B.由题干反应方程式可知,HO是气态,故上述反应平衡常数 ,B
2
错误;
C.其他条件相同,增大 ,即增大HCl的用量,化学平衡正向移动,则导致O 的
2
转化率增大,而HCl的转化率却降低,即不能提高HCl的转化率,C错误;
D.由题干方程式可知,反应中每消耗4molHCl转移4mol电子,则上述反应中消耗
1molHCl,转移电子的数目为6.02×1023,D正确;
故答案为:D。
16.(2023上·江苏南通·高三统考期中)已知:
,下列说法正确的是
A.该反应B.反应物的总煡能小于生成物的总煡能
C.反应平衡常数
D.平衡后升高温度, 增大, 减小,平衡向逆反应方向移动
【答案】B
【解析】A.该反应气体分子数增加,为熵增的反应,反应ΔS>0,故A错误;
B.该反应为放热反应,则反应物的总煡能小于生成物的总煡能,故B正确;
C.由方程式可知,反应的平衡常数 ,故C错误;
D.平衡后升高温度,正逆反应速率均增大,故D错误;
故选B。
17.(2023上·江苏南通·高三海安高级中学校考期中) 是一种重要的化工原料,向
溶液中通 可制 ;氨催化氧化得NO,NO继续被氧化为 ,
再与水反应生成硝酸,氨气与硝酸反应可制化肥硝酸铵;氨气与NaClO反应生成肼( ),
肼是一种火箭燃料推进剂,其燃烧热为624 。已知:
,下列说法正确的是
A.该反应
B.反应物的总键能小于生成物的总键能
C.反应平衡常数
D.平衡后升高温度, 增大, 减小,平衡向逆反应方向移动
【答案】B
【解析】A.该反应气体分子数增加,为熵增的反应,反应ΔS>0,故A错误;
B.该反应为放热反应,则反应物的总键能小于生成物的总键能,故B正确;
C.由方程式可知,反应的平衡常数 ,故C错误;
D.平衡后升高温度,正逆反应速率均增大,故D错误;
故选B。
18.(2023上·江苏连云港·高三统考期中)我国科学家使用双功能催化剂(能吸附不同粒子)
催化水煤气制 ,反应: ,在低温下获得高转
化率与高反应速率。反应部分过程如图所示:下列说法正确的是
A.该反应高温下不能自发进行,则反应的
B.该反应的平衡常数
C.在整个转化过程中,氧元素的化合价始终不变
D.步骤Ⅰ吸收的能量大于步骤Ⅱ放出的能量
【答案】A
【解析】A.反应为放热反应,根据 反应能自发进行,而该反应高温下不能自发
进行,则反应的 ,A正确;
B.平衡常数等于生成物浓度系数次方之积与反应物浓度系数次方之积的比;该反应的平
衡常数 ,B错误;
C.在步骤Ⅰ转化过程中,氧形成的共价键由2个变为1个,故氧元素化合价发生改变,C
错误;
D.化学键断裂吸收能量,化学键形成放出能量,反应为放热反应,则步骤Ⅰ吸收的能量
小于步骤Ⅱ放出的能量,D错误;
故选A。
19.(2023上·江苏徐州·高三统考期中)汽车安装尾气净化装置也可除去 ,反应方程
式为 ,关于反应
,下列说法正确的是
A.该反应的
B.选择合适的催化剂,可以使 完全转化成
C.及时移除 、 ,正反应速率增大,平衡向正反应方向移动
D.上述反应中每生成 ,转移电子的数目约为
【答案】D
【解析】A.根据气体的系数可知此反应的正反应是气体分子个数减小的反应,所以该反
应的 ,A错误;
B.催化剂只能改变反应速率不能改变转化率,B错误;C.及时移除 、 ,逆反应速率减小,正反应速率开始不变,平衡向正反应方向移动,
导致反应物浓度减小,正反应速率随之减小,C错误;
D.上述反应中当生成1mol氮气时,转移电子为8mol,所以每生成 ,转移电子的
数目约为 ,D正确;
故选D。
20.(2023上·江苏无锡·高三统考期中)CO 氧化乙苯脱氢制苯乙烯的反应方程式是:
2
(g)+CO (g) (g)+HO(g)+CO(g),其反应历程如
2 2
图所示。下列有关说法正确的是
A.该反应的
B.该反应的平衡常数表达式为 ( -表示苯基)
C.催化剂表面酸性越强,苯乙烯的产率越高
D.过程③可能生成副产物
【答案】D
【解析】A.由题干反应方程式可知,该反应正反应是一个气体体积增大的方向,故该反
应的 ,A错误;
B.由题干反应方程式可知,产物中HO为气态,故该反应的平衡常数表达式为
2
( -表示苯基),B错误;
C.根据反应历程可知,催化剂表面需要活化吸附 ,该微粒带负电荷,如果催化剂表面
酸性较强,则带负电荷的氢氧根离子较少,有利于 的吸附,且酸性物质不会和二氧化
碳反应,从而提高了乙苯的转化率,但酸性太强,催化剂表面吸附大量的带正电的H+,导
致 的吸附能力减弱,不利乙苯转化率的提高,故并不是催化剂表
面酸性越强,苯乙烯的产率越高,C错误;
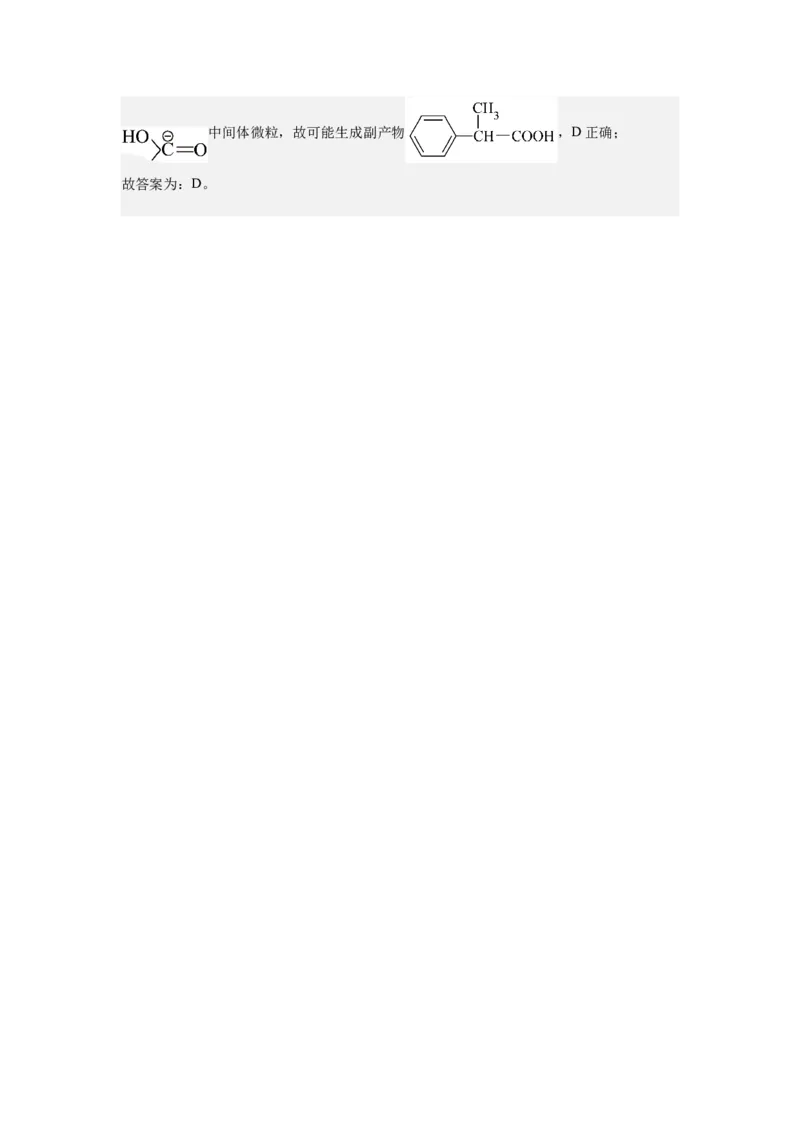
D.由题干反应历程图示信息可知,过程③中存在 和中间体微粒,故可能生成副产物 ,D正确;
故答案为:D。