文档内容
热点专项 信息型方程式的书写
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 氧化还原反应信息化学方程式书写...................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.信息氧化还原反应方程式书写程序...............................................................................................................
2.常见的氧化剂和还原剂、氧化产物和还原产物............................................................................................
3.氧化还原方程式配平的基本原则...................................................................................................................
4.“补缺”的技巧..............................................................................................................................................
【命题预测】...........................................................................................................................................................
题型二 非氧化还原反应信息化学方程式书写.................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.非氧化还原反应陌生化学方程式的书写.......................................................................................................
2.分步法书写非氧化还原方程式.......................................................................................................................
【命题预测】...........................................................................................................................................................
考点要求 考题统计 考情分析
2024·全国新课标卷,8,14分; 陌生方程式的书写是高考题中常见的题型,
氧化还原 2024·辽吉黑卷,16,14分; 往往通过陌生情境下题干语言或化工流程,
反应信息 2023•辽宁省选择性考试, 给出反应发生的环境,写出反应的化学方程
方程式 16(5);2022•河北省选择性考 式。这就要求通过阅读题干、发现本质、寻
试,15(3)(5);2022•湖南选择性 求规律,进而完成旧知识在新情景中的正确考试,17(2)(3);(2021·全国甲
迁移。2025年此考点将继续在非选择题呈
卷,26(2);
现。以现代工业生产为基础,一般简单介绍
该工艺生产的原材料和工艺生产的目的(包括
副产品),然后用框图形式将原料到产品的主
要生产工艺流程表示出来,根据生产过程中
非氧化还 2023•全国甲卷,26(5);2023•江 涉及的化学知识设计陌生离子方程式、氧化
原反应信 苏卷,17(1);2021·全国乙卷, 还原方程式的来进行书写。
息方程式 26(1)题型一 氧化还原反应信息方程式书写
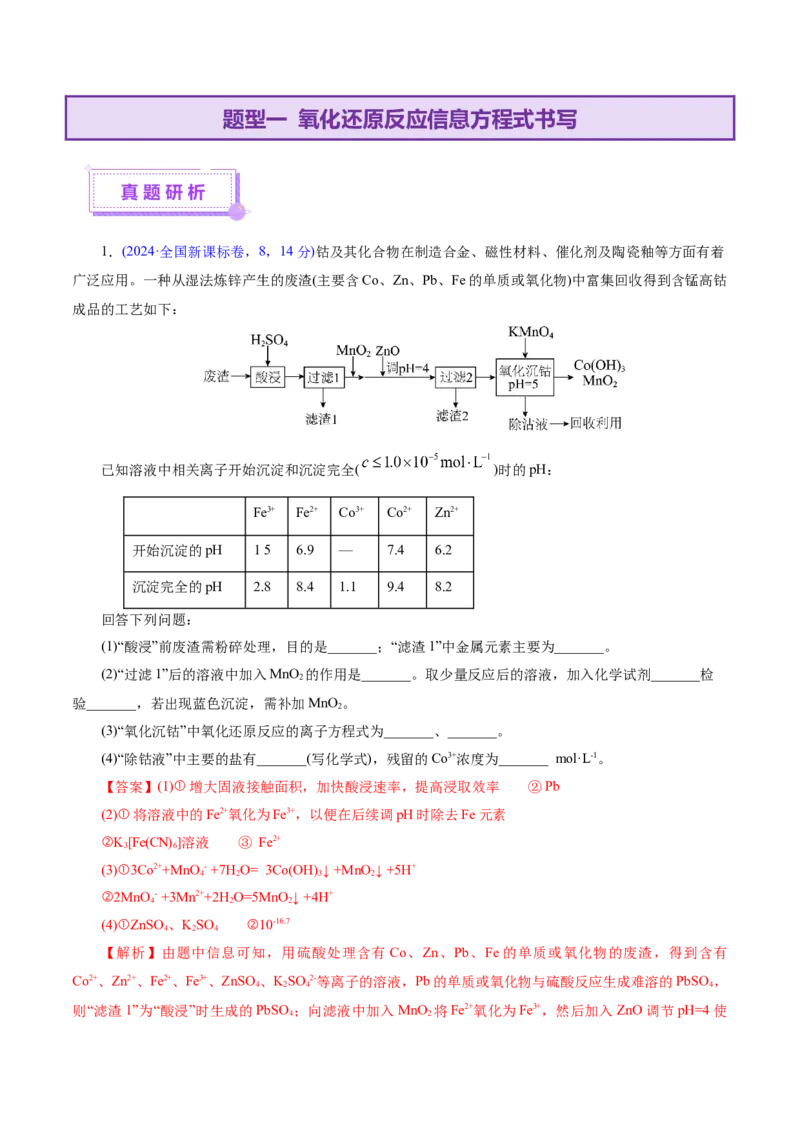
1.(2024·全国新课标卷,8,14分)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着
广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴
成品的工艺如下:
已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
Fe3+ Fe2+ Co3+ Co2+ Zn2+
.
开始沉淀的pH 15 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
回答下列问题:
(1)“酸浸”前废渣需粉碎处理,目的是_______;“滤渣1”中金属元素主要为_______。
(2)“过滤1”后的溶液中加入MnO 的作用是_______。取少量反应后的溶液,加入化学试剂_______检
2
验_______,若出现蓝色沉淀,需补加MnO 。
2
(3)“氧化沉钴”中氧化还原反应的离子方程式为_______、_______。
(4)“除钴液”中主要的盐有_______(写化学式),残留的Co3+浓度为_______ mol·L-1。
【答案】(1)①增大固液接触面积,加快酸浸速率,提高浸取效率 ②Pb
(2)①将溶液中的Fe2+氧化为Fe3+,以便在后续调pH时除去Fe元素
②K [Fe(CN) ]溶液 ③ Fe2+
3 6
(3)①3Co2++MnO - +7H O= 3Co(OH) ↓+MnO ↓+5H+
4 2 3 2
②2MnO - +3Mn2++2H O=5MnO ↓+4H+
4 2 2
(4)①ZnSO、KSO ②10-16.7
4 2 4
【解析】由题中信息可知,用硫酸处理含有 Co、Zn、Pb、Fe的单质或氧化物的废渣,得到含有
Co2+、Zn2+、Fe2+、Fe3+、ZnSO、KSO 2-等离子的溶液,Pb的单质或氧化物与硫酸反应生成难溶的PbSO ,
4 2 4 4
则“滤渣1”为“酸浸”时生成的PbSO ;向滤液中加入MnO 将Fe2+氧化为Fe3+,然后加入ZnO调节pH=4使
4 2Fe3+完全转化为 Fe(OH) ,则“滤渣Ⅱ”的主要成分为 Fe(OH) ,滤液中的金属离子主要是 Co2+、Zn2+和
3 3
Mn2+;最后“氧化沉钴”,加入强氧化剂KMnO ,将溶液中Co2+氧化为Co3+,在pH=5时Co3+形成Co(OH)
4 3
沉淀,而KMnO 则被还原为MnO ,KMnO 还会与溶液中的Mn2+发生归中反应生成MnO ,得到Co(OH)
4 2 4 2 3
和MnO 的混合物,“除钴液”主要含有ZnSO、KSO 。(1)在原料预处理过程中,粉碎固体原料能增大固
2 4 2 4
体与液体的接触面积,从而加快酸浸的反应速率,提高浸取效率;由分析可知,“滤渣1”的主要成分为
PbSO ,则“滤渣1”中金属元素主要为Pb;(2)酸浸液中含有Co2+、Zn2+、Fe2+、Fe3+、SO 2-等离子。由题表中
4 4
数据可知,当Fe3+完全沉淀时,Co2+未开始沉淀,而当Fe2+完全沉淀时,Co2+已有一部分沉淀,因此为了除
去溶液中的Fe元素且Co2+不沉淀,应先将Fe2+氧化为Fe3+,然后调节溶液的pH使Fe3+完全水解转化为
Fe(OH) 沉淀,因此,MnO 的作用是将 Fe2+氧化为 Fe3+,以便在后续调 pH 时除去 Fe 元素。常用
3 2
K[Fe(CN) ]溶液检验Fe2+,若生成蓝色沉淀,则说明溶液中仍存在Fe2+,需补加MnO ;(3)该过程发生两个
3 6 2
氧化还原反应,根据分析中两个反应的反应物、产物与反应环境(pH=5),结合得失电子守恒、电荷守恒和
原子守恒可写出两个离子方程式:3Co2++MnO - +7H O= 3Co(OH) ↓ +MnO ↓ +5H+、2MnO - +3Mn2+
4 2 3 2 4
+2H O=5MnO ↓ +4H+ ;(4)最终得到的“除钴液”中含有的金属离子主要是最初“酸浸”时与加入ZnO调pH
2 2
时引入的Zn2+、加入KMnO “氧化沉钴”时引入的K+,而阴离子是在酸浸时引入的SO 2-,因此其中主要的
4 4
盐有ZnSO 和KSO 。当溶液pH=1.1时c(H+)=10-1.1mol·L-1,Co3+恰好完全沉淀,此时溶液中c(Co3+)=1.0×10-
4 2 4
5mol·L-1,则 ,则 。“除
钴 液 ” 的 pH=5 , 即 c(H + )=10-5mol·L-1 , 则 , 此 时 溶 液 中
。
2.(2024·辽吉黑卷,16,14分)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧
化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS、 包
2
裹),以提高金的浸出率并冶炼金,工艺流程如下:回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为
_______(填化学式)。
(2)“细菌氧化”中,FeS 发生反应的离子方程式为_______。
2
(3)“沉铁砷”时需加碱调节pH,生成_______(填化学式)胶体起絮凝作用,促进了含As微粒的沉降。
(4)“培烧氧化”也可提高“浸金”效率,相比“培烧氧化”,“细菌氧化”的优势为_______(填标号)。
A.无需控温 B.可减少有害气体产生
C.设备无需耐高温 D.不产生废液废渣
(5)“真金不拍火炼”,表明Au难被O 氧化,“浸金”中NaCN的作用为_______。
2
(6)“沉金”中Zn的作用为_______。
(7)滤液②经HSO 酸化,[Zn(CN) ]2-转化为ZnSO 和HCN的化学方程式为_______。用碱中和HCN可
2 4 4 4
生成_______(填溶质化学式)溶液,从而实现循环利用。
【答案】(1)CuSO
4
(2)4FeS +15O +2H O 4Fe3++8SO2-+4H+
2 2 2 4
(3) Fe(OH) (4)BC
3
(5)做络合剂,将Au转化为[Au(CN) ]-从而浸出
2
(6)作还原剂,将[Au(CN) ]-还原为Au
2
(7) Na [Zn(CN) ] +2H SO =ZnSO +4HCN+ Na SO NaCN
2 4 2 4 4 2 4
【解析】矿粉中加入足量空气和HSO ,在pH=2时进行细菌氧化,金属硫化物中的S元素转化为硫酸
2 4
盐,过滤,滤液中主要含有Fe3+、SO 2-、As(Ⅵ),加碱调节pH值,Fe3+转化为Fe(OH) 胶体,可起到絮凝
4 3
作用,促进含As微粒的沉降,过滤可得到净化液;滤渣主要为Au,Au与空气中的O 和NaCN溶液反应,
2
得到含[Au(CN) ]-的浸出液,加入Zn进行“沉金”得到Au和含[Zn(CN) ]2-的滤液②。(1)“胆水”冶炼铜,
2 4
“胆水”的主要成分为CuSO ;(2)“细菌氧化”的过程中,FeS 在酸性环境下被O 氧化为Fe3+和SO 2-,离
4 2 2 4
子方程式为:4FeS+15O +2H O 4Fe3++8SO2-+4H+;(3)“沉铁砷”时,加碱调节pH值,Fe3+转化为
2 2 2 4
Fe(OH) 胶体,可起到絮凝作用,促进含As微粒的沉降;(4)A项,细菌的活性与温度息息相关,因此细菌
3
氧化也需要控温,A不符合题意;B项,焙烧氧化时,金属硫化物中的S元素通常转化为SO ,而细菌氧
2化时,金属硫化物中的S元素转化为硫酸盐,可减少有害气体的产生,B符合题意;C项,焙烧氧化需要
较高的温度,因此所使用的设备需要耐高温,而细菌氧化不需要较高的温度就可进行,设备无需耐高温,
C符合题意;D项,由流程可知,细菌氧化也会产生废液废渣,D不符合题意;故选BC;(5)“浸金”中,
Au作还原剂,O 作氧化剂,NaCN做络合剂,将Au转化为[Au(CN) ]-从而浸出;(6)“沉金”中Zn作还原剂,
2 2
将[Au(CN) ]-还原为Au;(7)滤液②含有[Zn(CN) ]2-,经过HSO 的酸化,[Zn(CN) ]2-转化为ZnSO 和HCN,
2 4 2 4 4 4
反应得化学方程式为:Na[Zn(CN) ] +2H SO =ZnSO +4HCN+ Na SO ;用碱中和HCN得到的产物,可实
2 4 2 4 4 2 4
现循环利用,即用NaOH中和HCN生成NaCN,NaCN可用于“浸金”步骤,从而循环利用。
3.(2023•辽宁省选择性考试,16)某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、
Fe3+、Mg2+和Mn2+)。实现镍、钴、镁元素的回收。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为_______。
【答案】(5)4Co(OH) +O =4CoO(OH)+2H O
2 2 2
【解析】(5) “沉钻镍”中得到的Co(OH) ,在空气中可被氧化成CoO(OH),该反应的化学方程式为:
2
4Co(OH) +O =4CoO(OH)+2H O。
2 2 2
4.(2022•河北省选择性考试)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
【答案】(1)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(2) +2 Fe(NH )Fe(CN) +ClO-+2H+=Fe(NH)Fe(CN) +H O+Cl-+NH+
4 2 6 4 6 2 4
【解析】(1)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO 2-,反应原理为:14Fe3+
4
+FeS +8H O=15Fe2++2 SO 2-+16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ;(2)沉铁工
2 2 4 2 4 3 2 2 4 2 4
序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,氧化工
4 2 6 6
序所发生的离子方程式为:6Fe(NH )Fe(CN) + ClO - +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 NH +。
4 2 6 3 4 6 2 4
5.(2022•湖南选择性考试,17改编)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成
分为TiO,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
2已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(2) TiO 与C、Cl,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl 中含 、 杂质的方法
4
是_______。
【答案】(2) 5TiO+6C+10Cl 5TiCl +2CO+4CO 随着温度升高,CO 与C发生反应C+CO
2 2 4 2 2 2
2CO
(3) 3VOCl +Al=3VOCl +AlCl 蒸馏
3 2 3
【解析】(2)①根据表中数据可知,该温度下C主要生成CO和CO ,根据相同条件下气体的压强之比
2
是物质的量之比可知TiCl 、CO和CO 的物质的量之比约是5:2:4,所以TiO 与C、Cl 反应的总化学方
4 2 2 2
程式为 5TiO+6C+10Cl 5TiCl +2CO+4CO ;②随着温度升高,CO 与 C 发生反应 C+CO
2 2 4 2 2 2
2CO,导致CO含量升高;(3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据
3 2
得失电子守恒和元素守恒配平方程式为3VOCl +Al=3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,
3 2 3 3 4 4
“除硅、铝"过程中可采用蒸馏的方法分离AlCl 、SiCl 。
3 4
6.(2021·全国甲卷,26节选)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答
下列问题:
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO,生成碘化物;再向混合溶
3 2 3 3
液中加入NaIO 溶液,反应得到I。上述制备I 的总反应的离子方程式为___________________________。
3 2 2
【答案】(2)2IO+5HSO===I +5SO+3H++HO
2 2【解析】先向NaIO 溶液中加入计量的NaHSO,生成碘化物即含I-的物质;再向混合溶液(含I-)中加
3 3
入NaIO 溶液,反应得到I ,上述制备I 的两个反应中I-为中间产物,总反应为IO与HSO发生氧化还原
3 2 2
反应,生成SO和I ,根据得失电子守恒、电荷守恒及原子守恒配平离子方程式即可得:2IO+5HSO===I
2 2
+5SO+3H++HO。
2
7.(2021·河北,15节选)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种
熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产
生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(4)工序③中发生反应的离子方程式为_____________________________________________。
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为_______
_______________________________________________________________________________,可代替
NaOH的化学试剂还有____________(填化学式)。
【 答 案 】 (4)2Na + + 2CrO + 2CO + HO===Cr O + 2NaHCO ↓ (5)4Fe(CrO ) + 7O +
2 2 2 3 2 2 2
16NaHCO =====8NaCrO+2Fe O+16CO+8HO NaCO
3 2 4 2 3 2 2 2 3
【解析】(4)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢钠沉淀,
反应的离子方程式为2Na++2CrO+2CO+HO===Cr O+2NaHCO ↓。
2 2 2 3
(5)碳酸氢钠代替高温连续氧化工序中的氢氧化钠发生的主要反应为高温下Fe(CrO ) 与氧气和碳酸氢钠
2 2
反 应 生 成 铬 酸 钠 、 氧 化 铁 、 二 氧 化 碳 和 水 , 反 应 的 化 学 方 程 式 为 4Fe(CrO ) + 7O +
2 2 2
16NaHCO =====8NaCrO+2Fe O+16CO+8HO;若将碳酸氢钠换为碳酸钠也能发生类似的反应。
3 2 4 2 3 2 2
8.(2021·湖南,17节选)Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要
2 3 3
以CePO 形式存在,还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备Ce (CO)·nHO的工
4 2 2 3 2 3 2 2 3 3 2
艺流程如下:回答下列问题:
(5)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为_______________________。
2 3 3 2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料
4 2 3 6 12 6 4
LiFePO ,同时生成CO和HO,该反应的化学方程式为________________________。
4 2
【 答 案 】 (5)6HCO + 2Ce3 + + (n - 3)H O===Ce (CO)·nHO + 3CO↑ (6)6FePO + 3LiCO +
2 2 3 3 2 2 4 2 3
C H O=====9CO↑+6HO↑+6LiFePO
6 12 6 2 4
【解析】(5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知,生成 Ce (CO)·nHO的离子方程
2 3 3 2
式为6HCO+2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑。(6)由在高温条件下,LiCO、葡萄糖(C H O)
2 2 3 3 2 2 2 3 6 12 6
和FePO 可制备电极材料LiFePO ,同时生成CO和HO可知,该反应中Fe价态降低,C价态部分降低、
4 4 2
部分升高,结合得失电子守恒、原子守恒可知该反应的化学方程式为 6FePO +3LiCO +
4 2 3
C H O=====9CO↑+6HO↑+6LiFePO 。
6 12 6 2 4
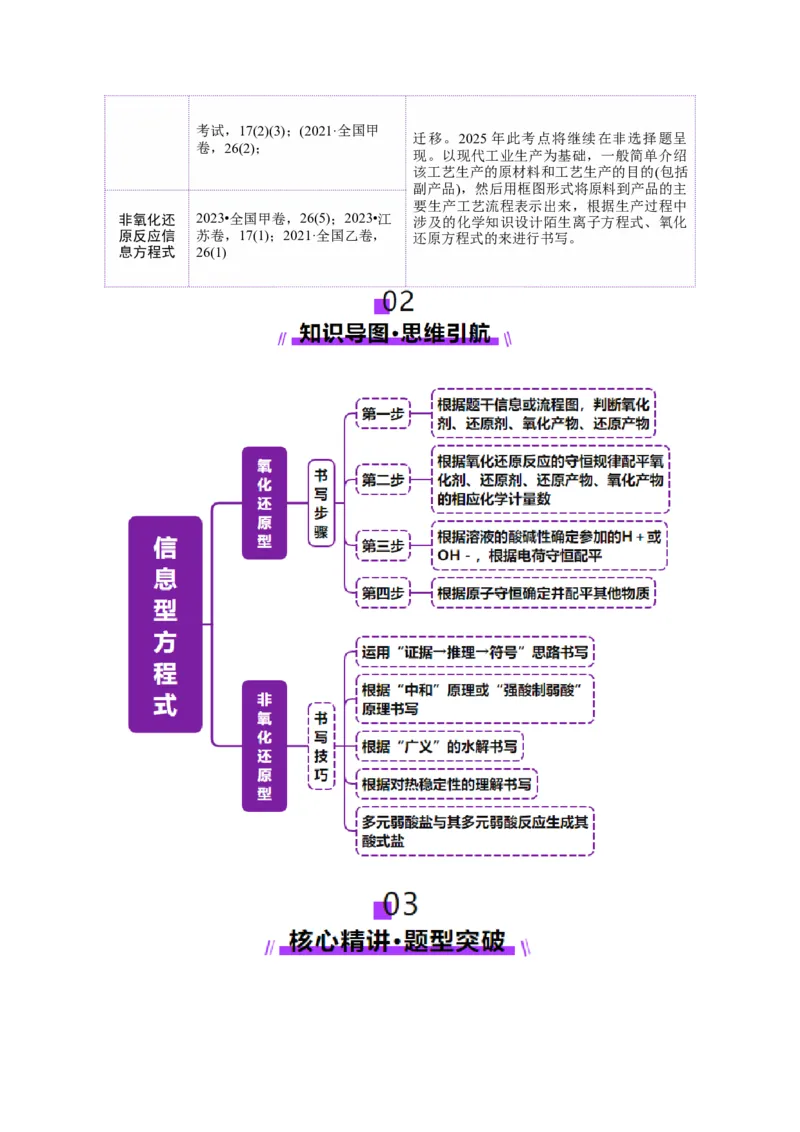
1 . 信息 氧化还原反应 方程式书写程序
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物
第2步:按“氧化剂+还原剂-还原产物+氧化产物”写出方程式,根据氧化还原反应的守恒规律配平氧
化剂、还原剂、还原产物、氧化产物的相应化学计量数。
第3步:根据电荷守恒和溶液的酸碱性,通过在反应方程式的两端添加 H+或OH-的形式使方程式的
两端的电荷守恒。
第4步:根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
新情境氧化还原反应化学(离子)方程式的书写程序
根据电子转移数或常见化 根据 根据溶液的 根据 根据原子
合价确定未知产物中元素 电子 酸碱性确定 电荷 守恒确定
→ → → →
的化合价;根据溶液的酸 守恒 参与反应的 守恒 并配平其
碱性确定未知物的类别 配平 H或OH 配平 他物质
2 . 常见的氧化剂和还原剂、氧化产物和还原产物
KMnO (H+) 、 KClO 、ClO
4 3
氧化剂 Cl O 浓HSO HNO Fe3+ HO
2 2 2 4 3 2 2
MnO -
2
还原产物 Cl- O2- SO NO 、 Mn2+ Fe2+ Cl- HO
2 2NO
2
S2 - SO 、
2
还原剂 I- CO、C Fe2+ NH HO
3 2 2
(H S) SO
2
氧化产物 I S CO Fe3+ NO 、N SO 2- O
2 2 2 4 2
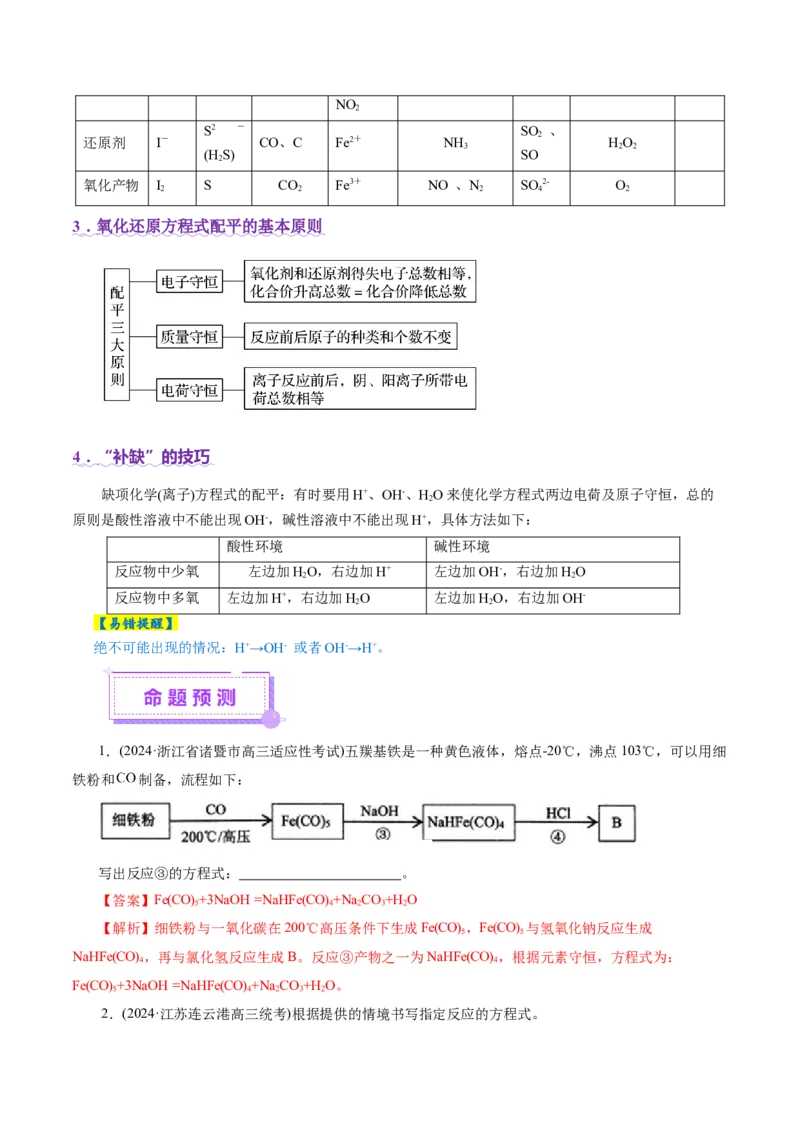
3 . 氧化还原方程式配平的基本原则
4 . “补缺”的技巧
缺项化学(离子)方程式的配平:有时要用H+、OH-、HO来使化学方程式两边电荷及原子守恒,总的
2
原则是酸性溶液中不能出现OH-,碱性溶液中不能出现H+,具体方法如下:
酸性环境 碱性环境
反应物中少氧 左边加HO,右边加H+ 左边加OH-,右边加HO
2 2
反应物中多氧 左边加H+,右边加HO 左边加HO,右边加OH-
2 2
【易错提醒】
绝不可能出现的情况:H+→OH- 或者OH-→H+。
1.(2024·浙江省诸暨市高三适应性考试)五羰基铁是一种黄色液体,熔点-20℃,沸点103℃,可以用细
铁粉和 制备,流程如下:
写出反应③的方程式: 。
【答案】Fe(CO) +3NaOH =NaHFe(CO) +NaCO+H O
5 4 2 3 2
【解析】细铁粉与一氧化碳在200℃高压条件下生成Fe(CO) ,Fe(CO) 与氢氧化钠反应生成
5 5
NaHFe(CO) ,再与氯化氢反应生成B。反应③产物之一为NaHFe(CO) ,根据元素守恒,方程式为:
4 4
Fe(CO) +3NaOH =NaHFe(CO) +NaCO+H O。
5 4 2 3 2
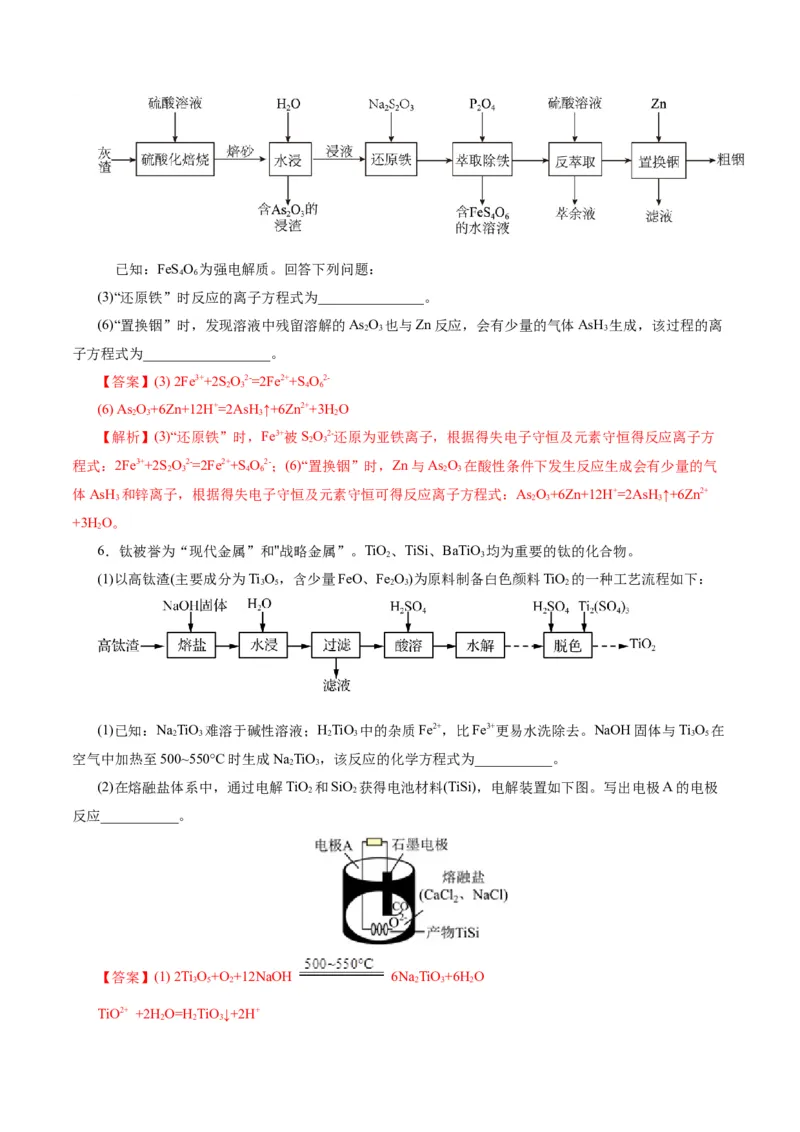
2.(2024·江苏连云港高三统考)根据提供的情境书写指定反应的方程式。一种以MnCO 为原料制取MnO 的流程如图所示,450℃,MnCO 在空气中灼烧得到三种锰的氧化物,
3 2 3
锰元素所占比例随温度变化的曲线如图所示。
(1)写出450℃,MnCO 在空气中灼烧生成主要产物的化学方程式: 。
3
(2)写出“浸取”时MnO 发生反应的离子方程式: 。
2 3
【答案】(1)2MnCO +O 2MnO +2CO
3 2 2 2
(2)Mn O+2H+=MnO+Mn2++H O
2 3 2 2
【解析】由题给流程可知,碳酸锰在空气中灼烧分解生成三氧化二锰和二氧化碳,向三氧化二锰中加
入稀硫酸浸取,三氧化二锰转化为二氧化锰和硫酸锰,过滤得到硫酸锰溶液和二氧化锰。(1)由图可知,
450℃时,二氧化锰的锰元素所占比例最大,说明碳酸锰在空气中灼烧分解生成二氧化锰和二氧化碳,反
应的化学方程式为2MnCO +O 2MnO +2CO ;(2)由分析可知,浸取时发生的反应为三氧化二锰与稀
3 2 2 2
硫酸反应生成二氧化锰和硫酸锰,反应的离子方程式为MnO+2H+=MnO+Mn2++H O。
2 3 2 2
3.以萃铜余液为原料制备工业活性氧化锌,其生产工艺流程如图所示:
(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na SO)氧化法除锰,写出Mn2+被氧化成MnO 的离
2 2 8 2
子方程式___________。
(3)用锌粉除镉(Cd2+ )的离子方程式为___________;沉锌生成碱式碳酸锌[2Zn(OH )·ZnCO·H O]的化学
2 3 2
方程式为___________。
(5)煅烧炉中发生反应的化学方程式为___________。
【答案】(1) Mn2+ +S O2- +2H O= MnO +2SO2-+4H+
2 8 2 2 4
(3) Zn+Cd2+=Zn2++Cd 3ZnSO + 3Na CO+3H O= 2Zn(OH) ·ZnCO·H O↓+3Na SO + 2CO↑
4 2 3 2 2 3 2 2 4 2(5) 2Zn(OH) ·ZnCO·H O 3ZnO+CO ↑+3H O
2 3 2 2 2
【解析】(1)铜萃余液含硫酸30~60g/L,设计采用过硫酸钠(Na SO)氧化法除锰,Mn2+被氧化成
2 2 8
MnO ,过硫酸根离子被还原为硫酸根离子,离子方程式为:Mn2+ + S O2- +2H O= MnO +2SO2-+4H+;
2 2 8 2 2 4
(3)锌与镉离子发生取代反应生成锌离子和单质镉,离子方程式为:Zn+Cd2+=Zn2++Cd;向硫酸锌溶液中加
入碳酸钠溶液生成碱式碳酸锌,相应的方程式为:3ZnSO+ 3Na CO+3H O=
4 2 3 2
2Zn(OH) ·ZnCO·H O↓+3Na SO + 2CO↑;(5)由流程可知,工业碱式碳酸锌在煅烧炉中煅烧生成活性氧化锌,
2 3 2 2 4 2
则相应的方程式为:2Zn(OH) ·ZnCO·H O 3ZnO+CO ↑+3H O。
2 3 2 2 2
4.高锰酸钾在化工生产和环境保护等领域应用十分广泛。以软锰矿(主要成分是MnO ,含有Fe O 和
2 2 3
SiO 等杂质)为原料制备高锰酸钾的工艺流程如图:
2
回答
下列问题:
(2)“焙烧”中有KMnO 生成,该步骤主要反应的化学方程式为_______。
2 4
(5) “歧化”过程中主要反应的离子方程式为_____。
【答案】(2)3MnO +6KOH+KClO 3KMnO +KCl+3H O
2 3 2 4 2
(5) 3MnO2-+4CO +2H O=2MnO -+ MnO ↓+4HCO-
4 2 2 4 2 3
【解析】(2)软锰矿(主要成分是MnO ,含有Fe O 和SiO 等杂质),加入KClO 和KOH,焙烧,将
2 2 3 2 3
MnO 氧化为KMnO ,化学方程式为3MnO +6KOH+KClO 3KMnO +KCl+3H O;(5)向滤液中通入足
2 2 4 2 3 2 4 2
量的CO,KMnO 发生歧化反应:3KMnO +4CO +2H O=2KMnO + MnO ↓+4KHCO ,离子方程式为:
2 2 4 2 4 2 2 4 2 3
3MnO 2-+4CO +2H O=2MnO -+ MnO ↓+4HCO-。
4 2 2 4 2 3
5.铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从高铟烟灰渣(主要含
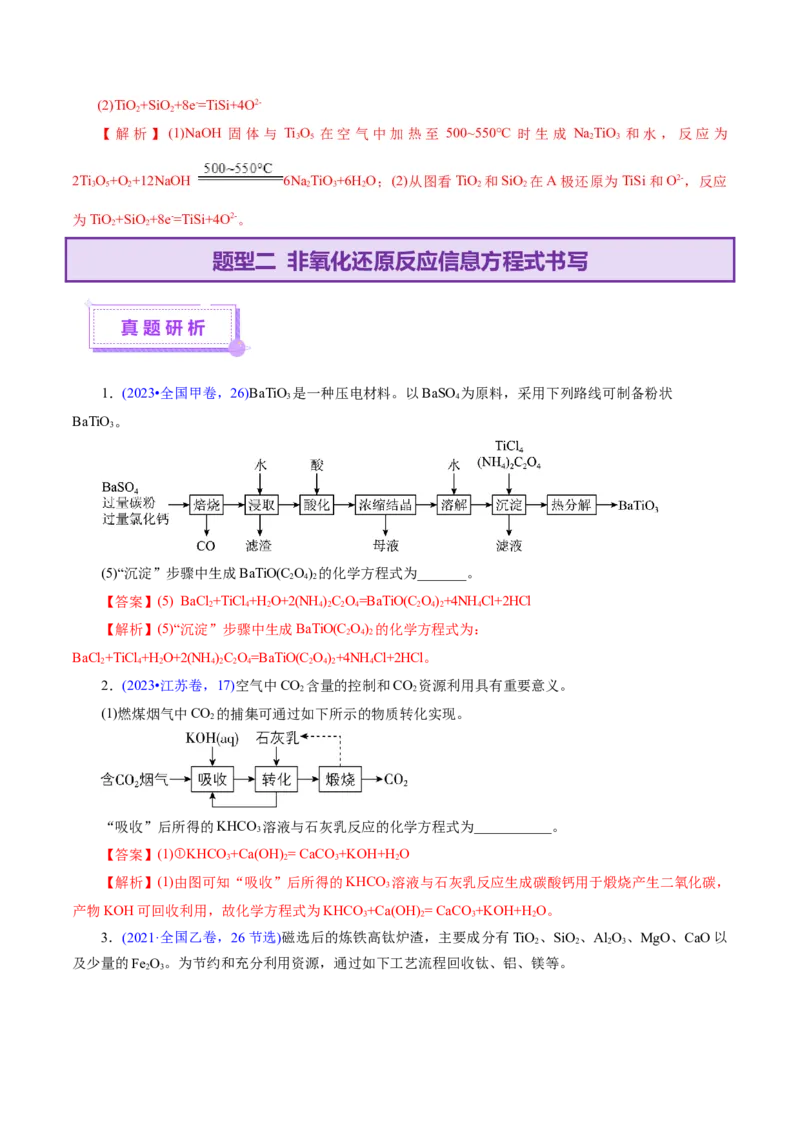
、SiO、FeAsO ·2H O、InO)中提取铟的工艺流程如下:
2 4 2 2 3已知:FeSO 为强电解质。回答下列问题:
4 6
(3)“还原铁”时反应的离子方程式为_______________。
(6)“置换铟”时,发现溶液中残留溶解的As O 也与Zn反应,会有少量的气体AsH 生成,该过程的离
2 3 3
子方程式为__________________。
【答案】(3) 2Fe3++2S O2-=2Fe2++S O2-
2 3 4 6
(6) As O+6Zn+12H+=2AsH ↑+6Zn2++3H O
2 3 3 2
【解析】(3)“还原铁”时,Fe3+被SO2-还原为亚铁离子,根据得失电子守恒及元素守恒得反应离子方
2 3
程式:2Fe3++2S O2-=2Fe2++S O2-;(6)“置换铟”时,Zn与As O 在酸性条件下发生反应生成会有少量的气
2 3 4 6 2 3
体AsH 和锌离子,根据得失电子守恒及元素守恒可得反应离子方程式:As O+6Zn+12H+=2AsH ↑+6Zn2+
3 2 3 3
+3H O。
2
6.钛被誉为“现代金属”和"战略金属”。TiO、TiSi、BaTiO 均为重要的钛的化合物。
2 3
(1)以高钛渣(主要成分为Ti O,含少量FeO、Fe O)为原料制备白色颜料TiO 的一种工艺流程如下:
3 5 2 3 2
(1)已知:NaTiO 难溶于碱性溶液;HTiO 中的杂质Fe2+,比Fe3+更易水洗除去。NaOH固体与Ti O 在
2 3 2 3 3 5
空气中加热至500~550°C时生成NaTiO,该反应的化学方程式为___________。
2 3
(2)在熔融盐体系中,通过电解TiO 和SiO 获得电池材料(TiSi),电解装置如下图。写出电极A的电极
2 2
反应___________。
【答案】(1) 2Ti O+O +12NaOH 6Na TiO+6H O
3 5 2 2 3 2
TiO2+ +2H O=HTiO↓+2H+
2 2 3(2)TiO+SiO +8e-=TiSi+4O2-
2 2
【解析】(1)NaOH 固体与 Ti O 在空气中加热至 500~550°C 时生成 NaTiO 和水,反应为
3 5 2 3
2Ti O+O +12NaOH 6NaTiO+6H O;(2)从图看TiO 和SiO 在A极还原为TiSi和O2-,反应
3 5 2 2 3 2 2 2
为TiO+SiO +8e-=TiSi+4O2-。
2 2
题型二 非氧化还原反应信息方程式书写
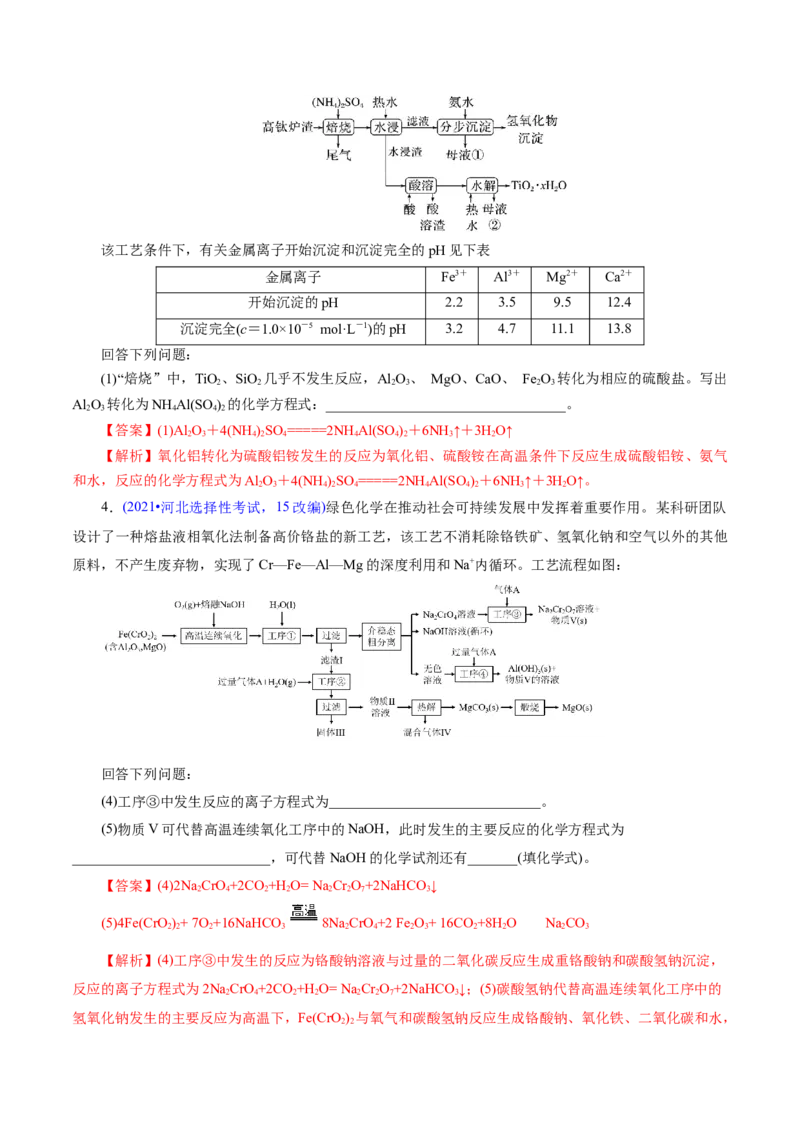
1.(2023•全国甲卷,26)BaTiO 是一种压电材料。以BaSO 为原料,采用下列路线可制备粉状
3 4
BaTiO 。
3
(5)“沉淀”步骤中生成BaTiO(C O) 的化学方程式为_______。
2 4 2
【答案】(5) BaCl+TiCl+H O+2(NH )C O=BaTiO(C O)+4NHCl+2HCl
2 4 2 4 2 2 4 2 4 2 4
【解析】(5)“沉淀”步骤中生成BaTiO(C O) 的化学方程式为:
2 4 2
BaCl+TiCl+H O+2(NH )C O=BaTiO(C O)+4NHCl+2HCl。
2 4 2 4 2 2 4 2 4 2 4
2.(2023•江苏卷,17)空气中CO 含量的控制和CO 资源利用具有重要意义。
2 2
(1)燃煤烟气中CO 的捕集可通过如下所示的物质转化实现。
2
“吸收”后所得的KHCO 溶液与石灰乳反应的化学方程式为___________。
3
【答案】(1)①KHCO +Ca(OH) = CaCO+KOH+H O
3 2 3 2
【解析】(1)由图可知“吸收”后所得的KHCO 溶液与石灰乳反应生成碳酸钙用于煅烧产生二氧化碳,
3
产物KOH可回收利用,故化学方程式为KHCO +Ca(OH) = CaCO+KOH+H O。
3 2 3 2
3.(2021·全国乙卷,26节选)磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以
2 2 2 3
及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、 MgO、CaO、 Fe O 转化为相应的硫酸盐。写出
2 2 2 3 2 3
Al O 转化为NH Al(SO ) 的化学方程式:__________________________________。
2 3 4 4 2
【答案】(1)AlO+4(NH )SO =====2NH Al(SO )+6NH ↑+3HO↑
2 3 4 2 4 4 4 2 3 2
【解析】氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫酸铝铵、氨气
和水,反应的化学方程式为Al O+4(NH )SO =====2NH Al(SO )+6NH ↑+3HO↑。
2 3 4 2 4 4 4 2 3 2
4.(2021•河北选择性考试,15改编)绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队
设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他
原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
(4)工序③中发生反应的离子方程式为______________________________。
(5)物质V可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为
____________________________,可代替NaOH的化学试剂还有_______(填化学式)。
【答案】(4)2Na CrO+2CO +H O= Na Cr O+2NaHCO↓
2 4 2 2 2 2 7 3
(5)4Fe(CrO )+ 7O +16NaHCO 8NaCrO+2 Fe O+ 16CO+8H O Na CO
2 2 2 3 2 4 2 3 2 2 2 3
【解析】(4)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢钠沉淀,
反应的离子方程式为2NaCrO+2CO +H O= Na Cr O+2NaHCO↓;(5)碳酸氢钠代替高温连续氧化工序中的
2 4 2 2 2 2 7 3
氢氧化钠发生的主要反应为高温下,Fe(CrO ) 与氧气和碳酸氢钠反应生成铬酸钠、氧化铁、二氧化碳和水,
2 2反应的化学方程式为4Fe(CrO )+ 7O +16NaHCO 8NaCrO+2 Fe O+ 16CO+8H O;若将碳酸氢钠换
2 2 2 3 2 4 2 3 2 2
为碳酸钠也能发生类似的反应。
5.(2021·福建卷,11改编)四钼酸铵是钼深加工的重要中间产品具有广泛的用途。一种以钼精矿(主要
含MoS,还有 、 的化合物及SiO 等)为原料制备四钼酸铵的工艺流程如下图所示。
2 2
回答下列问题:
(4)“净化”后,溶液中若有低价钼(MoO2-表示),可加入适量HO 将其氧化为MoO2-,反应的离子方
3 2 2 4
程式为_______。
(6)高温下用H 还原(NH )MoO 可制得金属钼,反应的化学方程式为_______。【已知:(NH )MoO
2 4 2 4 13 4 2 4 13
受热分解生成MoO】
3
【答案】(4) H O+MoO2-= MoO 2-+H O
2 2 3 4 2
(6) (NH )MoO +12H 4Mo+2NH +13H O
4 2 4 13 2 3 2
【解析】(4)溶液中若有低价钼(以MoO 2-表示),可加入适量HO 将其氧化为MoO 2-,则氧化剂为
3 2 2 4
HO,还原产物为-2价的O,还原剂为MoO 2-,氧化产物为MoO 2-,则反应的离子方程式为HO+MoO2-=
2 2 3 4 2 2 3
MoO 2-+H O;(6)高温下用H 还原(NH )MoO 可制得金属钼,结合得失电子守恒、原子守恒可知反应的化
4 2 2 4 2 4 13
学方程式为(NH )MoO +12H 4Mo+2NH +13H O。
4 2 4 13 2 3 2
6.(2021•湖南卷,17改编)Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主
2 3 3
要以CePO 形式存在,还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料制备Ce (CO)•nH O的
4 2 2 3 2 3 2 2 3 3 2
工艺流程如图:
回答下列问题:
(5)“沉铈”过程中,生成Ce (CO)•nH O的离子方程式为 ;
2 3 3 2
(6)滤渣Ⅱ的主要成分为 FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料
4 2 3 6 12 6 4LiFePO ,同时生成CO和HO,该反应的化学方程式为 。
4 2
【答案】(5)2Ce3++6HCO-+(n﹣3)HO=Ce (CO)•nH O+3CO↑
3 2 2 3 3 2 2
(6)6FePO +3Li CO+C H O 6LiFePO +9CO↑+6H O
4 2 3 6 12 6 4 2
【解析】(5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知生成Ce (CO)•nH O的离子方程式
2 3 3 2
为2Ce3++6HCO-+(n﹣3)HO=Ce (CO)•nH O+3CO↑↑; (6)由在高温条件下,LiCO、葡萄糖(C H O)和
3 2 2 3 3 2 2 2 3 6 12 6
FePO 可制备电极材料LiFePO ,同时生成CO和HO可知,该反应中Fe价态降低,C价态升高,结合得
4 4 2
失电子守恒、原子守恒可知该反应的化学方程式为6FePO +3Li CO+C H O 6LiFePO +9CO↑+6H O。
4 2 3 6 12 6 4 2
1 . 非氧化还原反应陌生化学方程式的书写
(1)书写非氧化还原反应化学(离子)方程式的步骤:
①根据实验事实写出反应物和生成物的化学式。
②配平化学方程式。
③注明化学方程式发生的条件并注明“↑ ”、“↓”。
(2)书写技巧
①运用“证据→推理→符号”思路书写新情况化学(离子)方程式的基本过程如下:“读”取题目中的
有效信息(证据),写出反应物和生成物的符号(推理+表征),再依据质量守恒、电荷守恒(基本规律),即可
轻松写出规范的方程式。
②根据“中和”原理或“强酸制弱酸”原理书写化学(离子)方程式,如酸(酸式盐)与碱可发生中和反应、
强酸与弱酸盐可以反应。③根据“广义”的水解书写化学(离子)方程式:广义的水解观认为,无论是盐的水解还是非盐的水解,
其最终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质。
④根据对热稳定性的理解书写化学(离子)方程式,如铵盐、弱酸酸式盐、难溶氢氧化物、难溶碳酸盐
受热易分解。
⑤多元弱酸盐与其多元弱酸反应生成其酸式盐。
2 . 分步法书写非氧化还原方程式
陌生的非氧化还原反应主要为复分解反应,抓住复分解反应条件推断产物,结合盐类水解、酸碱强弱
综合分析。这类复杂的化学反应可以采用分步思考,例如,碳酸钠、氢氟酸和氢氧化铝混合物在高温下反
应 制 备 冰 晶 石 , 可 以 分 三 步 理 解 : Al(OH) +3HF=AlF +3H O , NaCO+2HF=2NaF+CO ↑+H O ,
3 3 2 2 3 2 2
AlF+3NaF=Na AlF 。加合得到总反应式为2Al(OH) +3Na CO+12HF=2Na AlF+3CO ↑+9H O。再如在碳酸
3 3 6 3 2 3 3 6 2 2
氢钠溶液中加入少量硫酸亚铁溶液制备碳酸亚铁:Fe2++HCO-=FeCO ↓+H+,H++ HCO -=CO ↑+H O,加合
3 3 3 2 2
得总反应式为Fe2++2 HCO -=FeCO ↓+CO ↑+H O。
3 3 2 2
1.碳酸二甲酯 是一种环保性能优异、用途广泛的化工原料,可以通过下列流
程制备:
写出步骤Ⅲ的化学反应方程式 。
【答案】 CO(NH)+2CH OH= CO(OCH )+2NH
2 2 3 3 2 3
【解析】步骤Ⅲ是尿素和甲醇发生取代反应生成碳酸二甲酯和氨气,反应的化学反应方程式为
CO(NH)+2CH OH= CO(OCH )+2NH。
2 2 3 3 2 3
2.利用制磷肥的副产物氟硅酸钠(Na SiF)生产冰晶石(Na AlF)的工艺流程如下:
2 6 3 6(1)分解过程发生的反应为NaSiF+4NH ·H O===2NaF+4NH F+X↓+2HO。工业上把滤渣X叫白炭
2 6 3 2 4 2
黑,其化学式为____________。
(2)水浴加热过程中生成冰晶石的化学方程式为_________________________________________。
【答案】(1)SiO
2
(2)2NaF+4NH F+NaAlO ==========NaAlF↓+4NH ↑+2HO
4 2 3 6 3 2
【解析】(1)根据化学反应中原子守恒可得X的化学式。(2)根据流程信息和问题(1)反应中的产物可知,
水浴加热过程中氟化钠、氟化铵与偏铝酸钠生成冰晶石沉淀和氨气逸出,促使平衡正向移动。
3.处理含锌废渣在资源利用和环境保护方面具有重要意义。某含锌废渣主要化学组成及制备活性
ZnO工艺流程如下:
元素 Zn Pb Fe Al Cu
含量/% 39.81 12.81 6.66 0.84 0.42
回答下列问
题:
(2)加入KMnO 除去体系中Fe2+的反应离子方程式为_______。
4
(4)“制碱式盐”得到碱式碳酸锌,化学式为Zn(CO)(OH) ·2H O。生成碱式碳酸锌的离子方程式为
5 3 2 6 2
_______。
【答案】 (2) 3Fe2++MnO-+8H O=MnO(OH) ↓+3Fe(OH) ↓+5H+
4 2 2 3
(4)5Zn2++10HCO-=Zn(CO)(OH) ·2H O↓+8CO↑
3 5 3 2 6 2 2
【解析】(2)“氧化除杂”环节,“滤渣2”中含有MnO(OH) 、Fe(OH) ,说明Fe2+和KMnO 反应生成
2 3 4
Fe(OH) 和MnO(OH) ,根据得失电子守恒和电荷守恒配平离子方程式为:3Fe2++MnO-
3 2 4
+8H O=MnO(OH) ↓+3Fe(OH) ↓+5H+;(4)“制碱式盐”得到碱式碳酸锌,化学式为Zn(CO)(OH) ·2H O,说
2 2 3 5 3 2 6 2
明Zn2+和HCO -反应生成Zn(CO)(OH) ·2H O,离子方程式为:5Zn2++10HCO-
3 5 3 2 6 2 3
=Zn(CO)(OH) ·2H O↓+8CO↑。
5 3 2 6 2 2
4.钼是七种重要微量营养元素之一、钼酸钠可用于化学试剂、染料、颜料等领域。以钼矿(主要成分
为MoS )为原料制备金属钼和钼酸钠晶体的主要流程如图所示。
2(2)空气中煅烧钼矿的尾气用过量的氨水处理,反应的离子方程式为___________。
(4)由精钼矿制备钼酸钠的化学方程式___________。
【答案】(2)SO +2 NH ·H O=2NH ++SO2-+H O
2 3 2 4 3 2
(4)9NaClO+MoS +6 NaOH=Na MoO +2Na SO +9NaCl+3HO
2 2 4 2 4 2
【解析】(2)工业煅烧钼矿的尾气为二氧化硫,二氧化硫为酸性气体,能与氨水反应,反应的离子方程
式为:SO +2 NH ·H O=2NH ++SO2-+H O;(4)精钼矿制备钼酸钠时钼元素化合价升高到+6价,氯元素化合
2 3 2 4 3 2
价降低到-1价根据电子转移守恒配平,化学方程式:9NaClO+MoS +6
2
NaOH=Na MoO +2Na SO +9NaCl+3HO。
2 4 2 4 2
5.以钛铁矿(主要成分为FeO·TiO,还含有MgO、CaO、SiO 等杂质)为原料合成锂离子电池的电极材
2 2
料钛酸锂(LiTi O )和磷酸亚铁锂(LiFePO )的工艺流程如下:
4 5 12 4
“溶浸”后溶液中的主要金属阳离子包括Mg2+、Ca2+、TiOCl+,“滤液”经加热水解后转化为富钛渣
(钛元素主要以TiO·2H O形式存在),写出上述转变的离子方程式:_______。
2 2
【答案】TiOCl++3H O TiO·2H O+Cl-+2H+
2 2 2
【解析】第一步:依据题意写出主要反应物及生成物。“溶浸”后溶液中的主要金属阳离子包括
Mg2+、Ca2+、TiOCl+,加热过程中,TiOCl+水解生成TiO·2H O沉淀,过滤得到含有TiO·2H O的富钛渣,
2 2 2 2
则TiOCl++H O→TiO·2H O。第二步:依据质量守恒和电荷守恒完成方程式。①经分析,反应物中有氯元
2 2 2
素,且钛元素的价态未变化,可知右边应加上 Cl-:TiOCl++H O→TiO·2H O+Cl-。②右边比左边多两个
2 2 2
氧原子,且左边电荷数为+1,右边电荷数为-1,溶液呈酸性,根据电荷守恒,可知右边还应补充 H+:
TiOCl++H O→TiO·2H O+Cl-+H+。依据右边有4个氧原子,可知左边HO前的系数为3,氯原子与钛原
2 2 2 2
子个数相等,左边电荷数为+1,可知右边H+的系数为2,即TiOCl++3H O TiO·2H O+Cl-+2H+。
2 2 2
6.硫酸是一种重要的大宗工业化学品,应用广泛,可实现下列转化:(1)过程Ⅰ的化学方程式为 。
(2)已知硫酸分子结构为 过程Ⅱ生成了焦硫酸钠NaSO,画出其阴离子的结构式
2 2 7
;推测焦硫酸钠水溶液呈 (填“酸性”、“中性”或“碱性”),用离子方程式表明原因
。
(3) Na SO,高温下具有强氧化性,受热分解产生SO 气体。过程Ⅲ是将过量NaSO 固体与磁铁矿
2 2 7 3 2 2 7
熔融反应,产生了混合气体。写出NaSO 只与磁铁矿发生反应的总化学方程式 。
2 2 7
(4)过量的焦硫酸 HSO 和苯在加热条件下反应得到苯磺酸,写出反应的化学方程式 。
2 2 7
【答案】(1) NaCl+H SO (浓)=NaHSO +HCl↑
2 4 4
(2) 酸性 SO2-+H O=2H++2SO2-或SO2-+H O=2HSO -
2 7 2 4 2 7 2 4
(3)10NaSO+2 Fe O 10NaSO +3Fe (SO )+SO↑
2 2 7 3 4 2 4 2 4 3 2
(4) +H SO +H SO
2 2 7 2 4
【解析】浓硫酸与氯化钠固体在加热条件下反应生成硫酸氢钠和氯化氢气体,方程式为
NaCl+H SO (浓)=NaHSO +HCl↑,硫酸氢钠固体在加热条件下生产焦亚硫酸钠和水,焦亚硫酸钠和磁铁矿
2 4 4
(四氧化三铁)在加热条件下发生10NaSO+2 Fe O 10NaSO +3Fe (SO )+SO↑。(1)过程Ⅰ的化学方程
2 2 7 3 4 2 4 2 4 3 2
式为NaCl+H SO (浓)=NaHSO +HCl↑;(2)由硫酸的结构知,NaSO 中阴离子焦亚硫酸根SO2-的结构式为
2 4 4 2 2 7 2 7
;由于SO2-与水发生SO2-+H O=2H++2SO2-反应,故溶液显酸性;(3)NaSO,高温下具有强氧
2 7 2 7 2 4 2 2 7
化性,受热分解产生SO 气体,由分析知NaSO 固体与磁铁矿熔融发生10NaSO+2 Fe O
3 2 2 7 2 2 7 3 4
10NaSO +3Fe (SO )+SO↑;(4)过量的焦硫酸 HSO 和苯在加热条件下发生取代反应得到苯磺酸,反应的
2 4 2 4 3 2 2 2 7方程式为 +H SO +H SO 。
2 2 7 2 4