文档内容
高考热点专项 关系式法与热重分析在化学计算中的应用
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
题型一 关系式法.................................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.关系式法.........................................................................................................................................................
2.寻找关系式的方法..........................................................................................................................................
【命题预测】...........................................................................................................................................................
题型二 热重分析法.............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.热重分析法.....................................................................................................................................................
2.热重曲线图的分析方法................................................................................................................................
3.常见的热重曲线类型.....................................................................................................................................
【命题预测】...........................................................................................................................................................
考点要求 考题统计 考情分析
关系式法 2023•山东卷,9;2022·浙江省6 近年来高考试题中纯计算题不多,主要
月卷,27;2021•山东卷, 融入在工艺流程题、综合实验题目中,试题18(3); 常以信息给予题的形式出现,但落点仍是考
查基本计算技能,其中关系式法呈现较多,
热重曲线以图像和文字组合的形式呈现,考
查内容以书写方程式、判断某温度时物质组
2022•全国乙卷,11,6分;2000·
热重分析 成为重点,考查方式以填空、计算等形式较
广东卷;2014·全国Ⅱ卷,
法 为常见,综合考查学生获取信息的能力、处
27(4); 理据的能力和元素守恒的化学思想等题型一 关系式法
1.(2023•山东卷,9)一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含量,
3 2 3 3
实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
2
样品中羟基含量(质量分数)计算正确的是( )
A. B.
C. D.
【答案】C
【解析】用cmol·L-1NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,可以计算乙酸酐的总物质
的量,根据反应方程式[(CH CO) O+ROH→CH COOR+CH COOH]系数关系,得出ROH与乙酸酐反应后剩
3 2 3 3
余的乙酸酐的物质的量,由此可以计算与ROH反应的乙酸酐的物质的量,即R-OH的物质的量,即羟基的
含量。根据滴定过程中,用cmol·L-1NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,消耗标准溶液
VmL,需要消耗cmol·L-1NaOH-甲醇的物质的量为 ,即乙酸酐的总物质的量=
2;则ROH与乙酸酐反应后剩余的乙酸酐的物质的量= ,所以与ROH反应的
乙酸酐的物质的量= ,也即样品ROH中羟基的物质的量,所以ROH样品中羟
基质量分数= ,故选C 。
2.(2022·浙江省6月卷,27)联合生产是化学综合利用资源的有效方法。煅烧石灰石反应:CaCO (s)
3
=CaO(s)+CO(g) ΔH=1.8×102kJ·mol−1,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定
2
比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成CO,其热量有效利用率为50%。石灰窑中产
2
生的富含CO 的窑气通入氨的氯化钠饱和溶液中,40%的CO 最终转化为纯碱。已知:焦炭的热值为30
2 2
kJ·g-l (假设焦炭不含杂质)。请回答:
(1)每完全分解 石灰石(含CaCO 90%,杂质不参与反应),需要投料_______kg焦炭。
3
(2)每生产106kg纯碱,同时可获得_______kgCaO (列式计算)。
【答案】(1)10.8 (2)70
【解析】(1)完全分解100kg石灰石(含CaCO 90%,杂质不参与反应),需要吸收的热量是
3
=162000kJ,已知:焦炭的热值为30 kJ·g-l (假设焦炭不含杂质),其热量有效利
用率为50%,所以需要投料焦炭的质量是 =10800g=10.8kg。(2)根据(1)中计算可知消耗焦炭
的物质的量是 =900mol,参加反应的碳酸钙的物质的量是900mol,这说明参加反应的碳酸钙和焦
炭的物质的量之比为1:1,所以根据原子守恒可知生成氧化钙的质量是 =70kg。
3.(2021•山东卷,18节选)(3)利用碘量法测定WCl 产品纯度,实验如下:
6
①称量:将足量CS(易挥发)加入干燥的称量瓶中,盖紧称重为mg;开盖并计时1分钟,盖紧称重为
2 1mg;再开盖加入待测样品并计时1分钟,盖紧称重为mg,则样品质量为_________g(不考虑空气中水蒸
2 3
气的干扰)。
②滴定:先将WCl 转化为可溶的NaWO,通过IO -离子交换柱发生反应:WO2-
6 2 4 3 4
+Ba(IO )=BaWO +2IO -;交换结束后,向所得含IO -的溶液中加入适量酸化的KI溶液,发生反应:IO -
3 2 4 3 3 3
+5I-+6H+=3I +3H O;反应完全后,用NaSO 标准溶液滴定,发生反应:I+2S O2-=2I-+S O2-。滴定达终点
2 2 2 2 3 2 2 3 4 6
时消耗cmol•L-1的NaSO 溶液VmL,则样品中WCl(摩尔质量为Mg•mol-1)的质量分数为
2 2 3 6
________________。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗NaSO 溶液的体
2 2 3
积将______ (填“偏大”“偏小”或“不变”),样品中WCl 质量分数的测定值将_____ (填“偏大”“偏
6
小”或“不变”)。
【答案】(3)①( m +m- 2m ) ② % 不变 偏大
3 1 2
【解析】(3)①称量时加入足量的CS,盖紧称重为mg,由于CS 易挥发,开盖时要挥发出来,称量
2 1 2
的质量要减少,开盖并计时1分钟,盖紧称重mg,则挥发出的CS 的质量为(m - m )g,再开盖加入待测样
2 2 1 2
品并计时1分钟,又挥发出(m - m )g的CS,盖紧称重为mg,则样品质量为:mg+2(m- m )g-
1 2 2 3 3 1 2
mg=( m +m- 2m )g;②滴定时,根据关系式:WO2-~2IO -~6I ~12 SO2-,样品中n(WCl )=n(WO 2-)=
1 3 1 2 4 3 2 2 3 6 4
n(S O2-)= cV 10-3mol,m(WCl )= cV 10-3mol Mg/mol= g,则样品中WCl 的质量分数为:
2 3 6 6
100%= %;根据测定原理,称量时,若加入待测样品后,开盖时
间超过1分钟,挥发的CS 的质量增大,m 偏小,但WCl 的质量不变,则滴定时消耗NaSO 溶液的体积
2 3 6 2 2 3
将不变,样品中WCl 质量分数的测定值将偏大。
6
关系式法解题步骤1 . 关系式法
实际化工生产中以及化学工作者进行科学研究时,往往涉及到多步反应:从原料到产品可能要经过若
干步反应;测定某一物质的含量可能要经过若干步中间过程。对于多步反应体系,依据若干化学反应方程
式,找出起始物质与最终物质的量的关系,并据此列比例式进行计算求解的方法,称为“关系式”法。
关系式法常常应用于多步进行的连续反应。在多步反应中,第一步反应的产物,即是下一步反应的反
应物。根据化学方程式,每一步反应的反应物和生成物之间有一定的量的关系,即物质的量之比是一定的。
所以,可以利用某中间物质作为 “中介”,找出已知物质和所求物质之间的量的关系。它是化学计算中
的基本解题方法之一,利用关系式法可以将多步计算转化为一步计算,免去逐步计算中的麻烦,简化解题
步骤,减少运算量,且计算结果不易出错,准确率高。
用关系式法解题的关键是建立关系式,而建立关系式一般途径是:
(1) 利用化学方程式之间的化学计量数间的关系建立关系式;
(2) 利用化学方程式的加合建立关系式;
(3) 利用微粒守恒建立关系式。
2 . 寻找关系式的方法
(1)对于独立的化学反应,可以通过化学方程式,或反应中某原子、离子守恒,找
出它们物质的量之间的关系,然后进行计算。
(2)对于连续发生的多步化学反应,可以根据前后某元素的原子、离子的数量不变
找到关系式(假定反应过程中它没有损失),不过象氨氧化法制硝酸的中间反应,虽然有氮原子损失,但对
实际工业生产来说,由于NO的循环利用,故仍可认为有如下关系式:NH ~HNO ,否则应由多个化学反
3 3应找出关系式。
1.用黄铁矿可以制取 HSO ,再用 HSO 可以制取化肥(NH )SO 。煅烧含 FeS 80.2% 的黄铁矿
2 4 2 4 4 2 4 2
75.0 t,最终生产出79.2 t(NH )SO 。已知 NH 的利用率为 92.6%,HSO 的利用率为 89.8%,试求黄铁
4 2 4 3 2 4
矿制取 HSO 时的损失率为( )
2 4
A. 23.8% B. 33.4% C. 35.6% D. 63.8%
【答案】B
【解析】首先须搞清 HSO 的利用率与 FeS 利用率的关系。HSO 的利用率为 89.8%,与 HSO
2 4 2 2 4 2 4
的利用率是 100%、FeS 的利用率为 89.8% 是等价的。并排除 NH 利用率的干扰作用。其次,根据 S
2 3
原子守恒找出已知量 FeS 与未知量(NH )SO 的关系(设黄铁矿的利用率为x):
2 4 2 4
FeS ~ 2H SO ~ 2(NH )SO
2 2 4 4 2 4
120 264
75.0 t×80.2%×89.8%·x 79.2 t
x=66.6%[
黄铁矿的损失率为:1.00-66.6%=33.4%。
2.为测定某石灰石中CaCO 的质量分数,称取W g石灰石样品,加入过量的浓度为6 mol/L的盐酸,
3
使它完全溶解,加热煮沸,除去溶解的CO,再加入足量的草酸铵[(NH )C O ]溶液后,慢慢加入氨水降低
2 4 2 2 4
溶液的酸度,则析出草酸钙沉淀,离子方程式为:C O2-+Ca2+=CaC O↓,过滤出CaC O 后,用稀硫酸溶解:
2 4 2 4 2 4
CaC O+H SO =H C O+CaSO ,再用蒸馏水稀释溶液至V mL。取出V mL用a mol/L的KMnO 酸性溶液
2 4 2 4 2 2 4 4 0 1 4
滴定,此时发生反应: 2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O,若滴定终点时消耗a mol/L的
4 2 2 4 2 2
KMnO V mL,计算样品中CaCO 的质量分数。
4 2 3
【答案】
【解析】本题涉及到化学方程式或离子方程式为 :CaCO +2HCl=CaCl +H O+CO↑,C O2-
3 2 2 2 2 4
+Ca2+=CaC O↓,CaC O+H SO =H C O+CaSO ,2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O。由方程式可
2 4 2 4 2 4 2 2 4 4 4 2 2 4 2 2
以得出相应的关系式:
5CaCO ——5Ca2+——5CaC O——5HC O ——2MnO -
3 2 4 2 2 4 4
5 2
n(CaCO) aV ×10-3 mol
1 3 2n(CaCO) = 2.5 aV ×10-3 mol,样品中:n (CaCO) = 2.5 aV ×10-3× mol,则:ω(CaCO) =
1 3 2 3 2 3
。
3.为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(铁主
要以Fe O 存在)转变成重要的化工原料FeSO (反应条件略)。
2 3 4
活化硫铁矿还原Fe3+的主要反应为FeS +7Fe (SO ) +8HO===15FeSO +8HSO ,不考虑其他反应。
2 2 4 3 2 4 2 4
请回答下列问题:
假如烧渣中的铁全部视为Fe O ,其含量为50%。将a kg质量分数为b%的硫酸加入到c kg烧渣中浸
2 3
取,铁的浸取率为96%,其他杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按
上述流程,第Ⅲ步应加入FeCO________kg。
3
【答案】0.011 8ab-0.646c或-
【解析】n(Fe O)=mol,反应生成Fe (SO ) 消耗HSO 的物质的量为mol,用活化硫铁矿还原Fe3+生
2 3 2 4 3 2 4
成HSO 的物质的量为mol,则剩余HSO 的物质的量为n(H SO ) =×+-mol=(0.102ab-5.571c) mol,
2 4 2 4 2 4 剩
又因为 n(FeCO)~n(H SO ),则应加入 FeCO 的质量为 116 g/mol×(0.102ab-5.571c)mol=(11.832ab-
3 2 4 3
646.236c)g=(0.011 8ab-0.646c) kg或。
4.软锰矿(主要成分MnO ,杂质金属元素 Fe、Al、Mg等)的水悬浊液与烟气中 SO 反应可制备
2 2
MnSO ·H O,反应的化学方程式为:MnO +SO ===MnSO 。
4 2 2 2 4
(1)质量为17.40 g纯净MnO 最多能氧化________L(标准状况)SO 。
2 2
(2)准确称取0.171 0 g MnSO ·H O样品置于锥形瓶中,加入适量HPO 和NH NO 溶液,加热使Mn2+
4 2 3 4 4 3
全部氧化成Mn3+,用c(Fe2+)=0.050 0 mol·L-1的标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),
消耗Fe2+溶液20.00 mL。计算MnSO ·H O样品的纯度(请给出计算过程)。
4 2
【答案】(1)4.48
(2)n(Fe2+)=0.050 0 mol·L-1×=1.00×10-3mol,n(Mn2+)=n(Fe2+)=1.00×10-3mol,m(MnSO ·H O)=
4 2
1.00×10-3mol×169 g·mol-1=0.169 g;MnSO ·H O样品的纯度为:×100%=98.8%
4 2
【解析】(1)根据提供的化学方程式知,1 mol MnO 氧化1 mol SO ,则17.40 g纯净的MnO 最多能氧
2 2 2
化标准状况下SO 的体积为×22.4 L·mol-1=4.48 L。(2)根据滴定原理可得关系式:Mn2+~Mn3+~Fe2+,
2
n(Fe2+)=0.050 0 mol·L-1×0.02 L=1.00×10-3mol,则n(Mn2+)=n(Fe2+)=1.00×10-3mol,m(MnSO ·H O)=
4 2
1.00×10-3mol×169 g·mol-1=0.169 g,故MnSO ·H O样品的纯度为:×100%=98.8%。
4 2题型二 热重分析法
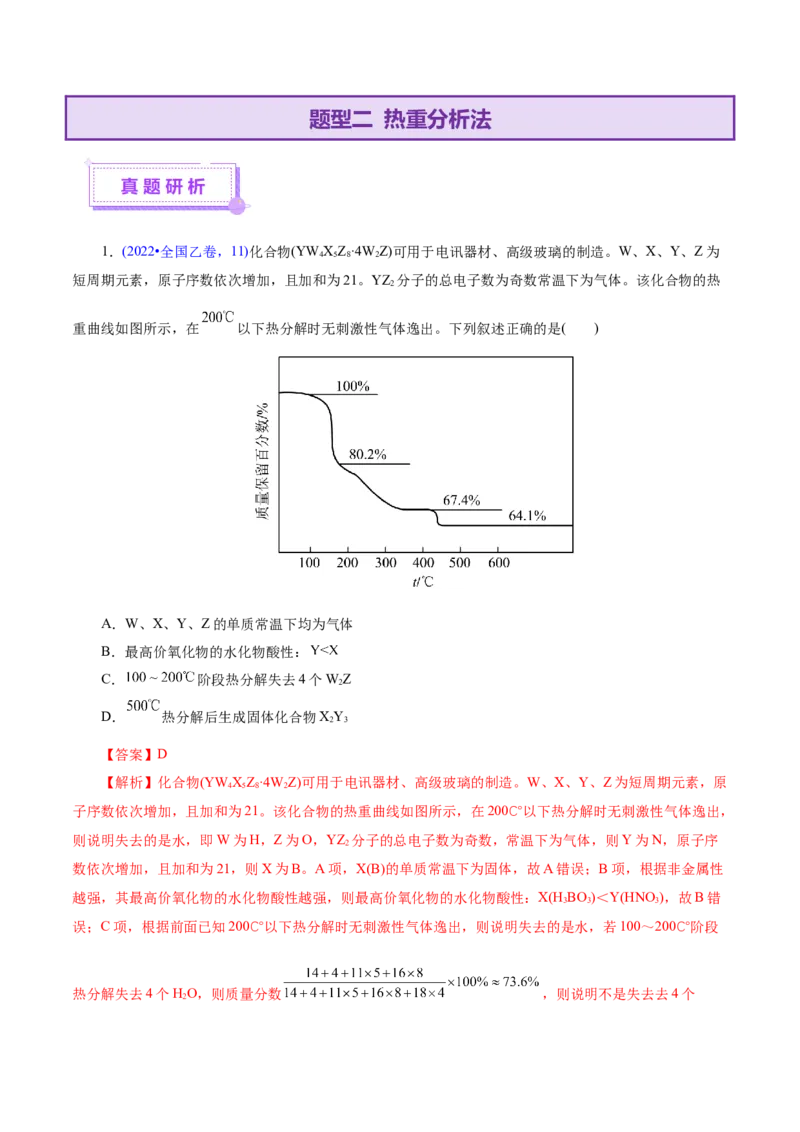
1.(2022•全国乙卷,11)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为
4 5 8 2
短周期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热
2
重曲线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是( )
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个WZ
2
D. 热分解后生成固体化合物XY
2 3
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原
4 5 8 2
子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,
则说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序
2
数依次增加,且加和为21,则X为B。A项,X(B)的单质常温下为固体,故A错误;B项,根据非金属性
越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错
3 3 3
误;C项,根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段
热分解失去4个HO,则质量分数 ,则说明不是失去去4个
2HO,故C错误;D项,化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元
2 4 5 8 2 2 3 2 3
素守恒,则得到关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。故选D。
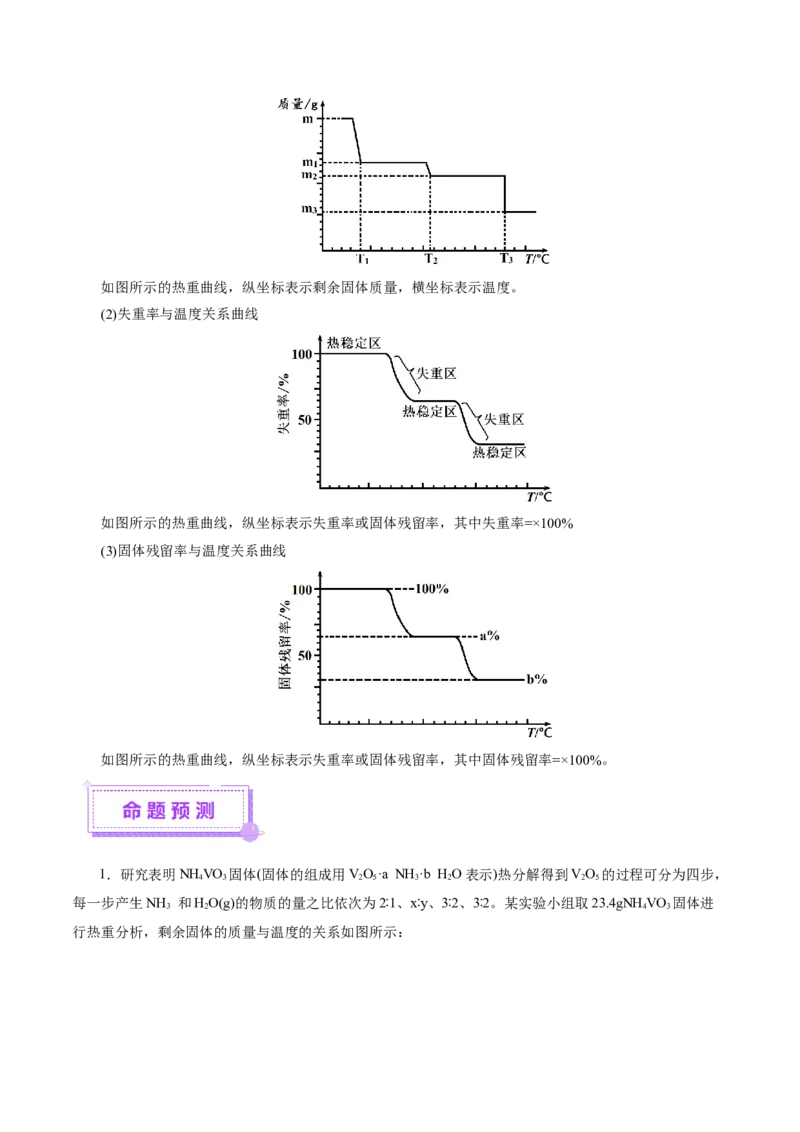
2.(2014·全国Ⅱ卷,27(4))PbO 在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点
2
为样品失重4.0%(即 ×100%)的残留固体。若a点固体组成表示为PbO 或
x
mPbO·nPbO,列式计算x值和m∶n值。
2
【答案】2∶3
【解析】由题意可得二氧化铅分解的化学方程式为PbO PbO + O↑,由失重曲线上的a点为样
2 x 2
品失重4.0%可得: ×32=239×4.0%,解得x=2- ≈1.4,由PbO 和mPbO·nPbO的铅原子和氧原
x 2
子个数比相同可得: =1.4,解得 。
3.(2000·广东卷)下图是100 mgCaC O·H O受热分解时,所得固体产物的质量随温度变化的曲线。试
2 4 2
利用图中信息结合所学的知识,回答下列各问题:(1)温度分别为t 和t 时,固体产物的化学式A是______________,B是______________。
1 2
(2)由CaC O·H O得到A的化学方程式为__________________________________。
2 4 2
(3)由A得到B的化学方程式为____________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
【答案】(1)CaC O CaCO (2)CaC O·H O CaC O +H O↑
2 4 3 2 4 2 2 4 2
(3)CaC O CaCO +CO↑ (4)56 CaO
2 4 3
【解析】(1)由图可知,t 时A点,100mg CaC O·H O的质量变为87.7mg。CaC O·H O的的摩尔质量
1 2 4 2 2 4 2
是146g/mol,设分解后产物的摩尔质量为M,则100×10-3/146=87.7×10-3/M ,解得M=128.04g/mol;
1 1 1
CaC O 的摩尔质量为128g/mol,因此可推测CaC O·H O的分解反应方程式为CaC O·H O CaC O
2 4 2 4 2 2 4 2 2 4
+H O↑;A的化学式是CaC O;t 时B点,87.7mg的CaC O 受热分解,设分解产物的摩尔质量为M ,则
2 2 4 2 2 4 2
87.7× 10 -3/M =68.5×10-3/M ,解得M=99.98g/mol,因此产物B应为CaCO ;(2)由CaC O·H O得到A的
1 2 2 3 2 4 2
化学方程式为CaC O·H O CaC O +H O↑;(3)根据以上分析可知由A得到B的化学方程式为CaC O
2 4 2 2 4 2 2 4
CaCO +CO↑;(4)加热至1000℃~1200℃时,由图可知分解产物C的质量约为38mg,设C点化合物的摩
3
尔质量为M,则68.5×10-3/M =38×10-3/M ,解得M=55.47g/mol;与CaO的摩尔质量(56g/mol)接近,分
3 2 3 3
解方程式应为:CaC O CaCO +CO↑,由此得出C的化学式为CaO,其分子量为56。
2 4 3
两步法”突破热重曲线分析及计算题
热重曲线问题的解题思路
(1)设晶体为1 mol,其质量为m。
(2)失重一般是先失水,再失非金属氧化物。(3)计算每步固体剩余的质量(m ): ×100%=固体残留率。
余
(4)晶体中金属质量不再减少,仍在残留固体(m )中。
余
(5)失重最后一般为金属氧化物,由质量守恒得得m(O),由n(金属)∶n(O),即可求出失重后物质的化学式。
(6)根据失重后物质的化学式,写出相应的化学方程式。
1 . 热重分析法
热重分析法是利用热分析天平记录的热分析曲线,它反映了样品的残留质量和固体残留率(即质量分
数)随温度或时间的变化关系。通过分析热重曲线,就可以知道被测物质在哪个温度段发生了什么变化,有
什么质量损失、失重率是多少、分几步分解、分解的温度范围、热稳定性、结晶水的鉴定等信息,并且可
根据物质失去的重量,求出百分比,由此也可推断出从体系中分离的是什么物质。
热重曲线试题主要以下类型:
(1)从失重的方式来分,热重曲线类试题可分为两类:第一类试样发生分解反应,以脱水、分解等方式
失重,气氛物质不参加反应;第二类试样发生氧化、还原等反应,以氧化、还原等方式失重。当然也有试
题形式上是两者的结合,但本质上可以分步处理,故仍属于上述类型。
(2)从选试样是否已知,热重曲线类试题可分为两类:第一类以已知试样确定产物组成的目标思维法试
题;第二类以未知试样需要确定组成的逆向思维法试题。
2 . 热重曲线图的分析方法
(1)识图。识图的关键是三看:一看轴即横、纵坐标所表示的化学含义(自变量X轴和函数Y轴表示的
意义),寻找X、Y轴之间的关系,因为这是理解题意和进行正确思维的前提;二看点即曲线中的特殊点
(顶点、始点、终点、拐点、交叉点);三看线即曲线的走势(变化趋势是上升、下降、波动、正态、偏态等
变化)。
(2)析图。分析图中为什么会出现这些特殊点,曲线为什么有这样的变化趋势和走向,分析曲线变化的
因果关系;通过联想,把课本内的有关化学概念、原理、规律等与图中的曲线和相关点建立联系。
(3)用图。将相关的化学知识与图中曲线紧密结合,在头脑中构建新的曲线——知识体系,然后运用新
的曲线——知识体系揭示问题的实质,解决实际问题。
3 . 常见的热重曲线类型
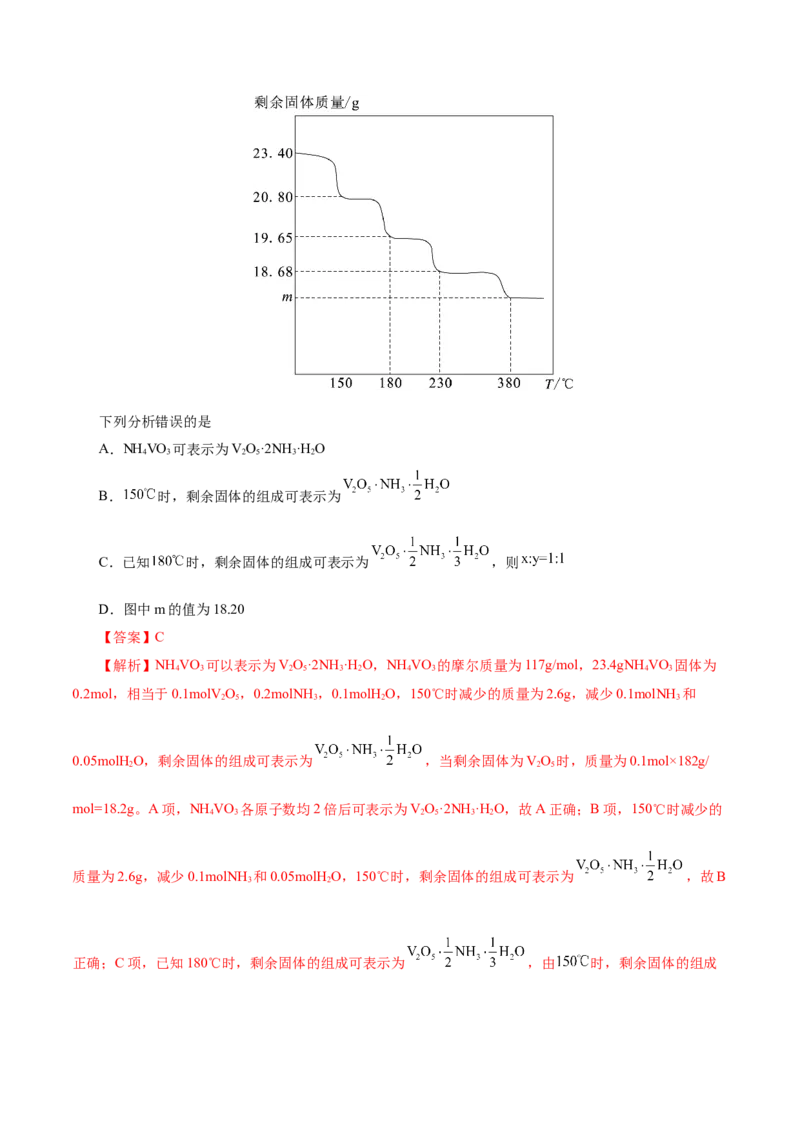
(1)剩余固体质量与温度关系曲线如图所示的热重曲线,纵坐标表示剩余固体质量,横坐标表示温度。
(2)失重率与温度关系曲线
如图所示的热重曲线,纵坐标表示失重率或固体残留率,其中失重率=×100%
(3)固体残留率与温度关系曲线
如图所示的热重曲线,纵坐标表示失重率或固体残留率,其中固体残留率=×100%。
1.研究表明NH VO 固体(固体的组成用VO·a NH ·b HO表示)热分解得到VO 的过程可分为四步,
4 3 2 5 3 2 2 5
每一步产生NH 和HO(g)的物质的量之比依次为2∶1、x∶y、3∶2、3∶2。某实验小组取23.4gNH VO 固体进
3 2 4 3
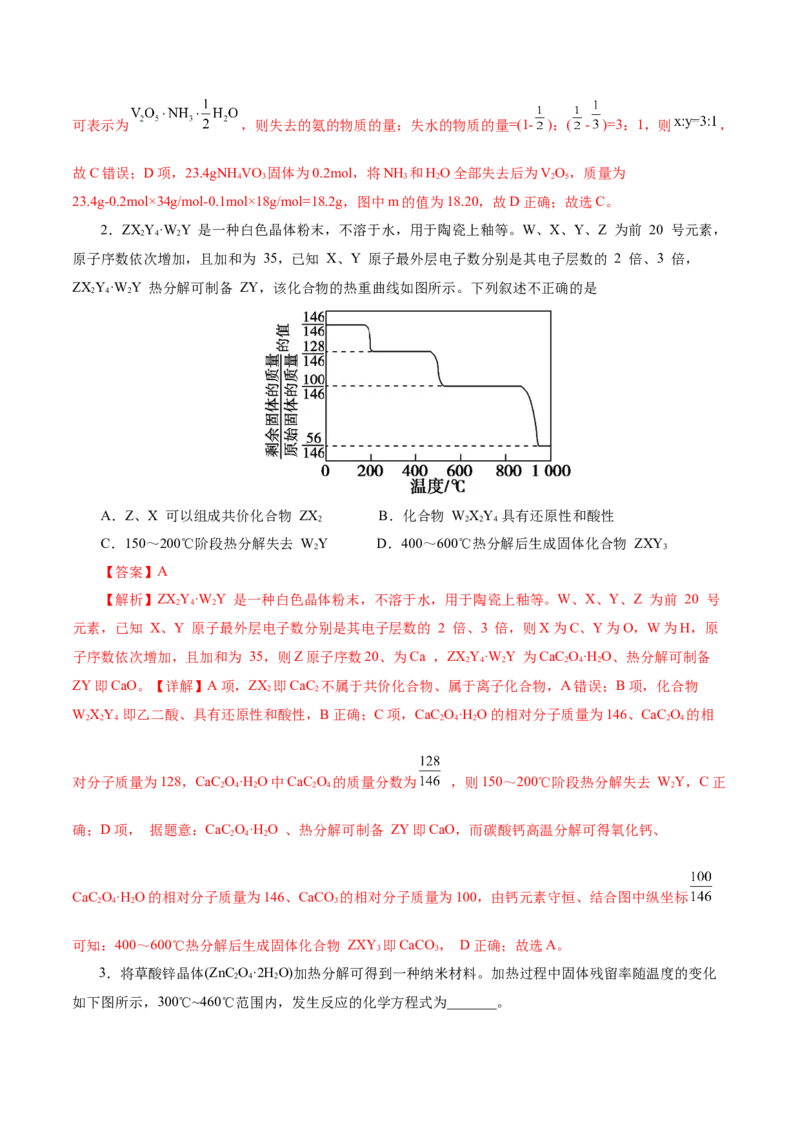
行热重分析,剩余固体的质量与温度的关系如图所示:下列分析错误的是
A.NH VO 可表示为VO·2NH ·H O
4 3 2 5 3 2
B. 时,剩余固体的组成可表示为
C.已知 时,剩余固体的组成可表示为 ,则
D.图中m的值为18.20
【答案】C
【解析】NH VO 可以表示为VO·2NH ·H O,NH VO 的摩尔质量为117g/mol,23.4gNHVO 固体为
4 3 2 5 3 2 4 3 4 3
0.2mol,相当于0.1molVO,0.2molNH ,0.1molHO,150℃时减少的质量为2.6g,减少0.1molNH 和
2 5 3 2 3
0.05molHO,剩余固体的组成可表示为 ,当剩余固体为VO 时,质量为0.1mol×182g/
2 2 5
mol=18.2g。A项,NH VO 各原子数均2倍后可表示为VO·2NH ·H O,故A正确;B项,150℃时减少的
4 3 2 5 3 2
质量为2.6g,减少0.1molNH 和0.05molHO,150℃时,剩余固体的组成可表示为 ,故B
3 2
正确;C项,已知180℃时,剩余固体的组成可表示为 ,由 时,剩余固体的组成可表示为 ,则失去的氨的物质的量:失水的物质的量=(1- ):( - )=3:1,则 ,
故C错误;D项,23.4gNHVO 固体为0.2mol,将NH 和HO全部失去后为VO,质量为
4 3 3 2 2 5
23.4g-0.2mol×34g/mol-0.1mol×18g/mol=18.2g,图中m的值为18.20,故D正确;故选C。
2.ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z 为前 20 号元素,
2 4 2
原子序数依次增加,且加和为 35,已知 X、Y 原子最外层电子数分别是其电子层数的 2 倍、3 倍,
ZXY·W Y 热分解可制备 ZY,该化合物的热重曲线如图所示。下列叙述不正确的是
2 4 2
A.Z、X 可以组成共价化合物 ZX B.化合物 WXY 具有还原性和酸性
2 2 2 4
C.150~200℃阶段热分解失去 WY D.400~600℃热分解后生成固体化合物 ZXY
2 3
【答案】A
【解析】ZXY·W Y 是一种白色晶体粉末,不溶于水,用于陶瓷上釉等。W、X、Y、Z 为前 20 号
2 4 2
元素,已知 X、Y 原子最外层电子数分别是其电子层数的 2 倍、3 倍,则X为C、Y为O,W为H,原
子序数依次增加,且加和为 35,则Z原子序数20、为Ca ,ZXY·W Y 为CaC O·H O、热分解可制备
2 4 2 2 4 2
ZY即CaO。【详解】A项,ZX 即CaC 不属于共价化合物、属于离子化合物,A错误;B项,化合物
2 2
WXY 即乙二酸、具有还原性和酸性,B正确;C项,CaC O·H O的相对分子质量为146、CaC O 的相
2 2 4 2 4 2 2 4
对分子质量为128,CaC O·H O中CaC O 的质量分数为 ,则150~200℃阶段热分解失去 WY,C正
2 4 2 2 4 2
确;D项, 据题意:CaC O·H O 、热分解可制备 ZY即CaO,而碳酸钙高温分解可得氧化钙、
2 4 2
CaC O·H O的相对分子质量为146、CaCO 的相对分子质量为100,由钙元素守恒、结合图中纵坐标
2 4 2 3
可知:400~600℃热分解后生成固体化合物 ZXY 即CaCO , D正确;故选A。
3 3
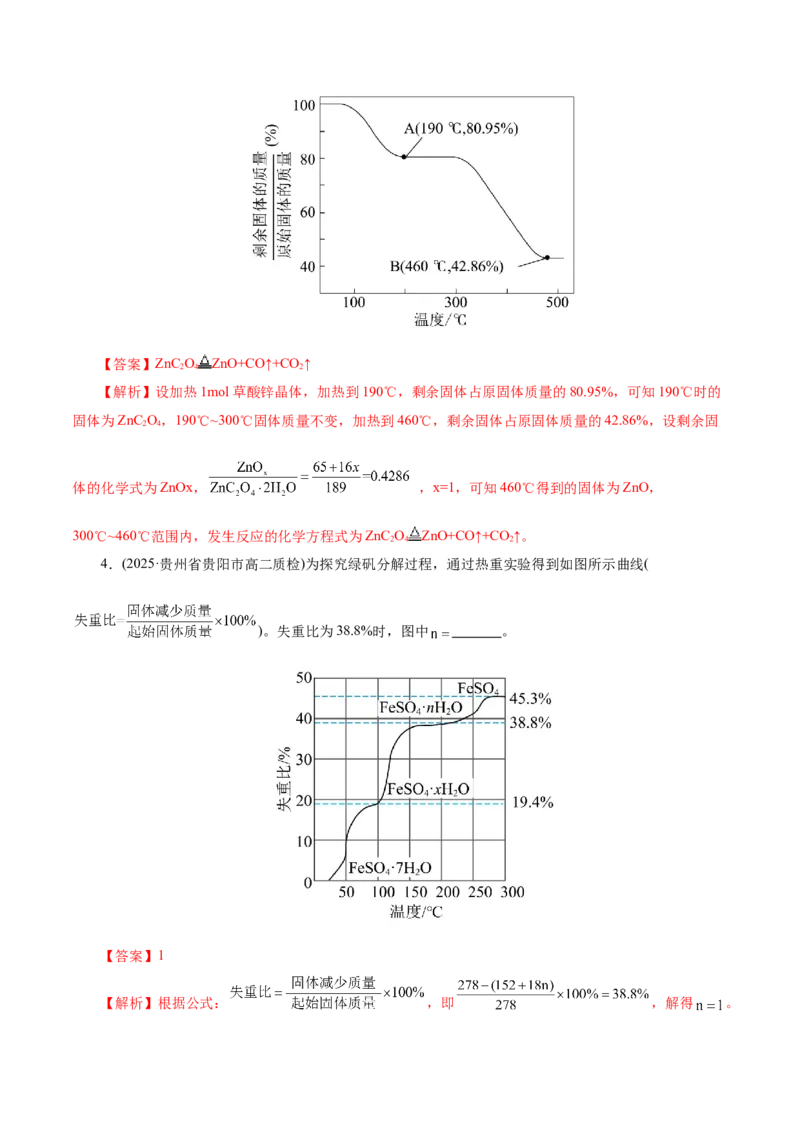
3.将草酸锌晶体(ZnC O·2H O)加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化
2 4 2
如下图所示,300℃~460℃范围内,发生反应的化学方程式为_______。【答案】ZnC O ZnO+CO↑+CO ↑
2 4 2
【解析】设加热1mol草酸锌晶体,加热到190℃,剩余固体占原固体质量的80.95%,可知190℃时的
固体为ZnC O,190℃~300℃固体质量不变,加热到460℃,剩余固体占原固体质量的42.86%,设剩余固
2 4
体的化学式为ZnOx, ,x=1,可知460℃得到的固体为ZnO,
300℃~460℃范围内,发生反应的化学方程式为ZnC O ZnO+CO↑+CO ↑。
2 4 2
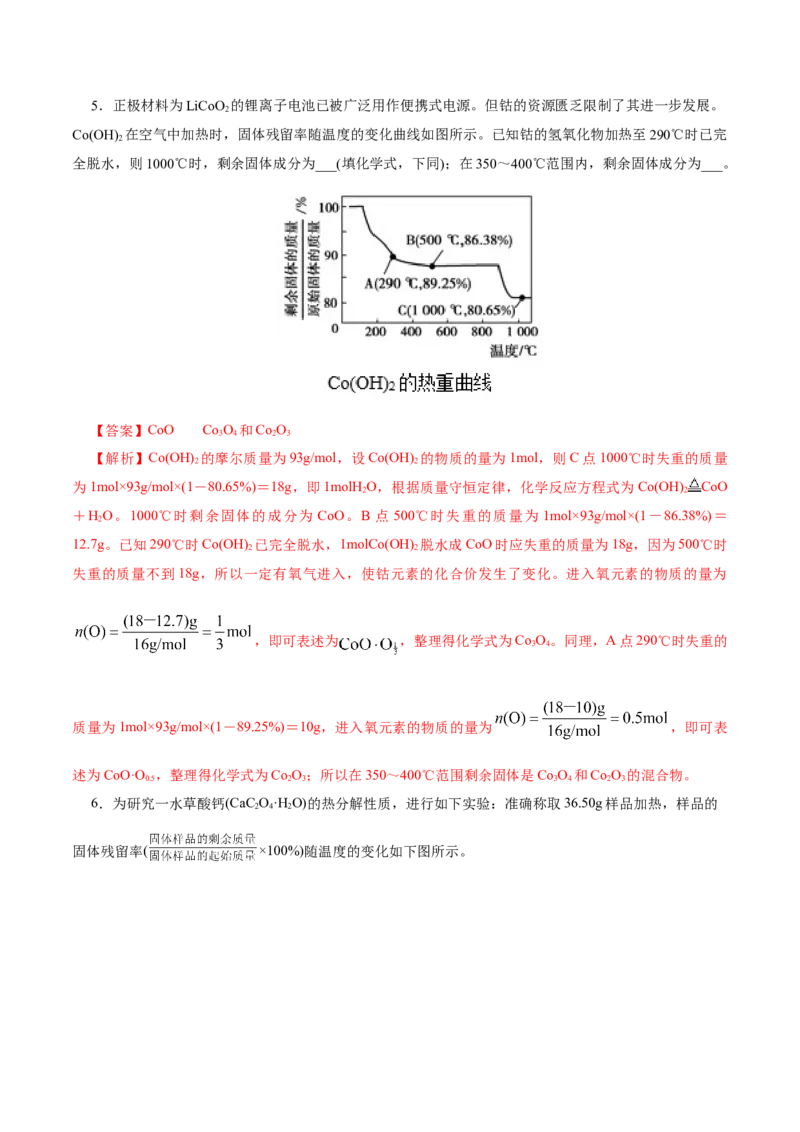
4.(2025·贵州省贵阳市高二质检)为探究绿矾分解过程,通过热重实验得到如图所示曲线(
)。失重比为38.8%时,图中 。
【答案】1
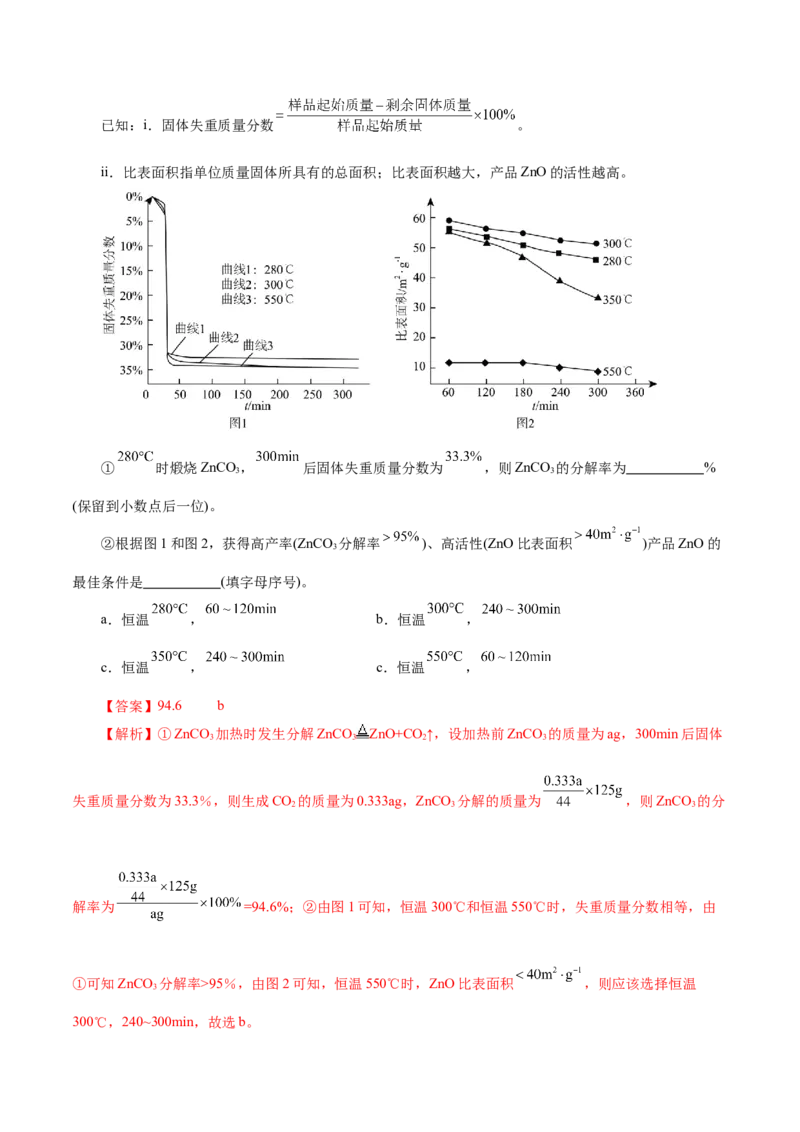
【解析】根据公式: ,即 ,解得 。5.正极材料为LiCoO 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
2
Co(OH) 在空气中加热时,固体残留率随温度的变化曲线如图所示。已知钴的氢氧化物加热至290℃时已完
2
全脱水,则1000℃时,剩余固体成分为___(填化学式,下同);在350~400℃范围内,剩余固体成分为___。
【答案】CoO Co O 和Co O
3 4 2 3
【解析】Co(OH) 的摩尔质量为93g/mol,设Co(OH) 的物质的量为1mol,则C点1000℃时失重的质量
2 2
为1mol×93g/mol×(1-80.65%)=18g,即1molH O,根据质量守恒定律,化学反应方程式为Co(OH) CoO
2 2
+HO。1000℃时剩余固体的成分为 CoO。B 点 500℃时失重的质量为 1mol×93g/mol×(1-86.38%)=
2
12.7g。已知290℃时Co(OH) 已完全脱水,1molCo(OH) 脱水成CoO时应失重的质量为18g,因为500℃时
2 2
失重的质量不到18g,所以一定有氧气进入,使钴元素的化合价发生了变化。进入氧元素的物质的量为
,即可表述为 ,整理得化学式为Co O。同理,A点290℃时失重的
3 4
质量为1mol×93g/mol×(1-89.25%)=10g,进入氧元素的物质的量为 ,即可表
述为CoO·O ,整理得化学式为Co O;所以在350~400℃范围剩余固体是Co O 和Co O 的混合物。
0.5 2 3 3 4 2 3
6.为研究一水草酸钙(CaC O·H O)的热分解性质,进行如下实验:准确称取36.50g样品加热,样品的
2 4 2
固体残留率( ×100%)随温度的变化如下图所示。(1)300 ℃时残留固体的成分为________,900 ℃时残留固体的成分为________。
(2)500℃时固体的成分及质量____________。
【答案】(1)CaC O CaO (2)固体的成分为12.8gCaC O 和15.0gCaCO
2 4 2 4 3
【解析】(1)n(CaC O·H O)= 0.25 mol,含有m(HO) =0.25 mol×18g/mol=4.50g,在300 ℃时,
2 4 2 2
×100%=87.67%,m(剩余)=36.50 g×87. 67%≈32 g,减少的质量为36.50 g-32 g=4.50g,故
此时失去全部的结晶水,残留固体为 CaC O ,在 900 ℃时, ×100%=38.36%,m(剩
2 4
余)=36.50 g×38.36%≈14 g,其中 Ca 的质量没有损失,含 m(Ca)=0.25 mol×40g/mol=10g,另外还含有
m(O)=14 g-10 g=4 g,n(O)=0.25 mol,则 n(Ca) : n(O)=1 : 1,化学式为 CaO;(2)在 600 °C 时,
×100%= 68.49%,m(剩余)=36.50 g×68. 49%≈25 g,从300 °C至600 C时,失去的总质量
为32 g-25 g=7 g,失去物质的摩尔质量为 ,则应为CO,所以CaC O 失去CO后,产
2 4
物为CaCO ,在500 °C时,应为CaC O 和CaCO 的混合物,样品中CaC O·H O物质的量为
3 2 4 3 2 4 2
=0.25mol,设 CaC O 和 CaCO 的物质的量分别为 xmol 和 ymol,根据 500 °C 时固体总质量可得
2 4 3
128x+100y=36.5×76. 16%,根据钙元素守恒可得x+y=0.25,解得x=0.1,y=0.15,m(CaC O)= 0.1 mol×128g/
2 4
mol=12.8g,m(CaCO )= 0.15 mol×100g/ mol=15g,500 °C时固体的成分为12.8gCaC O 和15.0gCaCO 。
3 2 4 3
7.(2025·北京师大附中开学考试)工业上利用锌焙砂(主要成分为ZnO,含有少量CuO、AsO、NiO
2 3
等)生产高纯ZnO。“煅烧”步骤中,不同温度下,ZnCO 分解的失重曲线和产品ZnO的比表面积变化情
3
况如图1、图2所示。已知:i.固体失重质量分数 。
ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品ZnO的活性越高。
① 时煅烧ZnCO , 后固体失重质量分数为 ,则ZnCO 的分解率为 %
3 3
(保留到小数点后一位)。
②根据图1和图2,获得高产率(ZnCO 分解率 )、高活性(ZnO比表面积 )产品ZnO的
3
最佳条件是 (填字母序号)。
a.恒温 , b.恒温 ,
c.恒温 , c.恒温 ,
【答案】94.6 b
【解析】①ZnCO 加热时发生分解ZnCO ZnO+CO ↑,设加热前ZnCO 的质量为ag,300min后固体
3 3 2 3
失重质量分数为33.3%,则生成CO 的质量为0.333ag,ZnCO 分解的质量为 ,则ZnCO 的分
2 3 3
解率为 =94.6%;②由图1可知,恒温300℃和恒温550℃时,失重质量分数相等,由
①可知ZnCO 分解率>95%,由图2可知,恒温550℃时,ZnO比表面积 ,则应该选择恒温
3
300℃,240~300min,故选b。