文档内容
热点强化练1 离子反应在生产、生活中的应用
1.(2020·宁夏大学附属中学高三月考)下列离子方程式不正确的是( )
A.热的纯碱溶液清洗油污:CO+H OHCO+OH-
2
B.用铜电极电解硫酸铜溶液:2Cu2++2H O=====2Cu↓+O ↑+4H+
2 2
C.用FeCl 饱和溶液制备Fe(OH) 胶体:Fe3++3H O(沸水)=====Fe(OH) (胶
3 3 2 3
体)+3H+
D.泡沫灭火器的灭火原理:Al3++3HCO===Al(OH) ↓+3CO ↑
3 2
答案 B
解析 热的纯碱溶液清洗油污,是因为碳酸根水解产生OH-,水解的离子方
程式为CO+H OHCO+OH-,A正确;用Cu电极电解硫酸铜溶液,阳极为Cu
2
失电子生成 Cu2+,阴极为 Cu2+得电子生成 Cu,故总反应不可能为 2Cu2++
2H O=====2Cu↓+O ↑+4H+,B错误;将FeCl 饱和溶液滴入沸水中,加热至液
2 2 3
体呈红褐色即制得 Fe(OH) 胶体,反应的离子方程式为 Fe3++3H O(沸
3 2
水)=====Fe(OH) (胶体)+3H+,C正确;泡沫灭火器原理是可溶性铝盐和碳酸氢
3
盐发生相互促进水解反应,反应的离子方程式为 Al3++3HCO===Al(OH) ↓+
3
3CO ↑,D正确。
2
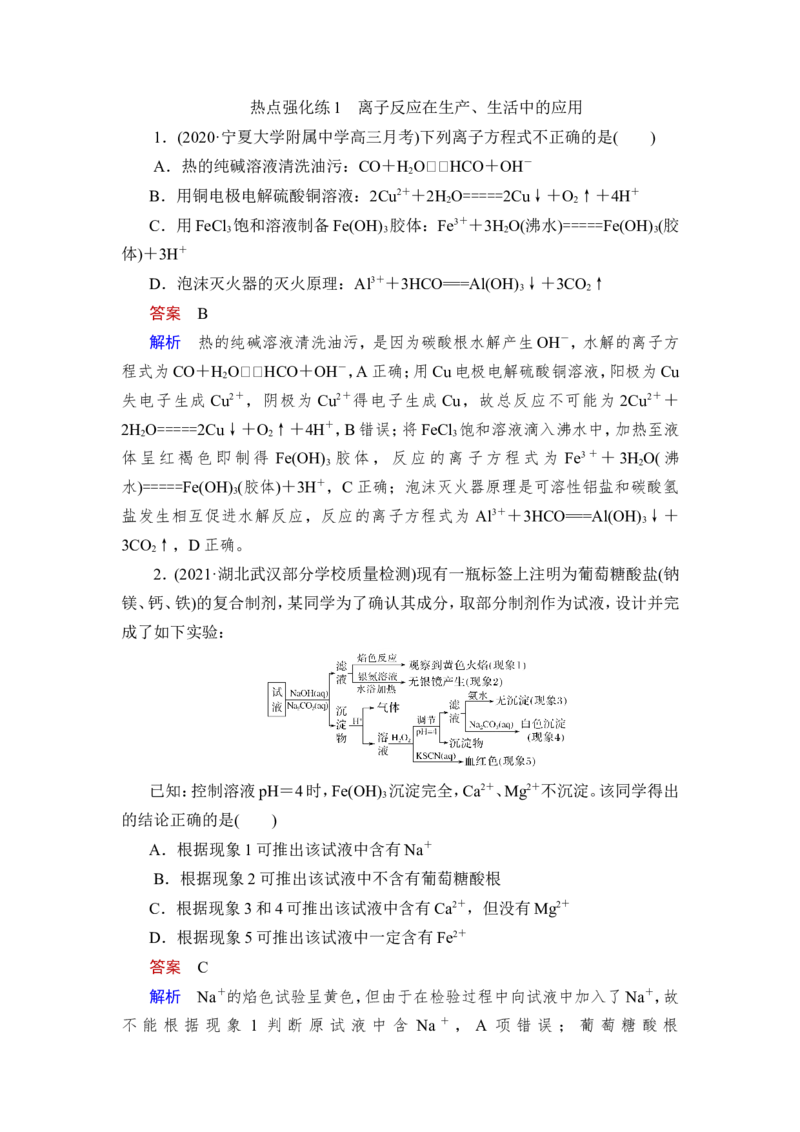
2.(2021·湖北武汉部分学校质量检测)现有一瓶标签上注明为葡萄糖酸盐(钠
镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完
成了如下实验:
已知:控制溶液pH=4时,Fe(OH) 沉淀完全,Ca2+、Mg2+不沉淀。该同学得出
3
的结论正确的是( )
A.根据现象1可推出该试液中含有Na+
B.根据现象2可推出该试液中不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+
答案 C
解析 Na+的焰色试验呈黄色,但由于在检验过程中向试液中加入了Na+,故
不 能 根 据 现 象 1 判 断 原 试 液 中 含 Na + , A 项 错 误 ; 葡 萄 糖 酸 根[CH OH(CHOH) COO-]中不含有醛基,不能发生银镜反应,因此不能通过银镜反
2 4
应来判断葡萄糖酸根是否存在,B项错误;调节pH=4时Fe3+全部沉淀,此时滤
液中可能存在的金属离子只有Ca2+和Mg2+,根据加入氨水后无沉淀生成可知滤
液中无Mg2+,根据加入Na CO 溶液后产生沉淀,可知存在Ca2+,C项正确;若原
2 3
试液中只含有Fe3+,通过图示操作,也可出现现象5,即原试液中不一定含有Fe2
+,D项错误。
3.某化工企业排放的废水中可能存在大量下表所列离子。取该废水样品100
mL,往废水样品中逐滴加入1 mol·L-1 NaOH溶液,生成沉淀的物质的量(n)与加
入NaOH溶液的体积(V)的关系如图所示。则下列说法正确的是( )
阳离子 H+、K+、Mg2+、Al3+、NH、Fe2+、Fe3+
阴离子 Cl-、Br-、I-、CO、AlO
A.该废水样品中一定不含的阴离子是CO、AlO,肯定含有Cl-、Br-、I-中的
一种
B.该废水样品中一定含有的阳离子是Al3+、H+、NH、Mg2+、Fe2+、Fe3+,可能
含有K+
C.该废水样品中n(H+)∶n(NH)∶n(Al3+)=V ∶(V -V )∶(V -V )
1 3 2 2 1
D.若V =10、V =40、V =70,则废水样品中 n(H+)∶n(NH)∶n(Al3+)=
1 2 4
1∶3∶1
答案 A
解析 向废水样品中不断加入NaOH溶液的过程中,开始时无沉淀产生,然
后沉淀逐渐增多,BC段沉淀量不变,最后沉淀全部溶解,说明溶液中存在H+、
NH、Al3+,肯定不存在CO、AlO、Fe2+、Fe3+、Mg2+,根据溶液呈电中性原则知,废
水中至少含有 Cl-、Br-、I-中的一种。根据图中沉淀变化曲线知,n(H
+)∶n(NH)∶n(Al3+)=V ∶(V -V )∶[(V -V )],若V =10,V =40,V =70,则有
1 3 2 2 1 1 2 4
n(H+)∶n(NH)∶n(Al3+)=1∶2∶1。
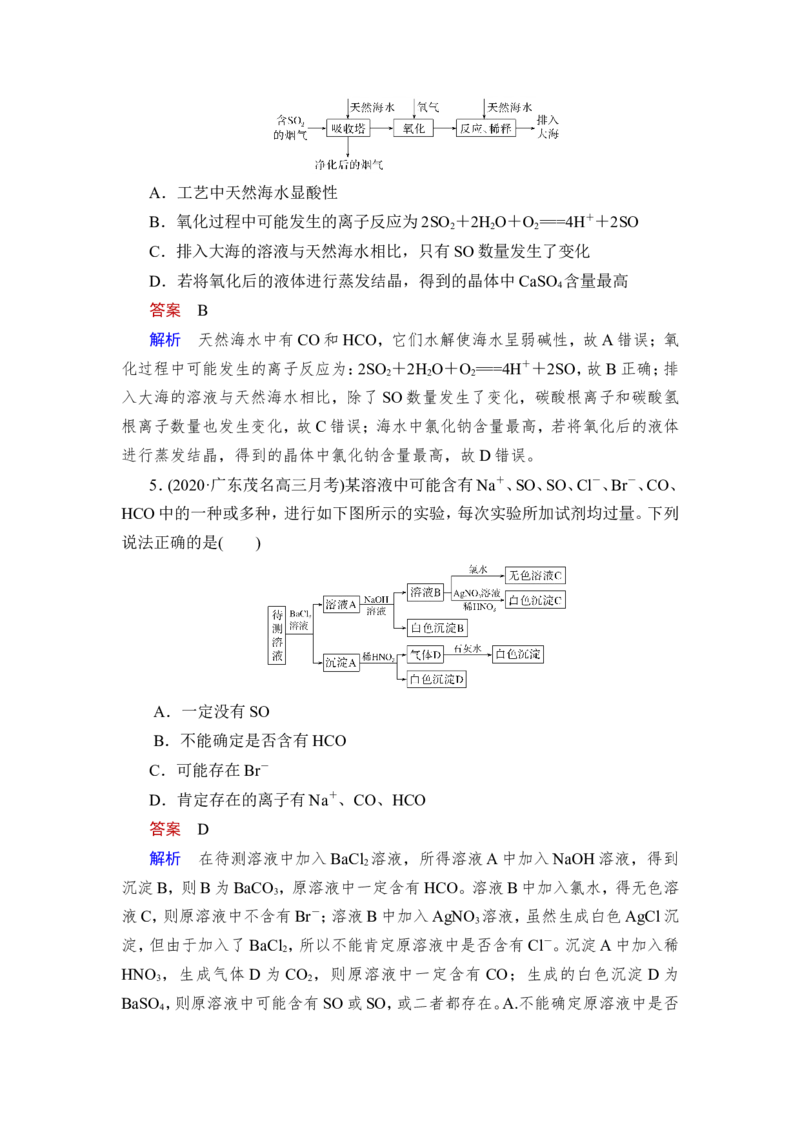
4.(2020·天津和平高三二模)海水的综合利用一直是研究课题。某地天然海水
(主要含Na+、K+、Ca2+、Mg2+、Cl-、SO、Br-、CO、HCO等离子),研究用海水吸收
燃煤排放的含有SO 烟气的工艺流程如图所示,下列说法中正确的是( )
2A.工艺中天然海水显酸性
B.氧化过程中可能发生的离子反应为2SO +2H O+O ===4H++2SO
2 2 2
C.排入大海的溶液与天然海水相比,只有SO数量发生了变化
D.若将氧化后的液体进行蒸发结晶,得到的晶体中CaSO 含量最高
4
答案 B
解析 天然海水中有CO和HCO,它们水解使海水呈弱碱性,故A错误;氧
化过程中可能发生的离子反应为:2SO +2H O+O ===4H++2SO,故B正确;排
2 2 2
入大海的溶液与天然海水相比,除了SO数量发生了变化,碳酸根离子和碳酸氢
根离子数量也发生变化,故C错误;海水中氯化钠含量最高,若将氧化后的液体
进行蒸发结晶,得到的晶体中氯化钠含量最高,故D错误。
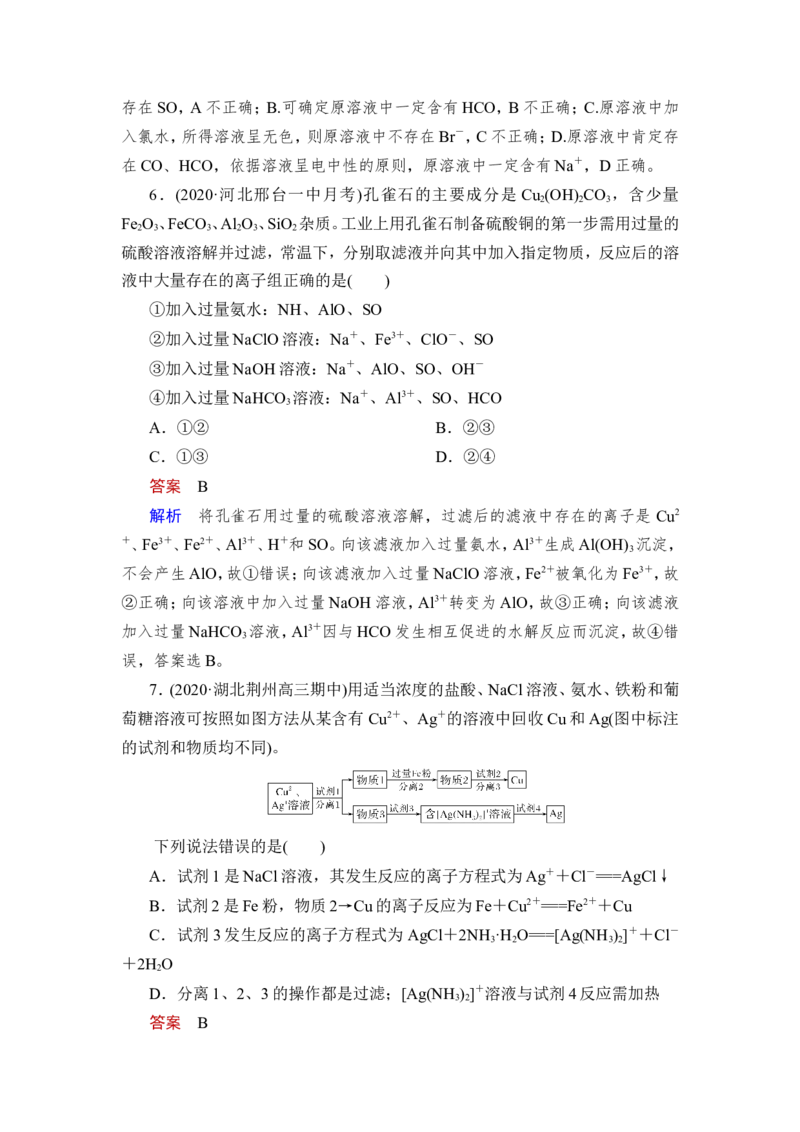
5.(2020·广东茂名高三月考)某溶液中可能含有Na+、SO、SO、Cl-、Br-、CO、
HCO中的一种或多种,进行如下图所示的实验,每次实验所加试剂均过量。下列
说法正确的是( )
A.一定没有SO
B.不能确定是否含有HCO
C.可能存在Br-
D.肯定存在的离子有Na+、CO、HCO
答案 D
解析 在待测溶液中加入BaCl 溶液,所得溶液A中加入NaOH溶液,得到
2
沉淀B,则B为BaCO ,原溶液中一定含有HCO。溶液B中加入氯水,得无色溶
3
液C,则原溶液中不含有Br-;溶液B中加入AgNO 溶液,虽然生成白色AgCl沉
3
淀,但由于加入了BaCl ,所以不能肯定原溶液中是否含有Cl-。沉淀A中加入稀
2
HNO ,生成气体 D为CO ,则原溶液中一定含有 CO;生成的白色沉淀 D为
3 2
BaSO ,则原溶液中可能含有SO或SO,或二者都存在。A.不能确定原溶液中是否
4存在SO,A不正确;B.可确定原溶液中一定含有HCO,B不正确;C.原溶液中加
入氯水,所得溶液呈无色,则原溶液中不存在Br-,C不正确;D.原溶液中肯定存
在CO、HCO,依据溶液呈电中性的原则,原溶液中一定含有Na+,D正确。
6.(2020·河北邢台一中月考)孔雀石的主要成分是 Cu (OH) CO ,含少量
2 2 3
Fe O 、FeCO 、Al O 、SiO 杂质。工业上用孔雀石制备硫酸铜的第一步需用过量的
2 3 3 2 3 2
硫酸溶液溶解并过滤,常温下,分别取滤液并向其中加入指定物质,反应后的溶
液中大量存在的离子组正确的是( )
①加入过量氨水:NH、AlO、SO
②加入过量NaClO溶液:Na+、Fe3+、ClO-、SO
③加入过量NaOH溶液:Na+、AlO、SO、OH-
④加入过量NaHCO 溶液:Na+、Al3+、SO、HCO
3
A.①② B.②③
C.①③ D.②④
答案 B
解析 将孔雀石用过量的硫酸溶液溶解,过滤后的滤液中存在的离子是 Cu2
+、Fe3+、Fe2+、Al3+、H+和SO。向该滤液加入过量氨水,Al3+生成Al(OH) 沉淀,
3
不会产生AlO,故①错误;向该滤液加入过量NaClO溶液,Fe2+被氧化为Fe3+,故
②正确;向该溶液中加入过量NaOH溶液,Al3+转变为AlO,故③正确;向该滤液
加入过量NaHCO 溶液,Al3+因与HCO发生相互促进的水解反应而沉淀,故④错
3
误,答案选B。
7.(2020·湖北荆州高三期中)用适当浓度的盐酸、NaCl溶液、氨水、铁粉和葡
萄糖溶液可按照如图方法从某含有 Cu2+、Ag+的溶液中回收Cu和Ag(图中标注
的试剂和物质均不同)。
下列说法错误的是( )
A.试剂1是NaCl溶液,其发生反应的离子方程式为Ag++Cl-===AgCl↓
B.试剂2是Fe粉,物质2→Cu的离子反应为Fe+Cu2+===Fe2++Cu
C.试剂3发生反应的离子方程式为 AgCl+2NH ·H O===[Ag(NH ) ]++Cl-
3 2 3 2
+2H O
2
D.分离1、2、3的操作都是过滤;[Ag(NH ) ]+溶液与试剂4反应需加热
3 2
答案 B解析 在含有Cu2+、Ag+的混合溶液中,加入试剂1,得到物质1和物质3,向
物质1中加入过量Fe粉,经一系列反应产生Cu单质,则物质1中含有Cu2+,加
入的试剂1将原混合物中的Ag+转化为沉淀,该试剂中含有Cl-,为NaCl溶液,
物质3是AgCl。向含有Cu2+的溶液中加入过量Fe粉,发生反应:Fe+Cu2+===Fe2
++Cu,过滤分离得到物质2中含Cu及过量的Fe,再向物质2中加入稀盐酸,Fe
与盐酸发生置换反应变为FeCl 进入溶液,Cu不与盐酸反应,通过过滤、洗涤可
2
分离得到Cu单质,则试剂2是盐酸。物质3是AgCl,向其中加入氨水得到银氨溶
液,试剂3为氨水,向银氨溶液中加入葡萄糖溶液,水浴加热,发生银镜反应,得
到Ag单质。根据上述分析可知:试剂1为NaCl溶液,试剂2是盐酸,试剂3是氨
水,试剂4是葡萄糖溶液,物质1是CuCl ,物质2是Fe、Cu混合物,物质3是
2
AgCl。试剂1是NaCl溶液,Cl-与Ag+反应产生AgCl沉淀,该反应的离子方程式
为:Ag++Cl-===AgCl↓,A正确;试剂2是盐酸,物质2是Fe、Cu混合物,物质
2→Cu的离子反应为Fe+2H+===Fe2++H ↑,B错误;试剂3是氨水,与AgCl发
2
生反应产生银氨溶液,反应的离子方程式为 AgCl+2NH ·H O===[Ag(NH ) ]++
3 2 3 2
Cl-+2H O,C正确;分离1、2、3都是分离难溶性固体与可溶性液体混合物的操
2
作,操作名称都是过滤;试剂4是葡萄糖溶液,葡萄糖与银氨溶液水浴加热发生
银镜反应产生Ag单质,D正确。
8.为了充分利用铜资源,某工厂利用废旧黄铜灰(含有Cu、Zn、CuO、ZnO及
少量的FeO、Fe O 、SiO 等)制取金属铜并得到副产物锌盐,其生产流程如下:
2 3 2
(1)滤渣1的主要成分为________。稀硫酸溶解黄铜灰的过程中,Cu是否参与
了反应?如果参与了,请写出该反应的离子方程式;如果没有参与反应,请写出
理由:____________________________________________________。
(2)滤渣1及滤渣2与浓硫酸反应的步骤中存在缺陷,可将实验改进为先让滤
渣 与 ________ 反 应 , 产 物 再 溶 于 稀 硫 酸 。 这 样 改 进 的 优 点 是
___________________________________________________________________。
(3)写出滤液3与H O 反应的离子方程式:___________________________。
2 2
答案 (1)Cu和SiO Cu+2Fe3+===2Fe2++Cu2+
2
(2)O 避免产生有毒气体SO 污染环境,同时减少了硫酸的用量(其他合理
2 2
答案均可)(3)2Fe2++H O +2H+===2Fe3++2H O
2 2 2
解析 (1)黄铜灰中不与稀硫酸反应的物质是Cu和SiO ,所以加入稀硫酸过
2
滤后的滤渣1的主要成分是单质Cu和SiO 。黄铜灰中有氧化铁,与稀硫酸反应
2
得到Fe3+,单质铜可以与其反应,离子方程式为Cu+2Fe3+===2Fe2++Cu2+(因为
氧化铁少量,所以最后一定剩余单质铜,滤渣1中应该有单质铜)。
(2)滤渣2主要含单质铜和铁,滤渣1主要含单质铜和二氧化硅,加入浓硫酸
发生反应,将单质铁和铜转化为盐溶液,滤渣3为二氧化硅。此步反应中最大的
问题是生成了污染性气体二氧化硫,所以应该先通入氧气氧化,将金属单质氧化
为金属氧化物,再与稀硫酸反应。同时这样操作可以减少硫酸的用量(因为用浓硫
酸时,一部分硫酸转化为二氧化硫,而使用稀硫酸时,所有的硫酸都转化为硫酸
盐)。
(3)在滤液3中加入稀硫酸和过氧化氢的目的是将Fe2+氧化为Fe3+,所以该反
应的离子方程式为2Fe2++H O +2H+===2Fe3++2H O。
2 2 2
9.(2020·山西运城高三月考)某中学化学兴趣小组为了调查当地某湖泊的水
质污染情况, 在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给
出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,
一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
阳离子 K+、Na+、Cu2+、Al3+
阴离子 SO、HCO、NO、OH-
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色试验,只有B、 C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中
都能产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C的化学式:________。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,
请写出A与E反应的离子方程式:_____________________________________。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________________。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理:_______________________________________________________________。
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH) 溶液,生成沉淀质量最
2
大为________g。
(6)若向一定量溶质C中加入适量氢氧化钠至恰好完全沉淀。过滤,并对沉淀
进行洗涤,请写出检验沉淀是否洗涤干净的具体操作过程:
______________________________________________________________。
答案 (1)KAl(SO ) 或KAl(SO ) ·12H O
4 2 4 2 2
(2)HCO+OH-===CO+H O
2
(3)2HCO+Ca2++2OH-===CaCO ↓+CO+2H O
3 2
(4)Al3++3H O===Al(OH) (胶体)+3H+,氢氧化铝胶体能吸附水中的悬浮物
2 3
从而达到净水目的
(5)233 (6)取最后一次洗涤液,向其中加入适量的氯化钡溶液(先加盐酸,再
加氯化钡也正确),若无沉淀,则证明沉淀洗涤干净
解析 ①将它们溶于水后,D为蓝色溶液,其他均为无色溶液,则D中含有
Cu2+;②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解,则C中含
有Al3+,E中含有OH-;③进行焰色试验实验,只有B、C为紫色(透过蓝色钴玻
璃),则B、C中含有K+,所以E是NaOH;④在各溶液中加入Ba(NO ) 溶液,再加
3 2
入过量稀硝酸,A中放出无色气体,则A中含有HCO,所以A是NaHCO ,C、D
3
中产生白色沉淀,则 C、D 中含有 SO,所以 D 是 CuSO ,C 是 KAl(SO ) 或
4 4 2
KAl(SO ) ·12H O;⑤将B、D两溶液混合,未见沉淀或气体生成,则B是KNO 。
4 2 2 3
(4)KAl(SO ) 中铝离子为弱碱阳离子,容易水解生成氢氧化铝胶体,氢氧化铝胶
4 2
体具有吸附悬浮杂质的能力,故离子反应方程式为:Al3++3H O===Al(OH) (胶
2 3
体)+3H+;(5)若向含0.5 mol KAl(SO ) 的溶液中逐滴加入Ba(OH) 溶液,生成沉
4 2 2
淀质量最大时为硫酸根与钡离子恰好完全反应,即生成硫酸钡为1 mol,质量为:
1 mol×233 g/mol=233 g;(6)若向一定量溶质KAl(SO ) 中加入适量氢氧化钠至
4 2
恰好完全沉淀,过滤,沉淀表面可能吸附有硫酸根离子,检验沉淀是否洗涤干净
的具体操作过程为:取最后一次洗涤液,向其中加入适量的氯化钡溶液(先加盐酸
再加氯化钡也正确),若无沉淀,则证明沉淀洗涤干净。
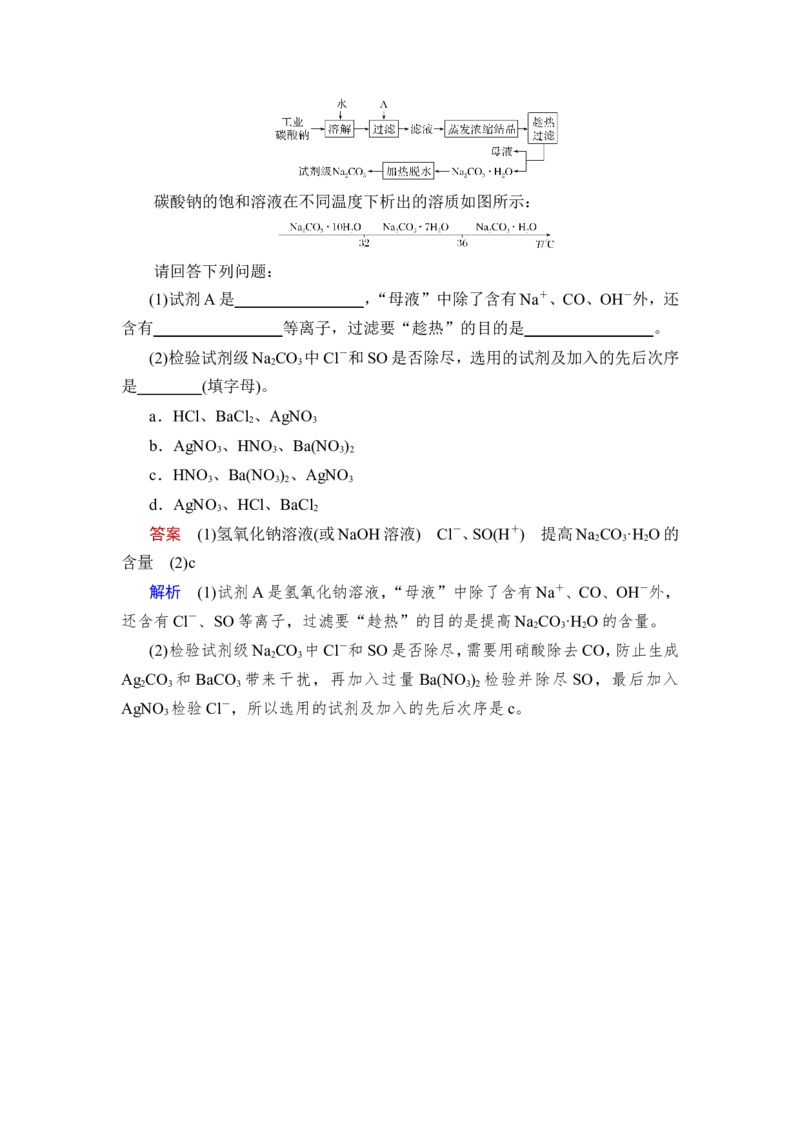
10.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸
钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO等杂质、提纯工艺线路如下:碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
请回答下列问题:
(1)试剂A是________________,“母液”中除了含有Na+、CO、OH-外,还
含有________________等离子,过滤要“趁热”的目的是________________。
(2)检验试剂级Na CO 中Cl-和SO是否除尽,选用的试剂及加入的先后次序
2 3
是________(填字母)。
a.HCl、BaCl 、AgNO
2 3
b.AgNO 、HNO 、Ba(NO )
3 3 3 2
c.HNO 、Ba(NO ) 、AgNO
3 3 2 3
d.AgNO 、HCl、BaCl
3 2
答案 (1)氢氧化钠溶液(或NaOH溶液) Cl-、SO(H+) 提高Na CO ·H O的
2 3 2
含量 (2)c
解析 (1)试剂A是氢氧化钠溶液,“母液”中除了含有Na+、CO、OH-外,
还含有Cl-、SO等离子,过滤要“趁热”的目的是提高Na CO ·H O的含量。
2 3 2
(2)检验试剂级Na CO 中Cl-和SO是否除尽,需要用硝酸除去CO,防止生成
2 3
Ag CO 和 BaCO 带来干扰,再加入过量 Ba(NO ) 检验并除尽 SO,最后加入
2 3 3 3 2
AgNO 检验Cl-,所以选用的试剂及加入的先后次序是c。
3