文档内容
知识清单 03 氧化还原反应
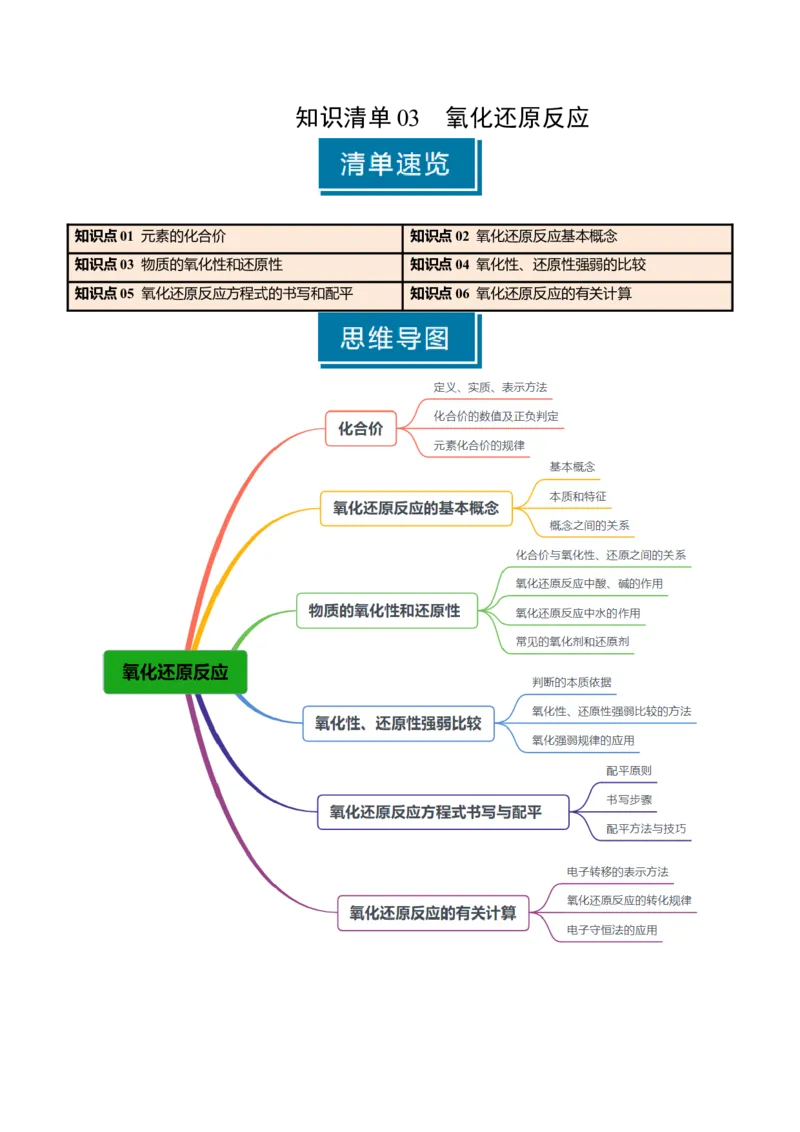
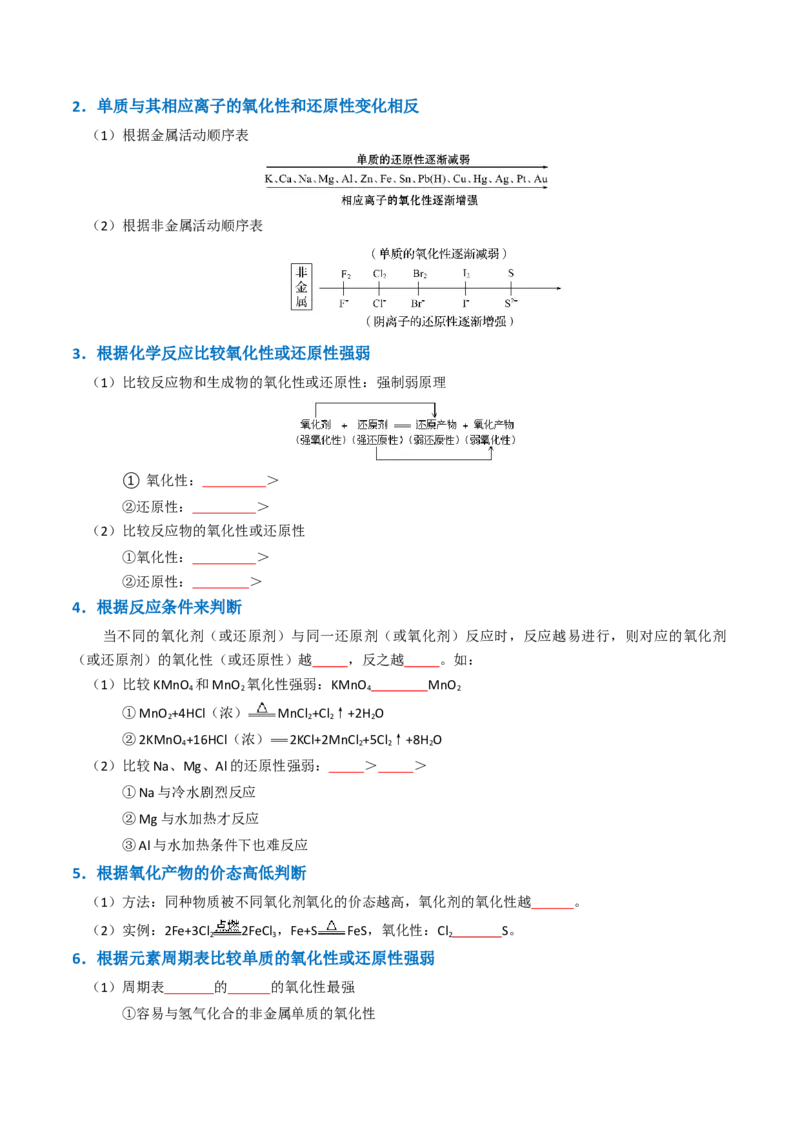
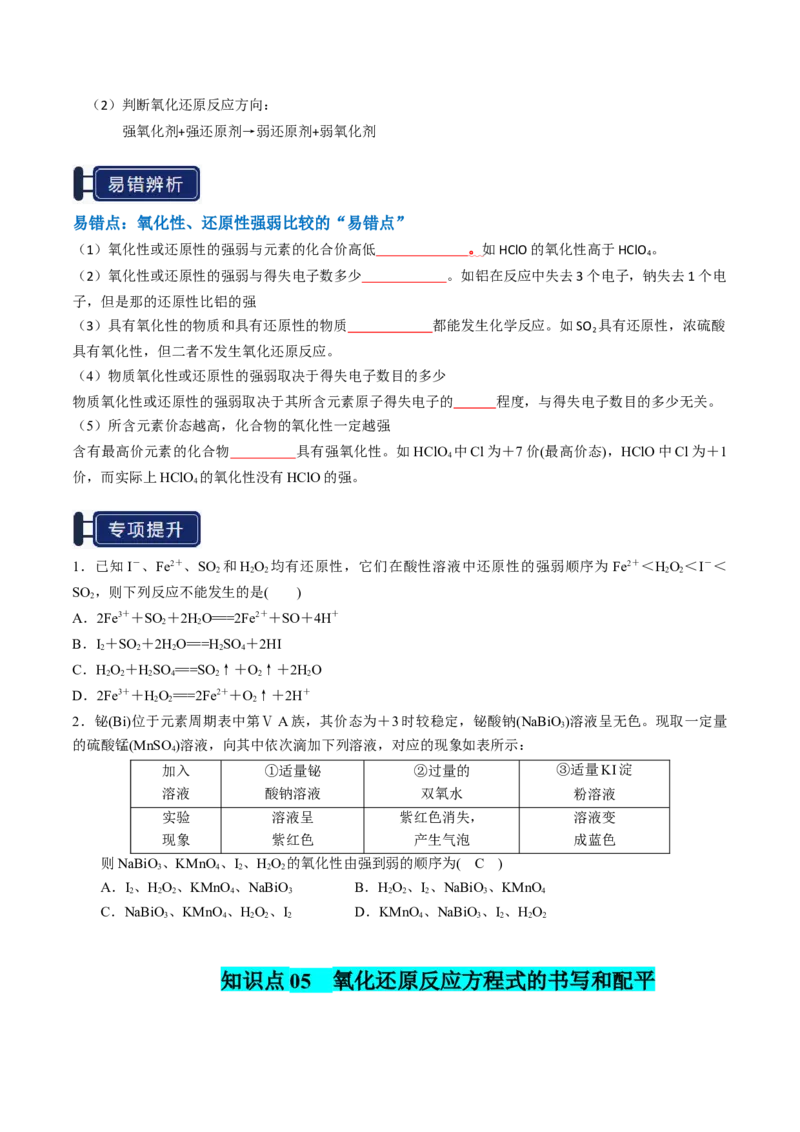
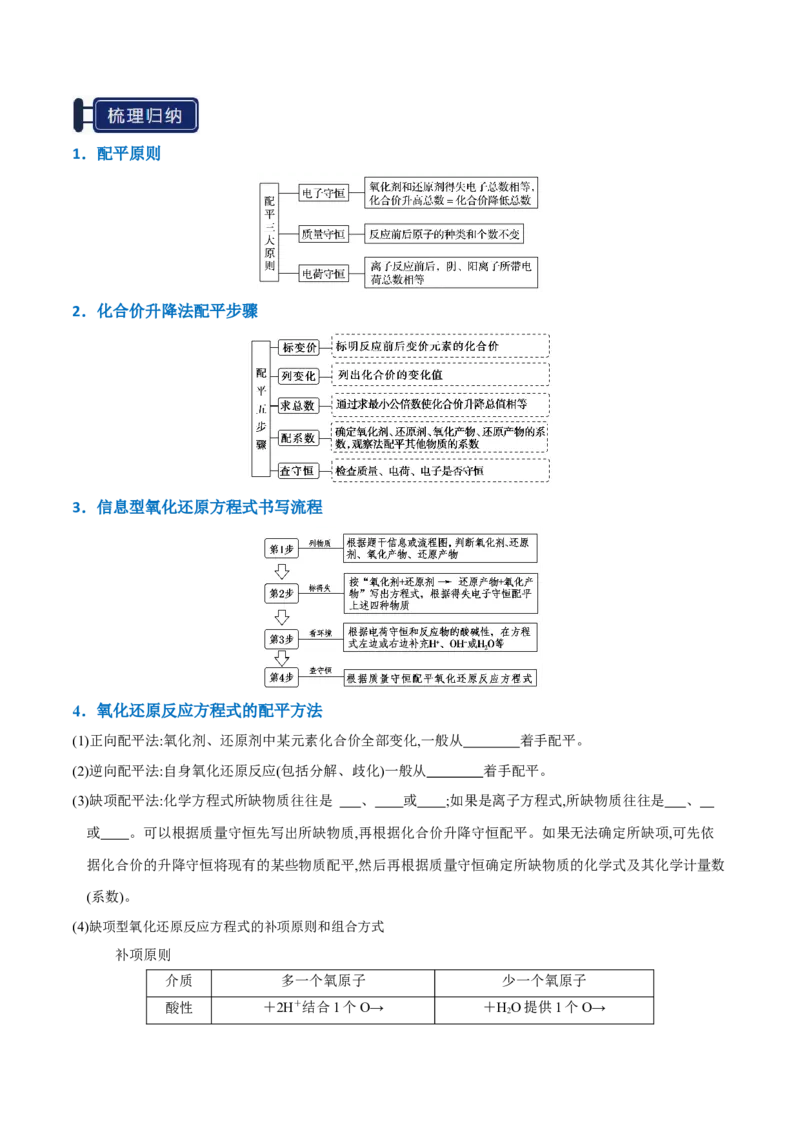
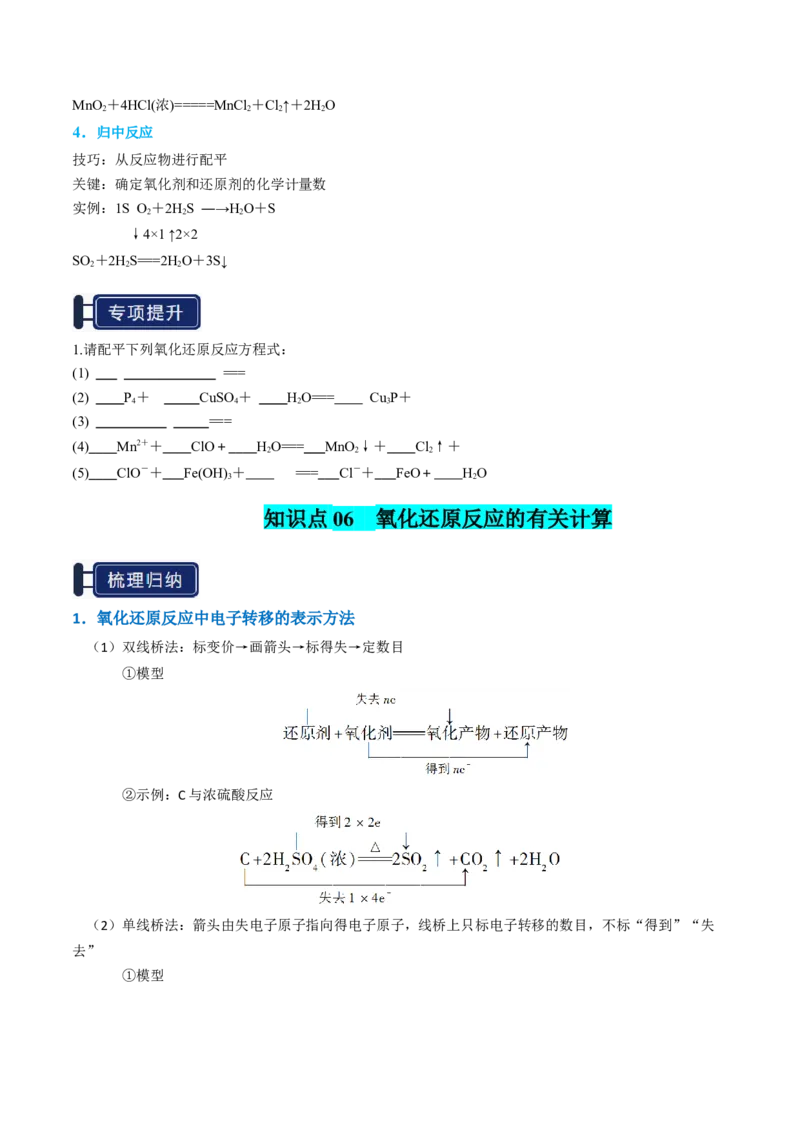
知识点01 元素的化合价 知识点02 氧化还原反应基本概念
知识点03 物质的氧化性和还原性 知识点04 氧化性、还原性强弱的比较
知识点05 氧化还原反应方程式的书写和配平 知识点06 氧化还原反应的有关计算知识点 01 元素的化合价
1.化合价的定义、实质和表示方法:
(1)定义:一种元素一定数目的原子跟其他元素一定数目的原子化合的性质。
(2)实质:化合价是元素在形成化合物时表现出的化学性质;单质的化合价为零。
(3)表示方法:在元素符号或原子团的 用+n或-n表示
① 位置:元素符号的 (如 ); ② 书写顺序:先写 ,后写 ;
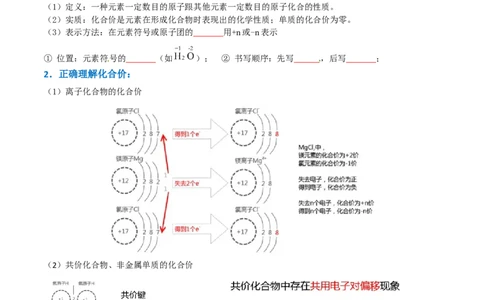
2.正确理解化合价:
(1)离子化合物的化合价
(2)共价化合物、非金属单质的化合价
3.化合价的数值及正负判定4.元素化合价的规律
(1)化合价原则:
①化合物中,正负化合价的代数和=
②离子中,正负化合价的代数和=
③在化合物里,氢通常显+1价,氧通常显-2价;
④金属元素通常显 价,非金属元素通常显 价,但在非金属氧化物里,氧显负价,
另一非金属元素显正价;
⑤单质中元素的化合价规定为 ;
⑥许多元素具有可变化合价,如:硫、碳等;
⑦“根”的化合价一定不为 。
(2)常用等量关系
①主族元素最高正价= =
②主族元素的最高正价+|最低负价|= 或
③最高正化合价与其最低负化合价代数和
a.等于0的短周期元素: 、 、 b.等于2的短周期元素: 、
c.等于4的短周期元素: d.等于6的短周期元素:
(3)化合价的范围: ≤最高价≤ , ≤最低价≤
5.化合价的特殊点
(1) 元素没有正化合价, 元素没有负化合价
(2) 元素有正化合价,但是没有其所在族的最高正化合价
(3)硼元素只有 价
(4)氢元素的化合价
①金属氢化物中,氢显 价,如NaH、NaAlH 、
4
②非金属氢化物中,氢一般显 价,如NH 、CH 、B H
3 4 2 6
(5)氧元素的化合价
①普通的含氧微粒中,氧显 价
②含O 2―或―O―O―的微粒中,氧显 价
2
③在S O 2―( )中,过氧键中的两个O显 ,其余的O显 价。
2 8④在CrO 中,两个过氧键中的4个O显 ,其余的O显 价。
5
6.简单阴离子或气态氢化物中,非金属元素显
易错点:某些微粒中元素的化合价
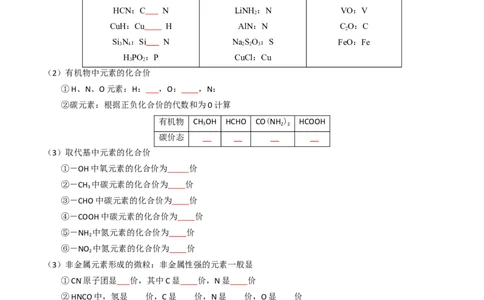
(1)近几年高考中一些特殊物质中元素化合价判断
CuFeS:Cu Fe KFeO:Fe LiNH:N
2 2 4 2
HCN:C N LiNH:N VO:V
2
CuH:Cu H AlN:N C O:C
2
Si N:Si N NaSO:S FeO:Fe
3 4 2 2 3
HPO :P CuCl:Cu
3 2
(2)有机物中元素的化合价
①H、N、O元素:H: ,O: ,N:
②碳元素:根据正负化合价的代数和为0计算
有机物 CH OH HCHO CO(NH ) HCOOH
3 2 2
碳价态
(3)取代基中元素的化合价
①-OH中氧元素的化合价为 价
②-CH 中碳元素的化合价为 价
3
③-CHO中碳元素的化合价为 价
④-COOH中碳元素的化合价为 价
⑤-NH 中氮元素的化合价为 价
2
⑥-NO 中氮元素的化合价为 价
2
(3)非金属元素形成的微粒:非金属性强的元素一般显
①CN-原子团显 价,其中C显 价,N显 价
②HNCO中,氢显 价,C显 价,N显 价,O显 价
③HFO中,H显 价,F显 价,O显 价
④BrI中I元素显 价,SiC中C元素显 价
(4)含CO、NH 、H O等分子的物质:
3 2
①Fe(CO) 中Fe显 价
5
②Cu(NH ) SO 中Cu显 价
3 4 4
(5)某些含铁、铜的硫化物物
FeS CuFeS
2 2
质
价 S Fe Cu Fe S
态
(6)无法判断价态的物质
物质 AlFe Fe P Fe C
2 3 3
Al Fe Fe P Fe C
价态
1.已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl ②Q+HO――→X+H ③Y+NaOH―→G+Q+HO ④Z+NaOH―→Q+X
2 2 2
+HO
2
这五种化合物中Cl元素化合价由低到高的顺序是( A )
A.G、Y、Q、Z、X B.X、Z、Q、G、Y
C.X、Z、Q、Y、G D.G、Q、Y、Z、X
【解析】 由①得出Q中价态高于G,因为G中价态介于Q和-1价的Cl之间,-1价为氯元素的最
低价;将该结论引用到③,Y介于Q与G之间,故有Q价态高于Y,Y价态高于G;分析②:HO中的H
2
化合价降低,则Q中的氯元素转变为X中的氯元素,化合价必升高,则得出X价态高于Q;最后分析④:
Z介于Q、X之间,则X价态高于Z,Z价态高于Q。
2.已知X、Y、Z、W、Q均为含氮化合物,它们在一定条件下有如下转换关系(未配平):
①X―→W+O
2
②Z+Y+NaOH―→HO+W
2
③Y+SO ―→Z+SO
2 3
④Q+Y―→Z+HO
2
⑤X+Cu+HSO (浓)―→Cu2++Y+SO
2 4
则这五种含氮化合物中氮元素的化合价由高到低的顺序为( C )
A.X>Y>Z>W>Q B.X>Z>Y>Q>W
C.X>Y>W>Z>Q D.W>X>Z>Q>Y
【解析】 ①X―→W+O 中,X中氧元素失电子化合价升高,则氮元素得电子化合价降低,所以氮
2
元素化合价X>W;③Y+SO ―→Z+SO 中,硫元素化合价升高,则Y中氮元素化合价Y>Z;②Z+Y+
2 3
NaOH―→HO+W为归中反应,则氮元素化合价W处于Z和Y中间,结合反应③可知,氮元素化合价
2
Y>W>Z;④Q+Y―→Z+HO为归中反应,Z处于Q和Y之间,根据③知,Y>Z,所以Z>Q;⑤X+Cu
2
+HSO (浓)―→Cu2++Y+SO,铜元素化合价升高,则X化合价降低生成Y,所以氮元素化合价,X>Y;
2 4
所以这五种含氮化合物中氮元素的化合价由高到低的顺序为X>Y>W>Z>Q。
知识点 02 氧化还原反应的概念1.氧化还原反应
反应前后元素的化合价
特征 氧化还原反应 反应前后元素的化合价
非氧化还原反应 反应前后元素的化合价
氧
化 本质 反应过程中有电子的 ,包括电子的
还
原 反应一定是氧化还原反应
反 和四种基本 反应一定不是氧化还原反应
应
反应类型的 有 参加的化合反应是氧化还原反应;
有 生成的分解反应是氧化还原反应
关系
2.氧化还原反应基本概念
含“氧”概念 含“还”概念
氧化 氧化 还原 还原
氧化剂 被氧化 氧化性 还原剂 被还原 还原性
反应 产物 反应 产物
电 电
化合价 化合价 化合价 化合价
子,化 化合价 化合价 子,化 化合价 化合价
得到 过程 得到 过程
合价 的反 的过 合价 的反 的过
的 生 成 表现的 的生成 表现的
的反 应 程 的反 应 程
物 性质 物 性质
应物 应物
3.氧化还原反应概念之间的关系
1.在氧化还原反应中,非金属单质不一定是氧化剂( √ )
2.某元素从游离态变为化合态,则该元素一定被还原( × )
3.有单质参加或生成的化学反应不一定是氧化还原反应( √ )
4.氧化还原反应中的反应物不是氧化剂就是还原剂( × )
5.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( × )
一、单质与氧化还原反应的关系
(1)有单质参加或生成的反应不一定是氧化还原反应,如 。
(2)没有单质参加的化合反应也可能是是氧化还原反应,如 。二、对氧化还原反应概念的理解
(1)氧化反应和还原反应存在于在同一个反应中,它们 发生、 存在,是相互对立统一的。
(2)氧化剂和还原剂可以是不同的物质,也可以是同种物质
①2KMnO KMnO +MnO+O ↑,氧化剂是 ,还原剂是
4 2 4 2 2
②2F+2H O O+4HF,氧化剂是 ,还原剂是
2 2 2
(3)氧化产物和还原产物可以是不同的物质,也可以是同种物质
①3S+6NaOH NaSO +2Na S+3HO,氧化产物是 ,还原产物是
2 3 2 2
②NO+NO +2NaOH 2NaNO +H O,氧化产物是 ,还原产物是
2 2 2
(4)被氧化的元素和被还原的元素可以是不同的元素,也可以是同种元素
①4HCl(浓)+MnO MnCl +Cl↑+2H O,被氧化的元素是 ,被还原的元素是
2 2 2 2
②2HS+SO 2HO+3S,被氧化的元素是 ,被还原的元素是
2 2 2
(5)可能有多种元素同时被氧化或被还原
①3Cu S+22HNO 6Cu(NO ) +10NO↑+3HSO +8H O,被氧化的元素是 和 ,被还原的元
2 3 3 2 2 4 2
素是
②2KNO+S+3C KS+N↑+3CO ↑,被氧化的元素是 ,被还原的元素是 和
3 2 2 2
(6)方程式中的系数与实际参加反应的氧化剂或还原剂的量不一定一致
①C+2H SO CO↑+2SO↑+2H O,n(氧化剂)∶n(还原剂)=
2 4 2 2 2
②Cu+2H SO CuSO +SO↑+2H O,n(氧化剂)∶n(还原剂)=
2 4 4 2 2
知识点 03 物质的氧化性和还原性
1.化合价和氧化性、还原性的关系
(1) 最高价态——只有 ,如Fe3+、HSO 、KMnO 等;
2 4 4
最低价态——只有 ,如金属单质、Cl-、S2-等;
中间价态——既有 又有 ,如Fe2+、S、Cl 等。
2
(2)常见元素的最高价态和最低价态
元素 Cl S N C H
最高价
最低价
2.氧化还原反应中酸或碱的作用
(1)氧化性:所含元素的化合价
(2)还原性:所含元素的化合价
(3)酸或碱性:所含元素的化合价 ,有相应的 生成
(4)具体反应分析①Zn+2HCl ZnCl +H ↑,盐酸表现
2 2
②CuO+2HCl CuCl +H O,盐酸表现
2 2
③MnO +4HCl(浓) MnCl +Cl ↑+2H O,盐酸表现
2 2 2 2
④2HCl H ↑+Cl ↑,盐酸表现
2 2
⑤3Cl +8NH N +6NH Cl,NH 表现
2 3 2 4 3
⑥Cu O+6HNO (浓) 2Cu(NO ) +2NO ↑+3H O,硝酸表现
2 3 3 2 2 2
△
⑦C+2H SO (浓) CO ↑+2SO ↑+2H O,浓硫酸只表现为 。
2 4 2 2 2
3.氧化还原反应中水的作用
(1)氧化性:有 产生
(2)还原性:有 产生
(3)氧化性和还原性:同时有 产生
(4)具体反应分析
①2F +2H O 4HF+O ,水表现
2 2 2
②3Fe+4H O Fe O +4H ,水表现
2 3 4 2
③2Na+2H O 2NaOH+H ↑,水表现
2 2
④2H O O ↑+2H ↑,水表现 和
2 2 2
⑤2Na O +2H O 4NaOH+O ↑,水
2 2 2 2
⑥Cl +H O HCl+HClO,水
2 2
⑦3NO +H O 2HNO +NO,水
2 2 3
4.常见的氧化剂和还原剂
(1)常见的氧化剂及产物预测
氧化剂 还原产物
Mn2+(酸性);MnO (中性);MnO 2-(碱
2 4
KMnO
4
性)
K Cr O (酸性)
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X (卤素单质)
2
H O OH-(碱性);H O(酸性)
2 2 2
Na O NaOH(或Na CO 等)
2 2 2 3
NaClO(或ClO
-)
NaClO Cl 、ClO 等
3 2 2
PbO Pb2+
2(2)常见的还原剂及产物预测
还原剂 氧化产物
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或H SO 、SO 2-)
2 2 3 3
S2-(或H S) S、SO (或SO 2-)、SO 2-
2 2 3 4
H C O CO (酸性);CO 2-(碱性)
2 2 4 2 3
H O
2 2
I-(或HI)
CO CO (酸性);CO 2-(碱性)
2 3
Zn2+、Fe2+(与强氧化剂反应生成Fe3+)
金属单质(Zn、Fe、Cu等)
Cu2+(与弱氧化剂反应生成Cu+)
易错点1:微粒具有性质判断的“易错点”
(1)金属单质处于最低价,只有 性
(2)非金属单质处于中间价态,既有氧化性又有还原性, 除外
(3)金属阳离子是高价,一定具有氧化性;但是亚铁离子具有 性,又有 性。
(4)从理论上讲任何一种化合物既有 性又有 性
易错点2:氧化性还原性的判断
(1)某元素由化合态变为游离态时,该元素一定被还原
某元素由化合态变为游离态时,该元素可能被 ,也可能被 。因为元素处于化合态时,其化合
价可能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,则其被还原。
(2)在氧化还原反应中,非金属单质一定只作氧化剂
在氧化还原反应中,非金属单质 只作氧化剂,大部分非金属单质往往既具有氧化性又具有还原性,
只是以氧化性为主。如在反应Cl+HO=HCl+HClO中,Cl 既表现氧化性又表现还原性。
2 2 2
(3)在氧化还原反应中,若有一种元素被氧化,则一定有另一种元素被还原
在氧化还原反应中,一种元素被 ,不一定有另一种元素被 ,有许多反应是一种元素既被氧化
又被还原。如在反应2NaO+2HO===4NaOH+O↑中,NaO 中氧元素的化合价既升高又降低。
2 2 2 2 2 2
易错点3:有关氧化性、还原性的易错点
1.具有氧化性的物质不一定是氧化剂,具有还原性的物质不一定是 ,应视具体反应而定。
2.对同一元素而言,一般价态越 ,氧化性越 ,如Fe3+>Fe2+>Fe;价态越低,氧化性越弱,如S2-