文档内容
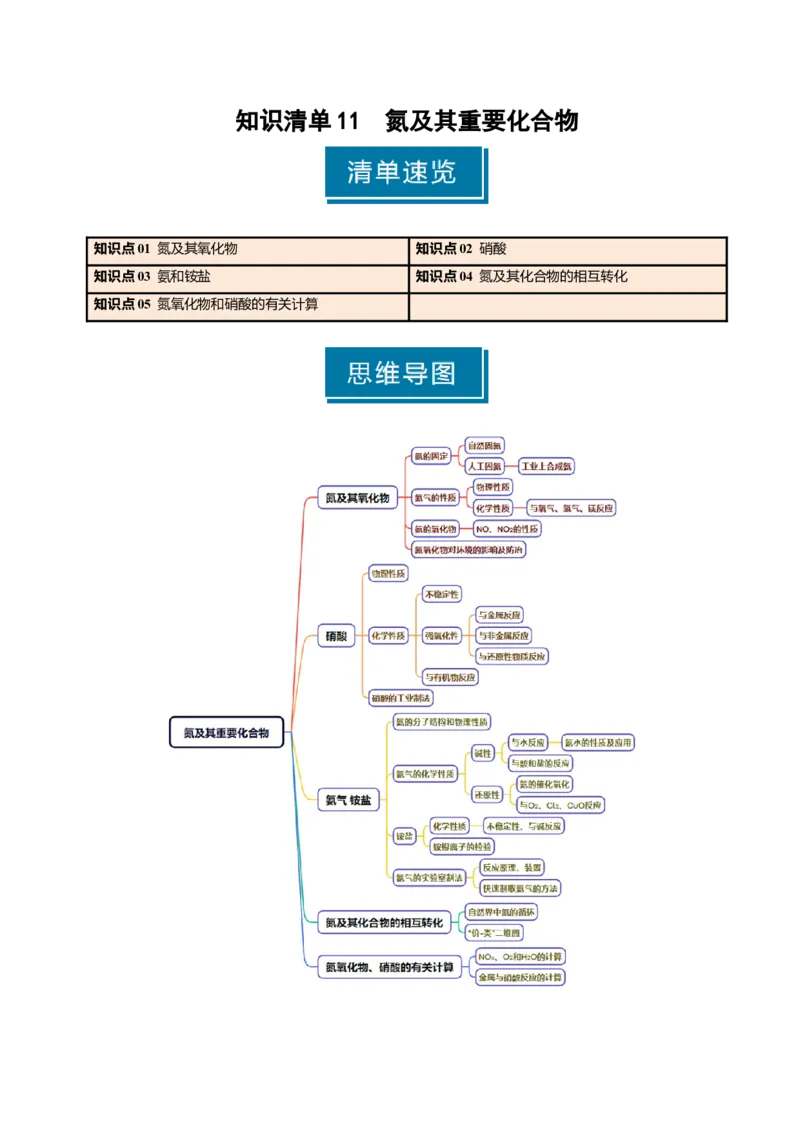
知识清单 11 氮及其重要化合物
知识点01 氮及其氧化物 知识点02 硝酸
知识点03 氨和铵盐 知识点04 氮及其化合物的相互转化
知识点05 氮氧化物和硝酸的有关计算知识点 01 氮及其氧化物
1.氮元素的存在和氮的固定
(1)氮元素的存在
游离态:N(空气中体积分数约为______)
2
化合态:动植物体内的__________中,还有部分存在于土壤、海洋里的__________和________中。
(2)氮的固定
①含义:将大气中游离态的氮转化为氮的_________的过程。
②分类:
氮的固定
2.氮气分子结构和性质
(1)氮分子的结构
氮气分子的电子式为_________,结构式为_________。
(2)氮气的化学性质
①与O 化合:___________________________。
2
②镁在氮气中燃烧:___________________________。
③与氢气化合:___________________________;应用:工业上合成氨。
(3)用途
①氮气常用作_________,如焊接金属、填充灯泡、保存食品等。
②氮气是_________、_________的重要原料。
③液氮可用作_________,应用于医学、科技等领域。
3.氮的氧化物
(1)氮的氧化物
N的化合价 +1 +2 +3 +4 +5
对应氧化物 NO(笑气) NO _______、NO _________
2 2 3 2 4
其中属于酸性氧化物的是_________和_________,对应的酸分别是_________和_________。
(2)NO和NO 的比较
2
性质 NO NO
2
_________色、有_________气
色、态、味 ____色、____味的气体
味的气体
溶解性 ____溶于水 与水反应
毒性 有毒,大气污染物之一 有毒,大气污染物之一与水反应 不反应
与氧气反应 不反应
(3)NO 的收集和检验
x
①NO采用_________收集,不用_________收集;NO 采用_________收集,不用_________收集。
2
②NO的检验:____________________________________。
4.氮氧化物对环境的污染及防治
(1)氮氧化物的来源
氮氧化物(NO )主要包括_________。__________________、__________________和__________
x
________是氮氧化物的主要来源。
(2)氮氧化物的危害
①形成酸雨:
NO 形成酸雨的过程为___________________________(用化学方程式表示)。
2
②光化学烟雾
在日光照射下,NO 使氧气经过复杂的反应生成臭氧(O ),臭氧与空气中的一些碳氢化合物在
2 3
__________________发生作用后,产生了一种有毒的烟雾,人们称之为光化学烟雾。
③破坏臭氧层:NO 可使平流层中的臭氧减少,导致地面紫外线辐射量增加。
2
④NO与血红蛋白结合使人中毒。
(3)氮氧化物污染治理方法
①汽车尾气“催化转化法”: ___________________________
②氨还原法:
____________________________________;____________________________________
③碱液吸收法:
____________________________________;____________________________________
(1)固氮反应一定属于氧化还原反应( )
(2)N 与O 在放电条件下直接化合成NO ( )
2 2 2
(3)用向上排空气法收集铜粉与稀硝酸反应产生的气体( )
(4)NO 溶于水时,NO 是氧化剂,水是还原剂( )
2 2
(5)可用NO 与水反应制取硝酸,故NO 是酸性氧化物( )
2 2
(6)CO、NO、NO 都是大气污染气体,在空气中都稳定存在( )
2
(7)利用AgNO 溶液、CCl 和HO均可鉴别NO 和溴蒸气( )
3 4 2 2
(8)NO 通入FeSO 溶液中,无明显现象( )
2 4
(8)可用湿润的淀粉碘化钾试纸鉴别NO 与溴蒸气( )
2
(9)一定条件下,1 mol N 可与3 mol H 充分反应反应生成NH ,转移的电子数为6N ( )
2 2 3 A
(10)SO 、CO、NO 都是可形成酸雨的气体( )
2 2 2一、氮气的性质及应用
1.Mg能与空气中的O、N 和CO 反应。
2 2 2
(1)Mg与CO 反应的方程式为:___________________________,该反应属于四种基本反应类型中的
2
____________。
(2)Mg与N 反应生成MgN。
2 3 2
①MgN 的电子式:__________________,Mg2+与N3-的半径大小为:_________
3 2
②MgN 与水反应的方程式:____________________________________
3 2
③MgN 与过量盐酸反应的方程式:____________________________________
3 2
2.除去N 中的O 的方法是___________________________。
2 2
二、氮氧化物的性质及应用
1.NO 与HO的反应中氧化剂与还原剂的物质的量之比为_________。
2 2
2. NO 与O 的混合气体被水完全吸收转化为HNO 的化学方程式:_______________________________,
2 2 3
NO与O 的混合气体被水完全吸收转化为HNO 的化学方程式:_____________________________。
2 3
3.NO 和溴蒸气均为红棕色气体,你用哪些实验方法鉴别二者?写出所用试剂和区别的现象。
2
方案一:试剂________________,现象__________________________________________。
方案二:试剂________________,现象__________________________________________。
方案三:试剂________________,现象__________________________________________。
4.NO 与NO 存在下列平衡:2NO NO △H<0。
2 2 4 2 2 4
(1)2mol NO与1 molO 反应,所得气体分子数_________2N 。
2 A
(2)实验测得NO 的平均相对分子质量_________46。
2
(3)将NO 气体加热,红棕色_________;②加压:颜色__________________,比加压前_______。
2
三、氮氧化物对环境的影响
1.汽车尾气中的CO、NO 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无
x
毒气体。写出NO与CO反应的化学方程式:_______________________________,该反应中NO表
现为______性。
2.用氨可将氮氧化物转化为无毒气体。氨气与NO 反应的化学方程式为:________________________,
2
该反应中NO 表现为_________性,氧化产物与还原产物的物质的量之比为________。
2
3.工业尾气中氮的氧化物常采用碱液吸收法处理。
(1)NO 被烧碱溶液吸收时,生成两种钠盐,其物质的量之比为1∶1,写出该反应的化学方程式:
2
___________________________________,1mol NO 参加反应,转移的电子数为_________。
2
(2)NO与NO 按物质的量之比1∶1被足量NaOH溶液完全吸收后只得到一种钠盐,写出该反应的化
2
学方程式:___________________________________。知识点 02 硝酸
1.硝酸的物理性质
硝酸是一种______色,______挥发,具有_________气味的液体。能与水__________________。
2.硝酸的化学性质
(1)硝酸是一元强酸,具有酸的通性。
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:____________________________________。
②硝酸和氧化钠反应:____________________________________。
③硝酸和碳酸钙反应:____________________________________。
(2)不稳定性
硝酸不稳定,见光或受热易分解,化学方程式为:____________________________________。
硝酸的保存方法:密封贮存在_________、_________处。
市售硝酸常因溶有少量_________略显黄色。
(3)硝酸的强氧化性
硝酸是一种_________性很强的酸,能与大多数金属(除Au、Pt等少数金属以外)、许多非金属以
及有机物发生氧化还原反应。
①HNO 与金属反应
3
浓硝酸、稀硝酸分别与Cu的反应方程式:
_____________________________________________
_____________________________________________
②硝酸与非金属的反应
写出C与浓硝酸反应的方程式:_____________________________________________。
③常温下浓硝酸可以使_________等金属发生钝化。可以用_________或_________容器盛放浓硝酸。
④与其他还原性物质反应
稀硝酸与Fe2+、HS、I-、SO 、SO反应的离子方程式:
2 2
_____________________________________________
_____________________________________________
_____________________________________________
_____________________________________________
_____________________________________________
(4)与有机物反应
①硝化反应(与 反应):_____________________________________________
②颜色反应:含有苯基的蛋白质遇到浓硝酸时变______色。
3.硝酸的工业制备原理写出上述转化的化学方程式。
①_________________________________________。
②_________________________________________。
③_________________________________________。
④_________________________________________。
(1)实验室也可用锌粒与稀硝酸制取氢气( )
(2)常温下,铁、铝在浓硝酸中的钝化为化学变化( )
(3)可用稀硝酸与FeS固体反应制取HS( )
2
(4)铜溶于稀硝酸不能体现硝酸的酸性(×)
(5)在酸性条件下,NO与I-、Fe2+、SO等离子能大量共存( )
(9)浓硝酸氧化性很强,常温下就可以和碳发生反应( )
(10)浓硝酸的还原产物是NO ,稀硝酸的是还原产物NO( )
2
一、硝酸的性质及应用
1.将浓硝酸存放在无色试剂瓶中,一段时间后观察到溶液变黄,用化学方程式解释变黄的原因,由此
得到启示,如何保存浓硝酸?
2.向一定量的浓硝酸中加入过量的铜片。
①反应开始阶段产生________________色气体,化学方程式为__________________________。
②反应进行一段时间后又产生无色气体,此时的化学方程式为_________________________。
③ 待 反 应 停 止 后 , 再 加 入 少 量 的 稀 硫 酸 , 这 时 Cu 片 上 又 有 气 泡 产 生 , 原 因 是
____________________。
3.将铁粉溶于稀硝酸,铁元素的存在形式可能为①__________、②________、③________。
4.将相同质量的铜分别与足量的浓硝酸、稀硝酸反应。
(1)消耗的硝酸的物质的量之比为________,被还原的硝酸的物质的量之比为________,相同条件下
产生的气体的体积之比为_________。
(2)反应中转移的电子总数浓硝酸______稀硝酸(填“大于”、“小于”或“等于”)。
(3)用排水法收集气体,理论上收集到气体的体积_________(填“相等”、“不相等”)
相同
4.往两支分别装有浅绿色的Fe(NO ) 和FeSO 溶液的试管中分别逐滴加入稀盐酸时,溶液的颜色变化应
3 2 4
该是:前者______________,后者______________。二、硝酸反应产物的实验探究
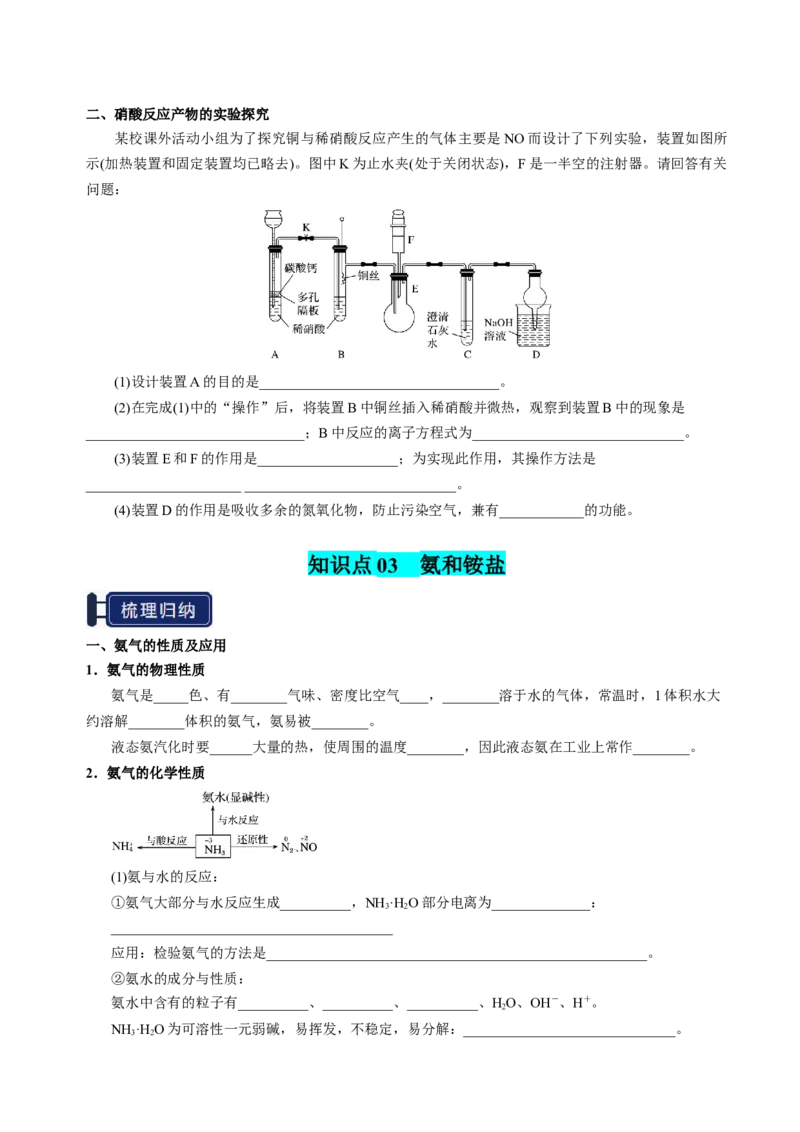
某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所
示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。请回答有关
问题:
(1)设计装置A的目的是__________________________________。
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸并微热,观察到装置B中的现象是
_______________________________;B中反应的离子方程式为______________________________。
(3)装置E和F的作用是____________________;为实现此作用,其操作方法是
______________________ ______________________________。
(4)装置D的作用是吸收多余的氮氧化物,防止污染空气,兼有____________的功能。
知识点 03 氨和铵盐
一、氨气的性质及应用
1.氨气的物理性质
氨气是_____色、有________气味、密度比空气____,________溶于水的气体,常温时,1体积水大
约溶解________体积的氨气,氨易被________。
液态氨汽化时要______大量的热,使周围的温度________,因此液态氨在工业上常作________。
2.氨气的化学性质
(1)氨与水的反应:
①氨气大部分与水反应生成__________,NH ·H O部分电离为______________:
3 2
________________________________________
应用:检验氨气的方法是______________________________________________________。
②氨水的成分与性质:
氨水中含有的粒子有__________、__________、__________、HO、OH-、H+。
2
NH ·H O为可溶性一元弱碱,易挥发,不稳定,易分解:______________________________。
3 2(2)氨与酸的反应
浓盐酸、浓硝酸等挥发性酸遇氨会产生__________,利用这点可以检验浓氨水或氨的存在。
硫酸难挥发,与氨气反应时不能观察到白烟生成。
浓氨水与盐酸、硝酸和硫酸反应的化学方程式:
__________________________、__________________________、__________________________
应用:工业上用氨气与酸反应制取铵盐,铵盐都能溶于水,是使用最广泛的化肥。
(3)与盐溶液的反应
如过量氨水与AlCl 反应的离子方程式:________________________________________。
3
(4)氨的还原性
NH 中的氮元素的价态为-3价,因此NH 不仅能被催化氧化生成NO,在纯氧中燃烧能生成N。在
3 3 2
一定条件下,NH 还能被Cl、CuO及氮氧化物等氧化。
3 2
氨的催化氧化:________________________________________,应用:工业上制取硝酸。
氨气在纯氧中燃烧:________________________________________。
氨气与氯气反应:___________________________________,应用:用浓氨水检验氯气的泄漏。
3.喷泉实验原理及应用
(1)实验原理
烧瓶内外产生__________,当烧瓶内压强__________外界压强时就会产生喷泉。
喷泉实验能否成功的关键因素:
①盛气体的烧瓶必须干燥;②气体要充满烧瓶;③烧瓶不能漏气(实验前应先检查装置的气密性);
④所用气体能大量溶于所用液体或气体与液体快速反应。
(2)常见喷泉的形成主要有以下两类:
①极易溶于水的气体(NH 、HCl、SO 等)与水可形成喷泉。
3 2
②酸性气体(HCl、SO 、NO 、CO、HS等)与NaOH(aq)也能形成喷泉。
2 2 2 2
二、铵盐及氨气的实验室制法
1.铵盐
(1)铵盐的物理性质
通常把铵根离子和酸根离子形成的__________化合物称为铵盐 ,它们多为_____色、_____溶于水
的晶体。
(2)铵盐的化学性质
①不稳定性:铵盐不稳定,受热易分解。
NH Cl分解的化学方程式为:________________________________________
4
NH HCO 分解的化学方程式为:________________________________________
4 3
②与碱反应:
铵盐与碱溶液反应的离子方程式:
a.在稀溶液中不加热:________________________________________。
b.加热时或浓溶液:________________________________________。
(3)铵盐的检验方法___________________________________________________________________________________。
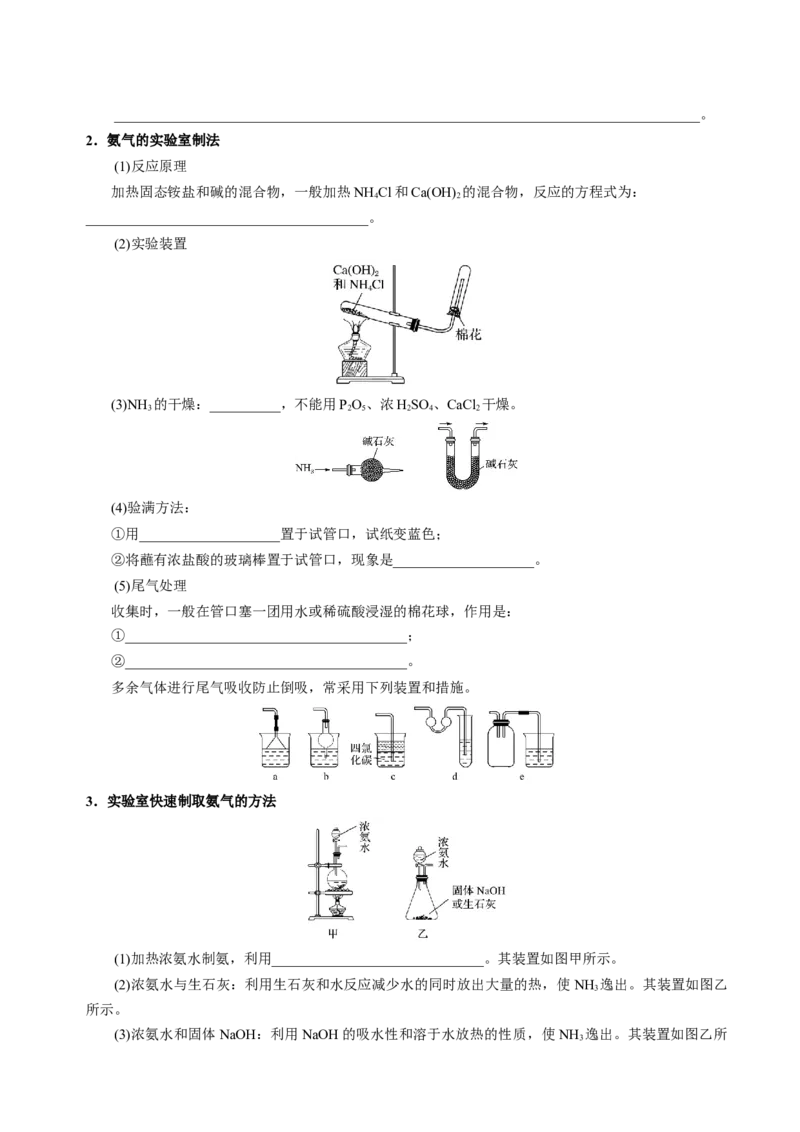
2.氨气的实验室制法
(1)反应原理
加热固态铵盐和碱的混合物,一般加热NH Cl和Ca(OH) 的混合物,反应的方程式为:
4 2
________________________________________。
(2)实验装置
(3)NH 的干燥:__________,不能用PO、浓HSO 、CaCl 干燥。
3 2 5 2 4 2
(4)验满方法:
①用____________________置于试管口,试纸变蓝色;
②将蘸有浓盐酸的玻璃棒置于试管口,现象是____________________。
(5)尾气处理
收集时,一般在管口塞一团用水或稀硫酸浸湿的棉花球,作用是:
①________________________________________;
②________________________________________。
多余气体进行尾气吸收防止倒吸,常采用下列装置和措施。
3.实验室快速制取氨气的方法
(1)加热浓氨水制氨,利用______________________________。其装置如图甲所示。
(2)浓氨水与生石灰:利用生石灰和水反应减少水的同时放出大量的热,使NH 逸出。其装置如图乙
3
所示。
(3)浓氨水和固体NaOH:利用NaOH的吸水性和溶于水放热的性质,使NH 逸出。其装置如图乙所
3示。
(1)液氨制冷、碘的升华、NH Cl气化都不涉及化学变化( )
4
(2)能用加热法除去NaCl中的NH Cl的原因是NH Cl为强酸弱碱盐( )
4 4
(3)现有1 mol·L-1的氨水,则该溶液中NH ·H O的浓度是1 mol·L-1( )
3 2
(4)浓氨水可检验氯气管道是否漏气( )
(5)因为NH HCO 受热易分解,所以可用作氮肥( )
4 3
(6)液氨可用作制冷剂,是因为其汽化时吸收大量的热( )
(7)氨水呈碱性,是因为NH 溶于水发生反应:NH +HONH+OH-( )
3 3 2
(8)铵盐都不稳定,受热分解都生成NH ( )
3
(9)向某溶液中加入稀NaOH溶液,湿润的红色石蕊试纸不变蓝,则原溶液中一定无NH( )
(10)NH HCO 与足量NaOH溶液共热时,发生反应的离子方程式为NH+OH-=====NH ↑+HO( )
4 3 3 2
(11)某同学根据铵盐受热分解的性质,认为可以采用加热NH Cl分解的方法来制取氨( )
4
(12)为加快产生NH 的速率,实验室可以用NaOH固体和NH Cl固体反应制NH ( )
3 4 3
一、氨和铵盐的性质及应用
1.施肥时,草木灰(有效成分为KCO)不能与NH Cl混合使用的原因是:_________________________。
2 3 4
2.用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是①______________________________;
②________________________________________
3.蘸有浓硝酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,能产生白烟现象吗?简述原因。若将浓硝酸改为
浓硫酸也会出现相同的现象吗?
4.(1)将氨与氯气混合也会产生白烟,用化学方程式解释产生白烟的过程_______________________。
(2)在饱和NH Cl溶液中滴加NaAlO ,产生刺激性气味的气体和白色沉淀,用离子方程式解释其现
4 2
象:_________________________________。
(3)实验室常用饱和氯化铵(NH Cl)与亚硝酸钠(NaNO )加热来制取氮气,写出发生反应的化学方程式
4 2
________________________。
二、氨、铵盐的性质实验探究
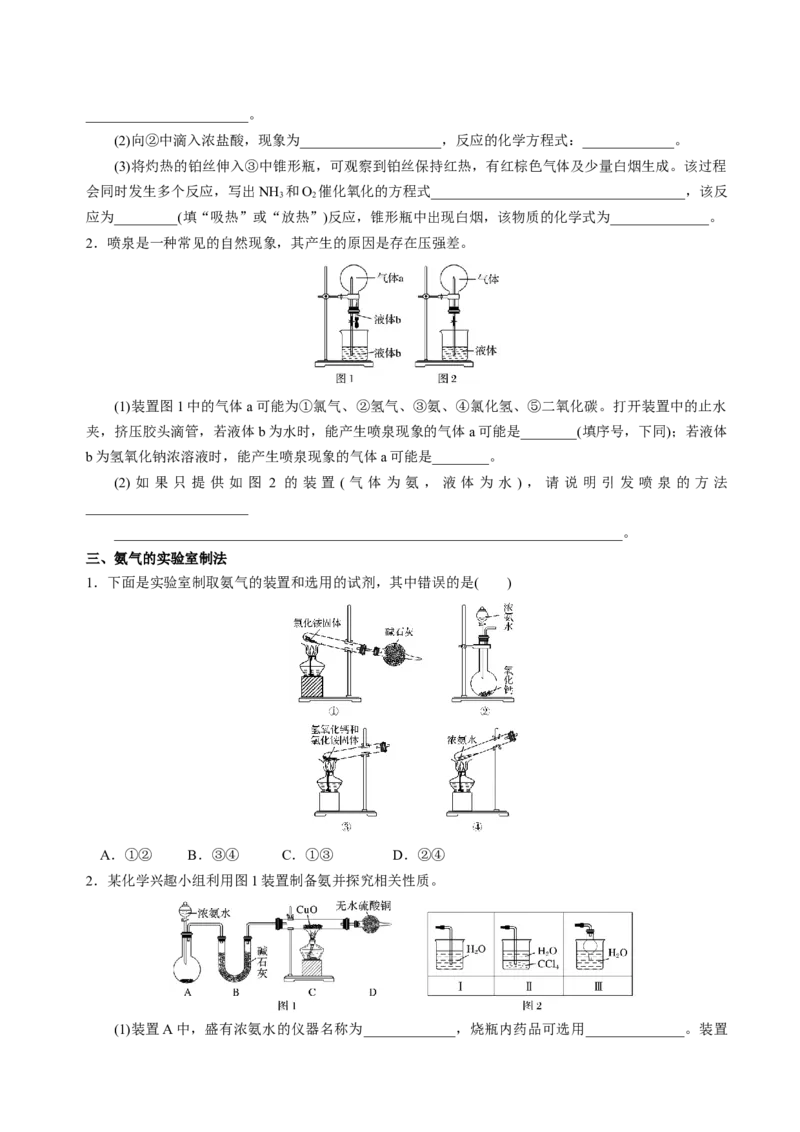
1.某化学兴趣小组利用下列图示装置探究氨的性质。
(1)① 中湿润的红色石蕊试纸__________,用化学用语表示产生该现象的原因_________________________________。
(2)向②中滴入浓盐酸,现象为____________________,反应的化学方程式:_____________。
(3)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程
会同时发生多个反应,写出NH 和O 催化氧化的方程式____________________________________,该反
3 2
应为_________(填“吸热”或“放热”)反应,锥形瓶中出现白烟,该物质的化学式为______________。
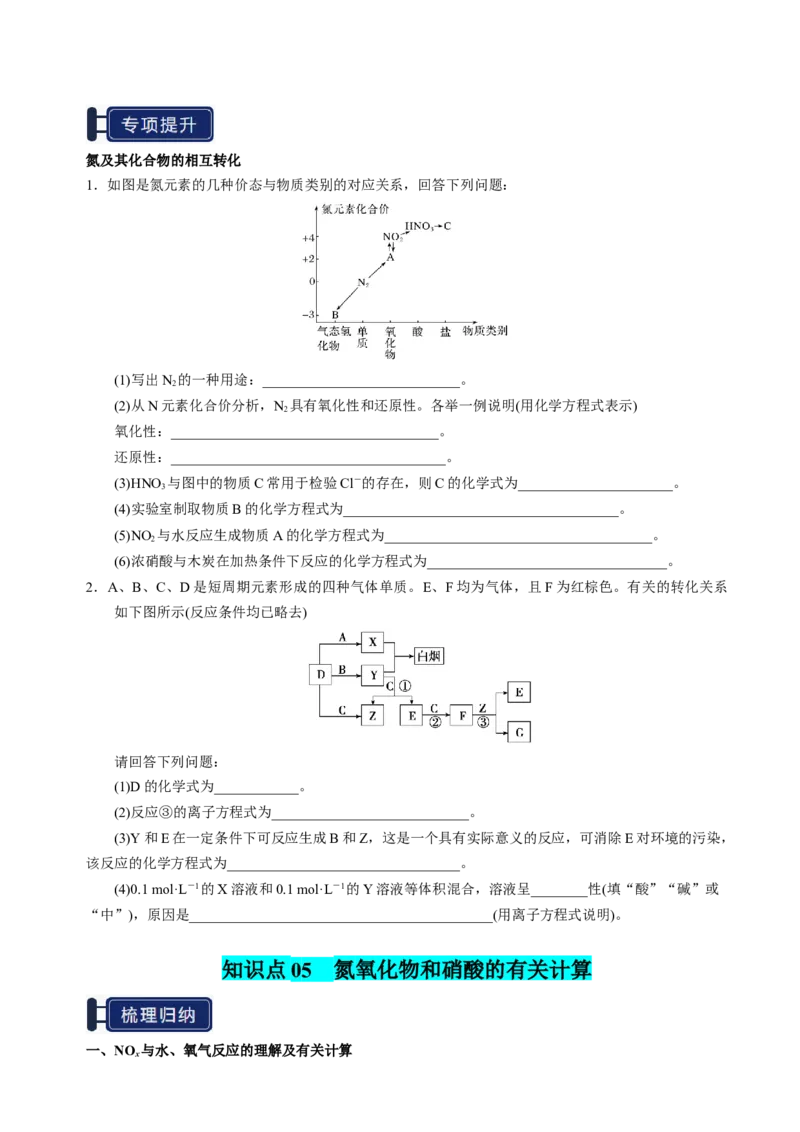
2.喷泉是一种常见的自然现象,其产生的原因是存在压强差。
(1)装置图1中的气体a可能为①氯气、②氢气、③氨、④氯化氢、⑤二氧化碳。打开装置中的止水
夹,挤压胶头滴管,若液体b为水时,能产生喷泉现象的气体a可能是________(填序号,下同);若液体
b为氢氧化钠浓溶液时,能产生喷泉现象的气体a可能是________。
(2) 如 果 只 提 供 如 图 2 的 装 置 ( 气 体 为 氨 , 液 体 为 水 ) , 请 说 明 引 发 喷 泉 的 方 法
_______________________
________________________________________________________________________。
三、氨气的实验室制法
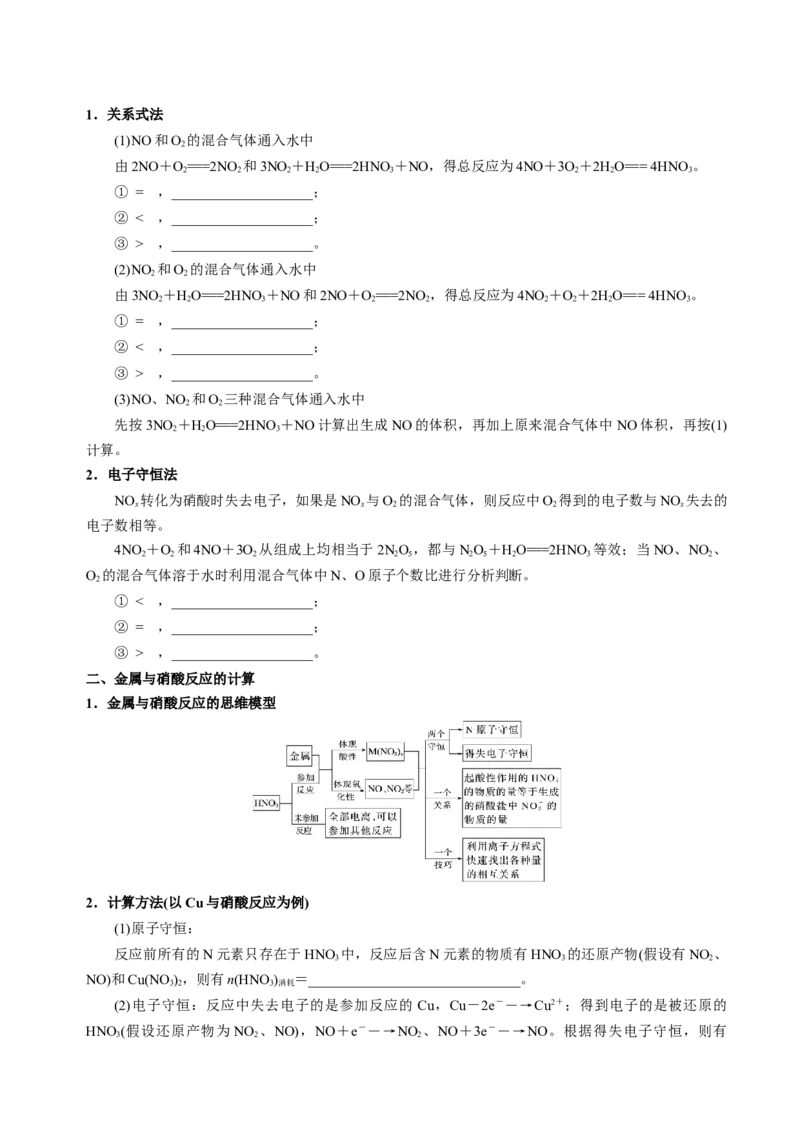
1.下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A.①② B.③④ C.①③ D.②④
2.某化学兴趣小组利用图1装置制备氨并探究相关性质。
(1)装置A中,盛有浓氨水的仪器名称为_____________,烧瓶内药品可选用______________。装置B的作用是________________________。
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关
化学方程式为______________________________________,该反应证明氨具有________性。
(3)该实验缺少尾气吸收装置,图2中能用来吸收尾气的装置是________(填装置序号)。
知识点 04 氮及其化合物的相互转化
1.含氮元素物质之间的转化关系
(1)横向转化为物质类别变化,非氧化还原反应,例如:
①氨气转化为铵盐:______________________________
②硝酸转化为硝酸盐:______________________________
(2)纵向、斜向转化为化合价变化反应,是氧化还原反应,例如:
①NH 转化为N:______________________________
3 2
②NH 转化为NO:______________________________
3
(3)歧化——同一物质中某元素的化合价在同一反应中既升高又降低。例如:
NO 与水反应:______________________________
2
NO 与NaOH溶液反应:______________________________
2
(4)归中——不同物质中同一元素的不同化合价在同一反应中只靠拢。例如:
NO与NH 反应:______________________________
3
NO、NO 混合气体与NaOH溶液反应:______________________________
2
2.氮元素的“价—类二维图”
氮元素有多种可变化合价,物质的种类较多,在复习时要从物质类别和价态变化理解这些物质之间
的转化关系。氮及其化合物的相互转化
1.如图是氮元素的几种价态与物质类别的对应关系,回答下列问题:
(1)写出N 的一种用途:____________________________。
2
(2)从N元素化合价分析,N 具有氧化性和还原性。各举一例说明(用化学方程式表示)
2
氧化性:______________________________________。
还原性:_______________________________________。
(3)HNO 与图中的物质C常用于检验Cl-的存在,则C的化学式为______________________。
3
(4)实验室制取物质B的化学方程式为_______________________________________。
(5)NO 与水反应生成物质A的化学方程式为______________________________________。
2
(6)浓硝酸与木炭在加热条件下反应的化学方程式为__________________________________。
2.A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系
如下图所示(反应条件均已略去)
请回答下列问题:
(1)D的化学式为____________。
(2)反应③的离子方程式为____________________________。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,
该反应的化学方程式为_________________________________。
(4)0.1 mol·L-1的X溶液和0.1 mol·L-1的Y溶液等体积混合,溶液呈________性(填“酸”“碱”或
“中”),原因是___________________________________________(用离子方程式说明)。
知识点 05 氮氧化物和硝酸的有关计算
一、NO 与水、氧气反应的理解及有关计算
x1.关系式法
(1)NO和O 的混合气体通入水中
2
由2NO+O===2NO 和3NO +HO===2HNO +NO,得总反应为4NO+3O+2HO=== 4HNO。
2 2 2 2 3 2 2 3
① = ,____________________;
② < ,____________________;
③ > ,____________________。
(2)NO 和O 的混合气体通入水中
2 2
由3NO +HO===2HNO +NO和2NO+O===2NO,得总反应为4NO +O+2HO=== 4HNO。
2 2 3 2 2 2 2 2 3
① = ,____________________;
② < ,____________________;
③ > ,____________________。
(3)NO、NO 和O 三种混合气体通入水中
2 2
先按3NO +HO===2HNO +NO计算出生成NO的体积,再加上原来混合气体中NO体积,再按(1)
2 2 3
计算。
2.电子守恒法
NO 转化为硝酸时失去电子,如果是NO 与O 的混合气体,则反应中O 得到的电子数与NO 失去的
x x 2 2 x
电子数相等。
4NO +O 和4NO+3O 从组成上均相当于2NO ,都与NO +HO===2HNO 等效;当NO、NO 、
2 2 2 2 5 2 5 2 3 2
O 的混合气体溶于水时利用混合气体中N、O原子个数比进行分析判断。
2
① < ,____________________;
② = ,____________________;
③ > ,____________________。
二、金属与硝酸反应的计算
1.金属与硝酸反应的思维模型
2.计算方法(以Cu与硝酸反应为例)
(1)原子守恒:
反应前所有的N元素只存在于HNO 中,反应后含N元素的物质有HNO 的还原产物(假设有NO 、
3 3 2
NO)和Cu(NO ),则有n(HNO) =______________________________。
3 2 3 消耗
(2)电子守恒:反应中失去电子的是参加反应的 Cu,Cu-2e-―→Cu2+;得到电子的是被还原的
HNO(假设还原产物为NO 、NO),NO+e-―→NO 、NO+3e-―→NO。根据得失电子守恒,则有
3 2 22n(Cu)=____________________。
若将生成的氮的氧化物气体与一定量的氧气共同通入水中,氮的氧化物完全生成硝酸,由于开始反
应物为硝酸,中间生成了氮的氧化物,但最终又变回了硝酸,所以相当于铜失的电子最终由氧气得到,
则有2n(Cu)=__________。
(3)电荷守恒:
在Cu与HNO 反应后的溶液中,若HNO 不过量,阳离子只有Cu2+,阴离子只有NO(此类计算不考
3 3
虑HO电离出的极少量的H+、OH-);若HNO 过量,溶液中的阳离子有Cu2+和H+,阴离子只有NO。
2 3
则有①若HNO 不过量:n(NO)=__________;②若HNO 过量:n(NO)=__________。
3 3
(4)离子方程式计算:
金属与硫酸、硝酸的混合酸反应时,由于硝酸盐中NO在硫酸提供H+的条件下能继续与金属反应,
故此类题目应用离子方程式来计算3Cu+8H++2NO===3Cu2++2NO↑+4HO。先作过量判断,然后根据
2
完全反应的金属或H+或NO进行相关计算,且要符合电荷守恒。
一、NO 与HO、O 反应的计算
x 2 2
1.有一充有20 mL NO和NO 混合气体的试管,倒置于盛有水的水槽中,充分反应后,仍有12 mL 无色
2
气体,则原混合气体中NO和NO 的体积之比为(气体体积均在相同状况下测得) __________。
2
2.将盛有12 mL NO 和O 的混合气体的量筒倒立于水槽中,充分反应后,还剩余2 mL无色气体。
2 2
(1)若剩余的气体是________,则NO 、O 的体积分别是________。
2 2
(2)若剩余的气体是________,则NO 、O 的体积分别是________。
2 2
二、金属与硝酸反应的计算
1.将14 g铜银合金与足量的硝酸反应,放出的气体与标准状况下体积为1.12 L的O 混合后再通入
2
水中,恰好全部吸收,则合金中铜的质量为__________g。
2.将3.84 g Cu和一定量的浓HNO 反应,当Cu反应完全时,共收集到气体2.24 L NO 和NO(标准
3 2
状况,不考虑NO 转化为NO),则反应中消耗HNO 的物质的量为__________mol。
2 2 4 3