文档内容
知识清单 31 物质的分离、提纯与鉴别
知识点01 物质的分离和提纯 知识点02用化学方法分离和提纯物质
知识点03 常见物质的检验
知识点 01 物质的分离和提纯
1.物质分离、提纯的区别
(1)物质的分离:将混合物的各组分分离开来,获得几种___________的过程。
(2)物质的提纯:将混合物中的杂质除去而得到___________的过程,又叫物质的净化或除杂。
2.依据物理性质选择分离、提纯的方法
(1)“固+固”混合物的分离(提纯)(2)“固+液”混合物的分离(提纯)
(3)“液+液”混合物的分离(提纯)
3.物理法分离、提纯物质所选装置
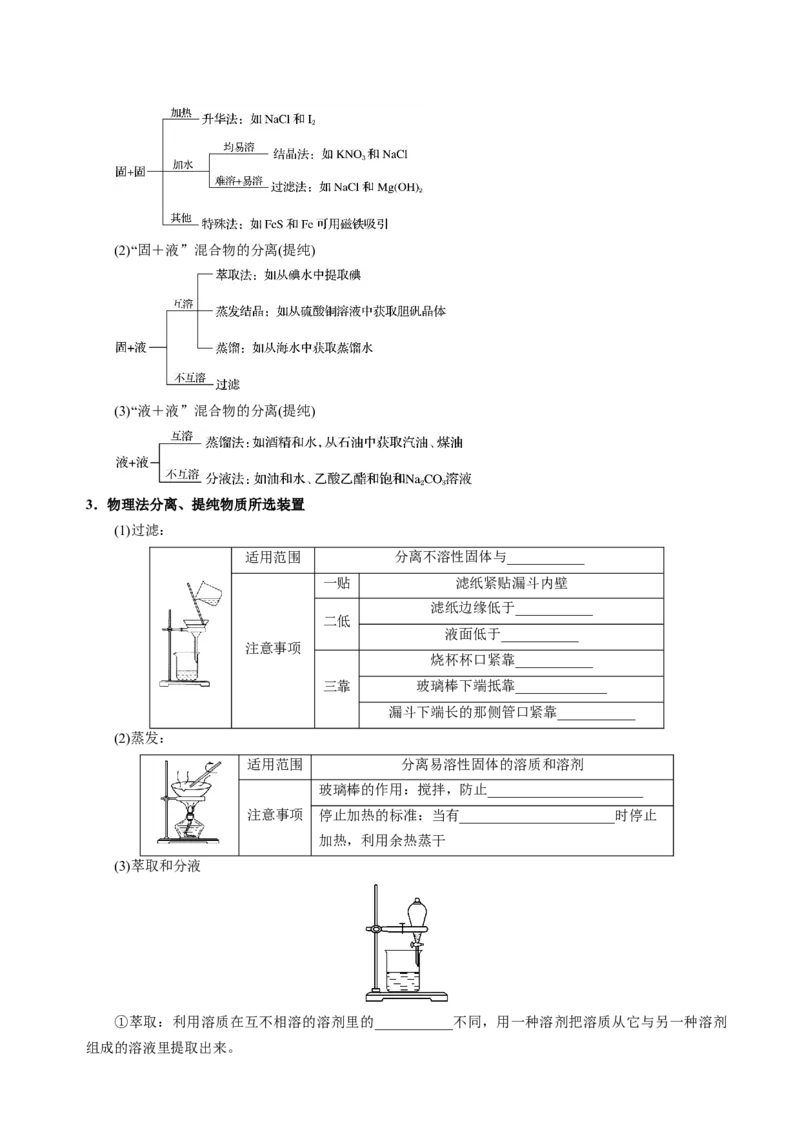
(1)过滤:
适用范围 分离不溶性固体与___________
一贴 滤纸紧贴漏斗内壁
滤纸边缘低于___________
二低
液面低于___________
注意事项
烧杯杯口紧靠___________
三靠 玻璃棒下端抵靠_____________
漏斗下端长的那侧管口紧靠___________
(2)蒸发:
适用范围 分离易溶性固体的溶质和溶剂
玻璃棒的作用:搅拌,防止______________________
注意事项 停止加热的标准:当有______________________时停止
加热,利用余热蒸干
(3)萃取和分液
①萃取:利用溶质在互不相溶的溶剂里的___________不同,用一种溶剂把溶质从它与另一种溶剂
组成的溶液里提取出来。②分液:分离两种___________且易分层的液体。
③萃取的条件
溶质在萃取剂中的溶解度比在原溶剂中大的多。
萃取剂与原溶剂不反应、不相溶。
萃取剂与溶质不反应。
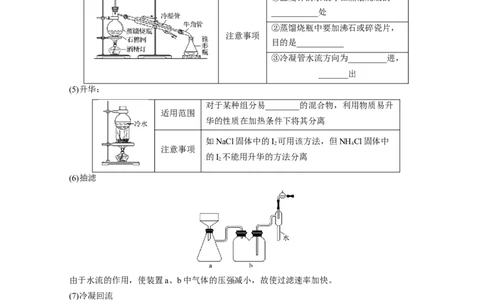
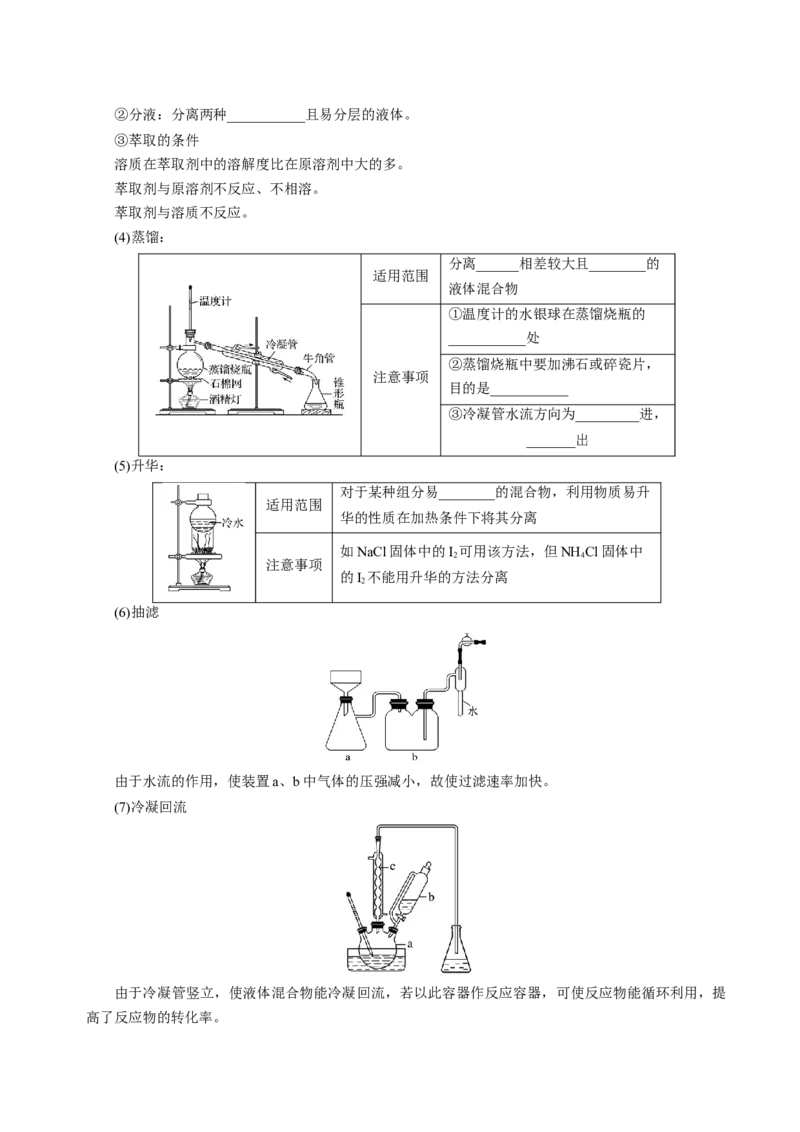
(4)蒸馏:
分离______相差较大且________的
适用范围
液体混合物
①温度计的水银球在蒸馏烧瓶的
___________处
②蒸馏烧瓶中要加沸石或碎瓷片,
注意事项
目的是___________
③冷凝管水流方向为_________进,
_______出
(5)升华:
对于某种组分易________的混合物,利用物质易升
适用范围
华的性质在加热条件下将其分离
如NaCl固体中的I 可用该方法,但NH Cl固体中
2 4
注意事项
的I 不能用升华的方法分离
2
(6)抽滤
由于水流的作用,使装置a、b中气体的压强减小,故使过滤速率加快。
(7)冷凝回流
由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器作反应容器,可使反应物能循环利用,提
高了反应物的转化率。(1)过滤时,为加快过滤速度,应用玻璃棒不断搅拌漏斗中液体( )
(2)根据食用油和汽油的密度不同,可选用分液的方法分离( )
(3)用乙醇萃取出溴水中的溴,再用蒸馏的方法分离溴与乙醇( )
(4)在蒸馏过程中,若发现忘加沸石,应停止加热立即补加( )
(5)利用加热的方法分离NH Cl和I 的固体混合物( )
4 2
(6)制取无水乙醇可向乙醇中加入CaO之后过滤( )
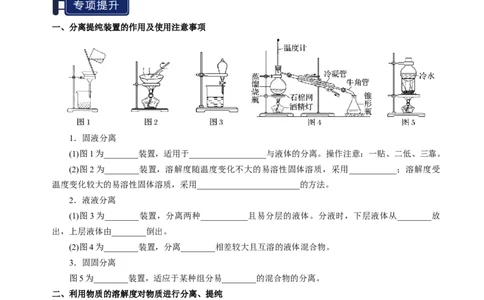
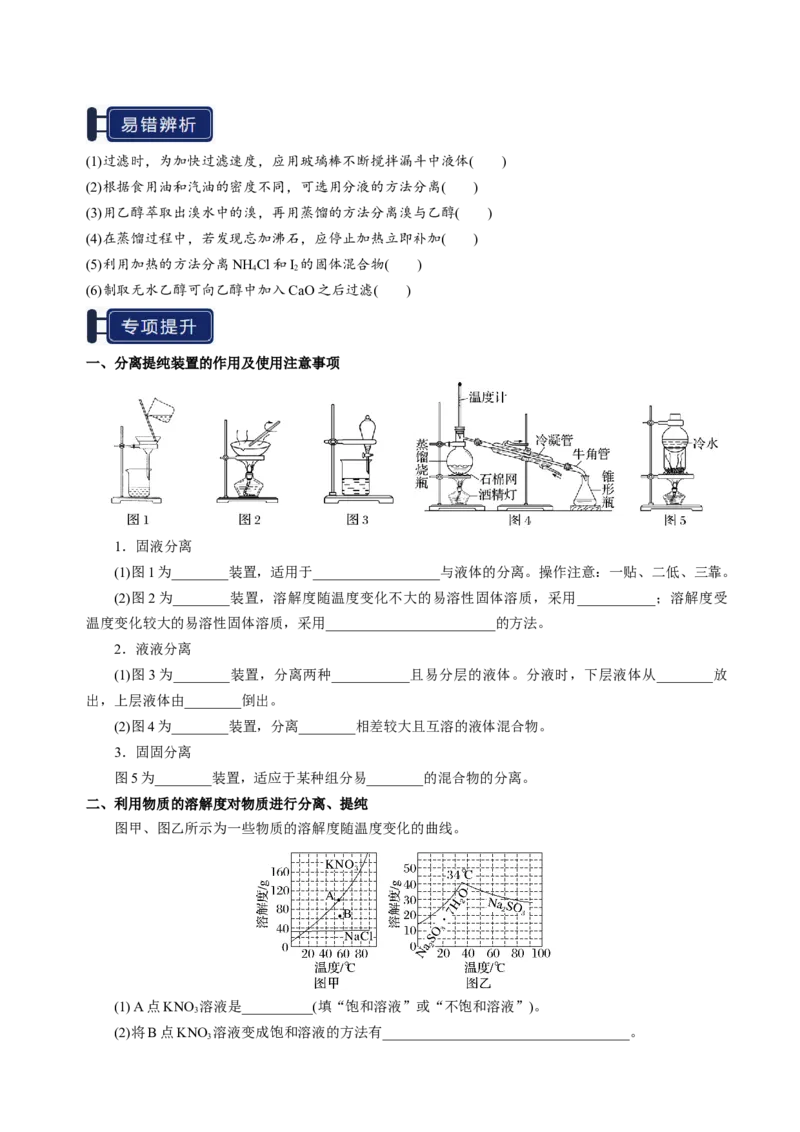
一、分离提纯装置的作用及使用注意事项
1.固液分离
(1)图1为________装置,适用于__________________与液体的分离。操作注意:一贴、二低、三靠。
(2)图2为________装置,溶解度随温度变化不大的易溶性固体溶质,采用___________;溶解度受
温度变化较大的易溶性固体溶质,采用________________________的方法。
2.液液分离
(1)图3为________装置,分离两种___________且易分层的液体。分液时,下层液体从________放
出,上层液体由________倒出。
(2)图4为________装置,分离________相差较大且互溶的液体混合物。
3.固固分离
图5为________装置,适应于某种组分易________的混合物的分离。
二、利用物质的溶解度对物质进行分离、提纯
图甲、图乙所示为一些物质的溶解度随温度变化的曲线。
(1) A点KNO 溶液是__________(填“饱和溶液”或“不饱和溶液”)。
3
(2)将B点KNO 溶液变成饱和溶液的方法有___________________________________。
3(3)常温下,由NaCl稀溶液获取NaCl固体的方法是__________。
(4)常温下由KNO 稀溶液获取KNO 固体的方法是____________________。
3 3
(5) NaCl固体中含少量KNO,提纯NaCl固体的方式是_______________________。
3
(6) KNO 固体中含少量NaCl,提纯KNO 固体的方式是_______________________。
3 3
(7)图乙所示为NaSO 的溶解度随温度的变化曲线。常温下由NaSO 稀溶液获取NaSO 固体的方法
2 3 2 3 2 3
是什么?_______________________________________________________。
三、物质分离操作注意事项
(1)从含有少量KNO 杂质的氯化钠溶液中分离出氯化钠固体的操作:________________、洗涤、干
3
燥。
(2)从MgSO 溶液中得到MgSO 固体的实验操作包括________、冷却结晶、________、洗涤、干燥
4 4
等一系列操作,在此过程中玻璃棒的作用是________(填序号)。
①引流 ②搅拌加速溶解 ③搅拌使溶液受热均匀,防止暴沸
(3)若滤液浑浊,需____________________。浑浊的原因可能是________________________。
(4)硫酸铝和硫酸铵的混合液经蒸发浓缩至溶液表面刚出现薄层晶体时即停止加热,然后冷却结晶,
得到铵明矾晶体[NH Al(SO )·12H O]。溶液不能蒸干的原因是__________________。
4 4 2 2
(5)分液时,分液漏斗中的液体很难滴下,可能的原因是______________________________。
知识点 02 用化学方法分离和提纯物质
1.物质分离、提纯的常用化学方法
方法 原理 实例
当混合物中混有热稳定性差的物质时, 如NaCl中混有NH Cl,NaCO 中
4 2 3
加热法 可直接加热,使热稳定性差的物质受热 混有NaHCO 等均可直接加热除
3
分解而分离出 去杂质
在混合物中加入某种试剂,使其中一种
如加适量的BaCl 溶液可除去
2
沉淀法 以沉淀的形式分离出去的方法。使用该
NaCl中混有的NaSO
2 4
方法一定要注意不能引入新的杂质
氧化还原 如果混合物中混有氧化性杂质,可以加 如将过量的铁粉加入混有FeCl 的
3
反应法 入适当的还原剂使其还原为被提纯物质 FeCl 溶液中,以除去FeCl 杂质
2 3
电解法 利用电解原理来分离、提纯物质 如电解精炼铜
调 节 pH 通过加入试剂来调节溶液的pH,使溶 如CuCl 2 溶液中含有FeCl 3 杂质,
法 液中某组分沉淀而分离的方法,一般是 可向溶液中加入CuO除去加入相应的难溶或微溶物来调节
2.除杂“四原则”
(1)不增,不得引入新杂质;
(2)不减,尽量不减少被提纯和分离的物质;
(3)易分,应使被提纯或分离的物质与其他物质易分离;
(4)易复原,被提纯物质转化后要易被复原。
3.除杂操作“四注意”
(1)除杂试剂要过量;
(2)过量试剂需除去;
(3)选择的途径要最佳;
(4)除去多种杂质时要考虑加入试剂的先后顺序。
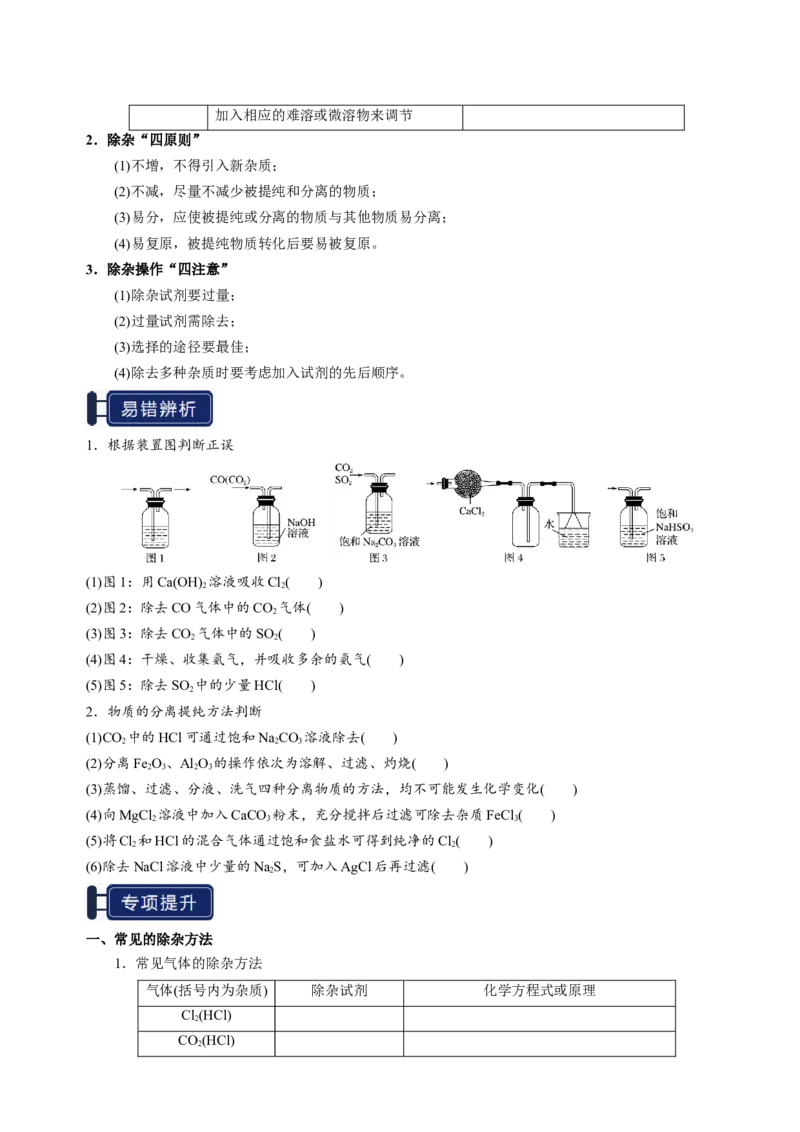
1.根据装置图判断正误
(1)图1:用Ca(OH) 溶液吸收Cl( )
2 2
(2)图2:除去CO气体中的CO 气体( )
2
(3)图3:除去CO 气体中的SO ( )
2 2
(4)图4:干燥、收集氨气,并吸收多余的氨气( )
(5)图5:除去SO 中的少量HCl( )
2
2.物质的分离提纯方法判断
(1)CO 中的HCl可通过饱和NaCO 溶液除去( )
2 2 3
(2)分离Fe O、Al O 的操作依次为溶解、过滤、灼烧( )
2 3 2 3
(3)蒸馏、过滤、分液、洗气四种分离物质的方法,均不可能发生化学变化( )
(4)向MgCl 溶液中加入CaCO 粉末,充分搅拌后过滤可除去杂质FeCl ( )
2 3 3
(5)将Cl 和HCl的混合气体通过饱和食盐水可得到纯净的Cl( )
2 2
(6)除去NaCl溶液中少量的NaS,可加入AgCl后再过滤( )
2
一、常见的除杂方法
1.常见气体的除杂方法
气体(括号内为杂质) 除杂试剂 化学方程式或原理
Cl(HCl)
2
CO(HCl)
2CO(SO )
2 2
CO(CO)
2
CO(CO )
2
N(O )
2 2
CH(CH==CH)
4 2 2
2.常见固体或溶液的除杂方法
物质(括号内为杂质) 除杂试剂或方法 化学方程式或原理
NaCO 固体(NaHCO )
2 3 3
FeCl 溶液(FeCl )
3 2
NaHCO 溶液(Na CO)
3 2 3
Cu(NO ) 溶液(AgNO)
3 2 3
I(SiO)
2 2
Fe O(AlO)
2 3 2 3
NH Cl溶液(FeCl )
4 3
KNO 固体(NaCl)
3
C(CuO)
CuS(FeS)
镁粉(铝粉)
二、常见物质分离操作方法、装置的选择
除去气体中的杂质通常有如下3套装置,请选择合适的装置序号填入下列空格中。
注:括号内为杂质气体
(1)CO (HCl):________。
2
(2)CO (CO):________。
2
(3)CO(CO ):________。
2
三、沉淀分离操作的规范解答
1.在测定NaSO 和NaCl的混合物中NaSO 的质量分数时,可以在混合物中加入过量BaCl 溶液,
2 4 2 4 2
沉淀SO,然后过滤、洗涤、烘干、称量得到BaSO 的质量,试问:
4
(1)怎样判断SO是否沉淀完全?
(2)过滤完毕后,为什么要洗涤沉淀(即洗涤沉淀的目的)?(3)沉淀的洗涤方法?
(4)怎样判断沉淀是否洗净?
2.利用工业FeCl 制取纯净的草酸铁晶体[Fe (C O)·5H O]的实验流程如图所示。
3 2 2 4 3 2
所得Fe (C O)·5H O需用冰水洗涤,其目的是______________________________________。
2 2 4 3 2
知识点 03 常见物质的检验
1.常见阳离子的检验与推断依据
根据离子性质不同而在实验中所表现出的现象不同,可以把检验离子的方法归纳为三种类型:
①生成沉淀;②生成气体;③显现特殊颜色。
(1)依据生成沉淀检验或推断
阳离子 试剂 实验现象(证据)
Mg2+ NaOH溶液 开始产生______色沉淀,NaOH溶液过量沉淀________
Al3+ NaOH溶液 开始产生_____色沉淀,NaOH溶液过量沉淀________
NaOH溶液 先产生____色沉淀,迅速变为________色,最后变为______色
Fe2+ K[Fe(CN) ]
3 6
产生________色沉淀
(铁氰化钾)溶液
Fe3+ NaOH溶液 产生________色沉淀
Cu2+ NaOH溶液 产生________色沉淀
(2)依据生成气体检验或推断
NH―――――→产生使________的_____色石蕊试纸________的气体。
(3)依据显示特殊颜色检验或推断
阳离子 试剂或方法 实验现象(证据)
H+ 紫色石蕊溶液 溶液变______
Na+ 焰色反应 _____色火焰
K+ 焰色反应 _____色火焰(透过____________)
Fe3+ KSCN溶液 溶液呈______色Fe2+ 先加KSCN溶液再加氯水 先______________,再变______色
2.常见阴离子的检验与推断依据
(1)依据生成沉淀检验或推断
阴离子 试剂 实验现象(证据)
Cl- 产生_____色沉淀AgCl
Br- AgNO 溶液和稀HNO 产生_____色沉淀AgBr
3 3
I- 产生_____色沉淀AgI
SO 稀盐酸和BaCl 溶液 加盐酸无明显现象,加BaCl 溶液产生_____色沉淀
2 2
加CaCl 溶液产生_____色沉淀,再加盐酸沉淀_____,产
2
CO CaCl 溶液和稀盐酸
2
生________________
(2)依据生成气体检验或推断
阴离子 试剂 实验现象(证据)
CO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水________的气体
HCO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水________的气体
加硫酸产生有________气味的气体,且气体能使品红
SO 稀HSO 和品红溶液
2 4
溶液________
加硫酸产生有________气味的气体,且气体能使品红
HSO 稀HSO 和品红溶液
2 4
溶液________
(3)依据显示特殊颜色检验或推断
①OH-—
②――→有机层(下层)
③I-――――――→溶液________,表明有_____。
3.常见气体的检验方法
气体 检验试剂或方法 实验现象
火焰呈________色,干冷的烧杯罩在火焰上方,烧杯内
H 点燃(纯氢)
2
壁有________产生
O 带火星的木条
2
Cl 湿润的淀粉-KI试纸
2
CO 通入澄清石灰水中 澄清石灰水________ (通入过量二氧化碳后又________)
2
SO 通入品红溶液中 品红溶液________,加热后又___________
2
NH 湿润的红色石蕊试纸
3
CO 在空气中燃烧 产生_______火焰,生成能使澄清石灰水________的气体
火焰呈________色,干冷的烧杯罩在火焰上方,烧杯内
CH 点燃
4
壁有________产生,加澄清石灰水振荡________
通入溴的四氯化碳溶液
C H
2 4
(或酸性KMnO 溶液)
4通入溴的四氯化碳溶液
C H
2 2
(或酸性KMnO 溶液)
4
4.常见有机物的检验
(1)常用的检验有机物的试剂
有机物的性质主要是由其官能团决定的,有机物的检验,主要是官能团的检验,常用的试剂有:
①酸性KMnO 溶液:含碳碳双键或碳碳三键的有机化合物、苯的同系物、醇、苯酚、醛、甲酸、甲
4
酸的酯或盐、葡萄糖、麦芽糖等皆可使之褪色。
②溴水:含碳碳双键或碳碳三键的有机化合物、酚、醛、甲酸、甲酸的酯或盐、葡萄糖与溴水反应
使溴水褪色;苯的同系物、四氯化碳等可萃取溴水中的溴,使溴水褪色。
③银氨溶液:含醛基的有机物皆可发生银镜反应(注意发生反应和形成银镜的条件)。
④新制的Cu(OH) (碱性):a.含醛基的物质与其混合加热煮沸生成砖红色沉淀;b.羧酸可使其溶解得
2
蓝色溶液;c.多羟基化合物(丙三醇、葡萄糖等)使之溶解得绛蓝色溶液。
(3)检验与鉴别有机物的四种主要方法
①检验有机物溶解性:通常是加水检查、观察是否能溶于水。例如:用此法可以鉴别乙酸与乙酸乙
酯、乙醇与氯乙烷、甘油与油脂等。
②检查液态有机物的密度:观察不溶于水的有机物在水中浮沉情况,可知其密度比水的密度小还是
大。例如,用此法可以鉴别硝基苯与苯、四氯化碳与1-氯丁烷。
③检查有机物燃烧情况:如观察是否可燃(大部分有机物可燃,四氯化碳和少数有机物不可燃)、燃
烧时黑烟的多少(可区分乙烷、乙烯和乙炔,己烯和苯,聚乙烯和聚苯乙烯)、燃烧时的气味(如识别聚氯
乙烯和蛋白质)。
④检查有机物的官能团:结构决定性质,官能团体现结构,选取典型试剂检验对应的官能团是有机
物检验的关键。
⑤FeCl 溶液遇苯酚显紫色;蛋白质(含苯环)与浓硝酸作用变黄色(颜色反应);淀粉与I 作用显蓝色。
3 2
(3)有机物的检验方法
物质 试剂与方法 现象与结论
饱和烃与不饱和烃 加入溴水或酸性KMnO 溶液
4
苯与苯的同系物 加酸性KMnO 溶液
4
加银氨溶液、水浴加热
醛基化合物
加新制的Cu(OH) 、加热
2
醇 加乙酸、浓硫酸
FeCl 溶液
3
酚
浓溴水
加NaCO 溶液
2 3
羧酸
加紫色石蕊溶液
淀粉 加碘水
蛋白质 灼烧加浓硝酸微热
(1)向某溶液中加入BaCl 溶液,有白色沉淀生成,再加入稀盐酸,沉淀不消失,则溶液中一定存在 SO(
2
)
(2)向某溶液中加入Ba(NO ) 溶液,产生不溶于稀HNO 的白色沉淀,则溶液中一定存在SO(
3 2 3
)
(3)向某溶液中加入Ca(OH) 溶液,有白色沉淀生成,则溶液中一定存在CO( )
2
(4)某溶液的焰色反应呈黄色,则溶液中一定有钠元素,不能确定是否有钾元素( )
(5)无色溶液加入CCl 无现象,滴加氯水后CCl 层呈紫红色,则溶液中一定存在I-( )
4 4
(6)向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体,溶液中一定存在CO( )
(7)向某溶液加入稀NaOH溶液,用湿润的红色石蕊试纸检验,不变蓝,则原溶液中不含NH( )
(8)向某溶液加入BaCl 溶液有白色沉淀生成,则原溶液中一定含CO( )
2
(9)向Fe(OH) 胶体中逐滴加入稀盐酸,实验现象为胶体溶解。( )
3
(10)检验某溶液中存在HSO的实验操作为取少量该溶液,滴加少量BaCl 溶液,无明显现象,再滴加过
2
量稀硝酸,若产生白色沉淀,说明含有HSO( )
1.离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施
SO
Cl- CO
OH-
CO
SO SO
Ag+
SO CO
CO SO
2.某含碘废水(pH约为8)中一定存在I,可能存在I-、IO中的一种或两种。请补充完整检验含碘废
2
水中是否含有I-、IO的实验方案:取适量含碘废水,用CCl 多次萃取、分液直到水层用淀粉溶液检验
4
不出有碘单质存在;____________________________________________________________。
已知:5SO+2IO+2H+===I +5SO+HO;可供选择的试剂:稀盐酸、淀粉溶液、FeCl 溶液、
2 2 3
NaSO 溶液。
2 3
3.按要求回答下列问题。
(1)结晶析出NaSO·5H O,其中可能含有NaSO 、NaSO 等杂质。利用所给试剂设计实验,检验
2 2 3 2 2 3 2 4
产品中是否存在NaSO ,简要说明实验操作、现象和结论:______________________________________
2 4__________________________________________________________________。
已知:NaSO·5H O遇酸易分解:SO+2H+===S↓+SO ↑+HO;
2 2 3 2 2 2 2
可供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl 溶液、AgNO 溶液。
2 3
(2)榴石矿石可以看作由CaO、FeO、Fe O 、Al O 、SiO 组成。试设计实验证明榴石矿石中含有
2 3 2 3 2
FeO(试剂任选,说明实验操作与现象):
_______________________________________________________________________________。