文档内容
第 01 讲 电离平衡
目录
01
考情透视·目标导航
02 知识导图·思维引航...................................................................................................................
03考点突破·考法探究....................................................................................................................
考点一 弱电解质的电离平衡.......................................................................................................
知识点1 弱电解质.....................................................................................................................
知识点2 弱电解质的电离平衡....................................................................................................
考向1 强、弱电解质及判断........................................................................................................
考向2 弱电解质的电离平衡........................................................................................................
考点二 电离平衡常数...................................................................................................................
知识点1 电离平衡常数............................................................................................................
知识点2 电离度.......................................................................................................................
考向1 电离平衡常数及其应用..................................................................................................
考向2 电离平衡常数等有关计算...............................................................................................
考点三 强酸(碱)和弱酸(碱)稀释图像..........................................................................................
知识点1 等体积、等浓度的盐酸、醋酸.............................................................................
知识点2 相同体积、相同pH的盐酸、醋酸......................................................................
知识点3 pH与稀释倍数的线性关系...................................................................................
考向1 酸或碱溶液的起始浓度相同.....................................................................................
考向2 酸或碱溶液的起始pH相同.......................................................................................
04真题练习·命题洞见....................................................................................................................考点要
考题统计 考情分析
求
2024·湖南卷13题,3分;2024·全
国新课标卷7题,3分;2024·河北
卷11题,3分;2023湖北卷12
强弱电解质 弱电解质的电离是中学化学基本理论中的重要
题,3分;2022江苏卷12题,3
比较 组成部分,也是学习中比较难理解的内容,更是近
分;2021浙江1月选考17题,2
几年高考命题的必考内容。高考命题热点主要集中
分;2021浙江6月选考19题,2
于影响弱电解质电离平衡的因素,通过图像分析
分;
强、弱电解质,电离常数和电离度,比较微粒浓度
2024·江苏卷12题,3分;2023湖
大小和pH的计算等,命题有时会与水解相结合增
加试题的难度。能用动态平衡的观点分析电离平
北卷14题,3分;2023浙江6月
衡,解决以图像或者文字的形式考查的平衡问题,
选考15题,3分;2022浙江1月
电离平衡常 根据溶液中离子浓度的大小变化,推断反应的原理
选考17题,2分;2022全国乙卷
数应用 和变化的强弱,提高证据推理能力。
13题,6分;2022湖北卷15题,
3分;2022辽宁卷15题,3分;
2021山东卷15题,4分;
复习目标:
1.了解电解质的概念,了解强电解质和弱电解质的概念。
2.理解电解质在水中的电离以及电解质溶液的导电性。
3.理解弱电解质在水中的电离平衡,能利用电离平衡常数进行相关计算。考点一 弱电解质的电离平衡
知识点1 弱电解质
1.概念
2.与化合物类型的关系
强电解质主要是大部分离子化合物及某些______化合物;弱电解质主要是某些_______化合物。
【名师点晴】
1.电解质导电的条件
电解质的导电条件是在水溶液中或高温熔融状态,共价化合物只能在水溶液中导电,离子化合物在熔
融状态和溶液中均可导电。
2.导电性强弱
知识点2 弱电解质的电离平衡
1.电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率______时,
电离过程达到了平衡。
3.外因对电离平衡的影响
以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOHCHCOO-+H+ ΔH>0的影响。
3 3 3
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 ______ ______ ______ ______
加入少量冰醋酸 向右 ______ ______ ______ ______
通入HCl(g) 向左 ______ ______ ______ ______
加NaOH(s) 向右 ______ ______ ______ ______
加CHCOONa(s) 向左 ______ ______ ______ ______
3
升高温度 向右 ______ ______ ______ ______
【名师提醒】
1.浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
2.温度:温度越高,电离程度越大。
3.同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的
方向移动。
4.化学反应:加入能与弱电解质电离出的离子反应的物质时,可使电离平衡向电离方向移动。考向1 强、弱电解质及判断
【例1】某同学拟用pH计测定溶液pH以探究某酸HR是否为弱电解质。下列说法正确的是( )。
A.25 ℃时,若测得0.01 mol·L-1NaR溶液的pH=7,则HR是弱酸
B.25 ℃时,若测得0.01 mol·L-1HR溶液的pH>2且pH<7,则HR是弱酸
C.25 ℃时,若测得HR溶液的pH=a,取该溶液10.0 mL,加蒸馏水稀释至100.0 mL,测得pH=b,b-
a<1,则HR是弱酸
D.25 ℃时,若测得NaR溶液的pH=a,取该溶液10.0 mL,升温至50 ℃,测得pH=b,a>b,则HR
是弱酸
【思维建模】
强电解质和弱电解质的证明实验(以证明某酸(HA)为弱酸为例)
实验方法 结论
(1)测0.01 mol·L-1 HA溶液的pH pH=2,HA为强酸;pH>2,HA为弱酸
(2)测NaA溶液的pH pH=7,HA为强酸;pH>7,HA为弱酸
(3)相同条件下,测相同浓度的HA和HCl溶 导电性相同,HA为强酸;导电性弱于盐
液的导电性 酸,HA为弱酸
(4)往同浓度的HA和HCl溶液中投入大小相 开始反应速率相同,HA为强酸;开始反应
同的Zn粒或CaCO 固体 速率比盐酸慢,HA为弱酸
3
(5)测相同pH的HA与HCl稀释相同倍数前 pH变化倍数相同,HA为强酸;pH变化倍数
后的pH变化 小于盐酸,HA为弱酸
【变式训练】.鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用GHCl表示)。已知GHCl水溶
液呈酸性,下列叙述正确的是( )
A.0.001 mol·L-1 GHCl水溶液的pH=3
B.0.001 mol·L-1 GHCl水溶液加水稀释,pH升高
C.GHCl在水中的电离方程式:GHCl=G+HCl
D.GHCl水溶液中:c(OH-)+c(Cl-)=c(GH+)+c(G)
考向2 弱电解质的电离平衡
【例2】(2024·天津市第二十中学高三第二次月考)25℃时,对于pH=2的CHCOOH溶液,下列判断不
3
正确的是( )
A.加水稀释,电离平衡正向移动,溶液中所有离子浓度都减小
B.通入少量HCl气体,电离平衡逆向移动,c(CHCOO-)减小,K 不变
3 a
C.加入少量冰醋酸,电离平衡正向移动,c(H+)增大,电离度减小D.升高温度,电离平衡正向移动,c(H+)增大,pH减小
【名师提醒】
外界条件对电离平衡影响的四个不一定:
1.加水稀释时,溶液中不是所有离子的浓度都减小;稀醋酸加水稀释时,溶液中的 c(H+)减小,
c(OH-)增大。
2.电离平衡右移,电离程度不一定增大,如增大弱电解质的浓度,使电离平衡向右移动,但电离程
度减小。
3.电离平衡右移,电解质分子的浓度不一定减小,如对于 CHCOOH CHCOO-+H+,平衡后,加
3 3
入冰醋酸,c(CHCOOH)增大,平衡右移,根据勒夏特列原理,只能“减弱”而不能消除,再次平衡时,
3
c(CHCOOH)比原平衡时大。
3
4.电离平衡右移,离子的浓度不一定增大,如在CHCOOH溶液中加水稀释或加少量NaOH固体,都
3
会引起平衡右移,但c(CHCOOH)、c(H+)都比原平衡时要小。
3
【变式训练】25 ℃时,醋酸溶液中存在电离平衡:CHCOOH CHCOO-+ H+。下列说法正确的是(
3 3
)。
A.向体系中加入少量CHCOONa固体,平衡向左移动,c(CHCOO-)减小
3 3
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动
考点二 电离平衡常数
知识点1 电离平衡常数
1.表达式
(1)一元弱酸HA的电离常数:根据HA H++A-,可表示为____________。
(2)一元弱碱BOH的电离常数:根据BOH B++OH-,可表示为____________。
2.特点
(1)电离平衡常数与______有关,与浓度无关,升高温度,K值______。
(2)电离平衡常数反映弱电解质的____________,K越大,表示弱电解质越易______,酸性或碱性
______。
(3)多元弱酸的各级电离常数的大小关系是K K K ……,故其酸性取决于______电离。
1 2 3
3.电离平衡常数的应用
≫ ≫
(1)判断弱酸(或弱碱)的相对强弱,电离常数越______,酸性(或碱性)越______。(2)判断盐溶液的酸性(或碱性)强弱:电离常数越______,对应的盐水解程度越______,酸性(或碱性)
越______。
(3)判断复分解反应能否发生:一般符合“强酸制弱酸”规律。
(4)判断微粒浓度或浓度比值的变化:利用温度不变电离常数就不变来判断溶液中微粒浓度或者比值的
变化情况,有时候还会结合 K 一起进行判断,如:0.1 mol·L-1 CHCOOH 溶液中加水稀释,
w 3
c(CH COO-) c(CH COO-)·c(H+) K
3 = 3 = a ,加水稀释,c(H+)______,K 值______,则
c(CH COOH) c(CH COOH)·c(H+) c(H+) a
3 3
c(CH COO-)
3 ______。
c(CH COOH)
3
【名师提醒】
1.电离平衡常数表达式中离子浓度指达到平衡时溶液中存在的离子浓度,不一定是弱电解质自身电
离的,可以对比水的离子积去掌握。
2.电离度与温度和浓度均有关,电离平衡常数只与温度有关。
知识点2 电离度
1.概念
在一定条件下的弱电解质达到______平衡时,已经电离的电解质分子数占_______________的百分比。
2.表示方法
α=×100%
也可表示为α=×100%
3.影响因素
(1)相同温度下,同一弱电解质,浓度越大,其电离度(α)越______。
(2)相同浓度下,同一弱电解质,温度越高,其电离度(α)越______。
4.电离度与平衡常数的关系
电离平衡常数与电离度(α)的关系(以一元弱酸为例)
HA H+ + A-
起始: c 0 0
酸
转化: c ·α c ·α c ·α
酸 酸 酸
平衡: c ·(1-α) c ·α c ·α
酸 酸 酸
K==,α很小,可认为1-α≈1,则K=______或α=。
a a
【思维建模】
电离常数的4大应用
电离常数越大,酸性(或碱性)越强。如:常温下,CHCOOH的K=1.
3 a
判断弱酸(或弱 8×10-5,HCO 的K =4.3×10-7、K =5.6×10-11。
2 3 a1 a2
碱)的相对强弱
则酸性:CHCOOH>H CO>HCO
3 2 3
电离常数越大,对应的盐水解程度越小,碱性(或酸性)越弱。如:利用
判断盐溶液的酸
上面电离常数的数值可知等浓度的CHCOONa、NaHCO 、NaCO 溶液
3 3 2 3性(或碱性)强弱 的pH由大到小的顺序为NaCO>NaHCO>CH COONa
2 3 3 3
一般符合“强酸制弱酸”规律。如:利用上面中电离常数的数值可知,
判断复分解反应
向NaCO 溶液中加入足量CHCOOH的离子方程式为CO+
能否发生 2 3 3
2CHCOOH===2CH COO-+HO+CO↑
3 3 2 2
弱电解质加水稀释时,能促进弱电解质的电离,溶液中离子和分子的浓
判断微粒浓度比 度会发生相应的变化,但电离常数不变,题目中经常利用电离常数来判
值的变化 断溶液中微粒浓度比值的变化情况。如把0.1 mol·L-1 CHCOOH溶液加
3
水稀释,==稀释时,c(H+)减小,K 值不变,则变大
a
考向1 电离平衡常数及其应用
【例1】(2024·河北省高三大数据应用调研联合测评)已知电离常数:K(HCN)=5.8×10-10,
a
K(HF)=6.9×10-4,K (H CO)=4.2×10-7,K (H CO))=4.7×10-11,下列离子方程式书写正确的是( )
a a1 2 3 a2 2 3
A.向NaHCO 溶液中滴加HCN:HCO -+HCN=CN-+CO+H O
3 3 2 2
B.向NaCO 溶液中通入过量HF:CO2-+HF=F-+ HCO-
2 3 3 3
C.向NaHCO 和NaCN混合溶液中通入少量HF:
3
D.向NaCN溶液中通入少量CO:2CN- + CO+H O=2HCN+CO 2-
2 2 2 3
【易错警示】
(1)判断强酸制弱酸的离子方程式正误时,若产物的物质之间还能发生反应,该离子方程式一定错误。
(2)强酸制弱酸原理只适用于复分解反应型离子反应。
【变式训练】(2024·湖北省第九届高三三模)已知溶剂分子结合H+的能力会影响酸给出H+的能力,某
温度下部分酸在冰醋酸中的pK 如下表所示,下列说法错误的是( )
a
分子式 HClO HSO HCl HNO
4 2 4 3
4.87 7.24(一级) 8.9 9.4
A.HClO 在冰醋酸中的电离方程式:HClO+CH COOH ClO -+CH COOH +
4 4 3 4 3 2
B.在冰醋酸中酸性:HClO>HSO >HCl>HNO
4 2 4 3
C.结合H+的能力:HO>CHCOOH
2 3
D.相同温度下醋酸在液氨中的pK 大于其在水中的pK
a a
考向2 电离平衡常数等有关计算
【例2】按要求回答下列问题。
(1)已知室温下HA的电离平衡常数K =1.0×10-5,则100mL0.lmol·L-1HA溶液中,HA的电离度为
a
。(2)已知次氯酸(HClO)的电离平衡常数为K=4.0×10-8,向20mL0.1mol•L-1的HClO溶液中滴加少量硫酸,
a
再加水稀释至40mL,此时测得c(H+)=0.05mol•L-1,则溶液中c(ClO-)= mol•L-1。
(3)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为
(已知:NH+H+ NH+的 ; )。联氨与硫酸形成的酸式盐的化学式为
2 4 2 5
。
(4)已知25℃,NH ·H O的K =1.8×10-5,HSO 的K =1.3×10-2,K =6.2×10-8。若氨水的浓度为
3 2 b 2 3 a1 a2
2.0mol·L-1,则溶液中的c(OH-)= mol·L-1。HSO 的电离常数表达式K= 。将SO 通
2
入该氨水中,当溶液中c(H+)为1.0×10-7mol·L-1时,溶液中的 = 。
【思维建模】
(1)已知c(HX)和c(H+),求电离平衡常数
HX H+ + X-
起始:c(HX) 0 0
平衡:c(HX)-c(H+) c(H+) c(H+)
则K=
c2(H+)
。由于弱酸只有极少一部分电离,c(H+)的数值很小,因此可做近似处理:
c(HX)-c(H+)
c2(H+)
c(HX)-c(H+)≈c(HX)。则K= ,代入数值求解即可。
c(HX)
(2)已知c(HX)和电离平衡常数,求c(H+)
HX H+ + X-
起始: c(HX) 0 0
平衡: c(HX)-c(H+) c(H+) c(H+)
则K=
c2(H+)
。由于K值很小,c(H+)的数值很小,可做近似处理:c(HX)-c(H+)≈c(HX),则
c(HX)-c(H+)
c(H+)=√K·c(HX),代入数值求解即可。
【变式训练】(1)碳氢化合物完全燃烧生成CO 和HO。常温常压下,空气中的CO 溶于水,达到平衡
2 2 2
时,溶液的pH=5.60,c(H CO)=1.5×10-5 mol·L-1。若忽略水的电离及HCO 的第二级电离,则HCO
2 3 2 3 2 3HC +H+的电离常数K = (已知:10-5.60=2.5×10-6)。
O- 1
3
(2)已知室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,此酸的电离常数约为 。
(3)在 25 ℃下,将 a mol·L-1的氨水与 0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中 c(N
H+
4
)=c(Cl-),则溶液显 (填“酸”、“碱”或“中”)性;用含a的代数式表示NH ·H O的电离常数K =
3 2 b
。
(4)常温下,将 a mol·L-1的醋酸与 b mol·L-1Ba(OH) 溶液等体积混合,充分反应后,溶液中存在
2
2c(Ba2+)=c(CHCOO-),则该混合溶液中醋酸的电离常数K= (用含a和b的代数式表示)。
3 a
(5)25 ℃时,向含a mol NH NO 的溶液中滴加b L氨水,溶液呈中性,则所滴加氨水的浓度为
4 3
mol·L-1。[已知K (NH ·H O)=2×10-5]
b 3 2
考点三 强酸(碱)和弱酸(碱)稀释图像
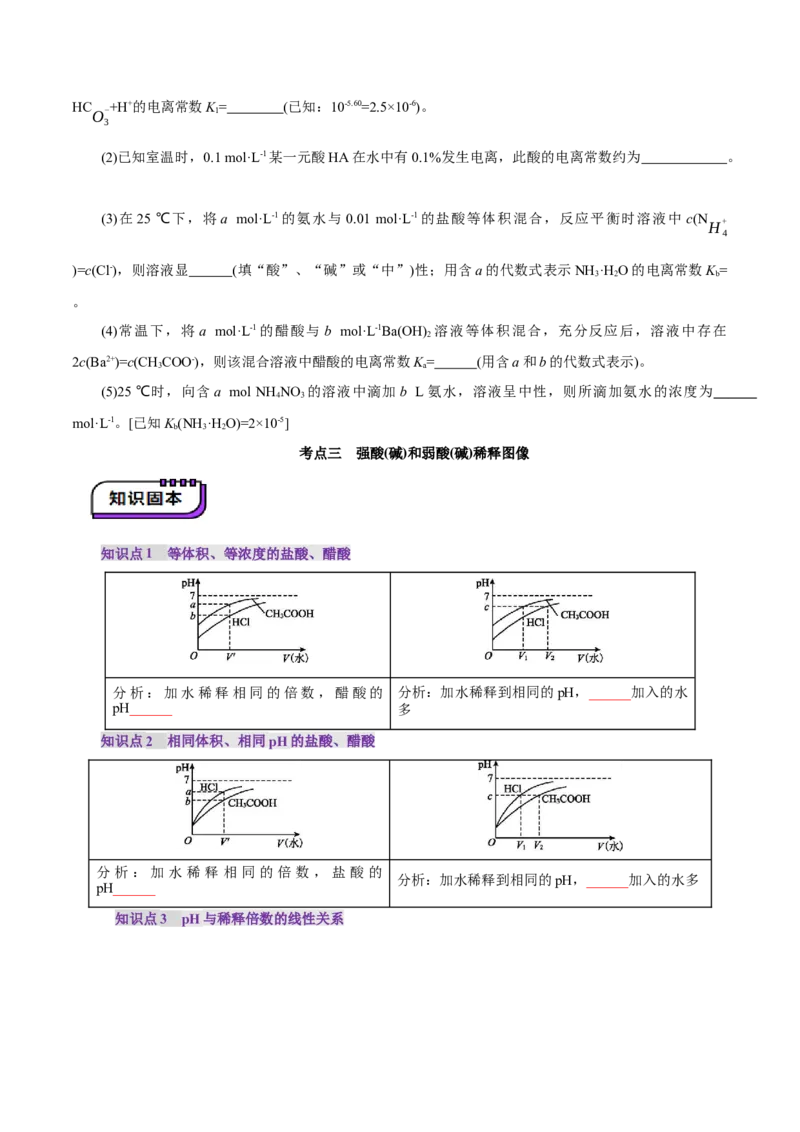
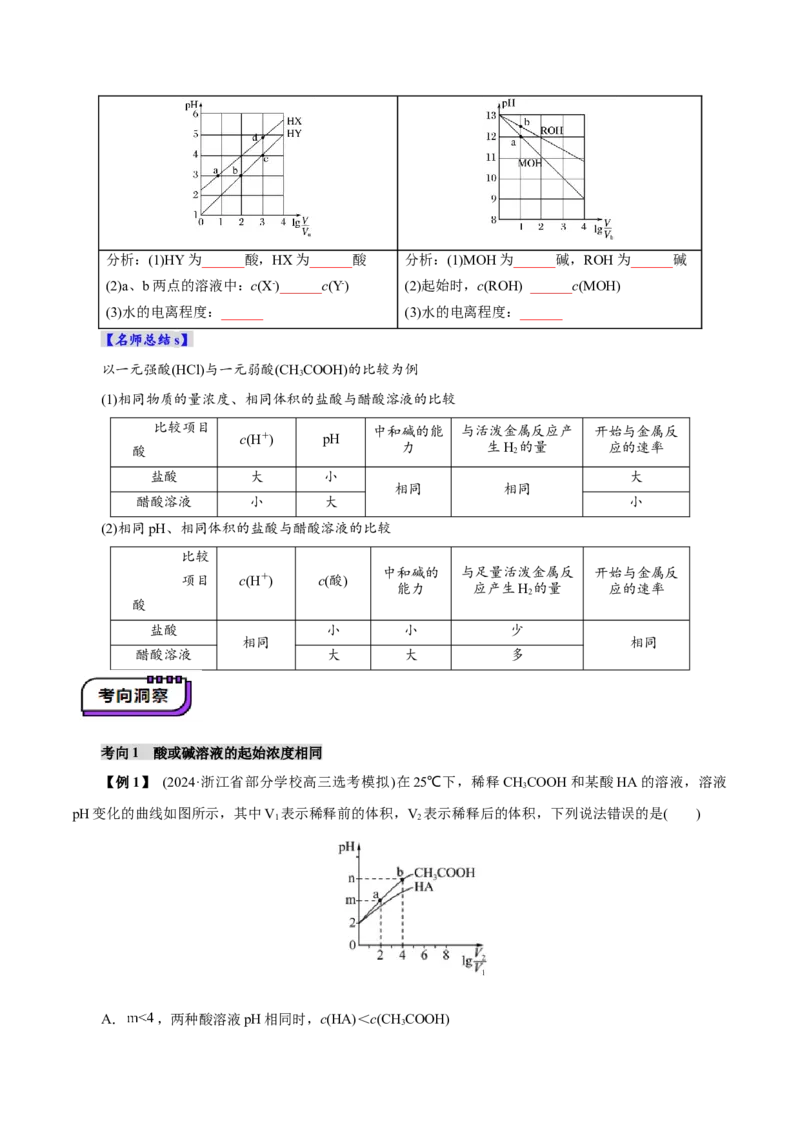
知识点1 等体积、等浓度的盐酸、醋酸
分析:加水稀释相同的倍数,醋酸的 分析:加水稀释到相同的pH,______加入的水
pH______ 多
知识点2 相同体积、相同pH的盐酸、醋酸
分析:加水稀释相同的 倍数,盐酸的
分析:加水稀释到相同的pH,______加入的水多
pH______
知识点3 pH与稀释倍数的线性关系分析:(1)HY为______酸,HX为______酸 分析:(1)MOH为______碱,ROH为______碱
(2)a、b两点的溶液中:c(X-)______c(Y-) (2)起始时,c(ROH) ______c(MOH)
(3)水的电离程度:______ (3)水的电离程度:______
【名师总结s】
以一元强酸(HCl)与一元弱酸(CHCOOH)的比较为例
3
(1)相同物质的量浓度、相同体积的盐酸与醋酸溶液的比较
比较项目 中和碱的能 与活泼金属反应产 开始与金属反
c(H+) pH
酸
力 生H
2
的量 应的速率
盐酸 大 小 大
相同 相同
醋酸溶液 小 大 小
(2)相同pH、相同体积的盐酸与醋酸溶液的比较
比较
中和碱的 与足量活泼金属反 开始与金属反
项目 c(H+) c(酸)
能力 应产生H 的量 应的速率
2
酸
盐酸 小 小 少
相同 相同
醋酸溶液 大 大 多
考向1 酸或碱溶液的起始浓度相同
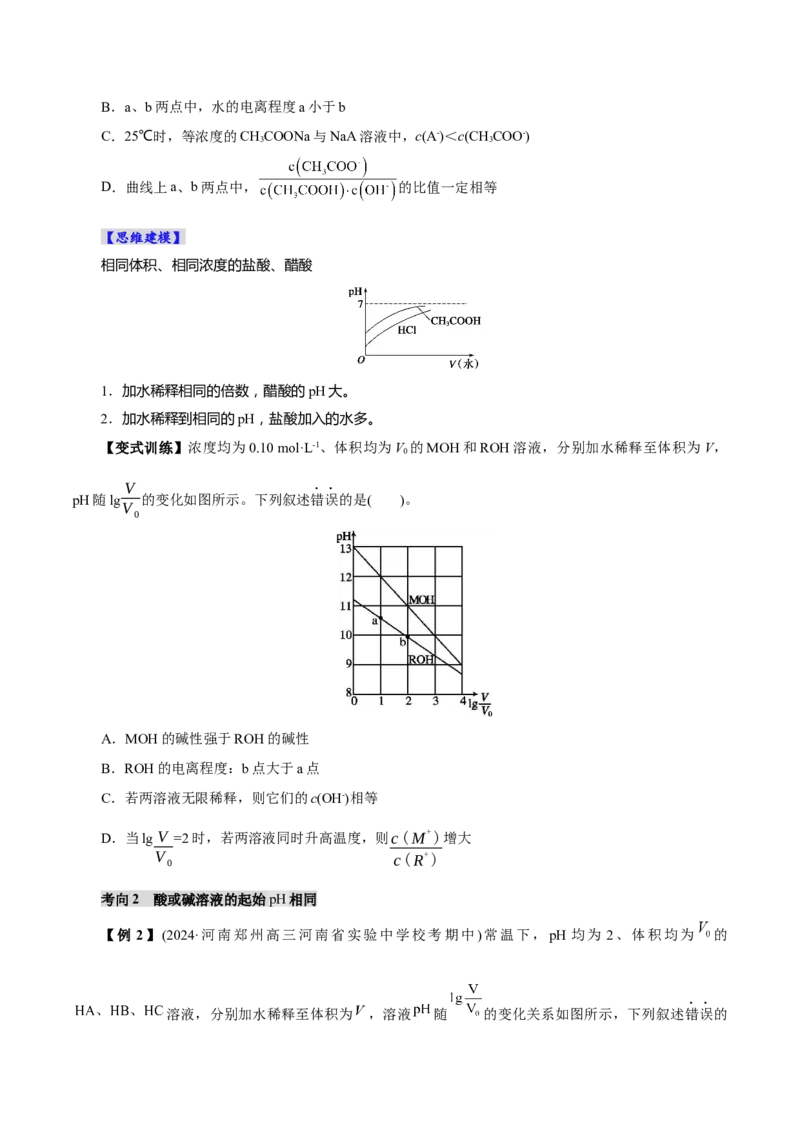
【例1】 (2024·浙江省部分学校高三选考模拟)在25℃下,稀释CHCOOH和某酸HA的溶液,溶液
3
pH变化的曲线如图所示,其中V 表示稀释前的体积,V 表示稀释后的体积,下列说法错误的是( )
1 2
A. ,两种酸溶液pH相同时,c(HA)<c(CHCOOH)
3B.a、b两点中,水的电离程度a小于b
C.25℃时,等浓度的CHCOONa与NaA溶液中,c(A-)<c(CHCOO-)
3 3
D.曲线上a、b两点中, 的比值一定相等
【思维建模】
相同体积、相同浓度的盐酸、醋酸
1.加水稀释相同的倍数,醋酸的pH大。
2.加水稀释到相同的pH,盐酸加入的水多。
【变式训练】浓度均为0.10 mol·L-1、体积均为V 的MOH和ROH溶液,分别加水稀释至体积为V,
0
V
pH随lg 的变化如图所示。下列叙述错误的是( )。
V
0
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点
C.若两溶液无限稀释,则它们的c(OH-)相等
D.当lg V =2时,若两溶液同时升高温度,则c(M+)增大
V c(R+)
0
考向2 酸或碱溶液的起始pH相同
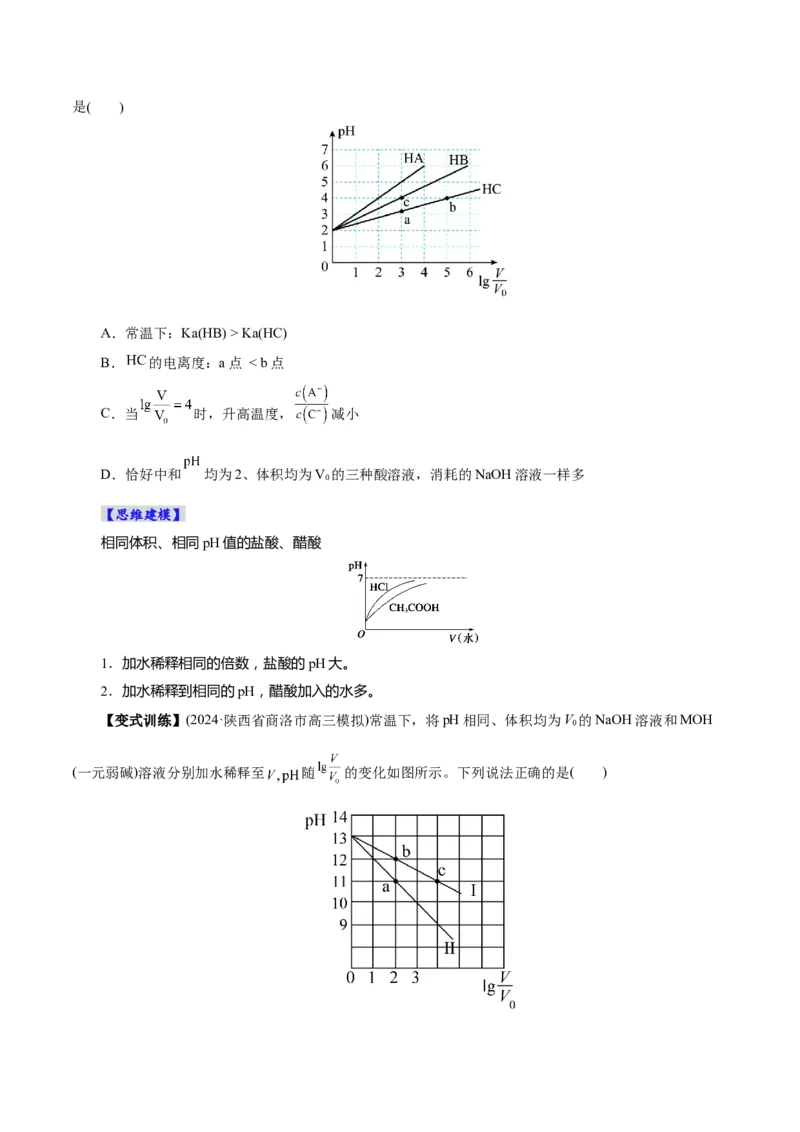
【例 2】(2024·河南郑州高三河南省实验中学校考期中)常温下,pH 均为 2、体积均为 的
溶液,分别加水稀释至体积为 ,溶液 随 的变化关系如图所示,下列叙述错误的是( )
A.常温下:Ka(HB) > Ka(HC)
B. 的电离度:a点 < b点
C.当 时,升高温度, 减小
D.恰好中和 均为2、体积均为V 的三种酸溶液,消耗的NaOH溶液一样多
0
【思维建模】
相同体积、相同pH值的盐酸、醋酸
1.加水稀释相同的倍数,盐酸的pH大。
2.加水稀释到相同的pH,醋酸加入的水多。
【变式训练】(2024·陕西省商洛市高三模拟)常温下,将pH相同、体积均为V 的NaOH溶液和MOH
0
(一元弱碱)溶液分别加水稀释至 随 的变化如图所示。下列说法正确的是( )A.曲线Ⅰ表示NaOH溶液
B.未稀释前,c(Na+)= c(M+)>c(MOH)
C.a,c两点溶液的离子总浓度相同
D.加水稀释过程中, 逐渐增大
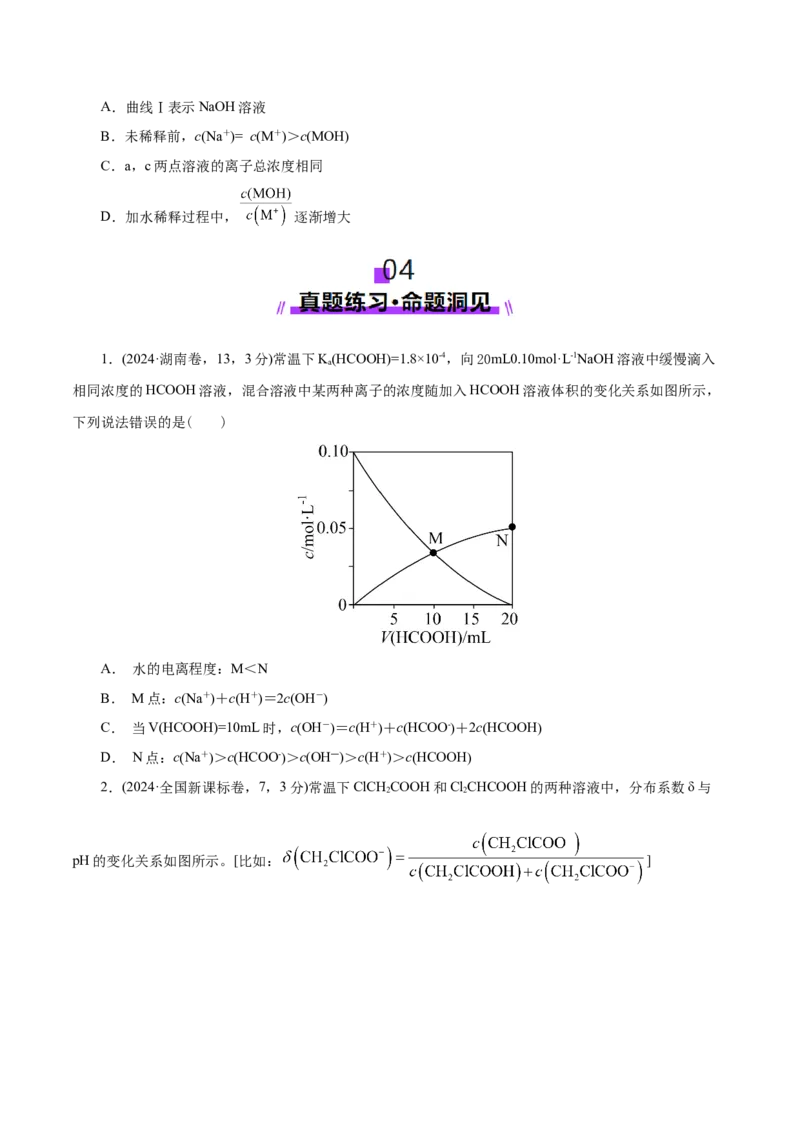
1.(2024·湖南卷,13,3分)常温下K(HCOOH)=1.8×10-4,向20mL0.10mol·L-1NaOH溶液中缓慢滴入
a
相同浓度的HCOOH溶液,混合溶液中某两种离子的浓度随加入HCOOH溶液体积的变化关系如图所示,
下列说法错误的是( )
A. 水的电离程度:M<N
B. M点:cNa++cH+=2cOH-
C. 当V(HCOOH)=10mL时,cOH-=cH++cHCOO-+2cHCOOH
D. N点:cNa+>cHCOO->c(OH―)>c(H+)>cHCOOH
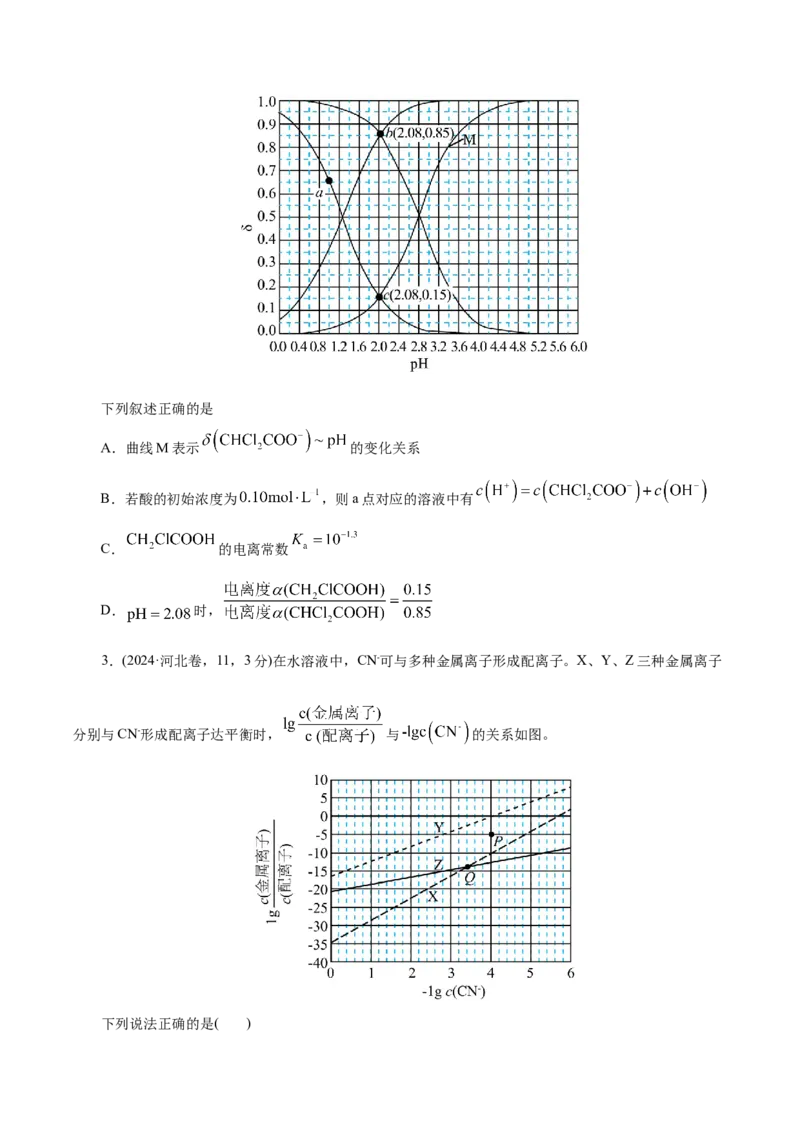
2.(2024·全国新课标卷,7,3分)常温下ClCHCOOH和ClCHCOOH的两种溶液中,分布系数δ与
2 2
pH的变化关系如图所示。[比如: ]下列叙述正确的是
A.曲线M表示 的变化关系
B.若酸的初始浓度为 ,则a点对应的溶液中有
C. 的电离常数
D. 时,
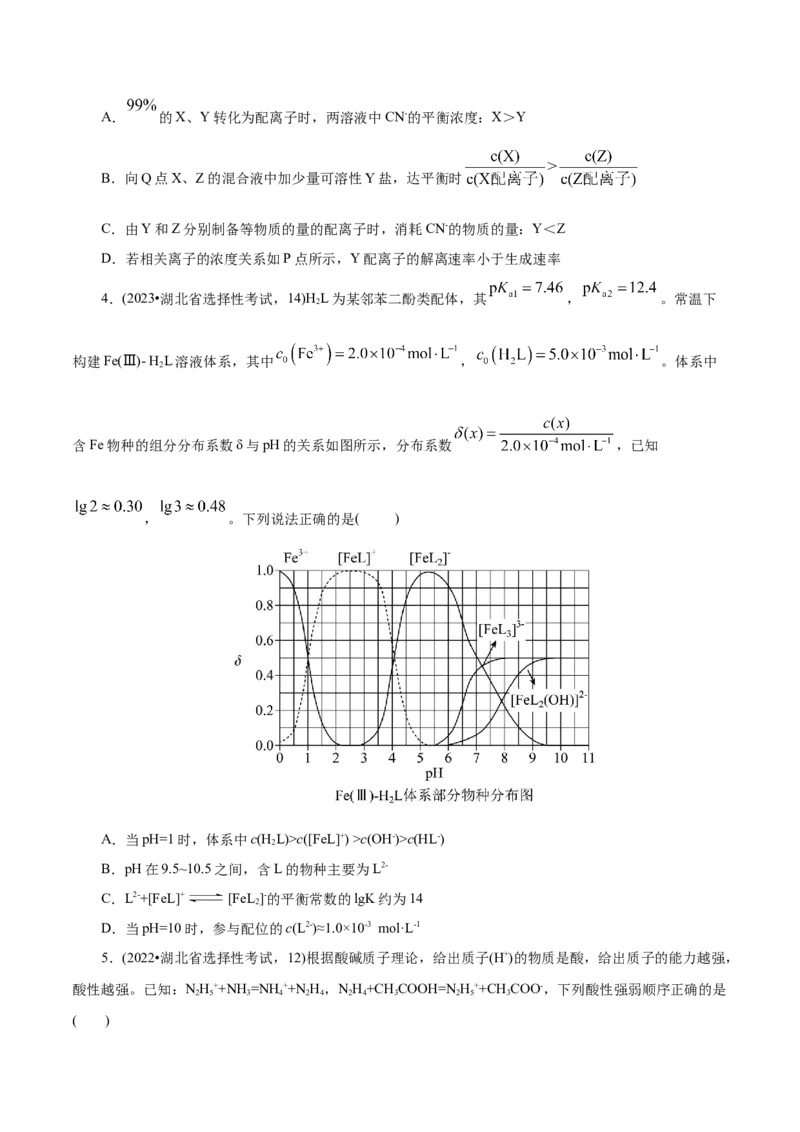
3.(2024·河北卷,11,3分)在水溶液中,CN-可与多种金属离子形成配离子。X、Y、Z三种金属离子
分别与CN-形成配离子达平衡时, 与 的关系如图。
下列说法正确的是( )A. 的X、Y转化为配离子时,两溶液中CN-的平衡浓度:X>Y
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时
C.由Y和Z分别制备等物质的量的配离子时,消耗CN-的物质的量:Y<Z
D.若相关离子的浓度关系如P点所示,Y配离子的解离速率小于生成速率
4.(2023•湖北省选择性考试,14)H L为某邻苯二酚类配体,其 , 。常温下
2
构建Fe(Ⅲ)- H L溶液体系,其中 , 。体系中
2
含Fe物种的组分分布系数δ与pH的关系如图所示,分布系数 ,已知
, 。下列说法正确的是( )
A.当pH=1时,体系中c(H L)>c([FeL]+) >c(OH-)>c(HL-)
2
B.pH在9.5~10.5之间,含L的物种主要为L2-
C.L2-+[FeL]+ [FeL ]-的平衡常数的lgK约为14
2
D.当pH=10时,参与配位的c(L2-)≈1.0×10-3 mol·L-1
5.(2022•湖北省选择性考试,12)根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,
酸性越强。已知:NH++NH=NH++N H,NH+CH COOH=N H++CH COO-,下列酸性强弱顺序正确的是
2 5 3 4 2 4 2 4 3 2 5 3
( )A.NH+>NH>NH + B.NH+>CHCOOH>NH +
2 5 2 4 4 2 5 3 4
C.NH >NH>CHCOO- D.CHCOOH>NH+>NH +
3 2 4 3 3 2 5 4
3.(2022•全国乙卷)常温下,一元酸 的K(HA)=1.0×10-3。在某体系中, 与A-离子不能穿过隔膜,
a
未电离的 可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
6.(2022·浙江省1月选考,17)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确
2 a1 a2
的是( )
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为
2 2
0.013%
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
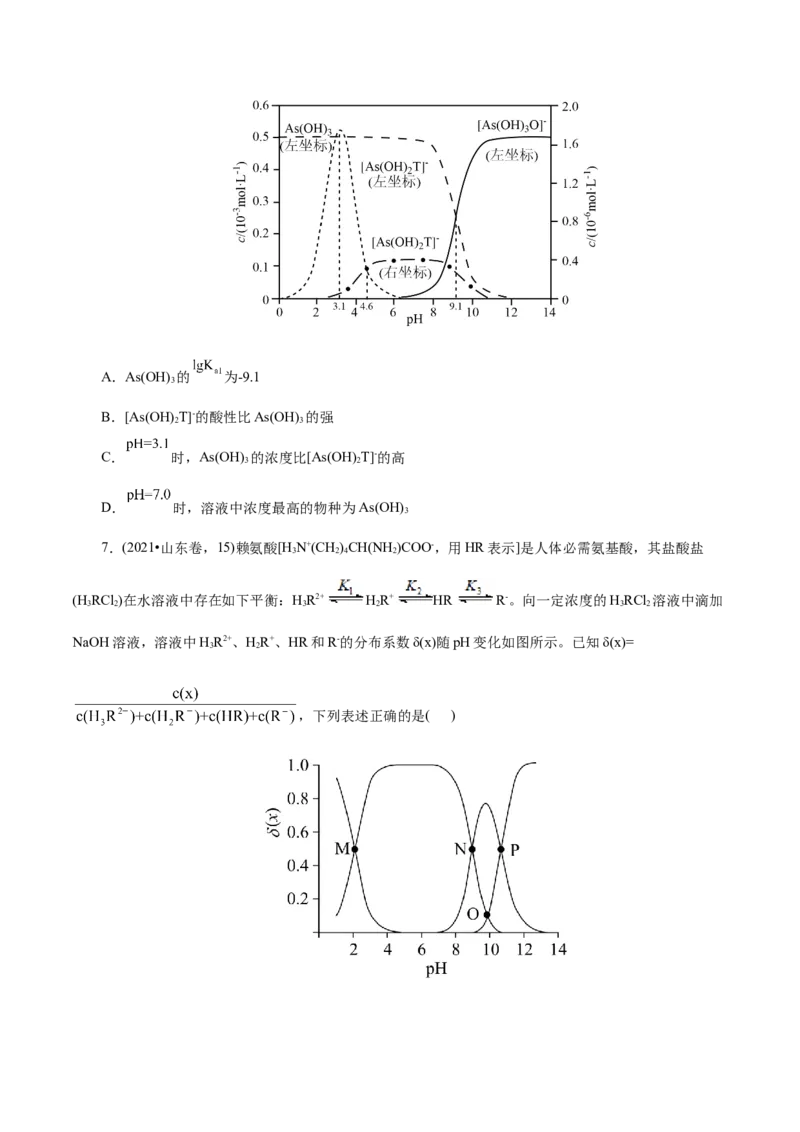
5.(2022•湖北省选择性考试,15)下图是亚砷酸As(OH) 和酒石酸 混合
3
体系中部分物种的 图(浓度:总 为 ,总T为 )。下列说法错误的是(
)A.As(OH) 的 为-9.1
3
B.[As(OH) T]-的酸性比As(OH) 的强
2 3
C. 时,As(OH) 的浓度比[As(OH) T]-的高
3 2
D. 时,溶液中浓度最高的物种为As(OH)
3
7.(2021•山东卷,15)赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,其盐酸盐
3 2 4 2
(H RCl )在水溶液中存在如下平衡:HR2+ HR+ HR R-。向一定浓度的HRCl 溶液中滴加
3 2 3 2 3 2
NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是( )A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)