文档内容
第 02 讲 原电池、化学电源
目录
01
考情透视·目标导航
02 知识导图·思维引航...................................................................................................................
03考点突破·考法探究....................................................................................................................
考点一 原电池的工作原理...........................................................................................................
知识点1 原电池的概念及构成条件.............................................................................................
知识点2 原电池的应用..............................................................................................................
考向1 原电池的工作原理.........................................................................................................
考向2 原电池电极判断及电极反应的书写.................................................................................
考向3 “盐桥”的作用与化学平衡的移动....................................................................................
考点二 化学电源...........................................................................................................................
知识点1 一次电池、二次电池电极反应式的书写......................................................................
知识点2 燃料电池...................................................................................................................
考向1 一次电池.......................................................................................................................
考向2 二次电池.......................................................................................................................
考向3 燃料电池.......................................................................................................................
04真题练习·命题洞见....................................................................................................................
04真题练习·命题洞见....................................................................................................................
考点要求 考题统计 考情分析2024·江苏卷8题,3分;2024·北京卷3
题,3分;2023广东卷6题,2分;2023
电化学知识是中学化学中的重要基本概
原电池原理 山东卷11题,4分;2022全国甲卷12
念,也是近年来高考化学的持续热点,在复
综合应用 题,6分;2022山东卷13题,4分;
杂、陌生、新颖的研究对象和真实问题情境
2021广东卷9题,2分;2021山东卷10
下,体现了对电化学知识基础性、综合性、
题,2分;
创新性和应用性的考查。近年高考中对电化
学的考查出现了新的变化,以装置图为载体
2024·安徽卷11题,3分;2024·全国甲
来考查电化学的相关知识,成为近年高考的
卷6题,3分;2024·河北卷13题,3
新亮点,考查的关键能力侧重于两个方面:
分;2023辽宁卷11题,3分;2023全国
一是理解与辨析能力,要求学生能够从图示
甲卷10题,6分;2022辽宁卷14题,3
新型二次电 电化学装置中提取有效信息,判断装置种
分;2022福建卷9题,4分;2021河北
池 类、辨别电极名称等;二是分析与推理能
卷9题,3分;2021辽宁卷10题,3
力,要求学生能够根据图示信息和电解池的
分;2021浙江1月选考22题,2分; 工作原理,分析电极反应的类型、电解质的
2021浙江6月选考22题,2分;2021湖 作用、离子的移动方向以及定量分析转移电
南卷10题,3分; 子的物质的量等。
燃料电池 2024·全国新课标卷6题,3分
复习目标:
1.理解原电池的构成、工作原理及应用,正确判断原电池的两极,能书写电极反应式和总反应方
程式。
2.了解常见化学电源的种类及其工作原理;了解燃料电池的应用。体会研制新型电池的重要性。
3.能够认识和书写新型化学电源的电极反应式。
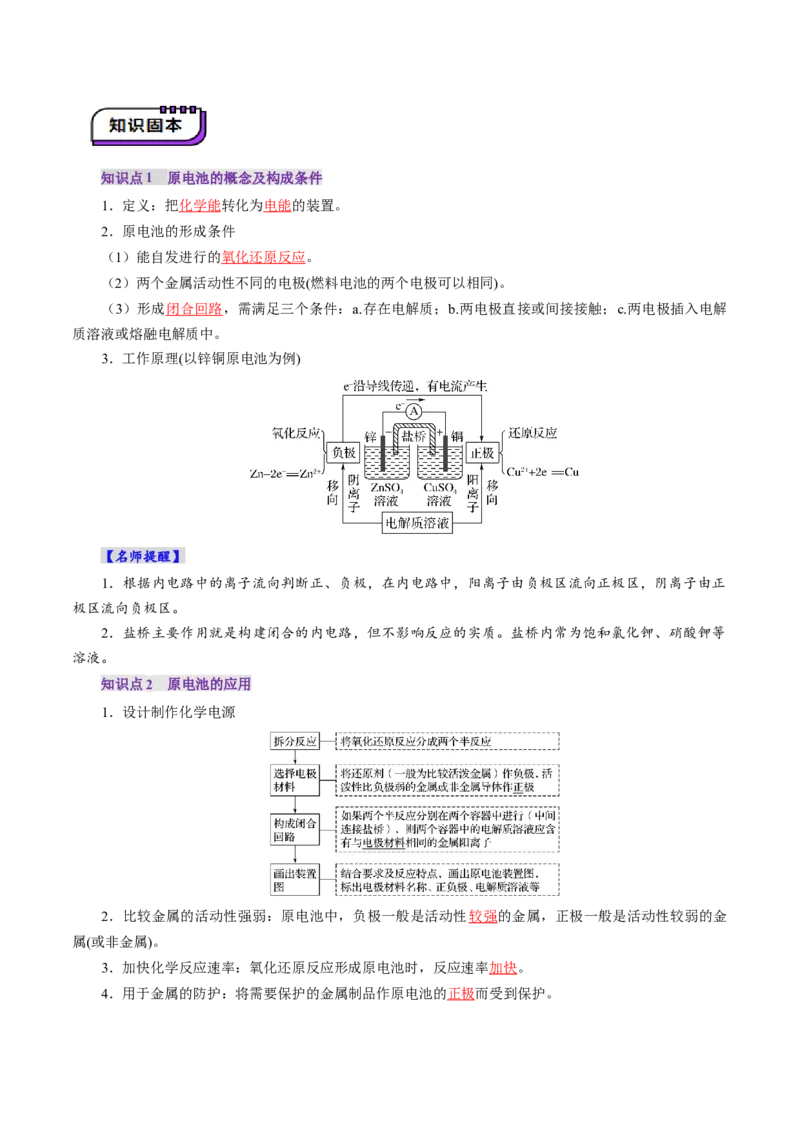
考点一 原电池的工作原理知识点1 原电池的概念及构成条件
1.定义:把化学能转化为电能的装置。
2.原电池的形成条件
(1)能自发进行的氧化还原反应。
(2)两个金属活动性不同的电极(燃料电池的两个电极可以相同)。
(3)形成闭合回路,需满足三个条件:a.存在电解质;b.两电极直接或间接接触;c.两电极插入电解
质溶液或熔融电解质中。
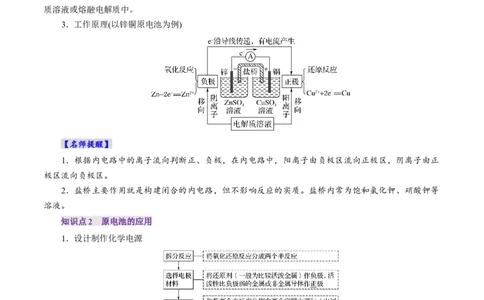
3.工作原理(以锌铜原电池为例)
【名师提醒】
1.根据内电路中的离子流向判断正、负极,在内电路中,阳离子由负极区流向正极区,阴离子由正
极区流向负极区。
2.盐桥主要作用就是构建闭合的内电路,但不影响反应的实质。盐桥内常为饱和氯化钾、硝酸钾等
溶液。
知识点2 原电池的应用
1.设计制作化学电源
2.比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性较弱的金
属(或非金属)。
3.加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
4.用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。考向1 原电池的工作原理
【例1】某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是 ( )
A.X和Y与电流表连接,电子由Cu极流向Zn极
B.X和Y与电流表连接,将Zn换成Fe测得电流更大
C.X和Y分别与电源“-”、“+”极相连,Cu极质量减轻
D.X和Y分别与电源“-”、“+”极相连,Zn极质量减轻
【答案】C
【解析】A项,Zn作负极,电子由Zn极流向Cu极,错误;B项,Fe、Cu的活动性相差小,测得电
流也小,错误;C项,X为Zn、Y为Cu,Cu作阳极,Cu被电解,质量减轻,C正确,D错误。
【名师点睛】
1.判断电极名称的基本方法是看电极反应物的反应类型,若电极反应物失去电子,发生氧化反应则
为负极,反之为正极。
2.双液铜、锌原电池(带盐桥)与单液原电池相比,最大的优点是Zn与氧化剂(Cu2+)不直接接触,仅有
化学能转化为电能,避免了能量损耗,故电流稳定,放电时间长。
3.无论是原电池还是电解池,电子均不能通过电解质溶液,即电子不下水,离子不上线。
【变式训练】(2024·四川省大数据精准教学联盟高三第二次统一监测)通过测定下图电池的标准电动
势 (V),可计算电池总反应的平衡常数 。已知: ,该电池z=1;盐桥中装有含KCl饱
和溶液的琼脂,离子可在其中自由移动。下列说法错误的是( )A.正极反应为AgCl+e-=Ag+Cl-
B.反应后,右侧烧杯中c(AgNO)增大
3
C.每转移1mole-,两个电极的质量共减少143.5g
D.若 ,Ag+(aq)+ Cl-(aq) AgCl(s)的平衡常数为
【答案】B
【解析】原电池Ag电极为负极,发生反应:Ag-e-=Ag+,电极做正极,电极反应为:AgCl+e-=Ag+
Cl-。原电池反应过程中Cl-向右侧烧杯迁移,K+向左侧迁移。A项,正极反应为AgCl+e-=Ag+ Cl-,负极反
应为Ag-e-=Ag+,A正确; B项,原电池反应过程中Cl-向右侧烧杯迁移,与2HO-4e- =O ↑+4H+生成
2 2
AgCl沉淀,右侧烧杯中AgNO 浓度保持不变,B错误;C项,正极反应为AgCl+e-=Ag+ Cl-,负极反应为
3
Ag-e-=Ag+,每转移1mole-时,负极质量减少108g,正极质量减少35.5g,两极共减少143.5g,C正确;D
项,z=1, 代入 , ,这是电池总反应AgCl(s) Ag+(aq)+ Cl-(aq)
的平衡常数,则Ag+(aq)+ Cl-(aq) AgCl(s)平衡常数 ,D正确;故选B。
考向2 原电池电极判断及电极反应的书写
【例2】分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6HO+6e-===6OH-+3H↑
2 2
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H ↑
2
【答案】B
【解析】②中Mg不与NaOH溶液反应,而Al能和NaOH溶液反应失去电子,故Al是负极;③中Fe
在浓硝酸中钝化,Cu和浓HNO 反应失去电子作负极,A、C错;②中电池总反应为2Al+2NaOH+
3
2HO===2NaAlO +3H↑,负极反应式为2Al+8OH--6e-===2AlO+4HO,二者相减得到正极反应式为
2 2 2 2
6HO+6e-===6OH-+3H↑,B正确;④中Cu是正极,电极反应式为O+2HO+4e-===4OH-,D错。
2 2 2 2
【思维建模】1.原电池电极判断
说明:原电池的正极和负极与电极材料的性质有关,也与电解质溶液有关,不要形成活泼电极一定作
负极的固定思维。
2.电极反应的书写
(1)一般电极反应的书写
(2)复杂电极反应的书写。复杂电极反应等于总反应减去较简单一极的电极反应。
考向3 “盐桥”的作用与化学平衡的移动
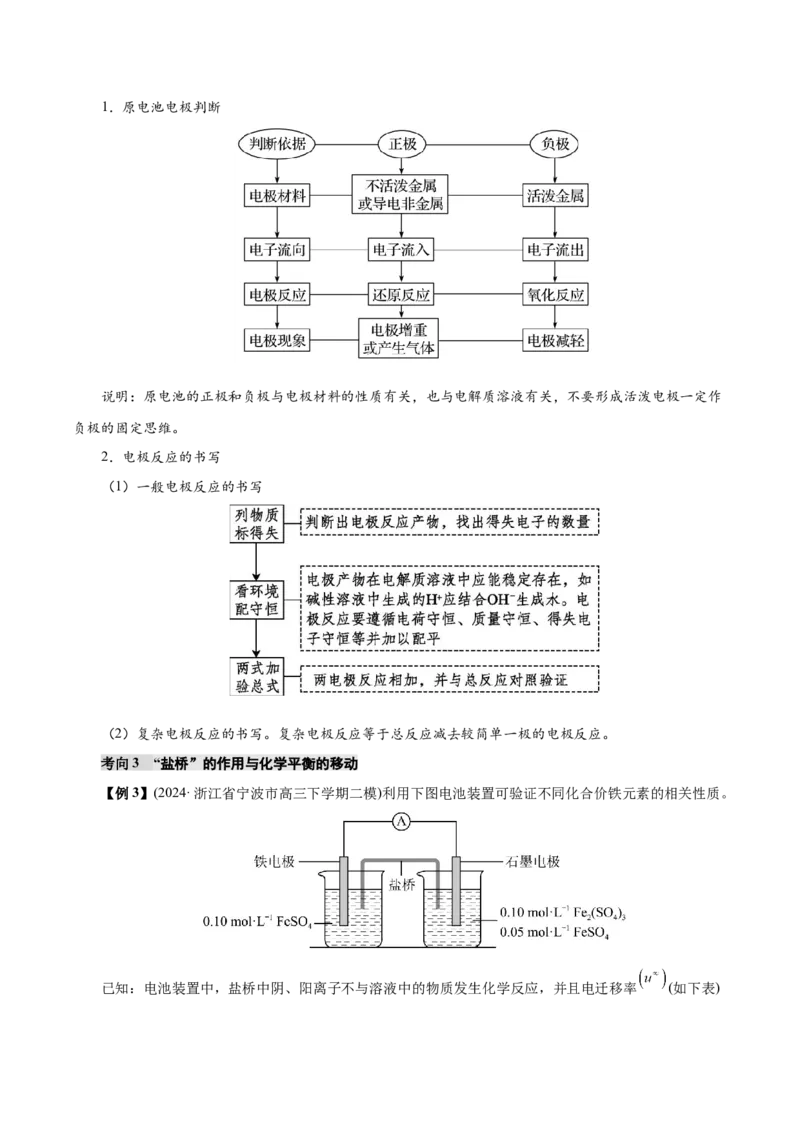
【例3】(2024·浙江省宁波市高三下学期二模)利用下图电池装置可验证不同化合价铁元素的相关性质。
已知:电池装置中,盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率 (如下表)应尽可能地相近;两烧杯中溶液体积相等。
离子 Li+ Na+ Ca2+ K+ HCO - NO - Cl- SO 2-
3 3 4
4.07 5.19 6.59 7.62 4.61 7.40 7.91 8.27
下列说法正确的是( )
A.根据上表数据,盐桥中应选择KNO 作为电解质
3
B.石墨电极上对应的电极反应式为:Fe2+-e-=Fe3+
C.反应一段时间后,当右池中c(Fe2+):c(Fe3+)=3:2时,左池中c(Fe2+)=0.15mol·L-1
D.盐桥中的阴离子进入石墨电极一侧溶液中
【答案】C
【解析】由题意和图知,铁电极为负极,电极反应式为Fe-2e-=Fe2+,石墨电极为正极,电极反应式为
Fe3++e-=Fe2+。A项,Fe2+、Fe3+能与HCO -反应,Ca2+与SO 2-不能大量共存,FeSO 、Fe (SO ) 都属于强酸
3 4 4 2 4 3
弱碱盐,水溶液呈酸性,酸性条件下NO -能与Fe2+反应,根据题意“盐桥中阴、阳离子不与溶液中的物质
3
发生化学反应”,盐桥中阴离子不可以选择HCO -、NO -,阳离子不可以选择Ca2+,盐桥中阴、阳离子的
3 3
迁移率(u∞)应尽可能地相近,根据表中数据,盐桥中应选择KCl作为电解质,A错误;B项,石墨电极为
正极,电极反应式为Fe3++e-=Fe2+,B错误;C项,由图知,右池中原c(Fe2+):c(Fe3+)=0.05:0.20,发生反
应为Fe3++e-=Fe2+,现c(Fe2+):c(Fe3+)=3:2,即c(Fe2+):c(Fe3+)=0.15:0.10,在此过程中c(Fe2+)增加了
0.10mol/L,转移的电子数为0.10mol/L,则由负极反应式Fe-2e-=Fe2+知,左池中c(Fe2+)增加了0.05mol/L,
即左池中c(Fe2+)=0.15mol·L-1,C正确;D项,盐桥中的阴离子流向负极,由分析知,进入铁电极一侧溶液
中,D错误; 故选C。
【思维建模】
1.把氧化剂、还原剂均为溶液状态的氧化还原反应设计成原电池时,必须使用盐桥才能实现氧化剂
与还原剂的分离,否则不会有明显的电流出现。
2.电子流向的分析方法:①改变条件,平衡移动;②平衡移动,电子转移;③电子转移,判断区域;
④根据区域,判断流向;⑤根据流向,判断电极。
【变式训练】控制适合的条件,将反应2Fe3++2I- 2Fe2++I 设计成如下图所示的原电池。下列
2
判断不正确的是 ( )A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl 固体,乙中的石墨电极为负极
2
【答案】D
【解析】由图示结合原电池原理分析可知,Fe3+得电子变成Fe2+被还原,I-失去电子变成I 被氧化,
2
所以A、B正确;电流计读数为零时Fe3+得电子速率等于Fe2+失电子速率,反应达到平衡状态;D项在甲
中溶入FeCl 固体,平衡2Fe3++2I- 2Fe2++I 向左移动,I 被还原为I-,乙中石墨为正极,D不正确。
2 2 2
考点二 化学电源
知识点1 一次电池、二次电池电极反应式的书写
1.新型一次电池
总反应:HO+2H++Mg===Mg2++2HO
2 2 2
Mg-HO 电池 正极 HO + 2H + + 2 e - == =2H O
2 2 2 2 2
负极 Mg-2e-===Mg2+
总反应:Mg+2AgCl===2Ag+MgCl
2
Mg-AgCl电池 正极 2AgCl + 2e - == =2Cl - + 2Ag
负极 Mg-2e-===Mg2+
总反应:2Na+xS===Na S
2 x
钠硫电池 正极 x S + 2e - == =S
负极 2Na-2e-===2Na+
总反应:2Li+Cu O+HO===2Cu+2Li++2OH-
2 2
锂-铜电池 正极 Cu O + H O + 2e - == =2Cu + 2OH -
2 2
负极 2Li-2e-===2Li+
总反应:xLi+LiV O===Li VO
3 8 1+x 3 8
锂钒氧化物电池 正极 x Li + + LiV O + x e - == =L i VO
3 8 1+x 3 8
负极 xLi-xe-===xLi+
2.新型充电(可逆)电池
总反应:Ag O+Zn+HO 2Ag+Zn(OH)
2 2 2
正极:Ag O+HO+2e-===2Ag+2OH-
2 2
锌银
负极: Zn + 2OH - - 2e - == =Zn(OH)
2
电池
阳极: 2Ag + 2OH - - 2e - == =Ag O + H O
2 2
阴极:Zn(OH) +2e-===Zn+2OH-
2
镍 镍铁 总反应:NiO+Fe+2HO Fe(OH) +Ni(OH)
2 2 2 2正极:NiO+2e-+2HO===Ni(OH) +2OH-
2 2 2
电池 负极: Fe - 2e - + 2OH - == =Fe(OH)
2
电
阳极:Ni(OH) + 2OH - - 2 e - == =NiO + 2H O
池 2 2 2
阴极:Fe(OH) +2e-===Fe+2OH-
2
镍镉 总反应:Cd+2NiOOH+2H 2 O Cd(OH) 2 +2Ni(OH) 2
电池
说明:参考镍铁电池自行书写。
总反应:3Zn+2KFeO+8HO 3Zn(OH) +2Fe(OH) +4KOH
2 4 2 2 3
正极:2FeO+6e-+8HO===2Fe(OH) +10OH-
2 3
高铁
负极: 3Zn - 6e - + 6OH - == =3Zn(OH)
2
电池
阳极:2Fe(OH) + 10OH - - 6 e - == =2FeO + 8H O
3 2
阴极:3Zn(OH) +6e-===3Zn+6OH-
2
总反应:Li CoO+LiC LiCoO +C (x<1)
1-x 2 x 6 2 6
正极:Li CoO+xe-+xLi+===LiCoO
1-x 2 2
锂离子
负极:LiC - x e - == = x L i + + C
x 6 6
电池
阳极:LiCoO - x e - == =L i CoO + x L i +
2 1-x 2
阴极:xLi++xe-+C ===LiC
6 x 6
总反应:2NaS+NaBr NaS+3NaBr
2 2 3 2 4
正极:NaBr +2e-+2Na+===3NaBr
钠硫 3
蓄电 负极:2NaS - 2 e - == =N a S + 2N a +
2 2 2 4
池
阳极:3NaBr-2e-===NaBr+2Na+
3
钠 阴极:NaS+2Na++2e-===2Na S
2 4 2 2
电
池 总反应:Na 1-m CoO 2 +Na m C n NaCoO 2 +C n
正极:Na CoO+me-+mNa+===NaCoO
钠离 1-m 2 2
子电 负极:Na C - m e - == = m N a + + C
m n n
池
阳极:NaCoO - m e - == =N a CoO + m N a +
2 1-m 2
阴极:mNa++C +me-===Na C
n m n
总反应:VO+2H++V2+ V3++VO2++HO
2
正极:VO+2H++e-===VO2++HO
2
全钒液
负极: V 2 + - e - == =V 3 +
流电池
阳极: VO 2 + + H O - e - == =VO + 2H +
2
阴极:V3++e-===V2+
【方法技巧】
化学电源电极反应的书写、、书写电极反应时,首先要根据原电池的工作原理准确判断正、负极,然
后结合电解质溶液的环境确定电极产物,最后再根据质量守恒和电荷守恒写出反应式。
(1)拆分法。①写出原电池的总反应;②把总反应按氧化反应和还原反应拆分为两个半反应,注明正、负极,并依据质量守恒、电荷守恒及得失电子守恒配平两个半反应。
(2)加减法。①写出总反应;②写出其中容易写出的一个半反应(正极或负极);③利用总反应与写出的
一极反应相减,即得另一个电极的反应。
知识点2 燃料电池
燃料电池(以CHOH燃料电池为例,体会不同介质对电极反应的影响)
3
总反应:2CHOH+3O===2CO +4HO
3 2 2 2
质子交换膜
H+ 正极 O + 4 e - + 4H + == =2H O
(酸性) 2 2
负极 CHOH-6e-+HO===CO ↑+6H+
3 2 2
总反应:2CHOH+3O+4OH-===2CO+6HO
3 2 2
碱性燃料电池 OH- 正极 O + 4 e - + 2H O == =4OH -
2 2
负极 CHOH-6e-+8OH-===CO+6HO
3 2
总反应:2CHOH+3O===2CO +4HO
3 2 2 2
固态氧化物燃
O2- 正极 O + 4 e - == =2O 2 -
2
料电池
负极 CHOH-6e-+3O2-===CO ↑+2HO
3 2 2
【名师点晴】
1.燃料电池的电极不参与反应,有很强的催化活性,起导电作用。
2.书写燃料电池的电极反应时,要注意溶液的酸碱性,溶液的酸碱性对电极反应和总反应都会产生
影响。
考向1 一次电池
【例1】(2024·江苏卷,8)碱性锌锰电池的总反应为Zn+2MnO +H O= ZnO+2MnOOH,电池构造示意
2 2
图如图所示。下列有关说法正确的是( )
A.电池工作时,MnO 发生氧化反应
2
B.电池工作时,OH-通过隔膜向正极移动
C.环境温度过低,不利于电池放电
D.反应中每生成1mol MnOOH,转移电子数为2×6.02×10-23
【答案】C【解析】Zn为负极,电极反应式为:Zn-2e-+2OH-= ZnO+H O,MnO 为正极,电极反应式为:MnO +
2 2 2
e-+H O= MnOOH+OH-。A项,电池工作时,MnO 为正极,得到电子,发生还原反应,故A错误;B项,
2 2
电池工作时,OH-通过隔膜向负极移动,故B错误;C项,环境温度过低,化学反应速率下降,不利于电
池放电,故 C 正确;D 项,由电极反应式 MnO + e-+H O= MnOOH+OH-可知,反应中每生成 1mol
2 2
MnOOH,转移电子数为6.02×10-23,故D错误;故选C。
【变式训练】(2024·北京市西城区高三一模)我国科学家设计可同时实现H 制备和海水淡化的新型电池,
2
装置示意图如图。
下列说法不正确的是( )
A.电极a是正极
B.电极b的反应式:NH-4e-+4OH-=N ↑+4H O
2 4 2 2
C.每生成1molN ,有2molNaCl发生迁移
2
D.离子交换膜c、d分别是阳离子交换膜和阴离子交换膜
【答案】C
【解析】该装置为原电池,电极a上氢离子得电子生成氢气,则a为正极,电极反应为2H++2e-=H ↑,
2
电极b上,NH 在碱性条件下失去电子生成N,b为负极,电极反应为NH-4e-+4OH-=N ↑+4H O,根据电
2 4 2 2 4 2 2
解池中,阳离子移向正极,阴离子移向负极,则钠离子经c移向左侧(a),氯离子经d移向右侧(b),
c、d分别是阳离子交换膜和阴离子交换膜。A项,电极a是正极,A正确;B项,电极b的反应式:NH-
2 4
4e-+4OH-=N ↑+4H O,B正确;C项,根据NH-4e-+4OH-=N ↑+4H O,每生成1molN ,转移4mol电子,根
2 2 2 4 2 2 2
据电荷守恒,有4molNaCl发生迁移,C错误;D项,离子交换膜c、d分别是阳离子交换膜和阴离子交换
膜,D正确;故选C。
考向2 二次电池
【例2】(2024·安徽卷,11)我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-
TCPP (局部结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质溶
4
液。下列说法错误的是( )A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:I-+Zn Zn2++3I-
3
C.充电时,阴极被还原的Zn2+主要来自Zn-TCPP
.
D 放电时,消耗0.65 g Zn,理论上转移0.02 mol电子
【答案】C
【解析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为
Zn-2e-=Zn2+,则充电时,该电极为阴极,电极反应式为Zn2++2e-=Zn;正极上发生3I-+2e-=3I-,则充电时,
3
该电极为阳极,电极反应式为3I--2e-=I -。A项,标注框内所示结构属于配合物,配位体中存在碳碳单键、
3
碳碳双键、碳氮单键、碳氮双键和碳氢键等多种共价键,还有由 N提供孤电子对、Zn2+提供空轨道形成的
配位键,A正确;B项,该电池总反应为I-+Zn Zn2++3I-,B正确;C项,充电时,阴极电极反应式为
3
Zn2++2e-=Zn,被还原的Zn2+主要来自电解质溶液,C错误;D项,放电时,负极的电极反应式为 Zn-2e-
=Zn2+,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移0.02 mol电子,D正确;故选C。
【思维建模】
思维模型
解题模型
例:xMg+Mo S Mg Mo S
3 4 x 3 4【变式训练】(2024·安徽省马鞍山市高三第二次教学质量检测)磷酸铁锂电池在充放电过程中表现出了
良好的循环稳定性,具有较长的使用寿命,放电时的反应为:LiC +Li FePO = 6C+LiFePO 。图1为某磷
x 6 1-x 4 4
酸铁锂电池的切面,图2为LiFePO 晶胞充放电时Li+脱出和嵌入的示意图。其中O围绕Fe和P分别形成
4
正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。下列说法不正确的是( )
A.放电时,负极反应: LiC - xe- = xLi++6C
x 6
B.(a)过程中1mol晶胞转移的电子数为 N
A
C.(b)代表放电过程, Li+脱离石墨,经电解质嵌入正极
D.充电时的阳极反应: LiFePO - xe-= Li FePO +xLi+
4 1-x 4
【答案】B
【解析】从总反应分析, LiC 变为C和Li+为氧化反应,该极为原电池的负极。而Li FePO 变为
x 6 1-x 4
LiFePO 发生还原反应,它为原电池的正极。A项,放电的负极为 LiC - xe- = xLi++6C,A正确;B项,a
4 x 6
过程由于Fe2+化合价升高为Fe3+,为了平衡电荷Li+脱嵌减少。从图看晶胞中减少了棱上1个和面心的一个
Li+总共减少 ,所以1mol晶体中转移 N 电子,B错误;C项,放电时,该材料在正极发生还原
A
反应,即Fe由+2变为+3为b过程,Li+嵌入正极,C正确;D项,充电时的总反应为 6C+LiFePO =
4
LiC +Li FePO ,阳极发生氧化反应为 LiFePO - xe-= Li FePO +xLi+,D正确;故选B。
x 6 1-x 4 4 1-x 4
考向3 燃料电池
【例3】(2024·全国新课标卷,6)一种可植入体内的微型电池工作原理如图所示,通过CuO催化消耗
血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
电池工作时,下列叙述错误的是
A.电池总反应为2C H O+O =2C H O
6 12 6 2 6 12 7
B.b电极上CuO通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18mg葡萄糖,理论上a电极有0.4mmol电子流入
D.两电极间血液中的Na+在电场驱动下的迁移方向为b→a
【答案】C
【解析】由题中信息可知,b 电极为负极,发生反应 Cu O+2OH--2e-=2CuO+H O,然后再发生
2 2
C H O+2CuO= C H O+Cu O;a电极为正极,发生反应O+2H O+4e-=4OH-,在这个过程中发生的总反应
6 12 6 6 12 7 2 2 2
为2C H O+O =2C H O 。A项,由题中信息可知,当电池开始工作时,a电极为电池正极,血液中的O
6 12 6 2 6 12 7 2
在a电极上得电子生成OH-,电极反应式为O+2H O+4e-=4OH-;b电极为电池负极, Cu O在b电极上失
2 2 2
电子转化成CuO,电极反应式为Cu O+2OH--2e-=2CuO+H O,然后葡萄糖被CuO氧化为葡萄糖酸,CuO被
2 2
还原为Cu O,则电池总反应为2C H O+O =2C H O ,A正确;B项,b电极上CuO将葡萄糖被CuO氧化
2 6 12 6 2 6 12 7
为葡萄糖酸后被还原为Cu O,Cu O在b电极上失电子转化成CuO,在这个过程中CuO的质量和化学性质
2 2
保持不变,因此,CuO 通过 Cu(Ⅱ)和 Cu(Ⅰ)相互转变起催化作用,B 正确;C 项,根据反应
2C H O+O =2C H O 可知,1mol C H O 参加反应时转移2 mol电子,18 mg C H O 的物质的量为0.1
6 12 6 2 6 12 7 6 12 6 6 12 6
mmol,则消耗18 mg葡萄糖时,理论上a电极有0.2 mmol电子流入,C错误;D项,原电池中阳离子从负
极移向正极迁移,故Na+迁移方向为b→a,D正确。故选C。
【方法技巧】
(1)注意介质是电解质溶液还是熔融盐或氧化物。
(2)通入负极的物质为燃料,通入正极的物质为氧气(或其他氧化剂)。(3)通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子参与靠近一极的电极反应。
(4)零价法秒杀负极反应的书写。若负极有机物燃料为CHO,产物中C元素为+4
价的CO2- 或HCO-
x y z 3 3
,则转移电子数为C数×4+H数×1+O数×(-2),若有机阴离子在负极反应(如CHCOO-),转移电子数则为C
3
数×4+H数×1+O数×(-2)+电荷数。
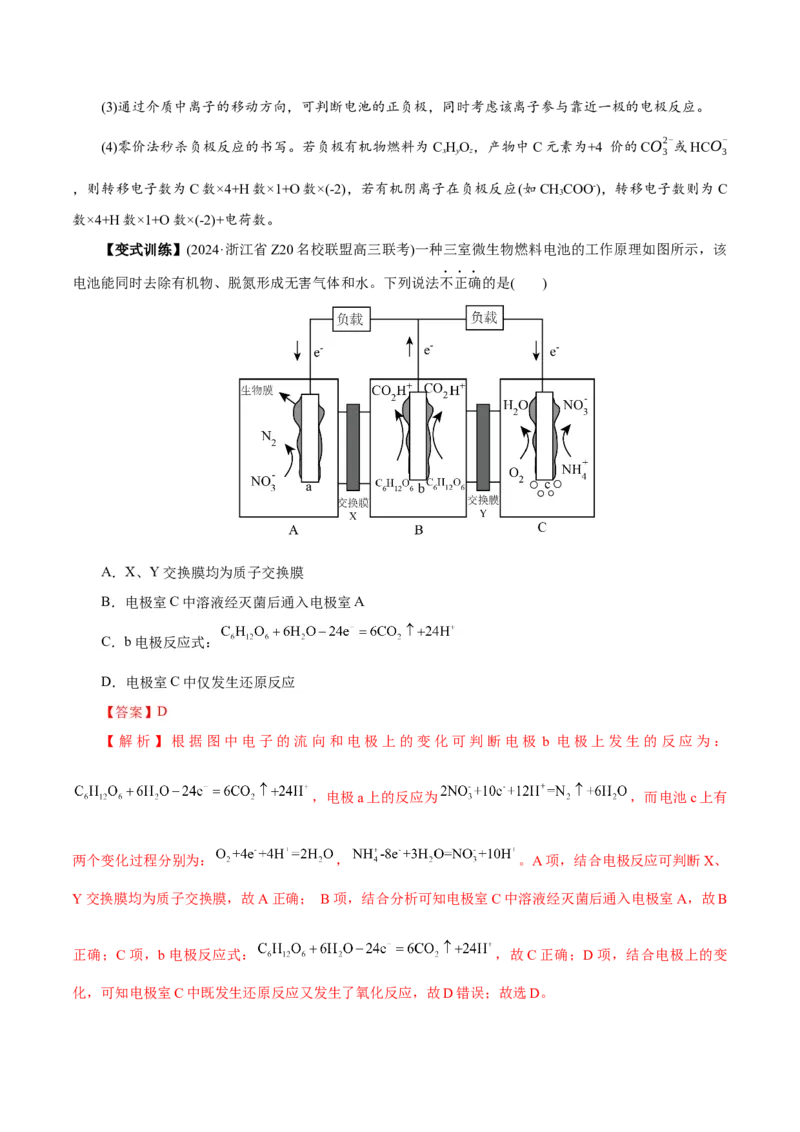
【变式训练】(2024·浙江省Z20名校联盟高三联考)一种三室微生物燃料电池的工作原理如图所示,该
电池能同时去除有机物、脱氮形成无害气体和水。下列说法不正确的是( )
A.X、Y交换膜均为质子交换膜
B.电极室C中溶液经灭菌后通入电极室A
C.b电极反应式:
D.电极室C中仅发生还原反应
【答案】D
【解析】根据图中电子的流向和电极上的变化可判断电极 b 电极上发生的反应为:
,电极a上的反应为 ,而电池c上有
两个变化过程分别为: , 。A项,结合电极反应可判断X、
Y交换膜均为质子交换膜,故A正确; B项,结合分析可知电极室C中溶液经灭菌后通入电极室A,故B
正确;C项,b电极反应式: ,故C正确;D项,结合电极上的变
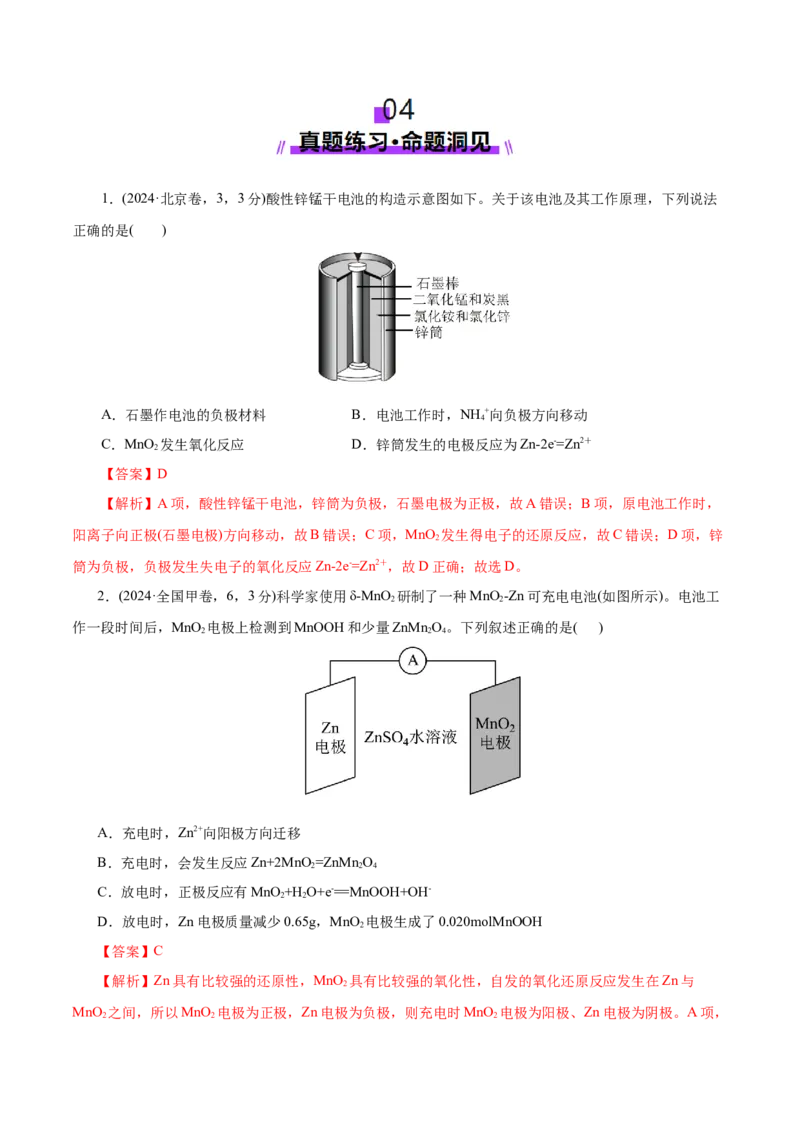
化,可知电极室C中既发生还原反应又发生了氧化反应,故D错误;故选D。1.(2024·北京卷,3,3分)酸性锌锰干电池的构造示意图如下。关于该电池及其工作原理,下列说法
正确的是( )
A.石墨作电池的负极材料 B.电池工作时,NH +向负极方向移动
4
C.MnO 发生氧化反应 D.锌筒发生的电极反应为Zn-2e-=Zn2+
2
【答案】D
【解析】A项,酸性锌锰干电池,锌筒为负极,石墨电极为正极,故A错误;B项,原电池工作时,
阳离子向正极(石墨电极)方向移动,故B错误;C项,MnO 发生得电子的还原反应,故C错误;D项,锌
2
筒为负极,负极发生失电子的氧化反应Zn-2e-=Zn2+,故D正确;故选D。
2.(2024·全国甲卷,6,3分)科学家使用δ-MnO 研制了一种MnO -Zn可充电电池(如图所示)。电池工
2 2
作一段时间后,MnO 电极上检测到MnOOH和少量ZnMn O。下列叙述正确的是( )
2 2 4
A.充电时,Zn2+向阳极方向迁移
B.充电时,会发生反应Zn+2MnO =ZnMn O
2 2 4
C.放电时,正极反应有MnO +H O+e-=MnOOH+OH-
2 2
D.放电时,Zn电极质量减少0.65g,MnO 电极生成了0.020molMnOOH
2
【答案】C
【解析】Zn具有比较强的还原性,MnO 具有比较强的氧化性,自发的氧化还原反应发生在Zn与
2
MnO 之间,所以MnO 电极为正极,Zn电极为负极,则充电时MnO 电极为阳极、Zn电极为阴极。A项,
2 2 2充电时该装置为电解池,电解池中阳离子向阴极迁移,即Zn2+向阴极方向迁移,A不正确;B项,放电时,
负极的电极反应为Zn-2e-=Zn2+,则充电时阴极反应为Zn2++2e-=Zn,即充电时Zn元素化合价应降低,而
选项中Zn元素化合价升高,B不正确;C项,放电时MnO 电极为正极,正极上检测到MnOOH和少量
2
ZnMn O,则正极上主要发生的电极反应是MnO +H O+e-=MnOOH+OH-,C正确;D项,放电时,Zn电
2 4 2 2
极质量减少0.65g(物质的量为0.010mol),电路中转移0.020mol电子,由正极的主要反应MnO +H O+e-
2 2
=MnOOH+OH-可知,若正极上只有MnOOH生成,则生成MnOOH的物质的量为0.020mol,但是正极上
还有ZnMn O 生成,因此,MnOOH的物质的量小于0.020mol,D不正确;故选C。
2 4
3.(2024·河北卷,13,3分)我国科技工作者设计了如图所示的可充电Mg-CO 电池,以Mg(TFSI) 为
2 2
电解质,电解液中加入1,3-丙二胺( )以捕获CO,使放电时CO 还原产物为MgC O。该设计克服了
2 2 2 4
MgCO 导电性差和释放CO 能力差的障碍,同时改善了Mg2+的溶剂化环境,提高了电池充放电循环性能。
3 2
下列说法错误的是( )
A.放电时,电池总反应为Mg+2CO= MgC O
2 2 4
B.充电时,多孔碳纳米管电极与电源正极连接
C.充电时,电子由Mg电极流向阳极,Mg2+向阴极迁移
D.放电时,每转移1mol电子,理论上可转化1mol CO
2
【答案】C
【解析】放电时CO 转化为MgC O,碳元素化合价由+4价降低为+3价,发生还原反应,所以放电时,
2 2 4
多孔碳纳米管电极为正极、Mg电极为负极,则充电时多孔碳纳米管电极为阳极、Mg电极为阴极:
电极 过程 电极反应式
放电 Mg-2e-=Mg2+
Mg电极
充电 Mg2++2e-= Mg
放电 Mg2++2CO+2e-=MgC O
2 2 4
多孔碳纳米管电极
充电 MgC O-2e-= Mg2+
2 4+2CO ↑
2
A项,放电时正极反应式为Mg2++2CO+2e-=MgC O、负极反应式为Mg-2e-=Mg2+,将放电时正、负电
2 2 4
极反应式相加,可得放电时电池总反应:Mg+2CO= MgC O,A正确;B项,充电时,多孔碳纳米管电极
2 2 4
上发生失电子的氧化反应,则多孔碳纳米管在充电时是阳极,与电源正极连接,B正确;C项,充电时,
Mg电极为阴极,电子从电源负极经外电路流向Mg电极,同时Mg2+向阴极迁移,C错误;D项,根据放电
时的电极反应式Mg2++2CO+2e-=MgC O 可知,每转移2mol电子,有2mol CO 参与反应,因此每转移
2 2 4 2
1mol电子,理论上可转化1mol CO,D正确;故选C。
2
4.(2023•广东卷,6)负载有 和 的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。
下列说法正确的是( )
A.Ag作原电池正极
B.电子由Ag经活性炭流向Pt
C.Pt表面发生的电极反应:O+2H O+4e-= 4OH-
2 2
D.每消耗标准状况下11.2L的O,最多去除1mol Cl-
2
【答案】B
【解析】O 在Pt得电子发生还原反应,Pt为正极,Cl-在Ag极失去电子发生氧化反应,Ag为负极。A
2
项, Cl-在Ag极失去电子发生氧化反应,Ag为负极,A错误;B项,电子由负极Ag经活性炭流向正极
Pt,B正确;C项,溶液为酸性,故Pt表面发生的电极反应为O+4H++4e-= 2H O,C错误;D项,每消耗
2 2
标准状况下11.2L的O,转移电子2mol,而2 mol Cl-失去2mol电子,故最多去除2mol Cl-,D错误。 故
2
选B。
5.(2023•辽宁省选择性考试,11)某低成本储能电池原理如下图所示。下列说法正确的是( )A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:Pb+SO2-+2Fe3+=PbSO+2Fe2+
4 4
【答案】B
【解析】该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳电极为正极,
4
正极上Fe3+得电子转化为Fe2+,充电时,多孔碳电极为阳极,Fe2+失电子生成Fe3+,PbSO 电极为阴极,
4
PbSO 得电子生成Pb和硫酸。A项,放电时负极上Pb失电子结合硫酸根离子生成PbSO 附着在负极上,
4 4
负极质量增大,A错误;B项,储能过程中,该装置为电解池,将电能转化为化学能,B正确;C项,放
电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的 H+通过质子交换膜移向右侧,C错误;D
项,充电时,总反应为PbSO +2Fe2+=Pb+SO 2-+2Fe3+,D错误;故选B。
4 4
6.(2023•全国乙卷,12)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-
硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸
作为另一电极。工作时,在硫电极发生反应: S+e-→ S , S +e-→S ,2Na++ S +2(1- )e-
8
→NaS
2 x
下列叙述错误的是( )
A.充电时Na+从钠电极向硫电极迁移B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++ S+2e-→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】A
【解析】由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。A项,充电
时为电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至钠电极,A错误;B项,放
电时Na在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电子与a电极释放出的
Na+结合得到NaS,电子在外电路的流向为a→b,B正确;C项,由题给的的一系列方程式相加可以得到
2 x
放电时正极的反应式为2Na++ S+2e-→NaS,C正确;D项,炭化纤维素纸中含有大量的炭,炭具有良好
8 2 x
的导电性,可以增强硫电极的导电性能,D正确;故选A。
7.(2022•全国甲卷,10)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 2-存在)。电池放电时,下列叙述错误的是( )
4
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 2-通过隔膜向Ⅱ区迁移
4
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O
2 4 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) 2-,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
4 2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 2-向Ⅱ区移动,Ⅲ区消耗OH-,生成
4
Zn(OH) 2-,Ⅱ区的SO 2-向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。A项,Ⅱ区的K+只能向Ⅰ区移动,A错误;
4 4B项,Ⅰ区的SO 2-向Ⅱ区移动,B正确;C项,MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C
4 2 2 2
正确;D项,电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) 2-+Mn2++2H O,D正确;故选A。
2 4 2
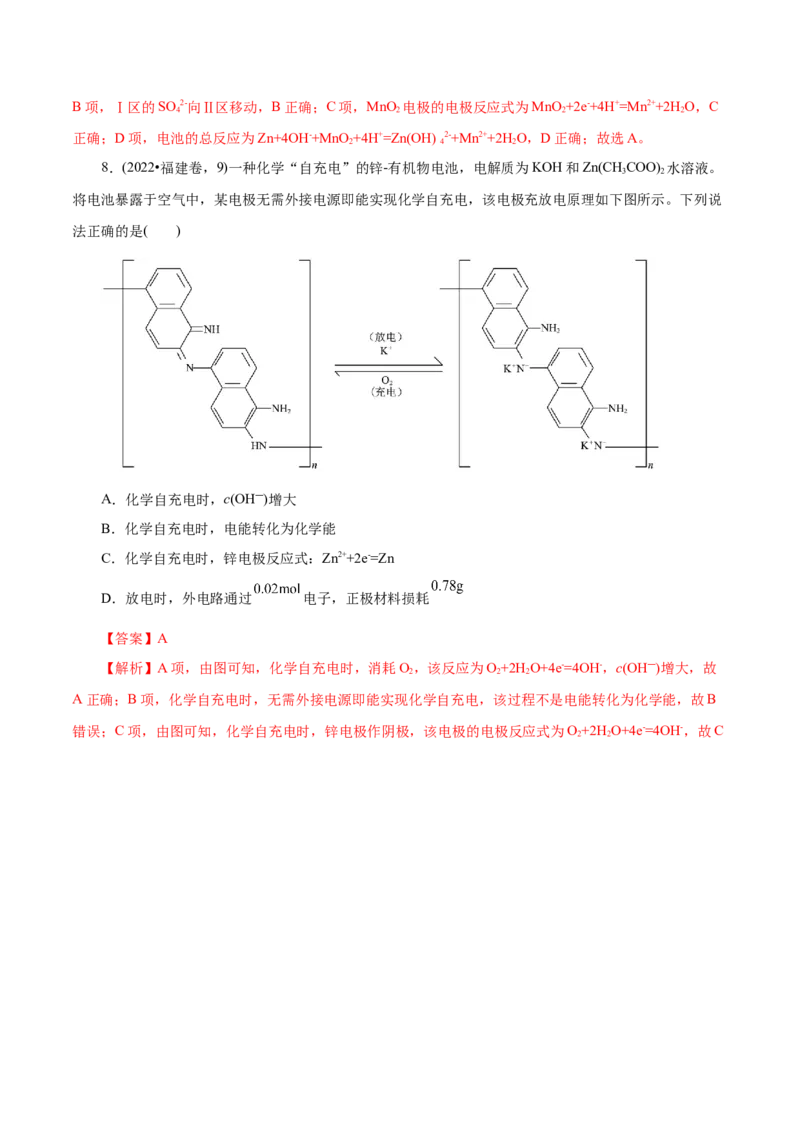
8.(2022•福建卷,9)一种化学“自充电”的锌-有机物电池,电解质为KOH和Zn(CHCOO) 水溶液。
3 2
将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。下列说
法正确的是( )
A.化学自充电时,c(OH―)增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:Zn2++2e-=Zn
D.放电时,外电路通过 电子,正极材料损耗
【答案】A
【解析】A项,由图可知,化学自充电时,消耗O,该反应为O+2H O+4e-=4OH-,c(OH―)增大,故
2 2 2
A正确;B项,化学自充电时,无需外接电源即能实现化学自充电,该过程不是电能转化为化学能,故B
错误;C项,由图可知,化学自充电时,锌电极作阴极,该电极的电极反应式为O+2H O+4e-=4OH-,故C
2 2错误;D项,放电时,1mol 转化为 ,消
耗2mol K+,外电路通过0.02 mol电子时,正极物质增加0.02mol K+,增加的质量为0.02mol×39g/mol
=0.78g,故D错误;故选A。
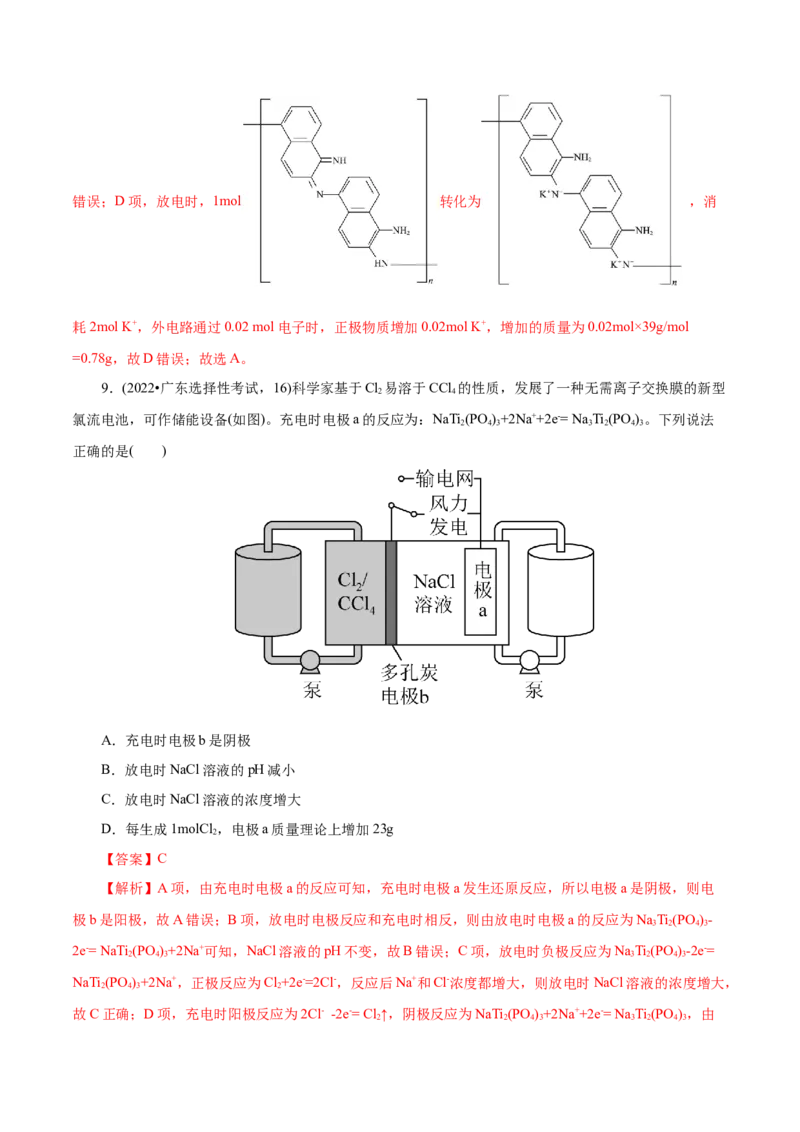
9.(2022•广东选择性考试,16)科学家基于Cl 易溶于CCl 的性质,发展了一种无需离子交换膜的新型
2 4
氯流电池,可作储能设备(如图)。充电时电极a的反应为:NaTi (PO )+2Na++2e-= Na Ti (PO )。下列说法
2 4 3 3 2 4 3
正确的是( )
A.充电时电极b是阴极
B.放电时NaCl溶液的pH减小
C.放电时NaCl溶液的浓度增大
D.每生成1molCl ,电极a质量理论上增加23g
2
【答案】C
【解析】A项,由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电
极b是阳极,故A错误;B项,放电时电极反应和充电时相反,则由放电时电极a的反应为NaTi (PO )-
3 2 4 3
2e-= NaTi (PO )+2Na+可知,NaCl溶液的pH不变,故B错误;C项,放电时负极反应为NaTi (PO )-2e-=
2 4 3 3 2 4 3
NaTi (PO )+2Na+,正极反应为Cl+2e-=2Cl-,反应后Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,
2 4 3 2
故C正确;D项,充电时阳极反应为2Cl- -2e-= Cl ↑,阴极反应为NaTi (PO )+2Na++2e-= Na Ti (PO ),由
2 2 4 3 3 2 4 3得失电子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;故选C。
2
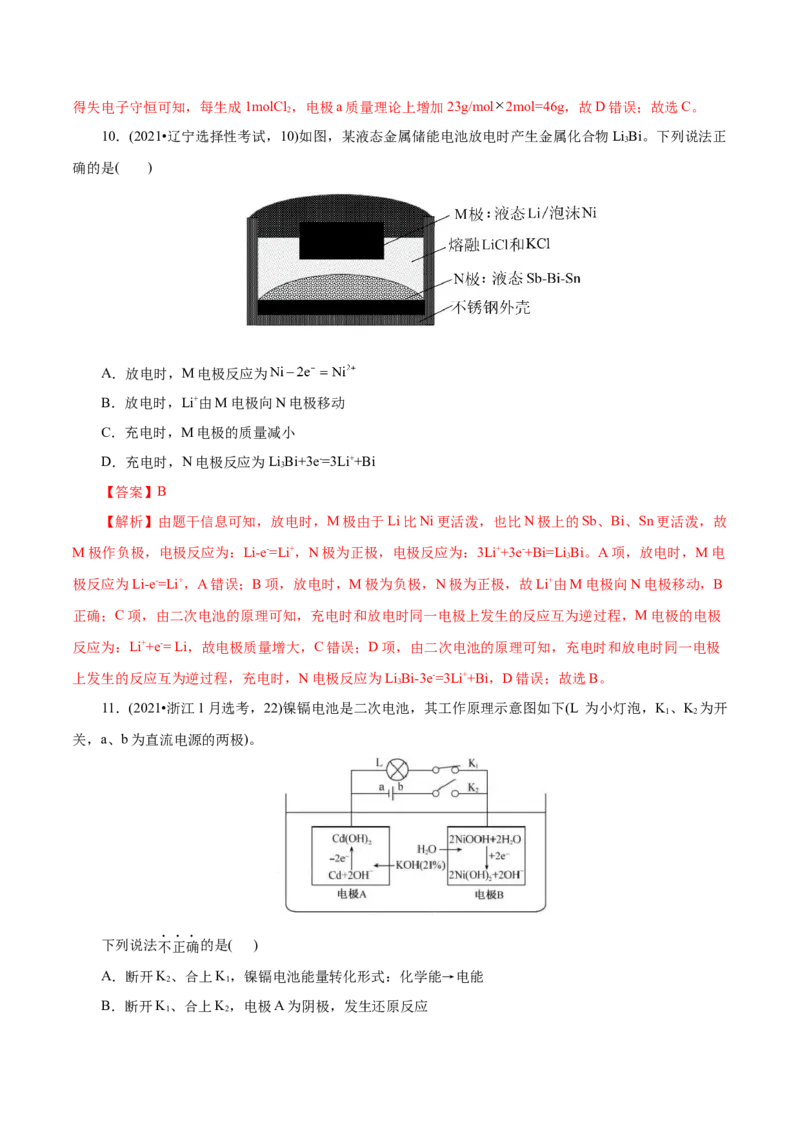
10.(2021•辽宁选择性考试,10)如图,某液态金属储能电池放电时产生金属化合物LiBi。下列说法正
3
确的是( )
A.放电时,M电极反应为
B.放电时,Li+由M电极向N电极移动
C.充电时,M电极的质量减小
D.充电时,N电极反应为LiBi+3e-=3Li++Bi
3
【答案】B
【解析】由题干信息可知,放电时,M极由于Li比Ni更活泼,也比N极上的Sb、Bi、Sn更活泼,故
M极作负极,电极反应为:Li-e-=Li+,N极为正极,电极反应为:3Li++3e-+Bi=Li Bi。A项,放电时,M电
3
极反应为Li-e-=Li+,A错误;B项,放电时,M极为负极,N极为正极,故Li+由M电极向N电极移动,B
正确;C项,由二次电池的原理可知,充电时和放电时同一电极上发生的反应互为逆过程,M电极的电极
反应为:Li++e-= Li,故电极质量增大,C错误;D项,由二次电池的原理可知,充电时和放电时同一电极
上发生的反应互为逆过程,充电时,N电极反应为LiBi-3e-=3Li++Bi,D错误;故选B。
3
11.(2021•浙江1月选考,22)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开
1 2
关,a、b为直流电源的两极)。
下列说法不正确的是( )
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Ca(OH) +2Ni(OH)
2 2 2
【答案】C
【解析】根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应
生成Cd(OH) ,负极反应式为Cd-2e-+2OH-=Cd(OH) ,电极B充电时为阳极,则放电时电极B为正极,正
2 2
极上NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为2NiOOH+2e-+2H O=2Ni(OH) +2OH-,放电
2 2 2
时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) 。A项,断开K、合上K,为放电过程,镍镉电池能量
2 2 2 2 1
转化形式:化学能→电能,A正确;B项,断开K、合上K,为充电过程,电极A与直流电源的负极相连,
1 2
电极A为阴极,发生还原反应,电极反应式为Cd(OH) +2e-=Cd+2OH-,B正确;C项,电极B发生氧化反
2
应的电极反应式为2Ni(OH) -2e-+2OH-=2NiOOH+2H O,则电极A发生还原反应的电极反应式为
2 2
Cd(OH) +2e-=Cd+2OH-,此时为充电过程,总反应为Cd(OH) +2Ni(OH) Cd+2NiOOH+2H O,溶液中
2 2 2 2
KOH浓度减小,C错误;D项,根据分析,放电时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,则镍
2 2 2
镉二次电池总反应式为Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,D正确;故选C。
2 2 2
12.(2021•湖南选择性考试,10)锌/溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源
储能和智能电网的备用电源等。三单体串联锌/溴液流电池工作原理如图所示:
下列说法错误的是( )
A.放电时,N极为正极
B.放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C.充电时,M极的电极反应式为Zn2++2e-═Zn
D.隔膜允许阳离子通过,也允许阴离子通过
【答案】B【解析】锌溴液流电池总反应为:Zn+Br ═ZnBr ,其中N为正极,发生还原反应,电极反应方程式为
2 2
Br +2e-=2Br-,M为负极,发生氧化反应,电极反应方程式为Zn﹣2e-=Zn2+,放电过程中,左侧Zn2+流向
2
右侧,左侧ZnBr 的浓度不断减少,充电过程中,发生反应ZnBr Zn+Br 。A项,依据分析可知,N为
2 2 2
正极,故A正确;B项,放电时,左侧为负极,发生氧化反应,电极反应方程式为Zn﹣2e-=Zn2+,左侧生
成的Zn2+流向右侧,故左侧ZnBr 的浓度不变,右侧ZnBr 的浓度变大,故B错误;C项,放电时,M为负
2 2
极,充电时,M及为阴极,发生还原反应,电极反应式为 Zn2++2e-═Zn,故C正确;D项,中间沉积锌位
置的作用为提供电解液,故其隔膜既可以允许阳离子通过,也允许阴离子通过,故D正确;故选B。