文档内容
第 02 讲 水的电离和溶液的酸碱性
目录
01 模拟基础练
【题型一】水的电离平衡及影响因素
【题型二】水的电离平衡图象分析
【题型三】 溶液的酸碱性与pH
【题型四】酸碱中和滴定操作及误差分析
【题型五】 酸碱中和滴定图像
【题型六】酸碱中和滴定拓展
02 重难创新练
03 真题实战练
题型一 水的电离平衡及影响因素
1. 下列条件变化会使HO的电离平衡向电离方向移动,且pH<7的是 ( )
2
A.将纯水加热到100 ℃ B.向水中加少量HCl
C.向水中加入少量NaOH D.向水中加少量NaCO
2 3
2.一定温度下,水存在HO H++OH- ΔH=Q(Q>0)的平衡,下列叙述一定正确的是( )
2
A.向水中滴入少量稀盐酸,平衡逆向移动,K 减小
w
B.将水加热,K 增大,pH减小
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.向水中加入少量固体硫酸钠,c(H+)=10-7 mol·L-1,K 不变
w
3.25°C时,水的电离达到平衡:HO H++OH-,下列叙述不正确的是( )
2
A.将纯水加热到95℃时,K 变大,pH减小,水仍呈中性
w
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,K 不变
w
C.向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,K 不变
W
D.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱
4.已知NaHSO 在水中的电离方程式为NaHSO===Na++H++SO。某温度下,向c(H+)=1×10-6
4 4
mol·L-1的蒸馏水中加入NaHSO 晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液
4
的叙述不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1×10-10 mol·L-1C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
题型二 水的电离平衡图象分析
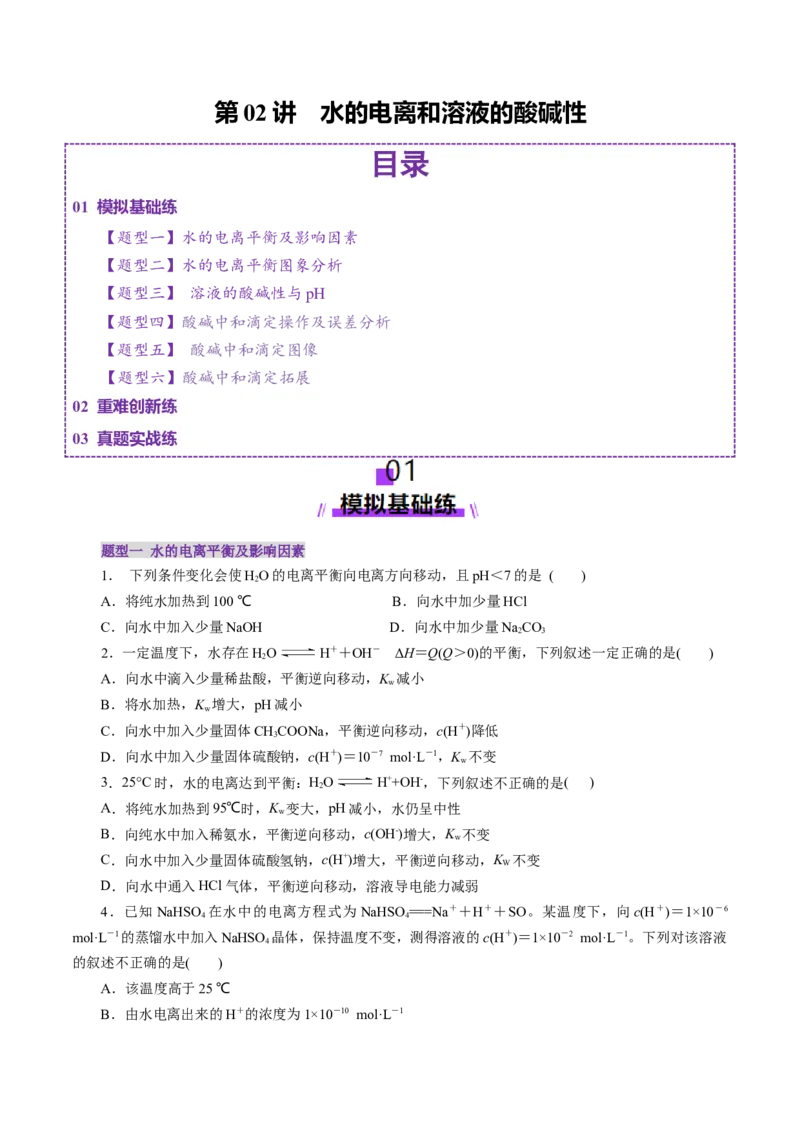
5.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
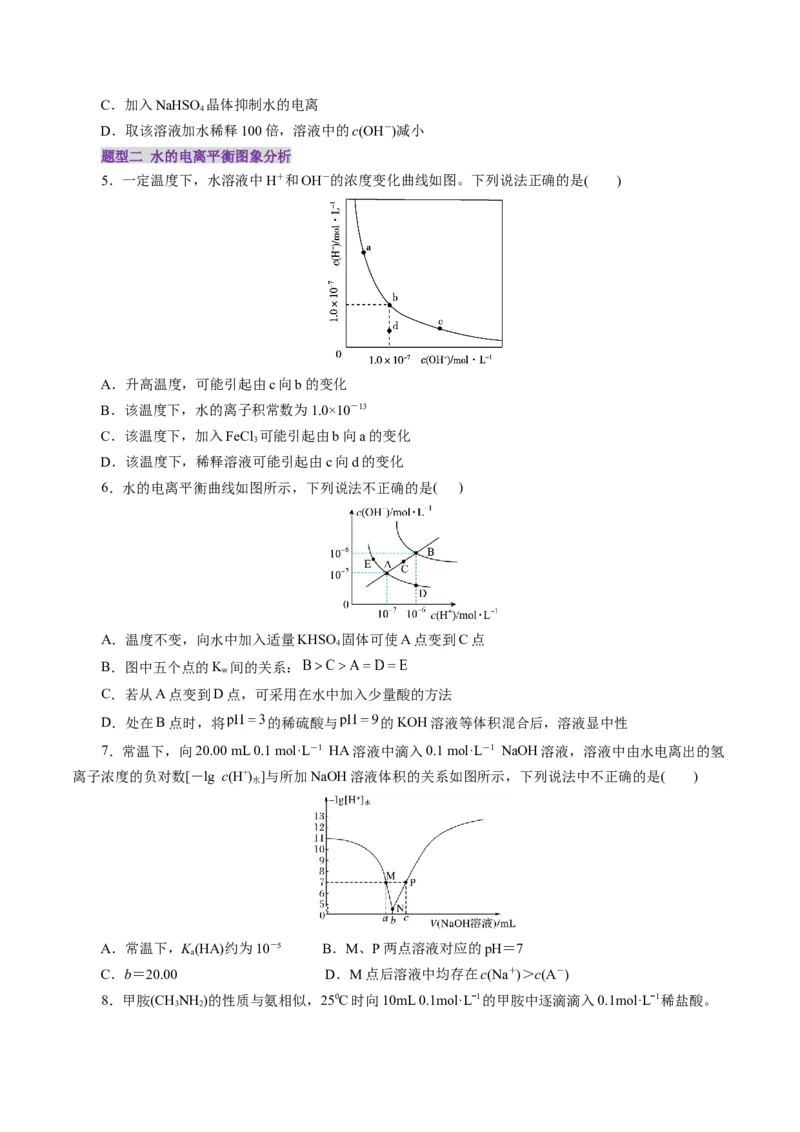
6.水的电离平衡曲线如图所示,下列说法不正确的是( )
A.温度不变,向水中加入适量KHSO 固体可使A点变到C点
4
B.图中五个点的K 间的关系:
w
C.若从A点变到D点,可采用在水中加入少量酸的方法
D.处在B点时,将 的稀硫酸与 的KOH溶液等体积混合后,溶液显中性
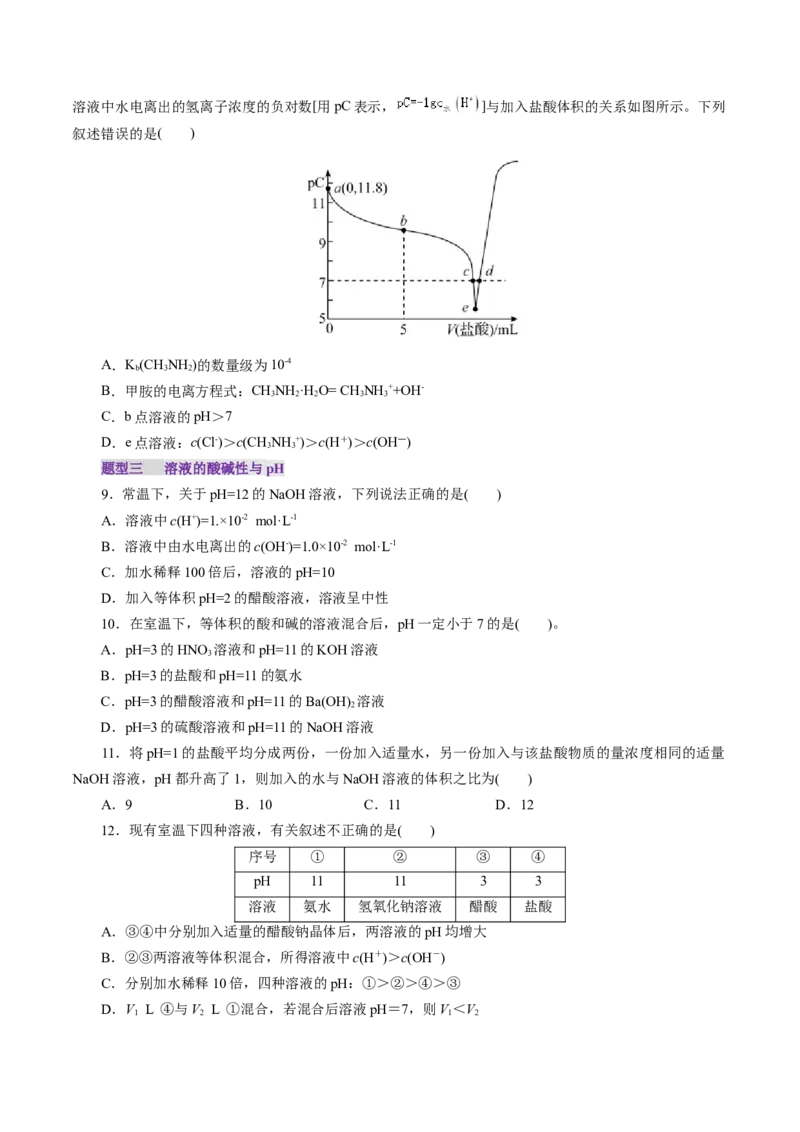
7.常温下,向20.00 mL 0.1 mol·L-1 HA溶液中滴入0.1 mol·L-1 NaOH溶液,溶液中由水电离出的氢
离子浓度的负对数[-lg c(H+) ]与所加NaOH溶液体积的关系如图所示,下列说法中不正确的是( )
水
A.常温下,K(HA)约为10-5 B.M、P两点溶液对应的pH=7
a
C.b=20.00 D.M点后溶液中均存在c(Na+)>c(A-)
8.甲胺(CHNH )的性质与氨相似,250C时向10mL 0.1mol·Lˉ1的甲胺中逐滴滴入0.1mol·Lˉ1稀盐酸。
3 2溶液中水电离出的氢离子浓度的负对数[用pC表示, ]与加入盐酸体积的关系如图所示。下列
叙述错误的是( )
A.K(CHNH )的数量级为10-4
b 3 2
B.甲胺的电离方程式:CHNH ·H O= CH NH ++OH-
3 2 2 3 3
C.b点溶液的pH>7
D.e点溶液:c(Cl-)>c(CHNH +)>c(H+)>c(OH―)
3 3
题型三 溶液的酸碱性与pH
9.常温下,关于pH=12的NaOH溶液,下列说法正确的是( )
A.溶液中c(H+)=1.×10-2 mol·L-1
B.溶液中由水电离出的c(OH-)=1.0×10-2 mol·L-1
C.加水稀释100倍后,溶液的pH=10
D.加入等体积pH=2的醋酸溶液,溶液呈中性
10.在室温下,等体积的酸和碱的溶液混合后,pH一定小于7的是( )。
A.pH=3的HNO 溶液和pH=11的KOH溶液
3
B.pH=3的盐酸和pH=11的氨水
C.pH=3的醋酸溶液和pH=11的Ba(OH) 溶液
2
D.pH=3的硫酸溶液和pH=11的NaOH溶液
11.将pH=1的盐酸平均分成两份,一份加入适量水,另一份加入与该盐酸物质的量浓度相同的适量
NaOH溶液,pH都升高了1,则加入的水与NaOH溶液的体积之比为( )
A.9 B.10 C.11 D.12
12.现有室温下四种溶液,有关叙述不正确的是( )
序号 ① ② ③ ④
pH 11 11 3 3
溶液 氨水 氢氧化钠溶液 醋酸 盐酸
A.③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B.②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C.分别加水稀释10倍,四种溶液的pH:①>②>④>③
D.V L ④与V L ①混合,若混合后溶液pH=7,则V<V
1 2 1 2题型四 酸碱中和滴定操作及误差分析
13.下列有关滴定操作的说法正确的是( )
A.用25 mL滴定管进行中和滴定时,用去标准液的体积为21.7 mL
B.用标准的KOH溶液滴定未知浓度的盐酸,洗净碱式滴定管后直接取标准KOH溶液进行滴定,则
测定结果偏低
C.用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中含有NaOH杂质,则测定
结果偏高
D.用未知浓度的盐酸滴定标准的KOH溶液时,若读取读数,滴定前仰视,滴定到终点后俯视,会导
致测定结果偏高
14.准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.1000 mol·L-1 NaOH溶液滴定,下列说法正
确的是( )
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液的滴入,锥形瓶中溶液的pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
15.现有下列仪器或用品:①铁架台(含铁圈、各种铁夹);②锥形瓶;③滴定管(酸式与碱式);④烧杯
(若干个);⑤玻璃棒;⑥天平(含砝码);⑦滤纸;⑧量筒;⑨漏斗。
有下列药品:①NaOH固体;②0.1000 mol·L-1的标准NaOH溶液;③未知浓度的盐酸;④NaCO 溶
2 3
液;⑤蒸馏水。
试回答以下问题:
(1)做酸碱中和滴定时,还缺少的试剂是___________。
(2)小明在做“研究温度对反应速率的影响”实验时,他往两支试管均加入4mL0.01 mol·L-1的KMnO
4
酸性溶液和2mL0.1 mol·L-1HC O(乙二酸)溶液,振荡,A试管置于热水中,B试管置于冷水中,记录溶液
2 2 4
褪色所需的时间。褪色所需时间t ___________t (填“>”“=”或“<”)。写出该反应的离子方程式:
A B
___________。
(3)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol·L-1KMnO 溶液装入酸
4
式滴定管中,进行滴定操作;当___________说明达到滴定终点。
③计算:重复操作2次,记录实验数据如下。则消耗KMnO 溶液的平均体积为___________mL,此样
4
品的纯度为___________。(已知HC O 的相对分子质量为90)
2 2 4
序号 滴定前读数 滴定后读数
1 0.00 20.01
2 1.00 20.99
3 0.00 21.20④误差分析:下列操作会导致测定结果偏高的是___________。
A.未用标准浓度的酸性KMnO 溶液润洗滴定管
4
B.滴定前锥形瓶有少量水
C.观察读数时,滴定前仰视,滴定后俯视
16.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。
请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛
________________________________。
(2)滴定终点的判断:____________________________________________。
(3)某学生根据3次实验分别记录有关数据如表:
待测NaOH 0.1000mol/L盐酸的体积/mL
滴定次数 溶液的体积
滴定前刻度 滴定后刻度 溶液体积/mL
/mL
第一次 25.00 0.00 26.11 26.11
第二次 25.00 1.56 30.30 28.74
第三次 25.00 0.22 26.31 26.09
根据表中数据该NaOH溶液的物质的量浓度为______________。
(4)以下操作会导致测得的NaOH溶液浓度偏高的是______________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.盛放碱液的碱式滴定管开始俯视读数,后来仰视读数
(5)氧化还原滴定实验的原理与中和滴定相同(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或
反之)。为测定某样品中所含晶体FeSO •7H O的质量分数,取晶体样品ag,溶于稀硫酸配成100.00mL溶
4 2
液,取出20.00mL溶液,用KMnO 溶液滴定(杂质与KMnO 不反应)。若消耗0.2000mol•L-1KMnO 溶液
4 4 4
20.00mL,所得晶体中FeSO •7H O的质量分数为_______________(用a表示)。
4 2
题型五 酸碱中和滴定图像
17.室温下,向20.00 mL 0.1000 mol·L-1盐酸中滴加0.1000 mol·L-1 NaOH溶液,溶液的pH随NaOH
溶液体积的变化如图。已知lg 5=0.7。下列说法不正确的是( )A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
18.用0.100 0 mol·L-1的标准盐酸分别滴定 20.00 mL的0.100 0 mol·L-1氨水和20.00 mL的0.100 0
mol·L-1氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(),纵坐标为滴定过程中溶液pH,甲基
红是一种酸碱指示剂,变色范围为4.4~6.2,下列有关滴定过程说法正确的是( )
A.滴定氨水,当滴定分数为50%时,各离子浓度间存在关系:c(NH)+c(H+)=c(OH-)
B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D.滴定氨水,当滴定分数为150%时,所得溶液中离子浓度有大小关系:c(Cl-)>c(H+)>c(NH)>c(OH
-)
19.25 ℃时,用0.100 mol·L-1的NaOH溶液分别滴定20.00 mL 0.100 mol·L-1的盐酸和20.00 mL 0.100
mol·L-1的醋酸溶液,得到如图所示的滴定曲线:
下列说法不正确的是( )
A.图1表示的是滴定盐酸的曲线
B.图2滴定应选用甲基橙作指示剂
C.图中A、D点水的电离程度:Ac(Na+)>c(H+)>c(OH-)
3
20.298 K时,向20.0 mL 0.10 mol·L-1 HA溶液中滴加0.10 mol·L-1 NaOH溶液,滴定曲线如图所示。
2
下列说法正确的是( )
A.该滴定过程应该选择石蕊溶液作指示剂
B.W点到X点发生的主要反应的离子方程式为HA+2OH-===A2-+2HO
2 2
C.Y点对应的溶液中c(Na+)+c(H+)=c(OH-)+2c(A2-)
D.反应HA+A2- 2HA-的平衡常数K=1.0×107.4
2
21.室温时,体积均为25.00 mL,浓度均为 0.0100 mol·L-1的苯酚溶液、CHCOOH溶液及盐酸分别用
3
0.0100 mol·L-1 NaOH溶液滴定,溶液的pH随V(NaOH)变化的曲线如图所示,下列说法正确的是( )
A.三个滴定过程中,均可用甲基橙作指示剂
B.室温时,苯酚的电离平衡常数为1.0×10-11
C.X点对应的溶液中存在:c(CHCOO-)CHCOONa>NaCl
6 5 3
题型六 酸碱中和滴定拓展
22.下列滴定中,指示剂的选择或滴定终点颜色变化有错误的是( )
提示:2KMnO +5KSO +3HSO ===6K SO +2MnSO +3HO、I+NaS===2NaI+S↓
4 2 3 2 4 2 4 4 2 2 2
选项 滴定管中的溶液 锥形瓶中的溶液 指示剂 滴定终点颜色变化
A NaOH溶液 CHCOOH溶液 酚酞 无色→浅红色
3
B HCl溶液 氨水 酚酞 浅红色→无色
C 酸性KMnO 溶液 KSO 溶液 无 无色→浅紫红色
4 2 3
D 碘水 NaS溶液 淀粉 无色→蓝色
2
23.白云石[CaMg(CO )]中钙含量测定常用KMnO 滴定的方法。具体做法是将其酸溶后转化为草酸钙,
3 2 4
过滤后用酸溶解,再用KMnO 滴定。则下列说法错误的是( )
4A.KMnO 滴定草酸发生反应的离子方程式为:2MnO -+5H C O+6H+=2Mn2++10CO ↑+8H O
4 4 2 2 4 2 2
B.实验过程中两次用酸溶解,均需使用稀盐酸
C.KMnO 滴定草酸过程中,标准状况下每产生448mLCO 气体理论上转移0.02mole-
4 2
D.滴定过程中若滴加KMnO 过快会发生反应4MnO -+12H+=4Mn2++5O ↑+6H O,将导致测定结果偏
4 4 2 2
高
24.(2024·浙江省镇海中学高三模拟)一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含
3 2 3 3
量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。根据上述实验原理,下列说法正确的是(
2
)
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
25.使用硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
4 2 4 2 2
步骤1:称量硫酸亚铁铵晶[(NH )Fe(SO )·6H O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L
4 2 4 2 2
(NH )Fe(SO ) 标准溶液。
4 2 4 2
步骤2:称取1.00 g青铜样品于250 mL维形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过硫酸
[(NH )SO]溶液,加热煮沸,使样品中的铬元素完全转化为HCrO,冷却后加蒸馏水配制成250 mL溶液,
4 2 2 8 2 4
摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用
(NH )Fe(SO ) 标准溶液满淀至终点。重复上述操作3次。测得消耗(NH )Fe(SO ) 标准溶液的体积分别为
4 2 4 2 4 2 4 2
18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:HCrO+Fe2++H+→Cr3++Fe3++H O (未配平)
2 4 2
下列说法不正确的是( )
A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
C.青铜中铬元素的质量分数为6.344%
D.实验中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,则测量结果将偏大
4 2 4 2
26.蛋壳是一种很好的绿色钙源,其主要成分为 CaCO 。以蛋壳为原料制备葡萄糖酸钙晶体
3
{M[Ca(C H O)·H O]=448 g·mol-1},并对其纯度进行测定,过程如下:
6 11 7 2 2
步骤Ⅰ.葡萄糖酸钙晶体的制备步骤Ⅱ.产品纯度测定——KMnO 间接滴定法
4
①称取步骤Ⅰ中制得的产品0.600 g置于烧杯中,加入蒸馏水及适量稀盐酸溶解;
②加入足量(NH )C O 溶液,用氨水调节pH为4~5,生成白色沉淀,过滤、洗涤;
4 2 2 4
③将②洗涤后所得的固体溶于稀硫酸中,用 0.02000 mol·L-1 KMnO 标准溶液滴定,消耗KMnO 标准
4 4
溶液25.00 mL。
根据以上两个步骤,回答下列问题:
(1)以上两个步骤中不需要使用的仪器有 (填字母)。
(2)步骤Ⅰ中“操作a”是 、过滤、洗涤、干燥。
(3)步骤Ⅱ中用氨水调节pH为4~5的目的为 。
(4)用KMnO 标准溶液滴定待测液的反应原理为 (用离子方程式表示),判
4
断滴定达到终点的现象为 。
(5)根据以上实验数据,测得产品中葡萄糖酸钙晶体的纯度为 (保留三位有效数字)。
1.(2024·安徽省亳州市高三联考)KHC O 在分析实验中可用作标定标准溶液的基准物质,也可用于除
2 4
去墨水渍点,洁净金属、木材等。常温下,用pH计测得0.1 mol·L-1 KHC O 溶液的 约为5.6,下列有
2 4
关该溶液的说法正确的是( )
A.常温下,由水电离出的c(H+)<10-7mol·L-1 B.滴加几滴石蕊溶液显红色
C.滴加几滴酚酞溶液显红色 D.滴加几滴甲基橙溶液显红色
2.(2024·重庆市乌江新高考协作体高三模拟)化学中常用pH表示水溶液的酸碱度,其定义为
。下列有关叙述不正确的是( )
A.0.1mol/L盐酸和0.1mol/L醋酸分别加水稀释至pH=5,盐酸加水体积更多
B.等质量的NaOH分别与pH均为3的盐酸和醋酸溶液恰好完全反应,消耗盐酸的体积更少
C.pH=3的醋酸溶液加水稀释使其体积变为原来的10倍,所得溶液pH小于4
D.向pH=3的醋酸溶液中加入等体积pH=3的盐酸溶液,醋酸的电离平衡不移动
3.(2024·贵州省高三三模)化学兴趣小组同学进行某补血剂中铁元素含量测定的实验操作如下:
①取10片补血剂样品,研磨,溶解除去不溶物(不损耗铁元素),并配制成100mL待测溶液;②量取25.00mL待测溶液于锥形瓶中;
③用酸化的c mol/L KMnO 溶液滴定至终点,记录消耗KMnO 溶液体积,重复一到两次实验。平均
4 4
消耗KMnO 溶液V mL。下列说法不正确的是( )
4
A.步骤①研磨是为了溶解时加快溶解速率
B.步骤②待测溶液装入锥形瓶中,不需要加入指示剂
C.步骤③c mol/L KMnO 溶液应装入酸式滴定管
4
D.每片补血剂中铁元素的质量为1.12cVg
4.(2024·山东省泰安市高三三模)利用工业废液生产CuSCN具有经济价值和社会效益。SCN⁻的测定方
法如下:
①准确称取CuSCN样品mg置于100mL烧杯中,加入30mL水,再加入20.00mL 溶
液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中速滤纸过滤于100mL容量瓶中,用
蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无SCN-,用去离子水稀释滤液到刻度,混匀,作为含
SCN-的待测试液。
②准确移取25.00mLSCN-待测试液于250mL锥形瓶中,加入8mL硝酸酸化,摇匀后,加入
VmL0.1000mol·L-1AgNO 标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.0500 mol·L-1NH SCN标准溶
1 3 4
液滴定至终点,平行滴定3次,记录平均消耗NH SCN标准溶液的体积为VmL。
4 2
已知:CuSCN+NaOH=NaSCN+CuOH↓,2CuOH=Cu O+HO;Ag++SCN-=AgSCN↓(白色)。
2 2
CuSCN样品中SCN-含量(质量分数)计算正确的是( )
A. B.
C. D.
5.(2024·吉林省长春市高三三模)常温下,用 溶液滴定磷酸的稀溶液,溶液的pH与 关系如
图所示, 为 、 、 。下列说法错误的是( )
A.直线 表示 与pH的关系B.
C. 的平衡常数为
D. 点溶液的pH =7.24
6.(2024·山东省青岛市高三二模)弱酸HA在有机相和水相中存在平衡:HA(环己烷) HA
2 2 2
(aq),平衡常数为 。25℃时,向VmL0.1 mol·L-1HA环己烷溶液中加入VmL水进行萃取,用NaOH(s)或
2
HCl(g)调节水溶液pH。测得水溶液中HA、HA-、A2-浓度、环己烷中HA的浓度 与水相萃取
2 2
率 随pH的变化关系如图。下列说法正确的是( )
已知:①HA在环己烷中不电离;②忽略体积变化;③ 。
2
A.
B. 时,
C.若调节水溶液 ,应加NaOH固体调节
D.若加水体积为2VmL,则交点N会由 移至
7.(2024·山东省德州市高三三模)工业碱的主要成分主要是NaOH和NaCO 或NaCO 和NaHCO (无
2 3 2 3 3
其他杂质)。实验室用盐酸做标准溶液,酚酞和甲基橙双指示剂来滴定测定工业碱的组成和含量。已知室温
下NaHCO 溶液的pH为8.32,饱和HCO 溶液的pH为3.89。实验步骤如下:
3 2 3
①量取6.0 盐酸5.0mL加入到245mL蒸馏水中混合均匀备用。
②称取1.06g无水NaCO 置于小烧杯中,加入适量蒸馏水溶解并转移到100mL容量瓶中,定容摇匀后
2 3
转移到试剂瓶中备用。
③量取15.00mL NaCO 溶液,加1~2滴甲基橙,用标准盐酸滴定至溶液由黄色变橙色,3次平行实
2 3
验所用盐酸平均体积为V mL,计算标准盐酸浓度。
④称取一定质量的工业碱置于烧杯中,加入适量蒸馏水溶解,配置成250mL溶液。量取25.00mL于锥
形瓶中,加入指示剂1,用标准盐酸滴定至终点1,记录所用盐酸体积;再加入指示剂2,继续用标准盐酸
滴定至终点2,记录所用盐酸体积。进行3次平行实验,终点1所用标准盐酸平均体积V mL,终点2所用
1标准盐酸平均体积为V mL。
2
下列说法正确的是( )
A.标准盐酸的浓度为0.12
B.步骤③中V可能等于12.50mL
C.若V>V,试样的成分为NaOH和NaCO
1 2 2 3
D.若V=12.00 mL,V=20.00 mL,则NaCO 的质量分数为34.57%
1 1 2 3
8.(2024·山东省聊城市高三二模)富马酸亚铁[Fe(OOCCH=CHCOO)]是一种治疗贫血的药物。其制备及
纯度测定实验如下:
I.制备
步骤1:将 富马酸HOOCCH=CHCOOH固体置于 烧杯中,加水 ,在加热搅拌下加
入NaCO 溶液 ,使其 为 。
2 3
步骤2:将上述溶液转移至如图所示装置中(省略加热、搅拌和夹持装置),通N 并加热一段时间后,
2
维持温度100℃,缓慢滴加 的FeSO 溶液,搅拌充分反应 ;
4
步骤3:将反应混合液冷却后,通过一系列操作,得到粗产品 。
Ⅱ.纯度测定
取 样品置于 锥形瓶中,加入煮沸过的 硫酸溶液 ,待样品完全溶解后,加入
煮沸过的蒸馏水 和2滴邻二氮菲指示剂(邻二氮菲遇 呈红色,遇 呈无色),立即用
标准溶液滴定至终点(反应的离子方程式为Fe2++Ce4+=Fe3++Ce3+)。平行测定三次,
消耗标准溶液的平均体积为 。
对于上述实验,下列说法正确的是( )
A.“步骤1”中发生反应的离子反应为2H++CO 2-=CO ↑+H O
3 2 2
B.为提高冷凝效果,仪器A可改用直形冷凝管
C.锥形瓶溶液由红色变为无色即达到滴定终点
D.富马酸亚铁产品的纯度为1. (2020·浙江7月选考,17)下列说法不正确的是( )。
A.2.0×10-7 mol·L-1的盐酸中c(H+)=2.0×10-7 mol·L-1
B.将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大
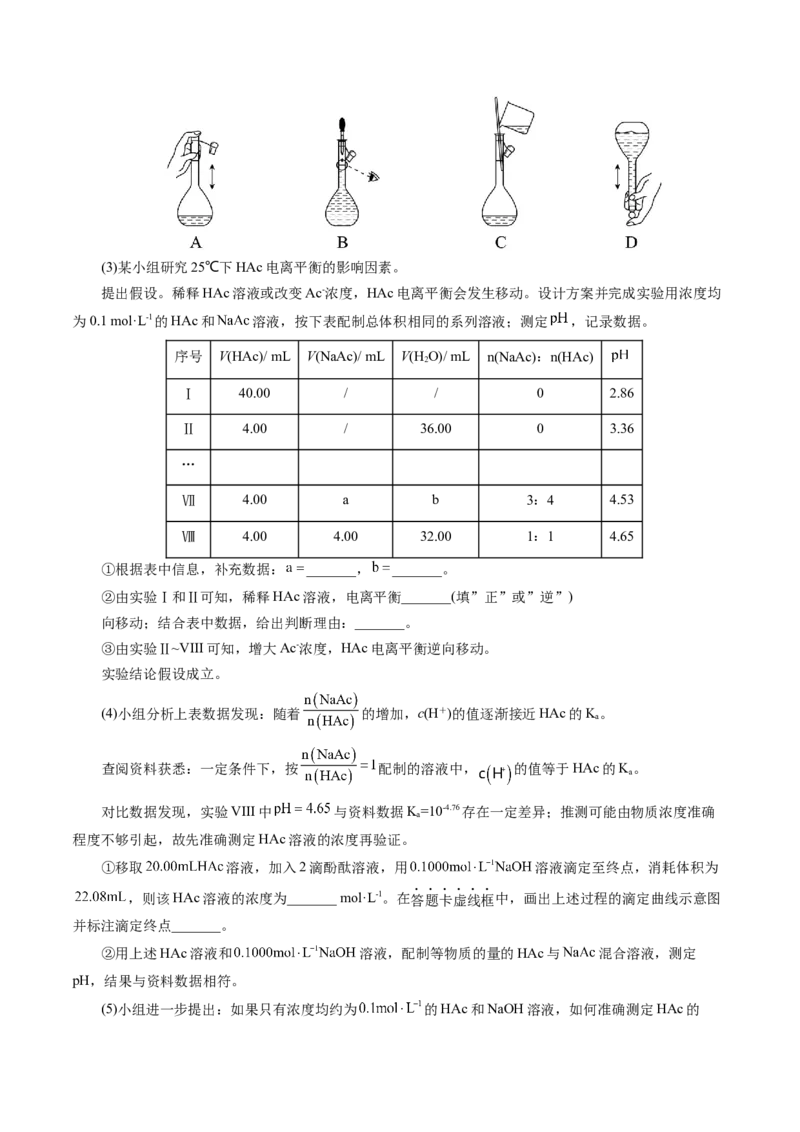
2.(2021•湖北选择性考试,14)常温下,已知HPO 溶液中含磷物料的浓度之和为0.1 mol·L1,溶液中
3 3
各含磷物种的pc-pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH的
浓度负对数[pOH=-lgc(OH)];x、y、z三点的坐标:x(7.3,1.3)、y(10.0,3.6)、z(12.6,1.3)。下列说法
正确的是( )
A.曲线①表示pc(H PO )随pOH的变化
3 3
B.HPO 的结构简式为
3 3
C.pH=4的溶液中:c(H PO )<0.1 mol·L1-2c(HPO 2)
2 2 3
D.HPO +HPO 2 2 HPO 的平衡常数K>1.0×105
3 3 3 2 3
3. (2012·新课标全国卷,11)已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的
w
一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
4.(2022•广东选择性考试)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应
用与其电离平衡密切相关。25℃时,HAc的K=1.75×105=10-4.76。
a
(1)配制 的HAc溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。设计方案并完成实验用浓度均
为0.1 mol·L-1的HAc和 溶液,按下表配制总体积相同的系列溶液;测定 ,记录数据。
序号 V(HAc)/ mL V(NaAc)/ mL V(H O)/ mL n(NaAc):n(HAc)
2
Ⅰ 40.00 / / 0 2.86
Ⅱ 4.00 / 36.00 0 3.36
…
Ⅶ 4.00 a b 3:4 4.53
Ⅷ 4.00 4.00 32.00 1:1 4.65
①根据表中信息,补充数据: _______, _______。
②由实验Ⅰ和Ⅱ可知,稀释HAc溶液,电离平衡_______(填”正”或”逆”)
向移动;结合表中数据,给出判断理由:_______。
③由实验Ⅱ~VIII可知,增大Ac-浓度,HAc电离平衡逆向移动。
实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加,c(H+)的值逐渐接近HAc的K。
a
查阅资料获悉:一定条件下,按 配制的溶液中, 的值等于HAc的K。
a
对比数据发现,实验VIII中 与资料数据K=10-4.76存在一定差异;推测可能由物质浓度准确
a
程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取 溶液,加入2滴酚酞溶液,用 溶液滴定至终点,消耗体积为
,则该HAc溶液的浓度为_______ mol·L-1。在答题卡虚线框中,画出上述过程的滴定曲线示意图
并标注滴定终点_______。
②用上述HAc溶液和 溶液,配制等物质的量的HAc与 混合溶液,测定
pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为 的HAc和NaOH溶液,如何准确测定HAc的K?小组同学设计方案并进行实验。请完成下表中Ⅱ的内容。
a
Ⅰ 移取20.00mL HAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V40.00mL
1
Ⅱ _______,测得溶液的pH为4.76
实验总结 得到的结果与资料数据相符,方案可行。
(6)根据K 可以判断弱酸的酸性强弱。写出一种无机弱酸及其用途_______。
a