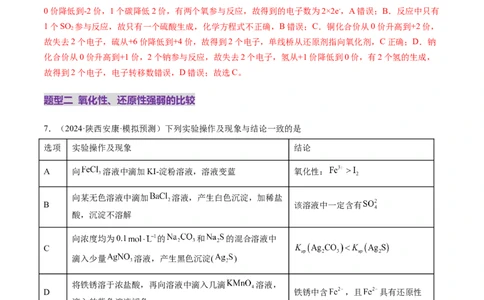
文档内容
第 04 讲 氧化还原反应的基本概念和规律
目录
01 模拟基础练
【题型一】氧化还原反应的基本概念及其表示方法
【题型二】氧化性、还原性强弱的比较
【题型三】氧化还原反应的基本规律及应用
02 重难创新练
03 真题实战练
题型一 氧化还原反应的基本概念及其表示方法
1.(2024·湖南·模拟预测)化学与生产生活密切相关,下列物质应用中涉及氧化还原反应的是
A.利用葡萄糖酸- -内酯使豆浆凝固 B.使用含氟牙膏预防龋齿
C.将植物油氢化以便于运输和储存 D.利用明矾溶液清除铜镜表面的铜锈
【答案】C
【解析】A.豆浆的凝固过程属于胶体的聚沉,没有发生氧化还原反应,A项不选;B.含氟牙膏预防龋齿
涉及难溶电解质间的转化,不属于氧化还原反应,B项不选;C.植物油氢化即植物油与氢气发生加成反
应,属于氧化还原反应,C项选;D.明矾中 水解使溶液呈酸性,可用于清除铜镜表面的铜锈[主要成
分为 ],不属于氧化还原反应,D项不选;答案选C。
2.(2024·河北·模拟预测)下列实验产生的现象中,是由于发生氧化还原反应的是
A.向碘水中加入 ,充分振荡静置,水层接近无色
B.将二氧化硫通入酸性高锰酸钾溶液中,溶液紫色褪去
C.用铂丝蘸取少量氯化铜溶液灼烧,火焰呈绿色
D.向乙酸乙酯中加入NaOH溶液,充分振荡并微热,静置,溶液不分层
【答案】B
【解析】A.向碘水中加入 ,充分振荡静置,水层接近无色,该过程为萃取,与氧化还原反应无关,A错误;B.将二氧化硫通入酸性高锰酸钾溶液中,二氧化硫具有还原性,被酸性高锰酸钾氧化,溶液紫
色褪去,与氧化还原反应有关,B正确;C.用铂丝蘸取少量氯化铜溶液灼烧,火焰呈绿色,为金属的焰
色,体现的是金属的物理性质,与氧化还原无关,C错误;D.向乙酸乙酯中加入NaOH溶液,充分振荡
并微热,乙酸乙酯水解生成乙酸和乙醇,乙醇被溶解,乙酸与NaOH反应生成可溶性乙酸钠,静置,溶液
不分层,与氧化还原反应无关,D错误;答案选B。
3.(2024·安徽阜阳·模拟预测)下列物质的颜色变化与氧化还原反应无关的是
A.新制氯水久置后,颜色变浅
B.切开的苹果断面变黄
C.染色衣服浸泡到含有双氧水的水中,一段时间再清洗褪色
D.向黄色的铬酸钾( )溶液中加入硫酸,溶液变为橙红色
【答案】D
【解析】A.新制氯水中,次氯酸见光易分解 ,导致溶液中的可逆反应
正向移动,溶液中Cl2被消耗,颜色变浅,涉及到两个可逆反应,A不符合
题意;B.切开的苹果断面变黄是因为苹果中的二价Fe2+被空气中O 氧化生成Fe3+,B不符合题意;C.双
2
氧水有弱氧化性,可以与有色物质发生氧化还原反应,C不符合题意;D.铬酸钾溶液中存在可逆反应
,加入硫酸,H+浓度增大,平衡正移,因此溶液由黄色变为橙色,不涉及氧
化还原反应,D符合题意。故选D。
4.(23-24高三上·江西宜春·10月考)下列化学方程式中,表示电子转移的方向和数目都正确的是
A.
B.
C.
D.
【答案】B
【解析】A.反应中钠化合价升高,失去2×1个电子,氧化合价降低得到2×1个电子,表示为
,A错误;B.反应中部分氯化合价升高得到次氯酸钙,失去2×1个电子,部分氯化合价降低生成氯化钙,得到2×1个电子,表示为 ,B正确;C.
根据化合价不能交叉的原则,氯酸钾中氯元素的化合价应从+5价降到0价,HCl中氯元素的化合价应从-1
价升高到0价,转移电子数是5mol,表示为 ,C错误;D.反应中铜
化合价升高,失去3×2个电子,氮化合价降低得到2×3个电子,表示为
,D错误;故选B。
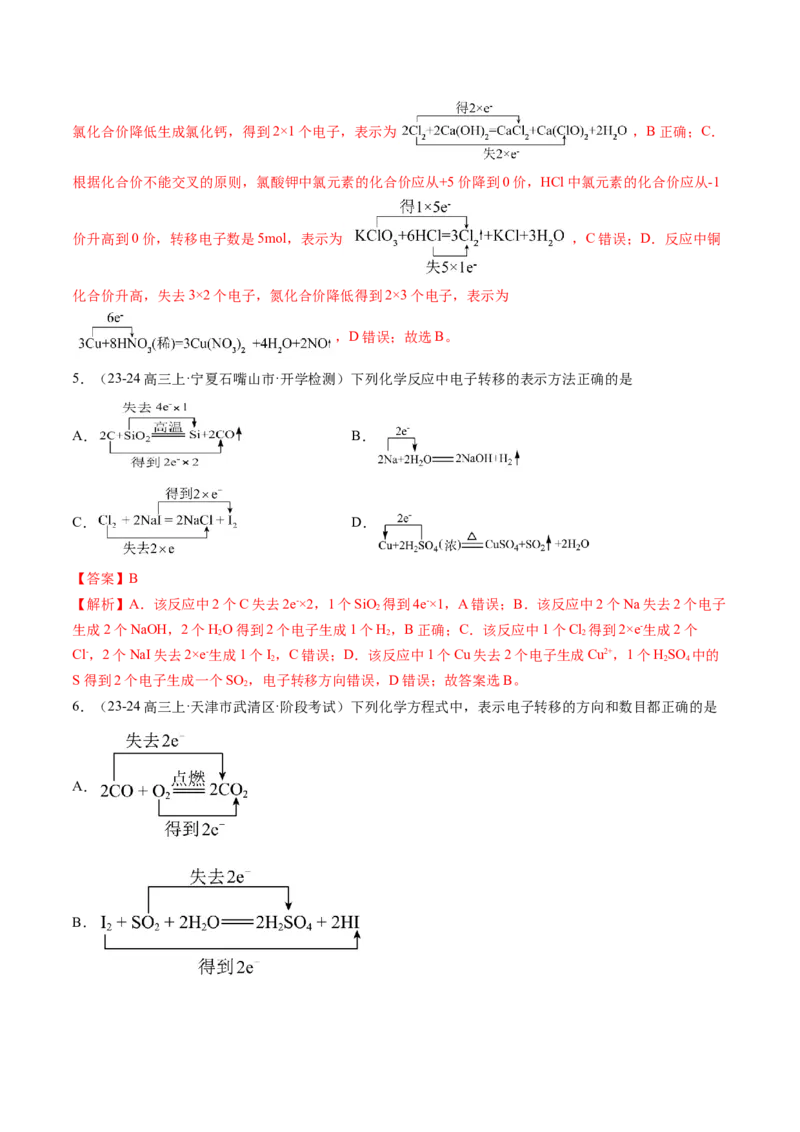
5.(23-24高三上·宁夏石嘴山市·开学检测)下列化学反应中电子转移的表示方法正确的是
A. B.
C. D.
【答案】B
【解析】A.该反应中2个C失去2e-×2,1个SiO 得到4e-×1,A错误;B.该反应中2个Na失去2个电子
2
生成2个NaOH,2个HO得到2个电子生成1个H,B正确;C.该反应中1个Cl 得到2×e-生成2个
2 2 2
Cl-,2个NaI失去2×e-生成1个I,C错误;D.该反应中1个Cu失去2个电子生成Cu2+,1个HSO 中的
2 2 4
S得到2个电子生成一个SO ,电子转移方向错误,D错误;故答案选B。
2
6.(23-24高三上·天津市武清区·阶段考试)下列化学方程式中,表示电子转移的方向和数目都正确的是
A.
B.C.
D.
【答案】C
【解析】A.碳从+2价升高到+4价,1个碳升高2价,有两个碳参与反应,故失去的电子数为2×2e-,氧从
0价降低到-2价,1个碳降低2价,有两个氧参与反应,故得到的电子数为2×2e-,A错误;B.反应中只有
1个SO 参与反应,故只有一个硫酸生成,化学方程式不正确,B错误;C.铜化合价从0价升高到+2价,
2
故失去2个电子,硫从+6价降低到+4价,故得到2个电子,单线桥从还原剂指向氧化剂,C正确;D.钠
化合价从0价升高到+1价,2个钠参与反应,故失去2个电子,氢从+1价降低到0价,有2个氢的生成,
故得到2个电子,电子转移数错误,D错误;故选C。
题型二 氧化性、还原性强弱的比较
7.(2024·陕西安康·模拟预测)下列实验操作及现象与结论一致的是
选项 实验操作及现象 结论
A 向 溶液中滴加KI-淀粉溶液,溶液变蓝 氧化性:
向某无色溶液中滴加 溶液,产生白色沉淀,加稀盐
B 该溶液中一定含有
酸,沉淀不溶解
向浓度均为0.1 的 和 的混合溶液中
C
滴入少量 溶液,产生黑色沉淀( )
将铁锈溶于浓盐酸,再向溶液中滴入几滴 溶液,
D 铁锈中含 ,且 具有还原性
滴入的紫色溶液褪色
【答案】A
【解析】A.溶液变蓝说明碘离子被铁离子氧化为碘单质,说明氧化性: , 项正确;B.向某无
色溶液中滴加 溶液,产生白色沉淀,加稀盐酸,沉淀不溶解,原溶液中可能含有 或 , 项
错误;C.更难溶的沉淀首先生成,产生黑色沉淀 ,说明 项错误;D.
浓盐酸易挥发,也能与高锰酸钾溶液发生反应而使其褪色,该实验无法确定铁锈中是否含有 项错
误。答案选A。8.(2024·河北·模拟预测)已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实
验:甲组:分别配制500mL KSCN溶液、 溶液;乙组:向 的KSCN溶液中滴加
酸性 溶液,酸性 溶液褪色;丙组:向 的 溶液中滴加酸性 溶液,酸
性 溶液褪色;丁组:分别取50mL KSCN溶液和50mL 溶液,混合,向
混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法错误的是
A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器
B.乙组实验中 将 氧化为
C.丙组实验发生反应的离子方程式:
D.丁组实验说明还原性:
【答案】D
【解析】A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器,A正确;B.实验乙中
阴离子SCN﹣被 氧化为(SCN) ,B正确;C.酸性高锰酸钾与亚铁离子反应的离子方程式:
2
,C正确;D.在等体积浓度均为0.1mol/L的KSCN和FeSO 混
4
合溶液中滴加酸性高锰酸钾,溶液先变红,说明亚铁离子先被高锰酸根离子氧化成铁离子,故还原性SCN-
PbO,步骤II中部分HCl被 氧化为Cl,根据化合
2 2 2
价变化可知该反应中氧化剂为+4价Pb,即氧化性PbO >Cl,无法比较PbO与Cl 的氧化性,B说法错误;
2 2 2
C.受热分解过程中,若PbO 完全分解只生成Pb O 和O, 的 表现氧化性,由于PbO 完全分解为
2 3 4 2 2Pb O、PbO混合物,所以超过 的 表现氧化性,C说法正确;D.若PbO 完全分解只生成Pb O 和
3 4 2 3 4
O,根据得失电子守恒,生成1mol Pb O 的同时生成1mol O,1mol Pb O 与浓盐酸反应生成1molCl ,由
2 3 4 2 3 4 2
于PbO 完全分解为Pb O、PbO混合物,所以生成O 的物质的量大于Cl,D说法正确;答案选B。
2 3 4 2 2
题型三 氧化还原反应的基本规律及应用
10.(2024·山东青岛·三模)H、C、N、O是自然界和化学研究中最重要的四种元素。下列有关说法错误
的是
A. 、 有还原性
B.C有多种同位素和同素异形体
C.浓硝酸可用于苯的硝化反应
D. 参与的反应一定为氧化还原反应
【答案】D
【解析】A.氢气中H元素的化合价为0价,易失电子表现出还原性, 中H元素的化合价为-1价,同
样易失电子表现出还原性,故A正确;B.C有多种同位素,如:12C、14C、16C等,C有多种同素异形
体,如:金刚石、石墨等,故B正确;C.在浓硫酸的作用下,浓硝酸可以与苯发生硝化反应,故C正
确;D.臭氧转化为氧气的反应不是氧化还原反应,故D错误;故答案选D。
11.(2024·湖南·模拟预测)某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用
酸化的 的 溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的 的
溶液中,铜粉溶解,溶液变为深棕色[经检验含 ],无气泡生成。下列分析正
确的是
A.①说明 的 溶液不与铜粉反应
B.②证明氧化性 还原性
C.③中 的生成速率一定小于 被还原的速率
D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色
【答案】D
【分析】铜与浓硝酸、稀硝酸均可以发生反应,生成硝酸铜,而在酸性条件下,硝酸根具有强氧化性,据
此作答。
【解析】A.实验①可能因为 的 溶液与铜粉反应慢,现象不明显,A错误。
B.②中发生反应 ,根据氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性
强于还原产物的还原性,氧化性 ,还原性 ,B错误;C.③中发生反应a.,反应b. 、反应c.
,由题干知③中无气泡产生,则说明反应b的反应速率小于或等于反应c,即
的生成速率大于或等于 被还原的速率,C错误;D.在①中加入少量绿矾,根据C项,先发
生反应b产生 , 再与铜反应,故铜粉可溶解,溶液变为深棕色,D正确;故答案选D。
12.(2024·湖北·二模)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势
(用“E”表示),E越大则该电对中氧化型物质的氧化性越强,E越低则该电对中还原型物质的还原性越强。
下表为部分电极的电极电势。根据表格数据分析,下列说法中错误的是
氧化还原电对(氧化型/还原型) 电极电势(E/V) 氧化还原电对(氧化型/还原型) 电极电势(E/V)
0.77 1.36
(或 ) 1.69 0.151
1.51 0.54
下列说法错误的是
A.向含0.2molFeCl 的溶液中加0.1molPbO ,滴加KSCN溶液,可观察到溶液变红
2 2
B.往淀粉-KI溶液中滴加SnCl 溶液,溶液不变蓝
4
C.还原性:
D.酸化高锰酸钾溶液时,可使用盐酸
【答案】D
【解析】A.由题干标准数据可知, (或 )的电极电势大于 的,说明PbO 的氧化
2
性强于Fe3+,则向含0.2molFeCl 的溶液中加0.1molPbO ,Fe2+被氧化,故滴加KSCN溶液,可观察到溶液
2 2
变红,A正确;B.由题干标准数据可知, 的电极电势大于 的,则往淀粉-KI溶液中滴加
SnCl 溶液,I-不能被Sn4+氧化,故溶液不变蓝,B正确;C.由题干标准数据可知,电极电势: >
4
> ,故可得出还原性: ,C正确;D.由题干标准数据可知,电极电
势: > ,即高锰酸根离子能够将Cl-氧化为Cl,故酸化高锰酸钾溶液时,不可使用
2
盐酸,应该使用硫酸,D错误;故答案为:D。
13.(2024·浙江温州·三模)有关反应 ,下列说法不正确的是( 为阿伏加德罗常数的值)
A. 发生还原反应
B. 既是氧化产物,又是还原产物
C.氧化剂与还原剂的物质的量之比为
D.生成 时,转移 个电子
【答案】D
【解析】A.HCl中氢得到电子,发生还原反应,A正确;B.Si失去电子得到SiHCl ,HCl中氢得到电子
3
得到SiHCl ,故SiHCl 既是氧化产物,又是还原产物,B正确;C.在反应中,HCl为氧化剂,Si为还原
3 3
剂,故氧化剂与还原剂的物质的量之比为3:1,C正确;D.由化学方程式可知,每生成1mol H 时,转移
2
4N 个电子,D错误;故选D。
A
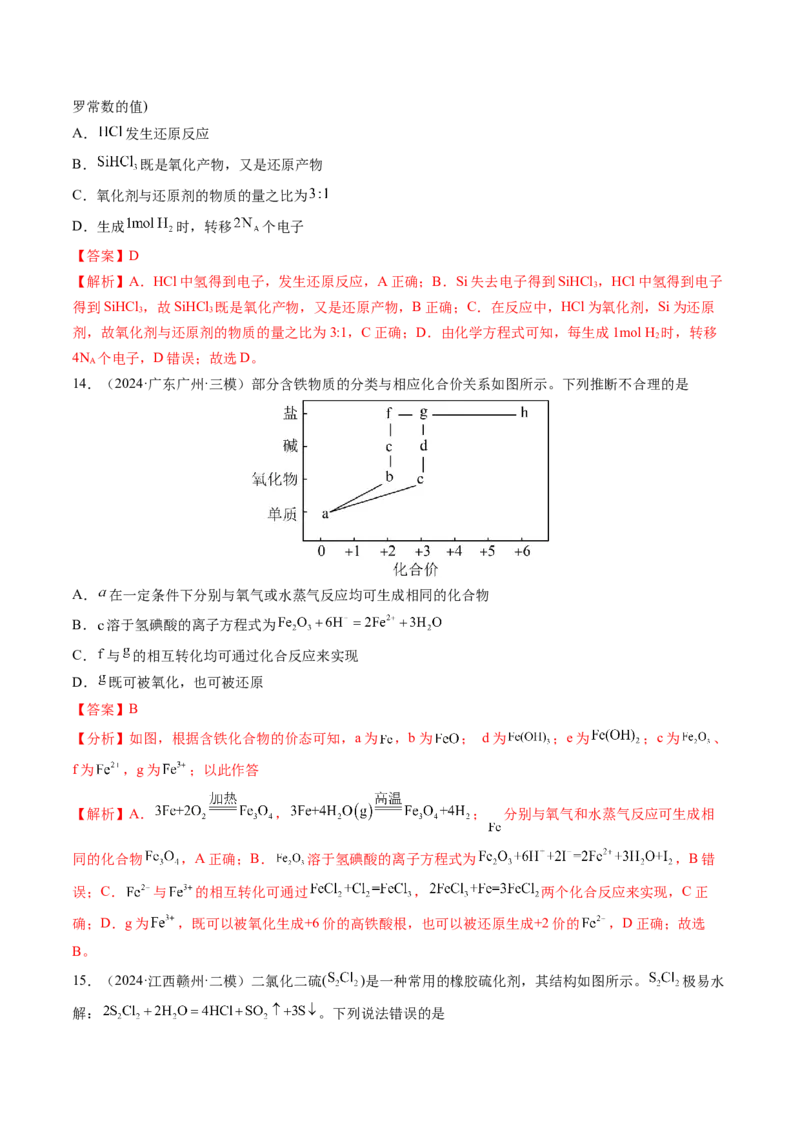
14.(2024·广东广州·三模)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A. 在一定条件下分别与氧气或水蒸气反应均可生成相同的化合物
B. 溶于氢碘酸的离子方程式为
C. 与 的相互转化均可通过化合反应来实现
D. 既可被氧化,也可被还原
【答案】B
【分析】如图,根据含铁化合物的价态可知,a为 ,b为 ; d为 ;e为 ;c为 、
f为 ,g为 ;以此作答
【解析】A. , ; 分别与氧气和水蒸气反应可生成相
同的化合物 ,A正确;B. 溶于氢碘酸的离子方程式为 ,B错
误;C. 与 的相互转化可通过 , 两个化合反应来实现,C正
确;D.g为 ,既可以被氧化生成+6价的高铁酸根,也可以被还原生成+2价的 ,D正确;故选
B。
15.(2024·江西赣州·二模)二氯化二硫( )是一种常用的橡胶硫化剂,其结构如图所示。 极易水
解: 。下列说法错误的是A. 中S为+1价
B. 是由非极性键与极性键构成的极性分子
C.上述反应中 既作氧化剂又作还原剂
D.上述反应中氧化产物与还原产物的质量比为3:1
【答案】D
【解析】A.氯元素在SCl 中为-1价,根据化合价规则知硫元素的化合价为+1价,故A正确;B.S-Cl键
2 2
是极性键,S-S键是非极性键,由于分子中正负电荷的重心不能重合,所以分子是极性分子,故B正确;
C.S元素的化合价由+1价升高为+4价,S元素的化合价由+1价降低为0,只有S元素的化合价变化,则
SCl 既作氧化剂又作还原剂,故C正确;D.氧化产物为SO ,还原产物为S,由反应可以知道二者的物
2 2 2
质的量比为1:3,故D错误;故答案选D。
16.(2024·天津北辰·三模)中国古代四大发明之一的黑火药,其爆炸过程中发生反应的化学方程式为
。下列说法正确的是
A.消耗1 mol KNO 转移电子数为6.02×1023
3
B.S和KNO 均为还原剂
3
C.反应过程中氮元素被还原
D.CO 为还原产物
2
【答案】C
【分析】在该反应过程中,N、S元素化合价降低,C元素化合价升高,所以KNO、S为氧化剂,KS、N
3 2 2
是还原产物;C为还原剂,CO 为氧化产物,根据反应过程中元素化合价升降总数等于反应过程中电子转
2
移总数计算反应过程中电子转移。
【解析】A.根据上述分析可知:KNO、S为氧化剂,得到电子被还原,每有2 mol KNO 反应,反应过程
3 3
中转移12 mol电子,则若反应消耗1 mol KNO,会转移6 mol电子,则转移的电子数为6×6.02×1023,A错
3
误;B.在反应过程中,S元素化合价由反应前S单质的0价变为反应后KS中的-2价,化合价降低,得到
2
电子被还原,因此S为氧化剂;N元素化合价由反应前KNO 中的+5价变为反应后N 中的0价,化合价降
3 2
低得到电子被还原,因此KNO 也是氧化剂,B错误;C.在反应过程中N元素化合价由反应前KNO 中的
3 3
+5价变为反应后N 中的0价,化合价降低得到电子被还原,C正确;D.在反应过程中C元素化合价由反
2
应前C单质的0价变为反应后CO 中的+4价,化合价升高,失去电子被氧化,因此C是还原剂,CO 是氧
2 2
化产物,D错误;故合理选项是C。
17.(2024·山东·模拟预测)电解能处理酸性工业废水中的乙醛,过程中电极反应存在如下物质间的转
化:
① ;② ;③ ;④ ;⑤。
下列说法错误的是
A.发生反应②⑤的电极电势较另一电极更高
B.乙醛既体现氧化性又体现还原性
C.当生成 乙醇时,电路中转移 电子
D.电解过程中,电极附近溶液的 :阴极 阳极
【答案】C
【解析】A.② ,⑤ ,涉及化合价升高,电解时为阳极,电势高,A正
确;B.③ ;④ ,两种转化,乙醛既体现氧化性又体现还原性,B
正确;C.当生成 乙醇时,同时又有其它复反应发生,④ ;⑤
,所以电路中转移电子数目不一定为 ,C错误;D.电解液为酸性,电解过程中氢离子在阴极得电
子,pH值增大,溶液的pH:阴极>阳极,D正确;故选C。
18.(2024·安徽·模拟预测)研究发现由铝原子构成的 和 团簇阴离子都能与水自发反应产生
氢气。下列说法正确的是
A. 和 互为同位素 B. 与水反应时作还原剂
C. 是由铝原子通过离子键结合而成 D. 的 含 个电子
【答案】B
【解析】A.同位素是指同一元素不同核素的关系,该三者团簇阴离子是多原子聚集体,A错误;B.
与水反应产生氢气,则 作还原剂,B正确;C.团簇是原子、分子或离子通过物理或化学结合力组成
的,不是简单的由铝原子通过离子键结合而成,C错误;D. 的 所含电子数是
,D错误;故选B。
19.(2024·山东泰安·一模) 和 均属于混盐(由一种阳离子与两种酸根阴离子组成的盐称为
混盐)。已知向 中加入足量稀硫酸时发生反应
。设 为阿伏加德罗常数的值,下列说法错误的是
A. 和足量稀硫酸反应时,每产生 时,转移 个电子
B. 固体中共含有 个离子
C. 与 的水溶液均显碱性
D.向 中加入足量稀硫酸会有 产生,被氧化与被还原的原子数相等
【答案】A
【解析】A.根据混盐定义判断,NaSO 由Na+、 、S2-构成,
4 2 3反应中,2个S化合价由-2升高为0,1个S化合价由
+4降低为0,生成3molS转移4mol电子,每产生9.6g S时转移电子数= ×N mol-1=0.4N ,故A
A A
错误;B. 由Na+、 、S2-构成,1mol 固体中共含有 个离子,故B正确;C.
由Na+、SO 、S2-构成,SO 、S2-水解使溶液呈碱性; 由Ca2+、 Cl-、ClO-构成,ClO-水
解使溶液显碱性,故C正确;D. 由Ca2+、 Cl-、ClO-构成,向 中加入足量稀硫酸,Cl-、
ClO-发生归中反应生成氯气,反应方程式为Cl-+ClO-+2H+=Cl +H O,被氧化与被还原的原子数相等,故
2 2
D正确;故选A。
20.(2024·上海·二模)实验室可由软锰矿(主要成分为MnO )制备KMnO ,方法如下:高温下使软锰
2 4
矿与过量KOH(s)和KClO(s)反应,生成KMnO (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
3 2 4
KMnO 转化为MnO 和KMnO ;再滤去沉淀MnO ,浓缩结晶得到KMnO 晶体。
2 4 2 4 2 4
请回答:
(1)用软锰矿制备KMnO 的化学方程式是 。
2 4
(2)KMnO 转化为KMnO 的反应中氧化剂和还原剂的物质的量之比为 。生成0.1mol还原
2 4 4
产物时转移电子 个。KMnO 、KMnO 和MnO 的氧化性由强到弱的顺序是
4 2 4 2
。
(3)KMnO 能与热的NaC O(aq,硫酸酸化)反应生成Mn2+和CO。若取用软锰矿制得的KMnO 产品
4 2 2 4 2 4
0.165g,能与0.335g Na C O 恰好完全反应(假设杂质均不能参与反应),该产品中KMnO 的纯度为
2 2 4 4
。
【答案】(1)6KOH + KClO + 3MnO =3 K MnO + KCl + 3H O;
3 2 2 4 2
(2)1:2 0.2N 或6.02×10-22 KMnO >KMnO >MnO
A 4 2 4 2
(3)0.958
【解析】反应物为KOH、KClO、MnO ,生成物为KMnO (锰酸钾)和KCl、水,该反应为
3 2 2 4
6KOH+KClO +3MnO=3KMnO +KCl+3H O,故答案为6KOH+KClO +3MnO=3KMnO +KCl+3H O;
3 2 2 4 2 3 2 2 4 2
(2)KMnO 转化为KMnO 的反应中KMnO =2KMnO +MnO,Mn元素的化合价由+6价升高为+7价,
2 4 4 2 4 4 2
Mn元素的化合价由+6价降低为+4价,则氧化剂和还原剂的物质的量之比为1:2,生成0.1mol还原产物
时转移电子0.1 N ×(6-4)=0.2N 或6.02×10-22,由氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,
A A
可知氧化性为KMnO >KMnO >MnO ,故答案为1:2;0.2N 或6.02×10-22;KMnO >KMnO >MnO ;
4 2 4 2 A 4 2 4 2
(3)KMnO 能与热的NaC O(aq,硫酸酸化)反应生成Mn2+和CO,设KMnO 的纯度为x,则由电子
4 2 2 4 2 4
守恒可知, (7-2)= 2 (4-3) ,解得x=0.958,故答案为0.958。
1.(2023·天津卷)常温下,二氧化氯(ClO )是一种黄绿色气体,具有强氧化性,已被联合国卫生组织
2(WTO)列为Al级高效安全消毒剂。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠
反应,其反应的化学方程式:CHOH+6NaClO +3H SO =CO ↑+6ClO ↑+3Na SO +5H O,则下列说法正确的
3 3 2 4 2 2 2 4 2
是
A.CO 是非极性分子
2
B.键角:ClO ClO ,B错误;C.该反应中,碳元素化合价由−2价变为+4
价,氯元素化合价由+5价变为+4价,所以氧化剂是NaClO,还原剂是甲醇,C错误;D.ClO 中Cl原子
3 2
提供1对电子,有一个O原子提供1个电子,另一个O原子提供1对电子,这5个电子处于互相平行的轨
道中形成大π键,Cl提供孤电子对与其中一个O形成配位键,Cl与另一个O形成的是普通的共价键(σ
键,这个O只提供了一个电子参与形成大π键),Cl的价层电子对数3,则Cl原子的轨道杂化方式为
sp2,ClO 分子空间构型为V形,D错误;故选A。
2
2.(2023·北京卷)离子化合物 和 与水的反应分别为① ;②
。下列说法正确的是
A. 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
【答案】C
【解析】A.NaO 中有离子键和非极性键,CaH 中只有离子键而不含非极性键,A错误;B.①中水的化
2 2 2
合价不发生变化,不涉及氧化还原反应,②中水发生还原反应,B错误;C.NaO 由Na+和 组成.
2 2
阴、阳离子个数之比为1∶2,CaH 由Ca2+和H-组成,阴、阳离子个数之比为2∶1,C正确;D.①中每生成1
2
个氧气分子转移2个电子,②中每生成1个氢气分子转移1个电子,转移电子数相同时,生成氧气和氢气
的物质的量之比为1∶2,D错误;
故选C。
3.(2023·浙江卷)关于反应 ,下列说法正确的是
A.生成 ,转移 电子 B. 是还原产物
C. 既是氧化剂又是还原剂 D.若设计成原电池, 为负极产物【答案】A
【解析】A.由方程式可知,反应生成1mol一氧化二氮,转移4mol电子,故A正确;B.由方程式可知,
反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,故B错误;C.由方程式可知,反应中氮元
2
素的化合价升高被氧化,NH OH是反应的还原剂,铁元素的化合价降低被还原,铁离子是反应的氧化剂,
2
故C错误;D.由方程式可知,反应中铁元素的化合价降低被还原,铁离子是反应的氧化剂,若设计成原
电池,铁离子在正极得到电子发生还原反应生成亚铁离子,亚铁离子为正极产物,故D错误;故选A。
4.(2022·浙江卷)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
【答案】B
【分析】NaSO+H SO =Na SO +S ↓+SO ↑ +H O,该反应的本质是硫代硫酸根离子在酸性条件下发生歧化
2 2 3 2 4 2 4 2 2
反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用是提供酸性环境。
【解析】A.HSO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发生还原反应,A
2 4
说法不正确;B.NaSO 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧化
2 2 3 2
剂又是还原剂,B说法正确;C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的
2
量之比为1:1,C说法不正确;D.根据其中S元素的化合价变化情况可知,1mol Na SO 发生反应,要转
2 2 3
移2 mol电子,D说法不正确。综上所述,本题选B。
5.(2022·浙江卷)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
【答案】D
【解析】A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错误;B.氢元
素化合价由-1价升为+1价,故SiH 发生氧化反应,B错误;C.反应中氧化剂为二氧化碳,还原剂为
4
SiH,则氧化剂与还原剂的物质的量之比为4:1,C错误;D.根据反应方程式可知,SiH 中氢元素的化合
4 4
价由-1价升为+1价,每消耗1molSiH ,生成1molSiO ,转移8mol电子,D正确;答案选D。
4 2
6.(2022·江苏卷)室温下,下列实验探究方案不能达到探究目的的是
选项 探究方案 探究目的
向盛有 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新制氯 具有还
A
水,观察溶液颜色变化 原性
B
向盛有 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察溶液颜 具有漂色变化 白性
的氧化性
C 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化
比 的强
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小
是弱电解质
【答案】D
【解析】A.向盛有 溶液的试管中滴加几滴 溶液,无现象,振荡,再滴加几滴新制氯水,溶
液变为红色,亚铁离子被新制氯水氧化,说明 具有还原性,A正确;B.向盛有 水溶液的试管中
滴加几滴品红溶液,品红溶液褪色,振荡,加热试管,溶液又恢复红色,说明 具有漂白性, B正确;
C.向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,溶液变为蓝色,说明 的氧化性比 的强,C正
确;D.用pH计测量醋酸、盐酸的pH用以证明 是弱电解质时,一定要注明醋酸和盐酸的物质
的量浓度相同,D错误。故选D。
7.(2023·浙江卷)化学烫发巧妙利用了头发中蛋白质发生化学反应实现对头发的“定型”,其变化过程
示意图如下。下列说法不正确的是
A.药剂A具有还原性
B.①→②过程若有 键断裂,则转移 电子
C.②→③过程若药剂B是 ,其还原产物为
D.化学烫发通过改变头发中某些蛋白质中 键位置来实现头发的定型
【答案】C
【解析】A.①→②是氢原子添加进去,该过程是还原反应,因此①是氧化剂,具有氧化性,则药剂A具
有还原性,故A正确;B.①→②过程中S的价态由−1价变为−2价,若有 键断裂,则转移
电子,故B正确;C.②→③过程发生氧化反应,若药剂B是 ,则B化合价应该降低,因此其
还原产物为 ,故C错误;D.通过①→②过程和②→③过程,某些蛋白质中 键位置发生了改变,
因此化学烫发通过改变头发中某些蛋白质中 键位置来实现头发的定型,故D正确。综上所述,答案为C。
8.(2022·湖南卷)为探究 的性质,进行了如下实验( 和 溶液浓度均为 )。
实验 操作与现象
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;将上述混合液分成两份,一份滴加
③
溶液,无蓝色沉淀生成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应
D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
【答案】D
【分析】铁离子水解显酸性,亚硫酸根离子水解显碱性,两者之间存在相互促进的水解反应,同时铁离子
具有氧化性,亚硫酸根离子具有还原性,两者还会发生氧化还原反应,在同一反应体系中,铁离子的水解
反应与还原反应共存并相互竞争,结合实验分析如下:实验①为对照实验,说明铁离子在水溶液中显棕黄
色,存在水解反应Fe3++3H O Fe(OH) +3H+,煮沸,促进水解平衡正向移动,得到红褐色的氢氧化铁胶
2 3
体;实验②说明少量亚硫酸根离子加入铁离子后,两者发生水解反应得到红褐色的氢氧化铁胶体;根据铁
氰化钾检测结果可知,同时发生氧化还原反应,使铁离子被还原为亚铁离子,而出现特征蓝色沉淀;实验
③通过反滴操作,根据现象描述可知,溶液仍存在铁离子的水解反应,但由于铁离子少量,没检测出亚铁
离子的存在,说明铁离子的水解反应速率快,铁离子的还原反应未来得及发生。
【解析】A.铁离子的水解反应为吸热反应,加热煮沸可促进水解平衡正向移动,使水解程度加深,生成
较多的氢氧化铁,从而使溶液显红褐色,故A正确;B.在5mLFeCl 溶液中滴加2滴同浓度的NaSO 溶
3 2 3
液,根据现象和分析可知,Fe3+既发生了水解反应,生成红褐色的氢氧化铁,又被亚硫酸根离子还原,得
到亚铁离子,加入铁氰化钾溶液后,出现特征蓝色沉淀,故B正确;C.实验③中在5mL Na SO 溶液中滴
2 3
加2滴同浓度少量FeCl 溶液,根据现象和分析可知,仍发生铁离子的水解反应,但未来得及发生铁离子
3
的还原反应,即水解反应比氧化还原反应速率快,故C正确;D.结合三组实验,说明铁离子与亚硫酸根
离子混合时,铁离子的水解反应占主导作用,比氧化还原反应的速率快,因证据不足,不能说明亚硫酸离
子对铁离子的水解作用无影响,事实上,亚硫酸根离子水解显碱性,可促进铁离子的水解反应,故D错
误。综上所述,答案为D。