文档内容
第 04 讲 金属材料及金属矿物的开发利用
目 录
01 考情透视·目标导航.........................................................................................................................2
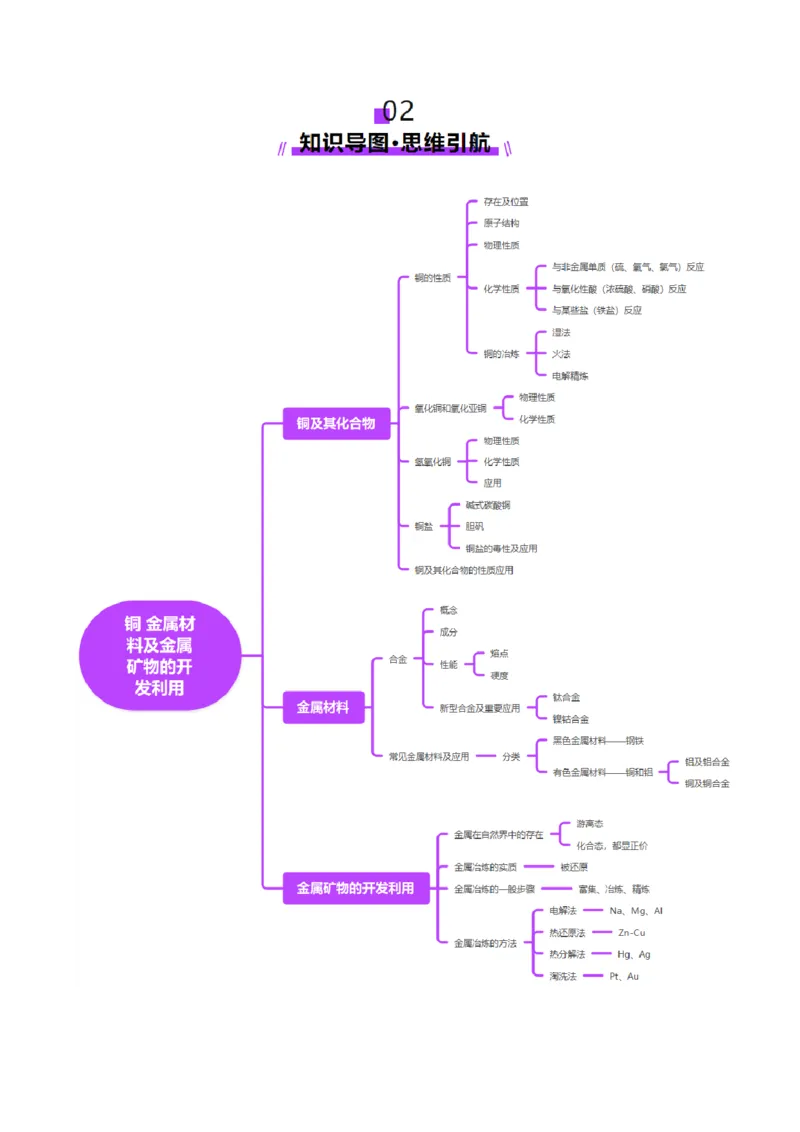
02 知识导图·思维引航.........................................................................................................................3
03 考点突破·考法探究.........................................................................................................................4
考点一 铜及其化合物.................................................................................................................4
知识点1 铜的性质...................................................................................................................4
知识点2 氧化铜和氧化亚铜...................................................................................................5
知识点3 氢氧化铜和氧化亚铜...............................................................................................5
知识点4 铜盐...........................................................................................................................6
知识点5 铜及其化合物的性质应用.......................................................................................6
考向1 考查铜及其化合物的性质与应用...............................................................................7
考向2 考查铜及其化合物的制备...........................................................................................9
考点二 金属材料及金属矿物的开发利用...............................................................................11
知识点1 金属材料.................................................................................................................11
知识点2 金属冶炼.................................................................................................................12
考向1 合金性质与金属材料的应用.....................................................................................14
考向2 金属矿物的开发利用.................................................................................................15
04 ........................................................................................................................................................16考点要求 考题统计 考情分析
2023全国乙卷第11题,6分 从近三年高考试题来看,铜及其化合物的性
2023湖北卷第18题,14分 质与应用和合金的组成、性质和应用仍是高
铜及其化合物的性质
2022山东卷第12题,4分 考的命题点;只有浙江考查了金属矿物的开
与应用
发利用。考查内容以金属及其化合物的性
2021湖北卷第2题,3分
质、合金的性质、金属的冶炼、提纯以及在
2020海南卷第7题,2分
日常生活、生产中的应用为主。题型以选择
2024山东卷第18题,13分
题和化工流程题为主。预测新的一年高考可
2023湖南卷第1题,3分
能会可能会在选择题中考查合金的性质和应
2023辽宁卷第2题,3分
用及金属矿物的开发利用,题目难度较小;
金属矿物的开发利用 2023辽宁卷第12题,3分
在工艺流程图题中考查铜及其化合物的转化
2022福建卷第6题,4分
与应用,题目综合性较强,难度较大。
2022广东卷1题,2分
2021河北卷1题,3分
复习目标:
1.能列举、描述、辨识铜及其化合物重要的物理和化学性质及实验现象。
2.了解合金的组成及其重要应用,能根据合金的性质分析生产、生活及环境中的某些常见问题。
3.能根据金属活动性顺序分析化学问题。考点一 铜及其化合物
知识点1 铜的性质
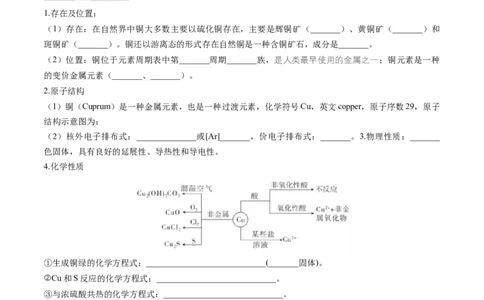
1.存在及位置:
(1)存在:在自然界中铜大多数主要以硫化铜存在,主要是辉铜矿(_______)、黄铜矿(_______)和
斑铜矿(_______)。铜还以游离态的形式存在自然铜是一种含铜矿石,成分是_______。
(2)位置:铜位于元素周期表中第_______周期_______族,是人类最早使用的金属之一;铜元素是一种
的变价金属元素(_______、_______)。
2.原子结构
(1)铜(Cuprum)是一种金属元素,也是一种过渡元素,化学符号Cu,英文copper,原子序数29,原子
结构示意图为:
(2)核外电子排布式:______________或[Ar]_______,价电子排布式:_______。3.物理性质:_______
色固体,具有良好的延展性、导热性和导电性。
4.化学性质
①生成铜绿的化学方程式:____________________________(_______固体)。
②Cu和S反应的化学方程式:____________________________。
③与浓硫酸共热的化学方程式:____________________________。
④与稀硝酸反应的离子方程式:____________________________。
⑤与浓硝酸反应的离子方程式:____________________________。
⑥与FeCl 溶液反应的离子方程式:____________________________。
3
5.铜的冶炼
(1)湿法炼铜:____________________________。
(2)高温炼铜:工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS+4O=====Cu S+3SO +2FeO(炉渣)
2 2 2 2
2Cu S+3O======2Cu O+2SO
2 2 2 22Cu O+Cu S======6Cu+SO ↑
2 2 2
(3)电解精炼铜:
粗铜中铜的含量为99.5%~99.7%,主要含有______________等杂质,粗铜通过电解精炼可得到纯度达
99.95%~99.98%的铜。电解精炼铜的原理是用粗铜作_______极,铜在_______极上_______电子变为
_______,用纯铜棒作_______极,_______在_______极上_______电子生成_______。
知识点2 氧化铜和氧化亚铜
1.氧化铜
(1)物理性质:_______色_______溶于水的固体。
(2)化学性质:与酸反应,可以用H、CO、Al还原出Cu。
2
①与酸反应(H+):CuO+2H+===Cu2++HO
2
②与H 反应:H+CuO ______________;
2 2
③与CO反应:CO+CuO ______________
2.氧化亚铜
(1)物理性质:_______色_______溶于水的固体。
(2)化学性质:
①与酸反应(H+)为____________________________。
②Cu O遇到HNO 发生氧化反应生成Cu2+。
2 3
③与H 反应:____________________________。
2
④CuO加强热的反应:____________________________。
知识点3 氢氧化铜和氧化亚铜
1.物理性质:_______色_______溶于水的固体。
2.化学性质及应用:
(1)
反应①的化学方程式:____________________________;
反应②的离子方程式:Cu(OH) +2H+===Cu2++2HO。
2 2
反应③的化学方程式:RCHO + 2Cu(OH) +NaOH RCOONa + Cu O↓ + 3HO
2 2 2
(2)应用
利用新制Cu(OH) 悬浊液检验有机化合物中含有的—CHO,乙醛与Cu(OH) 反应的化学方程式:
2 2
___________________________________。
知识点4 铜盐
1.Cu (OH) CO 的名称为碱式碳酸铜,是铜绿的成分,是铜在潮湿的空气中被锈蚀的结果,其受热分解的化
2 2 3
学方程式为___________________________________。2.CuSO ·5H O 为 蓝 色 晶 体 , 俗 称 _______ 、 胆 矾 , 其 受 热 分 解 的 化 学 方 程 式 为
4 2
________________________,蓝色晶体受热转化为白色粉末。无水 CuSO 遇水变蓝色(生成CuSO ·5H O),
4 4 2
可作为_______的检验依据。
3.铜盐的毒性:铜盐溶液有毒,主要是因为铜离子能与蛋白质作用,使蛋白质变性失去_______,因此人们
利用这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。铜盐溶液有毒,主要是因为
Cu2+作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活性,因此人们利用了它的这一性质用
胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的病毒。
知识点5 铜及其化合物的性质应用
1.区别红色物质Cu和Cu O的方法:向红色物质中加入_______,若溶液由无色变成_______色,则该红色
2
物质为_______,否则为_______,反应的化学方程式为____________________________。
2.通常利用热的铜网(反应______________)除去混合气体中的少量_______。
3.Cu与稀HSO 不反应,但在通入O 的条件下,Cu可在稀HSO 中逐渐溶解:
2 4 2 2 4
___________________________________。
4.无水硫酸铜只能作为检验_______的试剂,_______作为_______的吸收试剂而用于除杂。
5.CuO用于有机化合物中的元素分析——李比希法
将准确称量的样品置于一燃烧管中,经红热的氧化铜氧化后,再将其彻底燃烧成_______和_______,用纯
的_______把它们分别赶入烧碱石棉剂(附在石棉上粉碎的_______)及高氯酸镁的吸收管内,前者将排出
的_______变为_______,后者吸收水变为含有_______的高氯酸镁,这两个吸收管增加的重量分别表示生
成的_______和_______的重量,由此即可计算样品中的_______和_______的含量。
6.利用新制Cu(OH) 悬浊液检验有机化合物中含有的_______,如乙醛与Cu(OH) 反应的化学方程式:
2 2
__________________________________________
7.Cu用作_______催化氧化的催化剂。
考向1 考查铜及其化合物的性质与应用
例1(2024·安徽安庆·三模) 铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分Cu S)可以用
2
于制铜,制得的粗铜通过电解法进行精炼。Cu S与浓硝酸反应可得Cu(NO )。Cu在O 条件下能与氨水反
2 3 2 2
应生成[Cu(NH )]2+。向稀硫酸中加入Cu O,溶液变蓝色并有紫红色固体产生。2022年诺贝尔化学奖授予
3 4 2
了点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之
作,催化剂CuCl是白色难溶于水的化合物,溶于较浓盐酸时生成H[CuCl ] (强酸)。
2
上述叙述过程涉及的离子方程式,不正确的是A.Cu S与浓硝酸反应:
2
B.Cu O溶于稀硫酸:Cu O+2H+=Cu+Cu2++H O
2 2 2
C.Cu在O 存在下与氨水反应:
2
D.CuCl溶于较浓盐酸:CuCl+Cl-=[CuCl ]-
2
【题后归纳】铜及其化合物的颜色、状态及溶解性
物质 颜色 状态及溶解性 物质 颜色 状态及溶解性
紫 红 色 ,
固态,难溶于非氧化性 粉末,易溶于水,水溶
Cu 有 金 属 光 CuSO 白色
4
酸,易溶于强氧化性酸 液呈蓝色
泽
CuO 黑色 粉末,可溶于酸溶液 CuSO ·5HO 蓝色 晶体
4 2
固体,难溶于水,可溶
粉末,难溶于水,可溶
Cu O 砖红色 于酸溶液(生成 Cu 和 Cu (OH) CO 绿色
2 2 2 3
于酸溶液
Cu2+)
CuCl 难溶于水,可溶于酸溶
白色 粉末,难溶于水 Cu(OH) 蓝色
2
CuI 液
粉末,难溶于水及非氧
CuS 黑色 [Cu(NH )]2+ 深蓝色 络合离子,溶于水
3 4
化性强酸
【变式训练1】(2024·安徽阜阳·模拟预测)某同学进行如下实验:
实验 实验现象
溶液变蓝,液面上方呈浅红棕色;至不再产生气泡
ⅰ 将铜粉加入试管中,再加入稀
时,铜粉有剩余,余液呈酸性
继续向ⅰ中试管加入少量固体
ⅱ 又产生气泡,铜粉减少,液面上方呈浅红棕色
ⅲ 继续向ⅰ中试管滴加几滴浓硫酸 又产生气泡,铜粉减少,液面上方呈浅红棕色
下列说法不正确的是
A.铜与硝酸反应中,硝酸氧化性与氢离子、硝酸根浓度均有关
B.ⅰ、ⅱ中铜粉减少的原因能用相同的离子反应解释
C.继续向ⅰ中试管加入少量硫酸铜固体,也能发生ⅱ、ⅲ现象
D.用一定浓度的 与 也能使铜粉溶解
【变式训练2】(2024·湖南长沙·一模)部分含铜物质的分类与相应铜元素的化合价关系如图所示。下列说
法正确的是A.a、d均易溶于水
B.b既有氧化性又有还原性
C.加热条件下f与单质硫反应生成d
D.向固体c中通入 气体生成e
考向2 考查铜及其化合物的制备
例2(2024·河北衡水·模拟预测)以含有少量杂质Fe的粗铜为原料,制备蓝矾( )的工艺流程
如下图所示:
下列说法正确的是
A.“溶解”时,若忽略少量的杂质铁,理论上硫酸和硝酸的物质的量之比为3∶2
B.气体A为酸性氧化物,可与适量的氧气和水反应生成硝酸,循环利用
C.物质X可以使用氨水,且X过量对产物无影响
D.“操作Z”为蒸发结晶、趁热过滤
【变式训练1】(23-24高三上·甘肃兰州·期中)通过下列实验以印刷线路板碱性蚀刻废液(主要成分为
[Cu(NH )]Cl )为原料制备还原性物质CuCl。下列说法不正确的是
3 4 2
A.“沉铜”得到的沉淀主要为Cu(OH)
2
B.“还原”时离子方程式为SO +Cu2++Cl-+H O=CuCl↓+SO +2H+
2
C.“过滤”、“洗涤”时应该在隔绝空气的条件下进行
D.可循环利用的物质为HSO
2 4
【变式训练2】(2024·海南·一模)铁、铜及其化合物之间的转化具有重要应用。下列说法错误的是
A.常温下使用铁质容器盛装浓硫酸B.氯化铁溶液在聚合物的基材上蚀刻出铜电路
C.电解精炼铜时,粗铜连电源的正极
D.饱和 溶液中滴加稀氨水制备氢氧化铁胶体
考点二 金属材料及金属矿物的开发利用
知识点1 金属材料
1.合金
(1)概念:合金是指两种或两种以上的金属(或金属与_______)熔合而成的具有_______的物质。
(2)成分:一种金属为主,另一种或几种是金属或非金属。即合金中一定含_______元素,可能含非金属
元素(如钢中含碳) 。
(3)性能:合金具有不同于各成分金属的物理、化学性能或机械性能。
①熔点:一般比它的各成分金属的_______;
②硬度和强度:一般比它的各成分金属的_______。
【特别提醒】①构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含
金属元素。合金一定是混合物,没有固定的熔、沸点。
②常温下,多数合金是固,但钾、钠合金呈液态。
③合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面不同
于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
(4)新型合金及重要应用
①“蛟龙”号载人潜水器的耐压球壳用钛合金制造,利用了钛合金的硬度_______、机械强度_______、耐
_______等性质。
②喷气式飞机的发动机叶片由镍钴合金制造,利用了其熔点_______、耐_______的性质。
2.常见金属材料及应用
(1)金属材料的工业分类
黑色金属材料 有色金属材料
_______以及它们的合金 除黑色金属以外的其他金属及其合金
(2)黑色金属材料——钢铁
①钢是用量最_______、用途最_______的合金。
②钢
(3)有色金属材料——铜和铝
①铝及铝合金
②铜及铜合金
【特别提醒】合金的组成与性质(1)构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含金属元
素。合金一定是混合物。
(2)常温下,多数合金是固态,但钾、钠合金呈液态。
(3)合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面
不同于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
知识点2 金属冶炼
1.金属在自然界中的存在
(1)化合态—在金属化合物中,金属元素都显_______价
(2)游离态—金、_______等极少数金属
2.金属冶炼的实质
金属的冶炼过程就是把金属从_______态还原为_______态的过程。即:_____________________(写反应通
式,用M表示金属)。
3.金属冶炼的一般步骤
4.金属冶炼的方法——金属活动顺序与金属冶炼的关系
①电解法:适合冶炼金属活动性很强的金属(一般指在金属活动性顺序中排在锌前面的金属)。
工业上用电解法冶炼Na、Mg、Al的化学方程式分别为
a.2NaCl(熔融)=====______________
b.MgCl (熔融)=====______________
2
【注意】不能电解MgO,熔点_______,成本高。
c.2Al O=====______________。
2 3
【注意】不能电解AlCl ,AlCl 是_______化合物,液态时几乎不导电。
3 3
②热还原法:用还原剂(C、CO、H、Al等)还原金属氧化物,适合较活泼的金属。
2
a.CO还原Fe O:Fe O+4CO=====______________;
3 4 3 4
b.C还原ZnO:ZnO+C=====______________;或2ZnO+C=====______________
c.H 还原WO:WO+3H=====______________。
2 3 3 2
【注意】在高炉炼铁中,加入的还原剂是焦炭,但反应中真正作还原剂的是_______。
③热分解法:适用于不活泼的金属,如Hg和Ag。由HgO冶炼Hg的化学方程式:
_____________________;由Ag O冶炼Ag的化学方程式:____________________________。
25.铝热反应
Al和某些金属氧化物在高温下进行,反应迅速并放出大量的热,新生成的金属
实验原理
单质呈熔融态且易与Al O 分离
2 3
实验
装置
实验 ①镁带剧烈燃烧,放出一定的热,并发出耀眼的白光,氧化铁和铝粉在较高温
现象 度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
实验 高温下,铝与氧化铁发生反应,放出大量的热,反应的化学方程式为
结论 ___________________________________
原理 ①制取熔点较高、活泼性_______Al的金属铬、锰、钨等;②金属焊接,如野外
应用 焊接钢轨等
【特别提醒】铝热反应的三个注意事项
①铝热反应是在高温干态下进行的置换反应,铝只能与金属活动性顺序中排在铝之后的金属的氧化物反
应。
②铝热反应会放出大量的热(这一特性常出现在推断题中)。Mg条、KClO 的作用是产生高温,引发铝热反
3
应。
③铝热反应不能用来冶炼大量的金属铁、铜等(要考虑冶炼成本)。
6.特殊金属的冶炼方法:
有些很活泼的金属也可以用还原法来冶炼,如
Na+KCl=====K↑+NaCl
2RbCl+Mg=====MgCl +2Rb↑等
2
主要运用了化学平衡移动原理,利用K、Rb沸点_______,汽化离开反应体系,使化学反应得以向正反应
方向进行。
考向1 合金性质与金属材料的应用
例1(2024·山东·模拟预测)镧镍合金是一种具有实用价值的新型储氢合金材料。下列说法不正确的是
A.镧镍合金能大量吸收 形成金属氢化物
B.镍属于过渡元素,位于元素周期表d区
C.氢能是理想能源,具有来源广、热值高、无污染等优点
D.合金的熔点一定比各成分金属的熔点低
【变式训练1】(23-24高三上·辽宁沈阳·期中)化学与生活、生产、社会密切相关,下列说法正确的是A.制造镍氢电池使用的储氢合金是一类能与氢气结合成金属氢化物的材料,如钛锆合金,镧镍合金等
B. 等漂白剂均是利用强氧化性达到漂白效果
C.用于制作大运会火炬塔塔身的钛合金板具有硬度低、延展性好等特点
D.天和核心舱电推进系统腔体的氮化硼陶瓷属于传统无机非金属材料
【变式训练2】(23-24高三上·湖北孝感·开学考试)我国古典文献中有丰富的化学知识。《格古要论》
云:鍮石,自然铜之精也。今炉甘石(主要成分 )炼成者,假鍮也。崔昉《外丹本草》云:铜一斤,
炉甘石一斤,炼之成(假)鍮石。下列说法错误的是
A.假鍮石比鍮石更方便冲压成型
B.假鍮石的炼制过程会有气体产生
C.假鍮石的主要材质为合金
D.假鍮石的炼制过程涉及氧化还原反应
考向2 金属矿物的开发利用
例2(2024·辽宁葫芦岛·一模)下列有关金属的工业制法中,正确的是
A.制铜:火法炼铜,即将黄铜矿 受热分解以获得铜单质
B.制铁:以铁矿石、焦炭、石灰石为原料,CO还原得铁
C.制镁:用海水为原料,经一系列过程制得氧化镁固体, 还原得镁
D.制铝:从铝土矿制得氯化铝固体,再电解熔融的氯化铝得到铝
【变式训练1】(2024·湖南·二模)将含氧化铜的矿石与焦炭混合,在高温条件下可以冶炼金属铜,该冶炼
方法属于
A.电解冶炼法 B.热还原法 C.热分解法 D.物理分离法
【变式训练2】(2024·江苏南通·模拟预测)工业用镁还原 制备金属Ti,工艺流程如图。下列说法不
正确的是
A.工业上可通过电解熔融 制取金属Mg
B.用金属Mg还原 过程中需要通入 作保护气
C.“真空蒸馏”的目的是使Mg、 气化,实现与Ti的分离
D.制得海绵钛中含有少量金属Mg,可以用稀盐酸浸泡除Mg1.(2023·湖南卷)中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.青铜器“四羊方尊”的主要材质为合金
B.长沙走马楼出土的竹木简牍主要成分是纤维素
C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化
D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成
2.(2023·山东卷)利用热再生氨电池可实现 电镀废液的浓缩再生。电池装置如图所示,甲、乙两
室均预加相同的 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
A.甲室 电极为正极
B.隔膜为阳离子膜
C.电池总反应为:
D. 扩散到乙室将对电池电动势产生影响
3.(2023·全国卷)一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是
A 硫酸亚铁溶液出现棕黄色沉淀
B 硫化钠溶液出现浑浊颜色变深
C 溴水颜色逐渐褪去
D 胆矾表面出现白色粉末
4.(2022·浙江卷)下列说法不正确的是
A.用标准液润洗滴定管后,应将润洗液从滴定管上口倒出
B.铝热反应非常剧烈,操作时要戴上石棉手套和护目镜
C.利用红外光谱法可以初步判断有机物中具有哪些基团
D.蒸发浓缩硫酸铵和硫酸亚铁(等物质的量)的混合溶液至出现晶膜,静置冷却,析出硫酸亚铁铵晶体
5.(2021·河北卷)“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生
铁熔化灌入熟铁,再锻打成钢。下列说法错误的是
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
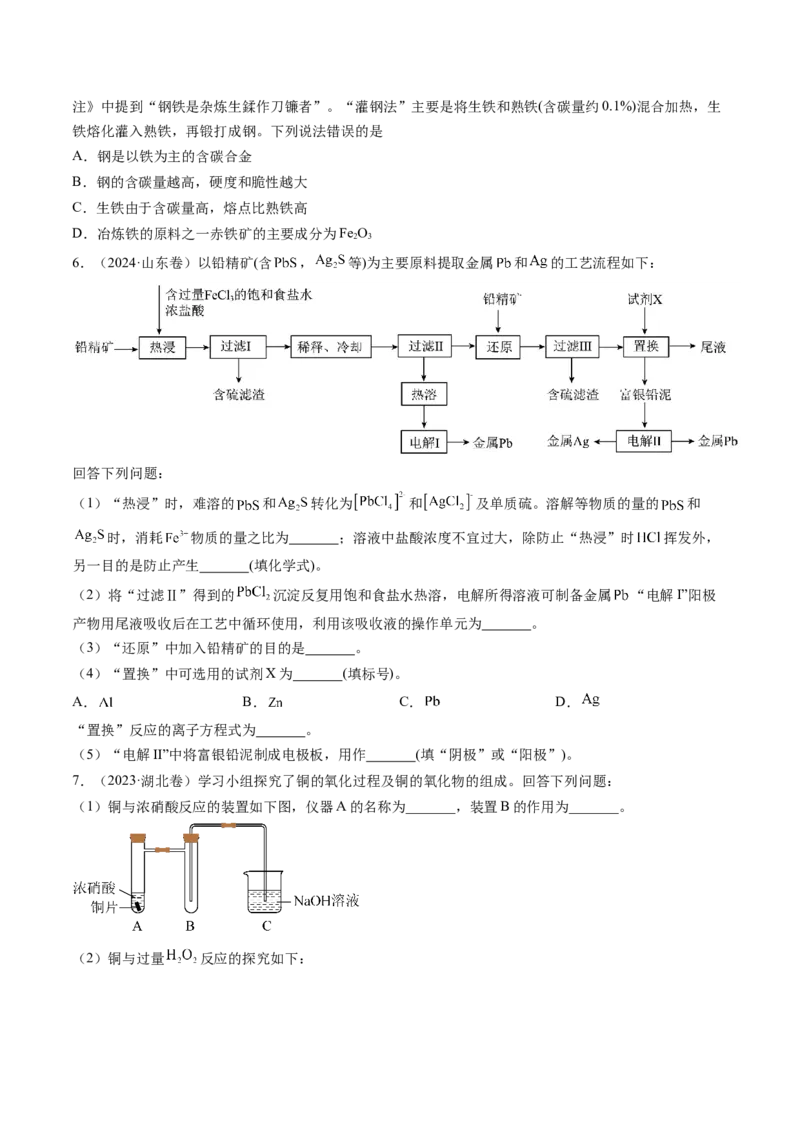
6.(2024·山东卷)以铅精矿(含 , 等)为主要原料提取金属 和 的工艺流程如下:
回答下列问题:
(1)“热浸”时,难溶的 和 转化为 和 及单质硫。溶解等物质的量的 和
时,消耗 物质的量之比为 ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,
另一目的是防止产生 (填化学式)。
(2)将“过滤Ⅱ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极
产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为 。
(3)“还原”中加入铅精矿的目的是 。
(4)“置换”中可选用的试剂X为 (填标号)。
A. B. C. D.
“置换”反应的离子方程式为 。
(5)“电解II”中将富银铅泥制成电极板,用作 (填“阴极”或“阳极”)。
7.(2023·湖北卷)学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,仪器A的名称为_______,装置B的作用为_______。
(2)铜与过量 反应的探究如下:实验②中Cu溶解的离子方程式为_______;产生的气体为_______。比较实验①和②,从氧化还原角度说
明 的作用是_______。
(3)用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X
在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y, 。X的化学式为_______。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI完全反应后,调节溶液至弱酸性。以淀粉为指
示剂,用 标准溶液滴定,滴定终点时消耗 标准溶液15.00mL。(已知:
, )标志滴定终点的现象是_______,粗品中X的相对含量
为_______。