文档内容
第 04 讲 金属材料及金属矿物的开发利用
01 模拟基础练
【题型一】铜及其重要化合物
【题型二】金属材料及金属矿物的开发利用
02 重难创新练
03 真题实战练
题型一 铜及其重要化合物
1.(2024·新疆乌鲁木齐·一模)中国三星堆出土了大量文物,如青铜面具、青铜大立人等。下列有关说法
正确的是
A.铜在空气中主要发生析氢腐蚀
B.三星堆出土的青铜器上有大量铜锈,其主要成分为Cu (OH) CO
2 2 3
C.用硝酸清洗铜器可以除去铜锈,保护铜器
D.青铜是铜中加入铅、锡制得的合金,其成分会加快铜的腐蚀
【答案】B
【解析】A.铜在空气中主要发生吸氧腐蚀,故A错误;B.铜锈的主要成分为 ,故B正
确;C.铜可以和硝酸反应,用硝酸清洗铜器可以除去铜绿,但也会破坏铜器,故C错误;D.铅、锡比
铜活泼,腐蚀反应中铜做正极,会减缓铜的腐蚀,故D错误;故答案选B。
2.(23-24高三上·河南·阶段考试)实验室进行浓硫酸和铜反应的相关实验时,下列装置或操作错误的是
A B C
蒸发 溶液
铜和浓硫酸反应 收集 并吸收尾气 测定剩余硫酸的浓度
制备 固体
【答案】D
【解析】A.铜与浓硫酸反应需加热,A正确;B.二氧化硫的密度比空气的密度大,应该长管进短管出,且二氧化硫不溶于四氯化碳,但溶于氢气化钠溶液,故该装置能收集二氧化硫并吸收尾气,且有防倒吸作
用,B正确;C.该操作应在蒸发皿中进行,C正确;D.氢氧化钠溶液应放在碱式滴定管中,图中为酸式
滴定管,D错误;故答案选D。
3.(2024·安徽滁州·一模)课外实验可以帮助我们更好地学习化学知识。金属活动性强弱的探究过程如
下,其中不正确的是(已知:白醋的水溶液显酸性,与稀盐酸的化学性质相似)
A.实验一证明铁的金属活动性比铜强
B.实验二的现象是铜丝不断减少,表面有银白色固体析出,无色溶液变为黄色
C.实验一烧杯②中发生的是置换反应
D.实验过程中存在不规范操作
【答案】B
【解析】A.实验一根据放铜片的烧杯内无现象,而放铁片的烧杯内有气体冒出且溶液变为浅绿色,说明
铜不能与醋中的醋酸反应,而铁与醋酸反应,则铁的金属活动性比铜强,故A正确;B.实验二铜与硝酸
银能反应生成硝酸铜和银,故现象是铜丝表面有银白色固体析出,无色溶液变为蓝色,故B错误;C.实
验一烧杯②中铁与醋酸反应后会生成亚铁盐和氢气,属于置换反应,故C正确;D.实验一向放铜片的烧
杯中加入白醋时,胶头滴管应正立于烧杯口的正上方,不能伸到烧杯内与内壁接触,操作不规范,故D正
确;故选B。
4.(23-24高三上·江苏·开学考试)铜及其重要化合物在生产中有着重要的应用。辉铜矿(主要成分 Cu S)
2
可以用于制铜,反应为Cu S +O 2Cu+SO,制得的粗铜通过电解法进行精炼。Cu S与浓硝酸反应可得
2 2 2 2
Cu(NO )。Cu在O 存在下能与氨水反应生成[Cu(NH )]2+。Cu O加入到稀硫酸中,溶液变蓝色并有紫红色
3 2 2 3 4 2
固体产生,下列说法正确的是
A.电解精炼铜时阴极反应:Cu-2e-=Cu2+
B.Cu S与浓硝酸反应Cu S+6HNO (浓) 2Cu(NO )+2NO↑+H S↑+HO
2 2 3 3 2 2 2 2
C.Cu O溶于稀硫酸:Cu O+2H+=Cu+Cu2++H O
2 2 2
D.Cu在O 存在下与氨水反应:2Cu+8NH+O +4H+=2[Cu(NH)]2++2H O
2 3 2 3 4 2
【答案】C
【解析】A.电解精炼铜时阴极上Cu2+得到电子被还原为Cu单质,电极反应:Cu2+ +2e-=Cu,A错误;
B.浓硝酸具有强氧化性,与Cu S反应不能产生具有还原性的HS气体,Cu S与浓硝酸反应会产生
2 2 2Cu(NO )、NO 、HSO 、HO,反应的化学方程式为:Cu S+14HNO (浓)
3 2 2 2 4 2 2 3
2Cu(NO )+10NO↑+H SO +6H O,B错误;C.Cu O溶于稀硫酸,在酸性条件下发生歧化反应产生Cu、
3 2 2 2 4 2 2
CuSO 、HO,反应的离子方程式为Cu O+2H+=Cu+Cu2++H O,C正确;D.氨水显碱性,不能大量存在
4 2 2 2
H+,反应的离子方程式为2Cu+8NH+O +2H O =2[Cu(NH )]2++4OH-,D错误;故合理选项是C。
3 2 2 3 4
5.(2024·广东汕头·二模)为解决铜与稀硝酸反应过程中装置内氧气对实验现象的干扰,以及实验后装置
内氮氧化物的绿色化处理问题。某实验小组对装置进行微型化改造,设计如图所示的装置(试管底部有孔
隙)。下列说法错误的是
A.装置内发生的化学反应方程式为:
B.实验开始前需除去试管内的氧气,可拉动注射器B
C.该装置可通过控制止水夹和注射器来控制反应的开始与停止
D.实验终止时,需将铜丝提拉上来后再拉动注射器A
【答案】B
【解析】A.装置内铜与稀硝酸反应,即 ,故A正确;B.实验
开始时先拉注射器A活塞,其目的是除去反应前试管内的空气,故B错误;C.该实验装置可通过控制止
水夹和注射器来控制反应的开始与停止,故C正确;D.反应停止后,提拉粗铜丝,使粗铜丝下端靠近软
胶塞A,再打开止水夹,缓慢拉注射器A活塞,可观察到试管内的无色气体被吸入注射器A内,试管内稀
硝酸液面逐渐上升,注射器B活塞缓慢向内移动,如不提拉铜丝会继续反应,故D正确;故答案选B。
6.(2024·湖南·二模)将含氧化铜的矿石与焦炭混合,在高温条件下可以冶炼金属铜,该冶炼方法属于
A.电解冶炼法 B.热还原法 C.热分解法 D.物理分离法
【答案】B
【解析】冶炼金属铜的反应为氧化铜与焦炭在高温条件反应生成铜和一氧化碳,该冶炼方法属于热还原
法,故选B。
题型二 金属材料及金属矿物的开发利用
7.(2024·浙江·三模)下列物质不能用作金属冶炼还原剂的是
A.C B.CO C. D.S
【答案】D
【解析】S与金属反应生成硫化物,不能作金属冶炼的还原剂,能用作金属冶炼还原剂的是还原剂C、H、CO。故本题选D。
2
8.(2024·河北张家口·三模)《天工开物》中记载了提炼金银的过程:“欲去银存金,则将其金打成薄
片,剪碎,每块以土泥裹涂,入坩埚中硼砂熔化,其银即吸入土内,让金流出,以成足色。”下列说法错
误的是
A.金的密度比银大 B.薄片的成分为金银合金
C.金银的延展性较好 D.硼砂的作用是使银被氧化
【答案】D
【解析】A.金单质的密度比银单质的密度大,A正确;B.欲去银存金,则将其金打成薄片,说明薄片中
含有金银,为金银合金,B正确;C.“打成薄片”反映了金属良好的延展性,C正确;D.硼砂的作用是
帮助熔化,不和银发生化学反应,D错误;故选D。
9.(2024·安徽滁州·一模)“中国制造”、“一带一路”的基础设施建设都需要用到大量钢铁。下列有关
钢铁的说法正确的是
A.钢是纯净物,生铁是合金 B.钢铁在潮湿的空气中容易生锈
C.生铁的熔点比纯铁高 D.生锈的钢铁制品没有回收价值
【答案】B
【解析】A.钢和生铁都是铁的合金,都属于混合物,A不符合题意;B.铁生锈的条件是铁与氧气和水接
触,故钢铁在潮湿的空气中容易生锈,B符合题意;C.生铁是铁的合金,合金比组成它的纯金属的熔点
低,故生铁的熔点比纯铁低,C不符合题意;D.生锈的钢铁,可以回收利用,D不符合题意;故选B。
10.(2024·安徽池州·二模)今年是我国传统文化中的龙年。龙的图腾最早可追溯到距今约6400年的仰韶
文化,仰韶文化中的龙是由贝壳拼成的蚌壳龙;距今约5000年的红山文化中,有龙形玉器;现发行的龙年
纪念硬币有金、银、合金等多种规格。以下说法正确的是
A.蚌壳的主要成分是硫酸钙,可用来烧石灰
B.玉是含水的钙镁硅酸盐,硬度大,不怕摔
C.合金属于金属材料,熔点一般低于各组分
D.“真金不怕火来炼”,是指金的熔点很高
【答案】C
【解析】A.蚌壳的主要成分是碳酸钙,故A错误;B.玉是含水的钙镁硅酸盐,硬度大,但脆易碎,怕
摔,故B错误;C.合金是两种或两种以上的金属或金属与非金属熔合而成的金属材料,熔点低于组分熔
点,故C正确;D.“真金不怕火来炼”是指金的性质稳定,不与其他物质反应,不易变色,并非指熔点
高,故D错误;故选:C。
11.(2024·湖南岳阳·一模)化学在科技强国中发挥着重要作用。下列有关叙述正确的是
A.铝合金中硬铝密度小,强度高,常用于制造飞机外壳
B.二氧化硅广泛用于航天器太阳能电池板
C.液氧甲烷运载火箭中的甲烷是烃的衍生物
D.医用无纺布防护服中常用聚乙烯作原料,聚乙烯属于天然纤维
【答案】A
【解析】A.硬铝密度小、强度高,适用于制造飞机外壳,A正确;B.单质硅广泛用于航天器太阳能电池板,B错误;C.液氧甲烷运载火箭中的甲烷属于烃,C错误;D.医用无纺布防护服中常用聚乙烯作原
料,聚乙烯属于合成纤维,D错误;故选A。
12.(2024·浙江绍兴·三模)回收铝制饮料罐得到铝与从铝土矿制铝相比,前者能耗仅为后者的3%-5%,
下列说法不正确的是
A.铝制饮料罐的回收再利用可以节约大量能源,缓解能源紧张的问题
B.铝表面容易生成一层致密的氧化铝保护膜
C.硬铝的硬度大但强度较小,不适合制造飞机的外壳
D.电解熔融Al O 时加入冰晶石,目的是降低Al O 的熔化温度
2 3 2 3
【答案】C
【解析】A.从题干信息可知,从铝土矿制铝能耗大,回收铝制饮料罐得到铝耗能小,A正确;B.铝易与
氧气反应,表面容易生成一层致密的氧化铝保护膜,B正确;C.硬铝的硬度大、强度大、密度小,适合
制造飞机的外壳,C错误;D.电解熔融Al O 时加入冰晶石,目的是降低Al O 的熔化温度,D正确;答
2 3 2 3
案选C。
13.(2024·湖南·模拟预测)某课外小组为探究金属铜的还原性,进行如下实验:①将金属铜投入用
酸化的 的 溶液中,现象不明显②将金属铜投入用盐酸酸化的 的
溶液中,铜粉溶解,溶液变为蓝绿色③将金属铜投入用 酸化的 的
溶液中,铜粉溶解,溶液变为深棕色[经检验含 ],无气泡生成。下列分析正
确的是
A.①说明 的 溶液不与铜粉反应
B.②证明氧化性 还原性
C.③中 的生成速率一定小于 被还原的速率
D.在①中加入少量绿矾,铜粉可溶解,溶液变为深棕色
【答案】D
【分析】铜与浓硝酸、稀硝酸均可以发生反应,生成硝酸铜,而在酸性条件下,硝酸根具有强氧化性,据
此作答。
【解析】A.实验①可能因为 的 溶液与铜粉反应慢,现象不明显,A错误;B.②中发生反应
,根据氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的
还原性,氧化性 ,还原性 ,B错误;C.③中发生反应a. ,反应b. 、反应c. ,由题干知③中无气泡产
生,则说明反应b的反应速率小于或等于反应c,即 的生成速率大于或等于 被还原的速率,
C错误;D.在①中加入少量绿矾,根据C项,先发生反应b产生 , 再与铜反应,故铜粉可溶
解,溶液变为深棕色,D正确;故答案选D。
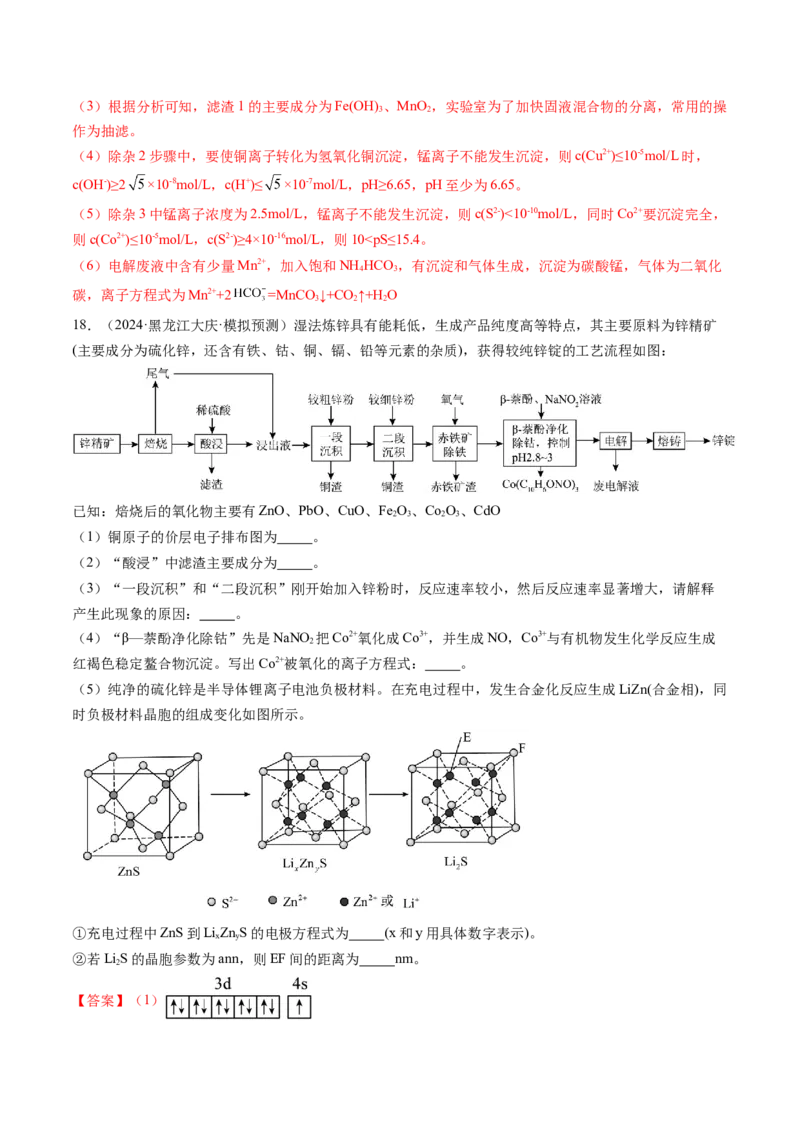
14.(2024·广西贵港·模拟预测)镁及其合金是用途很广的金属材料。从海水中获取镁的主要步骤如图所
示:
下列说法错误的是
A.试剂①可以选用 (或 ),试剂②可以选用
B.操作Ⅱ是蒸发浓缩至有大量晶体析出、趁热过滤、洗涤、干燥
C.实验室熔融无水 (熔点: )时需酒精喷灯、三脚架、泥三角、坩埚和坩埚钳等仪器
D.无水 电解生成镁的化学方程式为
【答案】B
【分析】海水中加入试剂①氢氧化钙沉淀镁离子生成氢氧化镁沉淀,操作Ⅰ为过滤操作,过滤后在氢氧化
镁沉淀中加入试剂②盐酸溶解,得到氯化镁溶液,通过操作Ⅱ浓缩蒸发,冷却结晶得到氯化镁晶体,在氯
化氢气流中加热失水得到无水氯化镁,电解熔融氯化镁得到金属镁,据此分析解。
【解析】A.分析可知试剂①可以选用的试剂为氢氧化钙溶液或者NaOH,用来沉淀镁离子,试剂②可以
选用稀盐酸或SOCl ,SOCl水解后生成HCl与SO ,A正确;B.操作Ⅱ是蒸发浓缩、冷却结晶、过滤、
2 2
洗涤、干燥得到MgCl ·6H O,B错误;C.实验室熔融无水MgCl (熔点:712°C)时需酒精喷灯、三脚架、
2 2 2
泥三角、坩埚和坩埚钳等仪器,C正确;D.无水MgCl 电解生成镁的化学方程式为:
2
,D正确;故选B。
15.(2024·辽宁朝阳·二模)钛铁矿( FeTiO )制取金属钛的流程如图所示(已知TiCl 为无色液体,极易水
3 4
解;Ti3+的还原性强于Fe2+)下列说法正确的是
A.钛铁矿( FeTiO )中Ti的化合价是+3
3
B.氯化过程中反应2FeTiO+6C+7Cl 2FeCl +6CO+ 2TiCl
3 2 3 4
C.镁与TiCl 置换时可以用氮气做保护气
4
D.制取金属钛时可以用Na与TiCl 溶液反应
4
【答案】B
【分析】FeTiO 中加入焦炭,再通入Cl,焦炭被氧化为CO,FeTiO 转化为FeCl 、TiCl ;再加入Mg粉,
3 2 3 3 4
在Ar存在的环境中加热至800℃,可制得Ti。
【解析】A.Ti3+的还原性强于Fe2+,则Fe3+能将Ti3+氧化为Ti4+,所以钛铁矿( FeTiO )中Ti的化合价是+4
3
价,A不正确;B.氯化过程中,Cl 将C氧化为CO,Fe2+氧化为Fe3+,则发生反应2FeTiO+6C+7Cl
2 3 2
2FeCl +6CO+ 2TiCl ,B正确;C.镁是活泼的金属元素,能与氮气反应生成氮化镁,则镁与TiCl 置换时
3 4 4
不能用氮气做保护气,C不正确;D.Na能与水反应,则制取金属钛时可以用Na与TiCl 的熔融液反应,
4
不能使用TiCl 的水溶液,D不正确;故选B。
4
16.(2024·广西河池·二模)铝电解厂烟气净化的一种简单流程如图所示。下列有关说法正确的是
A.不宜用陶瓷等硅酸盐产品作吸收塔内衬材料
B.吸收塔中发生的反应为
C.合成槽中发生的反应为
D.冰晶石可作为工业上电解熔融氯化铝制取金属铝时的助熔剂
【答案】A
【分析】烟气中的HF吸收塔中发生的反应为 ,合成槽中发生的反应为
,过滤后得到产物冰晶石。
【解析】A.硅酸盐产品能与烟气中的HF发生反应,故不宜用陶瓷等硅酸盐产品作吸收塔内衬材料,A正
确;B. 溶液过量,故吸收塔中发生的反应为 ,B错误;C.合成槽
中发生的反应为 ,C错误;D.冰晶石可作
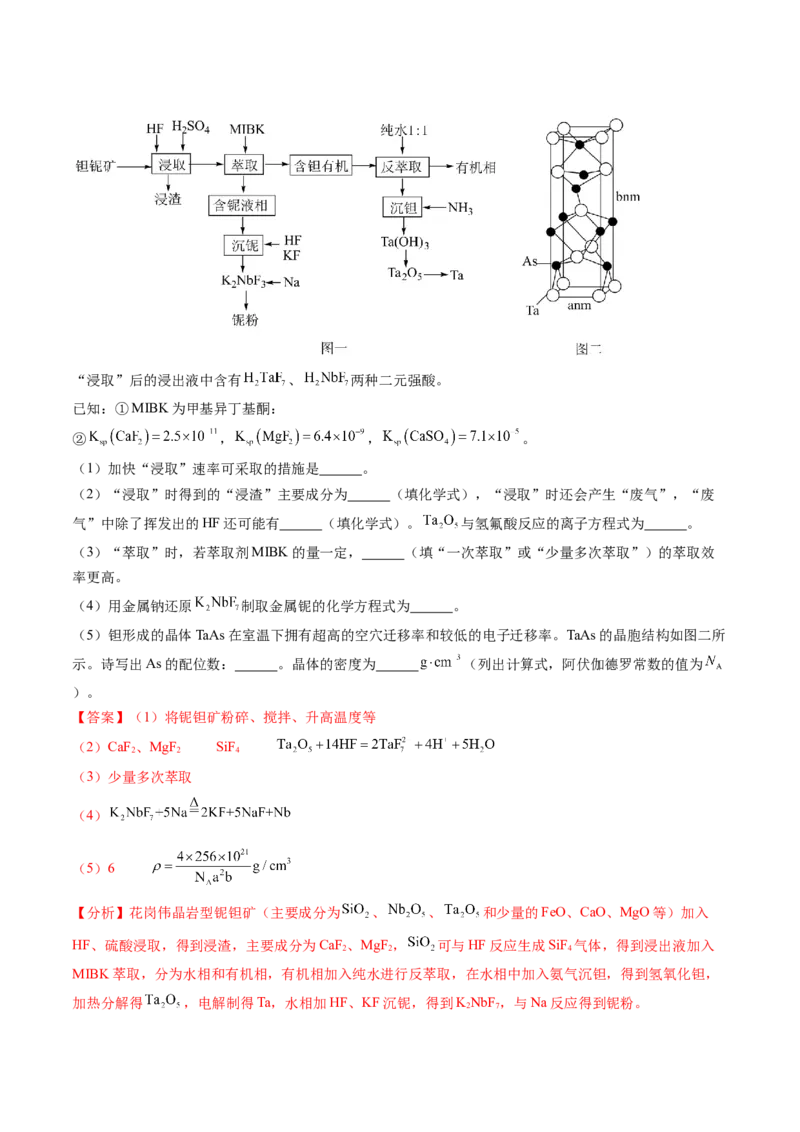
为工业上电解熔融氧化铝制取金属铝时的助熔剂,不是电解熔融氯化铝,D错误;故答案选A。17.(2024·山东聊城·三模)锰是生产各种合金的重要元素。工业上以含锰矿石(主要成分为 ,还含
有铁钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如下:
25℃时,部分物质的溶度积常数如下表所示。
物质 MnS CoS
回答下列问题:
(1)用硫酸浸取含锰矿石时,提高浸取速率的方法有 (写两种)。
(2)“氧化”步骤发生反应的离子方程式为 。
(3)滤渣1的主要成分是 ,实验室中为了加快固液混合物的分离,常采用的操作是 。
(4)当溶液中可溶组分浓度 时,可认为已除尽。“除杂2”步骤需要控制溶液的pH至少
为 (已知 )。
(5)“除杂3”步骤所得溶液中 ,则其 的范围是 。
(6)电解废液中还含有少量 ,向其中加入饱和 溶液,有沉淀和气体生成,该反应的离子
方程式为 。
【答案】(1)将矿石粉碎、适当提高硫酸浓度,适当提高温度等
(2)MnO +4H++2Fe2+=2Fe3++Mn2++2H O
2 2
(3)Fe(OH) 、MnO 抽滤
3 2
(4)6.65
(5)10