文档内容
第 05 讲 物质的量浓度及溶液配制
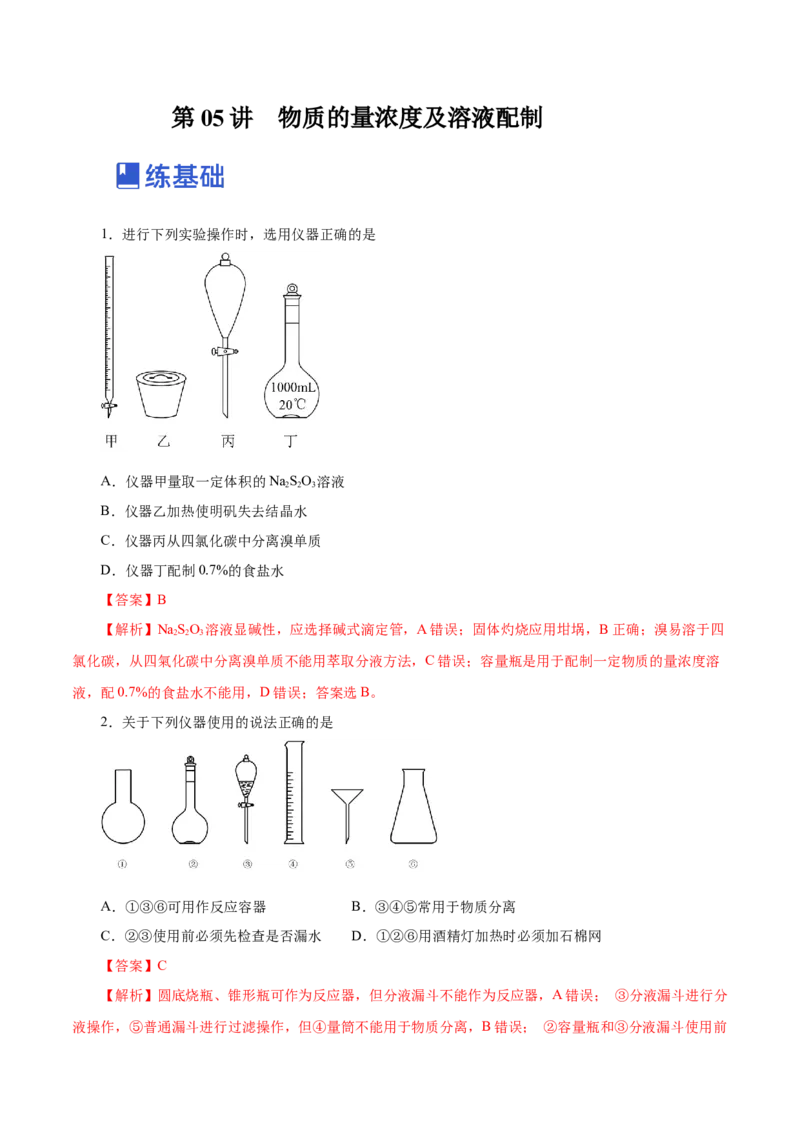
1.进行下列实验操作时,选用仪器正确的是
A.仪器甲量取一定体积的NaSO 溶液
2 2 3
B.仪器乙加热使明矾失去结晶水
C.仪器丙从四氯化碳中分离溴单质
D.仪器丁配制0.7%的食盐水
【答案】B
【解析】NaSO 溶液显碱性,应选择碱式滴定管,A错误;固体灼烧应用坩埚,B正确;溴易溶于四
2 2 3
氯化碳,从四氣化碳中分离溴单质不能用萃取分液方法,C错误;容量瓶是用于配制一定物质的量浓度溶
液,配0.7%的食盐水不能用,D错误;答案选B。
2.关于下列仪器使用的说法正确的是
A.①③⑥可用作反应容器 B.③④⑤常用于物质分离
C.②③使用前必须先检查是否漏水 D.①②⑥用酒精灯加热时必须加石棉网
【答案】C
【解析】圆底烧瓶、锥形瓶可作为反应器,但分液漏斗不能作为反应器,A错误; ③分液漏斗进行分
液操作,⑤普通漏斗进行过滤操作,但④量筒不能用于物质分离,B错误; ②容量瓶和③分液漏斗使用前必须先检查是否漏水,C正确;①圆底烧瓶和⑥锥形瓶用酒精灯加热时必须加石棉网,而②容量瓶不能加
热,D错误;故答案为C。
3.下列图示实验操作正确的是
A.①配制一定物质的量浓度的稀硫酸 B.②给试管中液体加热
C.③称量一定质量的食盐 D.④检查装置的气密性
【答案】D
【解析】配制一定物质的量浓度的稀硫酸,不能把浓硫酸直接倒入容量瓶,故A错误;给试管中液体
加热,液体体积一般不超过试管容积的三分之一,故B错误;称量一定质量的食盐,食盐放在托盘天平的
左盘,砝码放在托盘天平的右盘,故C错误;用手握住试管,若右侧管口有气泡、松手后右侧导管内有一
段水柱产生,说明气密性良好,故D正确;故选D。
4.已知10 mL某NaR溶液含Na+的数目为N,该NaR溶液的物质的量浓度为( )
2 2
A.N×10-2 mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
【答案】B
【解析】10 mL该NaR溶液中含Na+的数目为N,NaR的物质的量= mol,NaR的物质的量浓度=
2 2 2
mol÷0.01 L= mol·L-1。
5.将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到500 mL,关于稀释后的溶液叙述不正确的是( )
A.浓度为0.03 mol·L-1
B.从中取出10 mL溶液,其浓度为0.03 mol·L-1
C.稀释后的溶液中含NaOH 0.6 g
D.从中取出10 mL溶液,含NaOH 0.015 mol
【答案】D
【解析】溶液稀释前后溶质的物质的量不变。从一定物质的量浓度的溶液中取出任意体积的溶液,其
浓度不变,但所含溶质的物质的量或质量因体积的不同而不同。
6.某同学用碳酸钠配制0.10 mol·L-1 碳酸钠溶液的过程如图所示。你认为该同学的错误有( )A.①⑤⑥ B.②④⑦
C.①⑥⑦ D.⑤⑥⑦
【答案】C
【解析】称量碳酸钠固体时,应将被称量物放在托盘天平的左盘,砝码放在右盘,①错误;定容时,
视线应与凹液面最低处相切,⑥错误;摇匀时,应将容量瓶反复上下颠倒而不是左右摇,⑦错误,故 C项
正确。
7.某化学小组的同学要配制500mL0.6mol/L的NaOH溶液,具体操作如下:①用托盘天平称取
12.0g NaOH固体时所用时间较长;②向小烧杯中加水使氢氧化钠溶解并冷却至室温;③把溶液转移到洗
净但未干燥的容量瓶中,洗涤烧杯和玻璃棒三次并将洗涤液也转移到容量瓶中,振荡摇匀;④向容量中加
水定容,定容时俯视刻度线;⑤定容后塞上容量瓶塞子,上下颠倒摇匀,摇匀后发现液面低于刻度线,用
胶头滴管补加蒸馏水至刻度线。以上操作中会使所得溶液浓度偏低的有几项?
A.1 B.2 C.3 D.4
【答案】B
【解析】①氢氧化钠易潮解,称量时所用时间较长会导致称取的氢氧化钠中含部分水,氢氧化钠的量
偏少,①所得溶液浓度偏低;②操作正确,对溶液浓度无影响;③容量瓶不需要干燥,③操作正确,对溶
液浓度无影响;④定容时俯视刻度线会使溶液体积偏小,④所得溶液浓度偏高;⑤上下颠倒摇匀后液面低
于刻度线对浓度无影响,补加蒸馏水会使溶液稀释,⑤所得溶液浓度偏低。综上所述①⑤所得溶液浓度偏
低,因此答案选B。
8.用NaCl固体配制0.1 mol·L-1的NaCl溶液,下列操作或说法正确的是( )
A.将5.85 g NaCl固体放入1 000 mL容量瓶中,加水溶解并准确定容
B.称量时,将固体NaCl直接放在天平左盘上
C.固体溶解、冷却后将溶液直接转移到容量瓶中,然后向容量瓶中加水至刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
【答案】D
【解析】A项,固体应在烧杯中溶解,容量瓶不能用来稀释溶液或溶解固体;B项,称量固体NaCl时
不能直接放在天平左盘上,应放在称量纸上;C项,配制一定物质的量浓度的溶液时,转移溶液后需用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移至容量瓶中,然后再加蒸馏水,当加水至距离刻度线 1~
2 cm处时,要改用胶头滴管定容,不能直接加水至刻度线。
9.实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验用品及实验操作正确的是( )
选项 容量瓶容积 溶质质量 实验操作
A 480 mL 硫酸铜:7.68 g 加入500 mL水
B 480 mL 胆矾:12.0 g 配成500 mL溶液
C 500 mL 硫酸铜:8.0 g 加入500 mL水
D 500 mL 胆矾:12.5 g 配成500 mL溶液
【答案】D
【解析】实验室里需要配制480 mL 0.10 mol·L-1 CuSO 溶液,由于没有480 mL规格的容量瓶,根据
4
“大而近”的原则故需选择500 mL 容量瓶,溶质若为CuSO 则需要8.0 g,若溶质为胆矾则需要12.5 g。
4
应配成500 mL溶液而不是加入500 mL水。
10.实验室配制0.1 mol·L-1 的氯化钡溶液。
第一阶段:用托盘天平称取5.2 g无水BaCl 晶体。
2
第二阶段:溶解,配制0.1 mol·L-1的BaCl 溶液。
2
第一阶段操作有如下几步:A.将游码拨至0.2处;B.将游码拨至“0”处;C.在天平两边的托盘上各放一
张干净的等质量的称量纸,调节天平两边的螺母使天平平衡;D.取走药品,将砝码放回砝码盒内;E.向左
盘内逐步添加晶体至天平平衡;F.在右盘上放置5 g砝码。
(1)正确的操作顺序是B→________→________→A→________→________→________。
(2)E操作的具体方法是_________________________________________________________________。
(3)第二阶段操作中,应先将 5.2 g BaCl 加适量蒸馏水溶解,溶解过程中使用的主要仪器有
2
________________、________。冷却后将溶液转入______________中,再经________、________、
________、__________后即可得到0.1 mol·L-1的BaCl 溶液。
2
(4)下列操作使配制的BaCl 溶液浓度偏低的有______(填字母)。
2
A.将砝码放在左盘上,BaCl 放在右盘上进行称量
2
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
【答案】(1)C F E D B
(2)左手拿药匙,用右手轻轻拍左手手腕,小心振动药匙添加样品,直到天平平衡
(3)烧杯 玻璃棒 250 mL容量瓶 洗涤 振荡 定容 摇匀
(4)AC
【解析】(1)使用托盘天平的步骤为调零→放砝码→调游码→加物品→取物品→取砝码→游码回零。(3)溶解所需的主要仪器有烧杯、玻璃棒。(4)误差分析可根据c==,由m、V的大小判断。A项,将砝码放
错位置后,称得的BaCl 为4.8 g,所得溶液的浓度偏低;B项,无影响;C项,摇匀后再加水,即增大了
2
溶液的体积,所得溶液的浓度偏低。
11.实验室欲用NaCO·10H O晶体配制100 mL 1 mol·L-1的NaCO 溶液,下列说法正确的是( )
2 3 2 2 3
A.要完成实验需称取10.6 g Na CO·10H O晶体
2 3 2
B.本实验需用到的仪器有托盘天平、药匙、玻璃棒、烧杯、500 mL容量瓶
C.配制时若容量瓶不干燥,含有少量蒸馏水会导致溶液浓度偏低
D.定容时俯视刻度线会导致溶液浓度偏高
【答案】D
【解析】配制100 mL 1 mol·L-1的NaCO 溶液,需要NaCO·10H O晶体的质量m=1 mol·L-1×286
2 3 2 3 2
g·mol-1×0.1 L=28.6 g,A项错误;定容时,需要向容量瓶中加入蒸馏水,所以配制时若容量瓶不干燥,含
有少量蒸馏水对溶液浓度无影响,C项错误;定容时俯视刻度线,导致溶液体积偏小,依据c=可知溶液
浓度偏高,D项正确。
12.欲配制500 mL 2 mol·L-1的盐酸,需要36.5%的浓盐酸(密度约为1.2 g·cm-3)的体积为( )
A.27.4 mL B.83.3 mL
C.120 mL D.无法计算
【答案】B
【解析】溶液稀释时溶液的物质的量不变,0.500 L×2 mol·L-1=,V≈83.3 mL。
13.把V L含有MgSO 和KSO 的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁
4 2 4
离子完全沉淀为氢氧化镁;另一份加入含 b mol BaCl 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则
2
原混合溶液中钾离子的浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
【答案】D
【解析】由离子方程式:2OH-+Mg2+===Mg(OH) ↓可知,OH-为a mol,则Mg2+为 mol,MgSO 为
2 4
mol;由离子方程式:SO+Ba2+===BaSO ↓可知,Ba2+为b mol, SO为b mol,MgSO 和KSO 共b mol,
4 4 2 4
则KSO 为mol,其含有的K+为mol×2=(2b-a) mol;原混合溶液中的K+为2×(2b-a)mol,所以原混合溶
2 4
液中钾离子的浓度为 mol·L-1。
14.使用容量瓶配制溶液时,由于操作不当,会引起误差。下列情况一定会使所配溶液浓度偏低的是()
①用天平称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③转移溶液前容量瓶内有少量蒸馏水
④定容时,仰视容量瓶的刻度线
⑤定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①②⑤ B.②④⑤
C.③④⑤ D.①②④⑤
【答案】B
【解析】天平称量时使用游码,被称量物与砝码的位置放颠倒了,物质的质量=砝码的质量-游码的
质量,质量偏小,浓度偏低,若不使用游码,物质的质量=砝码的质量,对质量无影响,浓度不变;定容
时,仰视容量瓶的刻度线,体积偏大,浓度偏低;定容后摇匀,发现液面降低,又补加少量水,重新达到
刻度线,体积偏大,浓度偏低。
15.下列有关溶液浓度的说法正确的是( )
A.将500 mL 1 mol·L-1的硝酸溶液蒸发至100 mL,浓度变为5 mol·L-1
B.将10 mL 18.4 mol·L-1浓硫酸与90 mL水混合,得到的稀硫酸浓度为1.84 mol·L-1
C.配制1 mol·L-1KAl(SO ) 溶液100 mL,应称取明矾晶体47.4 g
4 2
D.实验室需要450 mL 0.2 mol·L-1的NaOH溶液,应准确称量烧碱3.6 g
【答案】C
【解析】硝酸易挥发,加热蒸发硝酸溶液,硝酸物质的量减少,A错误;混合后溶液体积小于 100
mL,稀硫酸浓度大于1.84 mol·L-1,B错误;称取明矾晶体[KAl(SO)·12H O]0.1 mol,即47.4 g,C正确;
4 2 2
需要450 mL溶液应配制500 mL溶液,应称量4.0 g NaOH,D错误。
16.下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的NaSO 溶液中含有Na+和SO的总物质的量为0.9 mol
2 4
B.50 mL 1 mol·L-1的KCl溶液和100 mL 0.25 mol·L-1 MgCl 溶液中,Cl-物质的量浓度相等
2
C.将10 mL 1 mol·L-1的HSO 稀释成0.1 mol·L-1的HSO ,可向其中加入100 mL水
2 4 2 4
D.20 ℃时,0.023 mol·L-1的氢氧化钙饱和溶液100 mL加入5 g生石灰,冷却到 20 ℃时,其体积小
于100 mL,它的物质的量浓度仍为0.023 mol·L-1
【答案】D
【解析】A项,溶液体积未知,不能计算离子物质的量,错误;B项,Cl-的物质的量浓度不相等,错
误;C项,所得稀硫酸的体积为100 mL,所加水的体积不是100 mL,错误;D项,温度恢复到20 ℃时,仍为氢氧化钙的饱和溶液,溶液体积减小,同温下同种溶质在同种溶剂中的饱和溶液的浓度不变,故 D正
确。
17.利用碳酸钠晶体(Na CO·10H O)来配制0.5 mol·L-1的碳酸钠溶液1 000 mL,假如其他操作均是准
2 3 2
确无误的,下列情况会引起配制溶液的浓度偏高的是( )
A.称取碳酸钠晶体100.0 g
B.定容时俯视刻度线
C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D.移液前,容量瓶中有少量蒸馏水
【答案】B
【解析】0.5 mol·L-1的碳酸钠溶液1 000 mL需称取NaCO·10H O 143.0 g,结果偏低,A不符合题
2 3 2
意;定容时俯视刻度线,会造成所配溶液的体积偏小,结果偏高,B符合题意;未冲洗溶解碳酸钠晶体的
烧杯,会造成碳酸钠损失,结果偏低,C不符合题意;容量瓶中有少量蒸馏水对所配溶液的浓度无影响,
D不符合题意。
18.实验小组用双指示剂法准确测定NaOH样品(杂质为Na CO )的纯度。步骤如下:
2 3
①称取m g样品,配制成100mL溶液;
②取出25mL溶液置于锥形瓶中,加入2滴酚酞溶液,用浓度为cmol⋅L−1的盐酸滴定至溶液恰好褪色
(溶质为NaCl和NaHCO ),消耗盐酸体积为V mL;
3 1
③滴入2滴甲基橙溶液,继续滴定至终点,消耗盐酸体积为V mL。
2
下列说法正确的是
A.①中配制溶液时,需在容量瓶中加入100mL水
B.②中溶液恰好褪色时:c(Na+)=c(HCO-)+2c(CO2-)+c(Cl-)
3 3
4c(V -V )×40
C.NaOH样品纯度为 1 2 ×100%
1000m
D.配制溶液时放置时间过长,会导致最终测定结果偏高
【答案】C
【解析】①中配制溶液时,在容量瓶中定容时溶液总体积为100mL,A错误;②中溶液恰好褪色时溶
质为NaCl和NaHCO ,由电荷守恒可知,c(Na+)+c(H+)=c(HCO-)+2c(CO2-)+c(Cl-)+c(OH-),此时溶液显
3 3 3
碱性,则氢氧根离子浓度大于氢离子浓度,故,c(Na+)>c(HCO-)+2c(CO2-)+c(Cl-);B错误;第1次滴定
3 3反应为OH-+H+=H O、CO2- +H+= HCO- ,第2次滴定反应为HCO❑ − +H+=H O+CO↑,则通过第2次滴定可
2 3 3 3 2 2
知,n(CO2- )=n(HCO❑ − )=cV ×10-3mol,第1次滴定中氢氧化钠消耗HCl的物质的量的为n(HCl) = cV ×10-
3 3 2 1
3mol -cV×10-3mol= c (V -V )×10-3mol=n(NaOH),故NaOH样品纯度为
2 1 2
100mL
c(V -V )×10−3mol× ×40g/mol
1 2 25mL ×100%= 4c(V 1 -V 2 )×40 ×100% ,C正确;配制溶液时放置时
mg 1000m
间过长,氢氧化钠吸收空气中二氧化碳生成碳酸钠,会导致最终测定结果偏低,D错误;故选C。
19.浓盐酸易挥发,无法直接配制具有准确浓度的标准溶液,因此配制HCl标准溶液的具体流程如
下:
按上述流程进行操作,下列仪器中不需要用到的有
A.1种 B.2种 C.3种 D.4种
【答案】A
【解析】配制一定物质的量浓度溶液需要的玻璃仪器:量筒、烧杯、玻璃棒、容量瓶、胶头滴管,准备
基准物质需要的仪器:托盘天平、量筒、烧杯、玻璃棒,中和滴定用到的仪器:酸式滴定管、碱式滴定管、
烧杯、锥形瓶,所以该实验用不到的仪器为试管;答案选A。
20.用质量分数为36.5%的浓盐酸(密度为1.16 g·cm-3)配制成1 mol·L-1的稀盐酸。现实验室仅需要这
种盐酸220 mL,试回答下列问题:
(1)配制稀盐酸时,应选用容量为________mL的容量瓶。
(2)经计算需要________mL浓盐酸,在量取时宜选用下列量筒中的________(填字母)。
A.5 mL量筒 B.10 mL量筒C.25 mL量筒 D.50 mL量筒
(3)在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸的温度与室温一致后,沿玻璃棒注入选定规格的容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的液
面与瓶颈的刻度线相切。
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是________(填序号)。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,则配制的稀盐酸浓度________(填“偏
高”“偏低”或“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度
________(填“偏高”“偏低”或“无影响”)。
【解析】(2)c(HCl)== mol·L-1=11.6 mol·L-1。加水稀释前后HCl的物质的量不变,所以11.6 mol·L-
1×V(HCl)=250 mL×1 mol·L-1,解得V(HCl)≈21.6 mL,应该选择25 mL量筒量取。
(4)用刚刚洗涤洁净的量筒来量取浓盐酸,量取的盐酸被稀释了,其物质的量偏小,所配制溶液的浓度
偏低;若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则一部分溶质损失,所配制溶液的浓度偏
低。
【答案】(1)250 (2)21.6 C (3)③①④② (4)偏低 偏低