文档内容
第 08 讲 钠及其重要化合物
目录
考性分析 图象
网络构建 知识点4 金属钠露置在空气中发生的一系
列变化
考点一 钠及其氧化物
【提升·必考题型归纳】
【夯基·必备基础知识梳理】
考向1 考查碳酸钠和碳酸氢钠性质与检验
知识点1 钠的性质及应用
考向2 考查侯氏制碱法
知识点2 钠的氧化物与氢氧化物
【提升·必考题型归纳】 考点三 碱金属 焰色试验
考向1 考查钠的性质及其应用 【夯基·必备基础知识梳理】
考向2 考查钠的氧化物及其应用 知识点1 碱金属的一般性与特殊性
知识点2 焰色试验
考点二 碳酸钠、碳酸氢钠
【提升·必考题型归纳】
【夯基·必备基础知识梳理】
考向1 考查碱金属的相似性、递变性
知识点1 Na CO3、NaHCO 的性质、用途
2 3
考向2 考查焰色试验
及制法
知识点2 Na CO 和NaHCO 性质的应用
2 3 3 真题感悟
知识点3 Na CO、NaHCO 与盐酸反应的基本
2 3 3
考点要 考题统计 考情分析
求
钠及其 1.分析近三年高考试题,高考命题在本讲有以下规律:
2023浙江1月5题,2
氧化物 1)从考查题型和内容上看,高考命题以选择题和非选择题呈现,主
分2022浙江6月9题,2 要选择一些重要的金属、非金属化合物或新型化合物结合氧化还原反
分 应、盐类水解、难溶物的溶解平衡等核心考点进行考查。
2021浙江6月9题,2 2)从命题思路上看,高考试题中元素化合物不单独出现,而是分散
分 到不同题型和题目中。选择题一般直接考查元素化合物的性质和应
2023浙江1月7题,2 用,填空题一般有两种形式,一是直接考查元素及其化合物的性质,
碳酸钠
分 通常以物质的判断、化学式的书写、微粒的检验和鉴定等形式;二是
碳酸氢
2022广东卷6题,2分 与基本概念和基本理论的知识相结合,如氧化还原反应、电化学、实
钠
验、计算等。
2021江苏卷11题,3分
3)新的一年高考可能会在选择题中考查钠与氧气反应时的电子转移
数目、钠与水或乙醇反应的原理、过氧化钠的电子式、过氧化钠的性
质或用途等,题目难度较小。
碱金属 2022海南卷5题,2分
2.根据高考命题的特点和规律,复习时要注意以下几点:
焰色试 2021河北卷5题,3分
1)注重常见金属和非金属元素及其化合物性质,构建知识网络化、系
验 2021海南卷6题,2分
统化的模型。
2)元素化合物是考查基本概念、基本理论、化学实验、化学计算等的
载体。
考点一 钠及其氧化物
知识点1 钠的性质及应用
1.钠的物理性质
_____色,有金属光泽的固体,质地柔软,熔点低(小于100 ℃),密度比水的_____,但比煤油的_____,即ρ(H O)>ρ(Na)>ρ(煤油)。
2
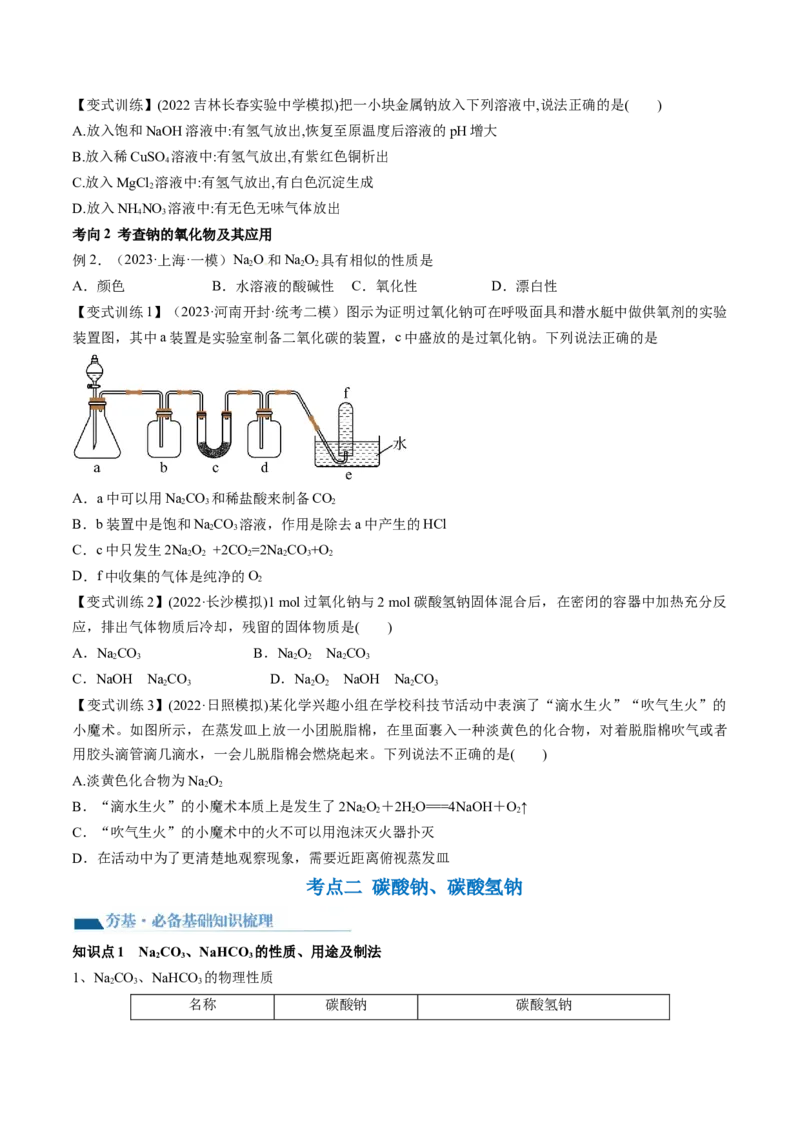
2.从钠原子的原子结构认识钠的化学性质——还原性
Na ―――――――――――→Na+
(1)与非金属单质(如O、Cl)的反应
2 2
O:常温:______________________________,加热:______________________________
2
Cl:___________________________________
2
(2)与水反应
①离子方程式:___________________________________。
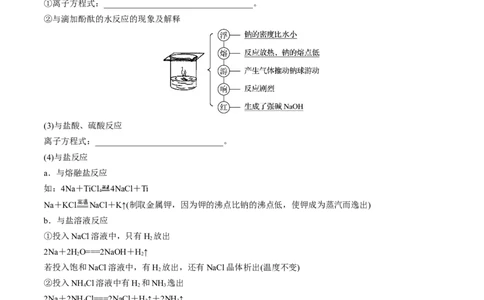
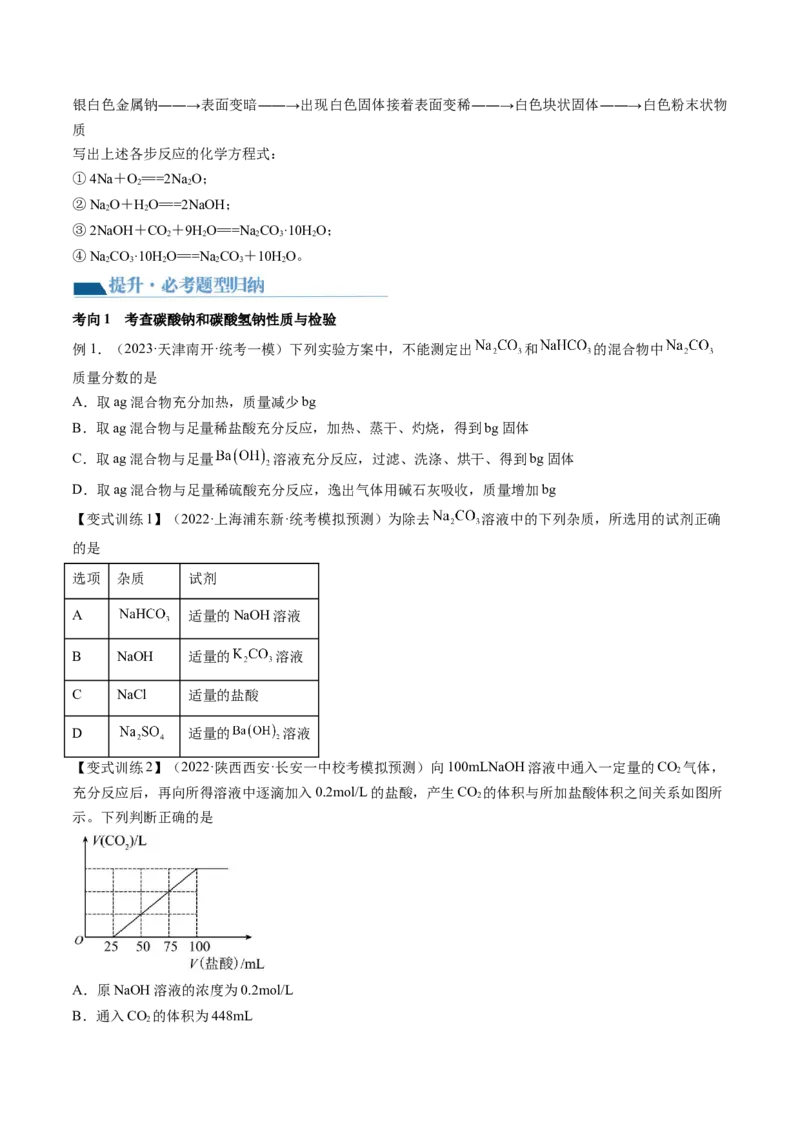
②与滴加酚酞的水反应的现象及解释
(3)与盐酸、硫酸反应
离子方程式:______________________________。
(4)与盐反应
a.与熔融盐反应
如:4Na+TiCl 4NaCl+Ti
4
Na+KCl NaCl+K↑(制取金属钾,因为钾的沸点比钠的沸点低,使钾成为蒸汽而逸出)
b.与盐溶液反应
①投入NaCl溶液中,只有H 放出
2
2Na+2HO===2NaOH+H↑
2 2
若投入饱和NaCl溶液中,有H 放出,还有NaCl晶体析出(温度不变)
2
②投入NH Cl溶液中有H 和NH 逸出
4 2 3
2Na+2NH Cl===2NaCl+H↑+2NH ↑
4 2 3
③投入CuSO 溶液中有H 逸出和蓝色沉淀生成
4 2
2Na+2HO===2NaOH+H↑
2 2
2NaOH+CuSO ===Cu(OH) ↓+NaSO
4 2 2 4
总反应:2Na+CuSO +2HO===Na SO +H↑+Cu(OH) ↓。
4 2 2 4 2 2
(5)与某些有机物(含羟基)反应
如:2Na+2CHCHOH―→2CHCHONa+H↑
3 2 3 2 2
2Na+2CHCOOH―→2CHCOONa+H↑
3 3 2【易错提醒】Na先与酸反应,再与水反应即先酸后水;与盐溶液反应时先与水反应,生成的碱与盐可能发
生复分解反应。
3.钠的制取及保存
(1)工业制取:___________________________________。
(2)保存:密封保存,通常保存在石蜡油或煤油中,钠易与空气中的 O、HO反应,且钠的密度比煤油的密
2 2
度大,不与煤油反应,故通常将少量钠保存在煤油中,大量钠保存在石蜡中。
4.钠的用途
(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属:钠能与钛、锆、铌、钽等氯化物(熔融)发生置换反应,金属钠具有强还原性,熔融状
态下可以用于制取金属,如4Na+TiCl =====4NaCl+Ti。
4
【特别提醒】
1.钠燃烧时不能用水灭火,应用沙土盖灭。
2.取用金属钠时,用镊子夹取金属钠,用滤纸擦干表面的煤油,放在洁净干燥的玻璃片上用小刀切割,
不能用手直接接触金属钠,并且将剩余的钠放回原试剂瓶中保存。
3.钠与溶液反应的共同现象
①浮:钠浮在液面上;②熔:钠熔化成光亮的小球;③游:在液面上不停地游动直至反应完全;④响:反
应中不停地发出“嘶嘶嘶”的响声。若溶液中H+浓度较大,与水相比反应更加剧烈,最后钠可能在液面
上燃烧。
4.钠性质的巧记口诀:银白轻低软,传导热和电;遇氧产物变,遇氯生白烟;遇水记五点,浮熔游响红;
遇酸酸优先,遇盐水在前。
5.考虑钠与酸、碱、盐的水溶液反应时,要注意Na与水反应的同时,生成的NaOH还可能继续与部分溶质
反应。
6.对钠与酸反应的计算问题,勿忽略Na若过量还可与HO反应。
2
知识点2 钠的氧化物与氢氧化物
1.氧化钠与过氧化钠的比较
NaO NaO
2 2 2
电子式
氧元素化合价 -2 -1
色、态 白色固体 淡黄色固体
阴、阳离子个数比 1∶2 1∶2
是否为碱性氧化物 是 不是
与水反应 NaO+HO=2NaOH 2NaO+2HO=4NaOH+O↑
2 2 2 2 2 2与CO 反应 NaO+CO=NaCO 2NaO+2CO=2NaCO+O
2 2 2 2 3 2 2 2 2 3 2
与盐酸反应 NaO+2HCl=2NaCl+HO 2NaO+4HCl=4NaCl+2HO+O↑
2 2 2 2 2 2
用途 氧化剂、供氧剂、漂白剂
2.过氧化钠的性质:
(1)强氧化性的五个表现
说明:①遇KMnO 等强氧化剂时,表现出还原性,氧化产物为__________。
4
②遇HO、H+则发生自身的氧化还原反应。
2
③遇还原性氧化物(即低价非金属氧化物),表现强氧化性,一般不生成氧气,而生成高价钠盐,如
NaO+SO ===Na SO 。
2 2 2 2 4
④遇最高价金属氧化物(酸酐)发生自身的氧化还原反应,有氧气生成,如 2MnO +2NaO===4NaMnO
2 7 2 2 4
+O。
2
⑤无论是过氧化钠还是其他过氧化物,具有强氧化性、漂白性等特殊性质的根本原因是这些物质中都含有
__________键。
(2)理解NaO 强氧化性的两个角度
2 2
①从结构角度
NaO 的结构中含有过氧键(—O—O—),含有过氧键结构的物质有较强的氧化性,以此类推,如 HO 、
2 2 2 2
HSO (过硫酸,相当于HO 中的一个H被—SO H取代)、NaSO(过二硫酸钠)中都有过氧键结构,都是很
2 5 2 2 3 2 2 8
强的氧化剂。
②从化合价的角度
NaO 中的氧元素为-1价,有很强的氧化性,能氧化一些常见的还原剂,如SO 、Fe2+、SO 2-、HSO -、
2 2 2 3 3
HS、S2-、I-。同时-1价的O也有还原性,如遇到强氧化剂KMnO 也可以被氧化成O。
2 4 2
【特别提醒】(1)过氧化钠是常用的工业漂白剂,但是不能用于食品的漂白;
(2)NaO 既有氧化性又有还原性,但主要表现为氧化性。当遇到 KMnO 等强氧化剂时,可表现出还原
2 2 4
性,氧化产物为O;
2
(3)NaO 遇到CO 、HO、H+发生自身氧化还原反应。NaO 既是氧化剂又是还原剂,且1 mol Na O 转
2 2 2 2 2 2 2 2
移的电子是1 mol而不是2 mol。
(4)NaO、NaO 中阴、阳离子个数比均为1∶2。
2 2 2
(5)NaO 与HO、CO 的反应规律
2 2 2 2
当NaO 与CO、HO反应时,物质的量关系为2NaO~O~2e-,n(e-)=n(Na O)
2 2 2 2 2 2 2 2 2
电子转移关系
=2n(O )
2气体体积变化 若CO、水蒸气(或两混合气体)通过足量NaO,气体体积的减少量是原气体体积
2 2 2
关系 的,等于生成氧气的量,ΔV=V(O )=V
2
CO、水蒸气分别与足量NaO 反应时,固体相当于吸收了CO 中的“CO”、水蒸
2 2 2 2
固体质量变化
气中的“H”,所以固体增加的质量Δm(CO)=28 g·mol-1×n(CO)、Δm(H O)=2
2 2 2 2
关系
g·mol-1×n(H O)
2
3.氢氧化钠
(1)物理性质:NaOH的俗名为_____、_____或苛性钠;它是一种白色固体,易溶于水并放出大量的热,有
吸水性;吸收空气中的水分而_____;有很强的_____性。
(2)化学性质
①具有碱的通性:能使酸碱指示剂变色;与强酸反应;与酸性氧化物、两性氧化物反应;与盐反应(强碱
制弱碱)。
②其他反应
与金属铝反应:________________________________________
与非金属单质反应:Cl+2OH-===Cl-+ClO-+HO
2 2
酯类水解:CHCOOC H+NaOH CHCOONa+CHCHOH
3 2 5 3 3 2
(3)NaOH的制取
①实验室(土法)制烧碱:NaCO+Ca(OH) ===CaCO ↓+2NaOH
2 3 2 3
②现代工业制碱:2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
(4)NaOH在有机反应中的应用
提供碱性环境,如卤代烃的水解和消去反应、酯类的水解和油脂的皂化等。
考向1 考查钠的性质及其应用
例1.(2023·北京海淀·统考二模)某小组同学探究溶液中的 能否被金属钠还原,进行实验:
①在干燥试管中加入绿豆大小的金属钠,逐滴滴加 溶液,产生无色气体,溶液由
紫红色变为浅绿色 。
②向 溶液中持续通入 ,水浴加热,溶液颜色无明显变化。
③向 溶液中加入 固体,溶液由紫红色变为浅绿色。
下列说法不正确的是
A.实验①中还可能观察到钠块浮在溶液表面,剧烈燃烧,发出黄色火焰
B.实验②中的现象说明实验①中溶液变色的原因与产生的气体无关
C.实验③中的现象说明实验①中可能发生的反应:
D.上述实验能证明溶液中的 可以被金属钠还原【变式训练】(2022吉林长春实验中学模拟)把一小块金属钠放入下列溶液中,说法正确的是( )
A.放入饱和NaOH溶液中:有氢气放出,恢复至原温度后溶液的pH增大
B.放入稀CuSO 溶液中:有氢气放出,有紫红色铜析出
4
C.放入MgCl 溶液中:有氢气放出,有白色沉淀生成
2
D.放入NH NO 溶液中:有无色无味气体放出
4 3
考向2 考查钠的氧化物及其应用
例2.(2023·上海·一模)NaO和NaO 具有相似的性质是
2 2 2
A.颜色 B.水溶液的酸碱性 C.氧化性 D.漂白性
【变式训练1】(2023·河南开封·统考二模)图示为证明过氧化钠可在呼吸面具和潜水艇中做供氧剂的实验
装置图,其中a装置是实验室制备二氧化碳的装置,c中盛放的是过氧化钠。下列说法正确的是
A.a中可以用NaCO 和稀盐酸来制备CO
2 3 2
B.b装置中是饱和NaCO 溶液,作用是除去a中产生的HCl
2 3
C.c中只发生2NaO +2CO =2Na CO+O
2 2 2 2 3 2
D.f中收集的气体是纯净的O
2
【变式训练2】(2022·长沙模拟)1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反
应,排出气体物质后冷却,残留的固体物质是( )
A.NaCO B.NaO NaCO
2 3 2 2 2 3
C.NaOH NaCO D.NaO NaOH NaCO
2 3 2 2 2 3
【变式训练3】(2022·日照模拟)某化学兴趣小组在学校科技节活动中表演了“滴水生火”“吹气生火”的
小魔术。如图所示,在蒸发皿上放一小团脱脂棉,在里面裹入一种淡黄色的化合物,对着脱脂棉吹气或者
用胶头滴管滴几滴水,一会儿脱脂棉会燃烧起来。下列说法不正确的是( )
A.淡黄色化合物为NaO
2 2
B.“滴水生火”的小魔术本质上是发生了2NaO+2HO===4NaOH+O↑
2 2 2 2
C.“吹气生火”的小魔术中的火不可以用泡沫灭火器扑灭
D.在活动中为了更清楚地观察现象,需要近距离俯视蒸发皿
考点二 碳酸钠、碳酸氢钠
知识点1 Na CO 、NaHCO 的性质、用途及制法
2 3 3
1、NaCO、NaHCO 的物理性质
2 3 3
名称 碳酸钠 碳酸氢钠化学式 NaCO NaHCO
2 3 3
俗名 纯碱或苏打 小苏打
颜色、状态 白色粉末 细小白色晶体
水溶性 易溶于水 水中易溶,但比NaCO 的溶解度小
2 3
2、NaCO、NaHCO 的化学性质
2 3 3
(1)热稳定性
①NaCO 性质稳定,受热难分解。
2 3
②NaHCO 性质不稳定,受热易分解,化学方程式为2NaHCO NaCO+HO+CO↑。
3 3 2 3 2 2
(2)与足量盐酸反应
①NaCO:CO+2H+===H O+CO↑。
2 3 2 2
②NaHCO :HCO+H+===H O+CO↑。
3 2 2
(3)与碱(NaOH溶液)反应
①NaCO:与NaOH溶液不反应。
2 3
②NaHCO :NaHCO +NaOH===Na CO+HO。
3 3 2 3 2
(4)相互转化
①NaCO―→NaHCO
2 3 3
向NaCO 溶液中通入CO,化学方程式为NaCO+HO+CO===2NaHCO。
2 3 2 2 3 2 2 3
②NaHCO ―→NaCO
3 2 3
NaHCO 固体加热分解转化成NaCO。
3 2 3
3、NaCO、NaHCO 的主要用途
2 3 3
(1)碳酸钠:用于造纸、制造玻璃、制皂、洗涤等。
(2)碳酸氢钠:用于制发酵粉、医药、灭火剂等。
4、NaCO 的制备—侯氏制碱法
2 3
①原料
食盐、氨气、二氧化碳——合成氨厂用水煤气制取氢气时的废气
其反应为C+HO(g)=====CO+H,CO+HO(g)=====CO+H。
2 2 2 2 2
②反应原理
产生NaHCO 反应:NH +NaCl+CO+HO===NaHCO ↓+NH Cl。
3 3 2 2 3 4
产生NaCO 的反应:2NaHCO NaCO+CO↑+HO。
2 3 3 2 3 2 2
③工艺流程
④循环使用的物质:CO、饱和食盐水。
2知识点2 Na CO 和NaHCO 性质的应用
2 3 3
1.Na CO、NaHCO 的鉴别
2 3 3
①固体的鉴别用加热法:产生使澄清石灰水变浑浊的气体的是NaHCO 固体。
3
②溶液的鉴别可用沉淀法、气体法和测pH法。
a.沉淀法:加入BaCl 溶液或CaCl 溶液,产生沉淀的是NaCO 溶液。
2 2 2 3
b.气体法:滴入稀盐酸,立即产生气泡的是NaHCO 溶液。
3
c.测pH法:用pH试纸测相同浓度的稀溶液,pH大的是NaCO 溶液。
2 3
2.Na CO、NaHCO 的除杂
2 3 3
序号 混合物(括号内为杂质) 除杂方法
① Na CO (s)(NaHCO ) 加热法
2 3 3
② NaHCO (aq)(Na CO ) 通入足量CO
3 2 3 2
③ Na CO (aq)(NaHCO ) 滴加适量NaOH溶液
2 3 3
【特别提醒】①NaHCO 与碱溶液反应的实质是HCO与OH-反应生成CO,CO有可能发生后续反应,如
3
NaHCO 与Ca(OH) 溶液反应可以生成白色沉淀CaCO ;
3 2 3
②不能用澄清石灰水来鉴别NaCO 与NaHCO :Ca(OH) 溶液与二者反应均生成白色沉淀CaCO ,无法区
2 3 3 2 3
别;
③用盐酸鉴别NaCO 溶液和NaHCO 溶液时,要求两溶液浓度相差不大,且加入的盐酸等浓度且不宜过大;
2 3 3
④NaCO 、NaHCO 与酸、碱、盐的反应均为复分解反应,因而反应能否进行应从复分解反应的条件来判
2 3 3
断。
知识点3 Na CO 、NaHCO 与盐酸反应的基本图象
2 3 3
若V(Oa)=V(ab)(即Oa
溶液中的溶质为 涉及离子方程式Oa:CO+H+===HCO;
段与ab段消耗盐酸的
Na 2 CO 3 ab:HCO+H+===H 2 O+CO 2 ↑
体积相同)
若V(Oa)>V(ab)(即Oa 涉及离子方程式Oa:OH-+H+===H
2
O、
溶液中的溶质为
段消耗盐酸的体积大于 CO+H+===HCO;
NaCO 和NaOH
2 3
ab段消耗盐酸的体积) ab:HCO+H+===H O+CO↑
2 2
若V(Oa)