文档内容
第 08 讲 钠及其重要化合物
(模拟精练+真题演练)
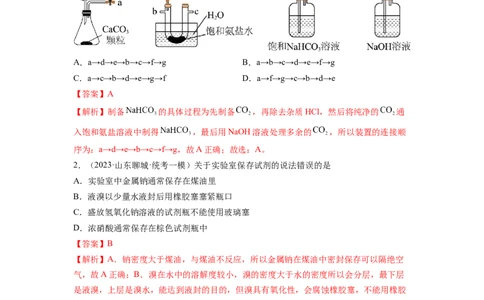
1.(2023·广东汕头·统考二模)某实验小组模拟并改进侯氏制碱法制备 ,下列有
关连接方式正确的是
A.a→d→e→b→c→f→g B.a→b→c→d→e→f→g
C.a→c→b→d→e→g→f D.a→f→g→c→b→d→e
【答案】A
【解析】制备 的具体过程为先制备 ,再除去杂质HCl,然后将纯净的 通
入饱和氨盐溶液中制得 ,最后用NaOH溶液处理多余的 ,所以装置的连接顺
序为:a→d→e→b→c→f→g,故A正确;故选:A。
2.(2023·山东聊城·统考一模)关于实验室保存试剂的说法错误的是
A.实验室中金属钠通常保存在煤油里
B.液溴以少量水液封后用橡胶塞塞紧瓶口
C.盛放氢氧化钠溶液的试剂瓶不能使用玻璃塞
D.浓硝酸通常保存在棕色试剂瓶中
【答案】B
【解析】A.钠密度大于煤油,与煤油不反应,所以金属钠在煤油中密封保存可以隔绝空
气,故A正确;B.溴在水中的溶解度较小,溴的密度大于水的密度所以会分层,最下层
是液溴,上层是溴水,能达到液封的目的,但溴具有氧化性,会腐蚀橡胶塞,不能用橡胶
塞塞紧瓶口,故B错误;C.氢氧化钠可腐蚀玻璃,与玻璃中二氧化硅反应生成粘性物质
硅酸钠溶液,导致玻璃瓶打不开,不能用带磨口玻璃塞试剂瓶盛放,可以用带有橡胶塞的
试剂瓶中盛放,故C正确;D.浓硝酸见光分解,所以应保存在棕色试剂瓶中,故D正确;
故选B。
3.(2023·上海嘉定·统考二模)一定条件下,下列金属中能与水发生置换反应并产生金属
氧化物的是
A.钾 B.镁 C.铁 D.铜
【答案】C
【解析】A. 钾和水反应生成KOH和氢气,故A不选;B. 加热条件下,镁和水反应生成氢氧化镁和氢气,故B不选;C. 加热条件下,铁和水蒸气反应生成四氧化三铁和氢气,故
C选;D. 铜和水不反应,故D不选。故选C。
4.(2023·上海嘉定·统考一模)我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图
如图所示),促进了世界制碱技术的发展.下列有关说法正确的是( )
A.沉淀池中的反应物共含有五种元素
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
【答案】D
【解析】A.沉淀池中发生的反应的反应物是氯化钠、氨气、二氧化碳和水,所以含有钠、
氯、氮、氢、碳、氧六种元素,故A错误;B.过滤得到的“母液”中含有的溶质有碳酸
氢钠、氯化铵,还有可能含有过量的氯化钠,故B错误;C.碳酸氢钠分解生成碳酸钠、
水、二氧化碳,所以X是二氧化碳,故C错误;D.氨气的水溶液显碱性,能更好的吸收
二氧化碳,使反应物浓度大,反应速度快,故D正确;故答案为D。
5.(2023·广东潮州·统考二模)作为广东文化的代表之一,岭南文化历史悠久。下列岭南
文化内容中蕴含的化学知识描述不正确的是
选 文化类
文化内容 化学知识
项 别
饮食文
A 早茶文化中的叉烧包 叉烧包中富含糖类、油脂、蛋白质等营养物质
化
劳动文 热的纯碱溶液洗涤餐
B 油脂在碱性条件下发生水解
化 具
服饰文
C “丝中贵族”香云纱 鉴别丝和棉花可以用灼烧的方法
化
节日文 烟花利用了“焰色试验”原理,该原理属于化
D 烟花舞龙
化 学变化
【答案】D
【解析】A.叉烧包中的叉烧含有肉、油脂、淀粉等,所以富含糖类、油脂、蛋白质等营
养物质,A正确;B. 水解使溶液显碱性,油脂在碱性条件下发生水解,所以可用纯碱去油污,B正确;C.丝为蛋白质,灼烧时有烧焦羽毛的气味,棉花为纤维素,所以可
以用灼烧的方法鉴别丝和棉花,C正确;D.烟花利用了“焰色试验”原理,焰色试验属
于物理变化,D错误;故选D。
6.(2023·广东江门·校联考模拟预测)氢化钠是一种重要的储氢试剂、缩合剂、还原剂、
烷基化试剂,在有机合成中具有重要作用,某学习小组利用如图装置制备少量氢化钠,下
列说法错误的是
A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分
B.装置乙和装置丁内盛放的试剂可以分别为无水氯化钙和碱石灰
C.实验过程中应先打开K,一段时间后,尾端验纯后再点燃酒精灯
1
D.m gH 储存到NaH中,与足量水反应也释放m gH ,遵从质量守恒定律
2 2
【答案】D
【解析】A.装置丙中将Na分散到NaCl晶体中可以增大接触面积,使反应更充分,A项
正确;B.装置乙和装置丁起干燥作用,盛放的试剂可以分别为无水氯化钙和碱石灰,B项
正确;C.实验过程中应先打开K,用生成的氢气排除装置中的空气,一段时间后,尾端
1
验纯后,说明空气已经排尽,再点燃酒精灯,C项正确;D.1 molNa吸收0.5molH 生成
2
1molNaH,NaH与水的反应为归中反应,1mol氢化钠与足量水完全反应,生成1mol氢气,
D项错误;故选D。
7.(2023·广东深圳·统考一模)化学实验是化学探究的一种重要途径。下列有关实验的描
述正确的是
A.用湿润的蓝色石蕊试纸检验
B.中学实验室中,可将未用完的钠放回原试剂瓶
C.进行焰色试验时,可用玻璃棒替代铂丝
D.酸碱中和滴定实验中,应先用待测液润洗锥形瓶
【答案】B
【解析】A. 溶于水呈碱性,可以用湿润的红色石蕊试纸检验 ,故A错误;B.
易燃物如钠、钾等不能随便丢弃,中学实验室可以将未用完的钠、钾等放回原试剂瓶,故
B正确;C.玻璃的成分里边有硅酸钠,钠盐的焰色试验为黄色,对其他元素的试验存在干
扰,进行焰色试验时,不可用玻璃棒替代铂丝,故C错误;D.酸碱中和滴定实验中,洗
锥形不能用待测液润洗,否则会导致测量结构偏大,故D错误;故选B。
8.(2023·上海奉贤·统考二模)实验室中利用侯氏制碱法制备NaCO 和NH Cl,流程如图。
2 3 4
下列说法正确的是A.气体N、M分别为 和
B.只有“食盐水”可以循环使用
C.为了加速过滤可用玻璃棒搅拌
D.向“母液”中通入NH 有利于析出NH Cl并提高纯度
3 4
【答案】D
【分析】侯氏制碱法制备碳酸钠和氯化铵,饱和食盐水中先通入NH 、再通入CO,此时
3 2
生成碳酸氢钠沉淀和氯化铵,过滤得到碳酸氢钠,加热碳酸氢钠生成碳酸钠、二氧化碳和
水,母液中加入NaCl和NH ,发生反应NaCl(s)+NH Cl(aq)=NaCl(aq)+NH Cl(s),过滤得到
3 4 4
氯化铵。
【解析】A.气体N为NH ,气体M为CO,A错误;B.从流程图可知,最后碳酸氢钠分
3 2
解生成的CO、母液生成的食盐水都可以循环利用,B错误;C.用玻璃棒搅动漏斗里的液
2
体,容易把滤纸弄破,起不到加速过滤的作用,C错误;D.向母液中通入NH ,增大溶液
3
中 的浓度,有利于NH Cl析出并提高纯度,D正确;故答案选D。
4
9.(2023·北京东城·统考二模)实验:将一小粒钠放在石棉网上,微热,待钠熔成球状时,
将盛有氯气的集气瓶迅速倒扣在钠的上方,钠剧烈燃烧,有白烟生成。下列分析不正确的
是
A.钠熔化后体积增大,说明钠原子间的平均距离增大
B.反应过程中, 的 键断裂
C. 的形成过程可表示为
D.该实验说明 的氧化性比 的强
【答案】D
【解析】A.钠熔化后体积增大,说明钠原子间的平均距离增大,故A正确;B.反应过程中, 的3p上的 键断裂,故B正确;C. 的形成过程钠原子失去电子,氯原
子得到电子,可表示为 ,故C正确;D.该实验没有对
比无法说明 的氧化性比 的强,故D错误;故选:D。
10.(2023·浙江·校联考三模)探究钠及其化合物的性质,下列方案设计、现象及结论都
正确的是
方案设计 现象 结论
向露置在空气中的 固体
A 溶液中产生气泡 固体已经变质
中加入稀盐酸
将一小块金属钠在燃烧匙中点 产生黑、白两种 钠的还原性强,与二氧化碳发生
B
燃,伸入盛有 的集气瓶中 固体 了置换反应
向2mL 2 溶液 该 溶液中混有
C 溶液中产生气泡
中滴加2滴4 稀盐酸 杂质
向插有温度计的10mL 0.1
有刺激性气味产
反应
D 溶液中加入一 生,温度计示数
为放热反应
增大
定量NaOH固体
【答案】B
【解析】A.过氧化钠本身与盐酸反应生成氧气,有气泡冒出,不能证明过氧化钠已经变
质,故A错误;B.钠与二氧化碳反应生成碳酸钠和碳,则产生黑、白两种固体,该反应
为置换反应,故B正确;C.碳酸根离子结合质子能力强于碳酸氢根离子的,盐酸少量,
碳酸钠与盐酸反应生成碳酸氢钠,无明显现象,不会产生气泡,故C错误;D.NH Cl溶
4
液中加入一定量NaOH固体中时,由于氢氧化钠固体溶于水本身放热,所以不能据此说明
该反应是放热反应,故D错误;故选:B。
11.(2023·重庆·重庆南开中学校考三模)向下列物质中加入NaOH溶液并加热,其成分
不发生改变的是
A.用聚四氟乙烯制 B.用于通信的光 C.用于焙制糕点的 D.从餐厨废弃物中
成的实验仪器 导纤维 小苏打 提取的地沟油【答案】A
【解析】A.聚四氟乙烯不和氢氧化钠溶液反应,故A符合题意;B.光导纤维的主要成分
是二氧化硅,二氧化硅与氢氧化钠溶液反应生成硅酸钠和水,离子方程式为
,故B不符合题意;C.小苏打的主要成分是碳酸氢钠,碳酸氢
钠与氢氧化钠反应生成碳酸钠和水,离子方程式为: ,故C不符
合题意;D.“地沟油”的成分是油脂,与碱溶液反应生成高级脂肪酸盐和甘油,故D不
符合题意;故答案选A。
12.(2023·湖南岳阳·统考一模)用如图装置来分离CO 和CO混合气体并干燥,图中a、
2
c、d为止水夹,b为分液漏斗活塞,通过Y形管和止水夹分别接两个球胆,现装置内空气
已排尽,为使实验成功,甲、乙、丙分别盛放的试剂为
甲 乙 丙
18.4mol·L-1
A 饱和NaHCO 溶液 12mol·L-1盐酸
3
HSO
2 4
B 饱和NaCO 溶液 2mol·L-1 HSO 饱和NaOH溶液
2 3 2 4
18.4mol·L-1
C 饱和NaOH溶液 2mol·L-1 HSO
2 4
HSO
2 4
18.4mol·L-1
D 18.4mol·L-1 HSO 饱和NaOH溶液
2 4
HSO
2 4
【答案】C
【解析】对于甲乙丙选择何种试剂,因为混合气体首先通过的是甲,由于CO 能与碱反应
2
生成碳酸盐,则剩余气体CO就很容易分离出,所以在甲中加入饱和NaOH溶液,与CO
2
反应生成碳酸钠和水,CO通过乙瓶顺利分离出来,由于实验中含有水分所以丙中加入浓
硫酸对其干燥;漏斗中乙液体是将生成的碳酸盐转变成CO,所以应该装的是稀硫酸,故
2
选C。
13.(2022·上海松江·统考二模)I.某化学兴趣小组采用如下图所示装置研究NaHCO 分解
3
的CO 与NaO 反应。
2 2 2完成下列填空:
(1)画出乙中实验装置图,并标出相应试剂_______。
(2)装置丙中仪器名称是_______,其中反应的化学方程式是_______,该反应中氧化剂与还
原剂的质量比为_______。
(3)装置丁中NaOH溶液的作用是_______,装置戊中澄清石灰水的作用是_______。
II.NaHCO 俗称小苏打,工业上可由通过侯氏制碱法制取(又称联合制碱法,由我国近代著
3
名的化工学家侯德榜发明)。
(4)写出侯氏制碱法中生成NaHCO 的离子方程式_______。操作时,往饱和食盐水中先通入
3
_______气体,原因是_______。
(5)在密闭容器中投入一定量的NaO 和NaHCO ,在300℃下充分反应。若残留固体为纯净
2 2 3
物,则起始时 应满足的条件是_______。
【答案】(1)
(2)(球形)干燥管 2NaO+2CO →2NaCO+O 1:1
2 2 2 2 3 2
(3)除去O 中的CO 检验O 中是否有CO
2 2 2 2
(4)Na++CO +NH+H O→NaHCO↓+ NH 氨气溶解性大而且溶液呈碱性后能吸收更
2 3 2 3 3
多二氧化碳,增大 浓度,有利于碳酸氢钠析出
(5)≥2
【分析】为研究NaHCO 分解的CO 与NaO 反应,甲装置中碳酸氢钠受热分解为碳酸钠、
3 2 2 2
二氧化碳、水,乙中用浓硫酸除去二氧化碳中的水蒸气,丙中二氧化碳和过氧化钠反应生
成氧气,丁中用氢氧化钠除去氧气中的二氧化碳,戊中澄清石灰水检验二氧化碳是否除尽,
己装置用排水法收集氧气。
(1)实验目的是研究NaHCO 分解的CO 与NaO 反应,碳酸氢钠分解放出的二氧化碳气体
3 2 2 2
中含有水蒸气,乙装置的作用是干燥二氧化碳,所以乙是盛有浓硫酸的洗气瓶,装置图为;
(2)根据图示,装置丙中仪器名称是球形干燥管,其中过氧化钠和二氧化碳反应生成碳酸钠
和氧气,反应的化学方程式是2NaO+2CO →2NaCO+O ,NaO 中氧元素的化合价由-1
2 2 2 2 3 2 2 2
升高为0、由-1降低为-2,根据得失电子守恒,氧化剂与还原剂的质量比为1:1。
(3)由丙装置出来的气体中含有氧气和二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠和水,
所以丁中NaOH溶液的作用是除去O 中的CO,装置戊中澄清石灰水的作用是检验O 中是
2 2 2
否有CO。
2
(4)侯氏制碱法中氯化钠、二氧化碳、氨气反应生成NaHCO 沉淀、氯化铵,反应的离子方
3
程式为Na++CO +NH+H O→NaHCO↓+ 。氨气溶解性大而且溶液呈碱性后能吸收更多
2 3 2 3
二氧化碳,增大 浓度,有利于碳酸氢钠析出,所以往饱和食盐水中先通入氨气。
(5)设投入xmolNa O 和ymolNaHCO,在300℃下充分反应,若残留固体为纯净物,则固体
2 2 3
产物为碳酸钠,根据元素守恒2n(C)≥n(Na),则2y≥(2x+y),则起始时 ≥2。
14.(2023·江西上饶·万年中学校考一模)图中A为一种中学化学中常见的金属单质,B、
C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
(1)B的化学式中阳离子和阴离子的个数比为______。
(2)以上6个反应中属于氧化还原反应的有____________(填写编号)。
(3)写出B→D反应的化学方程式________________________。
(4)若用所示装置验证D、E的热稳定性,则乙中装入的固体最好是______(填化学式)。
(5)向滴入酚酞的D溶液中滴入少量稀盐酸,现象是没有气泡生成,溶液__________,反应
的离子方程式为_______________,继续滴加盐酸至过量,现象是_______________(6)将一定量的B投入到含有下列离子的溶液中: 、 、 、 ,反应完毕后
溶液中上述离子数目明显增多的有______(填离子符号).
【答案】(1)2:1
(2)①②③④
(3)2Na O+2CO =2Na CO+O
2 2 2 2 3 2
(4)NaHCO
3
(5)仍呈红色 +H+= 溶液的红色褪去,且有气泡逸出
(6) 、Na+
【分析】A为一种中学化学中常见的金属单质,B、C、D、E是含有A元素的常见化合物。
它们的焰色试验均为黄色。由图中物质的转化关系,可确定A为Na,B为NaO,C为
2 2
NaOH,D为NaCO,E为NaHCO 。
2 3 3
【解析】(1)B的化学式为NaO,阳离子(Na+)和阴离子( )的个数比为2:1。答案为:
2 2
2:1;(2)以上6个反应分别为:2Na+O NaO、2Na+2HO=2NaOH+H ↑、
2 2 2 2 2
2NaO+2H O=4NaOH+O ↑、2NaO+2CO =2Na CO+O 、NaOH+CO =NaHCO、2NaHCO
2 2 2 2 2 2 2 2 3 2 2 3 3
NaCO+CO ↑+H O,属于氧化还原反应的有①②③④。答案为:①②③④;(3)由以
2 3 2 2
上分析可知,B→D为NaO 与CO 反应生成NaCO 和O,反应的化学方程式:
2 2 2 2 3 2
2NaO+2CO =2Na CO+O 。答案为:2NaO+2CO =2Na CO+O ;(4)若用如图所示装置
2 2 2 2 3 2 2 2 2 2 3 2
验证D、E的热稳定性,则乙中装入的固体,最好是低温条件下就能分解的NaHCO 。答案
3
为:NaHCO ;(5)向滴入酚酞的D溶液中滴入少量稀盐酸,发生反应
3
NaCO+HCl=NaCl+ NaHCO ,现象是没有气泡生成,溶液仍呈红色,反应的离子方程式为
2 3 3
+H+= ,继续滴加盐酸至过量,发生反应NaHCO +HCl=NaCl+H O+CO↑,现象
3 2 2
是:溶液的红色褪去,且有气泡逸出。答案为:仍呈红色; +H+= ;溶液的红色
褪去,且有气泡逸出;(6)将一定量的B投入到含有下列离子的溶液中,先与水反应,
反应方程式为2NaO+2H O=4NaOH+O ↑,生成的OH-再与 反应生成 ,则反应完
2 2 2 2
毕后溶液中上述离子数目明显增多的有 、Na+。答案为: 、Na+。
15.(2023·辽宁朝阳·朝阳市第一高级中学校联考二模)1943年我国化工专家侯德榜创立
了“侯氏制碱法”,提高了氯化钠的利用率,利用了水煤气厂的废气氨气,具有环保、节
能效果。
(1)“侯氏制碱法”以NaCl、 、 等为原料先制得 ,进而生产出纯碱。碳酸
氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的判断依据是_______。
A.碳酸氢钠难溶于水
B.碳酸氢钠受热易分解C.碳酸氢钠的溶解度相对较小,在溶液中首先结晶析出
(2)在实验室里甲同学做完氨喷泉实验的溶液配成含氨的饱和和食盐水,向其中通入二氧化
碳,以制备碳酸氢钠,实验装置如下图①所示(图中夹持、固定用的仪器未画出)。
①丁装置中稀硫酸的作用是_______。
②实验结束后,分离出 晶体的操作是_______(填分离操作的名称)。
(3)实验室里乙同学利用图②装置和现有仪器结合所学的知识,减少加热分解碳酸氢钠的步
骤,用实验室剩余NaOH溶液制备碳酸钠溶液。请回答下列问题:
①要完成制备实验,除图②装置中的仪器外还必需的仪器是_______。
②写出最后一步在试管中生成碳酸钠溶液的离子反应方程式为_______。
③实验准备就绪后,先打开活塞3,关闭活塞2,再打开活塞1(根据需要可关开)。一段时
间后,应该_______(填具体操作)。则Y可以是_______。
④该实验设计有不妥之处,排除混有NaOH或 杂质外,还可能在制备的碳酸钠溶
液中混有其他杂质,则该杂质及其产生的原因分别是_______。
(4)利用“双指示剂”滴定方法测定纯碱组成和含量。取一定量的纯碱配成溶液,用盐酸滴
定纯碱溶液得到图③曲线,若纯碱中含有的杂质为碳酸氢钠,则数据符合_______(用 、
大小关系表示)。
【答案】(1)C
(2)吸收未反应的 过滤
(3)量筒 关闭活塞3,打开活塞2 煤油或苯 因挥发出来HCl没有除去,易产成NaCl杂质
(4) 或
【分析】工业上“侯氏制碱法”是在饱和食盐水中依次通入氨气和二氧化碳,由于氨气在
水中的溶解度大,所以先通入氨气,通入足量的氨气后再通入二氧化碳,生成了碳酸氢钠,
由于碳酸氢钠的溶解度较小,所以溶液中有碳酸氢钠晶体析出,将碳酸氢钠晶体加热后得
纯碱碳酸钠。
【解析】(1)A.碳酸氢钠是钠盐易溶于水,故不选A;B.碳酸氢钠受热易分解,与其
在溶液中首先结晶析出无关,故不选B;C.碳酸氢钠的溶解度相对于氯化铵来说碳酸氢钠
的溶解度更小一些,所以在溶液中首先结晶析出,故选C;选C。
(2)氨气易挥发,丁装置中稀硫酸的作用是吸收未反应的 ,防止污染。
②实验结束后, 结晶析出,分离出 晶体的操作是过滤。
(3)NaOH与足量 很容易转化为 溶液, 转化为碳酸钠发生反应
, ,所以需要将NaOH分为两等份,
除图②装置中的仪器外还必需的仪器是量筒。
②最后一步氢氧化钠和碳酸氢钠反应生成碳酸钠,反应的离子反应方程式为
。
先将足量 通入右侧试管中,制备 溶液,然后再将烧瓶中的小试管里的NaOH
排到烧杯中与先生成的 发生反应。因此操作是关闭活塞3,打开活塞2,为防止
溶解于烧瓶中试管内的NaOH,用油封的方法,即Y为煤油(或苯);图二的设计中制
所用的盐酸挥发,HCl未除,与NaOH易生成杂质氯化钠。
(4)若只有碳酸钠,加入VmL盐酸发生反应 ,加入V~V mL盐酸发
1 1 2
生反应 ,则2V=V ,若纯碱中含有的杂质为碳酸氢钠,则数据
1 2
符合2V