文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海市黄浦区 2023 届高三一模考试
化学试题
(用时:60分钟 满分:100 分)
一、选择题(本题共40分,每小题2分,每小题只有一个正确答案)
1. 以下化学品用途正确的是
A. 二氧化硫——食品防腐剂 B. 铁粉——食品干燥剂
C. 生石灰——食品脱氧剂 D. 苏打——食品膨松剂
【答案】A
【解析】
【详解】A.二氧化硫可使蛋白质变性,可用于杀菌消毒、防腐蚀,控制 SO 的量可作葡萄酒防腐剂,抑
2
制细菌再生,故可用作食品防腐剂,A正确;
B.铁粉由于能与空气中O 反应,防止食品被氧化,故作食品脱氧剂,B错误;
2
C.生石灰能与水反应,吸收食品中的水蒸气,故可作食品干燥剂,C错误;
D.小苏打受热易分解放出无毒无害的气体,故可用作食品膨松剂,而纯碱即碳酸钠受热不分解,不能作
为食品膨松剂,D错误;
故答案为:A。
2. 下列变化都属于化学变化的是
A. 蒸馏、干馏 B. 潮解、裂解 C. 裂化、风化 D. 液化、升华
【答案】C
【解析】
【详解】A.蒸馏是利用互溶液体的沸点不同通过加热冷凝而分离物质,属于物理变化,干馏则是隔绝空
气对煤进行加强热,发生复杂的物理化学变化,A不合题意;
B.潮解是物理变化,裂解是将各种石油分馏产品分解,得到气态烃的过程,是化学变化,B不合题意;
C.裂化是将重油中的长链烃断裂为短链烃,获得轻质液体燃料特别是汽油的过程,是化学变化,风化是
指带结晶水的物质失去结晶水的过程,属于化学变化,C符合题意;
D.液化和升华均为物理变化,D不合题意;
故答案为:C。
3. 关于电子描述不合理的是
A. 质量极小 B. 运动速度极快
C. 活动空间极小 D. 能被准确测定位置
【答案】D
第 1 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【详解】A.电子的质量极小,其相对质量为 ,A不合题意;
B.电子在原子核外高速运转,其运动速度极快,B不合题意;
C.原子的半径非常小,故电子的活动空间极小,C不合题意;
D.由于电子的活动空间极小,运动速度极快,故不能被准确测定其所在位置,D符合题意;
故答案为:D。
4. 下列化学用语正确的是
A. 次氯酸的结构式:H-Cl-O
B. Cl原子的价电子轨道表示式:
C. 离子的结构示意图:
D. 四氯化碳的比例模型
【答案】B
【解析】
【详解】A.已知H、Cl周围都只能形成一对共用电子对,O周围能形成两对共用电子对,则次氯酸中心
原子为氧原子,结构式为:H-O-Cl,A错误;
B.已知Cl为17号元素,其基态原子的价电子排布式为:3s23p5,故Cl原子的价电子轨道表示式:
,B正确;
C. 离子的结构示意图为: ,C错误;
D.四氯化碳是正四面体构型,且Cl原子半径比C的大,故其的比例模型为: ,D错误;
第 2 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故答案为:B。
5. NaO和NaO 具有相似的性质是
2 2 2
A. 颜色 B. 水溶液的酸碱性 C. 氧化性 D. 漂白性
【答案】B
【解析】
【详解】A、氧化钠是白色的,但是过氧化钠是黄色的固体,故A错误;
B、氧化钠和水反应生成氢氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,水溶液呈碱性,故B正确;
C、氧化钠无氧化性,过氧化钠具有强氧化性,故C错误;
D、氧化钠无氧化性,无漂白性,过氧化钠具有强氧化性,能用于漂白,具有漂白作用,故D错误;
故选B。
6. 下列各组物质可用酸性KMnO 溶液鉴别的是
4
A. 油酸和硬脂酸 B. 苯和己烷 C. 乙烯和乙炔 D. 甲酸和甲醛
【答案】A
【解析】
【详解】A.油酸中含有碳碳双键,能使酸性高锰酸钾溶液褪色,而硬脂酸不含不饱和键,不能是酸性高
锰酸钾溶液褪色,故可用酸性高锰酸钾溶液鉴别,A符合题意;
B.苯和己烷分子中均不含不饱和键,不能使酸性高锰酸钾溶液褪色,故不可用酸性高锰酸钾溶液鉴别,B
不合题意;
C.乙烯和乙炔均可使酸性高锰酸钾溶液鉴别,故不可用酸性高锰酸钾溶液鉴别,C不合题意;
D.甲酸和甲醛均均有还原性,均可使酸性高锰酸钾溶液鉴别,故不可用酸性高锰酸钾溶液鉴别,D不合
题意;
故答案为:A。
7. 下列晶体变成液态的过程中破坏的作用力与其他不同的是
A. 食盐 B. 冰醋酸 C. 蔗糖 D. 干冰
【答案】A
【解析】
【详解】食盐即NaCl形成离子晶体,其变为液体即熔化过程中克服离子键,冰醋酸、蔗糖和干冰均形成
分子晶体,其变为液体即熔化过程中均克服分子间作用力即范德华力,故答案为:A。
8. 去了膜的铝条放入硫酸铜溶液中,不可能观察到的现象
A. 金属表面有气泡 B. 银白色金属转变为紫红色
C. 出现蓝色沉淀 D. 溶液蓝色变浅
【答案】C
【解析】
第 3 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【详解】A.硫酸铜溶液由于是强酸弱碱盐溶液,故Cu2+水解使溶液显酸性,把去了膜的铝条放入硫酸铜
溶液中,会生成氢气,金属表面产生气泡,A不合题意;
B.由2Al+3CuSO=Al(SO )+3Cu可知,银白色金属转变为紫红色,B不合题意;
4 2 4 3
C.由2Al+3CuSO=Al(SO )+3Cu可知,不会出现蓝色沉淀,C符合题意;
4 2 4 3
D.由2Al+3CuSO=Al(SO )+3Cu可知,溶液蓝色变浅,D不合题意;
4 2 4 3
故答案为:C。
9. 下列说法错误的是
A. 可制成导电塑料 B. HOCHO和HOCH CHO互为同系物
2
C. 和 互为同素异形体 D. 和 是同一种物质
【答案】B
【解析】
【详解】A. 为聚乙炔是导电塑料,A正确;
B.同系物是指结构相似,在分子组成上相差若干个CH 原子团,HOCHO是甲酸,属于羧酸类,
2
HOCH CHO含有羟基和醛基,结构不相似,不互为同系物,B错误;
2
C.同素异形体是指同一元素形成的不同单质,则 和 互为同素异形体,C正确;
D.有机物结构中单键可以旋转, 和 分子式相同,结构相同,是同一种物质,D正确;
故选B。
10. 有关如图的描述中,错误的是
第 4 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 溶液中粒子中心为黑球的是水合
B. X与电源的正极相连,Y与电源的负极相连
C. KCl溶液能导电,所以KCl溶液是电解质
D. KCl溶液能导电的原因是溶液中含有自由移动的离子
【答案】C
【解析】
【分析】K+离子半径小于Cl-,则黑球为K+,灰球为Cl-,K+向Y极移动,则Y极为阴极,与电源负极相连,
Cl-向X极移动,则X极为阳极,与电源正极相连。
【详解】A.据分析可知,溶液中粒子中心为黑球的是水合 ,A正确;
B.据分析可知,X与电源的正极相连,Y与电源的负极相连,B正确;
C.KCl溶液能导电,是因为KCl为电解质,而KCl溶液为混合物,不属于电解质,C错误;
D.KCl溶液能导电的原因是KCl在水中能电离出自由移动的钾离子和氯离子,D正确;
故选C。
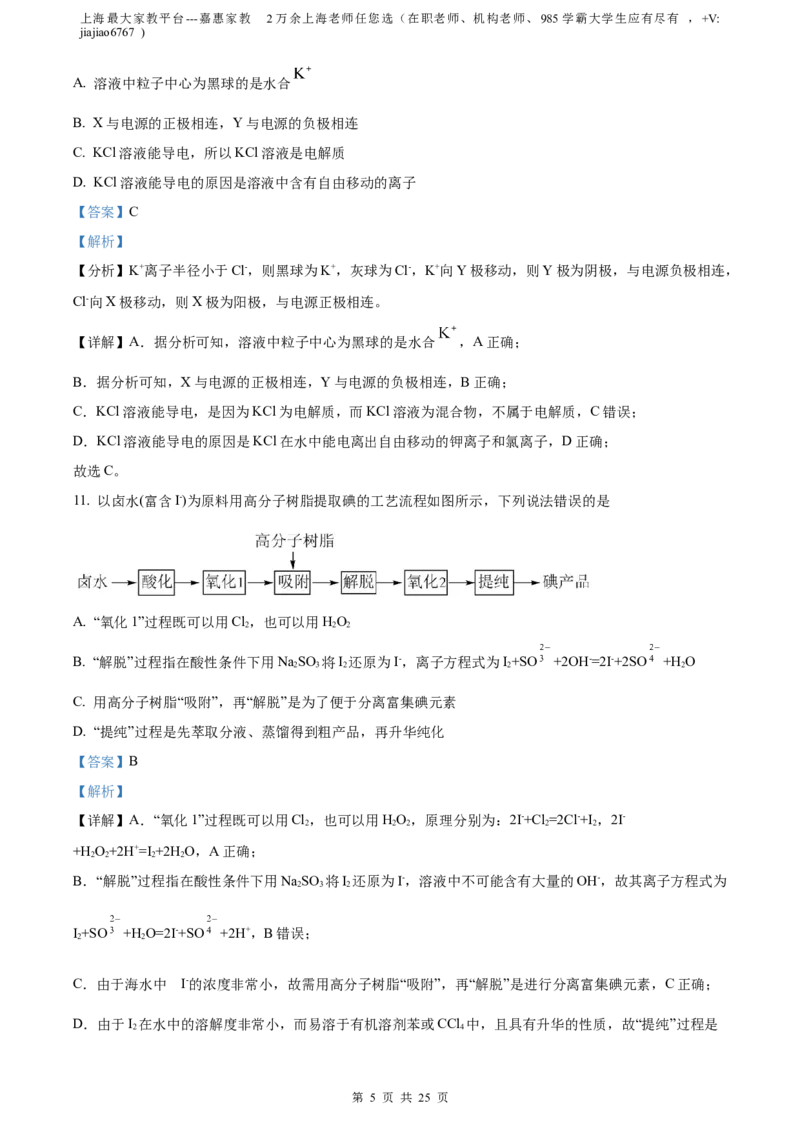
11. 以卤水(富含I-)为原料用高分子树脂提取碘的工艺流程如图所示,下列说法错误的是
A. “氧化1”过程既可以用Cl,也可以用HO
2 2 2
B. “解脱”过程指在酸性条件下用NaSO 将I 还原为I-,离子方程式为I+SO +2OH-=2I-+2SO +H O
2 3 2 2 2
C. 用高分子树脂“吸附”,再“解脱”是为了便于分离富集碘元素
D. “提纯”过程是先萃取分液、蒸馏得到粗产品,再升华纯化
【答案】B
【解析】
【详解】A.“氧化1”过程既可以用Cl,也可以用HO,原理分别为:2I-+Cl=2Cl-+I ,2I-
2 2 2 2 2
+H O+2H+=I +2H O,A正确;
2 2 2 2
B.“解脱”过程指在酸性条件下用NaSO 将I 还原为I-,溶液中不可能含有大量的OH-,故其离子方程式为
2 3 2
I+SO +H O=2I-+SO +2H+,B错误;
2 2
的
C.由于海水中 I-的浓度非常小,故需用高分子树脂“吸附”,再“解脱”是进行分离富集碘元素,C正确;
D.由于I 在水中的溶解度非常小,而易溶于有机溶剂苯或CCl 中,且具有升华的性质,故“提纯”过程是
2 4
第 5 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
先萃取分液,得到I 单质的有机溶液(如苯或CCl ),然后再蒸馏得到粗产品,再升华纯化,D正确;
2 4
故答案为:B。
12. 下列化合物的分子中,所有原子可能共平面的是
A. 甲苯 B. 乙烷 C. 丙炔 D. 1,3−丁二烯
【答案】D
【解析】
【详解】A、甲苯中含有饱和碳原子,所有原子不可能共平面,A不选;
B、乙烷是烷烃,所有原子不可能共平面,B不选;
C、丙炔中含有饱和碳原子,所有原子不可能共平面,C不选;
D、碳碳双键是平面形结构,因此1,3-丁二烯分子中两个双键所在的两个面可能重合,所有原子可能共
平面,D选。
答案选D。
13. 可以检验NaSO 固体部分变质的试剂是
2 3
A. Ba(NO ) 溶液 B. BaCl 溶液
3 2 2
C. BaCl 溶液、稀硝酸 D. BaCl 溶液、稀盐酸
2 2
【答案】D
【解析】
【分析】NaSO 固体部分变质说明含有杂质NaSO ;
2 3 2 4
【详解】A.Ba(NO ) 溶液与NaSO 或NaSO 反应均生成白色沉淀,无法检验NaSO 固体部分变质,A
3 2 2 3 2 4 2 3
不符合题意;
B.BaCl 溶液与NaSO 或NaSO 反应均生成白色沉淀,无法检验NaSO 固体部分变质,B不符合题意;
2 2 3 2 4 2 3
C.BaCl 溶液与NaSO 反应生成BaSO 白色沉淀,BaCl 溶液与NaSO 反应生成BaSO 白色沉淀,稀硝酸
2 2 3 3 2 2 4 4
具有氧化性,能将亚硫酸钡氧化为硫酸钡,硫酸钡不能和稀硝酸反应,所以白色沉淀不会消失,所以不含
硫酸钠也会有白色沉淀,无法检验NaSO 固体部分变质,C不符合题意;
2 3
D.BaCl 溶液与NaSO 反应生成BaSO 白色沉淀,BaCl 溶液与NaSO 反应生成BaSO 白色沉淀,BaSO
2 2 3 3 2 2 4 4 3
和稀盐酸反应生成BaCl 、HO、SO ,BaSO 和稀盐酸不反应,故NaSO 固体部分变质会有一部分沉淀溶
2 2 2 4 2 3
解在稀盐酸中,能检验NaSO 固体部分变质,D符合题意;
2 3
故选D。
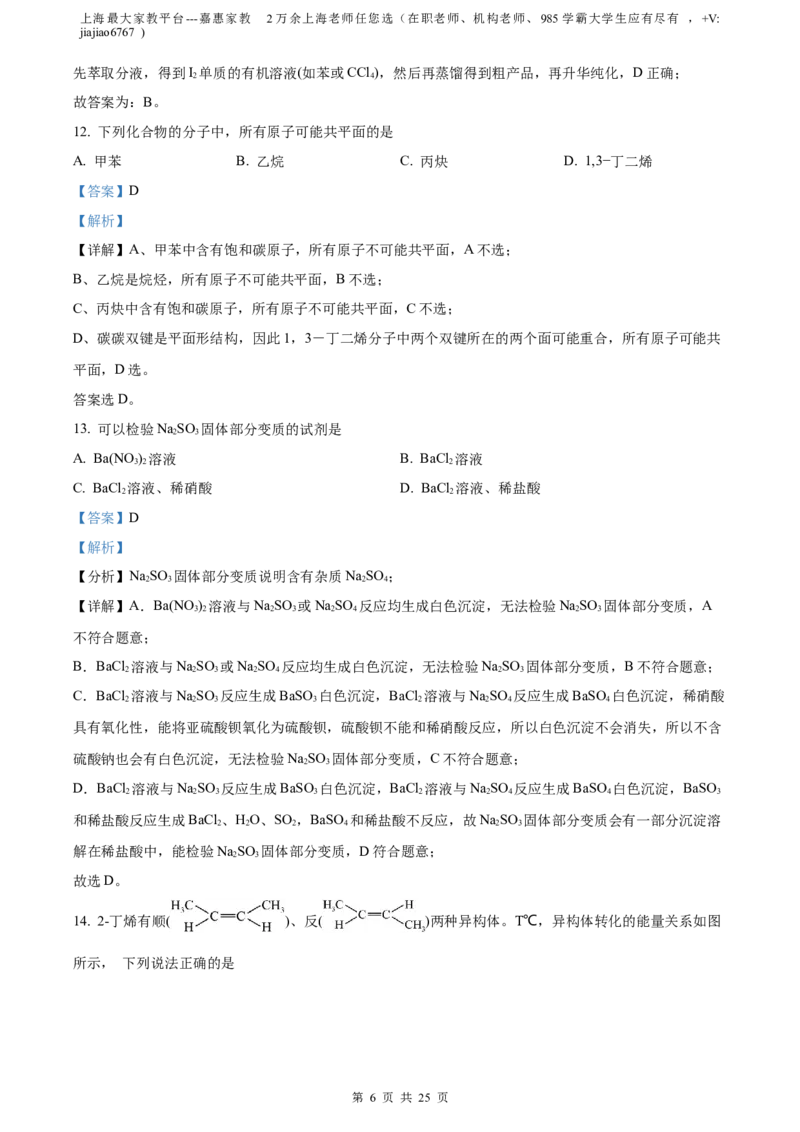
14. 2-丁烯有顺( )、反( )两种异构体。T℃,异构体转化的能量关系如图
所示, 下列说法正确的是
第 6 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 顺-2-丁烯转化为反-2-丁烯的过程属于物理变化
B. 顺-2-丁烯稳定性大于反-2-丁烯
C. 发生加成反应时,顺−2−丁烯断键吸收的能量低于反−2−丁烯断键吸收的能量
D. T℃,1mol顺−2−丁烯完全转化成反−2−丁烯放出热量(c-b)kJ
【答案】C
【解析】
【详解】A.由题干信息可知,顺-2-丁烯与反-2-丁烯互为同分异构体,故顺-2-丁烯转化为反-2-丁烯的过程
中有新的物质生成,故属于化学变化,A错误;
B.由题干能量转化图可知,顺-2-丁烯具有的总能量大于反-2-丁烯,能量越高越不稳定,故顺-2-丁烯稳定
性小于反-2-丁烯,B错误;
C.顺−2−丁烯和反−2−丁烯加成后均得到相同的产物,即终态的能量相同,而顺-2-丁烯具有的总能量大于
反-2-丁烯,即发生加成反应时,顺-2-丁烯放出的能量大于反-2-丁烯,形成过程中放出的总能量相同,故
顺−2−丁烯断键吸收的能量低于反−2−丁烯断键吸收的能量,C正确;
D.由题干能量转化图可知,T℃,1mol顺−2−丁烯完全转化成反−2−丁烯放出热量(a-b)kJ,D错误;
故答案为:C。
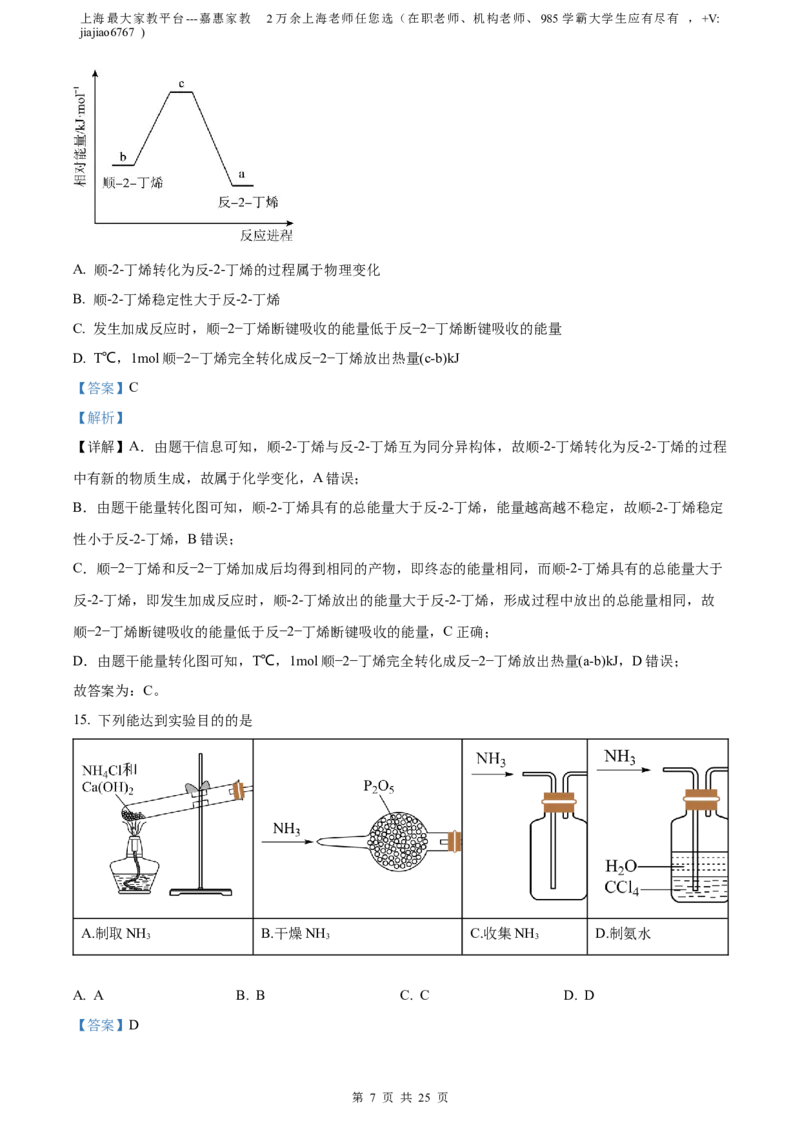
15. 下列能达到实验目的的是
A.制取NH B.干燥NH C.收集NH D.制氨水
3 3 3
A. A B. B C. C D. D
【答案】D
第 7 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【详解】A.固体加热试管口需要向下倾斜,A错误;
B.带有水蒸气的氨气能与PO 反应,故不能用PO 干燥氨气,B错误;
2 5 2 5
C.氨气密度小于空气需要用向上排空气法收集其他,在万能瓶中需要短进长出,C错误;
D.氨气极易溶于水,但不溶于四氯化碳,可以通过四氯化碳层在进入水层吸收氨气,可以防止倒吸,D
正确;
故答案为:D。
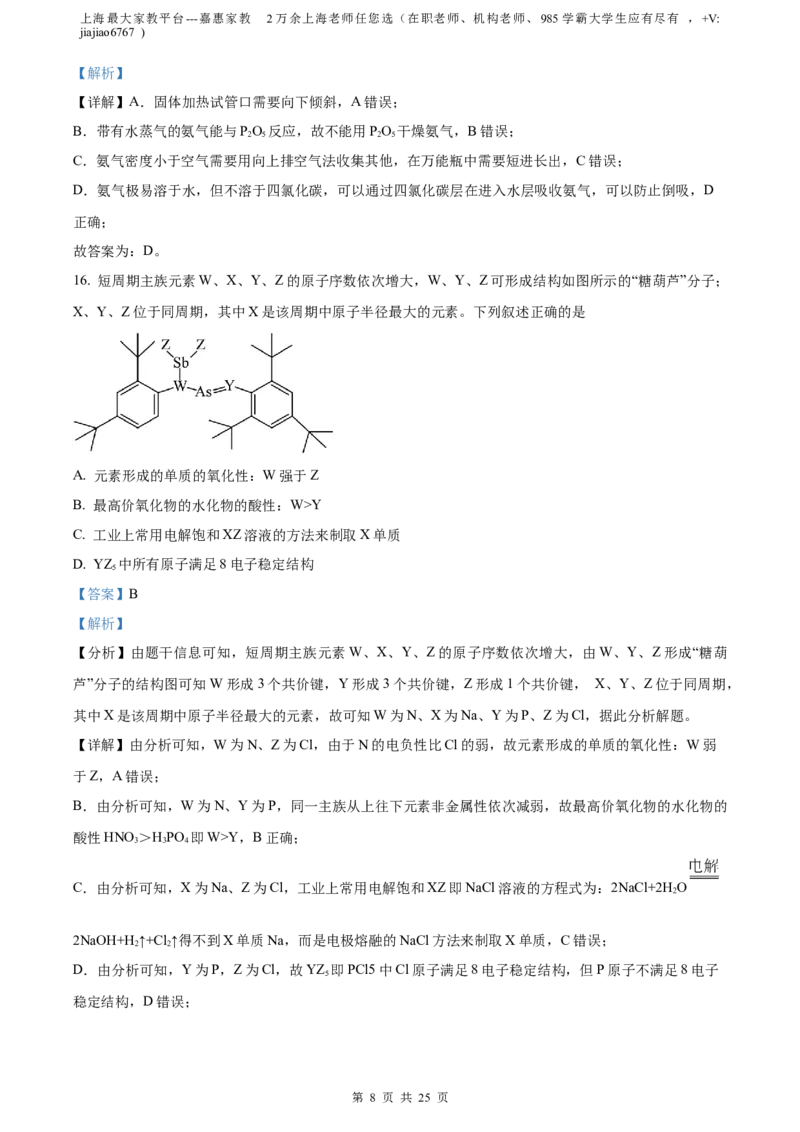
16. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y、Z可形成结构如图所示的“糖葫芦”分子;
X、Y、Z位于同周期,其中X是该周期中原子半径最大的元素。下列叙述正确的是
A. 元素形成的单质的氧化性:W强于Z
B. 最高价氧化物的水化物的酸性:W>Y
C. 工业上常用电解饱和XZ溶液的方法来制取X单质
D. YZ 中所有原子满足8电子稳定结构
5
【答案】B
【解析】
【分析】由题干信息可知,短周期主族元素W、X、Y、Z的原子序数依次增大,由W、Y、Z形成“糖葫
芦”分子的结构图可知W形成3个共价键,Y形成3个共价键,Z形成1个共价键, X、Y、Z位于同周期,
其中X是该周期中原子半径最大的元素,故可知W为N、X为Na、Y为P、Z为Cl,据此分析解题。
【详解】由分析可知,W为N、Z为Cl,由于N的电负性比Cl的弱,故元素形成的单质的氧化性:W弱
于Z,A错误;
B.由分析可知,W为N、Y为P,同一主族从上往下元素非金属性依次减弱,故最高价氧化物的水化物的
酸性HNO>HPO 即W>Y,B正确;
3 3 4
C.由分析可知,X为Na、Z为Cl,工业上常用电解饱和XZ即NaCl溶液的方程式为:2NaCl+2H O
2
2NaOH+H ↑+Cl↑得不到X单质Na,而是电极熔融的NaCl方法来制取X单质,C错误;
2 2
D.由分析可知,Y为P,Z为Cl,故YZ 即PCl5中Cl原子满足8电子稳定结构,但P原子不满足8电子
5
稳定结构,D错误;
第 8 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故答案为:B。
17. 某溶液含有K+、Fe3+、SO 、CO 、I-中的几种。取样,滴加KSCN溶液后显血红色。为确定该溶
液的组成,还需检验的离子是( )
A. K+ B. I- C. SO D. CO
【答案】A
【解析】
【分析】能反应的不共存、电解质溶液呈电中性,据此回答;
【详解】取样,滴加KSCN溶液后显血红色,则溶液含有Fe3+、Fe3+与CO 会发生双水解反应而不共存、
I-与Fe3+发生氧化还原反应而不共存,则阴离子只有SO ,电解质溶液呈电中性,故溶液中一定有SO
,为确定该溶液的组成,还需检验的离子只有K+;
答案选A。
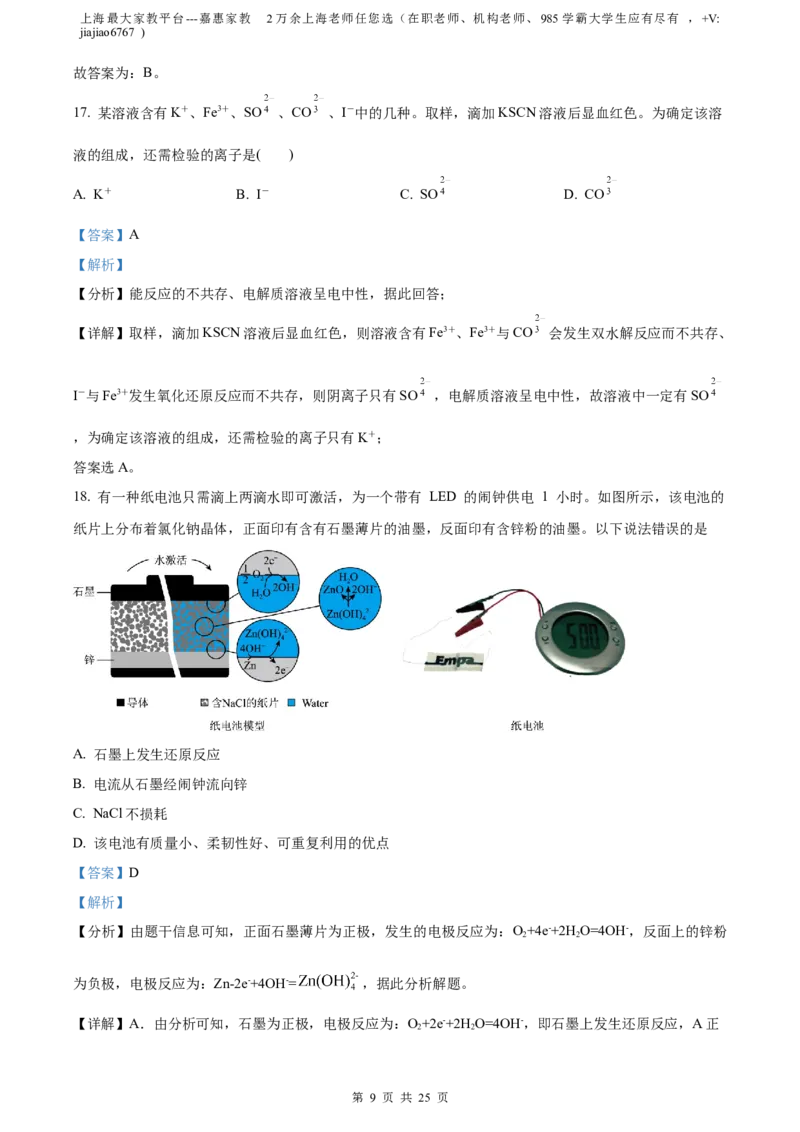
18. 有一种纸电池只需滴上两滴水即可激活,为一个带有 LED 的闹钟供电 1 小时。如图所示,该电池的
纸片上分布着氯化钠晶体,正面印有含有石墨薄片的油墨,反面印有含锌粉的油墨。以下说法错误的是
A. 石墨上发生还原反应
B. 电流从石墨经闹钟流向锌
C. NaCl不损耗
D. 该电池有质量小、柔韧性好、可重复利用的优点
【答案】D
【解析】
【分析】由题干信息可知,正面石墨薄片为正极,发生的电极反应为:O+4e-+2H O=4OH-,反面上的锌粉
2 2
为负极,电极反应为:Zn-2e-+4OH-= ,据此分析解题。
【详解】A.由分析可知,石墨为正极,电极反应为:O+2e-+2H O=4OH-,即石墨上发生还原反应,A正
2 2
第 9 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
确;
B.由分析可知,石墨为正极,锌粉电极为负极,故电流从石墨经闹钟流向锌,B正确;
C.由分析可知,反应过程中NaCl仅为电解质,参与导电,并未参与反应,故NaCl不损耗,C正确;
D.该电池有质量小、柔韧性好的优点,但由于上述反应不可逆,故不可重复利用,D错误;
故答案为:D。
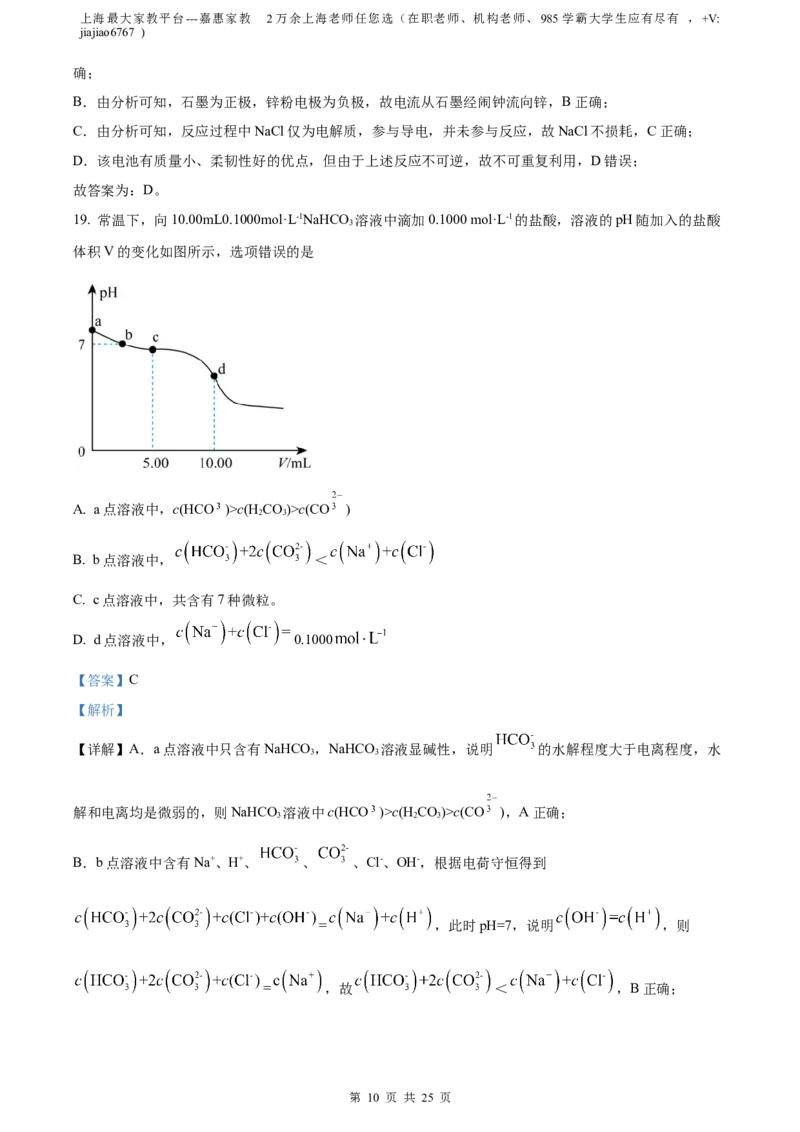
19. 常温下,向10.00mL0.1000mol·L-1NaHCO 溶液中滴加0.1000 mol·L-1的盐酸,溶液的pH随加入的盐酸
3
体积V的变化如图所示,选项错误的是
A. a点溶液中,c(HCO )>c(H CO)>c(CO )
2 3
B. b点溶液中, <
C. c点溶液中,共含有7种微粒。
D. d点溶液中, 0.1000
【答案】C
【解析】
【详解】A.a点溶液中只含有NaHCO ,NaHCO 溶液显碱性,说明 的水解程度大于电离程度,水
3 3
解和电离均是微弱的,则NaHCO 溶液中c(HCO )>c(H CO)>c(CO ),A正确;
3 2 3
B.b点溶液中含有Na+、H+、 、 、Cl-、OH-,根据电荷守恒得到
= ,此时pH=7,说明 ,则
= ,故 < ,B正确;
第 10 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.c点为向10.00mL0.1000mol·L-1NaHCO 溶液中滴加0.1000 mol·L-1的盐酸5mL,此时溶液中溶质为
3
NaHCO 和NaCl,溶液中含有Na+、H+、 、 、Cl-、OH-、HCO、HO,共含有8种微粒,C错
3 2 3 2
误;
D.d点为向10.00mL0.1000mol·L-1NaHCO 溶液中滴加0.1000 mol·L-1的盐酸10mL,恰好完全反应,溶液
3
中溶质只有NaCl, Na+、Cl-浓度均为0.0500 mol·L-1,则 0.1000 ,D正确;
故选C。
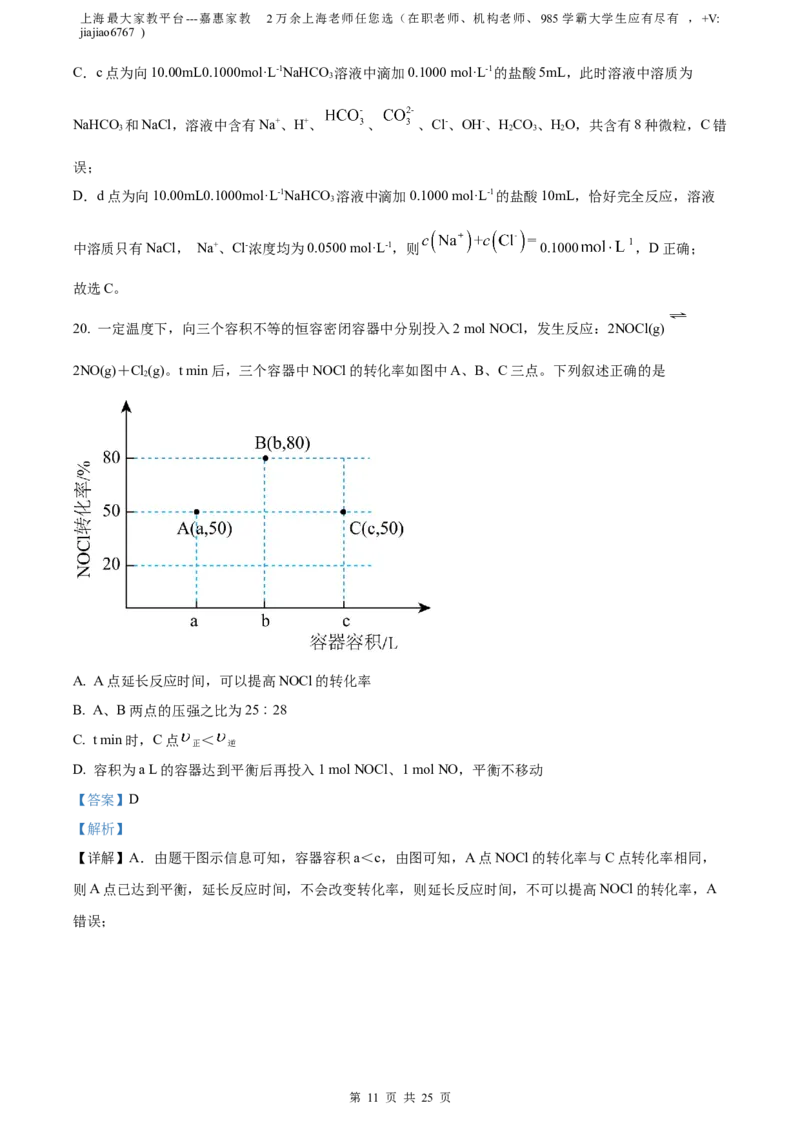
20. 一定温度下,向三个容积不等的恒容密闭容器中分别投入2 mol NOCl,发生反应:2NOCl(g)
2NO(g)+Cl(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
2
A. A点延长反应时间,可以提高NOCl的转化率
B. A、B两点的压强之比为25︰28
C. t min时,C点 <
正 逆
D. 容积为a L的容器达到平衡后再投入1 mol NOCl、1 mol NO,平衡不移动
【答案】D
【解析】
【详解】A.由题干图示信息可知,容器容积a<c,由图可知,A点NOCl的转化率与C点转化率相同,
则A点已达到平衡,延长反应时间,不会改变转化率,则延长反应时间,不可以提高NOCl的转化率,A
错误;
第 11 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
B.根据三段式分析可知, ,A、B两点的总
物质的量之比为:(1+1+0.5):(0.4+1.6+0.8)=25:28,但由于A、B两点对应的容器体积不同,故A、B两点
的压强之比不为25︰28,B错误;
C.由题干图示信息可知,容器容积a<c,由图可知,A点NOCl的转化率与C点转化率相同,则A点已
达到平衡,且增大容器体积相对于减小压强,则C点平衡时NOCl的转化率要大于50%,即t min时,C点
> ,C错误;
正 逆
D.由A项分析可知,A为平衡点,容积为a L的容器达到平衡后根据A点数据可知,K= =
= ,再投入1 mol NOCl、1 mol NO,Qc= = = =K,故平衡不
移动,D正确;
故答案为:D。
二、综合题(共60分)
(一)(共16分)
21. 海洋元素“溴”的单质及其化合物的用途广泛。
(1)Br原子的最外层电子排布式为_______,其中未成对电子的电子云形状为_______。
(2)能作为溴、碘元素原子得电子能力递变规律的判断依据是_______(填序号)。
a.IBr中溴为﹣1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br 、I 的熔点
2 2
(3)从原子结构角度解释氯的非金属性强于溴的原因:_______。
(4)Br 和碱金属单质形成的MBr熔点如表:
2
MBr NaBr KBr RbBr CsBr
熔点/℃ 747 734 693 636
NaBr的电子式_______,MBr熔点呈现表中趋势的原因是_______。
(5)海水提溴过程中,先向酸化的浓缩海水中通入_______,将其中的Br—氧化,再用“空气吹出法”吹出
Br ,并用纯碱吸收:Br +Na CO+H O→NaBr+NaBrO +NaHCO(未配平),则吸收1mol Br ,转移电子
2 2 2 3 2 3 3 2
第 12 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
_______mol,反应中氧化产物为_______。
(6)随后用硫酸酸化吸收液,得到Br 和NaSO 的混合溶液。相同条件下,若用盐酸酸化,则所得Br 的
2 2 4 2
质量减少,可能原因是_______。
【答案】(1) ①. 4s24p5 ②. 哑铃形
(2)ac (3)Cl的原子半径比Br的小,则原子核对最外层上的电子的束缚能力更强,导致 Cl的得电
子能力更强,失电子能力更弱
(4) ①. ②. 由于离子半径Na+<K+<Rb+<Cs+,导致MBr的离子键强度由NaBr到
CsBr依次减弱,故导致MBr熔点由NaBr到CsBr依次降低
(5) ①. Cl ②. ③. NaBrO
2 3
(6)酸性条件下,氯离子能被溴酸根离子氧化成氯气,而使生成的溴单质的量变少
【解析】
【小问1详解】
已知Br是35号元素,Br的基态原子核外电子排布式为:[Ar]3d104s24p5,Br原子的最外层电子排布式为
4s24p5,其中未成对电子为4p上的1个电子,p能级的电子云形状为哑铃形,故答案为:4s24p5;哑铃形;
【小问2详解】
a.IBr中溴为-1价,说明Br的电负性更强,即Br的非金属性更强,则Br原子得电子能力比I强,a符合
题意;
b.简单气态氢化物的酸性与其非金属性无关,即比较HBr、HI的酸性不能作为溴、碘元素原子得电子能
力递变规律的判断依据,b不合题意;
c.简单气态氢化物的稳定性与其非金属性一致,HBr的热稳定性比HI强,即Br的非金属性更强,则Br
原子得电子能力比I强,c符合题意;
d.非金属单质的熔点与其非金属性无关,即比较Br 、I 的熔点不能作为溴、碘元素原子得电子能力递变
2 2
规律的判断依据,d不合题意;
故答案为:ac;
【小问3详解】
由于Cl的原子半径比Br的小,则原子核对最外层上的电子的束缚能力更强,导致Cl的得电子能力更强,
失电子能力更弱,即氯的非金属性强于溴,故答案为:Cl的原子半径比Br的小,则原子核对最外层上的
电子的束缚能力更强,导致Cl的得电子能力更强,失电子能力更弱;
【小问4详解】
第 13 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
NaBr为离子化合物,故其的电子式为 ,由于离子半径Na+<K+<Rb+<Cs+,导致MBr的离子键
强度由NaBr到CsBr依次减弱,故导致MBr熔点由NaBr到CsBr依次降低,故答案为: ;由于
离子半径Na+<K+<Rb+<Cs+,导致MBr的离子键强度由NaBr到CsBr依次减弱,故导致MBr熔点由
NaBr到CsBr依次降低;
【小问5详解】
海水提溴过程中,先向酸化的浓缩海水中通入Cl,将其中的Br-氧化(2Br-+Cl=Br +2Cl-),再用“空气吹
2 2 2
出法”吹出Br ,并用纯碱吸收,根据氧化还原反应配平可知
2
3Br +6Na CO+3H O=5NaBr+NaBrO +6NaHCO,则吸收1mol Br ,转移电子 mol,反应中氧化产物为
2 2 3 2 3 3 2
NaBrO ,故答案为:Cl; ;NaBrO ;
3 2 3
【小问6详解】
用硫酸酸化吸收液,得到Br 和NaSO 的混合溶液;相同条件下,若用盐酸酸化,则所得Br 的质量减少,
2 2 4 2
原因是酸性条件下,氯离子能被溴酸根离子氧化成氯气,而使生成的溴单质的量变少,故答案为:酸性条
件下,氯离子能被溴酸根离子氧化成氯气,而使生成的溴单质的量变少。
(二)(共14分)
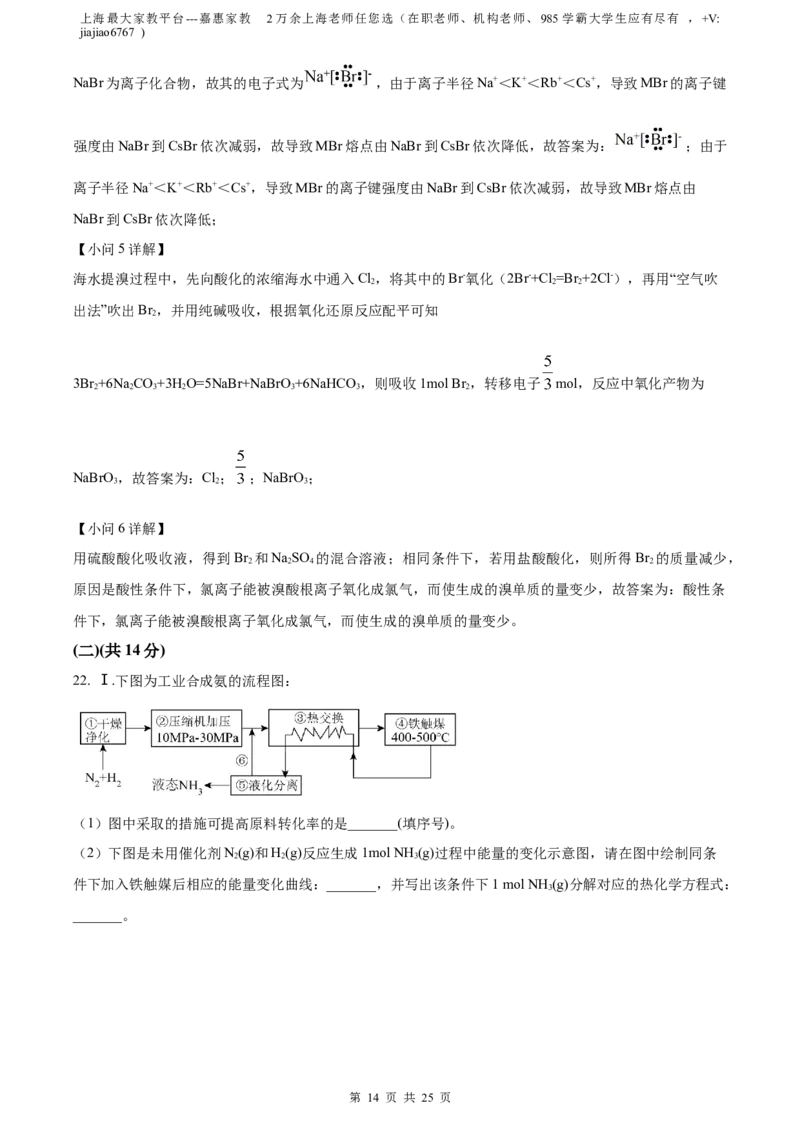
22. Ⅰ.下图为工业合成氨的流程图:
(1)图中采取的措施可提高原料转化率的是_______(填序号)。
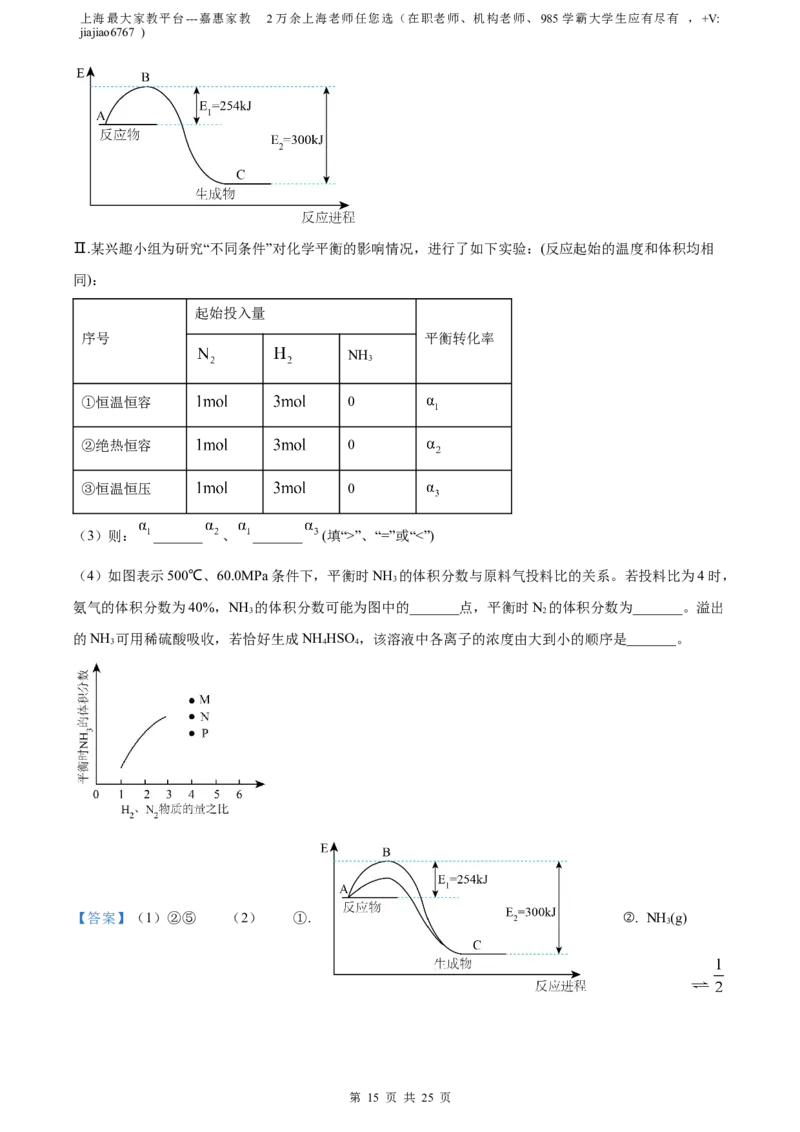
(2)下图是未用催化剂N(g)和H(g)反应生成1mol NH (g)过程中能量的变化示意图,请在图中绘制同条
2 2 3
件下加入铁触媒后相应的能量变化曲线:_______,并写出该条件下1 mol NH (g)分解对应的热化学方程式:
3
_______。
第 14 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
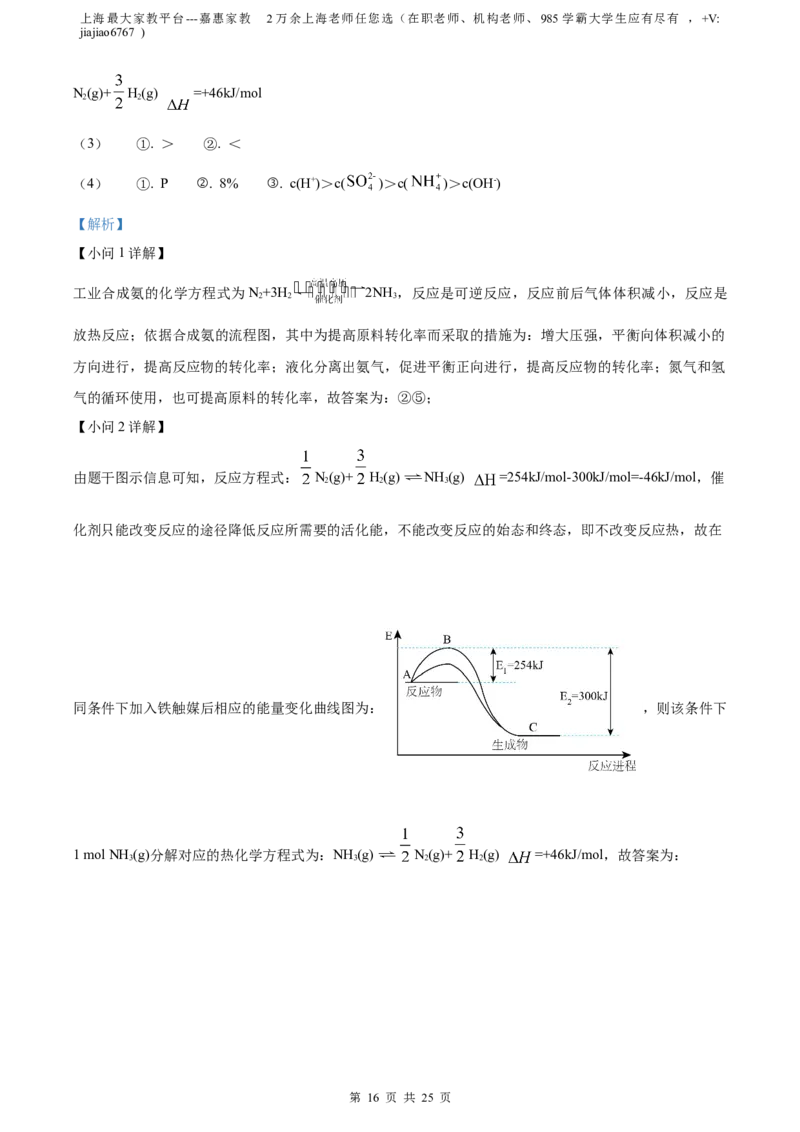
Ⅱ.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:(反应起始的温度和体积均相
同):
起始投入量
序号 平衡转化率
NH
3
①恒温恒容 0
②绝热恒容 0
③恒温恒压 0
(3)则: _______ 、 _______ (填“>”、“=”或“<”)
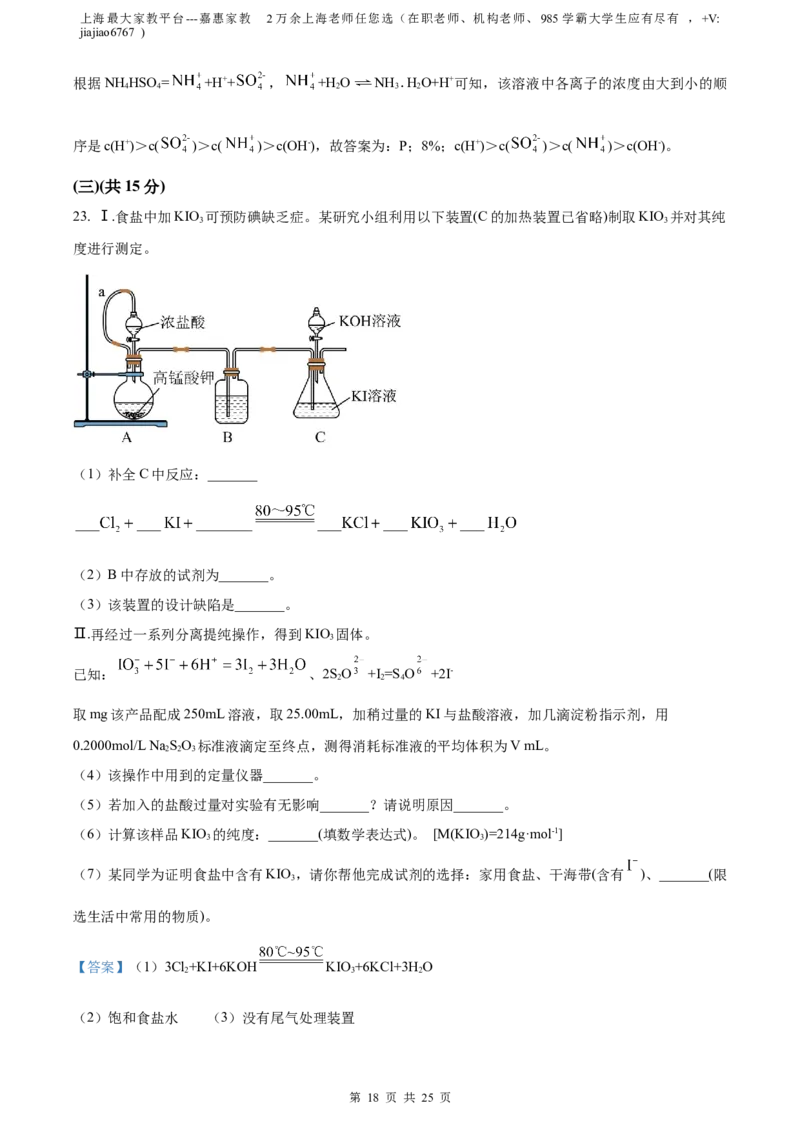
(4)如图表示500℃、60.0MPa条件下,平衡时NH 的体积分数与原料气投料比的关系。若投料比为4时,
3
氨气的体积分数为40%,NH 的体积分数可能为图中的_______点,平衡时N 的体积分数为_______。溢出
3 2
的NH 可用稀硫酸吸收,若恰好生成NH HSO ,该溶液中各离子的浓度由大到小的顺序是_______。
3 4 4
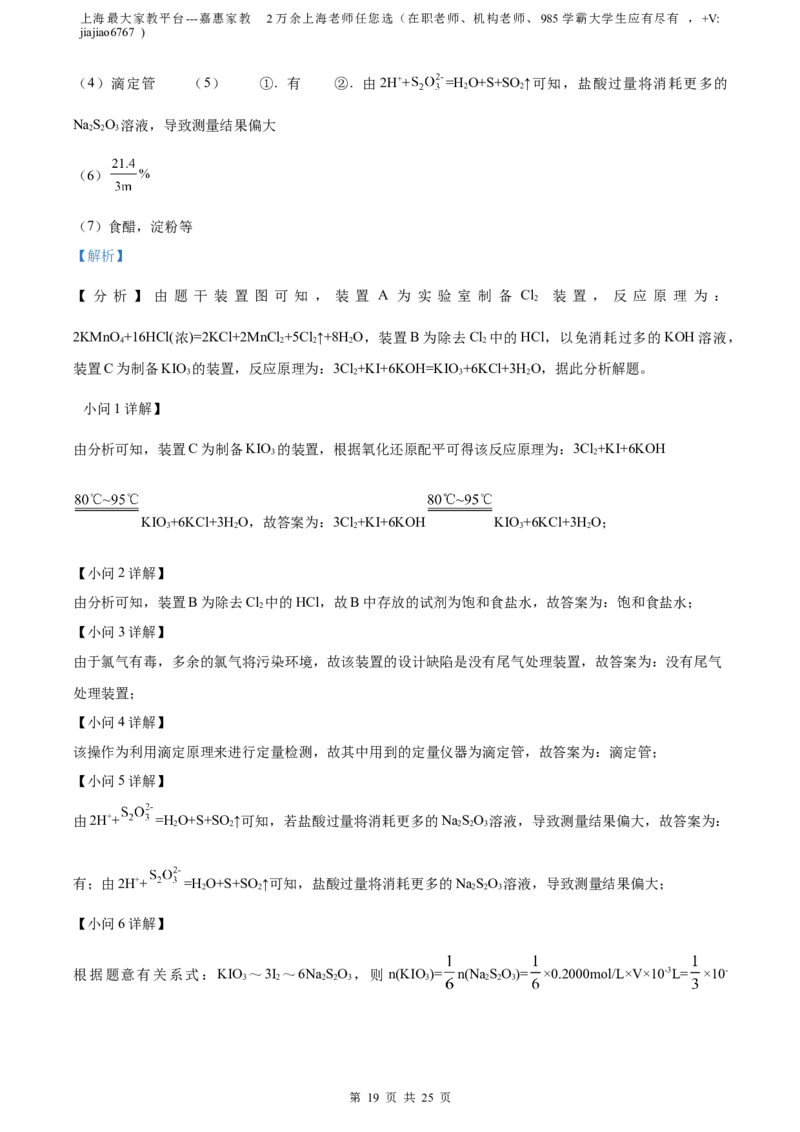
【答案】(1)②⑤ (2) ①. ②. NH (g)
3
第 15 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
N(g)+ H(g) =+46kJ/mol
2 2
(3) ①. > ②. <
(4) ①. P ②. 8% ③. c(H+)>c( )>c( )>c(OH-)
【解析】
【小问1详解】
工业合成氨的化学方程式为N+3H 2NH ,反应是可逆反应,反应前后气体体积减小,反应是
2 2 3
放热反应;依据合成氨的流程图,其中为提高原料转化率而采取的措施为:增大压强,平衡向体积减小的
方向进行,提高反应物的转化率;液化分离出氨气,促进平衡正向进行,提高反应物的转化率;氮气和氢
气的循环使用,也可提高原料的转化率,故答案为:②⑤;
【小问2详解】
由题干图示信息可知,反应方程式: N(g)+ H(g) NH (g) =254kJ/mol-300kJ/mol=-46kJ/mol,催
2 2 3
化剂只能改变反应的途径降低反应所需要的活化能,不能改变反应的始态和终态,即不改变反应热,故在
同条件下加入铁触媒后相应的能量变化曲线图为: ,则该条件下
1 mol NH (g)分解对应的热化学方程式为:NH (g) N(g)+ H(g) =+46kJ/mol,故答案为:
3 3 2 2
第 16 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
,NH (g) N(g)+ H(g) =+46kJ/mol;
3 2 2
【
小问3详解】
由(2)分析可知,合成氨反应为正反应是一个气体体积减小的放热反应,容器①②中加入的N 和H 分别相
2 2
同,但容器①恒温恒容、②绝热恒容则随着反应的进行,容器②的温度高于容器①,升高温度上述平衡逆
向移动,故 > ,容器①③中加入的N 和H 分别相同,但容器①恒温恒容、③恒温恒压,则随着反应
2 2
的进行,容器③的压强大于容器①,增大压强上述平衡正向移动,故 < ,故答案为:>;<;
【小问4详解】
图2表示500℃、60.0MPa条件下,平衡时NH 的体积分数与原料气投料比的关系,如果投料比为3时,达
3
到平衡状态时,氮气和氢气的转化率相等,此时氨气的体积分数最大,若投料比为4时,氮气的转化率升
高、氢气的转化率降低,NH 的体积分数减小;设投入的n(N )=xmol,n(H )=4xmol,设消耗的氮气
3 2 2
为zmol,由三段式分析可知: ,平衡时混合气体总物质的量=
(x-z+4x-3z+2z)mol=(5x-2z)mol,氨气的体积分数等于其物质的量分数= ×100%=40%,解
得z= ,此时N 的体积分数为: = =8%,故若投料比为4时,氨气的体
2
积分数为40%,NH 的体积分数可能为图中的P点,平衡时N 的体积分数为8%,若恰好生成NH HSO ,
3 2 4 4
第 17 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
根据NH HSO = +H++ , +H O NH HO+H+可知,该溶液中各离子的浓度由大到小的顺
4 4 2 3 2
序是c(H+)>c( )>c( )>c(OH-),故答案为:P;8%;c(H+)>c( )>c( )>c(OH-)。
(三)(共15分)
23. Ⅰ.食盐中加KIO 可预防碘缺乏症。某研究小组利用以下装置(C的加热装置已省略)制取KIO 并对其纯
3 3
度进行测定。
(1)补全C中反应:_______
(2)B中存放的试剂为_______。
(3)该装置的设计缺陷是_______。
Ⅱ.再经过一系列分离提纯操作,得到KIO 固体。
3
已知: 、2SO +I =S O +2I-
2 2 4
取mg该产品配成250mL溶液,取25.00mL,加稍过量的KI与盐酸溶液,加几滴淀粉指示剂,用
0.2000mol/L Na SO 标准液滴定至终点,测得消耗标准液的平均体积为V mL。
2 2 3
(4)该操作中用到的定量仪器_______。
(5)若加入的盐酸过量对实验有无影响_______?请说明原因_______。
(6)计算该样品KIO 的纯度:_______(填数学表达式)。 [M(KIO)=214g·mol-1]
3 3
(7)某同学为证明食盐中含有KIO ,请你帮他完成试剂的选择:家用食盐、干海带(含有 )、_______(限
3
选生活中常用的物质)。
【答案】(1)3Cl+KI+6KOH KIO +6KCl+3H O
2 3 2
(2)饱和食盐水 (3)没有尾气处理装置
第 18 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)滴定管 (5) ①. 有 ②. 由2H++ =H O+S+SO↑可知,盐酸过量将消耗更多的
2 2
NaSO 溶液,导致测量结果偏大
2 2 3
(6)
(7)食醋,淀粉等
【解析】
【 分 析 】 由 题 干 装 置 图 可 知 , 装 置 A 为 实 验 室 制 备 Cl 装的置 , 反 应 原 理 为 :
2
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O,装置B为除去Cl 中的HCl,以免消耗过多的KOH溶液,
4 2 2 2 2
装置C为制备KIO 的装置,反应原理为:3Cl+KI+6KOH=KIO +6KCl+3H O,据此分析解题。
3 2 3 2
【小问1详解】
由分析可知,装置C为制备KIO 的装置,根据氧化还原配平可得该反应原理为:3Cl+KI+6KOH
3 2
KIO +6KCl+3H O,故答案为:3Cl+KI+6KOH KIO +6KCl+3H O;
3 2 2 3 2
【小问2详解】
由分析可知,装置B为除去Cl 中的HCl,故B中存放的试剂为饱和食盐水,故答案为:饱和食盐水;
2
【小问3详解】
由于氯气有毒,多余的氯气将污染环境,故该装置的设计缺陷是没有尾气处理装置,故答案为:没有尾气
处理装置;
【小问4详解】
该操作为利用滴定原理来进行定量检测,故其中用到的定量仪器为滴定管,故答案为:滴定管;
【小问5详解】
由2H++ =H O+S+SO↑可知,若盐酸过量将消耗更多的NaSO 溶液,导致测量结果偏大,故答案为:
2 2 2 2 3
有;由2H++ =H O+S+SO↑可知,盐酸过量将消耗更多的NaSO 溶液,导致测量结果偏大;
2 2 2 2 3
【小问6详解】
根据题意有关系式:KIO ~3I ~6NaSO ,则 n(KIO )= n(Na SO)= ×0.2000mol/L×V×10-3L= ×10-
3 2 2 2 3 3 2 2 3
第 19 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
4mol,则原 KIO 样品中含有的 KIO 的质量为: ×10-4mol× ×214g/mol,故其纯度为:
3 3
=
故答案为: ;
【小问7详解】
根据反应方程式: 和I 遇到淀粉溶液变蓝的特性可知,为了证明食盐中含有
2
KIO ,可以选用试剂:家用食盐、干海带(含有I-)、食醋,淀粉等来完成,故答案为:食醋,淀粉等。
3
(四)(共15分)
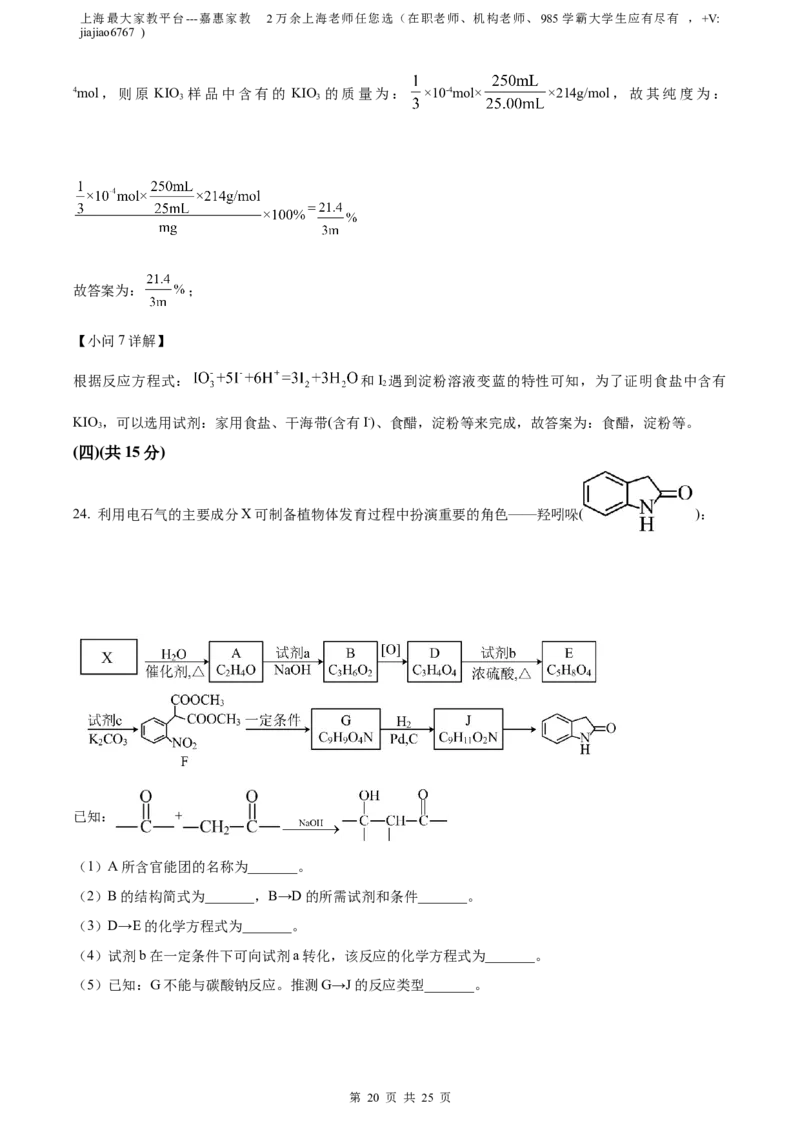
24. 利用电石气的主要成分X可制备植物体发育过程中扮演重要的角色——羟吲哚( ):
已知: +
(1)A所含官能团的名称为_______。
(2)B的结构简式为_______,B→D的所需试剂和条件_______。
(3)D→E的化学方程式为_______。
(4)试剂b在一定条件下可向试剂a转化,该反应的化学方程式为_______。
(5)已知:G不能与碳酸钠反应。推测G→J的反应类型_______。
第 20 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
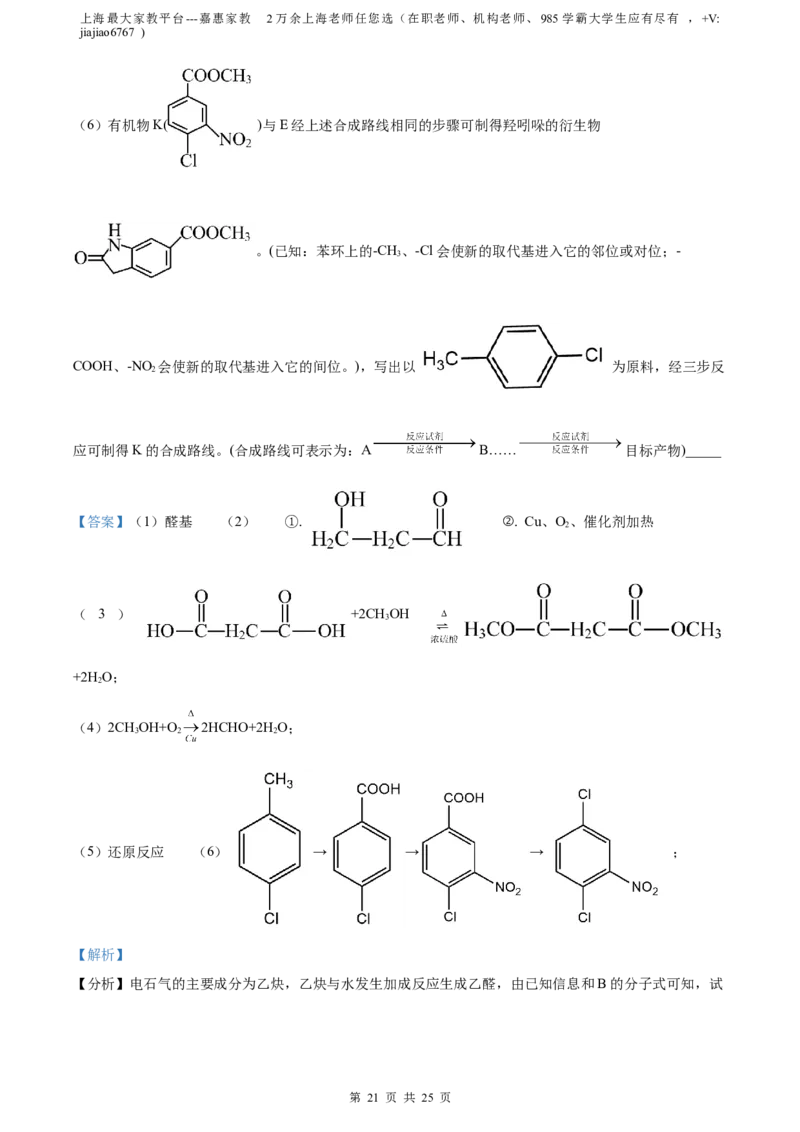
(6)有机物K( )与E经上述合成路线相同的步骤可制得羟吲哚的衍生物
。(已知:苯环上的-CH、-Cl会使新的取代基进入它的邻位或对位;-
3
COOH、-NO 会使新的取代基进入它的间位。),写出以 为原料,经三步反
2
应可制得K的合成路线。(合成路线可表示为:A B…… 目标产物)_____
【答案】(1)醛基 (2) ①. ②. Cu、O、催化剂加热
2
( 3 ) +2CH OH
3
+2H O;
2
(4)2CHOH+O 2HCHO+2H O;
3 2 2
(5)还原反应 (6) → → → ;
【解析】
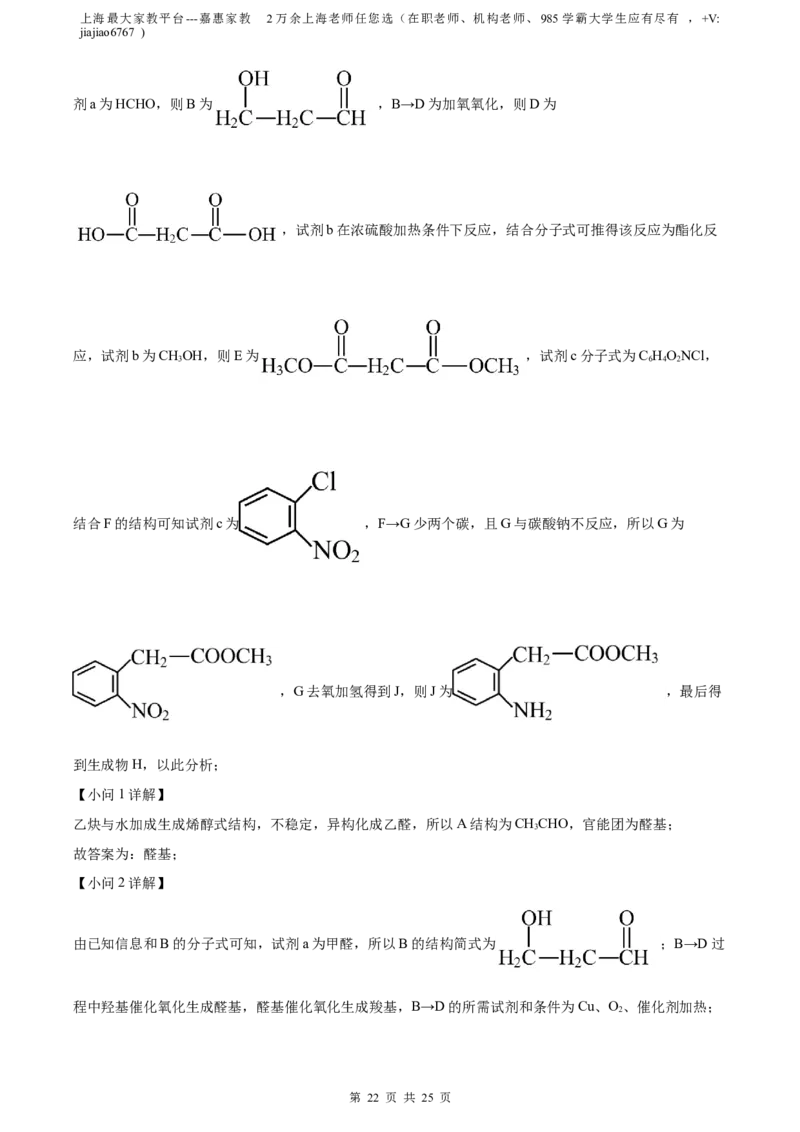
【分析】电石气的主要成分为乙炔,乙炔与水发生加成反应生成乙醛,由已知信息和B的分子式可知,试
第 21 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
剂a为HCHO,则B为 ,B→D为加氧氧化,则D为
,试剂b在浓硫酸加热条件下反应,结合分子式可推得该反应为酯化反
应,试剂b为CHOH,则E为 ,试剂c分子式为C HONCl,
3 6 4 2
结合F的结构可知试剂c为 ,F→G少两个碳,且G与碳酸钠不反应,所以G为
,G去氧加氢得到J,则J为 ,最后得
到生成物H,以此分析;
【小问1详解】
乙炔与水加成生成烯醇式结构,不稳定,异构化成乙醛,所以A结构为CHCHO,官能团为醛基;
3
故答案为:醛基;
【小问2详解】
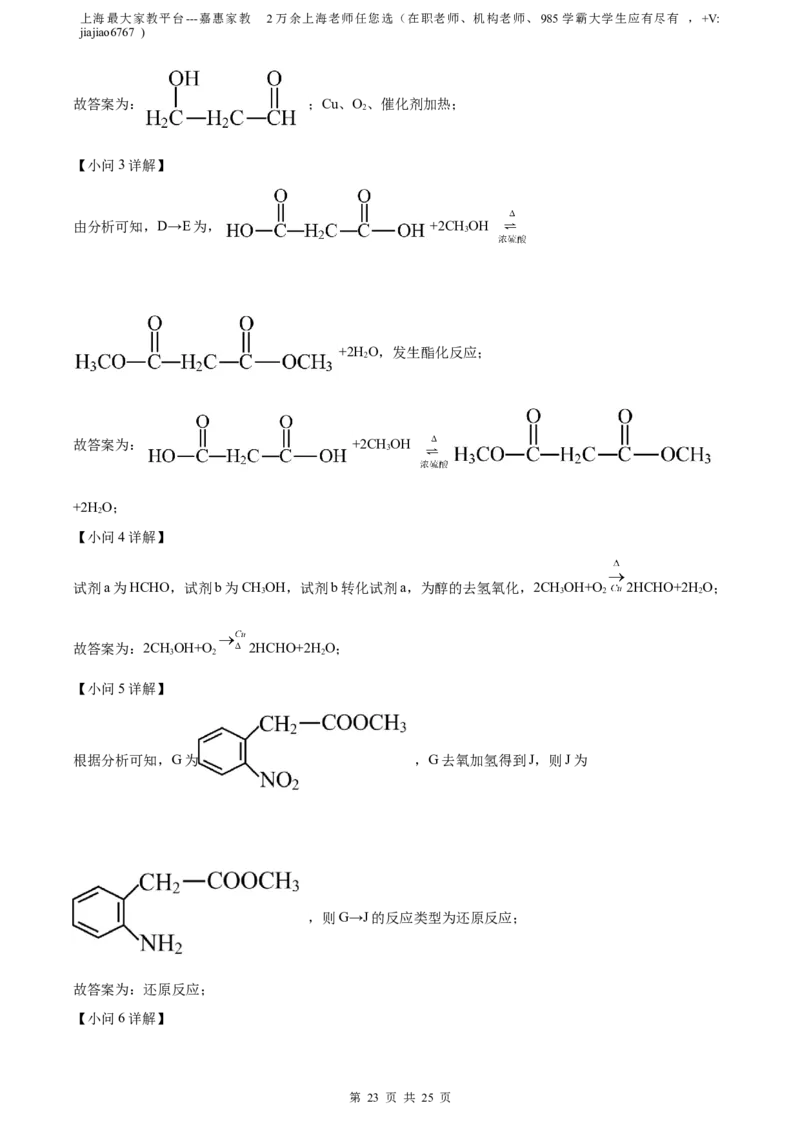
由已知信息和B的分子式可知,试剂a为甲醛,所以B的结构简式为 ;B→D过
程中羟基催化氧化生成醛基,醛基催化氧化生成羧基,B→D的所需试剂和条件为Cu、O、催化剂加热;
2
第 22 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
故答案为: ;Cu、O、催化剂加热;
2
【小问3详解】
由分析可知,D→E为, +2CH OH
3
+2H O,发生酯化反应;
2
故答案为: +2CH OH
3
+2H O;
2
【小问4详解】
试剂a为HCHO,试剂b为CHOH,试剂b转化试剂a,为醇的去氢氧化,2CHOH+O 2HCHO+2H O;
3 3 2 2
故答案为:2CHOH+O 2HCHO+2H O;
3 2 2
【小问5详解】
根据分析可知,G为 ,G去氧加氢得到J,则J为
,则G→J的反应类型为还原反应;
故答案为:还原反应;
【小问6详解】
第 23 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
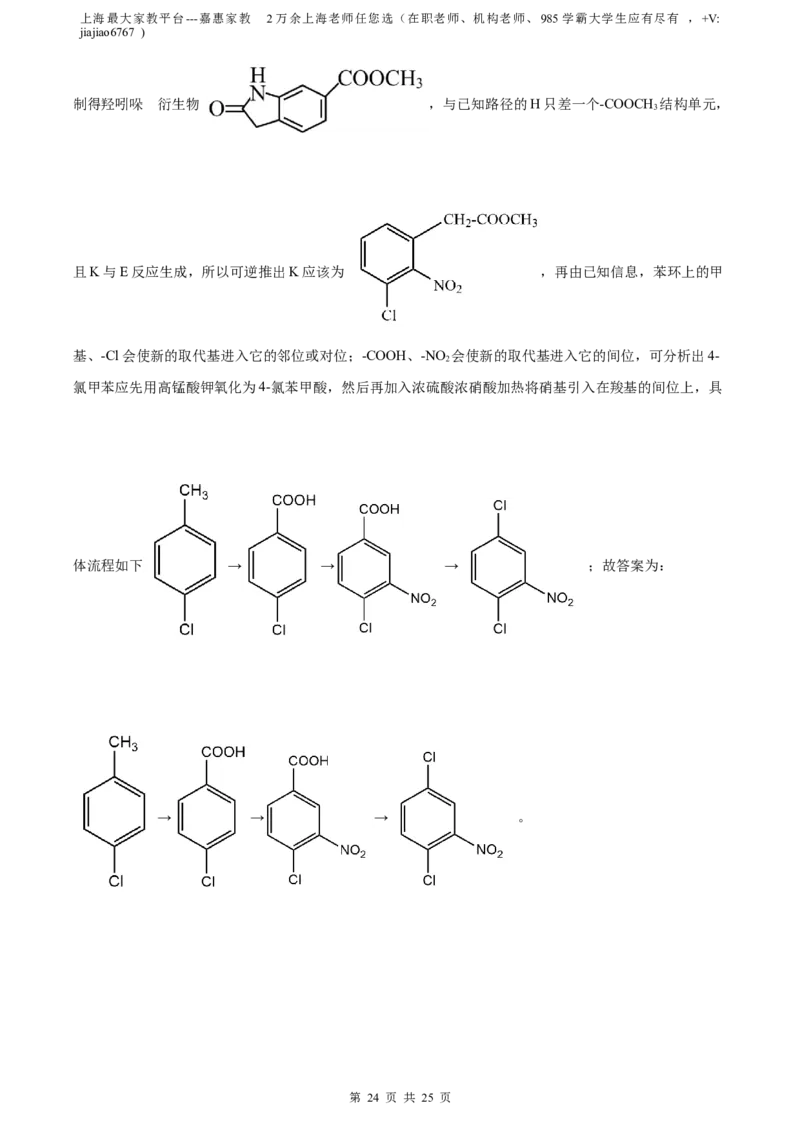
制得羟吲哚 衍生物 ,与已知路径的H只差一个-COOCH 结构单元,
3
的
且K与E反应生成,所以可逆推出K应该为 ,再由已知信息,苯环上的甲
基、-Cl会使新的取代基进入它的邻位或对位;-COOH、-NO 会使新的取代基进入它的间位,可分析出4-
2
氯甲苯应先用高锰酸钾氧化为4-氯苯甲酸,然后再加入浓硫酸浓硝酸加热将硝基引入在羧基的间位上,具
体流程如下 → → → ;故答案为:
→ → → 。
第 24 页 共 25 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
第 25 页 共 25 页