文档内容
1.Ⅰ.金属镁性质活泼,能与许多物质反应,某校课外活动小组根据镁能在二氧化碳中燃烧,
推测Mg也能在NO 中燃烧,可能产物为MgO、N 和MgN 。通过如图所示实验装置来验
2 2 3 2
证反应产物(夹持装置省略,部分仪器可重复使用)。已知:NO 气体能被NaOH溶液吸收,
2
MgN 极易与水反应。
3 2
(1)实验中,装置依次连接的顺序为A________(填字母);装置B的作用是________
________________________________________________________________________。
(2)用来检验N 的实验装置为______(填字母)。
2
(3)设计实验证明产物中存在MgN:_______________________________________
3 2
_______________________________________________________________________。
Ⅱ.工业上以菱镁矿为原料(主要成分为MgCO ,还有SiO、FeCO 等杂质)制备纳米氧化镁。
3 2 3
(4)根据反应流程要求,先除去FeCO ,采用先酸浸再氧化的方法,其中加入 HO 时,发生
3 2 2
反应的离子方程式为______________________________________________________
________________________________________________________________________。
(5)已知:在一定条件下CO(NH) 可与HO反应生成CO 和一种弱碱,流程后期,当除杂完
2 2 2 2
成后,再加入CO(NH) 开始沉淀Mg2+,该过程中发生的两个主要反应为(用化学方程式或
2 2
离子方程式表示)___________________________________________________________
________________________________________________________________________。
2.(2022·安徽芜湖模拟)硫代硫酸钠(Na SO)可用作分析试剂及还原剂,受热、遇酸易分解。
2 2 3
某学习小组用如图装置模拟古法制硫酸,同时利用生成的SO 气体制备硫代硫酸钠。
2
已知:①绿矾化学式为FeSO ·7H O,2FeSO ·7H O=====Fe O+SO ↑+SO ↑+14HO;
4 2 4 2 2 3 2 3 2
②SO 的沸点为44.8 ℃;
3
③NaSO 中S元素的化合价分别为-2价和+6价。
2 2 3
回答下列问题:
Ⅰ.硫代硫酸钠的制备(1)检查装置气密性,加入药品。NaS和NaCO 混合溶液用煮沸过的蒸馏水配制,煮沸的目
2 2 3
的是____________________________________________________________________;
B装置的作用是__________________________________________________________。
(2)从锥形瓶中得到NaSO 晶体需水浴加热浓缩至液体表面出现结晶为止,使用水浴加热的
2 2 3
原因是__________________________________________________________________。
Ⅱ.硫代硫酸钠性质的探究
①取NaSO 晶体,溶解,配成0.2 mol·L-1的溶液。
2 2 3
②取4 mL所配溶液,向其中加入1 mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑
浊物为S。
实验小组研究S产生的原因,提出了以下假设:
假设1:Cl 等含氯的氧化性微粒氧化了-2价硫元素。
2
假设2:酸性条件下,NaSO 分解产生S(不考虑空气中氧气氧化)。
2 2 3
依据假设设计实验方案:
所加试剂 现象
第①组 1 mL饱和氯水+4 mL Na SO 溶液 立即出现浑浊
2 2 3
一段时间后出现浑浊,且浑浊度比
第②组 1 mL某试剂+4 mL Na SO 溶液
2 2 3
①组小
(3)第②组实验中的某试剂是_________________________________________________。
(4)依据现象,S产生的主要原因是____________________________________________
___________________________________________________________(用离子方程式表示)。
3.(2022·北京,19)某小组同学探究不同条件下氯气与二价锰化合物的反应。
资料:ⅰ.Mn2+在一定条件下被Cl 或ClO-氧化成MnO (棕黑色)、MnO(绿色)、MnO(紫色)。
2 2
ⅱ.浓碱条件下,MnO可被OH-还原为MnO。
ⅲ.Cl 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
2
实验装置如图(夹持装置略):
C中实验现象
实验 物质a
通入Cl 前 通入Cl 后
2 2
产生棕黑色沉淀,且放置后
Ⅰ 水 得到无色溶液
不发生变化
Ⅱ 5%NaOH溶液 产生白色沉淀,在空气中 棕黑色沉淀增多,放置后溶缓慢变成棕黑色沉淀 液变为紫色,仍有沉淀
产生白色沉淀,在空气中 棕黑色沉淀增多,放置后溶
Ⅲ 40%NaOH溶液
缓慢变成棕黑色沉淀 液变为紫色,仍有沉淀
(1)B中试剂是________________。
(2)通入Cl 前,实验Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为_____________
2
________________________________________________________________________。
(3)对比实验Ⅰ、Ⅱ通入Cl 后的实验现象,对于二价锰化合物还原性的认识是____
2
________________________________________________________________________。
(4)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的
原因:
原因一:可能是通入Cl 导致溶液的碱性减弱。
2
原因二:可能是氧化剂过量,氧化剂将MnO氧化为MnO。
①用化学方程式表示可能导致溶液碱性减弱的原因:___________________________,
但通过实验测定溶液的碱性变化很小。
②取实验Ⅲ中放置后的1 mL悬浊液,加入4 mL 40% NaOH溶液,溶液紫色迅速变为绿色,
且绿色缓慢加深。溶液紫色变为绿色的离子方程式为__________________________
________________________________________________________________________,
溶液绿色缓慢加深,原因是MnO 被__________(填化学式)氧化,可证明实验Ⅲ的悬浊液中
2
氧化剂过量。
③取实验Ⅱ中放置后的1 mL悬浊液,加入4 mL水,溶液紫色缓慢加深,发生反应的离子
方程式是__________________________________________________________________。
④从反应速率的角度,分析实验Ⅲ未得到绿色溶液的可能原因:________________
________________________________________________________________________。
4.(2022·北京和平街第一中学模拟)某小组探究Cu和HO 的反应为氧化还原反应,从电极
2 2
反应角度分析物质氧化性和还原性的变化规律。
[实验探究]
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30%H O 溶液,一段时间内无明显现象,10
2 2
小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:______________________________________________
________________________________________________________________________。
[继续探究]
针对该反应速率较慢,该小组同学查阅资料,设计并完成了下列实验。
装置 实验 试剂a 现象20 mL 30%H O
2 2
Cu表面很快产生少量气
与4 mL
ⅱ 泡,溶液逐渐变蓝,产生
5 mol·L-1
较多气泡
HSO 混合液
2 4
20 mL 30%H O
2 2
溶液立即变为深蓝色,产
与4 mL
ⅲ 生大量气泡,Cu表面有
5 mol·L-1氨水
少量蓝色不溶物
混合液
(2)实验ⅱ中:溶液变蓝的原因是____________________________________________
______________________(用离子方程式表示);经检验产生的气体为氧气,产生氧气的原因
是______________________________________________________________________
________________________________________________________________________。
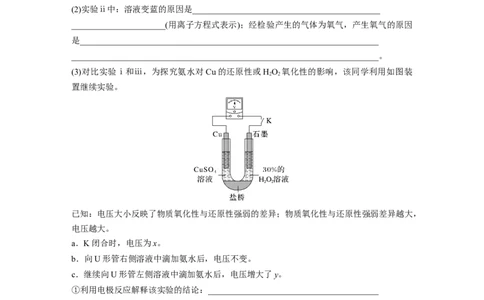
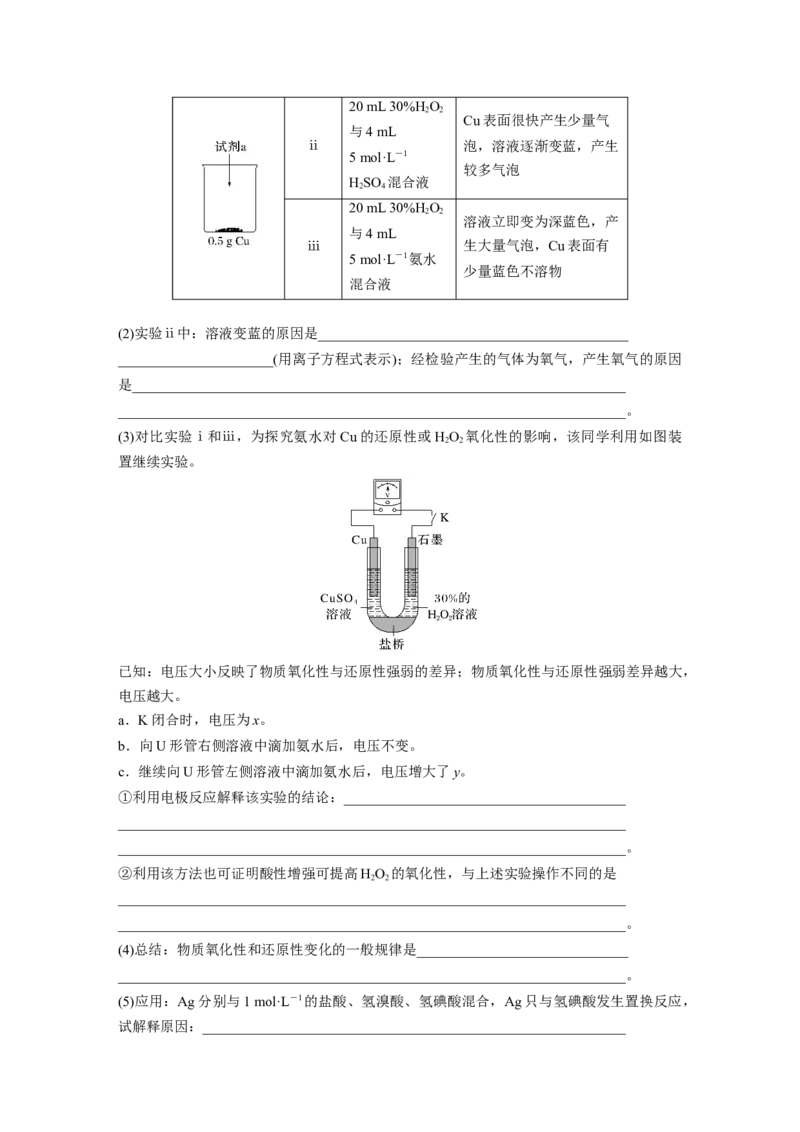
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或HO 氧化性的影响,该同学利用如图装
2 2
置继续实验。
已知:电压大小反映了物质氧化性与还原性强弱的差异;物质氧化性与还原性强弱差异越大,
电压越大。
a.K闭合时,电压为x。
b.向U形管右侧溶液中滴加氨水后,电压不变。
c.继续向U形管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:________________________________________
________________________________________________________________________
________________________________________________________________________。
②利用该方法也可证明酸性增强可提高HO 的氧化性,与上述实验操作不同的是
2 2
________________________________________________________________________
________________________________________________________________________。
(4)总结:物质氧化性和还原性变化的一般规律是______________________________
________________________________________________________________________。
(5)应用:Ag分别与1 mol·L-1的盐酸、氢溴酸、氢碘酸混合,Ag只与氢碘酸发生置换反应,
试解释原因:____________________________________________________________________________________________________________________________________
________________________________________________________________________。